摘要
背景
植物、真菌和细菌在土壤环境中形成复杂的、互利的群落。作为对植物根系分泌物中光合作用产生的糖的回报,这些根际群落中的微生物共生体为寄主植物提供了获取土壤中否则无法获得的营养物质的途径,并帮助植物抵御生物和非生物胁迫。细菌在这些群落中可能扮演的一个角色是菌根辅助细菌(MHB)。MHB是促进植物根和共生菌根真菌之间相互作用的细菌,虽然MHB对植物-真菌共生的形成和植物健康的影响已被充分记录,但MHB驱动植物根中的基因调控导致这些益处的具体分子机制在很大程度上仍未被表征。
结果
在这里,我们研究了这种细菌的影响荧光假单胞菌SBW25 (SBW25)对白杨根转录组的研究使用了由美洲山杨(白杨)幼苗和外生菌根真菌Laccaria二色的(Laccaria).结果表明,SBW25具有MHB活性,并通过以下途径促进白杨根菌根化Laccaria.通过对白杨根系在多种群落组成下的转录组分析,我们确定了与菌根化、SBW25的存在和mhb相关功能相关的共调控基因簇,并生成了一个组合逻辑网络,将白杨幼苗根系中观察到的基因表达模式的因果关系联系在一个布尔电路图中。预测的调节回路用于推断与MHB活性相关的调节机制。
结论
在我们的实验室条件下,SBW25增加的能力Laccaria通过抑制白杨根系抗真菌防御反应,与白杨幼苗根形成外生菌根相互作用。转录组数据分析表明,白杨根中响应MHB活性的潜在分子机制是与花粉识别传感器同源的蛋白质。花粉识别传感器集成了多个环境信号来下调花粉相关基因簇,使得与该系统具有同源性的蛋白质非常适合整合根际信息来下调根中抗真菌防御反应基因的预测机制。这些结果为白杨基因调控对MHB的响应提供了更深入的理解,并提出了额外的、假设驱动的生物学实验,以验证白杨MHB活性的假定分子机制Laccaria真菌共生关系。
背景
陆生植物很少是独居生物。相反,植物与生活在根际的真菌和细菌形成了复杂的、互利的群落,根际是植物根分泌物直接注入的狭窄的土壤带。植物向根际群落成员提供光合作用固定碳,主要以渗出糖和有机酸的形式[1].作为回报,植物从与根部相关的生物那里获得各种各样的生态服务,包括获得否则植物无法获得的营养来源,以及免受生物和非生物胁迫的保护[2,3.,4,5].的se interactions occur through the exchange of small molecules, such as nutrients, signaling compounds, and small secreted proteins between the community partners [6,7,8].
根际细菌提供的一种特殊生态服务是菌根辅助细菌(MHB),这是20多年前由Garbaye [9].MHB与植物和菌根真菌积极相互作用,以增强植物-真菌共生的功能[10,11].MHB活动已在许多细菌群中观察到,如放线菌,厚壁菌门,变形菌门,并与外生菌根和丛枝菌根共生[12].由于MHB物种和可能的真菌伙伴的多样性,包括外生菌根真菌(例如,[11])和丛枝菌根真菌(例如:[13]),任何单一的生物机制都不太可能解释所有MHB相互作用。相反,已经提出了许多MHB相互作用的一般和非排他性机制[10,11,14,15,16].MHB可促进真菌孢子在土壤中的萌发,促进菌丝生长,增强真菌在根际的存在[15].MHB可以通过去除毒素、抗生素或其他抑制根际真菌生长和植物-真菌相互作用的化合物来调节土壤[15].MHB还可以分泌植物细胞壁消化酶,使真菌更容易形成共生相互作用[17].然而,更重要的是,MHB通过产生效应物和/或激素促进植物-真菌相互作用,这些效应物和/或激素驱动植物根和菌根真菌菌丝的基因调控模式,从而增强它们随后的菌根相互作用[10,18].
宿主根、ECM真菌和MHB细菌共生体之间广泛的交叉对话导致广泛的代谢重塑,从而导致共生根的形态和功能变化[14,19,20.].这种交流的基础是可扩散分子及其传感器,它们将这些信号转化为调控结果。MHB可能操纵真菌中的基因调控,作为增加菌根化的一种方式,例如通过产生刺激性类黄酮或激素[19]以吸引菌根共生体,改变宿主的先天免疫反应,或通过真菌基因调节的广泛变化将菌丝体从自由生活状态转移到共生前状态[2,10].
MHB是一种众所周知的现象[3.],并研究了细菌对土壤真菌的转录组效应[10,21],植物根中使MHB活性起作用的转录组调控相互作用的研究较少。在这里,我们关注MHB对白杨幼苗根系转录谱的影响,以了解白杨根系对MHB存在可能的适应性反应。我们利用一个由三方组成的实验室系统美洲山杨(白杨)幼苗,外生菌根真菌Laccaria二色的(Laccaria)和植物生长促进(PGP)细菌荧光假单胞菌SBW25 (SBW25)用于研究白杨根基因调控MHB效应的分子机制。阿斯彭。Laccaria-假单胞菌系统是根际群落相互作用的优良实验室模型Laccaria在实验室很容易与白杨根形成外生菌根。虽然在本文发表之前,还没有关于SBW25具体作为MHB发挥作用的直接报道,但人们强烈期待SBW25的MHB活动。超过80%的假单胞菌从杨树根际对Laccaria增长(11].SBW25在白杨根部形成复杂动态的生物膜结构[22].此外,从具有植物生长促进(PGP)活性的植物根分离的细菌也经常被发现刺激菌丝生长和菌根形成[10,11而SBW25对白杨幼苗具有PGP效应,包括在氮磷营养限制条件下[23].
通过分析从不同组成的白杨苗木实验室群落中收集的转录组数据,我们确定了与菌根化、SBW25的存在和mhb相关功能相关的共调控基因簇。在实验条件下的基因簇表达模式被组装成预测的调节网络,突出了抑制抗真菌反应活性对MHB相互作用的重要性,并确定了杨根中可能使MHB相互作用成为可能的特定传感器蛋白。
结果
白杨三元群落的表型测定
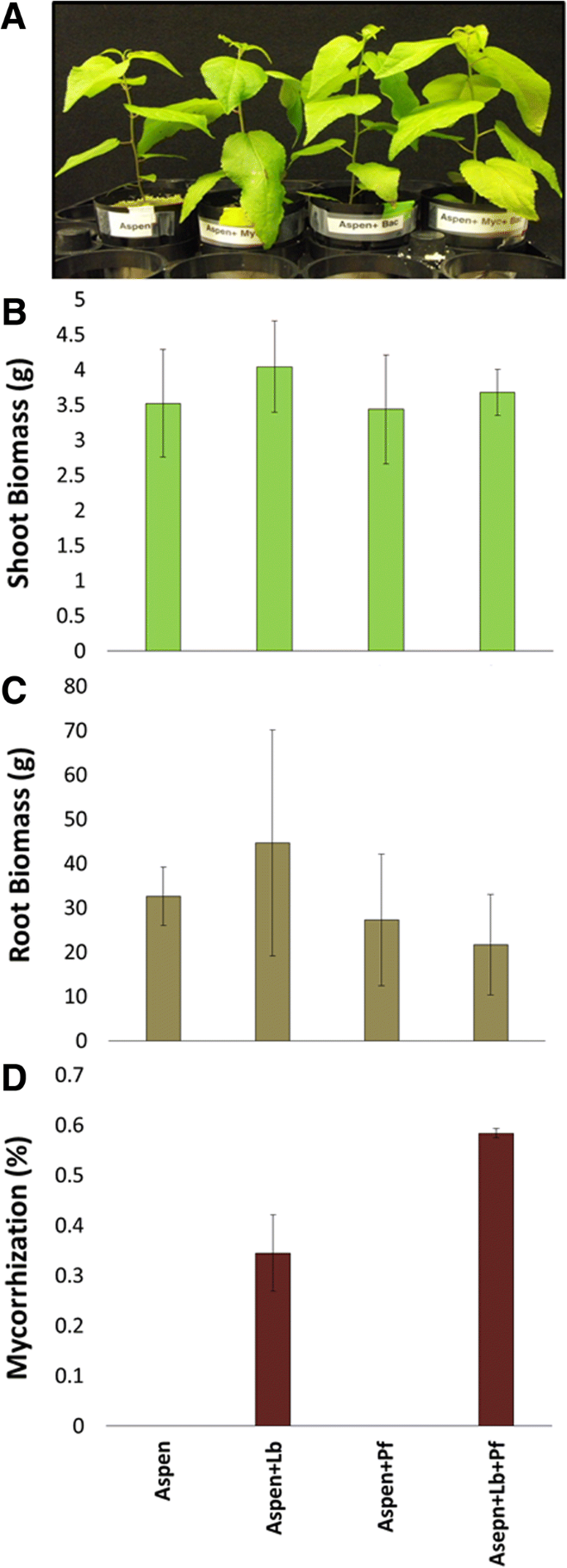
白杨幼苗在沙盆中进行培养,在沙盆中添加四种实验条件:白杨幼苗单独培养,白杨幼苗接种Laccaria白杨苗分别接种SBW25和两者共接种Laccaria和SBW25。对于每种条件,生成8个生物重复,其中5个用于测量幼苗生物量和量化根菌根化。三部菌根群落表型分析结果如图所示。1.存在Laccaria、SBW25或Laccaria加上SBW25在我们营养充足的实验室实验条件下,对茎部或根系生物量没有显著影响。然而,在SBW25存在的情况下,白杨根与菌根相互作用的百分比Laccaria显著增加1.7倍(双尾t检验p-value为0.006)。
对齐的RNA-seq读取到白杨,Laccaria、SBW25基因序列
每种条件下使用3棵白杨幼苗作为生物重复,收集根系转录组数据(见方法).在附加文件中总结了与每个群落成员的基因模型集对齐的序列读取总数1.在与三种群落生物中的一种排列的序列reads中,绝大多数(平均为> 99%)与白杨基因序列排列,其余的reads与任意一种排列Laccaria或SBW25基因序列(平均分别为总对齐reads的1.4和0.005%)。因为使用了50b长的RNA-seq数据,找到了一些匹配于'Laccaria'或' SBW25 '基因序列也不可避免地与aspen序列数据对齐[24].因此,由于一些序列读取会对准来自多个社区成员的基因,因此归属于社区成员的测序读取的总对齐百分比可能大于100%(表S1)。
来识别Laccaria或SBW25在转录组数据中存在于根际群落,我们确定了在转录组中是否可以检测到真菌或细菌reads的统计显著富集,其中SBW25或Laccaria存在相对到SBW25或Laccaria缺席。当Laccaria接种到社区后,有13.6倍的富集Laccaria转录组中的-对齐reads (p值0.065)。在将SBW25接种到群落的样品中,SBW25对齐的reads富集2.6倍(p值0.078)。当Laccaria和SBW25均存在于群落中,与apsen-SBW25培养条件相比,三方群落的细菌reads显著增加了3.5倍(p值为0.046)Laccaria在这种情况下,Reads与Laccaria只有社区。这些富集表明转录活性的SBW25和Laccaria在本实验系统中,根际细胞得以建立并发挥功能。此外,当SBW25以更高的丰度或更高的生物活性状态(即更高的转录率)存在时Laccaria也在场。根生物量与与SBW25基因组匹配的RNAseq reads百分比呈负相关(PCC = - 0.55),表明在三种条件下SBW25的存在增加不是由于根生物量的增加。
白杨根转录组中的差异基因表达
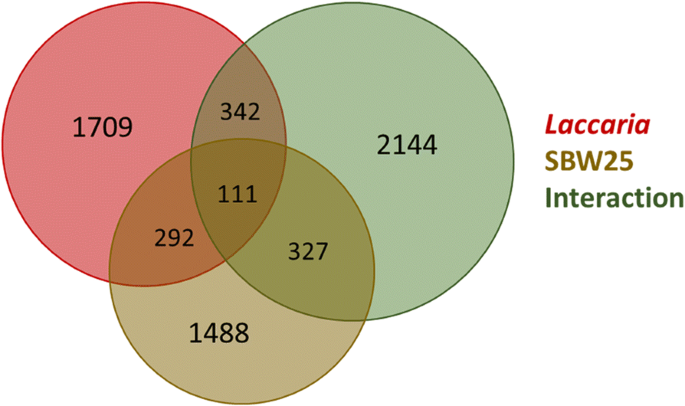
经fdr校正的2因素方差分析,共鉴定出6413个白杨基因(占全部白杨基因的15.5%)在群落组成方面存在显著差异表达p-值小于0.05(图;2).2454个基因(7%)存在差异表达Laccaria, 2218个基因(7%)在SBW25存在时存在差异表达,2924个基因(9%)在SBW25共同存在时存在差异表达Laccaria和SBW25。真菌和MHB之间共有403个基因(占所有差异表达基因的6.3%),111个基因(占所有差异表达基因的1.7%)Laccaria、SBW25和共同存在条件。所有基因表达值,折叠变化值和条件识别都可以在附加文件中找到2.
共调控基因簇
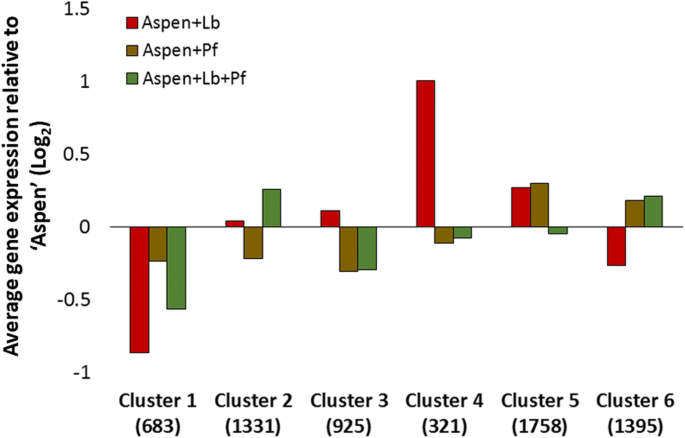
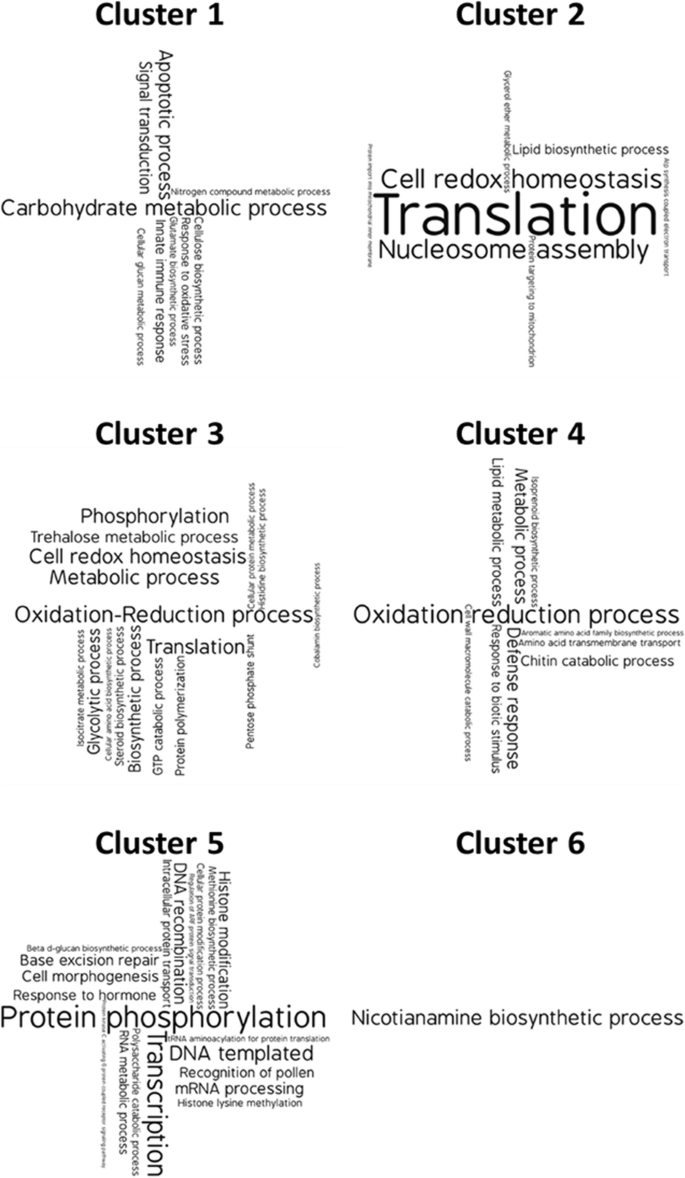
采用k -均值聚类法将表达差异显著的白杨基因分为6个表达模式相似的聚类。每一簇基因相对于白杨单独的平均表达量和每一簇基因数量的平均表达量总结在图中。3..完整的注释基因,他们的集群成员,和他们的表达水平可以在附加文件中找到3..基因本体论生物功能(GO-BF)注释被发现在每个聚类中统计上显著丰富,相对于注释在白杨基因组中的分布,如图所示为文本云。4丰富的GO-BF注释可以在附加文件中以表格格式找到4.
在白杨根共表达基因簇中富集GO-BP注释。每个共调控基因聚类中显著富集GO-BP注释项的标签云,标注标签大小与聚类中具有该标注的基因数量成正比。使用基于网页的WordArt工具生成的图形(https://wordart.com/).丰富的注释可以在附加文件中以表格格式找到4
在所有共培养条件下,第1簇基因相对于白杨根均下调,但当白杨苗仅与白杨根共培养时,下调幅度最大Laccaria(无花果。3.).Cluster 1中显著富集的注释与幼苗的先天免疫检测和反应有关:信号转导、应激反应、凋亡过程和先天免疫系统以及与植物细胞壁生物合成相关的基因(糖基代谢、碳水化合物代谢和纤维素生物合成)(图)。4).
簇2中的共调控基因在只有SBW25时下调,在只有SBW25时略有上调Laccaria存在,且当SBW25和Laccaria都存在(图;3.).该表达模式与菌根化百分比(PCC 0.99)强相关,显著高于与任何其他基因簇的菌根化百分比相关性(平均相关性为- 0.25,标准差为0.45,显著性)p- 0.002的值使用正态分布计算)。该簇中的富集注释用于调控和全球转录组重编程活动(核小体组装和大量翻译相关基因)(图。4).
共调控基因表达簇3和6仅受SBW25的存在调控,与SBW25的存在与否无关Laccaria(无花果。3.).当SBW25存在时,簇3基因下调。这种细菌特异性基因簇中的丰富注释与氨基酸代谢(组氨酸和氨基酸生物合成)、蛋白质生产和修饰功能(翻译、蛋白质聚合和蛋白质代谢过程)以及信号分子的生物合成(类固醇生物合成、异柠檬酸盐代谢和钴胺素生物合成)相关(图)。4).与聚类3的调控方向相反,聚类6的基因在SBW25存在时上调,在SBW25只存在时下调Laccaria是礼物。虽然簇6包含大量基因,但唯一显著富集的注释与烟胺合成相关(图6)。4),这表明这个簇可能捕获了对菌根或MHB相互作用不是特异性的基因功能。
簇4中的共同调控基因与先天免疫反应和抗真菌防御相关,在以下情况下调控最强Laccaria仅存在于菌根群落中(图;3.).簇4中的基因表明,只有在以下情况下,对病原真菌的防御(防御反应、对生物刺激的反应、氨基酸转运和几丁质分解代谢)才会高度上调Laccaria是礼物。该模式与先天免疫和细胞壁重塑反应基因簇1的表达模式(PCC -0.76)呈强反相关,是基因簇间相关性最显著的基因簇(平均相关系数为−0.13,标准差为0.43)。
簇5是已确定的共调控基因簇中最大的,显著富集的基因注释表明多种信号过程(信号通路、对激素的反应、信号识别和大量蛋白质磷酸化基因)的激活导致基因调控(组蛋白修饰、tRNA氨基酰化)和转录(转录和mRNA处理)(图)。4).
基因簇的调控模式被描述为布尔逻辑电路
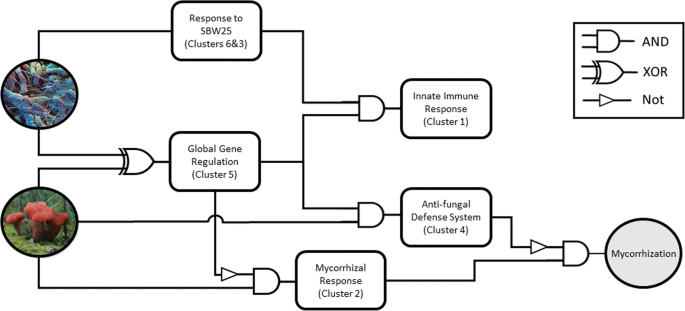
通过将上述共同调控基因簇的模式和丰富的注释与基因簇的贝叶斯信念网络和根际群落成员的存在/不存在(见方法)相结合,生成了一个反映基因簇与MHB活性之间因果关系的布尔逻辑电运图(图2)。5).
在布尔电路中,SBW25或Laccaria单独激活“全局基因调控”聚类(聚类5)。SBW25单独的存在也调控“对SBW25的反应”聚类(聚类3和6)和“先天免疫反应”聚类(聚类1)Laccaria单独导致“菌根反应”簇(簇2)的抑制和“抗真菌防御系统”簇(簇4)的激活,从而抑制“菌根化”簇。SBW25和Laccaria然而,不激活“全球基因调控”簇,然后允许激活“菌根反应”簇,抑制“抗真菌防御系统”簇,并导致mhb增强的白杨根菌根化(图。5).聚类5在电路中的位置以及上述调控相关功能标注的优势(图5。4)使得该簇可能成为与MHB检测和随后基因调控密切相关的白杨根调控元件的靶点。贝叶斯信念网络可以在附加文件中找到5.
讨论
森林树木广泛依赖菌根共生体来获取环境中有限的土壤养分。ECM真菌增加了根表面积,并为宿主树贡献了新的代谢能力,所有这些都改变了根-土壤的相互作用。外生菌根共生的形成需要对寄主根系免疫系统进行重塑,从而改变真菌-寄主特异性菌根的根系结构和功能特征。这种相互作用是真菌产生的效应物的结果,包括激素生长素和乙烯以及小分泌效应蛋白,这些效应物改变了宿主的转录和代谢,以促进ECM真菌对短根的定殖[20.].真菌信号引起的变化包括刺激侧根的产生以及细胞壁代谢的变化,从而培养菌根形成的位点。
除了共生菌根真菌外,根和菌根还被不同的细菌群落定植,其中许多细菌群落同样改变了宿主的生理,并贡献了新的代谢途径,促进了资源获取和宿主的环境应激抗性[3.,25].此外,微生物共生体之间的相互作用表明,细菌-真菌通信影响根际群落的生态结构和功能及其与植物根系的相互作用,MHB显著增加了树根的菌根化[11,18,21].虽然其中一些相互作用的分子信号已经开始被探索[10,21,26],但对支撑三方相互作用的宿主分子反应的关注却少得多。
荧光假单胞菌SBW25是一种菌根辅助菌
而SBW25的存在对白杨根系短根发育和菌根化有显著的正向影响Laccaria,既不LaccariaSBW25单独或联合施用对白杨幼苗生物量均无显著影响。因此,观察到的菌根化的增加不能与增加的叶片生物量或暴露在恒定真菌生物量下的不同数量的植物根产生的更高的光合化合物有关。因此,菌根化的增加完全是由于细菌的存在p .荧光SBW25及其对白杨代谢的影响,促进白杨和白杨之间的共生关系Laccaria.
这种菌根化的增加可能是由于细菌引起的宿主或真菌代谢的变化及其随后的相互作用(例如,[20.]),或通过更复杂的相互作用(尚待阐明)。外生菌根的形成需要复杂的通信和物理/生化相互作用,绕过宿主免疫系统,旨在保护根免受致病入侵者的侵害,同时为根定殖做好准备。由真菌产生的激素和其他效应物刺激根原基的产生并改变细胞壁生物化学。MiSSP7分泌的小蛋白质l二色的例如,已被证明定位于寄主根细胞核,在那里,寄主茉莉酸反应性基因转录被抑制,以有利于外生菌根化[26].此外,定植真菌可能会调节其抗原成分(如几丁质)的存在/反应性,这也会降低宿主的免疫反应[20.].
MHB可能通过使根易于定植而介入这些相互作用。Kurth等人(2015)[18]注意到一组上调的contigs与根部的感知和信号传递有关Quercus栎树包括水杨酸和茉莉酸信号通路的成员,以及大量与参与识别和信号传递的lrr受体样激酶同源的富亮氨酸重复序列(Leucine Rich Repeats, LRRs)。预计这些变化将对根对真菌定植的接受性产生重大影响。
MHB也可能通过影响真菌的定植反应来刺激菌根化。例如,Labbé等人(2014)[11]注意到假单胞菌菌株特异性基因调控l二色的与转录调节复合物和生物膜形成有关,可能在广泛的真菌代谢重组和真菌-细菌识别中发挥作用[10].与信号通路和真菌代谢相关的基因表达的变化也被诱导链霉菌属在陈放[21].
在目前的研究中,我们评估了杨根在双重和三方共生中的基因表达模式,以寻找MHB关系的线索。
SBW25中的MHB活性是抑制白杨根抗真菌防御反应的功能
先天免疫系统是组成性表达的,是植物的第一道防线,检测病原体和其他微生物[27].当先天免疫系统检测到特定威胁时,针对个别威胁的特定基因的表达就会被激活,先天免疫系统就会下调[28].提出的表达模式之间的关系是,当白杨幼苗单独种植时,先天免疫反应(簇1)的本构表达下调,并交换为更特定的抗真菌应激反应(簇4)Laccaria是礼物。为了使MHB受益,当SBW25存在时,该集群中的抗真菌系统将被削弱。在防御反应中Laccaria是那些参与甲壳素分解代谢以及许多“生物应激反应”基因,反映了入侵真菌病原体的主要潜在防御。然而,当与SBW25共接种时,这些反应总体上减弱,可能反映了MHB作用的一种途径。
在已鉴定的基因簇中,“全球基因调控”簇2与观察到的白杨根菌根化相关性最强(PCC = 0.99), RNAseq读数与SBW25对齐的百分比(PCC = 0.77)。这个簇中的基因在Laccaria目前进一步上调是什么时候Laccaria与SBW25共培养。该聚类主要由全球转录组重编程活动以及线粒体功能和ATP合成基因主导,这可能反映了MHB活动的结果:定植的增加增加了对能量的需求,以支持与支持菌根关联相关的增强代谢需求。
基因调控网络布尔电路分析
上述转录组数据的评估可能反映了导致MHB菌根化增加的三方关联相互作用的结果,但不一定是刺激代谢变化导致定殖增强的信号。而通过对表达模式的解释,可以将假定的生物学功能和它们被差异调节的实验条件归因于共同调节的基因簇(图2)。3.)和丰富的注释(图;4),我们使用布尔电路图来开发一个基因调控网络,该网络将解释在三方关联中差异调控的白杨基因簇(图2)。5).使用这种方法,集群5被确定为这个调控网络的关键。集群5由一个独占或(XOR)门控制,该门使用SBW25和Laccaria作为输入。异或门是一种逻辑操作,只有当输入不同时才输出真,即在该模型中当要么SBW25或Laccaria是存在的,但是不当两者或两者都不存在时。聚类5在电路中的位置以及上述调控相关功能标注的优势(图5。4)使得该簇可能成为与MHB检测和随后基因调控密切相关的白杨根调控元件的靶点。
与“花粉识别”蛋白同源的白杨膜结合传感器是防御反应的候选调节因子
虽然布尔逻辑电路图的分析表明,簇5对防御反应的调控是该系统中MHB活性的关键组成部分,但白杨根检测SBW25调控白杨根防御反应基因表达的具体分子机制并不明显。假设负责检测微生物群落的一些基因在这个实验系统中受到不同的调控,可以假设这一感觉机制的一组具体标准:(i)存在于由两者共同调控的集群中Laccaria和SBW25;(ii)丰富的调节功能,注释为能够集成多个输入的传感器;(iii) (ii)中的调控基因注释应在标准(i)识别的聚类中得到唯一富集。
对于第一个标准,异或门的存在SBW25和Laccaria集群5是整合社区成员存在信息的最佳集群(图5)。5).对于第二个标准,考虑丰富的注释集(图。4),一个相关的丰富注释是“识别花粉”(GO:0048544)。该注释由集群5中的8个基因共享(Potri.004G028000、Potri.005G014900、Potri.010G103300、Potri.013G121000、Potri.014G086900、Potri.019G119600、Potri.019G119700和Potri.T021600)。对于第三个标准,“识别花粉”注释确实在集群5(附加文件)中得到了独特的丰富4).
花粉的识别在控制植物育性中起着关键作用,涉及不同物种的不同分子特征。识别是基于花粉中的小配体(蛋白质、糖蛋白、脂质),这些配体必须被柱头识别,并具有适当的下游代谢反应[29,30.].受体也有很大的不同,包括激酶,rna酶和钙2 +-信号系统[30.].鉴于这种多样性,以及杨树中标注的基因可能涉及识别的许多方面,可以假设与花粉识别同源的蛋白质在MHB相互作用中的作用。在美国能源部联合基因组研究所植物基因数据数据库Phytozome中,第5簇中的所有8个“花粉识别”基因都被确定为在根组织中表达。31],这说明本实验对这些基因在根中的表达的检测并没有错误,也说明这些基因在根中的实际生物学功能并不是字面上的“检测花粉”。在柱头上,“花粉识别”蛋白通过整合花粉粒上存在的两个独立信号分子,下调启动授粉的基因,防止不亲和花粉的意外受精[32,33,34].这种机制,即整合来自两个细胞外信号的信息来下调一组相关基因,恰好与预测调控网络中xor门控基因表达模式的生物学机制相匹配。
结论
一个由白杨幼苗、外生菌根真菌组成的三方联合模型l二色的,以及PGPp .荧光通过对白杨根部转录组数据的分析,研究了MHB活性的机制。结果表明,SBW25是一种MHB,可通过促进白杨幼苗根菌根化LaccariaSBW25在沙罐培养的根际持续时间超过60 d。我们认为这是SBW25拥有MHB活动的第一份报告。在白杨根中发现了一组共调控基因,它们与白杨的菌根化水平密切相关Laccaria.我们认为,该簇的整体转录调控活动,包括染色质重塑和翻译活动的基因,表明了白杨根从自由生长的根向菌根共生的发育阶段转变的分子机制。当两个Laccaria和SBW25存在于根际群落中,一个与植物抗真菌反应相关的共调控基因簇显著下调,因此我们假设mhb介导的该系统菌根化的增加是通过抑制白杨根的抗真菌防御反应来促进的。从白杨幼苗中进一步鉴定了MHB活性的分子传感器机制。由于它们的表达模式和注释,8个与“花粉识别”蛋白质同源的基因被认为是根MHB相互作用的组成部分。假设这些蛋白质可以作为一个生物异或逻辑门,集成多种环境/生物信号,特别是两者同时存在Laccaria和SBW25,降低了白杨根的真菌防御反应。这些模型预测的MHB相互作用机制将为未来的生物实验设计提供信息,以验证我们提出的MHB活性的分子机制。
方法
菌根社区成员
阿斯彭
白杨及其相关树种是北美分布最广、基因变异最多的树种之一[35,36,37].美洲山杨(Michx.)种子来自加拿大自然资源国家树木种子中心(种子批# 20001017.0)。注释的白杨基因组来自Phytozome (Ptrichocarpa210 v3.0) [31,38].
Laccaria
在温带和北方生态系统中,外生菌根真菌与许多森林树木共生,如白杨[35,36,37].Laccaria二色的(Marie) S238 N (Institut National de la Recherche Agronomique, Nancy, France)从ATCC获得(写明ATCC®米娅- 4686™).的Laccaria注释基因组来自联合基因组研究所(Lacbi2) [39,40].
SBW25
SBW25是白杨幼苗在低氮和低磷条件下的PGP细菌[23]最初是从一种甜菜植物的叶表面分离出来的[9,14,41].p .荧光SBW25是英国牛津大学植物科学系Gail Preston博士赠送的礼物[42].注释基因组来自NCBI (NC012660) [41,43].
三部菌根群落相互作用的实验室条件
本试验考虑了四种群落条件:白杨单独;白杨,SBW25;阿斯彭和Laccaria;和白杨与SBW25和Laccaria.培养在直径6厘米× 25厘米深的花盆中(Cone-tainers™,Stuewe and Sons, Corvallis, OR, USA),含有酸洗粗细沙混合物(比例2:1),底部有尼龙网。每个试验条件设6个生物重复,共24盆。
Laccaria是引入沙罐社区的第一个社区成员。Laccaria如前所述,在改良的Melin Norkrans (MMN)琼脂培养基上培养[44].如Molina和Palmer所述,为生产沙罐接种物,培养物在液态MMN培养基中25°C在黑暗中静态培养3周[45].混合培养(三次脉冲,每次3秒),以产生真菌浆液,用于接种沙罐。为了建立菌根白杨幼苗,在花盆中添加一条真菌浆带,并覆盖约2厘米的额外沙子[46].对于非菌根条件,加入等量的MMN液体介质代替真菌浆液。
最初,每个砂盆都种植了几颗消毒过的白杨种子。在恒温生长箱(Caron 7305-22)中,光周期为(272±31 μmol m) 14 h−2年代−1),昼夜温度24/19±3°C;相对湿度随温度和时间的变化在60 ~ 70%之间波动。白杨种子每天用蒸馏水浇水3次保持湿润。5天后,将发芽的幼苗进行稀释,每盆留一株。在此选择之后,幼苗每天浇水三次,达到田间容量(60毫升一盆−1d−1)用含有1.2 mM NO的营养液3., 0.4 mM NH4, K为0.5毫米,H为0.1毫米2阿宝4, 0.2 mM Ca, 0.1 mM Mg, 0.1 mM SO4, 50.5 μM Cl, 20 μM Fe, 20 μM B, 2 μM Mn和Zn, 0.5 μM Cu, Na, Co和Mo。0.1 N NaOH调整溶液pH为5.6。
白杨幼苗减薄至每株5天后,沙罐群落接种SBW25。将SBW25细菌培养物接种于20ml Luria肉汤(LB;10g L−1色氨酸,5 g L−1酵母提取物,5 g L−1NaCl)培养基在28°C下过夜,以225转/分钟的转速摇晃,2400克离心20分钟,并在相同体积的无菌0.1 M MgSO中洗涤4.将细胞悬液调整到OD值600在每株白杨苗基部分别添加2.0和150 μL。对于非细菌处理,相同体积的无菌0.1 M MgSO4在白杨幼苗基部添加。
在添加细菌后,再培养63天,然后收获用于收集幼苗表型数据和元转录组测序。采收的方法是轻轻将白杨幼苗从花盆中取出,摇晃它们以除去大部分沙子,并将根与茎和叶组织分离。每个实验条件下3个生物重复的根立即冷冻在液氮中,用于RNA提取和转录组分析。其余3个重复用于测定幼苗生物量和根菌根化百分比。
为了定量测定真菌定殖量,用无菌水清洗根系,并在4℃无菌去离子水中保存,直到染色。外生菌根定殖量采用网格线相交法[47]由Brundrett等人对ECM根进行了修正。[48].各处理的根系样品用0.01% (v/v)酸性品红(Sigma-Aldrich, St. Louis, MO, USA)过夜[45之后,将根均匀分布在培养皿中,并在解剖显微镜下检查和枚举每个样本的尖端定植。使用剩余的根和芽组织进行生物量测量,在称量前在65°C下干燥72 h。
RNA提取和转录组测序
为了进行转录组学分析,收集整个根系,并立即冷冻在液氮中。所有用于RNA提取、rRNA去除和NGS文库制备的试剂均为无rnase分子生物学级。冷冻的植物根被研磨成细而均匀的粉末,同时保持在液氮中。大约100毫克冷冻根组织用于RNA提取。冷冻的根组织用1ml 3x Qiagen bacteria RNAprotect试剂在室温下处理5分钟。将处理过的浆液以13000 rpm离心3 min制成球团,然后从组织球团中去除上清。在Qiagen Plant RNeasy RLT裂解缓冲液中加入新鲜β-巯基乙醇450 μL,重悬至140 mM。其余步骤根据Qiagen RNeasy植物和丝状真菌试剂盒说明书进行,包括附录D中所述的柱上DNase文摘[49].纯化后的总RNA用80 μL水洗脱。样品用Zymo Research OneStep PCR抑制剂脱盐柱纯化,洗脱入水中。使用Nanodrop和安捷伦生物分析仪芯片在植物RNA协议上运行,对脱盐样品的产量和质量进行评估。第二次DNase处理使用震中基线- 0 DNase酶对1 - 3微克总RNA样本进行处理,每μg总RNA的酶活性为0.3 - 1.0单位,在37°C下持续15分钟。用Zymo Research RNA Clean & Concentrator-5柱直接纯化,洗脱至20 μL水中,抑制DNase活性。用50% - 50%混合的植物种子/根和细菌rRNA探针(epicentra /Illumina riboo -zero探针)去除浓缩的总RNA (rRNA)亚基。按照试剂盒说明书使用agourt RNAClean XP磁珠纯化mRNA样品,12 μL水洗脱。使用安捷伦生物分析仪Pico RNA芯片在mRNA协议上运行,成功去除了大部分rRNA亚基,并对样本进行了量化。
根据试剂盒说明,使用Epicentre Script-Seq试剂盒从样本mRNA中生成链特异性NGS转录组文库。每个库都附加了一个唯一的条形码,以实现样本多路复用,并使用推荐的故障安全聚合酶和缓冲液(震中)进行18个周期的扩增。按照试剂盒说明书使用Agencourt AMPure XP磁珠纯化文库,洗脱至16 μL水中。使用安捷伦HS DNA芯片和Qiagen HS DNA定量试剂对完整的文库进行表征和定量。NGS文库测序服务由芝加哥大学基因组学与系统生物学研究所HGAC测序核心提供。每个Illumina HiSeq200流式细胞复用多达6个文库,并按50 bp周期测序协议进行测序。
转录组数据分析
从测序读取生成元转录组数据
植物共生体群落的基因表达数据由RNAseq reads确定。领结(50]用于将短读序列对齐到社区(aspen,Laccaria, SBW25)基因模型(即预测编码序列)。所有社区成员的基因模型都是从上面列出的公共数据库中收集的。默认的Bowtie条件用于为基因模型的所有序列读取集生成比对,除了设置Bowtie以返回所有可能的序列比对。使用应用程序BowStrap在收集的转录组数据中检测基因模型表达[24].使用10,000次BowStrap迭代计算Reads Per KBase gene Per Million aligned Reads (RPKM)值的平均值和标准差。
基于累积正态分布(CND)确定基因表达的显著性p-value,由Benjamini-Hochberg (BH)错误发现率(FDR)校正调整[51].经bh校正的p值小于0.05,bootstrap RPKM表达量大于2,则认为该基因表达显著。所有基因表达值采用分位数归一化[52].
通过共调控模式聚类显著差异表达的基因
用MeV 4.5.1对显著差异表达(SDE)基因进行2因素方差分析(ANOVA),https://sourceforge.net/projects/mev-tm4/).方差分析考虑的因素是存在或不存在LaccariaSBW25是否存在。P-值基于10,000个显著性阈值小于0.05的排列计算。
所有SDE基因采用K-means聚类方法被归为共调控基因簇。考虑欧氏距离进行聚类,并使用' R-project '计算(v 3.0.3) (https://www.r-project.org/)。使用剪影系数确定所考虑的最佳簇数,评估2到12之间的所有簇大小,并选择提供最大剪影系数的簇大小[53].
识别基因子集中富集的基因注释
为了将基因簇置于更广泛的生物学背景中,特定的基因本体生物过程(GO-BP) [54相对于注释在白杨总基因组中的分布,这些注释在基因簇中富集。给定数据类型的GO-BP注释的富集量计算为累积超几何分布[55].阈值为p-value < 0.05用于判断GO-BP注释富集的显著性。
生成白杨根MHB调控网络
为了在共同调控基因簇之间产生因果相互作用的网络,使用了贝叶斯网络(BN)推理。对于每个重复的群落转录组,计算k均值聚类内基因的平均基因表达量。除平均基因簇表达外,节点为存在/不存在Laccaria和SBW25。BN由BANJO生成[56,57]使用如下参数:贪婪搜索算法,所有局部移动,每个节点最多5个父节点。此外,'的节点Laccaria'和' SBW25 '不允许是任何其他节点的子节点。然后,将得到的最高分网络中的冗余交互删除(例如,如果BN识别出因果交互A→B、B→C和A→C,那么交互A→C将从网络中删除)。
然后,修剪的BN被用作逻辑图的支架,由布尔电路实现,其中MHB活动的输出是存在或不存在的函数Laccaria只有SBW25。逻辑门的选择是对数据仔细解释的结果。虽然布尔关系不能捕获差异基因调控的整个可能范围,但该网络有效地总结了一个调控相互作用网络,该网络将数据中基因簇之间的关系浓缩为一个单一的图形表示。
缩写
- BN:
-
贝叶斯网络
- CND:
-
累积正态分布
- 罗斯福:
-
错误发现率
- GO-BP:
-
基因本体生物学过程
- MHB:
-
菌根辅助细菌
- MMN:
-
修改了梅林·诺克朗斯
- PGP:
-
促进植物生长
- RPKM:
-
每千碱基转录读数,每百万映射读数
参考文献
- 1.
史密斯SE,里德DJ。菌根共生关系。阿姆斯特丹:爱思唯尔学术出版社;2008.
- 2.
王晓明,张志刚,张志刚,张志刚。植物-外生菌根-根际细菌联合生长过程中磷不平衡的研究。土壤科学与植物营养学报,2015;15(2):464-85。
- 3.
李志强,李志强,李志强,等。植物根际和胚层促生长细菌的作用、定植、作用机制及应用前景。土壤生物化学。2010;42(5):669-78。
- 4.
菌根共生的生态学方面:特别强调涉及根外菌丝体的相互作用的功能多样性。中国机械工程学报,2008;29(5):529 - 529。
- 5.
丁志刚,李志刚,李志刚。植物-根际细菌相互作用缓解非生物胁迫条件。植物细胞环境学报。2009;32(12):1682-94。
- 6.
Podila GK, Sreedasyam A, Muratet MA。杨树根际与外生菌根相互作用组。植物学报,2009;28(5):359-67。
- 7.
ortizo - castro R, Contreras-Cornejo HA, macia - rodriguez L, Lopez-Bucio J.微生物信号在植物生长发育中的作用。植物信号行为学。2009;4(8):701-12。
- 8.
Garcia K, Delaux PM, Cope KR, Ane JM。建立和维持外生菌根共生所需的分子信号。植物学报。2015;208(1):79-87。
- 9.
菌根辅助细菌-菌根共生的新维度。中国植物学报。1994;41(4):517-21。
- 10.
Deveau A, Palin B, Delaruelle C, Peter M, Kohler A, Pierrat JC,等。菌根辅助菌Pseudomonas fluorescens BBc6R8对外生菌根真菌Laccaria bicolor S238N的生长、形态和基因表达具有特异性启动作用。中国生物科技,2007;26(4):344 - 344。
- 11.
Labbe JL, Weston DJ,敦刻尔克N, Pelletier DA, Tuskan GA。新发现的辅助细菌刺激杨树外生菌根的形成。4 .前沿植物科学2014;
- 12.
Navarro-Rodenas A, Berna LM, Lozano-Carrillo C, Andrino A, Morte A.有益的本地细菌提高了沙漠松露菌根植物在保育条件下的生存和菌根化。菌根。2016;26(7):769 - 79。
- 13.
Roesti D, Ineichen K, Braissant O, Redecker D, Wiemken A, Aragno M.与丛枝菌根真菌Glomus geosporum和Glomus constrictum孢子相关的细菌。应用环境微生物学,2005;71(11):6673-9。
- 14.
Frey-Klett P, Burlinson P, Deveau A, Barret M, Tarkka M, Sarniguet A.细菌-真菌相互作用:农业、临床、环境和食品微生物学家之间的连接。微生物学通报,2011;26(4):583。
- 15.
李志强,李志强,李志强,等。菌根辅助菌的研究进展。中国植物学报。2007;36(1):22-36。
- 16.
丛枝菌根真菌与土壤细菌的相互作用。中国生物医学工程学报,2011;29(4):344 - 344。
- 17.
在无菌条件下囊泡-丛枝菌根的建立。微生物学杂志,1962;27:209-520。
- 18.
Kurth F, Feldhahn L, Bonn M, Herrmann S, Buscot F, Tarkka MT.大规模转录组分析揭示了森林树木发育与有益菌根辅助细菌的相互作用。BMC基因组学。2015;16:658。
- 19.
Martin F, Duplessis S, Ditengou F, Lagrange H, Voiblet C, Lapeyrie F.外生菌根共生中的发育相声:信号和通信基因。生态学报,2001;26(1):344 - 344。
- 20.
普莱特,马丁。F.互惠效应者:共生的建筑师。入:Martin F, Kamoun S,编辑。植物-微生物相互作用中的效应子。霍博肯:威利;2012.p . 295 - 326。
- 21.
Schrey SD, Schellhammer M, Ecke M, Hampp R, Tarkka MT.菌根辅助菌链霉菌AcH 505诱导外生菌根真菌毒伞菌的差异基因表达。生态学报,2005;26(1):344 - 344。
- 22.
Noirot-Gros MF, Shinde S, Larsen PE, Zerbs S, Korajczyk PJ, Kemner KM,等。杨根被假单胞菌定殖的动态揭示了生物膜形成的菌株特异性和菌根特异性模式。前沿微生物,2018;9:853。
- 23.
Shinde S, Cumming JR, Collart FR, Noirot PH, Larsen PE。荧光假单胞菌转运体与营养胁迫下白杨幼苗的品系特异性植物生长促进有关。中国植物科学,2017;8:348。
- 24.
Larsen PE, Collart FR. BowStrap v1.0:使用短读转录组数据为表达基因分配统计显著性。BMC Res Notes. 2012;5:275。
- 25.
Lugtenberg B, Kamilova F.促进植物生长的根状细菌。微生物学报。2009;63:541-56。
- 26.
普莱特JM, Daguerre Y, Wittulsky S, Vayssieres A, Deveau A, Melton SJ,等。互惠菌的效应子MiSSP7Laccaria双色能稳定杨树JAZ6蛋白,抑制茉莉酸(JA)反应基因。中国科学(d辑),2014,26(3):344 - 344。
- 27.
丁香假单胞菌效应物AvrPto和AvrPtoB对植物免疫系统的抑制和激活。入:Martin F, Kamoun S,编辑。植物-微生物相互作用中的效应子。霍博肯:威利;2012.123 - 54页。
- 28.
Jones JDG, Dangl JL。植物免疫系统。大自然。2006;444(7117):323 - 9。
- 29.
诺克斯RB。植物的细胞识别:柱头表面的决定因素及其花粉相互作用。中国科学院学报(自然科学版),2001;26(3):389 - 397。
- 30.
西斯柯克SJ。植物自交不亲和反应中的花粉识别。中国生物医学杂志,2002;3(2):REVIEWS1004。
- 31.
Phytozome。可以从:https://phytozome.jgi.doe.gov.
- 32.
Wilkins KA, Poulter NS, Franklin-Tong VE。举一个例子:花粉中的自我识别和细胞自杀。中国机械工程学报,2014;26(5):529 - 529。
- 33.
李志强,李志强,李志强,等。植物自交不亲和的分子基础与进化动力学Pyrinae(蔷薇科).应用物理学报,2012;32(11):416 - 416。
- 34.
王志刚,王志刚,王志刚。植物自交不亲和的分子遗传学、生理生物学研究进展十字花科.P Jpn Acad b -物理。2012年,88(10):519 - 35。
- 35.
Slavov GT, DiFazio SP, Martin J, Schackwitz W, Muchero W, rogers - melnick E,等。基因组重测序揭示了白杨的多尺度地理结构和广泛的连锁失衡。植物科学进展。2012;36(3):344 - 344。
- 36.
Vigue LM, Lindroth RL。基因型、CO升高的影响2和升高的O3.对白杨植物化学和白杨叶甲虫性能的影响。昆虫学报。2010;12(3):267-76。
- 37.
Wullschleger SD, Weston DJ, DiFazio SP, Tuskan GA。回顾第一个树木基因组的测序:白杨。树物理学报,2013;33(4):357-64。
- 38.
图斯坎,李志刚,杨松,李志刚,等。黑杨木(Populus trichocarpa, Torr.)基因组。&灰色)。科学。2006;313(5793):1596 - 604。
- 39.
Martin F, Aerts A, Ahren D, Brun A, Danchin EGJ, Duchaussoy F,等。基因组Laccaria二色的提供洞察菌根共生。大自然。2008;452(7183):88 -得以。
- 40.
- 41.
Silby MW, Cerdeno-Tarraga AM, Vernikos GS, Giddens SR, Jackson RW, Preston GM,等。植物多样性和相互作用的基因组和遗传分析荧光假单胞菌.中国生物医学工程学报。2009;10(5):R51。
- 42.
Preston GM, Bertrand N, Rainey PB。III型分泌物促进植物生长荧光假单胞菌SBW25。中华微生物学杂志,2001;41(5):999-1014。
- 43.
NCBI。可以从:https://www.ncbi.nlm.nih.gov/genome.
- 44.
Cumming JR, Swiger TD, Kurnik BS, Panaccione DG。二色漆花和烟皮花暴露于铝的体外有机酸渗出。《中华人民共和国宪法》2001;31(4):703-10。
- 45.
李志强,李志强,李志强,等。外生菌根真菌的分离、维持及纯培养操作。入:Schenck N,编辑。菌根研究方法与原则。圣保罗:APS出版社;1982.115 - 29页。
- 46.
杨晓明,刘志刚,张志刚,张志刚。不同施肥条件下沙柳菌根形成的影响。森林生态杂志,2002;160(1-3):35-43。
- 47.
Brundrett MC, Piche Y, Peterson RL。囊泡-丛枝菌根形态观察的新方法。中国机械工程学报,2004;29(3):344 - 344。
- 48.
Brundrett MC, Bougher N, Dell B, Grove T, Malajczuk N。入:林奇P,编辑。林业和农业菌根:ACIAR;1996.p . 173 - 93。
- 49.
试剂盒。可以从:https://www.qiagen.com/us/resources.
- 50.
Langmead B, Trapnell C, Pop M, Salzberg SL.人类基因组短DNA序列的超快和内存高效对齐。中国生物工程学报。2009;10(3)。
- 51.
控制错误发现率——一种实用而有力的多重测试方法。中国生物医学工程学报。2001;26(1):1 - 7。
- 52.
Bolstad BM, Irizarry RA, Astrand M, Speed TP。基于方差和偏倚的高密度寡核苷酸阵列数据归一化方法比较。生物信息学。2003;19(2):185 - 93。
- 53.
Rousseeuw PJ。剪影-用于解释和验证聚类分析的图形辅助。应用数学学报。1987;20:53-65。
- 54.
Carbon S, Dietze H, Lewis SE, Mungall CJ, Munoz-Torres MC, Basu S,等。基因本体知识库和资源扩充。核酸研究,2017;45(D1): D331-D8。
- 55.
数学统计与数据分析(第三版)。波士顿:圣智学习;2013.
- 56.
刘志强,刘志强,刘志强。神经信息流网络的计算推理。公共科学图书馆,计算生物学,2006;2(11):e161。
- 57.
确认
下一代测序服务由芝加哥大学基因组学和系统生物学研究所(IGSB)的高通量基因组分析核心提供。
数据和材料的可用性
在当前研究中产生的原始转录组数据可根据合理要求从通讯作者处获得。在此研究过程中产生或分析的所有其他数据都包含在本文及其补充信息文件中。
资金
该研究在阿贡国家实验室的“环境传感与响应”科学重点领域(SFA)下进行,并得到了美国能源部(DOE)科学办公室(BER)生物与环境研究办公室(基因组科学计划)的支持。作者声明资助机构在研究设计和数据收集、分析、解释或撰写手稿方面发挥了任何作用。
作者信息
从属关系
贡献
SS, JC, FC和PL参与了实验设计。SS和JC监督生物学实验和分析,SZ进行RNA提取和转录组文库制备。PL进行了计算分析,所有作者都对结果的解释做出了贡献。PL, PN和JC撰写了手稿,所有作者都阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
美洲山杨(Michx.)种子来自加拿大自然资源国家树木种子中心。国家树木种子中心免费为科学研究提供少量种子。Laccaria二色的(Marie) S238 N从ATCC获得。
发表同意书
不适用。
相互竞争的利益
作者宣称他们之间没有利益冲突。
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
附加文件
附加文件1:
RNAseq对齐表。表中显示了每个测序反应的总读数,与每个社区成员对齐的读数,以及与每个社区成员对齐的总读数的百分比。(xlsx9kb)
附加文件2:
RPKM评分为所有样本。该文件包括Bowstap分析白杨基因表达的转录组数据和ANOVA结果。数据类型为“Unique RPKM”,它忽略了与多个基因对齐的序列片段,“Ave RPKM”是包括多个对齐序列在内的引导分析的结果,“SD RPKM”是引导对齐RPKM值的标准差,“Log2Norm RPKM”是标准化的基因表达值,“pVal”是由Bowstrap分析计算出的基因表达的显著性,ANOVA-pVal是存在方差分析的显著性Laccaria(LBI)、SBW25的存在以及相互作用条件。(CSV 22927kb)
附加文件3:
注释的转录组,按表达簇分组。数据以Excel文件的形式呈现,其中包含每个共同调控基因簇的工作表。在每个工作表中,给出了基因ID,基因表达(归一化RPKM),方差分析显著性,相对于白杨根条件的Log2倍变化,以及基因注释。注释数据包括“Phytozome”和“拟南芥信息资源”中附加基因信息的链接。(xlsx2256kb)
附加文件4:
按聚类划分的丰富GO-BP注释表。富集BP-GO注释按共表达基因簇进行分组。每个注释项后括号内的数字表示在聚类中具有该注释的基因的数量。(xlsx9kb)
权利和权限
开放获取本文根据创作共用属性4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),允许在任何媒介上不受限制地使用、分发和复制,前提是您对原作者和来源给予适当的赞扬,提供到创作共用许可证的链接,并注明是否进行了更改。创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)除另有说明外,适用于本条所提供的资料。
关于本文
引用本文
Shinde, S., Zerbs, S., Collart, F.R.et al。荧光假单胞菌白杨幼苗根系菌根化和抗真菌防御反应基因表达的调控。BMC植物生物学19日,4(2019)。https://doi.org/10.1186/s12870-018-1610-0
收到了:
接受:
发表:
关键字
- Ectomycorrhiza
- Laccaria二色的
- 菌根辅助细菌
- 美洲山杨
- 受体
- 转录组