摘要
背景
地瓜(番薯甘薯是全球种植的七大粮食作物之一。低温胁迫常引起甘薯块根蛋白表达模式和物质含量的变化。近年来,我们研究了新鲜甘薯的蛋白质代谢谱。(新乡),试图揭示块根类作物在采后贮藏过程中对冷胁迫的响应机制。
结果
4℃贮藏的根系CI指数、REC和MDA含量均显著高于对照温度(13℃)。SOD、CAT、APX、O2.-产量、脯氨酸、特别是可溶性糖含量均显著提高。大多数差异表达蛋白(DEPs)与代谢通路相关,尤其是苯丙素,其次是淀粉和蔗糖代谢。l -抗坏血酸过氧化物酶3和过氧化氢酶在低温贮藏过程中表达下调。α-淀粉酶、蔗糖合成酶和果糖激酶在淀粉和蔗糖代谢中显著上调,β-葡萄糖苷酶、葡萄糖-1-磷酸腺苷转移酶和淀粉合成酶则相反。此外,代谢组分析显示,硫代葡萄糖苷生物合成、莨菪烷、哌啶和吡啶生物碱的生物合成以及蛋白质的消化和吸收在根的代谢途径中起主导作用。亮氨酸、色氨酸、酪氨酸、异亮氨酸和缬氨酸在硫代葡萄糖苷生物合成中均显著上调。
结论
低温贮藏甘薯的蛋白质组学和代谢谱分析表明,甘薯的抗氧化酶活性、脯氨酸和可溶性糖含量显著提高。大多数DEPs与苯丙类化合物有关,其次是淀粉和蔗糖代谢。蛋白质组(l -抗坏血酸过氧化物酶3和过氧化氢酶)和生化(CAT/APX活性)数据之间的差异可能是由较高的H2O2抗坏血酸氧化还原状态增加,间接增强CAT/APX活性。硫代葡萄糖苷生物合成在代谢途径中起主导作用。亮氨酸、色氨酸、酪氨酸、异亮氨酸和缬氨酸在硫代葡萄糖苷生物合成中均显著上调。
背景
地瓜(番薯甘薯L.),一种双子叶植物,属于旋花科植物家庭是世界上第七大最重要的粮食作物。贮藏根作为植物的主要营养器官,含有大量的淀粉和光合产物。淀粉占干物质的50-80% [1,2].在一般的生产过程中,刚收获的块茎可溶性糖含量很低,为了促进淀粉-糖的相互转化,提高甜度以提高块茎食品的售前品质,采后储存在13-15℃的一定时间是必要的。值得注意的是,在5°C下暴露20 d可以增加“Kokei 14”根的甜度,然而,这种处理也会导致腐烂和碳水化合物的高损失率[3.].因此,更好地了解低温胁迫下块茎作物的生化和分子响应机制是延长块茎作物低温贮藏时间的必要条件。
与模式植物相比,甘薯由于其复杂的遗传背景,更难以找到与各种抗胁迫能力相关的基因。虽然有些基因组[4,5]和蛋白质组学[6,7,8[摘要]虽然目前已有甘薯的资源,但这些资料对阐明甘薯抗冷分子机制仍有一定的局限性。随着测序技术的发展,代谢组学被认为是获取代谢产物相关生物学信息的有力补充工具。代谢物不仅是某些基因表达的最终产物,也是基因组与其环境相互作用的结果。因此,通过将基因表达与代谢组学知识联系起来,很可能设想功能基因组学组装[9].
作为一种对寒冷敏感的热带作物,当温度降到10℃以下时,红薯就会受到不可挽回的损害。造成这种情况的主要原因是活性氧(ROS)积累增加所造成的氧化损伤[10,11,12,13,14,15,16].在植物中,胁迫诱导的ROS清除通常是通过酶促和非酶促的低分子代谢抗氧化剂来实现的[17,18].众所周知,红薯鲜根的淀粉含量约为15-30% [8].可溶性糖不仅是淀粉生产的底物,而且可能是块茎低温防御的信号。
为了更好地探索低温条件下甘薯的蛋白质和代谢途径,我们对新鲜甘薯进行了蛋白质代谢组学分析,以阐明其冷胁迫响应机制。整合蛋白质组学和代谢组学信息将为块根作物收获后贮藏的分子功能提供新的认识。这将为未来对这一重要作物的比较蛋白质组学研究提供基础,包括基因的发现和抗寒性的提高。
结果
冷库下的形态变化
研究低温胁迫对新鲜收获的甘薯贮藏的影响。在13℃(CK)和4℃(d)条件下保存14天。如图所示。1和表113°C时根系无冷害症状,4°C时根系表皮无冷害症状(图1)。1b)与保存在13°C下的相比,有明显斑点和枯萎(图。1a). CI指数也显著高于对照根。此外,水分含量在13℃下显著降低,而在低温(4℃)下无差异。
低温贮藏对氧化应激的影响
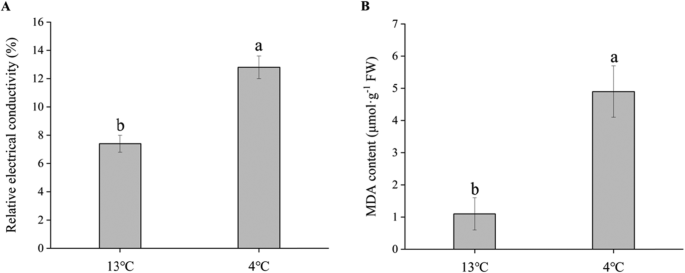
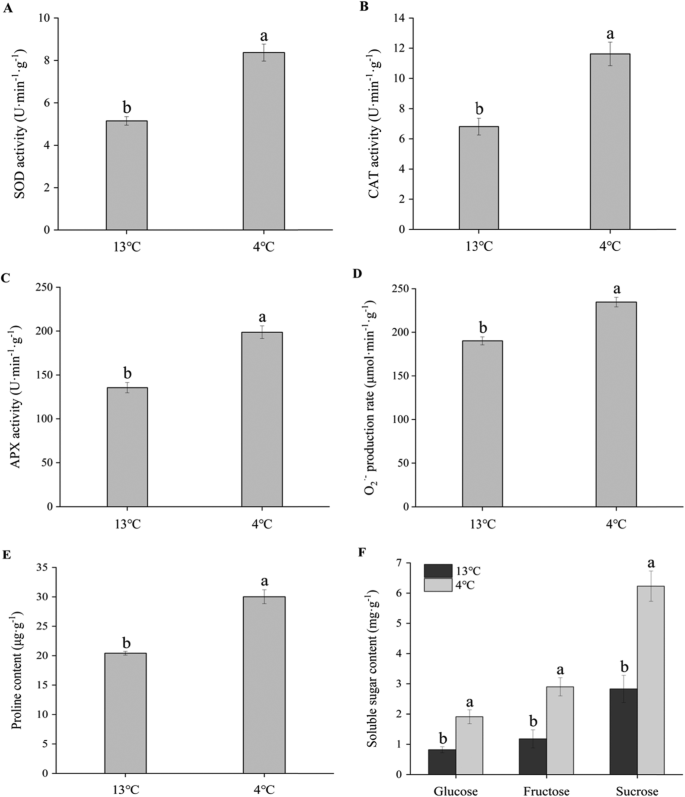
暴露在4℃条件下的根的相对电导率(REC)水平和丙二醛(MDA)含量显著高于暴露在13℃条件下的根(图2)。2).SOD、CAT、APX、O2.-产量、脯氨酸和可溶性糖含量如图所示。3..同样,低温(4℃)显著提高了抗氧化酶的活性(图5)。3.a, b, c)和O的产量2.-(无花果。3.d).此外,低温胁迫也增强了脯氨酸含量(图5)。3.e)、葡萄糖、果糖和蔗糖(图。3.f)的内容。值得一提的是,在上述生理指标中,3种可溶性糖含量增加最多,分别增加了112.4、145.6和139.4%。
蛋白质的分离和鉴定
与对照相比,在4℃贮藏的根中,发现266和158个蛋白分别被>显著上调和下调1.5倍(补充表S2额外的文件1和额外的文件2).蛋白条带清晰、均匀,各条带未降解(补充图S1).鉴定蛋白的分子质量分布在5-275 kDa,其中大部分(96%)蛋白分布在< 100 kDa范围内(补充图S2).提取的蛋白适合进一步的LC-MS/MS分析。
DEPs在GO分类、亚细胞定位和通路富集中的注释
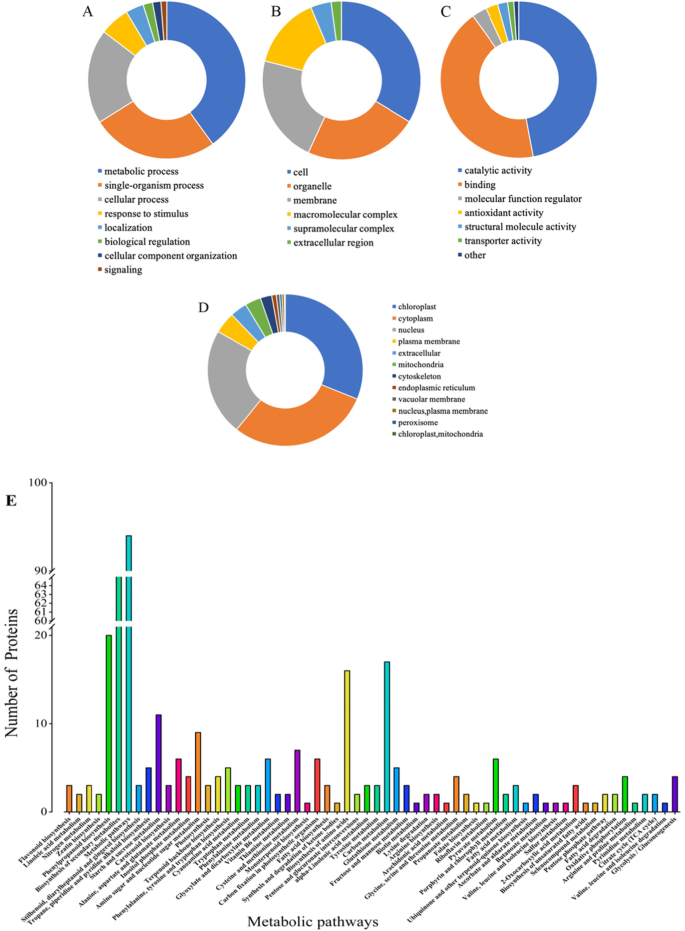
差异表达蛋白(DEPs)功能及其细胞位置的注释对于理解其在分子水平上的作用是必要的3.).结果显示,他们被分为15个不同的类别。这些蛋白主要参与代谢过程、细胞成分、催化活性和结合(图。4a, b, c)。主要与催化活性(~ 47%)有关,其次是结合活性(~ 43%)、代谢过程(~ 40%)、细胞活性(~ 34%)和细胞器活性(~ 23%)。
此外,副主管人员的委派取决于他们是否在特定的部门(附加文件4).大部分分布在叶绿体/细胞质中(~ 30%),其次是细胞核(~ 15%)和质膜(~ 5%)(图4)。4d)。
通过KEGG数据库进一步分析确定的蛋白质,以解释它们参与不同的代谢途径(附加文件5).大多数DEPs与代谢途径相关的通路有关(~ 22%),其次是次生代谢物的生物合成(~ 16%)和苯丙类化合物的生物合成(图。4e)。
参与苯丙烷生物合成的DEPs
如前所述,大部分蛋白质参与次生代谢产物的代谢途径和生物合成。苯丙氨酸解氨酶(PAL)、肉桂醇脱氢酶(CAD)、羟基肉桂酰基转移酶(HCT)调控的酚类化合物列于表中2.的p这些蛋白的价值与其在苯丙类生物合成途径中的意义呈负相关。因此,DEPs的显著性顺序为石草酸酯>过氧化物酶4 > 4-香豆酸辅酶a连接酶>细胞色素P450(细胞色素P450单加氧酶)> PAL>CAD。
差异倍数的DEPs参与淀粉和蔗糖的代谢
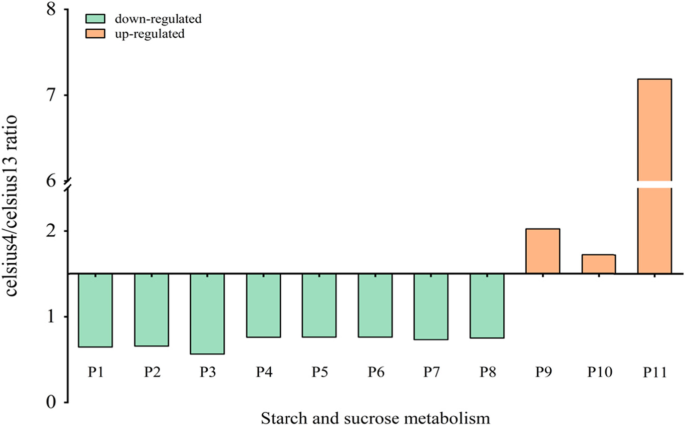
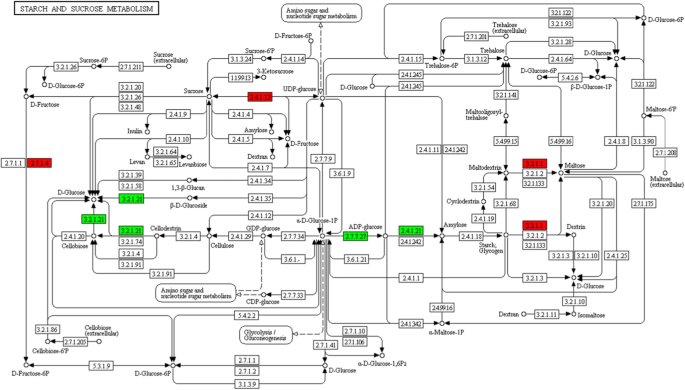
与13℃时相比,4℃时有11个DEPs参与淀粉和蔗糖代谢(图1)。5).过滤后的p值矩阵(p由函数x =−lg (p值)来评估celesius4/celesius13比值,该比值与DEPs的微分倍数正相关。3个蛋白(x > 1.5)上调,而其他蛋白(x < 1.5)在该代谢途径中呈现相反的趋势。蔗糖合酶(P11)和β-葡萄糖苷酶(P3)的比值分别为7.19和0.56,分别显著高于和低于其他蛋白质(图)。5).
DEPs在淀粉和蔗糖代谢中的功能网络
根系在冷胁迫下的功能网络如图所示。6.有三个上调的dep和三个下调的dep。与淀粉代谢和碳水化合物消化或吸收有关的α-淀粉酶(EC: 3.2.1.1,红色)在麦芽糊精或淀粉水解为麦芽糖时显著上调。与K01177 (β-淀粉酶:EC: 3.2.1.2)、K05992(产麦芽α-淀粉酶:EC:3.2.1.133)同源。同样,EC: 2.4.1.13(蔗糖合成酶)和EC: 2.7.1.4(果糖激酶)在氨基和核苷酸糖代谢中均显著上调。另一方面,EC: 3.2.1.21、EC: 2.7.7.27和EC: 2.4.1.21蛋白分别为β-葡萄糖苷酶、葡萄糖-1-磷酸腺苷转移酶和淀粉合成酶,在淀粉和蔗糖代谢途径中被显著下调。它们主要参与苯丙类生物合成、淀粉和次生代谢物的生物合成以及多糖的积累。淀粉降解为可溶性糖不仅能提高甜度,而且能显著提高抗寒性。
代谢组分析及其折叠变化分析
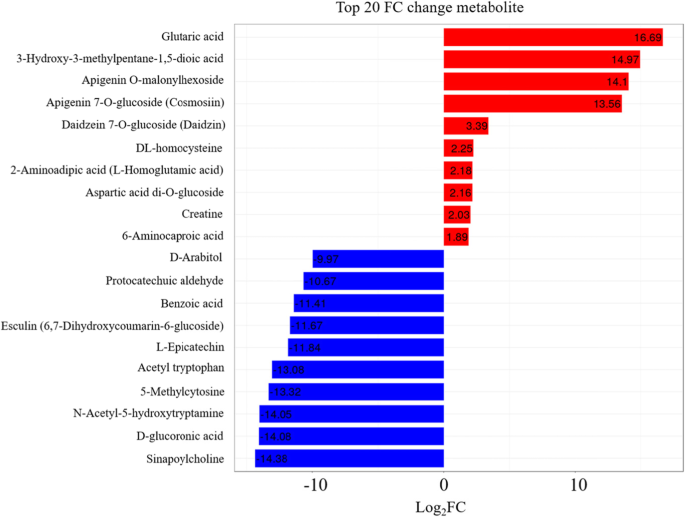
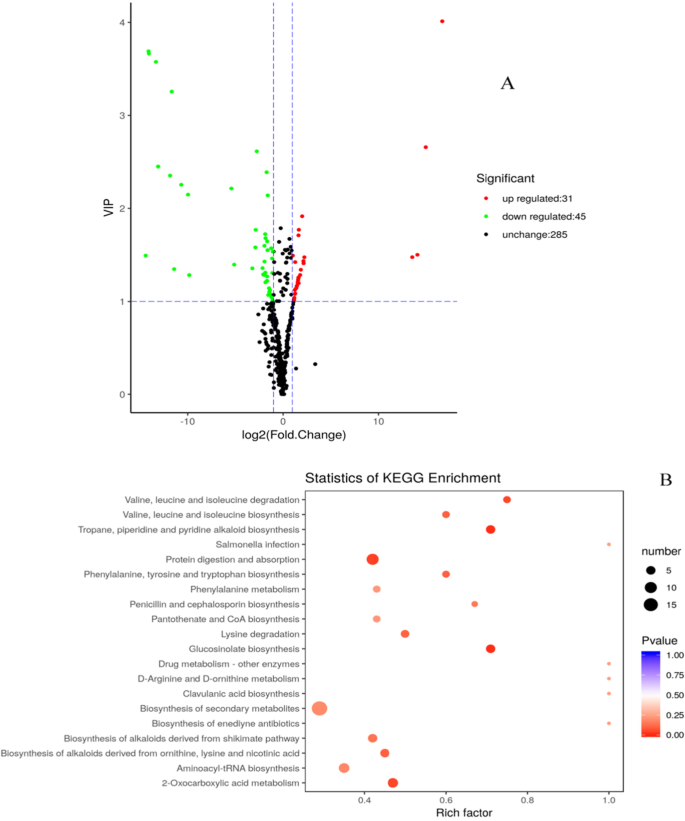
通过对甘薯块茎的代谢组分析,发现在4℃和13℃贮藏的甘薯块茎中存在76种差异表达代谢物(dem)。有31种代谢产物上调,45种代谢产物下调(补充表S3.和额外的文件6).折叠变化(FC)的绝对值水平与代谢成分的显著性密切相关。结果(图。7)表明绝对对数2上调代谢产物中4个成分的FC值均大于10.00,其中戊二酸(16.69)、3-羟基-3-甲基戊烷-1,5-二二酸(14.97)、芹菜素o -丙二醛己糖苷(14.1)、芹菜素7- o -葡萄糖苷(cosmosiin)(13.56)次之。然而,在下调的dem中,有9个成分的绝对值大于10,分别是胆碱(14.38)、d -葡醛酸(14.08)、n-乙酰-5-羟色胺(14.5)、5-甲基胞嘧啶(13.32)等。在4℃下,根系中大部分鉴定成分的代谢活性下降。
低温胁迫下根系中dem的筛选与分布
与折叠变化的绝对值水平相比,项目变量重要性(Variable Importance in Project, VIP)值(> 1)与相应类代谢化合物的显著性极相关。所有识别的dem被分为20类。其中大部分(约33%)属于核苷酸及其衍生物和氨基酸衍生物群。在VIP和Log的基础上2FC值,结果见表3.结果表明,除3-羟基-3-甲基戊烷-1,5-二酸和戊二酸外,其余成分均下调。VIP和日志2戊二酸的FC值最高,分别为4.01和16.69,其次为d -葡醛酸(3.69和14.08)、n -乙酰-5-羟色胺(3.66和14.05)和5-甲基胞嘧啶(3.58和13.32)(表3)3.和无花果。8a)碳水化合物以d -葡萄糖醛酸为代表,是糖代谢的重要成员。
此外,根据它们进行KEGG途径富集P-价值和丰富的因素。p值和富集因子分别与代谢化合物富集显著性呈负相关和正相关。硫代葡萄糖苷生物合成、莨菪烷、哌啶和吡啶生物碱生物合成的p值(9.94 × 10−3)明显低于蛋白质消化吸收(3.56 × 10)−2)(表4和无花果。8b)。
芥子油苷生物合成中差异代谢化合物的网络
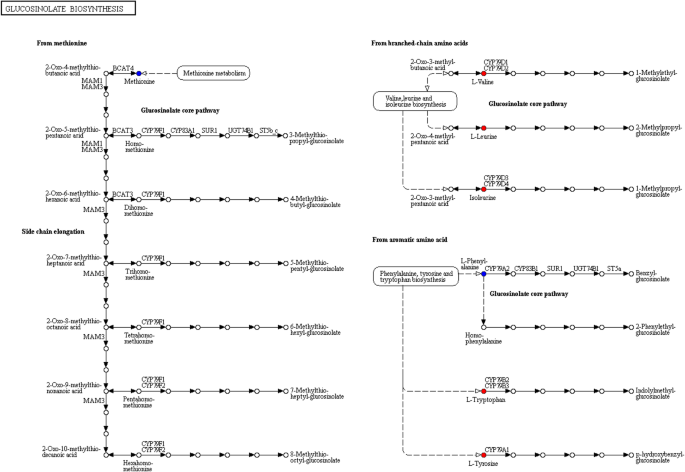
如前所述,由亮氨酸(Leu)、色氨酸(Try)、酪氨酸(Tyr)、异亮氨酸(Ile)和缬氨酸(Val)等氨基酸组成的硫代葡萄糖苷生物合成在提高甘薯根系耐冷性的代谢途径中具有重要作用。硫代葡萄糖苷可由蛋氨酸、支链氨基酸或芳香族氨基酸合成。9).Leu、Ile和Val参与支链氨基酸。Try和Tyr在芳香族氨基酸通路中是必不可少的。所有这些氨基酸在硫代葡萄糖苷生物合成中均显著上调。9).
讨论
活性氧清除和渗透调节物质
低温、干旱和盐碱等环境胁迫严重限制了高等植物的生长和生产力。丙二醛含量和离子泄漏是冷胁迫引起膜损伤的指标。吉尔等人[19]描述了过量ROS会导致MDA升高、膜渗漏和DNA破裂,对植物细胞造成严重的损伤。植物在ROS存在的情况下进化,并获得了专门的途径来保护自己免受氧化损伤,并对低水平ROS进行信号转导的精细调节[20.,21,22,23,24].清除ROS机制的酶促系统主要包括SOD、POD、CAT和APX [25].细胞内基因的表达CuZnSOD而且swAPX1与低温应力(4℃)显著相关[26].SOD能迅速将·OH转化为H2O2,生成的H2O2然后被CAT和APX转化为水和氧气[27,28,29].然而,水稻细胞质APXs基因双沉默(APX1/2 s)突变体的抗非生物胁迫能力增强[30.].在我们的研究中,l -抗坏血酸过氧化物酶3和过氧化氢酶在4°C存储期间被下调2),然而CAT/APX活性(图。3.B, c)增加。蛋白质组学和生化数据之间的差异可能是由H2O2抗坏血酸氧化还原状态增加,间接增强CAT/APX活性。
诱导渗透保护剂的生物合成是植物对低温的另一种反应。几项研究表明,提高非生物的耐受力是通过引入其他生物的简单代谢性状,如海藻糖和脯氨酸的产生[31].最近的数据表明过度表达DlICE1(花芽龙眼l .)转基因拟南芥通过增加脯氨酸含量和抗氧化酶如SOD、CAT、APX的含量来增强耐寒性[32].在我们的研究中,低温(4℃)显著提高了抗氧化酶的活性(图5)。3.a, b, c), O的产率2.-(无花果。3.d)和脯氨酸含量(图。3.e)与对照(13°C)相比。因此,膜脂过氧化对甘薯根系的损伤较小,能够在低温条件下继续正常代谢,具有较高的耐寒性。
非生物胁迫下酚类化合物和硫代葡萄糖苷生物合成的作用
苯丙素是由氨基酸苯丙氨酸合成的一组次级代谢物[33,34].植物抗非生物胁迫的苯丙素途径与植物的生理和分子机制密切相关。当植物面临多重非生物胁迫时,酚的积累通常被激活[35].增加酚水平在植物抵御低温胁迫中起着关键作用[36].高等人。[37]通过低温胁迫下桃的实验,证实了受到刺激的酚类生物合成是由于PAL、CAD和HCT的表达增强。在我们的研究中,苯丙类生物合成是主要的代谢途径,被大量蛋白质上调,尤其是HCT、PAL和CAD(图1)。4e和表2).因此,我们的结果与之前的研究是一致的。更重要的是,没有发现根系腐烂(图。1和表1)可能是由于植物细胞壁因酚积聚而增厚,有利于防止冷害[38,39].
硫代葡萄糖苷主要作为防御分子[40].它们也被称为芥子油糖苷。到目前为止,已经在植物中发现了100多种硫代葡萄糖苷。根据前体氨基酸的不同,硫代葡萄糖苷可分为吲哚型硫代葡萄糖苷、脂肪族硫代葡萄糖苷和芳香型硫代葡萄糖苷,分别来源于Trp、Ala、Leu、Ile、Val/Met和Phe和Tyr [41].这些结果与我们的研究结果一致4和无花果。9).先前的研究表明,在两种拟南芥突变体中,硫代葡萄糖苷生物合成中间体的积累可以限制苯丙素的产生ref2而且ref5[42,43].然而,苯丙酯和硫代葡萄糖苷的生物合成之间似乎没有明显的相互作用。
甘薯根中的糖作为抗氧化剂
甘薯因其较高的吸收强度而被认为是淀粉产量最高的作物之一[44].可溶性糖通过调节ROS的产生代谢途径,如线粒体呼吸或光合作用,与ROS的产生速率有关[45].块茎作物淀粉含量与蔗糖呈显著负相关,这是因为在低温贮藏条件下,呼吸频率降低,淀粉的分解代谢受到损害。在我们的研究中,三种可溶性糖含量明显增加(图。3.f).此外,α-淀粉酶、β-淀粉酶、蔗糖合成酶和果糖激酶显著上调,促进了低温下块茎根的甜度(图5)。5而且6).结果表明,甜度可以提高甘薯根系的抗寒性。
然而,近年来有人提出“糖是抗氧化剂”的概念[46],一些编码不同糖化合物的基因被证实可以增强矮牵牛、烟草和水稻的低温耐受性[47,48,49,50,51].水溶性碳水化合物(葡萄糖、果糖和蔗糖)被认为是植物对非生物/生物胁迫反应的关键调节因子,这一点已得到越来越多的认识。在干旱胁迫下,增加的可溶性糖的积累维持了高抗氧化保护拟南芥叶子(52].此外,低温还会影响植物的代谢活动,引起渗透胁迫。可溶性碳水化合物可稳定细胞膨压[53].因此,单糖和多糖都是植物在胁迫条件下生存所必需的[54,55].
结论
综上所述,我们对甘薯的蛋白质组学和代谢谱分析表明,在4℃贮藏的甘薯根的CI指数、REC和MDA含量远高于13℃贮藏的甘薯根。低温贮藏条件显著提高了SOD、CAT、APX、O的活性2.-产量,脯氨酸,特别是可溶性糖的含量。多数DEPs与代谢通路相关,尤其是苯丙类,其次是淀粉和蔗糖代谢。α-淀粉酶、蔗糖合成酶和果糖激酶在淀粉和蔗糖代谢中显著上调,β-葡萄糖苷酶、葡萄糖-1-磷酸腺苷转移酶和淀粉合成酶则相反。有趣的是,蛋白质组(l -抗坏血酸过氧化物酶3和过氧化氢酶)和生化(CAT/APX酶活性)数据存在差异,这可能是由于H2O2增加谷胱甘肽和抗坏血酸氧化还原状态,间接增强CAT/APX活性。此外,硫代葡萄糖苷生物合成在代谢途径中起主导作用。亮氨酸、色氨酸、酪氨酸、异亮氨酸和缬氨酸在硫代葡萄糖苷生物合成中均显著上调。这些结果将拓展我们对甘薯耐冷性蛋白质组和代谢组的认识。
方法
植物材料及贮存条件
地瓜(一、甘薯l .简历。),资料来自中国浙江省农业科学院(补充表S1),根据2018年的标准农业实践,在25-30°C的温室中,在长日照周期(16/8小时,明暗)下种植。选取大小相同、平均重量100 ~ 120 g的成熟根。他们没有身体损伤或细菌感染。然后随机分为2组,每组3个重复,分别在4℃和13℃(CK)的温湿度箱中饲养14 d(莱福MJX-280H,中国)。储存后,块茎切片至1mm厚,放入液氮中,在−80°C保存,以便进一步分析[26].
冷害指数的估计
表面凹陷、暗水样斑块和内部组织褐变是结节根的典型CI症状[26,56].每个重复选择10个根进行可视化CI评估。CI指数的计算根据Li等。[26].
相对电导率和丙二醛含量测定
相对电导率(REC)的测量方法如前所述,但作了一些修改[57].REC的计算是根据Hu等人的。[58].硫代-巴比妥酸法测定丙二醛含量[58].
测定抗氧化酶、O2·-产量和脯氨酸含量
为了测定酶活性,将新鲜根(0.1-0.5 g)均质于10ml 50mm预冷磷酸钾缓冲液(PBS;pH值7.8)下的低温条件[59].超氧化物阴离子(O2·-)生产速率根据蒋、张[60,只是做了一些修改。超氧化物歧化酶(SOD)、过氧化氢酶(CAT)和抗坏血酸过氧化物酶(APX)活性测定依据Dhindsa & Matowe [61], Aebi [62]、中野和浅田[63),分别。脯氨酸含量由Bates等人测定。[64].
可溶性糖组成的测定
采用高效液相色谱法(HPLC)测定根中可溶性糖(葡萄糖、果糖和蔗糖)的组成。高效液相色谱法的程序是根据Li等人。[26].
蛋白质提取和1-DE SDS-PAGE
将甘薯果肉用液氮研磨成细粉,用高强度超声处理器将4体积的裂解缓冲液(8 M尿素、1% trton -100、10 mM二硫苏糖醇和1%蛋白酶抑制剂鸡尾酒)加入超声提取液中,在冰上三次。超声时间为超声3s,暂停6s,共20个循环。蛋白质样品用12% SDS PAGE凝胶电泳,考马斯亮蓝R-250染色。
消化肽的LC-MS/MS
将胰蛋白酶肽加载到自制的反相分析柱(15 cm长,75 μm id)上。将消化后的肽进行NSI源检测,然后在Q Exactive™Plus (Thermo Scientific)中进行串联质谱(LC-MS/MS)分析。然后选择多肽进行MS/MS, NCE设为28,在Orbitrap中以17,500的分辨率检测片段[65].
蛋白质数据库检索
在单端口刚地弓形虫数据库中使用Maxquant搜索引擎(v.1.5.2.8)对生成的MS/MS数据进行处理。串联质谱检索Vert_tom_20141002数据库(117,248个条目)。半胱氨酸上的卡酰胺甲基被指定为固定修饰,Met上的氧化被指定为可变修饰[66].
生物信息学分析
基因本体(GO)注释蛋白质组来源于UniProt-GOA数据库(http://www.ebi.ac.uk/GOA/).识别的蛋白质结构域功能描述由InterProScan (http://www.ebi.ac.uk/interpro/)基于蛋白质序列比对方法采用InterPro域数据库。利用京都基因与基因组百科数据库(KEGG)注释蛋白质通路。用wolfpsort软件(PSORT/PSORT II)预测蛋白质的定位。对于功能富集,采用双尾Fisher’s精确试验来测试DEPs对所有识别的蛋白质的富集。
块茎的代谢组分析
块茎切片至1mm厚度,使用混合磨机(MM400, Retsch)与氧化锆珠在30 Hz下破碎1.5分钟。用1.0 ml 70%甲醇水溶液在4℃下提取100 mg肉粉过夜。样品提取采用LC-ESI-MS/MS系统(HPLC, Shim-pack UFLC SHIMADZU CBM30A, MS, Applied Biosystems 6500 Q TRAP)进行分析。阎等人提出了代谢组学方法。[67只是做了一些修改。
蛋白质和代谢物数据分析
在软件数据库(MWDB) (https://www.metware.cn).PubChem (https://pubchem.ncbi.nlm.nih.gov/)用于他们的分类。可能比较的显著性分析(p值)在p< 0.05。过滤后的p由函数x =−lg (pvalue)用于评价celesius4与celesius13的比值,该比值与DEP的表达倍数(x > 1.5)呈正相关。采用分析1.6.1、偏最小二乘-判别分析(PLS-DA)和正交偏最小二乘-判别分析(OPLS-DA)模型对所有代谢产物进行方差和均值分离分析。数据由origin2018绘制。
数据和材料的可用性
当前研究过程中生成的数据集可在PRIDE合作伙伴库中获得,登录号为PXD017728,https://www.ebi.ac.uk/pride/login,如有合理要求,可向通讯作者(杨胡清、yanghuqing@sohu.com).
缩写
- APX型:
-
抗坏血酸盐过氧化物酶
- 参数:
-
精氨酸
- 计算机辅助设计:
-
肉桂醇脱氢酶
- 猫:
-
过氧化氢酶
- 置信区间:
-
冷害
- 民主党:
-
差异表达代谢物
- DEPs:
-
差异表达的蛋白质
- 舰队指挥官:
-
褶皱变化
- 走:
-
基因本体论
- HCT:
-
Hydroxycinnamoyl转移酶
- Ile:
-
异亮氨酸
- KEGG:
-
京都基因和基因组百科全书
- 低浓缩铀:
-
亮氨酸
- 利斯河:
-
赖氨酸
- MWDB:
-
Metware数据库
- OPLS-DA:
-
正交偏最小二乘-判别分析
- 朋友:
-
苯丙氨酸氨裂解酶
- PLS-DA:
-
偏最小二乘-判别分析
- ROS:
-
活性氧
- O2:
-
超氧化物阴离子
- SOD:
-
超氧化物歧化酶
- 试一试:
-
色氨酸
- 酪氨酸:
-
酪氨酸
- 瓦尔:
-
缬氨酸
- 贵宾:
-
项目中的可变重要性
参考文献
- 1.
Scott GJ, Rosegrant MW, Ringler C.到2020年块茎作物全球预测。食品政策。2000;25:561 - 97。
- 2.
Tumwegamire S, Kapinga R, Rubaihayo PR, Labonte DR, Grüneberg WJ, Burgos G,等。东非甘薯干物质、蛋白质、淀粉、蔗糖、β-胡萝卜素、铁、锌、钙和镁含量评价[番薯甘薯(l) lam)种质。HortScience。2011; 46:348-57。
- 3.
增田D,福冈N,后藤H,卡野y。采后冷处理对甘薯含糖量及贮藏性的影响(番薯甘薯l .)。Horticult杂志2007;6:597 - 601。
- 4.
李锐,翟宏,康春,刘东,何硕,刘强。新创橙瓤甘薯转录组测序及类胡萝卜素生物合成相关差异表达基因分析。国际基因组学杂志2015;2015:802 - 12。
- 5.
王铮,方斌,陈杰,张旭,罗铮,黄磊,等。新创利用illumina配对测序对甘薯根系转录组的组装、鉴定及ssr标记的开发(番薯甘薯).BMC基因组学。2010;11:726。
- 6.
李俊杰,Park KW, Kwak Y-S, Ahn JY, Jung YH, Lee B-H,等。浅橙色和紫色红薯品种块根蛋白质组学的比较研究。植物科学。2012;193 - 194:120 9。
- 7.
李俊杰,金英华,郭秀云,安俊英,金普杰,李波夫,等。甘薯块根与贮藏根蛋白质组学差异的比较研究(番薯甘薯(l) lam)。植物生理与生物化学,2015;87:92-101。
- 8.
蒋勇,陈超,陶晓,王杰,张颖番薯甘薯(l)。块茎状的根。Mol Biol rep 2012; 39:8015-25。
- 9.
Shekhar S、Mishra D、Buragohain AK、Chakraborty S、Chakraborty N.两个对照甘薯品种植物化学成分和养分利用率的比较分析(番薯甘薯l .)。食品化学。2015;173:957 - 65。
- 10.
Suntres泽。抗氧化剂在百草枯毒性中的作用。毒理学。2002;180:65 - 77。
- 11.
黄晓明,王晓明,王晓明,等。紫外- b辐射对植物免疫应答的影响。平衡伤害和保护。植物杂志。2003;133:1420-8。
- 12.
Suzuki N ., Mittler R.活性氧种类和温度应力:信号传递和破坏之间的微妙平衡。杂志杆菌。2006;126:45-51。
- 13.
Torres MA, Jones jg, Dangl JL。对病原体作出反应的活性氧信号。植物杂志。2006;141:373-8。
- 14.
夏尔马SS,迪茨KJ。金属毒性与细胞氧化还原失衡的关系。植物学报2009;14:43-50。
- 15.
罗兰F,范登Ende W.植物细胞中糖信号与抗氧化网络的连接。2月j . 2010; 277:2022-37。
- 16.
杨晓燕,张晓燕,张晓燕,等。干旱和盐胁迫下活性氧的内稳态和信号转导。植物细胞环境学报2010;33:453-67。
- 17.
氧化应激、抗氧化剂与应激耐受性。植物学报2002;7:405-10。
- 18.
作物植物抗非生物胁迫中的活性氧种类和抗氧化机制。植物生理与生物学报2010;48:909-30。
- 19.
Gill RA,臧丽玲,Ali B, Farooq MA,崔鹏,杨姝,等。铬对4个品种的理化和超微结构的影响芸苔属植物显著l .臭氧层。2015;120:154 - 64。
- 20.
Choudhury FK, Rivero RM, Blumwald E, Mittler R.活性氧种类,非生物胁迫和胁迫组合。植物j . 2017; 90:856 - 67。
- 21.
植物氧化还原信号的研究进展。抗氧化氧化还原信号。2013;18:2087-90。
- 22.
Considine MJ, Sandalio LM, Foyer CH.阐明植物如何从ROS和NO反应中获益,同时抵抗氧化应激。安机器人。2015;116:469 - 73。
- 23.
迪茨KJ。高效的强光适应涉及多个机制层面的快速过程。J Exp Bot。2015;66:2401-14。
- 24.
Mignolet-Spruyt L, Xu E, Idanheimo N, Hoeberichts FA, Muhlenbock P, Brosche M,等。传播新闻:亚细胞和细胞器活性氧的产生和信号。J Exp Bot. 2016; 67:3831-44。
- 25.
活性氧:代谢、氧化应激和信号转导。植物生物学2004;55:373-99。
- 26.
李鑫,杨海强,陆国强。低温处理与冷藏相结合诱导甘薯块根快速增甜(番薯甘薯(l)Lam)同时抑制冷害。生物技术,2018;142:1-9。
- 27.
Gechev TS, Van Breusegem F, Stone JM, Denev I, Laloi C.活性氧作为调节植物胁迫反应和程序性细胞死亡的信号。Bioessays。2006;28:1091 - 101。
- 28.
Mittler R. ROS很好。植物科学进展2017;22:11-9。
- 29.
尤军,陈忠忠。作物非生物胁迫响应中活性氧的调控。植物科学进展2015;6:1092。
- 30.
Bonifacio A, Martins MO, Ribeiro CW, Fontenele AV, Carvalho FE, Margis-Pinheiro M,等。过氧化物酶在水稻非生物胁迫下对胞质抗坏血酸过氧化物酶敲除的补偿作用。植物细胞环境学报2011;34:1705-22。
- 31.
杨学勇,王锐,胡清良,李少林,毛晓东,景浩辉,等。DlICE1这是一种应激反应基因花芽龙眼,增强转基因的耐寒性拟南芥.植物生理与生物学报2019;142:490-9。
- 32.
木质素生物合成的遗传学:连接基因型与表型。Annu Rev Genet. 2010; 44:37 - 63。
- 33.
Vanholme R, Cesarino I, Rataj K, Xiao Y, Sundin L, Goeminne G,等。咖啡酰莽草酸酯酶(CSE)是木质素生物合成途径中的一种酶拟南芥.科学。2013;341:1103-6。
- 34.
范holme R, Storme V, Vanholme B, Sundin L, Christensen JH, Goeminne G,等。木质素生物合成扰动反应的系统生物学观点拟南芥.植物细胞。2012;24:3506-29。
- 35.
Sharma A, Shahzad B, Rehman A, Bhardwaj R, Landi M,郑BS。非生物胁迫下植物苯丙素通路的响应及多酚的作用。分子。2019;24:1-22。
- 36.
周鹏,李强,刘刚,徐楠,杨勇,曾伟,等。转录组和代谢组数据的综合分析揭示了多酚生物合成的关键代谢途径烟草下的压力。功能性植物生物学,2018;46:30-43。
- 37.
高红,张铮,吕旭,程宁,彭斌,曹伟。24-表油菜素内酯对桃果实冷害的影响与酚和脯氨酸代谢的关系。采后生物技术2016;111:390-7。
- 38.
格里菲斯M,雅什MW。越冬植物中的防冻蛋白:两个活动的故事。植物科学进展2004;9:39 - 405。
- 39.
Naikoo MI, Dar MI, Raghib F, Jaleel H, Ahmad B, Raina A,等。植物酚类物质在抗非生物胁迫中的作用及调控研究综述。在植物信号分子中。阿姆斯特丹:爱思唯尔;2019.p . 157 - 68。
- 40.
杨志强,陈建平。硫代葡萄糖苷的生物学和生物化学。植物学报2006;57:33 - 33。
- 41.
黄晓燕,张晓燕,张晓燕,等。葡萄糖苷在不同器官和发育阶段积累的变化拟南芥.植物化学,2003;62:471 - 81。
- 42.
张海明,吕格·莫,查普尔拟南芥ref2该突变体在编码CYP83A1的基因中存在缺陷,同时显示苯丙酸和硫代葡萄糖苷的表型。植物细胞。2003;15:179 - 94。
- 43.
Kim JI, Dolan WL, Anderson NA, Chapple C.吲哚硫代葡萄糖苷生物合成限制苯丙类化合物的积累拟南芥.植物细胞。2015;27:1529-46。
- 44.
Shekhar S, Mishra D, Gayali S, Buragohain AK, Chakraborty S, Chakraborty N.两种不同生态型甘薯蛋白质组学和代谢组学特征的比较(选用l .)。J蛋白质组。2016;143:306-17。
- 45.
Couée I,张文华,张文华。可溶性糖在植物活性氧平衡中的作用及其对氧化胁迫的响应。实验机器人2006;57:449-59。
- 46.
王晓燕,王晓燕,王晓燕。植物细胞中糖信号通路与抗氧化网络的关系。2月j . 2010; 277:2022-37。
- 47.
下调a-半乳糖苷酶对转基因植物抗冻性的影响佩妮.植物杂志。2003;133:901-9。
- 48.
蒋玉杰,Stushnoff C, McSay AE。过表达甘露醇-1-磷酸脱氢酶可增加甘露醇的积累,增强抗寒性佩妮.中国社会科学杂志2005;30(5):371 - 371。
- 49.
Parvanova D, Popova A, Zaharieva I, Lambrev P, Konstantinova T, Taneva S,等。转化为积累脯氨酸、果聚糖或甘氨酸甜菜碱的烟草植株的耐低温性。叶绿素荧光变化的证据。Photosynthetica。2004;42:179 - 85。
- 50.
李海军,杨爱芳,张晓春,高峰,张建军。转基因蔗糖烟草抗冻性的研究:蔗糖1-fructosyltransferase基因Lactucasativa.植物细胞组织器官,2007;89:37-48。
- 51.
川上一,佐藤一,吉田一。合成果聚糖和增强耐冷性水稻的基因工程。J Exp Bot 2008; 59:793-802。
- 52.
植物光合驯化过程中脯氨酸、糖和花青素的相互作用拟南芥干旱胁迫。植物生理学报,2012;169:577-85。
- 53.
糖在植物中的抗氧化剂作用。在:不利条件下作物改良。柏林:斯普林格出版社;2013.p . 285 - 308。
- 54.
Keunen E, Peshev D, Vangronsveld J, Ende WVD, Cuypers A.植物糖在非生物胁迫下的氧化挑战中是至关重要的角色:扩展传统概念。植物细胞环境学报,2013;36:1242-55。
- 55.
胁迫环境中的植物果实:新概念与未来展望。J Exp Bot 2008; 59:2905-16。
- 56.
巴士DH。低温贮藏下红薯的冷害、呼吸和糖的变化。中国科学(d辑:自然科学版)1987;
- 57.
曹文华,刘杰,何新军,穆瑞林,周海林,陈思思,等。乙烯反应的调节影响植物的盐胁迫反应。植物杂志。2007;143:707-19。
- 58.
胡廷祥,王永强,王qq,党宁宁,王磊,刘成昌,等。番茄2-氧戊二酸依赖的双加氧酶基因SlF3HL对低温胁迫的耐受性至关重要。Hortic杂志2019;6点45。
- 59.
崔勇,王强。玉米对单质硫和镉胁迫的生理响应。植物土壤环境,2006;52:523-9。
- 60.
脱落酸对玉米幼苗叶片活性氧、抗氧化防御系统及氧化损伤的影响。植物细胞物理学报2001;42:1265-73。
- 61.
两种藓类植物的耐旱性:与抗脂质过氧化酶防御相关。J Exp Bot 1981; 32:79-91。
- 62.
Aebi H.过氧化氢酶体外研究。方法Enzymol。1984;105:121-6。
- 63.
菠菜叶绿体中过氧化氢被抗坏血酸特异性过氧化物酶清除。植物细胞物理。1981;22:867-80。
- 64.
贝兹,华德仁,蒂雷。水胁迫下游离脯氨酸的快速测定。土壤植物。1973;39:205-7。
- 65.
张磊,王林林,梁永春,余建峰。FgPEX4参与了致病性和细胞壁的完整镰刀菌素graminearum.咕咕叫麝猫。2019;65:747-58。
- 66.
吕鑫,栾松,戴鹏,熊晓红,曹柏祥,罗凯。基于itraq的太平洋白虾急性氨毒性防御分子机制比较蛋白质组分析方面对虾.鱼类贝类Immun. 2018; 74:52-61。
- 67.
闫楠,杜艳梅,刘晓明,褚美梅,石俊,张海波,等。基于uhplc - qqq - ms的中国和北美野生水稻代谢组学比较研究。食品化学。2019;275:618-27。
确认
感谢吴烈红教授为我们提供了甘薯新品种“新乡”作为实验材料。
资金
基金资助:国家自然科学基金项目(31871857,杨海平);浙江省自然科学基金项目(LY19C200015,杨海平);国家特种(根茎作物)产业技术体系项目(car -10- b19,陆国强);浙江农林大学科研基金项目(2017FR026,崔鹏)。资助方在设计研究、分析、解释数据和撰写手稿方面没有发挥任何作用。
作者信息
从属关系
贡献
PC和HY构思了研究计划,分析了数据并撰写了手稿。CC和YH做了糖含量分析。YL和GL进行抗氧化酶测定。所有作者都阅读并认可了这个最终版本的手稿。
相应的作者
道德声明
额外的信息
出版商的注意
施普林格自然对出版的地图和机构附属的管辖权要求保持中立。
补充信息
额外的文件1。
蛋白质的多肽信息我.山芋与13°C (CK)下储存的块茎相比,储存在4°C下的根被置于NSI源中,然后在与UPLC在线耦合的Q ExactiveTM Plus (Thermo)中进行串联质谱(MS/MS)分析。
额外的文件2。
蛋白质描述的DEPs我.山芋根比>长1.5倍。
额外的文件3。
基因本体的功能分类(GO)注释我.山芋蛋白质。将蛋白质分为三大类:生物过程、细胞成分和分子功能。
额外的文件4。
差异表达蛋白(DEPs)的亚细胞定位由> 1.5倍于我.山芋根系在冷胁迫(4°C)下较CK有显著差异。
额外的文件5。
DEPs的KEGG注释我.山芋根系在冷胁迫(4°C)下较CK有显著差异。
额外的文件6。
差异表达代谢物(dem)信息我.山芋根系在冷胁迫(4°C)下较CK有显著差异。
附加文件7:表S1。
甘薯材料信息。表S2。差异表达蛋白的信息。表S3。差异表达的代谢数。图S1。块茎总蛋白的SDS-PAGE分析番薯甘薯l(每道30 μg蛋白质)。图S2。蛋白质按分子量的分布。
权利和权限
开放获取本文遵循创作共用署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),该协议允许在任何媒体或格式中使用、分享、改编、分发和复制,只要您给予原作者和来源适当的署名,提供创作共用许可协议的链接,并说明是否有更改。本文中的图片或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果材料不包含在文章的创作共用许可中,并且您的预期用途不被法律法规允许或超出了允许的用途,您将需要直接从版权所有者那里获得许可。欲查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献放弃书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文提供的数据,除非在数据的信用额度中另有说明。
关于这篇文章
引用这篇文章
崔鹏飞,李玉飞,崔丙飞。et al。低温贮藏反应的蛋白质组学和代谢谱分析选用林。块茎状的根。BMC植物杂志20.435(2020)。https://doi.org/10.1186/s12870-020-02642-7
收到了:
接受:
发表:
关键字
- 地瓜
- 低温存储
- Proteometabolomic
- 淀粉代谢
- 令人心寒的宽容