摘要
背景
丝裂原活化蛋白激酶(MAPK)级联反应是在真核细胞中发现的一种古老的信号转导机制。在植物中,MAPK级联反应与植物对各种非生物和生物胁迫(如植物病原体)的响应有关。MAPK通过顺序磷酸化实现级联功能:MAPK激酶激酶(MAPKKKs)磷酸化MAPK激酶(MAPKKs),磷酸化MAPKKs磷酸化MAPKs。在这三种激酶中,MAPKKKs在植物基因组中表现出最大的差异。尽管MAPKKs和MAPKs的数量相对有限,但它们的多样性使得MAPKKKs能够调控植物中许多特定的信号通路。虽然有些植物的MAPKKKs,包括MAPKKKα烟草benthamiana(NbMAPKKKα)在植物防御反应中起关键作用,但MAPKKK基因之间的功能关系尚不清楚。在这里,我们对MAPKKKs的功能进行了比较分析,以研究导致防御反应的信号通路。
结果
我们克隆了3个新的MAPKKK基因N. Benthamiana.:NbMAPKKKβ,NbMAPKKKγ,nbmapkkkkkkε2..瞬时过表达全长NbMAPKKKβ或NbMAPKKKγ或其激酶结构域N. Benthamiana.叶片诱导与过氧化氢产生相关的超敏反应(HR)样细胞死亡。这种活性依赖于过表达MAPKKK的激酶活性。此外,病毒诱导的沉默NbMAPKKKβ要么NbMAPKKKγ表达显著抑制病毒感染诱导的程序性细胞死亡(PCD)。此外,在NbMAPKKKβ、NbMAPKKKγ和nbmapkk α(先前被证明参与植物防御反应)之间的功能关系的上位性分析中,通过结合瞬时过表达分析和病毒诱导的基因沉默来进行NbMAPKKKα抑制了由NBMAPKKKβ激酶结构域或NBMAPKKγ的过表达诱导的细胞死亡,但沉默NbMAPKKKβ不能抑制NbMAPKKKα或NbMAPKKKγ过表达引起的细胞死亡。沉默的NbMAPKKKγ抑制NbMAPKKKβ激酶结构域诱导的细胞死亡,而不抑制NbMAPKKKα诱导的细胞死亡。
结论
这些结果表明,除了NbMAPKKKα外,NbMAPKKKβ和nbmapkk γ也具有PCD的正调节作用。此外,这三个MAPKKKs形成了导致PCD的线性信号通路;该通路从NbMAPKKKβ到NbMAPKKKγ再到nbmapkk α。
背景
由于植物缺乏适应性免疫系统,个体细胞对各种环境刺激(如由植物病原微生物引起的生物胁迫)的适当感知和反应是至关重要的。植物对生物胁迫的防御反应是由识别保守的病原体相关分子模式(PAMPs)或被称为诱导子或效应子的病原体菌株特异性因子触发的[1].由PAMP触发的响应被称为基础防御响应,而由特定elicitors触发的响应被称为过敏反应(HR)。在后者中,效应器被相应的植物抗性(R)蛋白质识别。人力资源经常伴随着编程的细胞死亡(PCD),其在防御生物营养病原体中起着特别重要的作用,但也是正常植物开发和分化中的基本功能[2].虽然已经鉴定出PCD相关HR所需的许多植物成分,但导致PCD的整个信号通路尚未阐明。
丝裂原活化蛋白激酶(MAPK)级联反应是真核细胞中高度保守的信号转导机制。在各种细胞外刺激的级联激活之后,信号通过顺序磷酸化传导到细胞内。在植物中,MAPK级联反应与发育和激素反应以及对非生物和生物因素的胁迫反应有关[3.].MAPK级联由三种功能连接的蛋白激酶组成:MAPK被MAPK激酶(MAPKK)磷酸化并激活,MAPK激酶又被上游MAPK激酶激酶(MAPKKK)激活。典型的MAPK底物是细胞质或核蛋白,如转录因子[3.].MAPKKKS是植物中这三种激酶最分歧的植物;这拟南芥基因组包含约60个MAPKKs、10个MAPKKs和20个MAPKs [4].
基于其催化激酶结构域的氨基酸序列的系统发育分析,植物MAPKKKS已被分为三组:A,B和C [4].A组包含许多参与PCD和压力和防御响应的MAPKKKS;例如。,A. Thaliana.AtMEKK1参与PAMPs诱导的基础防御信号通路[5], 和Medicago Sativa.MsOMTK1 [6[参与氧化应激诱导的细胞死亡。A组还包括HR Incuction中具有重要功能的MAPKKS。沉默编码的基因尼科尼亚塔哈瓦姆NPK1(NTNPK1)和烟草benthamianamapkkkα(nbmapkkkkα)抑制了N由烟草叶片病毒(TMV)复制酶的螺旋酶结构域诱导的基因介导的HR和PTO.-介导的HR两pv。番茄(PST)效应器AVRPTO分别[7,8].最近,N. Benthamiana.nbmapkkkkε及其番茄(茄属植物lycopersicum)同源基因SlMAPKKKε在抗革兰氏阴性细菌病原体HR的PCD诱导中有牵连[9].此外,沉默编码MAPKK MEK2和MAPK SIPK的基因,两者在NBMAPKKKα下游的行为,也衰减了N基因介导的HR对抗TMV [10.].相反,番茄MAPKK MEK1和MAPK NTF6同源基因的沉默导致烟草中ntnpk1下游的MAPKK MEK1和MAPK NTF6同源基因的缺失PTO.-介导的番茄HR [11.].因此,NTNPK1和NBMAPKKKα-发起的MAPK级联对于两者都是必不可少的N基因介导和PTO.-介导的HR,提示至少有两个不同的MAPK级联参与单个HR事件的调控[8].此外,现在越来越明显的是,两个不同的MAPK级联参与了非hr环境响应[12.].
植物通常似乎在不同的响应中使用相同的MAPKK / MAPK集合环境刺激。这A. Thaliana.MAPKKS ATMKK4和ATMKK5和/或其下游组件MPK6不仅涉及到ATMEKK1下游的基底防御,还涉及乙烯生产和气孔形成[5,13.,14.].鉴于植物中MAPKKs和MAPKs的数量相对有限,这些响应(功能)的多样性可能是由于MAPKKKs的巨大多样性[15.,16.].因此,需要MapKkks之间的比较功能分析,以揭示对环境压力各种反应的分子机制。
我们以前表明,全身性坏死,由Plantago Asiatica Mosaic病毒Li1(Plamv-Li1)引起的疾病症状伴随着类似于HR的抗性性状。使用烟草拨浪鼓病毒(TRV)的病毒诱导的基因沉默(Vigs)[17.,我们发现在HR中重要的NbSGT1和NbRAR1,以及包括nbapkkk α/NbMEK2在内的MAPK级联,对于PlAMV-Li1诱导的pcd相关系统性坏死是必不可少的[18.,19.].该结果和上述那些引导我们假设除Nbmapkkkα之外的其他Mapkkk基因也参与Plamv-Li1诱导的全身性坏死。
在本研究中,我们分离了3个新的A组MAPKKK基因N. Benthamiana.利用表达序列标签(EST)数据库对茄科模式植物进行了分析。这三个克隆基因已被指定NbMAPKKKβ,NbMAPKKKγ,nbmapkkkkkkε2..进一步的研究表明,NBMAPKKβ和NBMAPKKγ是PCD的正调节剂。此外,使用Vigs和Agroinfiltration进行的超越分析的结果表明,这些MapKkks(Nbmapkkkkβ和Nbmapkkγ)中的两个与Nbmapkkkα一起包括在PCD诱导中的线性信号通路。
结果
3个新的A群MAPKKK基因的克隆烟草benthamiana
为了对MAPKKK基因在防御反应中的作用进行比较分析,我们首先尝试克隆N. Benthamiana.MAPKKK基因属于A组。A组包括A1-A4四个亚组,其中包含许多参与植物防御反应的基因。获得一个N. Benthamiana.MAPKKK基因同源物从每一组A亚组中,我们选择如下拟南芥MAPKKK基因AtMEKK1[20.],AtMAPKKKγ,AtMAPKKKε1[21,22]作为A1,A2和A4子组的代表分别。对于A3子组,其中包括NTNPK1 [23]和Atanp1,我们能够放大N. Benthamiana.互补脱氧核糖核酸片段使用NTNPK1.特殊引物;扩增基因的核苷酸序列与编码NtNPK1激酶结构域的核苷酸序列一致98.0%,该基因在防御反应中的作用已被很好地描述[7].因此,A3亚组被排除在进一步研究之外。
利用编码AtMEKK1高度保守激酶结构域的核苷酸序列[19.[atmapkkkγ,和atmapkkkkε1作为爆炸搜查的疑问N. Benthamiana.,n .烟草,茄属植物lycopersicumEST数据库中,我们获得了三个EST序列:N. Benthamiana.TC15397,n .烟草BP133312,美国lycopersicum分别BI931567。基于这些序列,我们设计了特异性引物进行全长分离N. Benthamiana.MAPKKK cDNA克隆,如材料和方法所述。克隆的N. Benthamiana.预计MAPKKK基因预计将编码具有高度保守的激酶结构域的蛋白质和其他地区的差异,植物MAPKKK基因的一般特征[4].
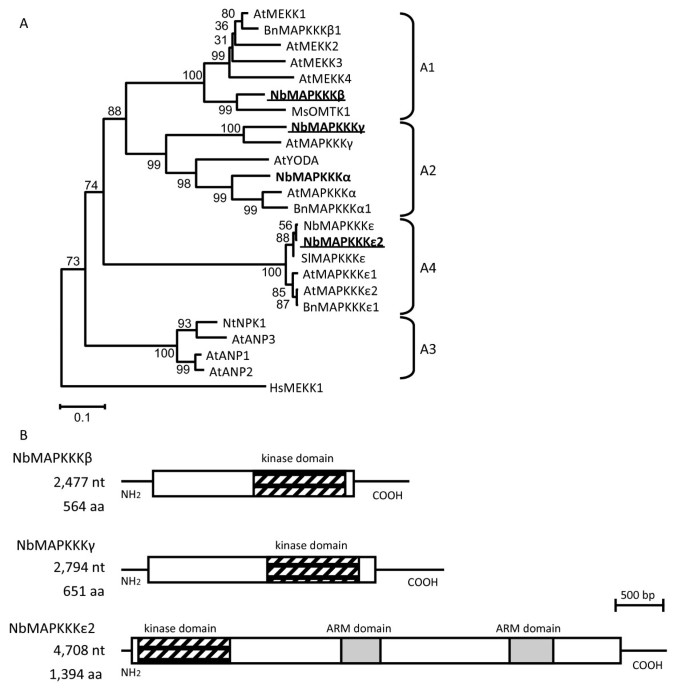
接下来,我们使用我们新克隆的MAPKKKS的激酶结构域的氨基酸序列和其他以前鉴定的MAPKKKS构建系统发育树(图1A).我们新克隆的MAPKKK基因以系统发育树中最接近的基因命名。因此,我们A2MAPKKK同族体被指定为NbMAPKKKγ后A. ThalianaAtmapkkkγ..在本研究的后期阶段,A4MAPKKK同族体,n benthamiana NbMAPKKKε, 已经报道 [9].虽然我们的A4同源物股票与之高序列相似之处NbMAPKKKε,该基因在核苷酸或氨基酸水平分别在核苷酸或氨基酸水平的96.6%或95.0%的同一性,并且长度不同。因为这些结果表明A4MAPKKK同源染色体在N. Benthamiana.由至少两个基因组成,我们的A4同源物被指定nbmapkkkkkkε2.后NbMAPKKKε.事实上,从最近发布的N. Benthamiana.基因组序列草图(http://solgenomics.net/),只有两个contigs具有高序列同源性(约90%)nbmapkkkkkkε2.每个序列对应的是nbmapkkkkkkε2.和NbMAPKKKε,分别。虽然我们的A1MAPKKK同源物最密切相关MSOMTK1,其在其基因产品的功能特征后指定,指定该基因“NbOMTK1,因为我们不知道我们的A1同源基因产品和MsOMTK1是否有类似的功能。紧随其后的是AtMEKK1和Brassica Napusbnmapkkkkβ1.因此,我们的A1同源物被指定NbMAPKKKβ后bnmapkkkkβ1,属于A1亚群的基因,与其他新克隆的基因一致NbMAPKKKγ和nbmapkkkkkkε2..这NbMAPKKKβ,NbMAPKKKγ,nbmapkkkkkkε2.本研究确定的cDNA序列保存在日本DNA数据库(DDBJ)中,登录号分别为AB649283、AB649284和AB649285。
三个新的MAPKKK基因的结构域如图所示1b .的NbMAPKKKβ,NbMAPKKKγ,nbmapkkkkkkε2.cDNA长度分别为2477、2794和4708 bp,分别编码564、651和1395个氨基酸。NbMAPKKKβ和NbMAPKKKγ的c端区域和NbMAPKKKε2的n端区域存在激酶结构域。NbMAPKKKε2的c端含有两个ARM(犰狳/β-catenin-like重复)结构域。这些蛋白质的结构域与它们各自的结构域相似A. Thaliana.同源染色体。
过表达NbMAPKKKβ和NbMAPKKKγ激酶结构域而不是NbMAPKKKε2激酶结构域会导致细胞死亡
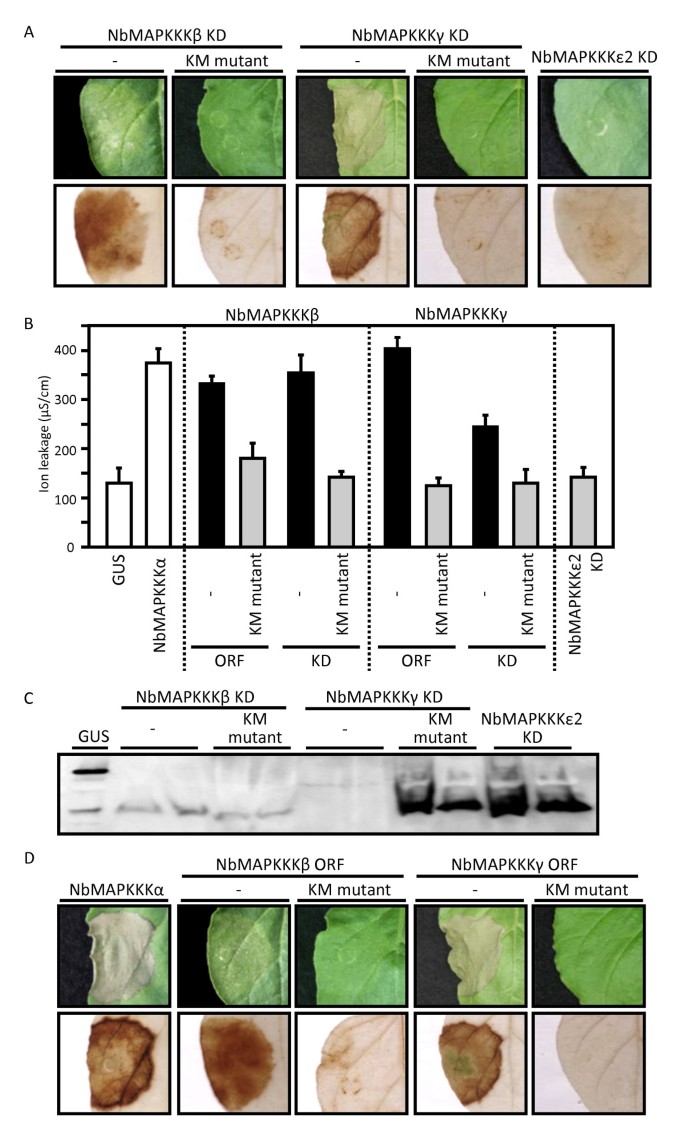
NBMAPKKKα,SLMAPKKKα的番茄同源物的激酶结构域的过度表达N. Benthamiana.据报道,通过农业渗透叶片可诱导非病原体细胞死亡[8].为了研究我们新鉴定的三个MAPKKKs是否也具有细胞死亡诱导活性,我们利用农业渗透对每个激酶域进行了瞬时过表达分析。NbMAPKKKβ和nbmapkk γ激酶域的瞬时过表达在浸润区诱导了非病原体细胞死亡(图)2A).在浸润区,细胞死亡与显著的过氧化氢产生相关,通过3,3'-二氨基联苯胺(DAB)染色后的特有棕色检测到这一点。这些结果通过使用离子泄漏法测定细胞死亡程度得到证实(图)2B),显示NbMAPKKKβ-和nbmapkkk γ过表达区离子泄漏显著增加。NbMAPKKKβ与NbMAPKKKγ的离子泄漏水平没有显著差异。相反,NbMAPKKKε2激酶结构域的过表达不能诱导细胞死亡或产生过氧化氢,也不能增加离子泄漏水平。使用抗myc单克隆抗体(Millipore, Billerica, MA, USA)进行Western blot分析,以评估这些激酶结构域的表达水平(图)2C).检测到NbMAPKKKβ和nbmapkk ε2激酶结构域的特异性信号,但没有NbMAPKKK的积累γ.发现了激酶结构域。然而,我们假设NbMAPKKKγ.即使在非常低的水平下,均匀表达激酶结构域,因为其过度表达迅速诱导细胞死亡。Western印迹分析还表明,NBMAPKKKKε2激酶结构域的累积表达水平,其过表达没有诱导细胞死亡,远大于NBMAPKKKβ和NBMAPKKγ激酶结构域的表达水平。因为这些结果表明NBMAPKKKE2不涉及病原体无关的细胞死亡的诱导,我们从进一步分析中排除了NBMAPKKKE2。
NBMAPKKKβ和NBMAPKKγ的过度表达诱导病原体无关的细胞死亡N. Benthamiana.叶子。N. Benthamiana.叶子被渗透过农杆菌属携带PearleyGate203的菌株[32含有突变或全长MAPKKKs编码序列的衍生物。所有实验,除图中所示4,至少重复了三次,得到了相似的结果。一个)渗透的症状N. Benthamiana.叶片区域过表达MAPKKK激酶结构域(KDs)或atp结合位点缺失(K→M) KD突变体。下图为DAB染色后同一片叶子的图像。DAB染色检测过氧化氢的产生,如前所述[18.].浸润后5天拍照。每个蛋白瞬时与沉默抑制因子p19共同表达。农杆菌属培养物生长到浊度(OD)600)为0.5,用于农业渗透。B过表达野生型或K→M突变体NbMAPKKKβ或NbMAPKKKγ或其野生型或K→M突变体KDs或NbMAPKKKε2 KD的叶区离子泄漏。GUS和nbapkkk α作为内对照。离子泄漏试验如前所述进行[18.].所示数据代表了至少三个独立工厂的平均值±标准偏差。C)对Myc标记的NBMAPKKKβ或NBMAPKKKγKD或其K→M突变体或NBMAPKKKKKKKKKD的Western印迹分析。MyC标记的GUS被用作内部控制。在5 dpi下从每个基因渗透区域中提取总蛋白质。为每个Myc标记的构造显示了两个复制。D)渗透叶区过表达全长野生型或K→M突变体NbMAPKKKβ或NbMAPKKKγ的症状。下图为DAB染色后同一片叶子的图像。
全长,催化活性Nbmapkkβ或Nbmapkkγ的过表达导致细胞死亡
为了进一步研究Nbmapkkkβ和Nbmapkkkγ在病原体无关的细胞死亡中的参与,我们使用它们的全长开放阅读框(ORF)进行了瞬时过表达实验。如图所示2D,NBMAPKKKβ或NBMAPKK的过度表达γ.诱发细胞死亡。观察到的离子泄漏水平类似于NBMAPKKKβ,NBMAPKKγ和NBMAPKKα的过度表达,其用作阳性对照(图2B)。
先前的一些研究已经证明,激酶活性是通过MAPK级联反应的一个组分的瞬时过表达触发非病原体细胞死亡所必需的[8,24,25].为了研究NbMAPKKKβ-和nbmapkkk γ诱导的细胞死亡是否也需要激酶活性,我们构建了ATP结合缺陷的MAPKKK全长和激酶结构域突变体。在这些突变体中,激酶结构域atp结合位点必需的保守赖氨酸残基(K)被蛋氨酸(M)取代[8].如图所示2一个和2D,这些K→M突变体过表达时均未引起细胞死亡。DAB染色证实了此结果(图)2一个和2D)和离子泄漏测定(图2B)。此外,这些激酶结构域K→M突变体的表达通过抗myc单克隆抗体的western blot分析得到证实(图)2C).这些结果表明,细胞死亡是由瞬时过表达N. Benthamiana.NbMAPKKKβ或NbMAPKKKγ依赖于它们的激酶活性。
沉默的NbMAPKKKβ要么NbMAPKKKγ抑制PlAMV-Li1-induced纤毛运动
鉴于上述发现,过表达全长NbMAPKKKβ或NbMAPKKKγ或其激酶结构域可诱导细胞死亡,我们预计沉默编码这些mapkk的基因可抑制病毒诱导的PCD。因此,我们采用了基于trv的VIGS系统[17.]沉默NbMAPKKKβ和NbMAPKKKγ.通过分析表达来确认每个基因的成功沉默NbMAPKKKβ,NbMAPKKKγ,NbMAPKKKα(控制)使用实时逆转录(RT)-PCR分析(图3.此外,使用激酶结构域特异性探针对每个基因进行Southern blot分析显示NbMAPKKKβ和NbMAPKKKγ分别以单拷贝和多拷贝的形式存在N. Benthamiana.基因组(附加文件1:图S1)。在N. Benthamiana.草案基因组,两个contigs显示高序列同源性(约>90%)NbMAPKKKγ,表明至少有两份NbMAPKKKγ同源染色体。因此,我们假设一个单一的基因是专门针对NbMAPKKKβ但一种或多种高度相似的基因可能会被用于NbMAPKKKγ沉默的植物。此后,我们使用“NbMAPKKKγ“ 以表示NbMAPKKKγ和/或其同源基因除了瞬时过度表达实验。与非沉默(Vigs Vector)对照植物相比,基因沉默的植物没有显示任何明显的表型差异(图3.B),表明NbMAPKKKβ和NbMAPKKKγ都不参与植物的正常生长发育。相反,NtNPK1的沉默,这是一种MAPKKK,参与了植物胞质分裂和细胞内的细胞板形成N基因介导的HR细胞死亡,导致植物的严重衰退[7].
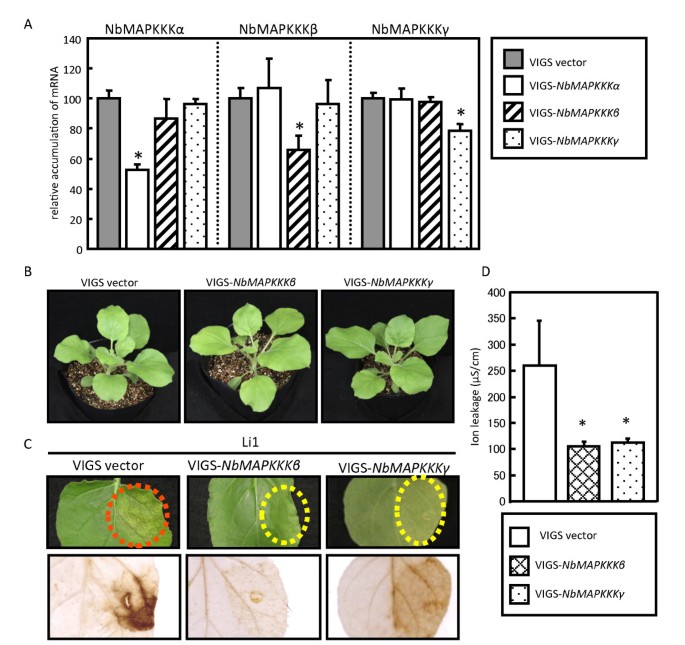
沉默的NbMAPKKKβ和NbMAPKKKγ抑制plamv-li1诱导的pcd。一个)在基因沉默的植物中确认特定MAPKKK基因沉默。相对批量NbMAPKKKα,NbMAPKKKβ,NbMAPKKKγmRNA在非沉默或NbMAPKKKα-,NbMAPKKKβ-,或NbMAPKKKγ-沉默的植物采用实时RT-PCR检测。将每个叶片组织样本的数据归一化到同一样本中Nb18S rRNA基因的表达水平。所示数据代表了至少三个独立工厂的平均值±标准偏差。星号表示与对照植物(P< 0.05)。B)在非沉默和典型中观察到的典型表型NbMAPKKKβ- 和NbMAPKKKγ沉默的植物。图片被拍了21 dpi。C) plamv - li1浸润区无症状和无症状NbMAPKKKβ- 要么NbMAPKKKγ- 相同叶子的植物(上面板)和DAB染色(下面板)。红色圆圈表示细胞死亡;黄色圆圈表明没有症状。叶子用plamv-li1表达渗透农杆菌属培养物生长到浊度(OD600)0.05。D)在Plamv-Li1渗透区域的离子泄漏,不沉默和NbMAPKKKβ- 要么NbMAPKKKγ——沉默植物。所示数据代表了至少三个独立工厂的平均值±标准偏差。星号表示与对照植物(P< 0.05)。
NbMAPKKKβ- 和NbMAPKKKγ-沉默植株和对照非沉默植株随后接种PlAMV-Li1,诱导pcd相关坏死N. Benthamiana..在非沉默植物plamv - li1浸润区,我们观察到特征性的坏死症状和棕色染色,表明过氧化氢的积累。然而,在李1的渗透NbMAPKKKβ-沉默的植物,细胞死亡和过氧化氢的产生完全受到影响。另外,在NbMAPKKKγ-沉默的植物,细胞死亡和过氧化氢的产生分别被完全和部分抑制,尽管只有大约20%的丰度下降NbMAPKKKγ转录物(图3.C).细胞死亡的抑制NbMAPKKKβ- 和NbMAPKKKγ-沉默植物被证实使用离子泄漏测定(图3.D).细胞死亡的抑制NbMAPKKKγ-沉默的植物尽管其mRNA水平略有下降,这可能是由于细胞死亡时严格要求高水平的NbMAPKKKγ蛋白所致。虽然有可能残留的NbMAPKKKγ蛋白有助于降低过氧化氢的产生水平,但其水平可能太低而不能诱导细胞死亡。这些结果表明,NbMAPKKKβ和NbMAPKKKγ参与了PlAMV-Li1诱导的过氧化氢生成和PCD。
NbMAPKKKα、NbMAPKKKβ和NbMAPKKKβ形成了诱导细胞死亡的线性信号通路
加上我们之前的研究发现,NbMAPKKKα参与plamv - li1诱导的PCD [19.[上述研究结果表明NbMAPKKKβ和NbMAPKKKγ对于这种病毒诱导的PCD也是必不可少的。为了确定这三个基因在PCD信号通路中的关系,我们设计了瞬时过表达和沉默这些基因组合的上位性实验。在这些实验中,带有特定的vigs沉默的MAPKKK基因的植物被农渗透农杆菌属表达不同MAPKKK基因的培养和离子泄漏水平。在简超实验之前,进行了初步实验以确定最小浊度农杆菌属每个基因接种量足以诱导细胞完全死亡。OD时,在以下细胞密度下观察到细胞完全死亡600:0.5,NBMAPKKKα;1.0,nbmapkkkβ;和0.05,nbmapkkkγ。虽然每个MAPKKK都以不同浓度过度表达农杆菌属接种时,不同浊度(0.05 ~ 1.0)的基底离子渗漏水平无显著差异农杆菌属在野生型植物中表达GUS基因的接种物(附加文件)2:图S2)。对于NBMAPKKKβ,全长ORF和激酶结构域诱导的细胞死亡缓慢且弱,但是由激酶结构域诱导的细胞死亡比通过全长ORF诱导的细胞死亡。在图中所示的离子泄漏测定中2B,虽然NbMAPKKKβ全长ORF和激酶结构域诱导的细胞死亡差异无统计学意义,但检测到这种趋势。以往的研究表明,MAPKKK的底物特异性不受瞬时激活激酶结构域的影响[5,8,26].因此,Nbmapkkkβ的激酶结构域用于进一步分析,而不是全长ORF。
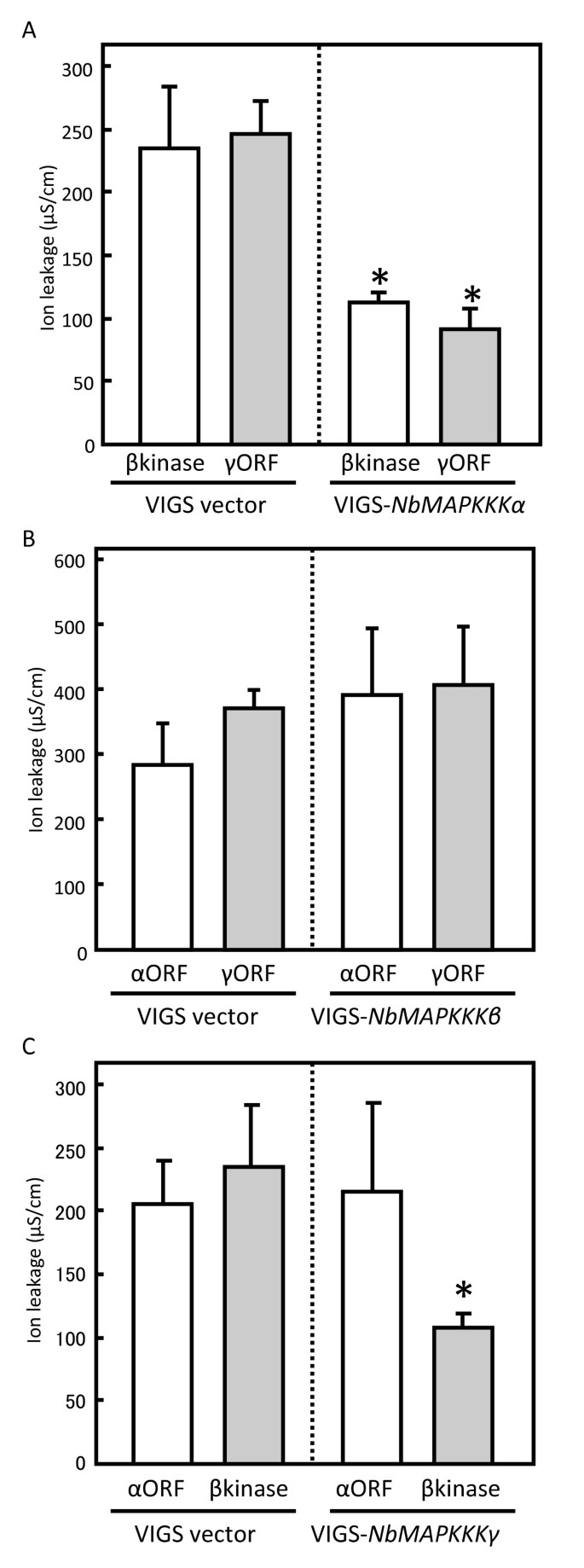
如图所示4A, NbMAPKKKβ激酶结构域或全长NbMAPKKKγ瞬时表达诱导的离子泄漏水平降低NbMAPKKKα- 比Vigs Vector-occ向量的控制植物,植物。NBMAPKKKβ和NBMAPKKγ诱导的细胞死亡始终抑制NbMAPKKKα-静音工厂与控制工厂比较(数据未显示)。这一结果表明,NbMAPKKKα要么在NbMAPKKKβ和NbMAPKKKγ诱导细胞死亡的过程中起下游作用,要么在NbMAPKKKβ和NbMAPKKKγ的相互依赖激活中起重要作用。而NbMAPKKKα和NbMAPKKKγ瞬时表达诱导的离子泄漏水平与NbMAPKKKα和NbMAPKKKγ瞬时表达诱导的离子泄漏水平相似NbMAPKKKβ- 植物和控制植物(图4B),提示NbMAPKKKα和NbMAPKKKβ的激活不是相互依赖的;相反,在细胞死亡信号通路中,NbMAPKKKβ在nbmapkk α的上游起作用。这一结果使我们假设NbMAPKKKβ在NbMAPKKKγ的上游起作用。正如所料,在NbMAPKKKγ与对照植物相比,NbMAPKKKβ激酶域瞬时过表达诱导的沉默植物、细胞死亡和离子泄漏水平显著降低(数据未显示和图中)4C,分别)。而NbMAPKKKα瞬时过表达诱导的细胞死亡和离子泄漏,则与NbMAPKKKα瞬时过表达诱导的细胞死亡和离子泄漏相似NbMAPKKKγ-silenced和控制植物(数据未显示和图形4C,分别),证实了NbMAPKKKβ在NbMAPKKKγ上游起作用,而NbMAPKKKγ在nbmapkk α上游起作用。在上位性分析中,离子泄漏水平与这些基因的所有组合的细胞死亡强度密切相关。因此,这三个MAPKKK基因形成了一个导致PCD的线性信号通路,其中NbMAPKKKβ和NbMAPKKKα分别作为三个mapkk组分的最远的上游和下游组分。
NBMAPKKKα,NBMAPKKKβ和NBMAPKKγ的功能关系的简化分析。通过分别通过瞬时过表达和VIGS激活和抑制特异性MAPKKKs组合进行上位性分析。浸润区细胞死亡采用4 dpi离子泄漏法进行量化。所显示的数据代表了至少五个工厂的平均值±标准偏差。星号表示与对照植物(P< 0.05)。图中所示的所有实验都重复了两次,结果相似。一个NbMAPKKKβ激酶域(β激酶)-或NbMAPKKKγ (γORF)-过表达区域的细胞死亡NbMAPKKKα沉默的植物。农杆菌属表达βkinase和γorf的培养物分别生长至1.0%和0.05的浊度,以渗透。BNbMAPKKKα (αORF)-或γ orf过表达区非沉默区细胞死亡NbMAPKKKβ沉默的植物。农杆菌属表达αORF和γORF的培养物分别培养至浊度为0.5或0.05时进行渗透。CαORF-或β激酶过表达区域的细胞死亡NbMAPKKKγ沉默的植物。农杆菌属表达αORF和β激酶的培养菌分别生长到浊度为0.5和1.0的培养基中进行渗透。
讨论
在我们之前的研究中[19.,我们发现包括nbapkkk α和NbMEK2在内的MAPK级联反应在PlAMV-Li1诱导的pcd相关系统性坏死中都是必需的处方- 对抗马铃薯病毒X的介导。几次研究表明,至少两个MAPK级联涉及各种环境刺激的植物反应[8,12.].植物MAPKKK基因的巨大多样性被认为是植物对各种环境刺激产生特定信号应答能力的基础[15.,16.].因此,为了更好地了解MAPKKKS在PCD的诱导中的功能,我们进行了对比较的功能分析N. Benthamiana.MAPKKK基因。在之前和现在的研究中,我们证明了其中三个基因,NbMAPKKKα[19.],NbMAPKKKβ,NbMAPKKKγ(和/或其同源物),作为plamv - li1诱导的PCD的正调节物,在细胞死亡信号通路中不具有功能冗余。在VIGS实验中,不仅如此NbMAPKKKγ但其同源基因也可能在TRV-中被敲除NbMAPKKKγ来华的植物。然而,在克隆实验中只获得了A2亚群中的一个基因,说明NbMAPKKKγ同源基因,其序列几乎与NbMAPKKKγ本身,必须有效地在TRV-NbMAPKKKγ来华的植物。此外,过度的表达NbMAPKKKγ全长ORF和激酶结构域可诱导细胞快速死亡。因此,NbMAPKKKγ本身可能在细胞死亡信号通路中发挥重要作用。
我们还通过基于所述超声测试基于所述三种MAPKKK基因的功能关系来探讨了这三种MAPKKK基因的功能关系,即如果信号蛋白B上游的功能,通过激活A的信号传导通过B表达沉默,而激活的B信号通过沉默表达式不会被抑制。我们的结果(图4)证明表示NBMAPKKKγ和/或其同源基因的NBMAPKKKα,NBMAPKKK和NBMAPKKγ形成导致细胞死亡诱导的线性信号传导途径,其中NBMAPKKβ作用于NBMAPKKKα上游的NBMAPKKγ和NBMAPKKγ的作用。类似的简超分析结果表明,在植物诱导PCD的MAPKKKKα/ MEK2 / SIPK MAPK级联下游的NPK1 / MEK1 / NTF6 MAPK级联功能[8].这些结果支持了NbMAPKKKα、NbMAPKKKβ、NbMAPKKKγ和NPK1启动四种不同的MAPK级联反应的可能性,它们共同参与了植物细胞的死亡。另外,不同的MAPK级联可能参与了不同植物-微生物相互作用诱导的细胞死亡信号通路。为了研究这个问题,需要进一步的研究来确定NbMAPKKKβ和nbmapkk γ是否参与了N基因介导的人力资源或抗TMV或PTO.-介导的HR对抗Pst。
在我们的实验中,AgroinFiltration的NBMAPKKKKE2激酶结构域的瞬时过度表达未诱导细胞死亡(图2然而,Melech-Bonfil和同事已经证明,番茄NbMAPKKKε2 (SlMAPKKKε)是在HR中诱导PCD对抗革兰氏阴性细菌病原体所必需的[9].此外,他们还发现番茄SlMAPKKKε激酶结构域瞬时过表达N. Benthamiana.诱导无关的细胞死亡。Nbmapkkkkkkkkkkkkkkkkkkkkkkkkkkkkkε的激酶结构域的氨基酸序列的比较仅表明了三个氨基酸差异。这三个残基并不高度保守,并且不预测对植物激酶催化活性至关重要,因此仅难以通过氨基酸序列水平来解释该功能差异。虽然乍一看,我们的结果似乎与他们相矛盾,结果不能直接比较,因为我们的瞬态过度表达实验中的三个因素不同于它们的:启动子,农杆菌属菌株、同源基因和物种起源。这三个因素可以影响过表达蛋白的表达水平,对于具有细胞死亡诱导活性的蛋白引起细胞死亡的执行是至关重要的[27,28].此外,我们实验中过表达的NBMAPKKKKKKKε2激酶结构域的量远远多于NBMAPKKKβ激酶结构域及其K→M突变体或NBMAPKKγ激酶结构域,其可以诱导细胞死亡,并且与NBMAPKKγ激酶结构域K→相当 M mutant. Therefore, NbMAPKKKε2 might be a less potent inducer of cell death than other MAPKKKs.
我们认为,在诱导细胞死亡的线性信号通路中,有几个MAPK级联反应引起了人们对它们在植物防御反应中的作用的关注。为了防止病原体入侵,植物通常采用两种类型的受体[NBS-LRR(核苷酸结合位点和富亮氨酸重复)受体和RLK(受体样激酶)型受体][1]来感知来自生物营养和坏死营养病原体的多种PAMPs或效应物。当植物感知到病原体时,一组共同的基因转录就会被激活,这些基因可以对抗各种类型的病原体[29,30.],随后产生许多防御反应,包括细胞死亡和低分子量信号化合物的产生,如乙烯和活性氧(ROS)。MAPKKKα/MEK2/SIPK级联活化可诱导乙烯和ROS的生成[31,32].NPK1启动另一个MAPK级联,由MAPKKKα启动的MAPK级联产生的ROS激活[26].类似地,紫花苜蓿MAPKKK MsOMTK1被过氧化氢激活[6].这些结果表明,由上游作用的MAPK级联诱导的化合物用作激活下游作用MAPK级联的信号分子。此外,他们表明,几个MAPK级联在防御反应中的参与使植物能够同时激活各种响应或协调来打击各种病原体。
结论
在这项研究中,我们展示了三个MapkkksN. Benthamiana.形成PCD的线性信号通路,提示植物防御反应中多个MAPK级联反应的参与使得植物同时表现出多种反应。通过进一步的分析鉴定直接被NbMAPKKKβ和NbMAPKKKγ磷酸化的下游MAPKK和MAPK基因,有助于阐明这些MAPKK基因参与细胞死亡的调控机制。此外,为了阐明植物防御反应中各个MAPK级联反应的顺序激活机制,必须确定直接激活这些MAPKKKs的上游成分或化合物。
方法
植物材料和病毒分离物
N. Benthamiana.植物在25°C的生长室中生长。利用含有花椰菜花叶病毒35 S启动子下游的车前草花叶病毒Li1分离物的全长cDNA的二元载体pLi1接种植物以病毒诱导PCD [33].
MAPKKK基因的克隆N. Benthamiana.
为了检索部分MAPKKK cDNA序列,使用激酶结构域的氨基酸序列来进行BLAST搜索拟南芥MAPKKK基因AtMEKK1,AtMAPKKKγ,AtMAPKKKε1作为对策的疑问N. Benthamiana.,n .烟草,美国lycopersicum基因指数项目的数据库在计算生物学和功能基因组学实验室网站(http://compbio.dfci.harvard.edu/tgi/cgi-bin/tgi/Blast/index.cgi)和理研生物资源中心的烟草BY-2 EST克隆数据库(http://www.brc.riken.go.jp/lab/epd/blast/index.shtml).利用检索到的部分cDNA序列和查询序列的一致核苷酸序列,分别为三个MAPKKK基因设计一对特异性引物。每对特异性引物对提取的总RNA进行RT-PCR扩增cDNA片段N. Benthamiana.叶子。RT-PCR产物经凝胶纯化,克隆到pGEM-T easy载体(Promega, Madison, WI, USA)中进行测序。然后根据获得的cDNA序列与查询序列的非同源区域设计新的引物(以防止非特异性扩增),并使用GeneRacer Kit (Invitrogen, Carlsbad, CA, CA)用于cDNA末端的5 ' -和3 ' -特异性快速扩增(RACE)。(美国)根据制造商提供的标准协议。本研究引物序列如表所示1.从至少3个独立的克隆中确定了MAPKKK基因的cDNA序列。
使用ORF Finder进行ORF和motif分析(http://www.ncbi.nlm.nih.gov/gorf/gorf.html.)和CD搜索(http://www.ncbi.nlm.nih.gov/structure/cdd/wpsb.cgi.)程序,分别。系统发育分析采用MEGA3.1,基于ClustalW创建的多个比对。用于系统发育分析的MAPKKK基因序列在GenBank数据库中列出,登录号如下:AtMEKK1(nm_116919),AtMEKK2(NM_116917),AtMEKK3(NM_116916),AtMEKK4(nm_117272),bnmapkkkkβ1(AJ010093),AtANP1(NM_100771),AtANP2(NM_104370),AtANP3(NM_111477),NTNPK1.(D26601),AtMAPKKKγ(NM_126084),AtYODA(AY357949),NbMAPKKKα(AY500155),AtMAPKKKα(NM_179472),AtMAPKKKε1(NM_112199),AtMAPKKKε2(NM_111677),MSOMTK1(AJ575100),BnMAPKKKα1(AJ010091),BnMAPKKKε1(AJ238845),SlMAPKKKε(GU192457),NbMAPKKKε(GU205153)。智人HsMEKK1(AF042838)作为外组。
瞬时表达野生型和突变型MAPKKKs和MAPKKK激酶结构域的质粒的构建和农业渗透
的编码区域NbMAPKKKα,NbMAPKKKβ,NbMAPKKKγ通过RT-PCR通过引物对Kp-Nbmapkkkka-1f / xH-Nbmapkkkka-1836r,Kp-Nbmapkkkb-1f / Ecv-nbmapkkkb-1695r和Kp-nbmapkkkg-1f / xh-nbmapkkkkg-1956r分别扩增。激酶域NbMAPKKKβ,NbMAPKKKγ,和nbmapkkk.ε2分别使用引物对kp - nbmapkkkkkinase - f / ecv - nbmapkkkkinase - r、Kp-NbMAPKKKgkinase-F/ xh - nbmapkkkkkkinase - r和kp - nbmapkkkkkinase - f / xh - nbmapkkkkinase - r进行扩增。
通过在激酶结构域中的ATP结合位点中取代甲硫氨酸来获得NBMAPKKKβ和NBMAPKKγ的函数突变体。这些突变体通过使用位点诱变使用引物NBMAPKKKB-K381M-F和NBMAPKKKB-K381M-R用于NBMAPKKKβ和NBMAPKKKG-K374M-F和NBMAPKKKG-K374M-R的NBMAPKKγ。将每个PCR扩增的MAPKKK基因片段亚克隆到35秒启动子下的PELLEYGATE 203载体中[34]通过Penta条目矢量[35克隆酶II混合酶(Invitrogen)。GUS基因在35 S启动子下亚克隆到pEarleyGate 203载体中。这些质粒载体被转化成农杆菌肿瘤术应变EHA105。如前所述进行农业渗透[27].
VIGS载体和VIGS的构建
如先前使用PTV:00衍生物和PBINTRA6 [17.].使用PTV诱导NBMAPKKα沉默:NbMAPKKKα[19.].对于NbMAPKKKβ和NbMAPKKKγ沉默,将pcr扩增的NbMAPKKKβ ORF全长5 '端390-bp的KpnI-PvuII片段和pcr扩增的NbMAPKKKγ全长ORF的576-bp的KpnI-EcoRV片段以反义方向导入pTV:00中生成pTV:NbMAPKKKβ和PTV:NbMAPKKKγ,分别。利用引物Kp-NbMAPKKKb-1 F和EcV-NbMAPKKKb-1695R扩增出NbMAPKKKβ ORF,利用引物Kp-NbMAPKKKg-1 F和Xh-NbMAPKKKg-1956R扩增出NbMAPKKKγ ORF。
实时rt - pcr
用于总RNA分离,cDNA合成和基因表达的定量分析的方法与先前描述的那些相同的方法18.].以18s rRNA的表达作为归一化标准。real-time RT-PCR的引物为nbapkkka - 255f、nbapkkka - 393r、nbapkkkb - 1179f、nbapkkkb - 1286r、nbapkkkg - 903f、nbapkkkg - 984r、Nb18S- 193f、Nb280R。
缩写
- 人力资源:
-
过敏反应
- 地图:
-
增殖蛋白激酶
- MAPKK:
-
MAPK激酶
- MAPKKK:
-
MAPKK激酶
- 纤毛运动:
-
程序性细胞死亡
- PlAMV:
-
Plantago Asiatica马赛克病毒
- 太平洋标准时间:
-
两pv。番茄
- 烟草花叶病毒:
-
烟草马赛克病毒。
参考
- 1。
Jones JD,Dangl JL:植物免疫系统。自然。2006,444(7117):323-329。10.1038 / Nature05286。
- 2.
罗杰斯HJ:植物中的细胞死亡和器官发展。Curr Top Dev Biol。2005,71:225-261。
- 3.
植物丝裂原活化蛋白激酶信号转导。植物生物学年鉴。61:621-649。
- 4.
植物丝裂原活化蛋白激酶级联:一个新的命名。植物科学进展,2002,7(7):301-308。10.1016 / s1360 - 1385(02) 02302 - 6。
- 5。
Asai T,Tena G,Plotnova J,Willmann Mr,Chiu Wl,Gomez-Gomez L,Boller T,Ausubel FM,Sheen J:在拟南芥中的映射激酶信号传导级联。自然。2002,415(6875):977-983。10.1038 / 415977A。
- 6。
Nakagami H,Kiegerl S,Hirt H:OMTK1,一种新颖的MAPKKK,通过直接MAPK交互通道氧化应力信号。J Biol Chem。2004,279(26):26959-26966。10.1074 / JBC.M312662200。
- 7。
Jin H, Axtell MJ, Dahlbeck D, Ekwenna O, Zhang S, Staskawicz, Baker B: NPK1, mekk1样丝裂原激活蛋白激酶激酶,调节植物的先天免疫和发育。系统工程理论与实践,2016,35(1):1- 5。10.1016 / s1534 - 5807(02) 00205 - 8。
- 8.
Del Pozo O,Pedley KF,Martin GB:Mapkkkα是与植物免疫和疾病相关的细胞死亡的正稳压因素。Embo J. 2004,23(15):3072-3082。10.1038 / sj.emboj.7600283。
- 9.
Melech-Bonfil S, Sessa G:番茄MAPKKKε是与植物免疫相关的细胞死亡信号网络的正调控因子。植物学报,2010,64(3):379-391。10.1111 / j.1365 - 313 x.2010.04333.x。
- 10。
金华,刘艳,杨启元,金春英,Baker B,张树文:N基因介导烟草抗性的丝裂原激活蛋白激酶途径的功能。植物学报,2003,33(4):719-731。10.1046 / j.1365 - 313 x.2003.01664.x。
- 11.
关键词:番茄抗病,MAPK, NPR1, TGA转录因子,pto植物学报,2003,36(6):905-917。10.1046 / j.1365 - 313 x.2003.01944.x。
- 12.
Yoo SD,Cho Yh,Tena G,Xiong Y,Sheen J:通过分叉MAPK级联C2H4信号传导的核EIN3双控制。自然。2008,451(7180):789-795。10.1038 / Nature06543。
- 13.
Zhang S:1-氨基环丙烷-1-羧酸合成酶MPK6的磷酸化,应力响应丝裂原蛋白激酶,诱导拟南芥乙烯生物合成。植物细胞。2004,16(12):3386-3399。10.1105 / TPC.104.026609。
- 14.
王H,Ngwenyama N,Liu Y,Walker JC,张S:气孔发育和图案化由拟南芥中环保偶极丝裂解的蛋白激酶进行调节。植物细胞。2007,19(1):63-73。10.1105 / TPC.106.048298。
- 15.
张绍峰,张志强,张志强。MAPK在植物防御信号中的级联作用。植物科学进展,2001,6(11):520-527。10.1016 / s1360 - 1385(01) 02103 - 3。
- 16。
Pedley Kf,Martin GB:丝裂剂活化蛋白激酶在植物免疫中的作用。CurrOp植物BIOL。2005,8(5):541-547。10.1016 / J.PBI.2005.07.006。
- 17。
Ratcliff F,Martin-Hernandez Am,Baulcombe DC:烟草拨浪鼓病毒作为沉默分析基因功能的载体。工厂J.2001,25(2):237-245。
- 18.
Komatsu K,Yamaji Y,Ozeki J,Hashimoto M,Kagiwada S,Takahashi S,Namba S:七种日本植物叶片叶片病毒病毒(Plamv)的核苷酸序列分析:一种独特的Potexvirus:物种内具有明显高的基因组和生物变异性的独特Potexvirus.拱病毒。2008,153(1):193-198。10.1007 / s00705-007-1078-y。
- 19.
Komatsu K,Hashimoto M,Ozeki J,Yamaji Y,Maejima K,Senshu H,Himeno M,Okano Y,Kagiwada S,Namba S:植物中的病毒诱导的全身性坏死涉及编程的细胞死亡和病毒繁殖的抑制作用由独立途径调节。Mol植物微生物相互作用。2010,23(3):283-293。10.1094 / mpmi-23-3-0283。
- 20.
mizoguchi t,irie k,hirayama t,hayashida n,yamaguchi-shinozaki k,matsumoto k,shinozaki k:编码丝裂原激活的蛋白激酶激酶激酶的基因与丝裂原激活的蛋白激酶和s6核糖体的基因同时诱导拟南芥中的触摸,冷和水胁迫蛋白激酶。美国国家科学院学报。1996,93(2):765-769。10.1073 / pnas.93.2.765。
- 21。
Jouannic S, Champion A, Segui-Simarro JM, Salimova E, Picaud A, Tregear J, testilano P, Risueno MC, Simanis V, Kreis M,等:蛋白激酶AtMAP3Kε1和BnMAP3Kε1是S. pombe cdc7p的功能同源物,可能参与细胞分裂。植物学报,2001,26(6):637-649。10.1046 / j.1365 - 313 x.2001.01065.x。
- 22。
Chaiwongsar S, Otegui MS, Jester PJ, Monson SS, Krysan PJ: MAP3Kε1和MAP3Kε2是拟南芥花粉活力所必需的蛋白激酶基因。植物学报,2006,48(2):193-205。10.1111 / j.1365 - 313 x.2006.02863.x。
- 23。
Banno H, Hirano K, Nakamura T, Irie K, Nomoto S, Matsumoto K, Machida Y: NPK1,烟草基因,编码与酵母BCK1, STE11和Byr2蛋白激酶同源的蛋白。中国生物医学工程学报。1998,13(8):445 - 452。
- 24。
任D,杨肯,李GJ,刘y,张S:NTF4,烟草丝裂剂激活蛋白激酶的激活,植物防御响应期间及其参与过敏反应的细胞死亡。植物理性。2006,141(4):1482-1493。10.1104 / pp.106.080697。
- 25.
张某,刘y:激活水杨酸诱导的蛋白激酶,丝丝化活化蛋白激酶,诱导烟草中多种防御反应。植物细胞。2001,13(8):1877-1889。
- 26.
陈志强,陈志强,陈志强:氧化应激激活的丝裂原活化蛋白激酶级联的功能分析。美国国家科学院学报。acta photonica sinica, 2000, 97(6): 2940-2945。10.1073 / pnas.97.6.2940。
- 27。
Komatsu K,Hashimoto M,Maejima K,Shiraishi T,Neriya Y,Miura C,Minato N,Okano Y,Sugawara K,Yamaji Y,Namba S:一种被症状和无症状的植物Asiatica Mosaic病毒分离物编码的坏死诱导的Elicitor域,其表达式由病毒复制调制。Mol植物微生物相互作用。2011,24(4):408-420。10.1094 / mpmi-12-10-0279。
- 28。
张艳艳,王志强,王志强:RPS4在烟草中的表达诱导了一个avrps4独立的HR,需要EDS1、SGT1和HSP90。植物学报,2004,40(2):213-224。10.1111 / j.1365 - 313 x.2004.02201.x。
- 29。
Navarro L, Zipfel C, Rowland O, Keller I, Robatzek S, Boller T, Jones JD:对flg22的转录先天性免疫反应。Avr基因依赖的防御反应和细菌发病机制相互作用和重叠。植物营养与肥料学报。2004,29(2):429 - 434。10.1104 / pp.103.036749。
- 30.
陈伟:拟南芥与紫花假单胞菌亲和和不亲和互作反应的数量特性。植物学报。2003,15(2):317-330。10.1105 / tpc.007591。
- 31.
金春英,刘玉华,杨华,福岛海,Gassmann W, Hildebrand D, Sharp RE, Zhang S:胁迫反应性丝裂原活化蛋白激酶级联反应诱导植物乙烯生物合成。植物学报。2003,15(11):2707-2718。10.1105 / tpc.011411。
- 32.
Liu Y Y, Ren D ., Pike S ., Pallardy S ., Gassmann W ., Zhang S .:叶绿体产生的活性氧参与了丝裂原激活蛋白激酶级联介导的超敏反应样细胞死亡。植物学报,2007,51(6):941-954。10.1111 / j.1365 - 313 x.2007.03191.x。
- 33。
Ozeki J,Takahashi S,Komatsu K,Kagiwada S,Yamashita K,Mori T,Hirata H,Yamaji Y,Ugaki M,Namba S:胰岛素的RNA依赖性RNA聚合酶中的单个氨基酸有助于系统性坏死.拱病毒。2006,151(10):2067-2075。10.1007 / S00705-3-006-0766-3。
- 34。
Earley KW,Haag Jr,Pontes O,Opper K,Juehne T,Song K,Pikaard CS:网关兼容植物功能基因组学和蛋白质组学的载体。工厂J. 2006,45(4):616-629。10.1111 / J.1365-313x.2005.02617.x。
- 35。
Himeno M, majima K, Komatsu K, Ozeki J, Hashimoto M, Kagiwada S, Yamaji Y, Namba S:明显低水平的小RNA积累源自一个包被真菌病毒与dsRNA基因组。病毒学。396(1):69-75。
致谢
我们感谢David Baulcombe博士(剑桥大学,剑桥,英国)烟草响尾病毒载体和沉默抑制基因p19。这项工作得到了日本科学促进协会(Japan Society for the Promotion of Science)的巨额资助,部分还得到了JSPS研究员的巨额资助,以及创新生物科学基础研究活动促进计划(PROBRAIN)的支持。
作者信息
从属关系
相应的作者
额外的信息
作者的贡献
MH、KK、YY、SN设计实验。MH和KK与KM、YO、YY、SN一起进行了实验并进行了数据分析。TS、KI和YT提供了新的试剂和分析工具。MH, KK和SN撰写了论文。所有的作者讨论了结果并批准了最终的手稿。
作者的原始提交的图像文件
权利和权限
开放获取本文在“生物资源”中央有限公司的许可下公布了这是一个开放式访问条款,分配根据创意公约归因许可证的条款(https://creativecommons.org/licenses/by/2.0)提供任何介质中的不受限制使用,分发和再现,所以提供了正确的工作。
关于这篇文章
引用这篇文章
桥本,M.,小松,K.,前岛,K.。et al。3个MAPKKKs形成的线性信号通路导致程序性细胞死亡的鉴定烟草benthamiana.BMC植物BIOL.12,103(2012)。https://doi.org/10.1186/1471-2229-12-103
收到了:
接受:
发表:
关键字
- 计划细胞死亡
- 激酶域
- 过敏反应
- 植物防御反应
- MAPK Cascade.