抽象的
背景
水稻转录因子WRKY45在水杨酸(SA)/苯并噻二唑(BTH)诱导的抗病性中发挥关键作用。它的敲除严重降低了bth诱导的对真菌病原体的抗性Magnaporthe oryzae以及细菌病原体黄oryzaepv。oryzae.(XOO).相反,WRKY45的过表达诱导了对这两种病原体的非常强的抗性。为了阐明wrky45依赖的抗病性的分子基础,我们利用水稻转化子和瞬时基因表达系统分析了wrky45调控的基因表达。
结果
我们使用了微阵列分析WRKY45击倒(WRKY45-KD)米植物,并鉴定了BTH响应基因中的Wrky45依赖性基因。260个基因的BTH反应性依赖于Wrky45。其中220个基因(85%),其中许多编码的PR蛋白和与二次代谢相关的蛋白质进行了次数,通过Bth上调。这些基因的一小部分与由OSNPR1 / NH1调节的那些重叠,支持稻SA途径分支到WRKY45-调节和OSNPR1 / NH1调节的细胞道。地塞内甲酮诱导水稻中Myc标记Wrky45的表达立即上调内源性转录WRKY45据报道,编码转录因子Wrky62,OSNAC4和HSF1的基因,据报道,所有这些都具有与防御相关的功能。随后是对编码Pr蛋白和次级代谢酶的防御基因的上调。许多这些基因也被诱导m.oryzae.感染。他们的时间转录模式与地塞米松诱导后一致WRKY45表达式。在由水稻科鞘细胞的粒子轰击组成的瞬态表达系统中,Wrky45用作效应物,以转移输出报告基因,其中荧光素酶编码序列融合到上游和腺体序列WRKY62和OsNAC4.转录的反式激活是通过w -box的上游序列发生的OsNAC4W箱中的突变废除了逆激活。
结论
这些数据表明wrky45在Bth诱导的疾病抗性中的作用作为转录级联的母稳压器调节水稻SA途径中的两个分支中的一种防御反应。
背景
水杨酸(SA)防御信号通路在中介诱导的防御反应中起着至关重要的作用,包括系统性获得的阻力。在拟南芥中,转录共同诱变剂NPR1在调节SA信号通路时发挥关键作用[1].水稻有一个NPR1对应物OsNPR1/NH1(以下简称OsNPR1),它在抵抗稻瘟病和叶枯病中起主要作用Magnaporthe oryzae以及细菌病原体黄oryzaepv。oryzae.(XOO),分别2那3.].被称为“植物激活剂”的化学防御诱导剂可以通过作用于植物SA信号通路来保护植物抵抗各种疾病[4.-8.].植物激活剂提供对广泛的病原体的保护,它们的“启动效应”减轻了植物生长防御反应的成本[9.].
WRKY转录因子(TFs)是一个超级家族,参与植物的各种调控过程。它们通过绑定到CIS.被称为“W-box”的元素,存在于目标基因的启动子中[10-12].几项研究强调了Wrky TFS在各种植物物种中对不同入侵病原体的植物反应重新编程的重要性[13].WRKY家族有109名稻米家族成员[14].其中一些与SA通路相关的防御反应有关,主要基于过表达研究的实验证据[15-18].然而,大多数獾TF的精确功能仍然是未知的。
以前,我们鉴定了植物活化剂苯并噻唑(Bth)的转型诱导的稻腕45 [19].WRKY45属于WRKY家族的第三组[20.那21]它最近的拟南芥同源物是Atwrky70 [22].WRKY45在水稻对重要病原菌的抗性中发挥着重要作用m.oryzae.和XOO,并由多种植物激活剂诱导[19那23].在我们之前的研究中,WRKY45的过度表达赋予两者极强的抵抗力m.oryzae.和XOO[19那23].微观分析表明,爆炸阻力WRKY45-overexpressing(WRKY45-ox)米基于两层机制:预侵入性防御,可防止真菌菌丝入侵水稻细胞,并伴随人力资源治疗的后侵袭性防御,而探针唑治疗的水稻植物仅显示后侵袭防御[23].我们已经证明WRKY45是由泛素-蛋白酶体降解调控的,类似于拟南芥的NPR1 [24].我们提出,在没有病原体的情况下,这种调节可以在抑制不必要的防御激活中发挥作用[25].最近,我们报道了WRKY45也在介导的抗爆中发挥作用圆锥花序爆炸1,一种通过蛋白质-蛋白质相互作用,具有结合富亮氨酸重复结构的螺旋状核苷酸的blast抗性基因[26].
在拟南芥中,NPR1通过调节超过99%的SA/ bth调控基因在SA通路中发挥主要作用[27],而npr1独立通路也在病原体感染的早期阶段起作用[22那28那29].然而,实验证据表明,水稻中的SA通路与拟南芥中的不同。基于上位性分析的结果,我们提出,由于水稻和拟南芥之间的进化差异,水稻分枝中的sa信号通路进入了wrky45依赖和osnpr1依赖的子通路[19那30.].Arabidopsis NPR1同样调节基因的上调和下调[27,但在水稻中,WRKY45下游调控的分子事件在很大程度上尚不明确。
为了阐明Wrky45依赖性抗病性的分子基础,我们使用水稻转化体分析了Wrky45调节基因表达WRKY45RNAi抑制表达。然后,我们对化学诱导后的代表性基因进行了进一步的表达分析WRKY45表达和m.oryzae.感染。为了验证WRKY45调控的转录级联,我们还对TF基因进行了反式激活实验。
结果
水稻wrky45依赖的bth响应基因的鉴定
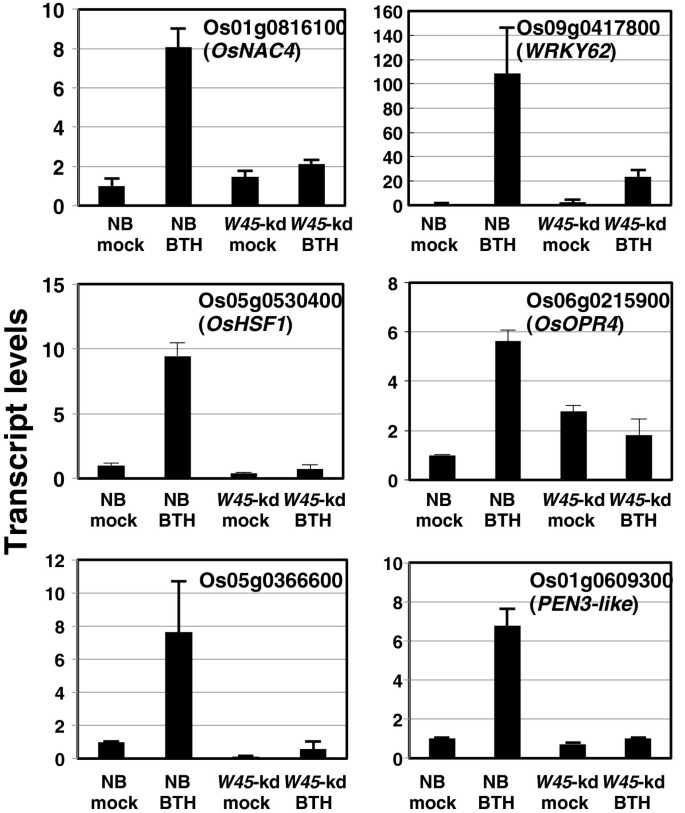
为了确定wrky45依赖的bth应答基因可能在bth诱导的抗病中发挥作用,我们在Nipponbare (NB)和2个株系(#3和#15)中进行了基因表达分析WRKY45- 使用水稻寡核苷酸DNA微阵列覆盖29,923个基因的水稻植物。在以前的一项研究中,我们表明,植物活化剂诱导的爆炸和叶枯肠疾病的水稻抵抗部分受到部分损害WRKY45kd线(23].对具有四种生物复制实验的Bth和模型处理Nb之间基因表达谱的比较,然后分析方差(Anova),确定了1,510个Bth-encipactive基因(P.值<0.05,>表达变化2倍)。双向方差分析差异表达与治疗(BTH或mock)和基因型(NB和WRKY45-kd #3)鉴定了881个具有统计学意义的wrky45依赖的bth应答基因[即wrky45依赖的bth应答基因]。,应用错误发现率(FDR)多次测试修正后q值< 0.2的[31].在这些881个基因中,277显示,BTH处理的NB和线#3之间的2倍变化WRKY45kd植物。其中,第15行中有260个基因也是具有统计学意义的wrky45依赖的bth响应基因(q值< 0.2)WRKY45kd植物(31].这260个基因被定义为wrky45依赖的bth响应基因1:表S1)。在依赖WRKY45的BTH应答基因中,有220个基因(85%)对BTH应答上调,只有40个基因下调,这与我们之前的研究结果一致,表明WRKY45是一个转录激活因子[19].我们进行了定量RT-PCR (qRT-PCR)分析,量化了选定的几个基因的转录水平,其中一些进一步描述如下。qRT-PCR结果验证了微阵列分析的结果(图)1).
qRT-采用PCR方法检测bth应答基因对wrky45的依赖性。在附加文件中用于微阵列分析的相同rna样本(第3行)1通过qRT-PCR分析选定基因的转录模式,验证微阵列分析确定的bth响应性和wrky45依赖性的表达。模拟和bth治疗NB和WRKY45(W45)-kd植物(相对于模拟处理NB)的标准差(SD,N= 3)。rubq1.用于内部控制。
wrky45依赖的bth应答基因的功能分类
鉴定为Wrky45依赖性BTH响应基因的基因在功能分类(附加文件2).编码有病因相关(PR)蛋白的几种基因,例如几丁质酶,葡聚糖酶和过氧化物酶,以及它们中编码富含浓含量的含有含少的重复推定抗性(R)蛋白质的基因。最近对粉末状霉菌真菌 - 拟南芥患者的抗性的研究已经确定了涉及预侵入性阻力机制的一些组分(PEN1,PEN2和PEN3)[32-34].有趣的是,一个编码pen3样ABC转运体的基因(Os01g0609300,附加文件3.),以前涉及非生物应激反应[35],Wrky45依赖性上调。Wrky45依赖性基因还包括许多可能参与次生新陈代谢的许多基因,包括编码细胞色素P450的那些(15个基因,附加文件2).细胞色素p450与抗菌素的生物合成和外源性物质的代谢有关[36以及植物激素。家族1的udp -葡萄糖醛酸基/ udp -葡萄糖基转移酶(GT)家族蛋白[37]已经涉及二次代谢物和激素的糖基化[38那39].我们在wrky45依赖基因中发现了11个编码家族1 GTs的基因2).其中,水杨酸葡萄糖基转移酶(OsSGT1, Os09g0518200)有助于植物激活剂诱导的抗病[40].另一个wrky45依赖家族的直系亲属1GT.基因Os01g0176000在拟南芥中具有病原菌诱导作用,其突变体表现出抗性降低P..雷丁pv。西红柿,AvrRpm1[41].水稻基因组含有59个编码调节谷胱甘肽S-转移酶(GST)的基因,其中22个是Wrky45依赖性上调的(附加文件2).除了抗氧化活性外,谷胱甘肽还通过将谷胱甘肽与底物结合来解毒。编码烯氧合酶(allene oxide synthase)和12-氧植物二烯酸还原酶(12-oxophytodienoic acid reductase, OPR)的基因也依赖wrky45上调,这两种酶是十八烷通路中导致氧化脂肪酸(oxylipin)生成的酶。茉莉酸(oxylipin jasmonic acid, JA)在植物防御中的作用是众所周知的;然而,最近的研究表明,除了JA外,oxylipin还积极参与植物防御机制[42].有趣的是,OsOPR7,负责JA合成[43],不是三个WRKY45依赖性上调OsOPRs(附加文件2).这些osopr的底物和产物及其生物合成途径的最终产物仍然是未知的。
一些编码tf的基因被BTH依赖于wrky45上调(附加文件2).在水稻中,据报道Wrky62负面调节基础和Xa21介导的细菌枯萎病的抗性[44那45].OsNAC4是与超敏反应(HR)相关的程序性细胞死亡的正调节因子[46那47].OSHSF1是病变模拟突变体的致病基因,自发的病变7(SPL7.),其产物通过降低细胞ROS水平负调控植物细胞死亡[48那49].
地塞米松诱导后wrky45依赖基因的时间表达模式WRKY45表达式
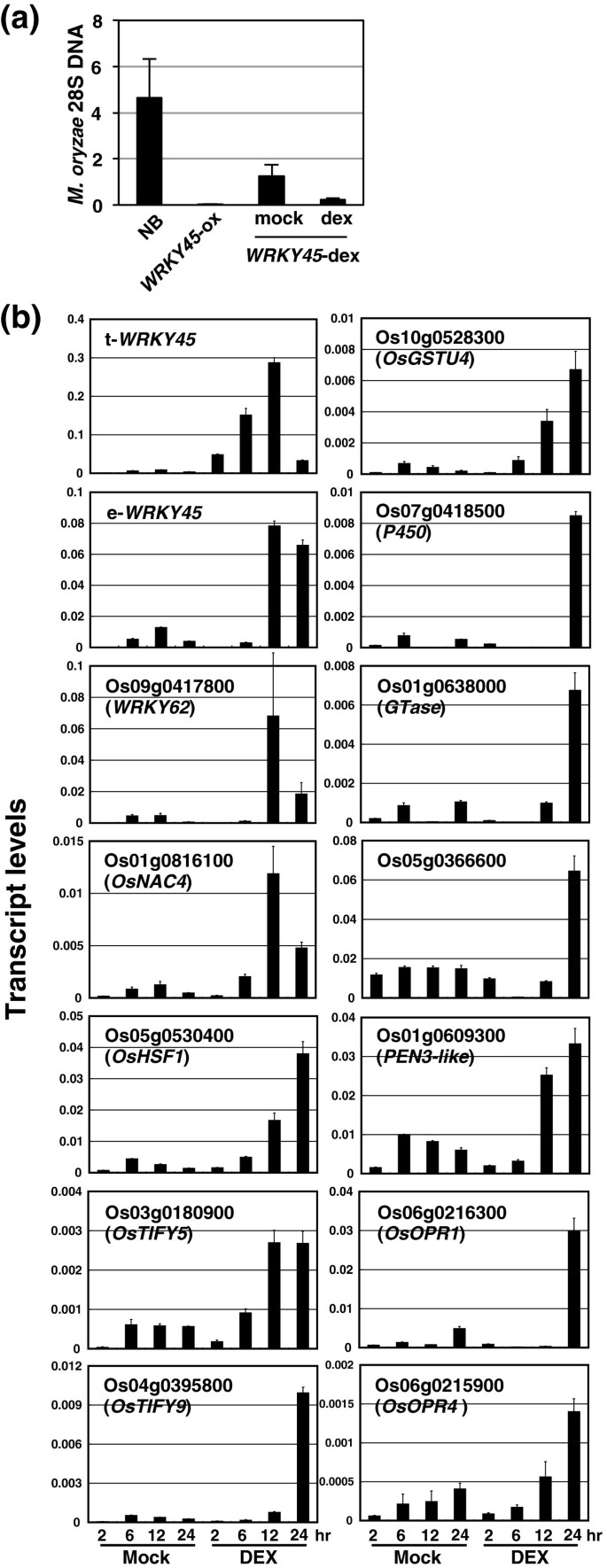
为了表征WRKY45依赖基因表达的时间模式,我们构建了在地塞米松(DEX)诱导启动子控制下表达c末端myc标记WRKY45的转基因水稻植株(WRKY45-myc)。WRKY45敏捷)[50].为了测试WRKY45-myc蛋白是否有功能,我们测试了WRKY45-DEX转化骨线(T2纯合)用于抗抗烫。结果表明WRKY45-dex植物比未转化的日本晴具有更强的抗性m.oryzae.,即使在没有DEX治疗的情况下,推测是由于WRKY45-我的C.阻力WRKY45DEX治疗进一步增强了植物(图2一种)。这些结果证实Wrky45-Myc蛋白保留了其功能。WRKY45在土壤上生长的植物(线#1和#4)用60μmDex或在4-5叶阶段的碎片溶液中喷洒,并且在2,6,12和24小时收获第四片叶子每次治疗。QRT-PCR分析显示转基因衍生的WRKY45转录物(T-WRKY45)在DEX治疗后6小时内开始增加(图2b和附加文件4.:图S2)。有趣的是,内源的转录水平WRKY45在dex诱导的t-增加后很快增加WRKY45(数字2b),提示WRKY45具有自动调节作用。然而,我们没有观察到WRKY45在一个瞬时表达系统中,WRKY45基因通过一个瞬时表达系统(见下文),这表明自动调节是间接的或需要一个额外的因子。
dex诱导后wrky45调控基因的时间表达模式WRKY45表达式。(一)稻瘟病抗性的WRKY45敏捷水稻。用60 μM DEX (0.2% [v/v]乙醇/ 0.01% [v/v] Silwet L-77)或模拟溶液(仅溶剂)处理10株T3纯合子gwg - wrky45 -myc转化株(1号株系),然后喷雾接种m.oryzae.1天后。植物过表达WRKY45受玉米的控制泛素启动子(19以作比较。数量的m.oryzae.28S核糖体DNA (rDNA)泛素1接种后6 d测定mRNA水平。使用SD显示平均值。(b)T3纯合子GVG-WRKY45-myc转化子(第1行)用DEX或模拟溶液处理,如上所述。每处理4株,分别在处理后2、6、12和24 h收获第4片叶片。提取总RNA,采用qRT-PCR分析所选基因的转录水平。三个实验的平均值用SD (N= 3)。模拟处理诱导低水平的转基因和候选下游基因的转录本;原因尚不清楚。
其他wrky45依赖的bth应答基因表现出不同的时间表达模式。编码两个tf的基因,WRKY62(AK067834)和OsNAC4(AK073848),在t-诱导后较早诱导WRKY45,几乎伴随着内源性WRKY45,而编码另外两种tf的基因,OSHSF1(AK100412)和OsTIFY5(AK073589),随后诱导(图2).我们还分析了从其他官能团随机选择的其他基因的表达。这些基因中的一些比内源性高于上调WRKY45,一些[例如,细胞色素p450(ak072220)和Osopr1(ak103067)]比其他人激活,[例如,osgstu4(ak103453)和osprop4(ak072596)](图2).类似的表达分析使用另一个独立的转基因线(附加文件4.给出了一致的结果。
WRKY45监管基因对的反应m.oryzae.感染
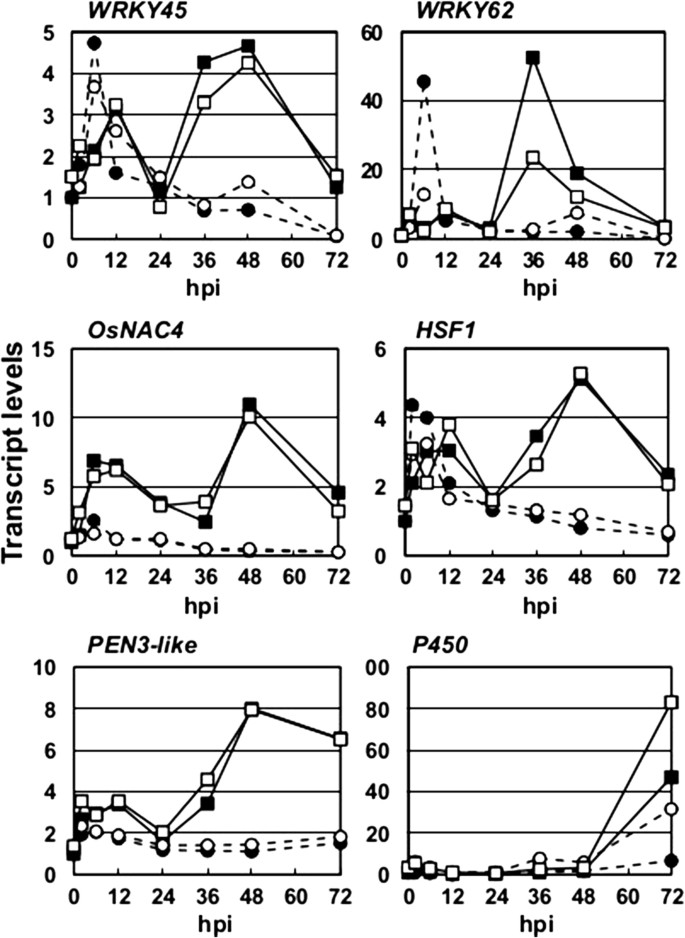
我们分析了NB水稻中部分wrky45调控的基因对稻瘟病菌侵染的响应(图)3.).用兼容的种族接种切割稻草叶子m.oryzae.(race 007.0)或mock处理,并测定选定的wrky45调控基因的转录水平。的转录水平WRKY45在模拟处理的叶片中短暂增加,推测是由于非生物胁迫,如高湿度,然而m.oryzae.接种延迟了这种早期的转录WRKY45.此外,m.oryzae.接种诱导第二个大峰WRKY4536 h后的转录模式WRKY62和OSHSF1相似于WRKY45.的转录模式OsNAC4不同之处在于它是在不久之后引起的m.oryzae.接种36 h后再次接种。PEN3-像(AK058981)和P450.(AK072220)基因的诱导时间晚于编码WRKY45等转录因子的基因。这些wrky45调控基因的转录时间相对于WRKY45,特别是转录第二峰的时间,与dex诱导表达后观察到的相似WRKY45.这些结果表明,WRKY45在后防御基因表达中起主要作用m.oryzae.感染。
反演OsNAC4和WRKY62基因由WRKY45
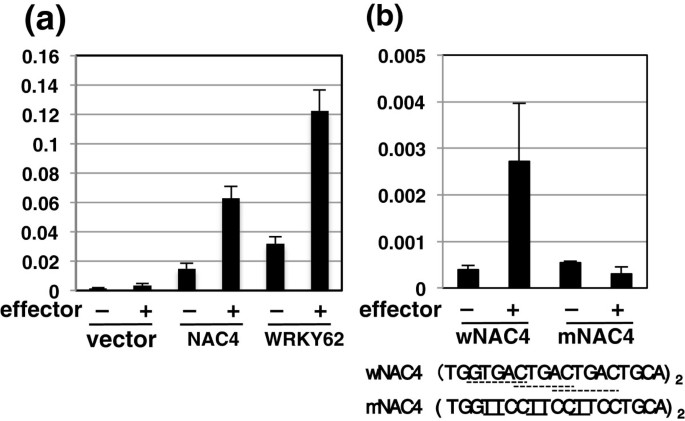
dex诱导的WRKY45-myc蛋白的表达,导致除WRKY45外,编码tf的一些WRKY45依赖的bth应答基因立即上调(图)2).这些结果使我们利用WRKY45在水稻胚芽鞘中的瞬时表达检测其基因的反式激活。Co-delivery的WRKY45效应基因显著激活报告基因hrLUC报告基因在上游和基因内序列的下游融合OsNAC4基因(图4.一种)。上游地区存在W字体(TTGACC / T)OsNAC4在-498年。这些w -box的突变大大降低了反式激活活性,证实了这些是WRKY45相互作用的顺式元件(图)4.b).在上游区域也存在W-boxWRKY62在-454(图4.a).然而,该序列并不介导报告基因的激活(数据未显示)。这些结果表明,WRKY45有可能与非W-box顺式元件或转录起始位点下游的W-box相互作用WRKY62.或者,WRKY45间接调节WRKY62.
反演OsNAC4和WRKY62由WRKY45基因。(一)反演WRKY62和OsNAC4瞬时反式激活试验中的基因。上游和基因内区WRKY62(-1,070 - +1,838)或OsNAC4(- 1000 - + 1272)融合到hrLUC以pGL4.7载体(Promega)中的基因作为报告基因。萤火虫Luc.由玉米泛素启动子驱动的基因用作参考基因。报告基因与效应基因(120ng)与效应基因(120ng)共同递送到水稻上(+)或没有( - )WRKY45cDNA和内参基因(萤火虫Luc.).在三个生物复制中测定了荧光素酶的活性。使用SD显示平均值。(b)w -box突变分析OsNAC4瞬时转发测定中的上游区域。副本的副本OsNAC4上游序列(-504—485)包含野生型(wNAC4)或突变型(mNAC4)的w -box样序列融合成萤火虫Luc.基因被用作报告基因。报告基因与上述( - )与上述( - )WRKY45 cDNA的(+)或没有( - )WRKY45 cDNA共同递送500ng效应基因。hrLUC参考基因。荧光素酶活性在三次重复中测定。使用SD显示平均值。
讨论
WRKY45调节许多BTH响应基因
为了了解特定TF的功能,识别由其直接或间接调控的基因是很重要的。TFs的结构性过表达可以产生新形态表型,但不一定反映所研究的TFs的真正功能[51],因为过表达的TFS偶尔会与非物质学靶标结合。为了避免这个问题,我们使用了WRKY45结合BTH处理鉴定wrky45调控基因。基于微阵列的筛查发现了200多个依赖于wrky45的bth响应性的基因1和2).与WRKY45作为一个转录激活因子一致[19,约85%的基因在BTH反应中上调。考虑到bth诱导的对真菌和细菌疾病的抗性在WRKY45米饭,这些结果表明Wrky45监管基因功能的累积效应在强外防反应中达到了高潮。
Wrky45在稻米SA路径中的作用
在拟南芥中,大于99%的BTH响应基因的表达依赖于NPR1,并且几个腕表TFS在NPR1下游进行了转录调节[27].我们之前的上位性分析表明,在水稻中,WRKY45和OsNPR1在sa信号通路中基本上是相互独立的[19].根据我们的成绩单分析[30.,在osnpr1依赖的子通路中,三分之二的bth应答基因是bth下调。这些下调的基因包括几个参与光合作用和蛋白质合成的基因,表明OsNPR1的主要作用之一是将能量和资源从细胞的家务活动转移到防御活动[30.].这与本研究中发现的wrky45依赖的BTH应答基因形成对比,其中约85%的基因被BTH上调。值得注意的是,它们中的大多数是独立于OsNPR1的(附加文件1和2),而它们在拟南芥中假定的对应基因是依赖于npr1的[27].这些结果与我们的提议一致,即水稻分枝中的sa信号通路进入wrky45依赖和osnpr1依赖的子通路[19].与NPR1类似,WRKY45被蛋白酶体降解,而我们没有观察到OsNPR1的降解[25].这些差异也似乎反映了WRKY45和OSNPR1在水稻中的角色。
拟南芥AtWRKY70与水稻WRKY45系统发育相似[22那52]并在NPR1的下游受到监管[27].的归纳AtWRKY70在诱导早期阶段期间,SA的基因部分独立于NPR1 [22那29],但后来它变成NPR1依赖[27].这表明AtWRKY70与水稻WRKY45之间存在进化关系。
WRKY45可能调控入侵前防御基因
我们的显微分析显示了一种有效的入侵前防御反应WRKY45牛水稻;也就是相容性的感染m.oryzae.在真菌菌丝侵入水稻细胞之前被强烈阻断[23].从wrky45调控的基因库来看,这很有趣。在双子叶植物中,PR蛋白在SAR过程中通过蛋白分泌途径分泌到细胞外[53那54]和非宿主抗性期间[33].的WRKY45- 依赖上调公关基因提示PR蛋白参与了wrky45依赖的入侵前防御。拟南芥对大麦白粉病的非寄主抗性研究(Blumeria茎f . sp。HORDEI.)确定了入侵前防御机制的一些组成部分[32-34].Bednarek等.[55]提出,位于血浆膜中的ABC转运蛋白,在血浆膜穿过抗微生物二次代谢物(葡萄糖苷),这在血浆膜上发挥作用,导致其细胞外累积。特定细胞色素P450s,GST和GTase也涉及抗菌次级代谢物的合成[55].值得注意的是,用于与PEN3类似的ABC转运蛋白以及几种细胞色素P450s,GST和GTAse的一些基因在本研究中鉴定的Wrky45依赖性受调节基因中。米饭缺乏葡萄糖苷途径;然而,涉及尚未鉴定的抗微生物化合物的类似防御机制可以参与Wrky45依赖性预侵入防御反应。在我们的实验条件下用探针处理的水稻植物中未观察到预侵入性防御反应[23].因此,我们不能得出这样的结论:在自然条件下,WRKY45诱导入侵前防御的功能是内在的。需要进一步的研究来解决这个问题。
WRKY45在调控植物细胞死亡中的可能作用
与人力资源相关的编程细胞死亡是各种抗微生物防御系统的重要组成部分。反应性氧物种(ROS)在HR相关的防御机制中发挥作用,也可以作为信号分子和编程细胞死亡的生物化学触发。Iwai.等.[5.[报道,当用探针唑接种喷砂真菌时,在水稻叶片上形成的HR病变。在先前的研究中,微观分析表明,伴随人力资源细胞死亡后侵入性防御在胆管唑治疗的水稻植物中发生了Wrky45m.oryzae.感染(23].鉴于这些观察,它特别有趣OsNAC4作为WRKY45的直接靶标调控BTH。过度的OsNAC4培养的水稻细胞中的cDNA导致HR细胞死亡,并伴有质膜完整性的丧失和核DNA的碎裂[46].因此,OsNAC4可能在植物激活剂诱导的抗病过程中调控HR细胞的死亡。蛋白磷酸化是OsNAC4核定位和HR细胞死亡所必需的[46].这可能是丙苯唑处理水稻接种真菌后HR细胞死亡的原因。OsNAC4通过其下游基因调控HR细胞死亡,OsHSP90和IREN,分别参与质膜完整性的丧失和细胞核DNA的碎裂[46那47].既不OsHSP90也不IREN在微阵列分析中发现依赖于wrky45(附加文件1),也没有在dex诱导表达myc标记的WRKY45后上调(数据未显示)。这些结果与OsNAC4诱导HR细胞死亡需要翻译后调控这一事实相一致[46]并且也与缺乏人力资源细胞死亡相一致WRKY45-牛稻在无病原菌接种的情况下。
OsHSF1是TF的显性负突变体SPL7.显示病变模拟自发细胞死亡(山口等., 2002),其中ROS水平增加(Kojo等, 2006)。因此,OsHSF1的正常功能可能是通过保护植物细胞免受ROS引起的细胞氧化损伤来抑制植物细胞死亡。坏死的植物细胞死亡在植物体的广泛区域可能是有害的,也有利于半生物营养病原体,如m.oryzae..因此,防止植物坏死细胞死亡可能是植物防御反应的重要组成部分。
结论
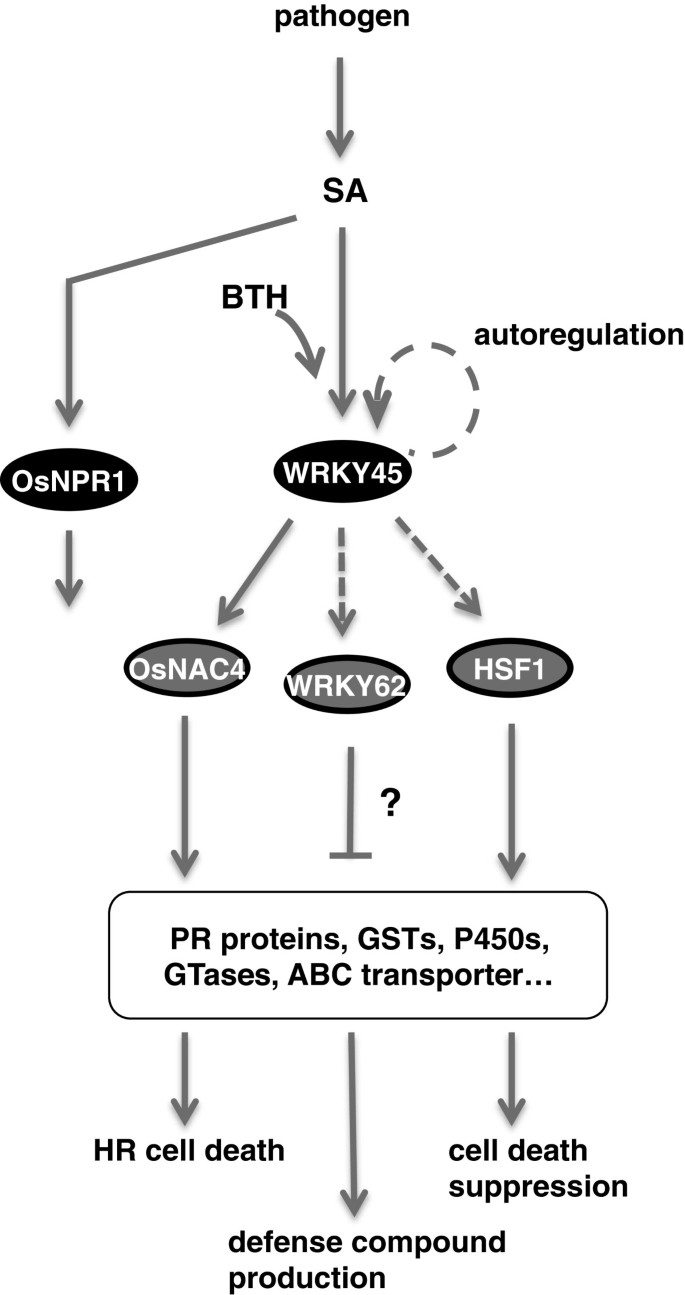
在bth应答基因中,wrky45依赖的基因库与水稻SA通路分为两个子通路的观点相一致(图)5.).转录因子和防御基因编码基因的序列表达,以及WRKY45对TF基因的反转录激活,表明在转录级联中,WRKY45调控下游转录因子编码基因,而下游转录因子编码基因又调控不同的防御基因集(图)5.).Wrky45的过表达诱导对真菌病原体的极强抗性m.oryzae.以及细菌病原体XOO.这种TF的强大潜力可能是因为它控制SA途径介导的防御反应作为该转录级联的主TF。Wrky45调节基因的鉴定为Wrky45调节的防御反应提供了一些见解,以及表型WRKY45-kd和-ox变换器。这些分析也提出了一些问题,比如为什么WRKY62,它编码一种负调控因子XOO电阻(44],由Wrky45调节。每个下游TF的功能表征将有助于对WRKY45调节的防御机制进行解剖,并为其实际应用提供重要信息。
方法
植物材料和化学品
米 (栽培稻ssp。粳稻简历。日本晴(Nipponbare)植物在生长室中生长,并用BTH处理,如前所述[19].DEX处理采用60 μM DEX溶液(0.2% [v/v]乙醇/ 0.01% [v/v] Silwet L-77 (OSI Specialties Inc., Danbury, CT, USA)喷于4- 5叶期水稻叶片。在模拟处理中,只将溶剂喷洒在植物上。
质粒建设和植物转化
在水稻细胞中构建了驱动dex诱导表达myc标记的WRKY45蛋白的质粒WRKY45通过PCR与引物扩增XHO.i-wrky45fw(5'-ctcgagatgacgtcatcgatgtc-3')和BamHI-WRKY45RV(5“-GGATCCAAAGCTCAAACCCATAATG-3”)。然后将扩增片段插入pGEM-T Easy载体(Promega,http://www.promega.com/)生成包含的PGEM-Wrky45,其中包含了WRKY45cd和一个BamH我网站之间XHO.我和囊我的网站。编码三个连续重复的DNA片段我的C序列(3×我的C, 5 ' - atggagcaaaagcttatcagtgaggaagacttgaacgagcagaagctgattccgaagaggatctcaacgagcaaaagctcatctcggagagacctgctc -3 ')插入BamH我和囊我在PGEM-Wrky45中的网站。含有含有的DNA接头Xba我网站插入了囊我和Nsi我在PGEM-Wrky45中的网站。最后,一个片段编码WRKY45CD和3× 我的C序列用XHO.我和Xba我,和插入之间XHO.我和SpeI在DEX诱导基因表达载体中的遗址PTA7002 [50].水稻是通过转基因技术转化的农杆菌(菌株EHA105)介导的方法[56]以产生转基因GVG-WRKY45-myc植物。
微阵列分析
NB和WRKY45击倒(WRKY45在生长室内用0.5 mM BTH (0.5% [v/v]丙酮/ 0.05% [v/v] Tween 20)或模拟溶液处理水稻植株。然后,从每个处理/基因型的4株植株上收获第4片叶片,并根据不同处理和基因型进行汇总。从每个库中分离出总RNA,用Cy3标记,并与Agilent Rice Oligo Microarray (44 k,定制,http://www.home.agilent.com.).我们分析了每种治疗基因型组合的四组生物重复样本。如前所述进行了微阵列实验和数据分析[19那30.].简而言之,基于两个意义,在Nb米中鉴定出Bth-encection基因[AnovaP.- 根据Benjamini和Hochberg的方法,在使用FDR多次测试校正后value <0.05 [31]]和-fold变化(2倍)。这些基因通过双向方差分析进行筛选,同时考虑了基因型和治疗效果。wrky45依赖的b - th响应基因被定义为在两个系列中b - th响应表达减少(小于NB中相应表达的1/2)的基因WRKY45-采用FDR多次测试修正后q值< 0.2的kd大米(#3和#15)[31].
m.oryzae.接种
水稻在温室里种植了20天。在四叶期,最嫩的叶子被剪下来,放在塑料盒的湿纸上。在25°C预培养6 h后,用5.0 × 105.兼容的0.02%Tween 20的孢子/ mlm.oryzae.分生孢子(race 007.0),然后在黑暗中保存3天。
QRT-PCR分析
利用Trizol试剂(Invitrogen,http://www.lifetechnologies.com),用RNeasy迷你试剂盒纯化(Qiagen,http://www.qiagen.com).使用上标II rnase H(Invitrogen)和寡核苷酸(DT)23引物进行逆转录(Sigma-Aldrich,http://www.sigmaaldrich.com/).qRT-PCR在Thermal Cycler Dice TP800系统(TaKaRa,http://www.takara-bio.co.jp/),使用SYBR预混ExTaq混合物(TaKaRa),循环95°C 5 s, 55°C 10 s和72°C 20 s。杜白蛋白1(rubq1.;AK121590)作为内标。所使用的引物在附加文件中列出5..
瞬时表达检测
反式活化试验中,将水稻内叶鞘切成块,并排放置在含有0.4 M甘露醇的琼脂平板上。有或没有质粒WRKY45CDNA由花椰菜马赛克病毒驱动35个年代pUCAP载体中的启动子作为效应基因。将效应质粒和3 μg的报告基因和500 ng的内参基因一起导入叶鞘荧光素酶(Luc.)使用PDS-1000 / HE生物粒子输送系统(Bio-rad,http://www.bio-rad.com).在28°C孵育6 h后,采集样品并在液氮中研磨。采用DualGlo荧光素酶报告基因分析系统(Promega)检测荧光素酶活性,计算报告基因产物与内参基因产物活性的比值。
可获得的支持数据
支持本文结果的微阵列数据集可以在基因表达综合库GSE23733中找到。http://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE23733.
参考
- 1.
曹辉,董晓东:拟南芥系统获得性抗性诱导突变体的研究进展。植物学报,1994,6(11):1583-1592。
- 2.
水稻NPR1同源物的过度表达导致防御反应的结构性激活和对光的超敏反应。植物与微生物学报,2005,18(6):511-520。10.1094 / mpmi - 18 - 0511。
- 3.
袁勇,钟胜,李强,朱震,娄阳,王磊,王静,王明,李强,杨东,等:水稻的功能分析NPR1类基因表明,OsNPR1/NH1是水稻抗病与增强草食动物易感性的同源基因。植物营养与肥料学报,2011,30(2):531 - 534。10.1111 / j.1467-7652.2007.00243.x。
- 4.
丙苯唑诱导小鼠系统性获得性耐药拟南芥具有新颖的行动。工厂J. 2001,25(2):149-157。10.1046 / J.1365-313x.2001.00952.x。
- 5.
Iwai T, Seo S, Mitsuhara I, Ohashi Y: probenazol诱导的水杨酸积累带来抗性稻瘟病菌在成人稻植物中。植物细胞生理。2007,48(7):915-924。10.1093 / PCP / PCM062。
- 6.
Friedrich L, Lawton K, Ruess W, Masner P, Specker N, Rella MG, Meier B, Dincher S, Staub T, Uknes S,等:苯并噻唑衍生物诱导烟草系统性获得性抗性。植物学报,1996,10(1):61-70。10.1046 / j.1365 - 313 x.1996.10010061.x。
- 7.
Lawton Ka,Friedrich L,Hunt M,Weymann K,Delaney T,Kessmann H,Staub T,Ryals J:苯并噻唑诱导疾病抗病拟南芥通过激活全系统获得的电阻信号转导通路。工厂J.996,10(1):71-82。10.1046 / J.1365-313x.1996.10010071.x。
- 8。
Yasuda M, Kusajima M, Nakajima M, Akutsu K, Kudo T, Yoshida S, Nakashita H:噻二唑羧酸部分,SV-03诱导烟草无水杨酸积累的系统获得性抗性。昆虫科学,2006,31(3):329-334。10.1584 / jpestics.31.329。
- 9。
Conrath U,Pietersecm,Mauch-Mani B:植物病原体相互作用的启动。趋势植物SCI。2002,7(5):210-216。10.1016 / s1360-1385(02)02244-6。
- 10.
Rushton PJ, Torres JT, Parniske M, Wernert P, Hahlbrock K, somsich IE:诱导子诱导的dna结合蛋白与欧芹启动子中诱导子响应元件的相互作用PR1基因。中国海洋大学学报(自然科学版),1996,15(20):2690 - 2600。
- 11.
植物防御信号的早期核事件:WRKY转录因子的快速基因激活。中国海洋大学学报(自然科学版),1996,18(17):4689-4699。10.1093 / emboj / 18.17.4689。
- 12.
马立克,李文,Eulgem,摩根,Schmid, Lawton, Dangl JL, Dietrich RA:转录组拟南芥在系统性获得性抗性期间。中国生物医学工程学报,2000,26(4):403-410。10.1038/82521。
- 13.
Pandey SP, somsich IE: WRKY转录因子在植物免疫中的作用植物营养与肥料学报。2009,30(4):453 - 457。10.1104 / pp.109.138990。
- 14.
刘勇,沈庆杰:《中国科学院大学学报》WRKY大米的基因家庭(栽培稻).J Intent Plant Biol。2007,49(6):827-842。10.1111 / J.1744-7909.2007.00504.x。
- 15.
邱D,Xiao J,Ding X,Xiong M,Cai M,CaO Y,Li X,Xu C,王S:Oswrky13通过调节水杨酸和茉莉依赖信号传导中的防御相关基因介导水稻疾病抗性。Mol植物微生物相互作用。2007,20(5):492-499。10.1094 / mpmi-20-5-0492。
- 16.
邱丹丹,肖军,谢伟,刘红霞,李晓霞,熊磊,王树峰:水稻抗病正向调控基因OsWRKY13的表达谱分析。acta botanica sinica, 2017, 36(3): 531 - 534。10.1093 / mp / ssn012。
- 17.
关键词:OsWRKY03,水稻,OsNPR1,防御信号通路,转录激活子细胞研究,2005,15(8):593-603。10.1038 / sj.cr.7290329。
- 18。
Liu X, Bai X, Wang X, Chu C: OsWRKY71转录因子参与水稻防御反应。植物生理学杂志。2007,164(8):969-979。10.1016 / j.jplph.2006.07.006。
- 19。
Shimono M, Sugano S, Nakayama A, Jiang CJ, Ono K, Toki S, Takatsuji H:水稻WRKY45在苯并噻唑诱导的稻瘟病抗性中起关键作用。植物学报。2007,19(6):2064-2076。10.1105 / tpc.106.046250。
- 20.
植物转录因子的WRKY超家族。植物科学进展,2000,5(5):199-206。10.1016 / s1360 - 1385(00) 01600 - 9。
- 21.
Kalde M, Barth M, somsich IE, Lippok B:成员拟南芥WRKY组III转录因子是不同植物防御信号传导途径的一部分。Mol植物微生物相互作用。2003,16(4):295-305。10.1094 / mpmi.2003.16.4.295。
- 22.
Li J, Brader G, Palva ET: WRKY70转录因子:茉莉酸介导和水杨酸介导信号在植物防御中的融合节点。植物学报。2004,16(2):319-331。10.1105 / tpc.016980。
- 23.
Shimono M,Koga H,Akagi Aya,Hayashi N,Goto S,Sawada M,Kurihara T,Matsushita A,Sugano S,Jiang C-J等:米Wrky45在真菌和细菌疾病抵抗中起重要作用。莫尔植物途径。2012,13(1):83-94。10.1111 / J.1364-3703.2011.00732.x。
- 24.
Spoel Sh,Mou Z,Tada Y,Spivey NW,Genschik P,Dong X:蛋白酶体介导的转录同型患者NPR1在调节植物免疫力方面发挥双重作用。细胞。2009,137(5):860-872。10.1016 / J.Cell.2009.03.038。
- 25.
Matsushita, Inoue H, Goto S, Nakayama A, Sugano S, Hayashi N, Takatsuji H:核泛素蛋白酶体降解影响水稻防御程序中的WRKY45功能。植物学报,2013,73(2):302-313。10.1111 / tpj.12035。
- 26.
Inoue H, Hayashi N, Matsushita A, xinqiang L, Nakayama A, Sugano S, Jiang CJ, Takatsuji H: WRKY45介导的CC-NB-LRR蛋白Pb1的抗性。中国科学(d辑:地球科学),2013,32(6):591 - 598。10.1073 / pnas.1222155110。
- 27.
王东,董晓东:植物系统获得性抗性转录网络中调控节点的基因组识别方法。公共科学图书馆。2006,2 (11):e123-10.1371/journal.ppat.0020123。
- 28.
Blanco F, Salinas P, Cecchini N, Jordana X, Van Hummelen P, Alvarez M, Holuigue L:拟南芥对水杨酸的早期基因组反应。植物学报,2009,40(1):97 - 101。
- 29.
关键词:拟南芥,WRKY70, rpp4,抗性,透明质粒寄生性植物与微生物学报,2007,20(2):120-128。10.1094 / mpmi - 20 - 2 - 0120。
- 30.
Sugano S, Jiang C- j, Miyazawa S- i, Masumoto C, Yazawa K, Hayashi N, Shimono M, Nakayama A, Miyao M, Takatsuji H: OsNPR1在水稻防御计划中的作用。acta botanica sinica(云南植物学报),2010,34(6):549-562。10.1007 / s11103 - 010 - 9695 - 3。
- 31.
Benjamini Y,Hochberg Y:控制虚假的发现率:一种实用而强大的多种测试方法。J Royal统计SOC。1995年,B57:289-300。
- 32.
Lipka V,Dittgen J,Bednarek P,Bhat R,Wiermer M,Stein M,Landtag J,Brandt W,Rosahl S,Scheel d等:Postinvasion防御既有助于非健康抵抗拟南芥.中国科学(d辑):地球科学(d辑)。10.1126 / science.1119409。
- 33.
Collins NC,Thordal-Christensen H,Lipka V,BAU S,Kombrink E,邱J-L,Huckelhoven R,Stein M,Freialdenhoven A,Somerville Sc,等:植物细胞壁的陷阱蛋白介导的抗病性抗性。自然。2003,425(6961):973-977。10.1038 / Nature02076。
- 34.
Stein M, Dittgen J, Sanchez-Rodriguez C, Hou B-H, Molina A, Schulze-Lefert P, Lipka V, Somerville S拟南芥PEN3/PDR8是一种ATP结合盒转运体,有助于对通过直接穿透进入的不适当病原体产生非宿主抗性。植物学报,2006,18(3):731-746。10.1105 / tpc.105.038372。
- 35.
Moons A:Ospdr9在水稻根系中,重金属、缺氧胁迫和氧化还原干扰均可诱导pdr型ABC转运体。王志强,王志强,王志强,等。10.1016 / s0014 - 5793(03) 01060 - 3。
- 36.
de Montellano PR O, Nielsen K, Møller B:植物细胞色素p450。细胞色素P450。我们:施普林格;2005:553 - 583。
- 37.
曹鹏杰,刘志刚,刘志刚:水稻糖基转移酶系统基因组数据库的构建及分化糖基转移酶的鉴定。acta botanica sinica, 2017, 36(5): 531 - 534。10.1093 / mp / ssn052。
- 38.
B:糖基转移酶:小分子的管理者。植物生态学报,2005,8(3):254-263。10.1016 / j.pbi.2005.03.007。
- 39.
植物天然产物合成中的糖基转移酶:一个表基因家族的特性。植物科学进展,2000,5(9):380-386。10.1016 / s1360 - 1385(00) 01720 - 9。
- 40。
UMEMURA K,SATOU J,IWATA M,Uozumi N,Koga J,Kawano T,Koshiba T,Anzai H,Mitomi M:水杨酸葡萄糖三种转移酶,OSSGT1的贡献,在水稻植物中化学诱导疾病抗性。工厂J.2009,57(3):463-472。10.1111 / J.1365-313x.2008.03697.x。
- 41。
糖基转移酶基因的致病菌应答表达UGT73B3.和UGT73B5有必要抵抗吗假单胞菌含油光伏番茄拟南芥.植物理性。2005,139(4):1890-1901。10.1104 / pp.105.067223。
- 42。
Blée E:植物氧合脂在植物防御中的作用。植物科学进展,2002,7(7):315-322。10.1016 / s1360 - 1385(02) 02290 - 2。
- 43.
Tani T,Sobajima H,Okada K,Chujo T,Arimura S-I,Tsutsumi N,Nishimura M,Seto H,Nojiri H,Yamane H:鉴定OsOPR7水稻茉莉酸生物合成中12-氧植物二烯酸还原酶的基因编码。植物学报。2008,27(3):517-526。10.1007 / s00425 - 007 - 0635 - 7。
- 44.
PENG Y,BARTLEY LE,CHEN X,DARDICK C,CHERN M,Ruan R,Canlas PE,Ronald PC:OSWRKY62是基础的负稳压器Xa21- 反对防御黄oryzaepv。oryzae.在大米。植物学报。2008,31(3):446-458。10.1093 / mp / ssn024。
- 45.
Park CJ, Ronald PC:水稻XA21免疫受体的切割和核定位。国家自然科学基金,2012,3:920-
- 46.
Kaneda T,Taga Y,Takai R,Iwano M,Matsui H,Takayama S,Isogai A,Che F-S:转录因子Osnac4是植物过敏细胞死亡的关键正调节因子。Embo J. 2009,28(7):926-936。10.1038 / emboj.2009.39。
- 47.
Taga Y,Takai R,Kaneda T,Matsui H,Isogai A,Che FS:OSHSP90和IREN,CA2 +依赖性核酸酶的作用,在植物过敏细胞死亡中由转录因子OSNAC4诱导。植物信号表现。2009,4(8):740-742。10.4161 / PSB.4.8.9087。
- 48.
yanouchi U, Yano M, Lin H, Ashikari M, Yamada K:水稻斑点叶基因,Spl7,编码热应激转录因子蛋白。中国科学(d辑:地球科学),2002,19(11):1397 - 1399。10.1073 / pnas.112209199。
- 49.
Kojo K,Yaeno T,Kusumi K,Matsumura H,Fujisawa S,Terauchi R,IBA K:ROI代的监管机制受米饭的影响spl突变。植物细胞生理。2006,47(8):1035-1044。10.1093 / PCP / PC9074。
- 50.
Aoyama T,Chua NH:转基因植物中的糖皮质激素介导的转录诱导系统。工厂J. 1997,11(3):605-612。10.1046 / J.1365-313x.1997.11030605.x。
- 51.
张建忠:植物转录因子的过表达分析。植物生态学报,2003,6(5):430-440。10.1016 / s1369 - 5266(03) 00081 - 5。
- 52.
Ryu H-S, Han M, Lee S- k, Cho J-I, Ryoo N, Heu S, Lee Y-H, Bhoo S, Wang G-L, Hahn T-R等:综合表达分析WRKY水稻防御反应中的基因超家族。植物学报,2006,25(8):836-847。10.1007 / s00299 - 006 - 0138 - 1。
- 53.
王丹丹,王志伟,董晓东:诱导蛋白分泌途径对系统性获得性抗性的作用。中国科学:地球科学。10.1126 / science.1108791。
- 54.
Kalde M, Nühse TS, Findlay K, Peck SC: syntaxin SYP132有助于植物抗细菌和分泌致病相关蛋白1。中国科学(d辑:地球科学),2007,38(4):531 - 534。10.1073 / pnas.0701083104。
- 55.
bennarek P, pislewka -Bednarek M, Svatos A, Schneider B, Doubsky J, Mansurova M, Humphry M, concenni C, Panstruga R, Sanchez-Vallet A, et al .:硫代葡萄糖苷代谢途径在植物细胞中介导广谱抗真菌防御。中国科学:地球科学。10.1126 / science.1163732。
- 56.
Toki S, Hara N, Ono K, Onodera H, Tagiri A, Oka S, Tanaka H:盾状组织早期感染农杆菌允许水稻的高速变换。工厂J. 2006,47:969-976。10.1111 / J.1365-313x.2006.02836.x。
确认
这项工作得到了日本农业,林业和渔业部的批准(农业创新的基因组,GMA0001,PMI0008和GMO1006B)。NIA技术支持系统支持稻米转型。我们感谢NIAS的稻米基因组资源中心用于使用米微阵列分析系统,以及Y.NAGAMURA博士和R. Motoyama女士进行技术支持。
作者信息
从属关系
相应的作者
附加信息
相互竞争的利益
两位作者宣称他们没有相互竞争的利益。
作者的贡献
设计实验,进行基因芯片和基因表达分析,撰写稿件。SG分析了植物的基因表达和抗稻瘟病性。SF和AM进行了反式激活实验。MS和SS生成了变压器。AA、MY、CJ、HI帮助基因表达分析。HT设计了这项研究,解释了数据,并撰写了手稿。所有作者阅读并批准了最终的手稿。
电子补充材料
作者为图像提交的原始文件
权利和权限
开放获取本文由BioMed Central Ltd授权发表。这是一篇开放获取的文章,是根据知识共享署名许可协议(https://creativecommons.org/licenses/by/2.0),允许在任何媒介上无限制地使用、分发和复制,但必须正确引用原作。
关于这篇文章
引用这篇文章
中山、福岛、后藤等等。水稻中介导苯并噻二唑诱导防御反应的wrky45调控基因的全基因组鉴定BMC植物杂志13,150(2013)。https://doi.org/10.1186/1471-2229-13-150
收到了:
公认:
发表:
关键词
- WRKY
- 水杨酸
- Benzothiadiazole
- Magnaporthe oryzae
- OsNPR1