摘要
背景
以前,我们已经报道了硫胺素(维生素B1)诱导抗性的能力霜霉在一个易受影响的小道消息中。霞多丽。然而,维生素,特别是硫胺诱导葡萄抗病性的机制仍不清楚。在这里,我们评估了硫胺素是否可以调节葡萄植物中苯丙类途径衍生的植物抗逆素,以及这些次生代谢产物在硫胺素诱导的抗性过程中的作用P.viticola.
结果
我们的数据表明,硫胺素处理诱导了苯丙烷途径基因在葡萄植株中的表达。这些基因的表达与二苯乙烯、酚类化合物、类黄酮和木质素的积累有关。此外,与未处理的对照植物相比,硫胺践踏植物的总抗氧化潜力提高了3.5倍。四种酚类化合物占经硫胺处理的植物抗氧化潜力的97%。在这些化合物中,有caftaric acid,属于羟基肉桂酸家族。这种元素自己贡献了总抗氧化潜力的20%。Epifluorescence显微镜分析显示伴有未支化的改变P.viticola接种过硫胺的植株叶片叶肉中菌丝体和二苯乙烯的产生,表明二苯乙烯是硫胺诱导葡萄抗性的重要组成部分。
结论
这项工作首次显示了硫胺素作为一种维生素,在调节葡萄植物次级代谢中的作用,有助于增强抵抗P.viticola这是葡萄园中最具破坏性的真菌疾病。
背景
小道消息(葡萄)是世界上最重要的园艺水果作物之一。不幸的是,所有品种都易受几种疾病的影响;真菌和卵菌是影响该植物栽培和经济效益的主要病原菌。由专性生物营养菌引起的霜霉病霜霉葡萄枯萎病是最具破坏性的葡萄病害之一。这种疾病降低果实质量和产量,或直接感染浆果,或由于叶片感染导致光合作用和植株活力降低[1].为了保护葡萄品种免受这种病原体的侵害,需要从萌芽到成熟期间多次施用化学物质。然而,使用杀菌剂控制疾病导致了耐药菌株的出现P.viticola[2]、环境污染、食品有毒残留等。在过去十年中,一种疾病控制的新技术被开发出来,它涉及诱导宿主防御机制,作为化学杀菌剂的替代品。
这种植物自身防御系统的激活,被称为诱导抗性(IR),可以通过应用模拟病原体入侵的诱导剂来实现。3.].IR在小道消息中反对P.viticolaH2O2[4],增强具有抗菌活性的致病相关(PR)蛋白的表达,如几丁质酶和葡聚糖酶[4,5],植物抗毒素的产生[6,7],以及胼胝质沉积[4,5].
最近,使用药理学方法证实了苯丙烷通路在葡萄IR机制中的作用[5].苯丙类途径衍生的防御反应,如类黄酮、木质素、二苯乙烯和酚类化合物的合成,已被证明与β-氨基丁酸(BABA)-IR有关P.viticola在小道消息中[5,6].苯丙类途径衍生的植物抗毒素的显著表达,包括不同的二苯基形式,也被报道与IR有关P.viticola在葡萄中使用壳聚糖低聚物[7].此外,β-1,3-葡聚糖- ir对P.viticola在葡萄中伴随着酚类化合物的大量积累[4],它们是次级代谢产物,包括由苯丙烷途径产生的生物遗传学上结构多样化的几种天然产物[8].
酚类物质是植物中主要的天然抗氧化剂,可作为还原剂、自由基清除剂、单线态氧猝灭剂和促氧化剂的潜在络合物[9].酚类物质似乎通过不同的机制来抑制疾病的发展,包括抑制细胞外真菌酶(纤维素酶、果胶酶、漆酶、木聚糖酶等)、抑制真菌氧化磷酸化、营养剥夺(形成金属复合物、蛋白质不溶性)和植物组织中的抗氧化活性[10,11].
由胁迫诱导的具有抗菌活性的低分子次生代谢产物被统称为植物抗毒素,是植物防御系统的重要组成部分。植物抗毒素是一组异质化合物[12],显示出对多种病原体的生物活性,并被认为是抗病性的分子标记。
在过去十年中,来自Vitaceae家族的植物抗毒素一直是许多研究的主题,因为这些化合物被认为对植物病理学和人类健康都有影响[13].虽然大多数植物抗毒素的植物毒性比合成杀菌剂小,但它们可以在植物组织内大量积累,远远超过抑制真菌生长所需的浓度[13].
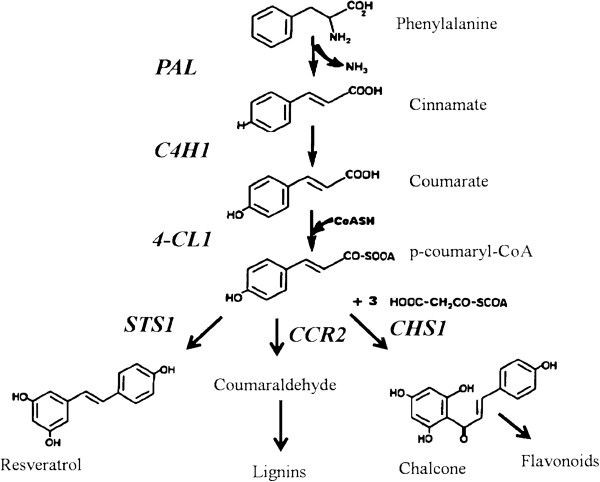
一般的苯丙类代谢产生一系列次级代谢物,这些代谢物以莽草酸途径的少数中间产物为核心单位[6].更相关的葡萄科植物抗毒素包括一组属于二苯乙烯家族的分子[13].二苯乙烯由苯丙氨酸经苯丙酸/丙二酸途径合成,苯丙氨酸经苯丙氨酸解氨酶(朋友)。肉桂酸4-羟化酶的连续作用C4H)和4-香豆酸辅酶a连接酶(4 cl)将肉桂酸转化为对香豆酰辅酶a。从这一途径衍生的化合物,统称为多酚,是通过查尔酮合酶(CHS)、二苯乙烯合酶(STS)和肉桂酰辅酶a还原酶(CCR),分别为黄酮类化合物、二苯乙烯类化合物和木质素(图1) [13,14].
二苯乙烯家族的成员是反式-白藜芦醇结构(3,5,4 .′-trihydroxystilbene)。Piceide (5 4′-二羟基二苯乙烯-3- o -β-吡喃葡萄糖苷)是一种糖基化白藜芦醇衍生物和翼苯乙烯(3,5-二甲氧基-4′-羟基二苯乙烯)是二甲基白藜芦醇衍生物[13].最近研究表明,ε-viniferin的一种异构体δ-viniferin是受感染的葡萄叶片白藜芦醇氧化产生的主要二苯乙烯之一P.viticola[15].Pezet等人[16]测试了这些二苯乙烯类化合物对动物游动孢子的毒性P.viticola(在-体外),发现δ-viniferin和紫檀二苯乙烯是毒性最强的二苯乙烯。
目前,在确定外源应用可以激活植物防御并保护植物免受病原体感染的化学物质方面有巨大的科学和商业兴趣。
诱导子通过模拟病原体攻击或其他胁迫诱导植物抗毒素的产生[3.],可以是病原起源的物质(外源)或植物对病原作用的反应释放的化合物(内源)。
诱导剂在可持续作物生产中具有潜在用途。作为许多生理过程的关键组成部分,维生素可能影响植物-病原体相互作用的结果。近年来,维生素作为营养物质和作为不同疾病的控制剂的重要性已得到证实[17,18].安等人。[17]已经报道了硫胺素(维生素B1)作为植物抗病激活剂的作用。Thiamine-treated大米,拟南芥蔬菜作物表现出对真菌、细菌和病毒感染的抵抗力。硫胺- ir在水稻和拟南芥中的瞬时表达公关基因通过水杨酸和钙2 +相关信号通路。在以前的一项研究中,我们已经报道了硫胺素诱导抗性的能力P.viticola在易感葡萄品种“霞多丽”中通过双重作用模式,包括直接抗真菌活性和诱导宿主防御反应,包括H2O2代,上调公关基因与超敏细胞死亡[19].然而,葡萄中维生素- ir,特别是硫胺- ir的作用机制尚不清楚。在本研究中,我们研究了苯丙类途径代谢在硫胺- ir中的作用P.viticola的小道消息。通过实时定量聚合酶链反应(real-time q-PCR)实验表明,巯基丙氨酸通路基因在硫胺处理后被上调。此外,利用高效液相色谱-二极管阵列检测(HPLC-DAD)、超高效液相色谱-质谱联用(UPLC-MS)、色谱在线抗氧化检测系统(COADS)和组织化学分析进行的定性和定量分析表明,硫胺素处理葡萄藤后,可有效诱导苯丙类植物抗毒素如黄酮类、酚类、木质素和二苯乙烯类等。此外,荧光显微镜观察表明,二苯乙烯可能参与限制P.viticola硫胺处理葡萄叶片叶肉中的菌丝生长。
结果
硫胺素处理对霜霉病发病的影响
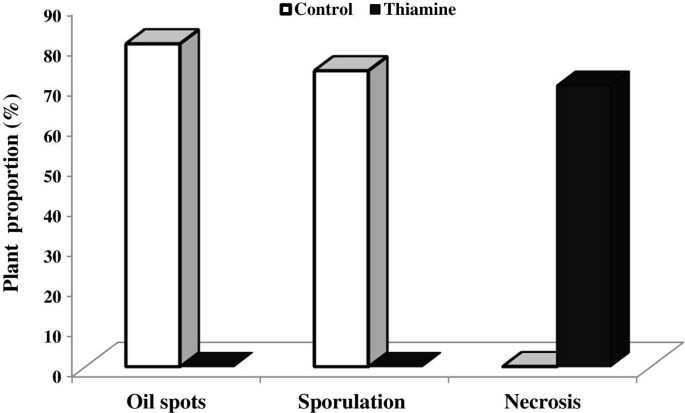
结果如图所示2根据Unger等人的研究,葡萄植株的发病率与具有明显症状的植株的平均百分比相对应。[20.].该数据表明,在对照条件下,出现病原菌产孢的植株平均为63.4%,出现病原菌油斑的植株平均为70.3%,出现坏死的植株平均为0%。相比之下,在硫胺素处理下,出现病原菌产孢症状的植物平均为0%,出现病原菌油斑的植物平均为0%,出现坏死的植物平均为70%。总的来说,这些数据证实了硫胺素在葡萄霜霉病防治中的有效性。
用硫胺素(实心条)或水(白色条)处理的葡萄插枝的发病率(有明显症状的植物的平均百分比)。在温室、对照条件下生长的葡萄植株,用水(对照)或30 mM硫胺素处理,叶片背面接种孢子囊悬浮液,接种量为5 × 104孢子囊/毫升。以出现坏死、油斑和产孢症状的植物的比例,评估7 dpi的发病率[20.].每个处理取6株,试验重复3次。硫胺素处理的各项指标均与对照显著差异(5%)。
硫胺素上调苯丙素通路基因表达
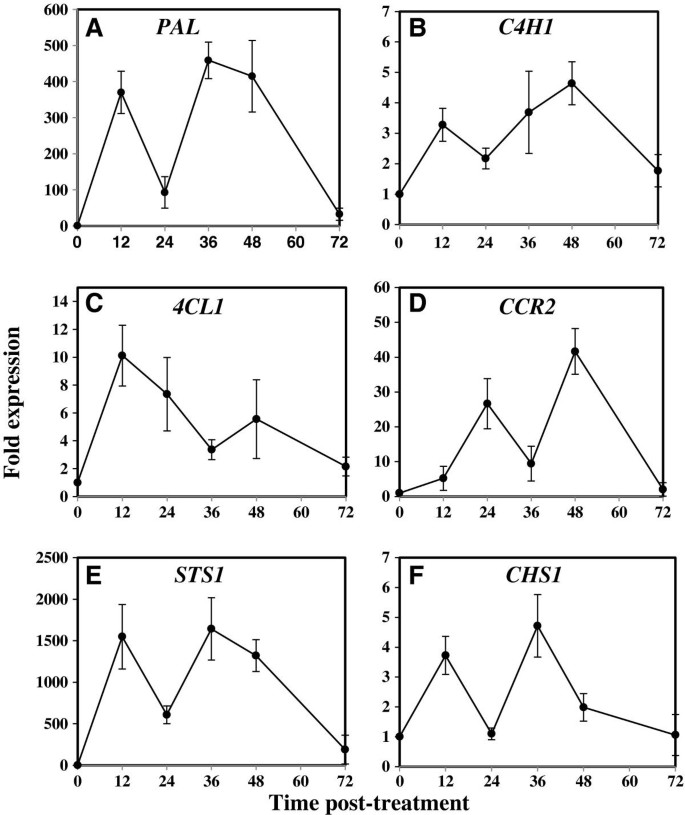
获得的数据(图3.A)表明,硫胺素处理诱导迅速而强烈的积累朋友葡萄植物叶片中的mRNA转录物。的朋友硫胺素诱导在2个时间点达到峰值。第一个峰值在治疗后12小时内检测到,表达量为370倍,而第二个峰值在治疗后36 hpt检测到,表达量为459.11倍,随后逐渐下降至72 hpt(表达量为32.62倍)。
硫胺处理后苯丙烷途径基因转录物积累的时间进程。葡萄藤植物(简历)用30 mM硫胺素(固体条)或水(白色条)处理霞多丽(Chardonnay),并在处理后的不同时间间隔(12、24、36、48和72 hpt)收集叶片。real-time q-PCR检测基因表达。感兴趣的基因有:(一个)朋友(苯丙氨酸解氨酶),(B)C4H1(肉桂酸4-羟基化酶),(C)4 cl14-香豆酸酯:辅酶A连接酶,(D)CCR2(肉桂酰:辅酶A还原酶),(E)CHS1(查尔酮合成酶)及(F)STS1(芪synthase1)。结果显示,在同一时间点,硫胺处理过的样本中防御基因的归一化折叠表达与水处理过的对照组的表达相比(设为1)。结果为3次独立实验的均值±标准差。
C4H1(图3.B)和4 cl1(图3.C)硫胺素处理也诱导mRNA转录,表现出相似的动力学。事实上,两者都有C4H1而且4 cl1诱导量首次在12 HPT内达到峰值(分别为3.27和10.11倍表达量),第二次在48 HPT内达到峰值(分别为4.64和5.56倍表达量),然后逐渐下降到72 HPT(分别为1.77和2.15倍表达量)。
硫胺素处理也上调了CCR2基因(图3.D)葡萄藤植物。CCR2诱导在24 hpt内第一次达到峰值(表达量为26.67倍),在48 hpt内第二次达到峰值(表达量为41.65倍),然后在72 hpt时下降(表达量为2.01倍)。
这两个STS1(图3.E)和CHS1(图3.F)基因经硫胺素处理诱导,其动力学特征与朋友基因。的确,STS1而且CHS1mRNA转录物第一次在12 hpt达到峰值(分别为1548和3.72倍的表达),第二次在36 hpt达到峰值(分别为1641.5和4.715倍的表达)。随后,STS1而且CHS1基因表达逐渐下降,直到72 HPT(分别为188.14和1.06倍表达)。总的来说,这些结果清楚地证明了硫胺素诱导葡萄植物增强苯丙烷途径基因表达的能力。
硫胺素诱导二苯乙烯的产生
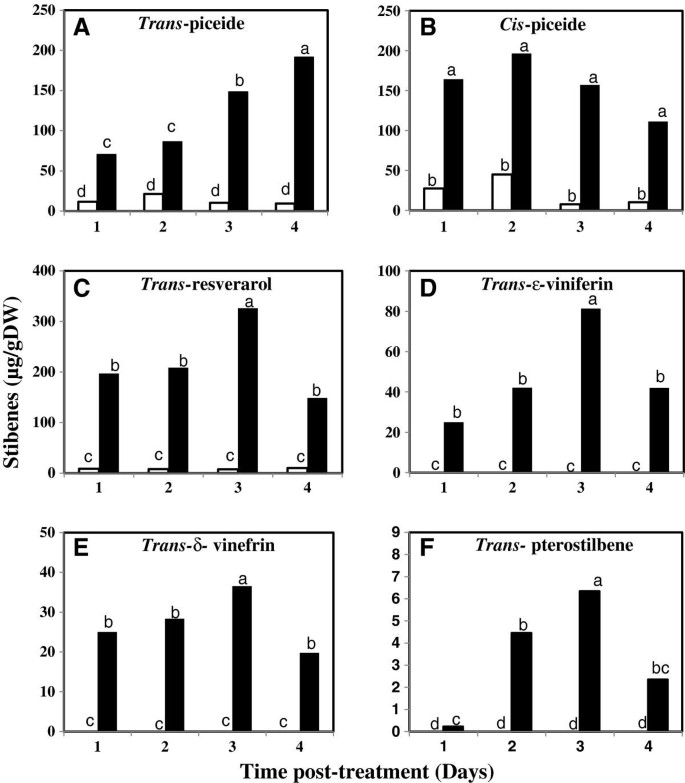
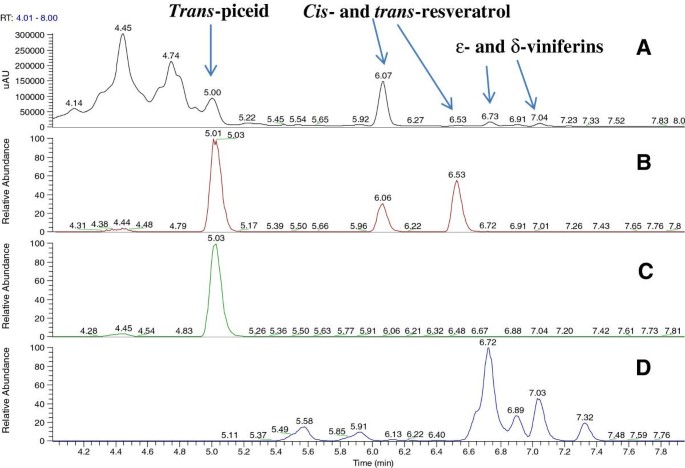
寻找两者之间的相关性STS1利用高效液相色谱- dad法测定处理后不同时间间隔内不同二苯乙烯类化合物(二苯乙烯类)的含量(图4)。用于HPLC-DAD分析的样品中不同二苯乙烯类化合物的身份也通过ULPC-DAD-MS得到确认(图5)。我们的结果表明,两者的含量反式-piceide(图4一)和独联体-piceide(图4B)在4个研究时间点,与水处理样品相比,经硫胺处理的植物显著升高。的反式-piceide含量随施硫胺时间间隔的增加而增加,在施硫胺后4 d达到最大值,为191.52 μg/g干重(DW)。然而,浓度最高的独联体硫胺处理植株在2 dpt时产生-白皮苷(196.52 μg/g DW)。相反,两者都较少反式- - -独联体在所有取样时间,水处理样品中均检测到-皮塞德。反式-白藜芦醇是硫胺处理后产生的量最多的二苯乙烯类化合物(图4C)。反式-白藜芦醇的诱导作用从1 dpt开始(197.6 μg/g DW),随着时间的推移逐渐增加,在3 dpt时达到最大值(326.23 μg/g DW),在4 dpt时下降(148.76 μg/g DW)。只有非常少的数量反式-白藜芦醇在水处理植物的不同采样时间点被检测到。
反式- - - - - -ε-viniferin(图4D)和反式- - - - - -δ-viniferin(图4E)仅在硫胺处理过的植物中检测到。这两个反式-ε和反式-δ-viniferins在硫胺处理的植物中从1dpt开始生产;此后,其含量逐渐增加,在3dpt内达到最大值(分别为81.34 μg/g DW和36.56 μg/g DW),在4dpt时下降(分别为42.03 μg/g DW和19.78 μg/g DW)。反式-翼苯乙烯,两者都是反式-ε和反式-δ-viniferins在所有采样时间点均未在水处理植物中检测到。相比之下,在硫胺处理过的植物中,它显著地产生(图4F)从1分开始。随着时间的推移,其含量逐渐增加,在3dpt时达到最大值(6.34 μg/g DW),在4dpt时下降(2.35 μg/g DW)。
硫胺素处理引起酚类和木质素的积累
采用组织化学方法研究了硫胺素对木质素和苯酚合成的影响。用水或硫胺素处理葡萄藤,每隔1 dpt收割叶片。为了检测木质素,从水和硫胺处理过的植物叶片中打孔,用间苯三酚染色,并在光学显微镜下检查。叶盘呈红色表明木质素的存在。在硫胺处理过的植物叶片中观察到阳性反应(红色)(图5A, C),表明在实质组织中木质素合成有明显的诱导作用,而在水处理植物的叶盘中(图5B),我们没有观察到任何木质素积累。
为了检测酚类物质,用低温切片机获得了10 μm厚的叶片切片,并在荧光显微镜下进行了观察。在紫外线下观察到酚类物质的生成为蓝色。经硫胺处理的植物叶片呈强烈的蓝色,表明酚类物质的积累(图5D, F),不同于水处理植物的叶盘(图5E)。
硫胺素诱导黄酮类化合物的诱导效果显著
我们的分子研究结果表明,硫胺素上调表达CHS1该基因负责葡萄类黄酮的生物合成。因此,我们研究了硫胺素激活该基因是否与类黄酮的积累相关。黄酮类化合物的亚细胞检测由Wilson 's Reagent染色完成。此外,我们还评估了槲皮素3的含量OHPLC-DAD测定不同时间点葡萄糖苷(一种黄酮醇)含量。我们的结果(图6H, I)表明,硫胺素处理诱导黄酮类化合物的显著积累,威尔逊试剂染色后出现强烈的黄色,而这种黄色的强度在水处理的植物中明显不明显(图6F)。
槲皮素含量3-O-葡萄糖苷黄酮醇受硫胺素处理的葡萄植株影响不显著(图7)。考虑到植物中基础类黄酮结构(黄酮、二氢黄酮醇、黄酮、异黄酮、异黄酮、翼果类)的多样性,硫胺素会诱导产生其他特异性代谢产物。
硫胺素通过诱导特定的酚类化合物(包括一种caftaric acid)来增强葡萄植物的抗氧化潜能
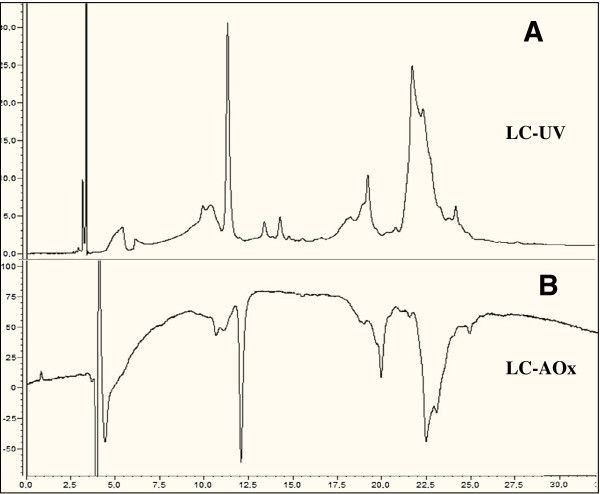
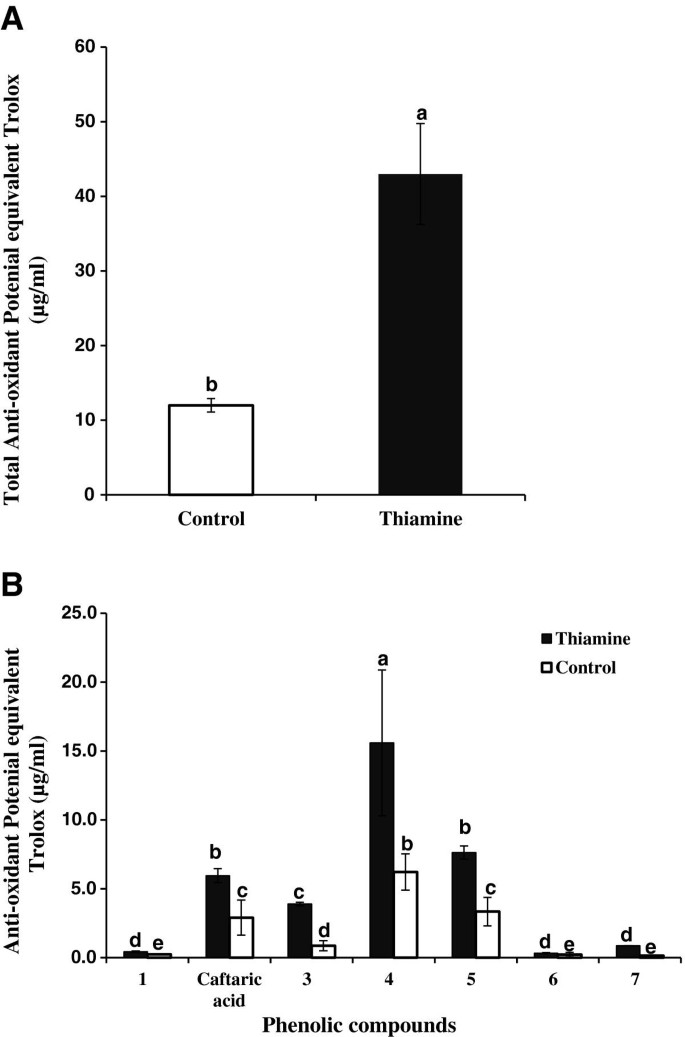
数字8显示了硫胺处理葡萄植物甲醇提取物中分离出的酚类化合物的COADS色谱图及其相应的抗氧化活性。图中上半部分的结果是在254 nm处用紫外直接检测得到的,下半部分的结果是柱后反应后在412 nm处用可见光检测得到的。对每个处理,测定COADS色谱图,并对峰面积求和,用于表示总抗氧化活性,用3次测定的平均值±SD表示(图2)8A).总抗氧化活性结果以Trolox当量(μg/ml)表示。硫胺处理植株的总抗氧化潜能为43±6.8 μg/ml Trolox当量,而水处理植株的总抗氧化潜能为12±0.9 μg/ml,表明硫胺处理植株的总抗氧化潜能是对照植物的3.58倍(图)9A).最大的抗氧化贡献仅来自4种化合物,它们占硫胺处理植物抗氧化潜力的97%。其中,我们鉴定出一种属于羟基肉桂酸家族的caftaric acid,其本身约占总抗氧化潜力的20%(图9B).鉴别其他未知酚类化合物的工作正在进行中。
二苯乙烯可能在P.viticola硫胺素限制
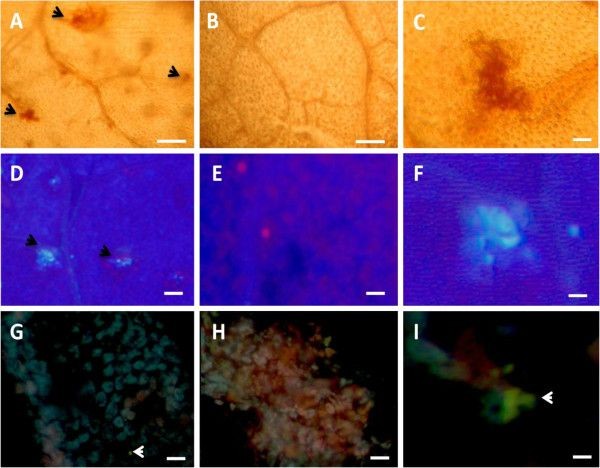
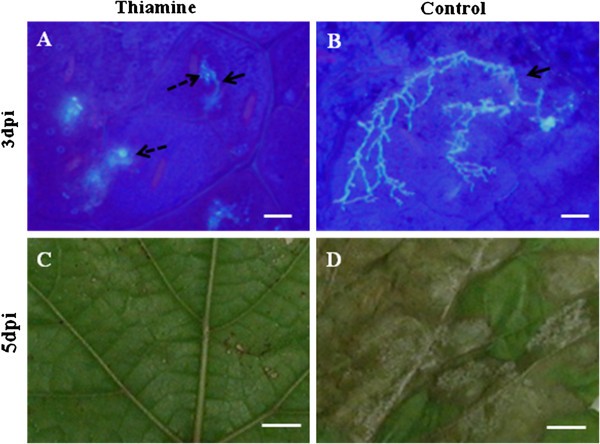
据报道,二苯乙烯具有生物杀灭作用P.viticola游动在体外[16].在这里,我们评估了它们对葡萄植物中由硫胺素诱导的病原体菌丝生长的影响(在活的有机体内)。利用荧光显微镜(紫外光下)在叶面组织中检测到二苯乙烯和病原体菌丝体的积累。结果(图10),清楚显示有改变(图10A),叶带内未分枝的病原体菌丝,显示出强烈的蓝色,与硫胺处理的植物叶片中二苯乙烯的积累相对应。相比之下,在经过水处理的植物中,我们观察到叶子叶肉中菌丝发育正常且广泛,我们没有观察到任何二苯乙烯的积累(图10B).因此,在硫胺处理过的植物叶片中,改变的、不分枝的菌丝体和二苯乙烯的产生同时存在,表明这种植物抗毒素家族可能对P.viticola通过抑制菌丝在叶叶肉中的扩散来限制。此外,硫胺素的直接作用也可能在病原菌菌丝的改变中发挥作用。在接种后5天,我们观察到严重的感染P.viticola在水处理过的植物的叶子中,白色孢子症状的发展证明(图10D),而在硫胺处理的样品中,我们只观察到与超敏反应相关的细胞死亡相对应的坏死区的发展(图10C)。
二苯乙烯类可能在限制的作用P.viticola通过硫胺素处理发展。葡萄简历。用水或硫胺素处理霞多丽植株24 h后,进行喷雾接种P.viticola孢子囊悬浮液(104孢子囊/毫升)。(一个)二苯乙烯类对应的自发荧光下存在荧光物质(间断箭头)[6],围绕不分枝和退化的菌丝(中断箭头)P.viticola在经硫胺处理的植物叶片的叶肉中。(B)无二苯乙烯类积累和广泛分支P.viticola水处理植物叶片叶肉细胞间隙中的菌丝。(C坏死区(HR)的形成和抑制P.viticola硫胺处理植物的产孢。(D)发展P.viticola水处理植物的产孢症状。Bars = 40 μM for (A、B)和1厘米(C, D)。
讨论
主要由植物抗毒素产生V.酿酒用葡萄病原体感染期间的品种有白藜芦醇及其衍生物、白皮苷(糖基化形式)、δ-葡萄素和ε-葡萄素(氧化二聚体)以及翼苯乙烯(甲基化衍生物)[21].在我们的实验中,硫胺素处理导致诱导反式- - -独联体-piceide形成,每个化合物分别在4和2 dpt内获得最高水平。硫胺素的处理也诱导其积累反式-白藜芦醇,在3 dpt内观察到最高水平。在敏感葡萄品种中,白藜芦醇被大量合成,但它很快被糖基化成无毒的化合物白塞醚。这可以解释两者的高浓度独联体- - -反式硫胺处理过的植物,这是由于高浓度的反式白藜芦醇。此外,硫胺素引起了重要的二苯基形式的积累,葡萄素,这是积极对抗P.viticola;δ-维尼弗林的毒性是ε-维尼弗林的5倍[16].ε-和δ-葡萄素均在3 dpt时达到最高水平。ε-和δ-葡萄素在水处理植物中均不存在。硫胺处理的植物在3dpt时白藜芦醇合成的增加为viniferins的合成提供了一个重要的池,也发生在3dpt。此外,硫胺素处理诱导翼苯乙烯合成,在3 dpt时也观察到最大诱导水平。
研究发现,在高胆固醇血症的仓鼠中,紫檀二苯乙烯作为一种降脂/脂蛋白剂非常有效,这可能是因为,与贝特类药物一样,紫檀二苯乙烯被证明是一种过氧化物酶体增殖物激活受体激动剂[22].此外,紫檀二苯乙烯具有与白藜芦醇类似的抗氧化和抗癌特性[23].在小鼠乳腺器官培养模型中,发现紫檀二苯乙烯在预防致癌性肿瘤前病变方面非常有效[24],对大鼠结肠癌有预防作用[25].
黄酮醇是苯丙类代谢物,大部分由对香豆油酰辅酶a和丙二酰辅酶a合成,它们的前体与木质素生物合成途径相同[26].然而,一些罕见的黄酮类化合物是由底物如肉桂酸或二氢香豆酸的辅酶a酯合成的。类黄酮也有助于抵抗病原体。在我们的实验中,硫胺素诱导黄酮类化合物的积累。与之相反,所有易感葡萄品种在接种病原体后均不存在这种代谢反应[27].许多属于黄酮和黄酮类的特殊类黄酮已被证明对水果和蔬菜储存期间常见的真菌病原体有活性。曲霉属真菌sp。葡萄孢菌而且尖孢镰刀菌[8].黄酮类化合物也被报道参与限制P.viticola中间抗性种的生长葡萄属rotundifolia而且葡萄属rupestris[28].
植物抗毒素的一部分具有抗氧化剂的功能,从而有助于植物抵抗病原体[29].在我们的研究中,硫胺素的应用诱导了具有抗氧化特性的特定酚类化合物的显著积累,这导致了COADS分析所证明的葡萄植物的总抗氧化潜力的增加。先前的研究表明,在耐药植物中,在苯丙烷途径的关键酶(PAL和CHS)活性增加后,细胞通常通过增加感染部位已有的抗真菌酚的水平来做出反应[30.].细胞壁材料中的酚酯化作用通常被认为是增加对真菌水解酶的抗性,以及防止真菌渗透的物理屏障[11].酚类物质提供抗病能力的第一个例子是洋葱鳞片积累了足够数量的儿茶酚(I)和原儿茶酸(II)来预防洋葱污迹病,炭疽菌circinans.抗性洋葱品种的彩色外洋葱鳞片含有足够的这两种酚,以减少孢子萌发C.circinans到2%以下,而在缺乏这些化合物的敏感品种中,发芽率超过90% [30.].足够水平的绿原酸(III)解释了马铃薯块茎的抗性5种[30.].据报道,酚类物质也涉及限制P.viticola中间抗性种的生长V.rotundifolia而且V.rupestris[28].相比之下,在易感葡萄品种中,接种病原体后不存在这种代谢反应[27].此外,据报道,酚类物质的积累与葡萄的IR机制有关,如β-1,3-葡聚糖-和壳聚糖-IRP.viticola[4,7].
另一方面,酚类物质含量的增加可能为多酚氧化酶(PPO)和/或过氧化物酶(POD)催化的氧化反应提供了充足的底物,这些反应通过消耗氧气和产生真菌性醌类物质,使培养基不利于病原体的进一步发展[8].凡西等人。[31]已经报道过氧化物酶活性使用特定的酚类化合物作为底物导致木质素的形成。
我们的研究揭示了硫胺处理葡萄藤中酚类物质和木质素的增加。据报道,这些化合物在限制真菌扩展方面发挥了关键作用[32].此外,Cohen等人。[33)假设木质素包裹细胞的甜瓜吸器侵入Pseudoperenospora cubensis通过阻断养分流入和流出细胞,防止真菌生长和诱导宿主细胞死亡。综上所述,这些发现表明酚类物质和木质素都可能在硫胺- ir反应中发挥作用P.viticola的小道消息。
之前(19],我们报道了硫胺素处理与病原接种之间间隔3天是最大抗性的最佳时间P.viticola.在目前的工作中,我们发现硫胺素处理对特定二苯乙烯(ε-和δ-viniferin和翼苯乙烯)的最大诱导也发生在3 dpt。因此,这些结果可能表明二苯乙烯积累与IR to之间密切相关P.viticola通过硫胺素治疗。此外,我们的显微观察清楚地证明了改变的,不分枝的伴随存在P.viticola硫胺处理植物中菌丝体和二苯乙烯的积累。总的来说,这些结果表明二苯乙烯在硫胺ir中可能的贡献P.viticola的小道消息。
结论
综上所述,本文的研究结果强调了苯丙基代谢通路在硫胺- ir代谢中的作用P.viticola的小道消息。事实上,硫胺素的应用上调了苯丙烷途径基因的表达,并诱导植物积累特定的二苯乙烯,如ε-和δ-长春花素和紫檀二苯乙烯,否则植物中不存在这些。此外,硫胺素诱导酚类物质、木质素和类黄酮的积累,这些都是抗性的标志P.viticola在中等抗性葡萄品种中。由于这些分子和细胞的变化,葡萄植株的抗氧化潜力增强,这可能为硫胺素抑制霜霉病提供了额外的机制。此外,我们还发现在硫胺处理过的植物叶片叶肉中同时存在植物抗毒素衍生的二苯乙烯和退化的病原菌丝体结构,这表明二苯乙烯可能参与了硫胺- ir的作用P.viticola的小道消息。因此,我们认为,利用硫胺素诱导苯丙类途径来源的植物抗菌素对开发除化学杀菌剂外的葡萄园霜霉病防治策略可能具有重要价值。此外,这一发现将打开一个大的社区的大门体外培养学家,他们广泛研究了植物培养物用于工业生产二级化合物(主要是制药和染料)的可能用途。
方法
植物材料和生长条件
葡萄“霞多丽”植株是从草本扦插中获得的。它们被种植在含有泥炭和珍珠岩混合物的罐子里(4:1,v/v)。在受控的温室条件下(24°C,光照16小时,暗光照8小时,RH 70%)种植,直到生长出11片叶子。每2天用营养液(1克/升)给植物浇水(Plant Prod 15-10-30,法国)。
致病源
霜霉孢子囊(34],在上面繁殖V.酿酒用葡萄简历。霞多丽脱落的叶子保存在密封的培养皿中,放在潮湿的Whatman 3MM纸上。在叶片背面喷洒新鲜收集的孢子囊,重悬于水中,浓度为5 × 104孢子囊/毫升。接种后的叶片置于20°C和100% RH的黑暗生长室中24小时,然后在16 h的光照下,8 h的黑暗光周期下,70% RH的光照下,6天。剂的P.viticola用蒸馏水清洗带有新鲜孢子囊病变的葡萄叶的下部,制备孢子囊。然后将孢子囊悬浮液调整到浓度为104光镜下血球仪计数后孢子囊/ml。
治疗
用压缩空气手动喷雾器在葡萄植株的上下叶表面分别喷洒30 mM硫胺素或水(对照),直至流出。处理后的植株在25°C的生长室中,光照16 h,暗光照8 h, RH 70%。
病原接种程序及发病率的确定
在温室、对照条件下生长的葡萄植株,用水(对照)或30 mM硫胺素处理,叶片背面接种孢子囊悬浮液,接种量为5 × 104孢子囊/毫升使用压缩空气手动喷雾器装置。接种后的植株在80% RH和20℃的黑暗条件下孵育过夜,然后在24℃、光照16 h和暗光照8 h、70% RH的受控条件下生长室中保存。在5 dpi时,将植物在80% RH和20°C的黑暗环境中培养过夜,使霜霉病产孢,并根据出现坏死、油斑和产孢症状的植物的比例评估疾病发病率[20.].每个处理取6株,试验重复3次。
RNA提取与逆转录(RT)
根据制造商的说明,使用RNeasy植物迷你试剂盒(Qiagen, Germany)从葡萄植物叶片中分离总RNA,并使用Nanodrop nt -1000分光光度计(Thermo Scientific, Waltham, MA)进行定量。残留的基因组DNA通过使用RNase-Free DNase set (Qiagen)进行柱上DNase I消化去除。以总RNA (500 ng)为模板,使用供应商推荐的SuperScript II逆转录酶(Invitrogen, Carlsbad, CA)和oligodT-18进行RT。
实时定量聚合酶链反应(RT q-PCR)
苯丙烷通路基因的表达模式(表1)在硫胺处理后的霞多丽植株中测定。采用绝对qPCR SYBR Green Mix (Eurogentec, Belgium)在96孔板中,在含有1× SYBR Green Mix(含)的缓冲液中,以25 μl的体积进行RT q-PCRTaq聚合酶,dNTP和SYBR绿色染料),100 nM引物和5倍稀释的逆转录RNA。PCR条件为95°C下5分钟,然后进行40个循环,每个循环包括一个变性步骤(95°C下20秒),一个杂交步骤(55°C下30秒)和一个退火步骤(60°C下1分钟)。为了检查PCR产物的特异性,分析了每个数据点的熔化曲线。在没有模板的对照中检查引物二聚体形成的缺失。以泛素基因(Ubq)为内对照,测定转录水平的动力学。Ubq(接入号tc32075)引物序列为5条′GTGGTATTATTGAGCCATCCTT3′正向反应和5′AACCTCCAATCCAGTCATCTAC3′反向。每个时间点被确定为3个独立实验的平均值。用公式计算相对基因表达量,折叠诱导= 2——ΔΔCt,其中ΔΔCT= (CTGI[未知样本]- CTGI[参考样品])- (CTUbq[未知样本]- CTUbq[参考样本]),先前由Trouvelot等人报道。[4].GI是我们感兴趣的基因。参考样本是选择代表感兴趣基因的1×表达的水处理样本。
HPLC-DAD和UPLC-MS分析所用的化学溶剂及其参考文献
HPLC-MS级乙腈和甲酸由赛默飞世尔科技公司提供;水由Millipore水净化系统(Millipore, Bedford, MA)提供。参考化合物包括反式白藜芦醇,反式-piceide,反式-紫檀苯乙烯和ε-viniferins由瑞士Changins的R. Pezet购买或提供。与峰恒等式相关反式白藜芦醇,反式-piceide,反式-紫檀二苯乙烯通过比较保留时间、紫外光谱和真实标准品的精确质谱进行了验证。
二苯乙烯类化合物的HPLC-DAD定量
在温室条件下生长的葡萄扦插用水(对照)或硫胺素(30 mM)处理,从顶端开始的第4和第5个位置的叶子在处理后的不同时间间隔收割,称重,并用于甲醇提取。根据Poutaraud等的方法进行二苯乙烯提取和HPLC-DAD分析[35].简单地说,在160 mg (FW)叶片组织中加入800 μl甲醇,在60°C下用加热块孵育45 min,然后以12000 rpm的速度离心两次10 min。将20微升回收的上清液注入HPLC-DAD系统。HPLC系统包括一个1100四元泵(惠普,安捷伦技术,Massy,法国),配备了一个1100光电二极管阵列多波长探测器(惠普),一个1100真空脱气器(惠普),和一个234自动注入模块(Gilson, Villiers-le-Bel,法国)。分析在Lichrospher端盖RP-18色谱柱(5 μm, 250 mm × 4.6 mm, Merck, Lyon, France)上进行,温度为20℃。在200 ~ 400 nm之间测量吸收,在307 nm处记录色谱图。通过比较二苯乙烯类化合物的保留时间和紫外吸收光谱,对其进行了鉴定。
UHPLC-MS条件
通过HPLC-DAD分析的叶片甲醇提取物中二苯乙烯的每个峰的身份是使用超高性能液相色谱系统(UHPLC, Ultimate 3000, Dionex, Thermofisher Scientific,加州圣何塞)确认的,该系统配备了一个二元泵,一个在线脱气器,一个恒温自动进样器,一个恒温控制柱室和一个二极管阵列检测器。色谱柱为Agilent RRHD C18 SB柱(150 × 2.1 mm, 2.7 μm粒径),温度为20℃。流动相为0.1%甲酸乙腈(溶剂A)和0.1%甲酸水(溶剂B),流速为0.25 ml/min。梯度洗脱程序为:0 ~ 1 min, 80% B;1-11 min, 80-0% B;11 ~ 12 min, 0% b,每个提取物进样量为1 μl。在190 ~ 400 nm之间测量了吸收,在280 ~ 307 nm记录了色谱图。液相色谱系统与Exactive Orbitrap质谱仪(Thermo Fischer Scientific公司)耦合。
质谱计由一个负模式的电喷雾电离(ESI)源组成。离子转移毛细管温度为300℃,针压为−2500 V。氮气鞘气体和辅助气体雾化分别维持在40和6个任意单位。仪器在5万分辨率下工作,光谱采集在m/z质量范围100 - 1000a.m.u内。仪器操作程序为ExactiveTune,数据处理软件为XcaliburQual。
系统使用Thermo Fischer Scientific公司的校准混合物进行外部校准,扫描范围为m/z 100 - 2000a.m.u。使用MSCAL6-1EA每7天进行一次校准。这样的校准给出了至少2ppm的精度。通过比较二苯乙烯类化合物的保留时间和质谱,并获得其伪分子离子峰(M-H),建立了精确的分子式,证实了二苯乙烯类化合物的鉴定。
COADS法测定总抗氧化势和酚类化合物
利用在线高效液相色谱柱后反应法筛选葡萄植物提取物中单个酚类化合物的自由基清除能力[36].该检测方法是基于自由基清除化合物减少绿-蓝色2,2的能力′-azinobis-3-乙基苯并噻唑啉-6-磺酸(ABTS[*][+])自由基阳离子转化为无色形式。这导致在412 nm处吸光度下降。测定每种处理的COADS色谱图,并将峰面积相加,用于表示总抗氧化活性。HPLC系统(Ultimate 3000, Dionex, ThermoScientific, Gometz le Châtel,法国)由一个DGP 3600泵,一个WPS-3000T自动进样器,一个3000二极管阵列检测器和一个3100可变波长检测器组成。使用长3米,内径0.25米的PEEK反应线圈。数据采集和处理采用Dionex Chromeleon 6.8数据系统。
采用Hypersil BDS C18高效液相色谱柱(5 μm, 250 × 4.6 mm i.d, ThermoScientific, Gometz-le-Châtel, France)在室温下进行分离。流动相,以1ml /min的速度输送,由含0.1%甲酸(洗脱液a)和乙腈(洗脱液B)的梯度混合物组成。使用以下梯度:0-25分钟,3-25% B;25-29 min, 25% B;29-37 min, 25-30% B;37-47 min, 30% B;47-57 min, 30-65% B;57-67 min, 65% B. (ABTS[*][+])溶液以0.5 ml/min的速度给药。柱后与(ABTS[*][+])反应后,在280 nm和412 nm分别检测酚类化合物的抗氧化活性。结果以水溶性合成维生素E衍生物6-羟基-2,5,7,8-四甲基铬酸-2-羧酸Trolox当量为标准抗氧化剂,表达量为μg/ml。
黄酮类化合物、酚类和木质素的组织化学检测
植物叶片经水处理(对照)或硫胺素处理(30 mM),使用低温恒温切片机(徕卡2800)在-20°C下制备叶片切片(10 μm厚)。为了检测黄酮类化合物,切片在100ml无水乙醇中柠檬酸:硼酸(5/5,w/w)组成的Wilson试剂中浸泡15分钟,装入75% (v/v)的甘油中,在紫外线(BP 340-380 nm, LP 425 nm)下使用epifluorescence显微镜(NIKON, F 1200)检查。黄色荧光表明黄酮类化合物的存在[27].
为了检测酚类物质,将叶片切片放在玻片上,用玻片覆盖,并在荧光显微镜(尼康,F 1200)的帮助下进行检查(激发滤波器390-420 nm,发射滤波器425-450 nm)。酚类化合物在紫外光照射下发出蓝色荧光[28].为了观察木质素,从对照和硫胺处理过的植物叶片中穿孔叶盘,在95%乙醇中煮沸10分钟,然后用间三酚(10克在95毫升无水乙醇中)处理3分钟。叶盘在25% HCl中洗涤,装在甘油(75%)中,并在光学显微镜下检查[37].
显微评估P.viticola结构
为了观察P.viticola将生长在葡萄叶组织中的菌丝体、经硫胺素或水处理和接种的叶片(直径1.4 cm)在100℃1 M KOH中孵育15分钟,在水中洗涤3次15分钟,在0.067 M K中用0.05% (w/v)苯胺蓝染色2根据Diez-Navajaz等人的方法,在紫外光(激发340 nm,发射380 nm,停止滤光器LP 430 nm)下,用epifluorescence显微镜(NIKON, F 1200)观察HPO4 (pH 9-9.5) 15 min。[34].苯胺蓝与β-1,3-葡聚糖反应生成P.viticola菌丝在这些条件下可见为蓝色荧光。每个处理从6株植物中随机分离20个叶盘进行显微观察,整个实验重复3次。
统计分析
使用Statistica 7.1软件程序(StatSoft, Tulsa, OK, USA)对数据进行方差分析。几乎用Tukey’s HSD检验来判断平均值之间差异的显著性(P≤0.05)。
缩写
- abt [*] [+]:
-
2、2′-azinobis (3-ethylbenzothiazoline-6-sulfonic酸)
- COADS:
-
色谱在线抗氧化检测系统
- DPT:
-
天后处理
- DPI:
-
天post-inoculation
- 成:
-
小时后处理
- 红外光谱:
-
诱导阻力
- Trolox:
-
6-hydroxy-2 5 7 8-tetramethylchroman-2-carboxylic酸。
参考文献
- 1.
Kortekamp A:接种寄主和非寄主病原体后葡萄叶片防御相关基因的表达分析。植物化学学报,2006,44:58-67。10.1016 / j.plaphy.2006.01.008。
- 2.
陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰,陈文杰。环境科学与技术,2007,29(3):344 - 344。10.1128 / AEM.00507-07。
- 3.
Sticher L, Mauch-Mani B, Metraux JP:系统性获得性耐药。中国植物学报,1997,34(3):344 - 344。10.1146 / annurev.phyto.35.1.235。
- 4.
Trouvelot S, Varnier AL, Allegre M, Mercier L, Baillieuil F, Arnould C, Gianinazzi-Pearson V, Klarzynski O, Joubert JM, Pugin A, Daire X: β -1,3硫酸葡聚糖诱导葡萄抗性霜霉通过启动防御反应,包括hr样细胞死亡。植物与微生物相互作用,2008,21:232-243。10.1094 / mpmi - 21 - 2 - 0232。
- 5.
Hamiduzzaman MM, Jakab G, Barnavon L, Neuhaus JM, mauh - mani B: β-氨基丁酸诱导葡萄对霜霉病的抗性通过增强胼胝质形成和茉莉酸信号通路起作用。植物微生物相互作用,2005,18:819-829。10.1094 / mpmi - 18 - 0819。
- 6.
Slaughter A, Hamiduzzaman MM, Gindro K, Neuhaus JM, Mauch-Mani B: β -氨基丁酸诱导葡萄对霜霉病的抗性:涉及紫檀二苯乙烯。中国植物病理学杂志,2008,22(1):1 - 5。10.1007 / s10658 - 008 - 9285 - 2。
- 7.
Aziz A, Trotel-Aziz P, Dhuicq L, Jeandet P, Couderchet M, Vernet G:壳聚糖寡聚物和硫酸铜诱导葡萄防御反应和对灰霉病和霜霉病的抗性植物病理学杂志,2006,26(3):344 - 344。10.1094 /发朵- 96 - 1188。
- 8.
Lattanzio V, Lattanzio VMT, Cardinali A:酚类物质在植物对真菌病原体和昆虫抗性机制中的作用。植物化学,2006,37:23-67。
- 9.
Y清明,P先辉,K卫宝,Y宏,S一丹,李震,Z亚楠,Y玉玲,兰丹,L国安:大麦麦芽提取物对各种氧化应激的体外和体内抗氧化活性食品化学,2010,18:84-89。10.1016 / j.foodchem.2009.04.094。
- 10.
单宁酸对小麦茎锈病易感叶片的抑菌特性。植物化学学报,2001,29(3):344 - 344。10.1016 / 0031 - 9422 (91) 83426 - l。
- 11.
Stadnik MJ, Buchenauer H:苯丙氨酸解氨酶的抑制抑制苯并噻二唑诱导的小麦对小麦青霉病抗性。tritici。中国生物医学工程学报,2000,29(4):344 - 344。10.1006 / pmpp.2000.0276。
- 12.
Ahuja I, Kissen R, Bones AM:植物抗毒素防御病原体。植物科学进展,2012,17:73-90。10.1016 / j.tplants.2011.11.002。
- 13.
Jeandet P, Douillet-Breuil AC, Bressis R, Debord S, Spaghi M, Adrian M:植物抗毒素的生物合成、转基因植物抗毒素基因表达、抗真菌活性和代谢。食品化学学报,2002,30(4):349 - 349。10.1021 / jf011429s。
- 14.
李维泽,李志强,陈志强,陈志强,陈志强,等,Martínez-Zapater J:甲基茉莉酸盐和环糊精对二苯乙烯合成途径基因表达和白藜芦醇产量的影响。BMC Res Not 2008, 1: 132。10.1186 / 1756-0500-1-132。
- 15.
Pezet R, Perret C, Jean-Denis JB, Tabacchi R, Gindro K, Viret O: δ- vinifin,一种白藜芦醇脱氢二聚体:由葡萄叶合成的主要二苯乙烯之一。中国农业科学,2003,29(4):489 - 497。10.1021 / jf030227o。
- 16.
白藜芦醇,长春花素和紫檀二苯乙烯对白藜芦醇的影响霜霉动物孢子的流动性和疾病发展。葡萄,2004,43:145-148。
- 17.
安叶平,金松,李永华:维生素B1是植物抗病的激活剂。植物科学学报,2004,29(3):344 - 344。10.1104 / pp.104.058693。
- 18.
安晓平,李玉华,徐秀生:维生素b1诱导的拟南芥启动依赖于过氧化氢和NPR1基因。植物科学学报,2007,29(3):344 - 344。
- 19.
杨晓明,王晓明,王晓明,王晓明,杨晓明,杨晓明。硫胺素诱导抗性的研究进展霜霉并引发宿主防御反应,包括hr样细胞死亡。植物化学学报,2012,29(3):344 - 344。
- 20.
昂格尔S,布埃切C,博索S,卡塞梅耶HH:两种不同的殖民过程葡萄属基因型的霜霉指示相容和不相容的宿主-病原体相互作用。中国植物学报,2007,27(3):366 - 366。10.1094 /发朵- 97 7 - 0780。
- 21.
Pezet R, Gindro K, Viret O, Spring JL:白藜芦醇的糖基化和氧化二聚化分别与葡萄品种对霜霉病的敏感性和抗性有关。中国生物医学工程学报,2004,29(3):344 - 344。10.1016 / j.pmpp.2005.03.002。
- 22.
Rimando AM, Nagmani R, Feller DR, Yokoyama W:翼芪,一种新的过氧化物酶体增殖物激活受体α亚型激动剂,降低高胆固醇血症仓鼠血浆脂蛋白和胆固醇。中国农业科学,2005,29(3):349 - 349。10.1021 / jf0580364。
- 23.
张敏,蔡l, Udeani GO, Slowin KV, Thomas CV, Beecher CWWB, Fong HHS, Farnsworth NR, Kinghorn AD, Mehta RG:葡萄天然产物白藜芦醇的化学预防癌症活性。科学通报,1997,27(3):344 - 344。10.1126 / science.275.5297.218。
- 24.
Rimando AM, Kalt W, Magee JB, Dewey J, Ballington JR:越桔中的白藜芦醇,紫檀二苯乙烯和白藜芦醇。中国农业科学,2004,29(4):457 - 457。10.1021 / jf040095e。
- 25.
Suh N, Paul S, Hao X, Simi B, Xiao H, Rimando AM, Reddy BS:蓝莓的活性成分Pterostilbene抑制氮氧甲烷诱导大鼠结肠癌模型中异常隐窝灶的形成。中国癌症杂志,2007,13:357 - 357。10.1158 / 1078 - 0432. - ccr - 06 - 1528。
- 26.
类黄酮的进化:一种酶的方法。植物科学学报,1997,26(3):366 - 366。10.1104 / pp.96.3.680。
- 27.
戴春华,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明:3种葡萄相互作用的组织化学研究,葡萄,V.rupestris而且V.rotundifolia还有绒毛真菌霜霉.中国生物医学工程学报,2004,26(3):357 - 357。10.1006 / pmpp.1995.1014。
- 28.
戴洪华,Andray C, cosonlm, Boubals D:多酚与葡萄抗性(葡萄属.至霜霉病(霜霉)。园艺学报,1994,29(3):366 - 366。
- 29.
Treutter D:通过植物化学耕作和育种来管理作物植物中的苯酚含量。愿景和约束。中华分子生物学杂志,2010,29(3):457 - 457。10.3390 / ijms11030807。
- 30.
Hammerschmidt R:植物抗毒素积累:反应或防御。中国生物医学工程学报,2003,29(3):344 - 344。10.1016 / s0885 - 5765(03) 00080 - 8。
- 31.
万斯CP,柯克TK,舍伍德RT:木质化作为一种抗病机制。植物学报,2000,18(4):379 - 379。10.1146 / annurev.py.18.090180.001355。
- 32.
罗伯森B:内聚半乳糖醛酸酶枝孢属法测定诱导黄瓜下胚轴木质化。植物化学学报,1987,31:361-374。10.1016 / 0885 - 5765(87) 90050 - 6。
- 33.
李志刚,张志刚,张志刚,张志刚甜瓜中对霜霉病敏感和抗性基因型的冰孢假孢子菌.植物化学学报,1998,34:27-44。
- 34.
Diez-Navajas AM, Greif C, Poutaraud A, Merdinoglu D:两种简化荧光染色技术观察卵菌感染结构霜霉在葡萄叶组织中。光电子学报,2007,29(3):344 - 344。10.1016 / j.micron.2006.09.009。
- 35.
Poutaraud A, Latouche G, Martins S, Meyer S, Merdinoglu D, Cerovic ZG:葡萄叶片中二苯乙烯含量的局部快速测定在活的有机体内荧光测定术。中国农学通报,2007,29(3):349 - 349。10.1021 / jf070348e。
- 36.
Leitao C, Marchioni E, Bergaentzl M, Zhao M, Didierjean L, Taidi B, Ennahar S:工艺步骤对啤酒酚含量和抗氧化活性的影响。食品化学学报,2011,59:1249-1255。10.1021 / jf104094c。
- 37.
戴洪华,陈志明,陈志伟,陈志伟,陈志伟,陈志伟:葡萄愈伤组织对霜霉病抗性的影响(霜霉)。中华病毒学杂志,2001,30(4):344 - 344。
致谢
作者非常感谢Julie Chong博士和Pr. Christophe Bertsch (Laboratoire Vigne,生物技术和环境,Université de hate - alsace de Colmar, France)提供的植物材料。这项工作在“法国科尔马国家农学研究所”进行,并得到了突尼斯高等教育和科学研究部的资助。
作者信息
从属关系
相应的作者
额外的信息
相互竞争的利益
作者宣称他们之间没有利益冲突。
作者的贡献
HB构思研究,对葡萄植株进行培养、处理和接种,评估病害严重程度,Real Time q-PCR分析防御相关基因表达,组织化学分析细胞防御反应,评估P.viticola对二苯乙烯类化合物的高效液相色谱分析有帮助,并撰写了手稿。AP实现了二苯乙烯类化合物和槲皮素黄酮醇的HPLC-DAD分析,并协助撰写稿件。M-AW参与了数据的统计分析,并帮助起草了稿件。CC、DS和CM实现了对葡萄总抗氧化潜力的HPLC-AOx分析,并鉴定了涉及的酚类化合物。RB实现了ULPC-MS分析,以确认二苯乙烯类化合物的身份,并帮助撰写了手稿。AM和IS-G协调研究项目并监督工作。所有作者都阅读并批准了最终的手稿。
权利和权限
本文由BioMed Central Ltd授权发布。这是一篇开放获取文章,根据创作共用属性许可协议(http://creativecommons.org/licenses/by/2.0),允许在任何媒介上不受限制地使用、传播和复制,前提是正确地引用原始作品。
关于本文
引用本文
Boubakri, H., Poutaraud, A., Wahab, ma .et al。硫胺素调节苯丙类途径的代谢,导致增强抵抗霜霉的小道消息。BMC植物生物学13,31日(2013年)。https://doi.org/10.1186/1471-2229-13-31
收到了:
接受:
发表:
关键字
- 硫胺素
- 霜霉
- 对称二苯代乙烯
- 苯丙类途径基因
- 木质素
- 类黄酮
- 小道消息
- 诱导阻力
- 实时q-PCR
- 高效液相色谱法
- UPLC-MS