摘要
背景
的opaque2突变体可用于生产营养价值更高的玉米品种。然而,它改善蛋白质质量和创造软胚乳质地的确切机制尚不清楚。鉴于提高粮食作物营养品质的重要性,有必要更好地了解这些性状的生理基础。
结果
在这项研究中,我们结合了转录谱分析和蛋白质组学分析,以更好地了解哪些基因和蛋白质被改变了opaque2在W64A自交系中。这些分析表明,一些富含赖氨酸的蛋白质,如山梨醇脱氢酶和甘油醛-磷酸脱氢酶的积累在成熟籽粒中增加,可能对赖氨酸含量有很大的贡献opaque2胚乳。一些防御蛋白,如-葡萄糖苷酶聚集因子,被强烈下调,可能直接调控opaque2。突变体还改变了许多淀粉生物合成基因的表达,这与更高结晶的淀粉有关。
结论
这些研究结果为进一步提高高赖氨酸玉米品系的营养品质和农艺性能提供了特定的靶标基因,特别是那些基于赖氨酸的玉米品系opaque2突变。支链淀粉分支模式的改变opaque2淀粉有助于产生柔软的淀粉质胚乳。
背景
玉米是一种主要的粮食和饲料作物,由于对玉米的需求增加,预计未来几十年用于玉米种植的面积将显著增加[1].大部分玉米作物用于喂养牲畜,但在中美洲、非洲和亚洲的大部分地区,玉米是人类的主要粮食。为了最大限度地提高土地生产力,作物的营养质量应该是考虑的因素之一,其他因素还包括水和氮的利用效率、产量、抗虫害能力和作物生产力的其他决定因素[2].
玉米蛋白缺乏必需氨基酸赖氨酸和色氨酸,这限制了它对单胃动物的价值。因此,在过去的几十年里,人们一直在努力培育具有更高必需氨基酸含量的玉米品系。20世纪60年代,普渡大学的默茨和纳尔逊的研究小组发现了几种赖氨酸含量增加的突变体,opaque2(o2),floury2特别是,其必需氨基酸含量要高得多[3.,4].然而,这些突变导致软的、白垩质的胚乳表型不适合农艺生产,因为对昆虫和真菌害虫的易感性增加,产量下降[5,6].的O2基因被发现编码b-zip转录因子[7]调节胚乳中几种基因的表达,特别是编码22 kDa α-玉米溶蛋白储存蛋白的基因[8].α-醇溶蛋白合成的大量减少导致蛋白质体变小,数量减少,同时非醇溶蛋白胚乳蛋白也随之增加[3.].这些蛋白质积累的变化导致胚乳的赖氨酸和色氨酸含量几乎是野生型玉米的两倍[3.],这大大提高了对一夫一妻制动物的价值[9].因此,育种家开始反复选育o2高赖氨酸和硬胚乳的品系,称为优质蛋白玉米[10].
近年来,利用转基因技术培育玉米品系和优化氨基酸平衡已取得长足进展。11- - - - - -13]和通过标记辅助选择的传统育种方法[14,15].最成功的转基因策略是用RNA干扰(RNAi)方法特异性敲除玉米蛋白储存蛋白或赖氨酸分解代谢基因的表达[11- - - - - -13,16].减少缺乏赖氨酸的玉米蛋白的合成和其他蛋白质的补偿性增加显著改善了谷物的营养质量。平衡两者氨基酸含量的基本机制o2和RNAi尚不清楚,尽管它依赖于玉米蛋白储存蛋白合成的减少和非玉米蛋白含量的代偿性增加[17].一般而言,相对于野生型籽粒,总蛋白质含量仅略有降低[12,17,18],通过RNAi敲除高蛋白系和低蛋白系的19-和22-kDa α-zeins仅能较亲本水平轻微改变总蛋白含量,表明总蛋白含量受遗传控制[17].核糖体的mRNA转录本之间的竞争可能是最终蛋白质组成的原因,正如大豆中所提出的那样[19].
尽管在培育具有更高营养价值的玉米品系方面取得了这些进展,但导致软粒的潜在生理和分子机制仍然没有得到很好的理解。一些研究已经调查了转录模式的变化引起o2突变(20.- - - - - -23].他们之间一致的观察指向基因表达的多效性变化,但很难确定解释软核表型的生理途径和蛋白质合成的变化有助于改善胚乳的氨基酸组成。内质网(ER)应激反应相关基因在不透明突变体中持续上调[22],糖酵解途径中的许多基因以及其他通常与缺氧应激生理反应相关的基因,如乙醇脱氢酶和山梨醇脱氢酶[21,22,24],但它们在不透明表型表达中的作用尚不清楚。过程中蛋白质积累的蛋白质组学分析o2发育通常与微阵列分析观察到的基因表达模式一致[25].
在本研究中,我们分析了基因表达o2胚乳使用基于扩增片段长度多态性(AFLP)的方法,该方法是开放的,不依赖于已知或预测的基因序列。我们还对成熟种子进行了蛋白质组学分析,以确定对赖氨酸和色氨酸含量增加有不成比例贡献的特定蛋白质,以便将这些更丰富的基因产物与成熟胚乳中的基因表达联系起来。除了确认之前描述的总体基因表达模式外o2在突变体中,我们发现了与野生型胚乳相比,mRNA转录水平的其他一些差异。与防御反应相关的几种基因产物也大幅下调o2胚乳,这可以进一步解释它对耳腐和害虫更敏感的原因。淀粉生物合成基因表达改变o2并与淀粉粒结构的变化有关。此外,对成熟种子中蛋白质积累的分析显示,一些富含赖氨酸的蛋白质在种子中含量更高o2胚乳。这些变化可以解释W64A中赖氨酸含量增加的很大一部分原因o2。讨论了基因表达、蛋白质含量和淀粉结构的变化对不透明胚乳发育的影响。
结果与讨论
成绩单分析概述
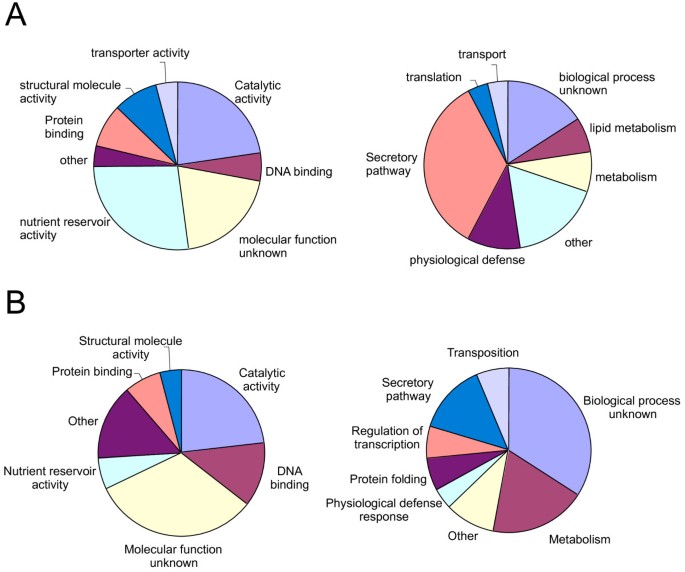
系统比较W64A +和W64A的基因表达模式o2胚乳发育中代谢最活跃的阶段,转录本分析由GeneCalling™在Curagen Corp.(纽黑文,康涅狄格州)进行[26授粉后22天(DAP)。GeneCalling™方法不依赖于基因序列的先验知识,因此可以识别序列数据库中不存在的基因的表达差异。用47对不同的限制性内切酶生成cDNA片段,并比较相应基因片段的表达水平。共有470个推测基因在W64A +和W64A中被鉴定为差异表达o2通过GeneCalling™软件使用t检验。差异表达基因片段的一个子集的序列可以通过寡核苷酸竞争,即“中毒”,用未标记的基因特异性引物或在中毒失败时通过克隆和测序片段来确认。确认了274个基因片段的身份,范围在50 ~ 500 bp,代表了151个基因产物。通过BLASTN和BLASTX对Genbank和玉米基因组序列数据库(http://www.maizesequence.org)。利用基因本体数据库(G.O.;http://www.geneontology.org)及其分子功能和生物学过程的分类,见图1。附加文件中提供了差异表达基因及其特性的综合表1:表S1。W64A有26种不同的生物学功能受到影响o2,包括碳水化合物代谢和应激反应,这与大豆胚乳表型的改变有关o2突变体。其中,23个功能类群的70个基因表达上调,16个功能类群的81个基因片段表达下调o2。
GO功能类的上调和下调基因
正如预期的那样,大量下调的基因具有与营养库活性相关的分子功能(图1),这是由于一些19-和22-kD α-zein基因的积累和27-kD γ-zein的显著减少o2。这些蛋白由具有高度保守序列的大型基因家族编码,是O2调控的良好特征靶点[27,28].营养库基因功能降低o2其次是催化活性(23%)、结构分子活性(8%)、蛋白质结合(8%)、DNA结合(6%)、转运蛋白活性(4%)和其他次要类别(4%),如离子结合和酶调节活性。在生物过程中,34%的下调基因参与了分泌途径,这可能反映了对er -常驻zein存储蛋白积累减少的反应。其他下调的功能类别包括生理防御(11%)、代谢(8%)、脂质代谢(7%)、转运(4%)、翻译(4%)和其他(17%)。分别有20%和16%的基因分子功能和生物学过程未知。
对于基因的上调o2,只有一小部分具有养分库活性(6%)的功能。相反,上调基因中催化活性占比最大(23%),其次是DNA结合(13%)、蛋白质结合(7%)、结构分子活性(4%)和其他(15%)。这与代谢是受影响最大的生物功能(19%)相一致,其次是分泌(14%),蛋白质折叠(6%),转录(6%),转位(6%)和生理防御反应(4%)。在上调的基因中,32%不能被分配到分子功能,34%不能被分配到生物过程。
基因o2下调
正如预期的那样,玉米醇溶蛋白基因家族的成员在o2(19 kDa和22 kDa α-zeins和27 kDa γ-zein)。有少数玉米醇溶蛋白基因表达增加o2。然而,这种分析转录本的方法对等位基因差异非常敏感,上调的zein基因可能代表了这种等位基因。据报道,一些参与生物和非生物胁迫防御反应的基因也显著下调o2,例如核糖体失活蛋白(RIP) b-32,它对病原体和病毒具有防御作用,是玉米中众所周知的O2调节靶标[29,30.].β -葡萄糖苷酶聚集因子样蛋白(BGAF)也被强烈下调;据报道,这些蛋白质参与了对病原体和食草动物的防御[31,32].bgaf样蛋白可能是一个值得进一步研究的特别有趣的基因,因为它具有O2一致结合序列[24,33]在−227 nt处预测的转录起始点。然而,还有其他几种与防御相关的转录物在较小程度上下调,枯草菌素-凝乳蛋白酶抑制剂CI-1B (CI-1B),它对损伤有反应[34]、花卉特有的γ -硫硫蛋白(防御素SD2),对动物细胞有毒,可抵御寄生虫[35]和基底层抗真菌蛋白2 (BAP2)。这是可能的高灵敏度o2对真菌和害虫的抑制作用是由于降低了植物b-32和BGAF蛋白水平的协同作用o2胚乳。
一些核糖体蛋白,如40S亚基蛋白S3a和60S核糖体亚基蛋白L19-3,以及真核细胞质核糖体小亚基的结构RNA 18S RNA基因都被下调o2。其中一些核糖体成分的变化可能是细胞对整个mRNA库变化的反应,其中缺乏丰富的er靶向α-zein mRNAo2。其他下调的转录本包括NAC (N点,一个TAF和CUC转录因子)结构域包含蛋白48,被预测作为植物特异性转录因子参与多种发育事件,以及生物和非生物应激反应[36].在信号转导中起作用的基因,如yt521 - b样家族蛋白、谷胱甘肽s -转移酶GST 31、FAR-RED impairment RESPONSE 1蛋白等也表现出较低的表达o2。这些转录因子和信号转导蛋白在不透明表型形成中的作用,如果有的话,尚不清楚。
一些在氨基酸代谢中起作用的基因也被下调,包括色氨酸转氨酶(TA1)和酮酸还原异构酶,后者催化了支链氨基酸缬氨酸、亮氨酸和异亮氨酸生物合成途径的两个步骤[37]和丙氨酸-乙醛转氨酶2。令人惊讶的是,LKR-SDH1被认为是受O2调控的[38],但W64A +和W64A的转录量差异不显著o2这可能表明其表达受遗传背景或环境的影响。大量氨基酸生物合成酶可能在一定程度上受到O2的调节。酵母O2的同源物,b-zip转录因子GCN4 (GeneralC控制Non- deresible 4),已知可诱导大量氨基酸生物合成基因的表达,以响应氨基酸饥饿[39),gcn4突变体可以通过玉米的表达来补充O2基因(40].
W64A中几个与细胞结构和发育相关的基因被下调o2,包括:katanin p60 atp酶,参与调控微管动力学[41]调节植物细胞的分裂和生长[42];阿拉伯半乳聚糖蛋白(AGP),作为细胞身份和命运的标志,在植物营养生长发育、继发性细胞壁增厚和程序性细胞死亡中起作用[43];油菜素内酯类生物合成蛋白,是胚胎后生长所需的天然生长调节剂[44];和母体效应胚胎发育阻滞21 (MEE21),其调节胚胎发育和成熟[45].虽然还不知道这些蛋白质是如何影响不透明表型的,但它们可能会引起细胞组织的变化,从而使胚乳细胞倾向于在淀粉颗粒之间形成特征间隙,这是不透明胚乳的一个标志。
基因o2上调
W64A中许多编码初级碳水化合物代谢酶的基因上调o2。糖酵解途径中的两种酶,胞质三磷酸异构酶(TIM)和胞质磷酸甘油酸激酶(PGK)表达上调。果糖激酶-1通过葡萄糖-6-磷酸的形成在糖酵解的入口点起作用,并维持碳对淀粉形成的通量,增加了1.85倍。糖酵解酶表达的许多变化和乙醇脱氢酶1的上调2.86倍与缺氧反应一致。研究表明,与胚胎相比,玉米胚乳是一个高度缺氧的环境,这可能导致碳分流成淀粉而不是油[46].然而,目前还不清楚为什么o2突变体缺氧反应增加,淀粉含量增加o2胚乳基本上与W64A背景中的野生型相同(未显示)。
参与淀粉生物合成的酶增加o2,包括颗粒结合淀粉合酶I (GBSSI),它是合成直链淀粉所必需的。支链淀粉合成所需的酶也被上调,包括普鲁兰酶型淀粉去分支酶1 (Zpu1),它水解聚葡聚糖的α-1,6-葡萄糖键,1,4- α-葡聚糖分支酶2 (BE2),它催化α-1,6葡聚糖的形成,是淀粉颗粒表面支链淀粉合成所必需的。海藻糖-6-磷酸合酶也增加,这与ADP-Glc磷酸化酶的氧化还原活化有关,ADP-Glc磷酸化酶催化淀粉合成的第一步[47,48].先前的研究表明,不透明突变体改变了淀粉的生化特性[49],但其潜在机制仍不清楚。一种或多种淀粉生物合成酶的表达变化可导致所观察到的性状o2淀粉,尽管改变一种淀粉生物合成酶的表达或突变会对多种酶的活性产生复杂的影响。
内质网中参与蛋白质维持和折叠的几种蛋白质被上调。钙依赖蛋白伴侣Calnexin、calreticulin2和伴侣DNA J2的表达在W64A中增加了约两倍o2。胞质小伴侣蛋白、16.9 kDa I类热休克蛋白3和热休克蛋白18c也上调。参与半胱氨酸氧化形成二硫键的其他ER酶,包括蛋白质二硫异构酶(PDI)和ER膜定位氧化还原酶1 (ERO1)增加[50].这些基因与未折叠蛋白反应有关,它们的上调可能是由于内质网中蛋白质体结构的改变[22].
W64A的应激反应和防御基因上调o2包括以下:蒜氨酸裂解酶2(蒜氨酸酶)和胱抑素6,这是对食草动物防御反应的一部分[51,52];木聚糖酶抑制剂蛋白1和甘氨酸-天冬氨酸-丝氨酸-亮氨酸(GDSL)基序脂肪酶/水解酶样蛋白,这两种酶都参与了对真菌病原体的防御[53,54];一个Pi饥饿诱导蛋白和一个aba响应的40 kDa蛋白[55- - - - - -57].一个MAP激酶上调,几个MAP激酶反应基因也上调。这些包括呼吸爆发氧化酶蛋白,同源物B (RBOHB)和NADPH氧化酶的诱导形式,NADPH氧化酶是丝裂原活化蛋白激酶(MAPK)调控信号通路中的下游效应物,产生活性氧(ROS),并在应对各种应激时触发先天免疫[58]。此外,WRKY转录因子上调,在生物和非生物胁迫下,WRKY转录因子被MAPKs磷酸化并激活[59].这些上调的应激反应不太可能增强对害虫的抗性,而很可能是对突变的多效性反应o2,因为有充分的证据表明o2更容易受到害虫的影响。
不透明型和野生型的蛋白质组学比较
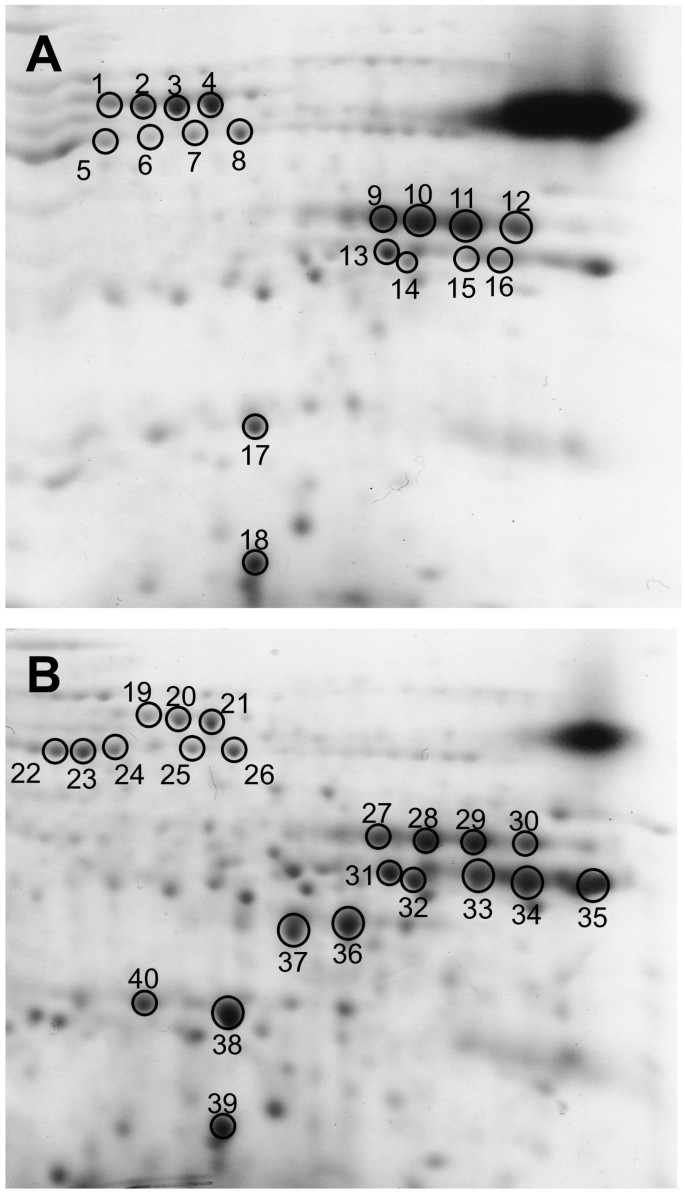
为了检测W64A非玉米蛋白积累的差异o2利用硼酸盐萃取法从成熟胚乳中纯化的等量非玉米蛋白进行2D SDS-PAGE分析[60].对成熟籽粒进行分析,以确定在胚乳发育过程中,促进赖氨酸增加的丰富的非玉米蛋白是否与其基因表达一致。在凝胶的可视化和对齐后,从凝胶中切除40个差异溶解或显示改变积累水平的蛋白质点以进行识别(图2)。通过对蛋白质斑点的胰蛋白酶消化物进行MALDI-TOF肽质量图谱鉴定感兴趣的蛋白质。GBSSI、烯醇化酶1、豆荚样蛋白、GAPDH、TIM和SDH的积累增加o2烯醇化酶2和HSP3的积累无变化(表21)。许多蛋白质积累的最大差异反映在22 DAP时通过转录谱测定的转录水平上。例外的是GBSSI和烯醇化酶1,在多项研究中存在不一致的折叠变化[20.- - - - - -22].这可能是由于所分析的品系的遗传背景不同,或者材料生长的环境不同。然而,在W64A背景下,转录谱分析和蛋白质组学数据显示烯醇化酶1的积累在W64A中更高o2(图2)。值得注意的是,含有超过8%赖氨酸的GAPDH的积累显著增加(~1.8倍),但在转录本分析数据中没有发现转录本丰度有显著差异。与野生型玉米胚乳相比,某些SDH1异构体的赖氨酸含量增加了2.5倍,其中含有4%的赖氨酸,低于GAPDH,但比野生型玉米胚乳典型的总赖氨酸含量高出近2倍。GAPDH和SDH1的增加可能是W64A赖氨酸水平升高的重要原因o2,这些非常丰富的蛋白质的表达可能与翻译伸长因子1A (EFIA)的表达有关,EFIA与玉米胚乳中赖氨酸含量相关,但不足以解释赖氨酸含量的总增加[61].
W64A +和W64A的2D SDS-PAGE分析o2。来自W64A +的非玉米蛋白(一个)和W64Ao2(B)系从成熟胚乳面粉中提取,用2D SDS-PAGE分离。从凝胶中切除圈出、编号的点,通过MALDI-TOF肽质量图谱确定蛋白身份,并与表中的行对应1。
基因表达验证
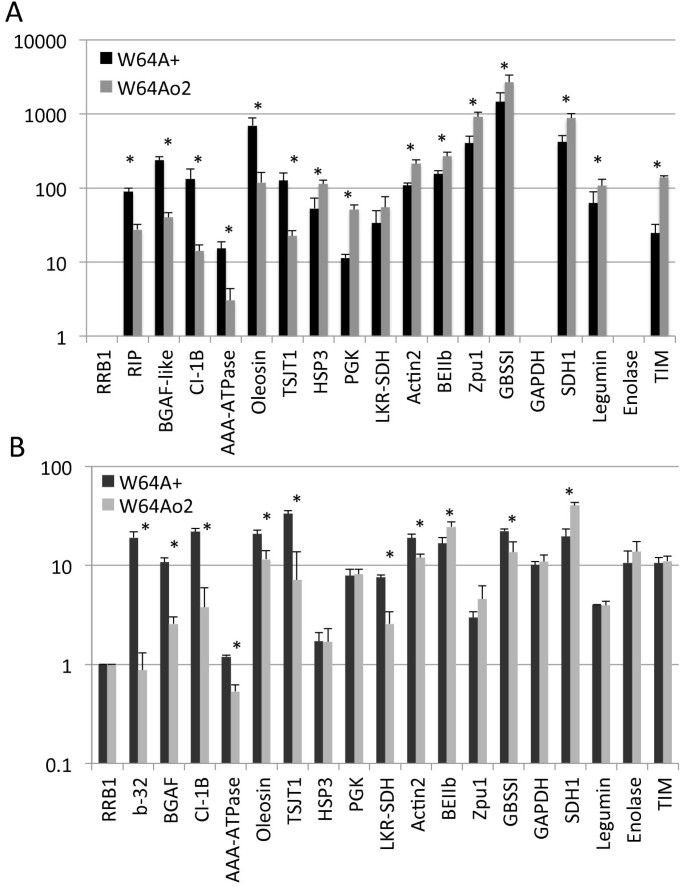
定量实时聚合酶链式反应(qRT-PCR)对W64A中编码上调和下调转录本的几个基因进行了检测o2以验证来自两种基因型的胚乳在22dap时的转录谱分析实验结果。视网膜母细胞瘤相关蛋白1 (RRB1)作为内参基因,因为它在两种基因型中都有一致表达(见材料和方法)。选择RIP基因b-32作为qRT-PCR的阳性对照,因为已知该基因在体内下调o2突变体(30.].基因的选择基于以下类别:1)基因的表达高度降低o2分析实验中发现的蛋白体调节亚基AAA-ATPase (AAA-ATPase)、茎特异性蛋白(TSJT1)、16-kDa oleosin、CI-1B和BGAF等突变,这些突变在以往的研究中未被鉴定;2)淀粉生物合成基因,如Zpu1、淀粉分支酶IIb (BEIIb)、GBSSI;3)转录谱分析或2D SDS-PAGE分析中改变的碳水化合物代谢相关基因,包括GAPDH、山梨醇脱氢酶1 (SDH1)、TIM、烯醇化酶1和PGK;4) W64A中出现变化的其他基因o2根据分析结果,如actitin2, legumin1, 17.4 kDa I类热休克蛋白3 (HSP3)和LKR-SDH1。
qRT-PCR中各样品间转录物的相对表达量与分析结果基本一致(Pearson相关系数)r= 0.80,方差分析p < 0.001;额外的文件2:图S1)。然而,在某些情况下,Gene Calling检测到的转录本折叠变化高于qRT-PCR。已知o2调控基因b-32的转录水平显著降低o2通过转录谱分析和qRT-PCR(图3.一个和3.B),与以往报告一致[20.- - - - - -22].BGAF、16 kDa oleosin、CI-1B、TSJT1和AAA-ATPase转录水平均显著降低o2,qRT-PCR与W64A +相比(图3.B)和Gene Calling(图3.A和附加文件1:表S1)。qRT-PCR分析也证实了淀粉合成基因的表达上调o2如Zpu1和BEIIb [20.,22)(图3.)。尽管在Zpu1的情况下,GeneCalling结果的增加更大(2.27倍比qRT-PCR的1.55倍)。这些结果表明,大多数基因表达的变化都是基因突变的结果o2突变,而不是遗传背景或现场环境条件。另一方面,一些基因表达不一致,尤其是LKR-SDH和GBSSI。如前所述,LKR-SDH在转录谱分析数据中没有显著差异(图3.A),但当用qRT-PCR对生长在不同环境中的个体进行测量时,有显著差异(图3.B).同样,GBSSI成绩单水平的差异在以往的报告中也不一致[20.- - - - - -22].GBSSI成绩单增加o2而qRT-PCR分析显示,基因表达水平显著下降。这些结果与之前的研究数据一起表明,GBSSI和LKR-SDH的表达可能取决于基因型和环境条件。
碳水化合物代谢相关基因显著影响o2通过GeneCalling或2D SDS-PAGE分析,qRT-PCR检测。在所检测的基因中,只有SDH1在o2在22 DAP(图3.)。最后,通过qRT-PCR检测HSP3和actin2的表达与GeneCalling结果不一致,但actin2的水平下降o2在其他实验中观察到[21,22].这种差异有可能是由于引物特异性,因为HSP和肌动蛋白都属于多基因家族,而且还有其他家族成员具有显著的序列相似性。因此,qRT-PCR可以同时检测到多个基因家族成员。
Western blot分析opaque2和野生型系
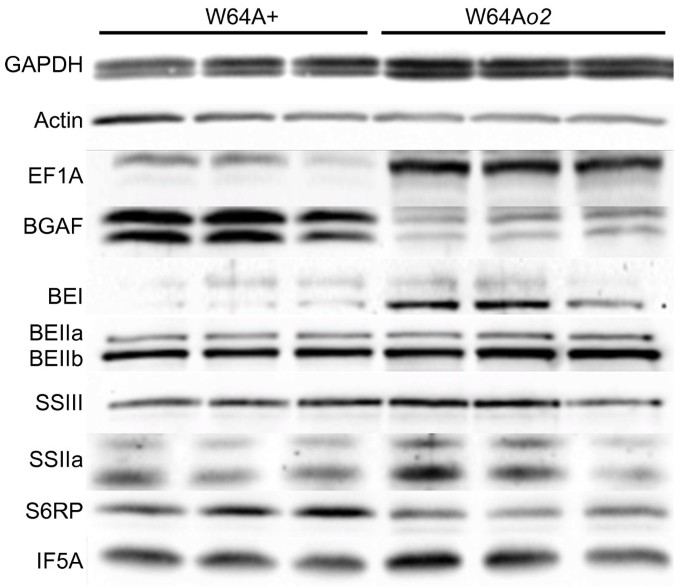
Western blot分析22个磷酸酶W64A +和W64Ao2对玉米胚乳进行转录谱分析和蛋白质组学分析(图4);密度法定量测量见表2。与基因表达数据形成对比的是o22D SDS-PAGE和western blot分析均显示突变体中GAPDH蛋白丰度增加。这表明GAPDH蛋白在胚乳细胞中可能特别稳定,因此在种子发育过程中积累到比其转录丰度高得多的水平。虽然actin2的表达在o2在转录谱分析数据中,western blots没有观察到可测量的蛋白质差异(图4)。然而,据报道,抗肌动蛋白抗体可以识别多个王国的许多蛋白质异构体。因此,在目前的分析中,对于基因上调的产物并不是特异性的。正如预期的那样,EF1A在o2而W64A中其他翻译相关因子(翻译起始因子5A, IF5A)略高或略低(核糖体蛋白S6, S6RP)o2。然而,真核翻译起始因子4G (eIF4G)、真核翻译起始因子2α亚基(eIF2α)或真核翻译起始因子4E (eIF4E)没有可测量的差异(未显示)。淀粉生物合成酶的分析表明,BEIIa和BEIIb之间没有差异o2还有野生型。而淀粉合酶IIa (SSIIa)和淀粉分支酶I (BEI)的积累增加o2。这两种酶在突变或被RNAi敲除后都对淀粉结构有显著影响,导致葡聚糖链较短的支链淀粉的积累[62,63].相比之下,在an中,BEI优先产生较长的链长分支(>16),而BEIIb优先产生较短的分支(<12)在体外分析(64].综上所述,这些观测结果表明,在W64A中o2突变体支链淀粉分支平均链长大于W64A +。
Western blot分析W64A +和W64A中所选蛋白o2。使用抗血清对左侧所示的蛋白质进行Western blot。分别从22 DAP冷冻的独立穗上取3个重复样品,分别用SDS-PAGE和western blotting分离25 μg蛋白。用密度法对每个条带进行分析,计算出每种蛋白质的折叠变化值,其数值见表2。
淀粉分析
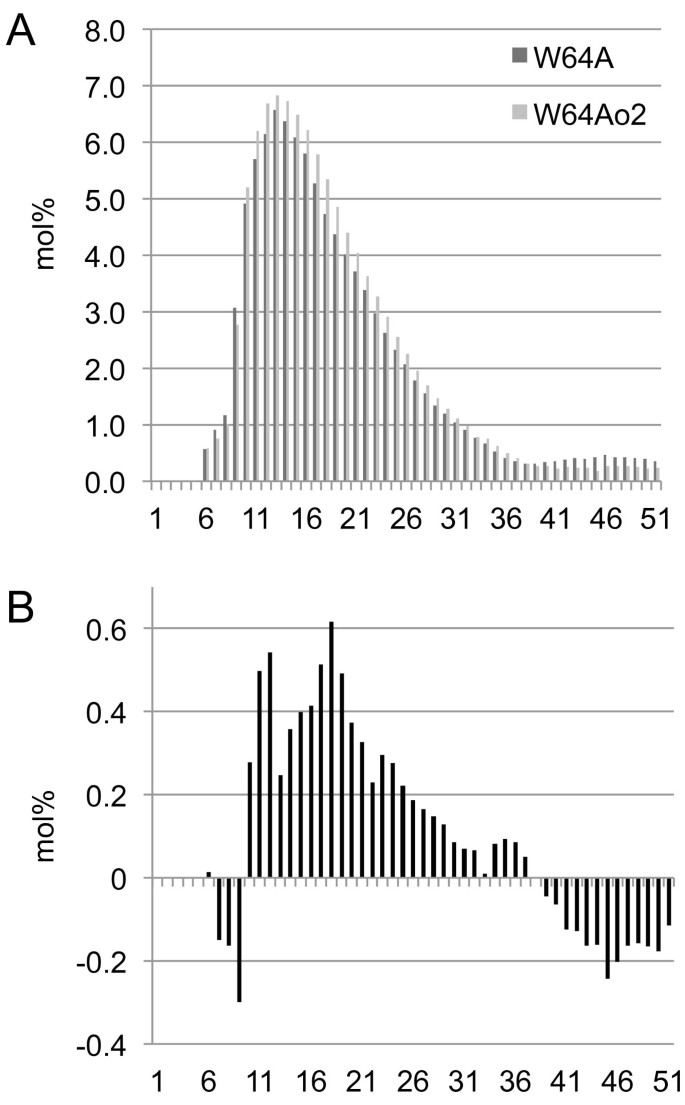
几个淀粉生物合成基因的表达在W64A +和W64A之间存在差异o2基于基因表达分析和2D SDS-PAGE。有趣的是,o2是8个不同的等基因不透明突变系中唯一在淀粉生物合成基因表达上有显著差异的突变体([22,吉本和拉金斯未发表)。因为一些淀粉生物合成酶的水平在o2特别是对W64A +和W64A淀粉的性质进行了研究o2用差示扫描量热法(DSC)分析,以确定这些变化是否影响了淀粉结构。W64A的起温温度、峰温温度以及糊化总焓均显著高于W64Ao2(表3.)。这些热性质的数值越高o2与支链淀粉分支较长、结晶淀粉含量较高的淀粉相一致。为了进一步表征淀粉的结构,研究了W64A +和W64A支链支链长度的分布o2被测量。用毛细管电泳分离出脱支淀粉葡聚糖,比较得到的支长分布(图5)。两种基因型葡聚糖摩尔百分比含量相近,但W64A葡聚糖的分布不同o2向更高的聚合度转移(图5A).差异图清楚地显示,在W64A中,聚合度在15到25个葡萄糖亚基之间的葡聚糖链显著增加o2(图5B).这些结果与先前观察到的相似o2在CM105自交系中[49].western blot分析和淀粉结构分析表明,增强的BEI或SSIIa活性导致W64A中葡聚糖链显著延长的支链淀粉o2。W64A结晶度和分支模式的这些变化o2淀粉可以改变淀粉颗粒与胚乳蛋白质的联系,从而促进软,不透明表型的形成。
结论
分析opaque2Gene Calling的转录模式显著扩展了之前使用微阵列的研究结果,并且通过将转录谱分析与蛋白质组学分析相结合,我们能够记录某些与初级碳代谢相关的富含赖氨酸的蛋白质的存在。这与之前对发育中的籽粒的蛋白质组学分析相一致[25],但相对水平似乎在成熟的籽粒中比例要高得多。SDH1和GAPDH蛋白含量最高,赖氨酸含量分别为4.2%和8.5%。特别是对于GAPDH,其在成熟胚乳中较高的积累可能贡献了相当大比例的赖氨酸增加o2。上述结果可以解释W64A中赖氨酸含量较高的原因o2胚乳,以及玉米自交系中该性状表型变异的基础[65].
导致有害表型的额外基因o2在分析中发现了与害虫抗性有关的基因。RIP是著名的o2在真菌发病机制中发挥防御作用的靶基因[66].同样地,BGAF被强烈下调,并且被认为具有在伤口部位集中β -葡萄糖苷酶的作用,以促进糖基化防御化合物的激活[31].其他下调的防御蛋白包括Cl-1B, BAP2和防御素SD2。这种防御蛋白的下调可能协同促进了高易感性o2对真菌和昆虫有害。这些基因的研究o2或修改o2背景可能有助于发展性能更好的高赖氨酸玉米系。
最后,o2是唯一显示淀粉生物合成基因表达显著改变的不透明突变体。特别是,BEI和/或SSIIa的上调似乎解释了淀粉颗粒的产生,这些淀粉颗粒在性质上更结晶,这可能有助于不透明表型的产生。前人研究表明,淀粉粒结构的改变可能是玻璃体胚乳恢复的重要因素o2QPM中的修饰语[49].我们最近的研究表明,QPM中的普鲁兰酶活性明显较高,并与胚乳修饰程度密切相关,这种变化很可能是由于相对于软聚糖链的葡聚糖链长度的减少o2突变体(Wu和Gibbon未发表的数据)。因此,通过转基因手段或利用BEI或SSIIa的天然等位基因调控淀粉品质可能是提高籽粒品质和抑制不透明表型的一种途径,可用于QPM或其他高赖氨酸玉米品系的改良。
方法
通过GeneCalling™进行转录谱分析
近等基因玉米的植株(玉米l)自交系W64A +和W64Ao2(22]于1998年夏天在弗吉尼亚州约翰斯顿的先锋国际高级育种遗传苗圃的田间地块上种植。每一自交系丰产穗于22 DAP收获后立即冷冻于液氮中。为了尽量减少耳朵间生物变异对基因表达分析的影响,从三个耳朵的中间部分收集了相同数量的胚乳。用PURE分离总RNA脚本试剂盒(Gentra Systems, Inc., Minneapolis), mRNA分析由GeneCalling™在Curagen(纽黑文,CT)进行[26].简而言之,cDNA由三个独立池化的W64A +和三个独立池化的W64A合成o2胚乳样本(生物学重复)。6种cDNA制剂分别分为3个等分(技术重复),每个基因型提供9个重复用于分析。每个cDNA都用47种不同的限制性内切酶组合进行酶切。每个摘要的片段被连接到适配器上;这些片段被带有独特标记的引物放大(一端是生物素,另一端是荧光标记)。用链霉亲和素珠纯化标记的片段,用高分辨率凝胶电泳分离得到峰的位置和高度米rcDNA片段丰度(s)。GeneCalling™软件编译了一个差异丰富的片段列表,并为每个检测到的差异分配了一个排名(显著性)。该软件进一步在核酸数据库中搜索具有相同长度和末端序列的片段,并预测可能的候选基因。预测片段的身份通过未标记的基因特异性引物(“中毒”)竞争性扩增或通过克隆和测序片段来确认[26].包含确认的基因序列标签的文件作为附加文件提供3.。
实时荧光定量PCR检测表达差异
植物材料
W64A +和o2用于定量聚合酶链反应(qRT-PCR)和western blotting的籽粒于2012年夏天在德克萨斯州的Elm Mott种植。籽粒在22 DAP下收获,并在- 80°C冷冻保存。每基因型3穗作为3个生物重复。每耳6个胚乳解剖,用研钵和杵在液氮中研磨成细粉。对于RNA分离,使用了多达0.1克的材料。对于蛋白质萃取,取50 mg称量,在硼酸盐萃取缓冲液(12.5 mM NaBO)中均质3., 1%十二烷基硫酸钠和2% 2-巯基乙醇[v/v])。
RNA分离、cDNA合成及qRT-PCR
按照制造商的说明,使用Purelink™植物RNA试剂(Invitrogen, Carlsbad, CA)从冷冻胚乳中分离总RNA。RNA样品稀释至最终浓度~100 ng/μl,在NanoDrop ND-1000紫外/可见分光光度计(NanoDrop Technologies, Wilmington, DE)上定量,通过260 nm和280 nm的吸收比检查其纯度,所有样品的吸收比均≥2.0。第一链cDNA使用qScript™cDNA SuperMix (Quanta Biosciences, Gaithersburg, MD)从1 μg RNA合成,随后在水中稀释10倍。
qRT-PCR引物基于Primer3 Plus软件(http://www.bioinformatics.nl/cgi-bin/primer3plus/primer3plus.cgi)。引物设计为62°C退火温度,并跨越外显子-外显子连接,以控制基因组DNA污染(附加文件4:表S2)。
基因表达分析使用Corbett rotor - gene™3000 (Qiagen, Velancia, CA)在72孔转子中进行qRT-PCR。每个20 μl反应含有10 μl PerfeCTa®SYBR®Green FastMix®(Quanta Biosciences, Gaithersburg, MD), 2.5 μl 10倍稀释cDNA或1 μl质粒标准,拷贝数为105到108,每个引物涂1 μM。PCR程序为:50°C保持2 min自动扩增优化,95°C初始变性10 min, 95°C持续15 s, 60°C持续1 min,循环50次。从55°C加热到95°C,以1°C / s的斜坡速率获得熔解曲线,以确认单个扩增子。W64A +和W64A基因表达水平o2针对相应基因型中RRB1基因的表达进行归一化[67],因为在初步实验中两种基因型之间没有差异表达。基因表达的归一化使用Q-Gene Core Module文件[68].W64A +与W64A基因表达水平的统计学差异o2使用JMP统计软件(SAS Institute Inc., Cary, NC)对来自转录谱分析和qRT-PCR结果的基因表达水平进行非配对双尾t检验,用Pearson相关系数计算基因表达水平的一致性,用方差分析确定显著性。
核蛋白提取,SDS-PAGE和western blotting
采用含12.5 mM硼酸钠、1% (w/v) SDS、2% β-巯基乙醇、pH 10 [69].将1 ml硼酸盐萃取缓冲液加入50 mg磨碎的玉米粒中,在室温下摇晃至少2小时。室温下,16000 × g离心15 min,去除粗提物中不溶性细胞碎片。将清除的蛋白质提取物搅拌并保存在−80°C。
每个样品中的25 μg总蛋白在1X SDS- page运行缓冲液(25 mM Tris, 192 mM甘氨酸,0.1% (w/v) SDS)中用12% SDS- page分离,然后使用TE 22 Mighty Small Transphor Tank Transfer Unit (GE Healthcare, Piscataway, NJ)转移到BioTrace™PVDF膜(Pall Corporation, Pensacola, FL)。使用预染色的蛋白质标记物(Precision Plus protein™All Blue standard, Bio-Rad, Hercules, CA)目视检查蛋白质转移的质量,并用Ponceau S (0.1% [w/v]在5% [v/v]醋酸中)染色膜。用3%脱脂干奶粉在1X TBST缓冲液(10 mM Tris-HCl, Ph 8.0, 150 mM NaCl, 0.1% (v/v) Tween-20)中堵塞膜,室温震动1小时。
免疫印迹的一抗如下:RPS6由Julia Bailey-Serres提供;BGAF由Asim Esen提供;GAPDH由施明哲提供;eIF2α, eIF4E和eIF4G由Karen Browning提供;SSIIa由关汉平提供;SSIII、BEI和BEIIa/b由Alan Myers提供;抗肌动蛋白小鼠单克隆抗体(Cat;不。A0480, Sigma St. Lois MO)。用TBST稀释的一抗(根据抗体效价,1:1000 ~ 1:3000)室温孵育1小时或4℃过夜,用TBST洗涤,然后用二抗(辣根过氧化物酶偶联山羊抗兔或山羊抗小鼠; Invitrogen, Carlsbad, CA) diluted in TBST (1:30,000). After washing with TBST, the membrane was treated with 1 ml SuperSignal West Pico Chemiluminescent Substrate (Pierce, Rockford, IL) for 2 min and the signals were detected using the Ultra- LUM Gel Imager System and UltraQuant 6.0 software (Ultra-Lum, Incorporated, Claremont, CA). The intensity of bands was quantified using the ImageJ software [70]以及W64A +和W64A蛋白表达水平的统计学差异o2使用JMP统计软件(SAS Institute Inc., Cary, NC)采用未配对双尾学生t检验进行评估。
2 d sds - page
成熟籽粒的胚乳在ddH中浸泡过夜2O在4°C。去除果皮和胚,胚乳在冷冻干燥机中干燥;干燥的胚乳用磨珠机磨成面粉。面粉样品在37℃的硼酸盐萃取缓冲液中摇晃一夜提取[69].通过70%乙醇沉淀,将蛋白质提取物分离为玉米醇溶蛋白和非玉米醇溶蛋白;无玉米蛋白颗粒用70%乙醇洗涤2次,干燥后在IPG复水缓冲液(8 M尿素,2% CHAPS, 20 mM二硫苏糖醇,0.005%溴酚蓝)中重悬。在凝胶复水化过程中,样品直接装入pH值为4-7的固定梯度条带中。根据制造商的说明,在Multiphor II或etan IPGphor 2 (GE Healthcare, Piscataway, NJ)上进行第一维分离。根据制造商的说明,使用Mini-Protein II垂直凝胶仪(Bio-Rad, Hercules, CA)进行二次元分离。用考马斯亮蓝观察蛋白质。使用Prodigy SameSpots凝胶分析软件(非线性动力学,纽卡斯尔泰恩,英国)对凝胶进行比较和斑点强度量化。
蛋白质识别
从丙烯酰胺凝胶中切除感兴趣的蛋白质点,并使用凝胶内消化程序用胰蛋白酶消化。简单地说,凝胶片通过50%乙腈在室温下孵育15分钟,并改变2到3次溶液来染色。凝胶片在Speed-Vac干燥器中干燥1小时,并在胰蛋白酶消化缓冲液(50 mM碳酸氢铵,5 mM氯化钙)中孵育再水化2, 15 μg/ml测序级胰蛋白酶(Sigma, St. Louis, MO)) 10分钟。除去多余的缓冲液,加入足够的无胰蛋白酶消化缓冲液,使其几乎覆盖凝胶片;然后将样品在37°C下孵育过夜。将缓冲溶液移至新鲜管中,凝胶片在50%乙腈和1%甲酸中孵育5分钟,并与原始上清液混合,清洗两次。根据制造商的说明,使用C-18 Zip-Tips (millipore, Billerica, MA)对肽进行浓缩和脱盐。
蛋白质鉴定是在亚利桑那大学质谱设施通过MALDI-TOF肽质谱进行的。从质谱中得到的峰列表使用ProFound肽映射工具在更新于7/1/11的Genbank非冗余数据库中进行搜索([71];http://prowl.rockefeller.edu/)。使用单同位素质量进行搜索,具有以下参数:分类学,其他绿色植物;常数改性,碘乙酰胺;部分修饰,蛋氨酸氧化;质量公差,200ppm。
淀粉结构分析
淀粉颗粒基本上按照Gutierrez所描述的那样得到纯化et al。(72].成熟籽粒用0.5% Na浸泡2年代2O5将胚乳从果皮和胚芽中分离出来,用研钵轻轻研磨。样品与50 mM NaCl混合30 s,并通过两层miraccloth (Calbiochem, San Diego, CA)过滤。将过滤后的材料在1:4甲苯:50 mM NaCl中离心5次,然后用丙酮提取2次。淀粉在使用前干燥48 h。
称干淀粉,悬浮在1:3 [w:v]浆液中去离子水。浆液被密封在密封盘进行DSC。样品盘装入DSC仪器(Q200, TA Instruments, New Castle, DE)样品座,参考座上有一个空的密封盘。样品在35°C平衡,然后在35 - 95°C以5°C/min的速度加热进行DSC扫描。使用TA Universal Analysis 2000软件(TA Instruments, New Castle, DE)计算了起始温度、峰值吸热和总焓。
采用毛细管电泳法测定支链淀粉葡聚糖链长分布。将淀粉溶解在DMSO中,加热至95°C 15分钟。用异淀粉酶(Megazyme, Wicklow,爱尔兰)分离溶解淀粉的一小部分样品,在氰化硼烷醚钠存在下,用8-氨基-1,3,6-芘三磺酸标记得到的葡聚糖。样品的标记反应被稀释,荧光标记葡聚糖链分离和定量荧光辅助毛细管电泳。绘制并比较了每个峰值面积百分比的直方图。
缩写
- AAA-ATPase:
-
蛋白质体调节亚基aaa - atp酶
- 妊娠:
-
扩增片段长度多态性
- AGP:
-
阿拉伯半乳聚糖蛋白
- BAP2:
-
基底层抗真菌蛋白2
- 贝:
-
淀粉分支酶I
- BEIIa:
-
淀粉分支酶IIa
- BEIIb:
-
淀粉分支酶IIb
- BGAF:
-
-葡萄糖苷酶聚合因子
- CI-1B:
-
枯草菌-凝乳蛋白酶抑制剂CI-1B
- DSC:
-
差示扫描量热法
- 衣冠楚楚的:
-
授粉后几天
- EF1A:
-
平移伸长因子1 α
- eIF2α:
-
真核翻译起始因子2 α亚基
- eIF4E:
-
真核翻译起始因子4E
- 如果:
-
真核翻译起始因子4G
- 呃:
-
内质网
- ERO1:
-
ER膜局部氧化还原酶
- GAPDH:
-
glyceraldehyde-3-posphate脱氢酶
- 陶瓷:
-
一般控制不可减压4
- GDSL:
-
Glycine-aspartic acid-serine-leucine
- GBSSI:
-
颗粒结合淀粉合成酶I
- HSP3:
-
17.4-kDa I类热休克蛋白
- IF5A:
-
翻译起始因子5A
- LKR-SDH1:
-
赖氨酸-酮戊二酸还原酶/糖苷脱氢酶
- MAPK:
-
丝裂原活化蛋白激酶
- MEE21:
-
母亲影响胚胎停止21
- 南京:
-
N点,一个TAF和CUC转录因子
- 氧气:
-
Opaque2
- PDI:
-
蛋白质二硫异构酶
- PGK:
-
胞质磷酸甘油酸激酶
- 存在:
-
实时定量聚合酶链反应
- RBOHB:
-
呼吸突发性氧化酶蛋白同源物B
- 撕裂:
-
Ribosome-inactivating蛋白质
- RNAi:
-
RNA干扰
- ROS:
-
活性氧
- RRB1:
-
视网膜母细胞瘤相关蛋白
- S6RP:
-
核糖体蛋白S6
- SDH1:
-
山梨醇脱氢酶1
- SSIIa:
-
淀粉合成酶IIa
- SSIII:
-
淀粉合成酶III
- TSJT1:
-
Stem-specific蛋白质
- TA1:
-
色氨酸转氨酶
- 蒂姆:
-
磷酸三糖异构酶
- Zpu1:
-
普鲁兰酶型淀粉去分支酶。
参考文献
平阿里PL: CIMMYT 1999-2001事实与趋势。满足世界玉米需求。公共部门的技术机会和优先事项。El Batán: CIMMYT;2001.
测试者M, Langridge P:在不断变化的世界中增加作物产量的育种技术。科学通报,2010,27(3):344 - 344。10.1126 / science.1183700。
Mertz ET, Bates LS, Nelson OE:改变玉米胚乳蛋白质组成和增加赖氨酸含量的突变基因。科学通报,2004,27(4):349 - 349。10.1126 / science.145.3629.279。
Nelson OE, Mertz ET, Bates LS:影响玉米胚乳蛋白质氨基酸模式的第二突变基因。科学学报,1995,15(3):344 - 344。10.1126 / science.150.3702.1469。
Schoonhoven AV, Wassom CE, Horber E:玉米象虫在近等基因玉米自交系不透明-2和面粉-2籽粒上的发育。作物科学,1997,12:862-863。10.2135 / cropsci1972.0011183X001200060044x。
Warren HL:正常和高赖氨酸玉米自交系抗镰孢菌引起的粒腐病的比较。植物病理学杂志,1998,18(3):332 - 332。10.1094 /发朵- 68 - 1331。
Schmidt RJ, Burr FA, Aukerman MJ, Burr B:玉米调控基因transparent -2编码一种与玉米蛋白DNA结合的亮氨酸拉链基序蛋白质。美国国家科学研究院。1990, 27(1): 1 -5。10.1073 / pnas.87.1.46。
Schmidt RJ, Ketudat M, Aukerman MJ, Hoschek G:不透明-2是一种识别22-Kd-zein基因中特定靶位点的转录激活因子。植物科学学报,1994,4:689-700。
Mertz ET, Veron OA, Bates LS, Nelson OE:不透明玉米对大鼠生长的影响。科学学报,1995,18(3):344 - 344。10.1126 / science.148.3678.1741。
王晓明,王晓明,王晓明,王晓明,王晓明。硬胚乳不透明材料的遗传修饰及育种策略。谷物和青贮用玉米品质性状的改良。编辑:Pollmer WG, Phillips RH。伦敦:法;1980: 37 - 73。
Huang S, Frizzi A, Florida CA, Kruger DE, Luethy MH: 19-和22-kD α -zeins减少导致的高赖氨酸和高色氨酸转基因玉米。中国生物医学工程学报,2006,29(4):457 - 457。10.1007 / s11103 - 006 - 0027 - 6。
Huang SS, Kruger DE, Frizzi A, D 'Ordine RL, Florida CA, Adams WR, Brown WE, Luethy MH:通过增强赖氨酸生物合成和减少玉米醇溶蛋白积累相结合生产高赖氨酸玉米。中国生物工程学报,2005,3:555-569。10.1111 / j.1467-7652.2005.00146.x。
王晓明,王晓明,王晓明,等。玉米不透明变种的研究进展。遗传学报,2003,16(3):387-397。
Scrimshaw NS:优质蛋白质玉米。食品营养学报,2006,27:265-266。
Vivek BS, Krivanek AF, palacoos - rojas N, Twumasi-Afriyie S, Diallo AO:育种优质蛋白玉米(QPM): QPM品种的培育方案。墨西哥,D.F:: CIMMYT;2008.
洪纳德NM, Mainville JL, Bonin CP,黄S, Luethy MH, Malvar TM:利用RNAi抑制胚乳赖氨酸分解代谢产生高赖氨酸玉米。中国生物工程学报,2007,27(5):531 - 531。10.1111 / j.1467-7652.2007.00265.x。
吴yr, Messing J: RNA干扰可以在不损失硬胚乳的情况下平衡玉米种子氮库。PLoS One, 2012, 7: e32850。10.1371 / journal.pone.0032850。
王晓明,王晓明,王晓明,王晓明。玉米胚乳优质蛋白改良及其氨基酸含量的表型分析。作物科学,2008,48:1714-1722。10.2135 / cropsci2007.08.0429。
Schmidt MA, Herman EM:大豆种子蛋白质组的再平衡可以促进外源蛋白质的积累。中国生物工程学报,2008,6:832-842。10.1111 / j.1467-7652.2008.00364.x。
Frizzi A, Caldo RA, Morrell JA, Wang M, Lutfiyya LL, Brown WE, Malvar TM, Huang S:通过不透明2突变和RNAi抑制获得的还原玉米蛋白核的组成和转录分析。中国生物医学工程学报,2010,29(4):569-585。10.1007 / s11103 - 010 - 9644 - 1。
Hartings H, Lauria M, Lazzaroni N, Pirona R, Motto M:通过蛋白质、氨基酸和转录组分析,玉米mays突变体不透明2和不透明7揭示了胚乳代谢的广泛变化。BMC基因组学杂志,2011,12:41。10.1186 / 1471-2164-12-41。
Hunter BG, Beatty MK, Singletary GW, Hamaker BR, Dilkes BP, Larkins BA, Jung R:玉米不透明胚乳突变引起基因表达模式的广泛变化。植物学报,2002,29(4):344 - 344。10.1105 / tpc.003905。
贾H, Nettleton D, Peterson JM, Vazquez-Carrillo G, Jannink JL, Scott MP:不同遗传背景下野生型和o2型玉米胚乳转录谱的比较。作物科学,2007,47:S45-S59。10.2135 / cropsci2006.03.0207。
傅瑞琪,黄,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚:利用双功能基因表达调控玉米赖氨酸生物合成和分解代谢。植物学报,2008,6:13-21。
Damerval C, Le Guilloux M:受o2突变影响并在玉米胚乳发育过程中表达的新蛋白的表征。中国生物医学工程学报,1998,27(3):354-361。10.1007 / s004380050657。
Shimkets RA, Lowe DG, Tai JT, Sehl P, Jin H, Yang R, Predki PF, Rothberg BE, Murtha MT, Roth ME:结合基因数据库查询的转录谱分析基因表达。中国生物工程学报,1999,17:798-803。10.1038/11743。
Song RT, Llaca V, Linton E, Messing J:玉米22-kD α - zein基因家族的序列、调控与进化。基因组学报,2001,11:1817-1825。
宋rt, Messing J:玉米19-kD玉米蛋白基因家族的连续基因组DNA序列。植物科学学报,2002,29(3):326 - 326。10.1104 / pp.012179。
嘿,TD, Hartley M, Walsh TA:玉米核糖体失活蛋白(b-32)。相关物种的同源性,对玉米核糖体的影响,以及前肽缺失对活性的调节。中国农业科学,2004,27(4):457 - 457。10.1104 / pp.107.4.1323。
Bass HW, Webster C, Obrian GR, Roberts JKM, Boston RS:玉米核糖体失活蛋白受转录激活子不透明-2控制。中国生物医学工程学报,1994,4:366 - 366。
陈建军,陈建军,陈建军,陈建军。玉米β -葡萄糖苷酶聚合因子(BGAF)的鉴定及BGAF结合区域的定位。中国生物医学工程学报,2001,26(3):344 - 344。10.1074 / jbc.M008872200。
Kittur FS, Lalgondar M, Yu HY, Bevan DR, Esen A:玉米β -葡萄糖苷酶聚集因子是一种多特异性的与jaclin相关的嵌合凝集素,其凝集素结构域负责β -葡萄糖苷酶聚集。中国生物医学工程学报,2007,28(3):339 - 339。
杨晓明,王晓明,王晓明,王晓明,王晓明,王晓明,王晓明。基于opopaque2 bZIP因子的协同DNA结合与序列鉴别。植物学报,1998,10:441 - 455。
植物蛋白酶抑制剂:植物的防御策略。生物工程学报,2007,2:68-85。
防御素:先天免疫的抗菌肽。中华免疫杂志,2003,3:710-720。10.1038 / nri1180。
杨晓明,陈晓明,陈晓明,陈晓明,陈晓明:NAC转录因子的研究进展。植物科学进展,2005,10:79-87。
杜尔纳J, Knorzer OC, Boger P:大麦酮酸还原异构酶(纯化,性质和特异性抑制)。中国农业科学,2003,23(4):457 - 457。
Kemper EL, Neto GC, Papes F, Moraes KCM, Leite A, Arruda P: Opaque2在玉米胚乳发育过程中赖氨酸降解活性的控制作用。中国生物医学工程学报,1999,30(4):344 - 344。
Hinnebusch AG:酵母中氨基酸生物合成基因的一般控制。生物化学学报,1986,21:277-317。10.3109 / 10409238609113614。
Mauri I, Maddaloni M, Lohmer S, Motto M, Salamini F, Thompson R, Martegani E:玉米转录激活子不透明-2在转化酵母中的功能表达。中国生物医学工程学报,2003,26(3):319-326。
Nakamura M, Ehrhardt DW, Hashimoto T:拟南芥皮层阵列中微管成核复合体的微管和katanin依赖动力学。中国生物医学工程学报,2010,12:1064-1070。10.1038 / ncb2110。
Panteris E, Adamakis IDS, Voulgari G, Papadopoulou G: katanin在植物细胞分裂中的作用:fr2和lu1突变拟南芥根细胞分裂中的微管组织。中国生物医学工程学报,2011,29(3):344 - 344。10.1002 / cm.20522。
阿拉伯半乳糖蛋白:结构、表达和功能。中国生物医学工程学报,2001,29(3):344 - 344。10.1007 / PL00000784。
Clouse SD, Sasse JM:油菜素内酯:植物生长发育的重要调节因子。植物化学学报,2004,19(4):344 - 344。10.1146 / annurev.arplant.49.1.427。
Pagnussat GC, Yu HJ, Ngo QA, Rajani S, Mayalagu S, Johnson CS, Capron A, Xie LF, Ye D, Sundaresan V:拟南芥雌性配子体发育和功能基因的遗传和分子鉴定。《科学进展》,2005,32(3):344 - 344。10.1242 / dev.01595。
刘志刚,刘志刚,刘志刚,王志刚:玉米籽粒淀粉/脂质平衡与胚资源分配的关系。植物学报,2005,29(4):589 - 589。10.1111 / j.1365 - 313 x.2005.02352.x。
Eastmond PJ, van Dijken AJ, Spielman M, Kerr A, Tissier AF, Dickinson HG, Jones JD, Smeekens SC, Graham IA:海藻糖-6-磷酸合成酶1催化海藻糖合成的第一步,对拟南芥胚胎成熟至关重要。植物学报,2002,29(4):344 - 344。10.1046 / j.1365 - 313 x.2002.01220.x。
海藻糖生物合成在植物中的作用。植物科学学报,2007,44(3):344 - 344。10.1104 / pp.104.900223。
Gibbon BC, Wang X, Larkins BA:淀粉结构的改变与优质蛋白玉米胚乳的修饰有关。美国国家科学研究院。2003, 30(4): 357 - 357。10.1073 / pnas.2136854100。
Onda Y, Kumamaru T, Kawagoe Y: ER膜定位氧化还原酶Ero1是水稻胚乳中二硫键形成所必需的。美国国家科学研究院。2009, 26(4): 457 - 457。10.1073 / pnas.0904429106。
Kuettner EB, Hilgenfeld R, Weiss MS:大蒜中蒜氨酸酶的纯化、表征和结晶。生物化学学报,2002,29(4):349 - 349。10.1016 / s0003 - 9861(02) 00088 - 7。
Martinez M, Cambra I, Carrillo L, Diaz- mendoza M, Diaz I:大麦中整个胱抑素基因家族的特征及其目标组织蛋白酶L样半胱氨酸蛋白酶,种子萌发过程中hordein动员的伙伴。植物科学学报,2009,29(3):344 - 344。10.1104 / pp.109.146019。
Igawa T, Ochiai-Fukuda T, Takahashi-Ando N, Ohsato S, Shibata T, Yamaguchi I, Kimura M:新的taxi型木聚糖酶抑制剂基因对六倍体小麦病原菌和伤害具有诱导作用。中国生物医学工程学报,2004,29(4):344 - 344。10.1093 /卡式肺囊虫肺炎/ pch195。
Oh IS, Park AR, Bae MS, Kwon SJ, Kim YS, Lee JE, Kang NY, Lee SM, Cheong H, Park OK:通过对拟南芥脂肪酶的分泌组分析,发现了一种参与对抗油菜互链病菌的脂肪酶。植物学报,2005,17:2832-2847。10.1105 / tpc.105.034819。
Vierling E:热休克蛋白在植物中的作用。植物化学学报,2001,26(4):349 - 349。10.1146 / annurev.pp.42.060191.003051。
刘春梅,刘春梅,刘春梅,王晓明,王晓明:磷酸饥饿诱导基因的负调控。中国农业科学,2001,27(4):344 - 344。10.1104 / pp.010876。
穆恩斯A,鲍w G, Prinsen E, Vanmontagu M, Vanderstraeten D:盐敏和耐盐籼稻根系对脱落酸和盐的分子和生理响应。植物营养学报,2004,27(3):357 - 357。10.1104 / pp.107.1.177。
Asai S, Ohta K, Yoshioka H: MAPK信号通路调控benthamiana烟草一氧化氮和NADPH氧化酶依赖性氧化爆发。植物学报,2008,20:1390-1406。10.1105 / tpc.107.055855。
潘迪SP, Somssich IE: WRKY转录因子在植物免疫中的作用植物科学进展,2009,30(4):457 - 457。10.1104 / pp.109.138990。
Lending CR, Larkins BA:玉米胚乳发育过程中蛋白体玉米蛋白组成的变化。植物科学学报,1998,12(4):344 - 344。
Habben JE、Moro GL、Hunter BG、Hamaker BR、Larkins BA:伸长因子1 α浓度与玉米胚乳赖氨酸含量高度相关。美国国家科学研究院。1995, 32(3): 344 - 344。10.1073 / pnas.92.19.8640。
中村Y:为了更好地理解植物支链淀粉生物合成的代谢系统:水稻胚乳作为模型组织。中国生物医学工程学报,2002,29(4):344 - 344。10.1093 /卡式肺囊虫肺炎/ pcf091。
张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲,张晓玲。中国生物医学工程学报,2004,54:865-879。10.1007 / s11103 - 004 - 0312 - 1。
关HP,李P, ImparlRadosevich J, Preiss J, Keeling P:比较大肠杆菌分枝酶和玉米分枝酶的性质。中国生物工程学报,1997,37(3):344 - 344。10.1006 / abbi.1997.0115。
Moro GL, Habben JE, Hamaker BR, Larkins BA:正常和不透明玉米胚乳赖氨酸含量变异的研究。作物科学,1996,36:1651-1659。10.2135 / cropsci1996.0011183X003600060039x。
Ferreira RB, Monteiro S, Freitas R, Santos CN, Chen Z, Batista LM, Duarte J, Borges A, Teixeira AR:植物防御蛋白在真菌发病中的作用。中国生物医学工程学报,2007,29(3):377 - 388。10.1111 / j.1364-3703.2007.00419.x。
Sabelli PA, Dante RA, leeva - neto JT, Jung R, Gordon-Kamm WJ, Larkins BA: RBR3,玉米视网膜母细胞瘤相关家族成员,受RBR1/E2F通路调控。美国国家科学研究院。中国科学院学报(自然科学版)10.1073 / pnas.0506160102。
Simon P: Q-Gene:实时定量RT-PCR数据处理。生物信息学,2003,19:1439-1440。10.1093 /生物信息学/ btg157。
Wallace JC, Lopes MA, Paiva E, Larkins BA:新的提取和定量方法揭示了改良不透明2玉米中γ -zein的高含量。中国农业科学,2000,27(3):349 - 349。10.1104 / pp.92.1.191。
Schneider CA, Rasband WS, Eliceiri KW: NIH Image to ImageJ: 25年的图像分析。工程物理学报,2012,29(3):344 - 344。10.1038 / nmeth.2089。
张伟,Chait BT: ProFound:一个利用质谱肽图谱信息进行蛋白质鉴定的专家系统。中国生物医学工程学报,2000,29(3):344 - 344。10.1021 / ac991363o。
Gutierrez OA, Campbell MR, Glover DV:涉及软淀粉(h)基因的单突变和双突变玉米胚乳基因型的淀粉颗粒体积。作物科学,2002,42:355-359。10.2135 / cropsci2002.0355。
确认
我们感谢Asim Esen提供BGAF抗血清,Julia Bailey-Serres提供核糖体蛋白S6抗血清,Ming-Che Shih提供GAPDH抗血清,Hanping Guan提供SSIIa抗血清,Karen Browning提供eIF2α、eIF4E和eIF4G抗血清。我们也感谢Alan Myers抗BEI, BEIIa/b和SSIII的血清,以及Tracie Hennen-Bierwagen进行毛细管电泳。这项工作得到了USDA-NIFA拨款2010-65115-20375的支持,贝勒大学URSA奖给BCG, Pioneer Hi-Bred资助给BAL。这项工作的一部分是由贝勒大学分子生物科学中心实现的。
作者信息
从属关系
相应的作者
额外的信息
相互竞争的利益
作者声明没有利益竞争。
作者的贡献
实验数据及撰写。KC实验数据。HW实验数据RJ实验设计与数据。BAL写作和实验设计。BCG写作,实验设计和数据。所有作者都阅读并批准了最终的手稿。
电子辅助材料
12870 _2012_1266_moesm1_esm.docx
附加文件1:表S1:确认序列的差异表达带的基因表达值。(docx110 kb)
12870 _2012_1266_moesm2_esm.pdf
附加文件2:图S1: qRT-PCR与转录谱分析基因表达值的相关性分析。为了检验基因表达测量的可重复性,将qRT-PCR确认的基因值与GeneCalling转录谱测量的值进行对比。Pearson相关性分析(r = 0.80),方差分析(ANOVA)检验线性回归是否有统计学意义(p < 0.001)。通过Grubbs检验,qRT-PCR中b-32的值被确定为显著异常值,因此从图和回归分析中删除了两个试验中b-32的折叠变化值。(pdf 27kb)
12870 _2012_1266_moesm3_esm.txt
附加文件3:用于确定基因身份的序列标签。FastA格式的序列文本文件。通过竞争性PCR或条带测序确认的每个条带的序列被用于使用基本的局部比对和搜索工具BLASTN和BLASTX搜索非冗余genbank数据库,以确定基因身份。(txt 34kb)
权利和权限
开放获取本文由BioMed Central Ltd授权发布。这是一篇开放获取文章,根据创作共用归属许可协议(https://creativecommons.org/licenses/by/2.0),允许在任何媒介上不受限制地使用、传播和复制,前提是正确地引用原始作品。
关于本文
引用本文
贾敏,吴H,克莱,刘国强et al。富赖氨酸蛋白和淀粉生物合成基因的鉴定与鉴定opaque2转录和蛋白质组学分析的突变体。BMC植物生物学13日,60(2013)。https://doi.org/10.1186/1471-2229-13-60
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/1471-2229-13-60
关键字
- 不透明的胚乳
- Opaque2
- 优质蛋白玉米
- 淀粉生物合成
- 蛋白质质量