抽象的
背景
喷雾切割菊花是一个重要的花卉,在世界上具有较高的观赏价值和普及。然而,大多数喷雾切口菊花的过量花粉分散量是其开花期内的不利因素,并且可以显着降低其观赏价值并迅速缩短其花瓶生命。更严重的是,空气中的过度花粉粒通常对人们有害,特别是对于花粉过敏的人。Therefore, in order to obtain some valuable information for developing spray cut chrysanthemum with less-dispersed or non-dispersed pollen in the future breeding programs, we here investigated the factors affecting quantity of pollen dispersal of spray cut chrysanthemum with four cultivars, i.e. ‘Qx-097’, ‘Noa’, ‘Qx-115’, and ‘Kingfisher’, that have different quantity of pollen dispersal.
结果
Qx-097具有较高的花粉散布量,每花药有819个花粉粒,每花序有196.4个花盘小花,每花序有80多万个花粉粒。花粉散布量低的‘Noa’对应的数据分别为406、175.4和35万以上;无花粉传播的Qx-115分别为219、144.2和近16万。无花粉散布的“翠鸟”每花序有202.8个花盘小花,但花药无花粉粒。此外,‘Qx-097’的花药开裂程度非常高,几乎导致花粉粒从花药中完全分散。“诺亚”的花药开裂程度适中,花药中的花粉粒没有完全分散。然而,“Qx-115”和“翠鸟”的花药完全不开裂。在‘Qx-097’中,小孢子发生和花粉发育正常,而在‘Noa’中有大量小孢子或花粉退化,在‘Qx-115’中大部分小孢子或花粉夭折,在‘Kingfisher’中全部降解。
结论
这些结果表明,喷雾切割菊花中的花粉分散量主要由花粉量确定每种花粉量,以及花粉分散的能力。微生物发生和花粉发育过程中的异常显着影响每种花粉量。花粉分散能力与花药裂开程度密切相关。微孔或花粉的整个退化,或花粉裂开的完全失败会导致花粉分散的完全失败。
背景
菊花(菊花莫瑞菊(拉马特)KITAMURA)是中国十大最受欢迎的传统花卉之一,以及世界上四大盛大的鲜花之一。因此,由于其高装饰价值,该物种占据了鲜花的重要地位[1,2].喷切菊是菊花的一种,在菊花生产中占有重要地位。它已成为中国最重要的切花,在美国和欧洲是第二大切花类型,因为它的花色和形状丰富,开花均匀,以及大量的喷花[3.,4].而插花菊的观赏价值和花瓶寿命通常随花期中管状两性花花粉散布量的增加而下降。更严重的是,喷切菊花花期产生的大量花粉颗粒会漂浮在空中,可能会引起严重的过敏反应,对人,尤其是对花粉过敏的人有害[5- - - - - -7].因此,解决喷切菊开花过程中的花粉污染问题是十分必要和迫切的。
在切割百合花的生产中也存在类似的问题。为了减少花粉污染的不良反应,提高装饰价值和百合花瓶的寿命,生产者通常在收获之后服用切割百合花的花树,当花药尚未开始分散花粉时[8- - - - - -10].虽然这是耗时,但增加产品成本略有耗时,但这一措施的优势超过了整体的缺点。这项措施在百合甚至一些其他切花中是可行的,甚至是大花药,但在喷雾切割菊花中不可行。主要原因是喷雾切割菊花的花序结构不适合人工去除花药或阉割,每个菊花花序由20-30射线小花组成,只有雌蕊和100-200小型中央盘花香,其中雌蕊和雄蕊(数字1).因此,人工摘除花药几乎是不可能的。即使生产者也可以阉割小花盘小花,但这种阉割会使喷切菊花立即失去观赏价值[1].因此,解决喷切菊花期花粉分散问题的最佳途径是通过育种方案,培育花粉分散较少或不分散的新品种。
有一些关于影响喷雾切割菊花的花粉分散量的因素的重要信息将是非常有用的。在开始开发出一种分散较少花粉的新品种或根本不会通过育种方法处理花粉的新品种。但是,此类信息现在不可用。Therefore, we are the first time to carry out a systematic investigation on factors controlling quantity of pollen dispersal of spray cut chrysanthemum in this study using four cultivars with different quantity of pollen dispersal, i.e. ‘Qx-097’ with high quantity of pollen dispersal, ‘Noa’ with low quantity of pollen dispersal, ‘Qx-115’ and ‘Kingfisher’ without pollen dispersal. Our overall aim was to reveal the main causes influencing quantity of pollen dispersal of spray cut chrysanthemum, and the expected outputs will provide valuable information for effectively developing new cultivars with less-dispersed or non-dispersed pollen in the near future.
方法
实验材料
根据对花粉传播形态特征的观察,筛选了4个不同花粉传播量的喷切花菊花品种,并在南京农业大学菊花种质资源保存中心(32°05′N)进行了栽培。(118°90′E),分别为花粉散布量高的‘Qx-097’、花粉散布量低的‘Noa’、花粉不散布的‘Qx-115’和‘Kingfisher’(图5)1).
每花序花粉量的测定
由于每朵菊花的花序通常由20-30个只含雌蕊的外围射线小花和100-200个既有雌蕊又有雄蕊的小花盘小花组成,因此只有花盘小花才能产生花粉和分散花粉[1].因此,在每个品种开花盛期随机取样10个花序,测定每个花序中心盘小花的数量。另外,随机选取10个花盘小花,测定每个花盘小花的花药数。此外,从每个品种中随机取样60个花药,以估算每个花药的花粉数量。花药置于10ml离心管中,50℃保存约24小时。之后,6毫升20% (NaPO3.)6在离心管中加入溶液(w/v),然后摇匀离心管,使离心管完全倒置,形成花粉悬浮液。在血细胞计上加入2 μl花粉悬浮液,Olympus BX41显微镜下计数花粉量。花粉粒数按公式[花粉粒数(花粉粒数/花药)= 2 μl悬浮花粉粒数× 3000/60]计算。每个实验重复6次。花粉数量每花序计算根据每个花药花粉数量,数量的花药/磁盘小花,每花序和磁盘小花的数量,即花粉数量每花序=每个花药花粉数量×每小花×数量的磁盘数量的花药小花每花序。
花粉分散的测定
在每种品种的完整开花阶段,捕获花粉的花粉图像是为了评估花粉分散的形态特征。此外,收集了花粉分散后的花药,用于测定每种方法的花粉裂化水平和花粉的量留下。此外,花粉分散后的一些花药受到以下显微镜技术。
微孢子发生和花粉发育
用石蜡切片法测定了4个品种的小孢子发生和花粉发育。11,12经过一些修改。采集各品种不同发育阶段的花蕾和花盘花,立即浸泡在FAA溶液(福尔马林5ml,醋酸5ml,酒精70% 90ml)中使用。样品通过一系列分级的乙醇溶液脱水,然后包埋在石蜡中。切片切至8 μm厚,Heidenhain苏木精染色。切片在Olympus BX41显微镜下观察成象。数字图像是用Axiocam MRC相机拍摄的。
此外,对不同发育阶段的‘Qx-097’和‘Noa’的花药进行了透射电镜(TEM)分析。13,14经过一些修改。新鲜花药从花盘中央的小花中剥离,立即浸入2.5% (v/v)戊二醛中(0.1 mol/L磷酸盐缓冲液,pH 7.2),用注射器轻轻排出,4℃保存至使用。然后用相同的磷酸盐缓冲液冲洗花药5次,并在1.5%四氧化锇中固定5 h。25更易与L玫瑰;10更易与L EGTA;2 L MgCl更易2;pH 7. 0)和乙醇溶液,然后嵌入EPON 812中。使用LKB-V超微单方(Bromma,Sweden)切割成80nm的厚度,并用乙酸铀酰染色并柠檬酸铅染色。然后在透射电子显微镜(Hitachi H-7650)下观察和成像在80kV下的切片。
统计分析
采用SPSS 16.0软件(SPSS Inc, Chicago, IL, USA)对数据进行单因素方差分析,采用Bonferroni t检验(alpha = 0.05)比较均值。
结果
每花序花粉数量
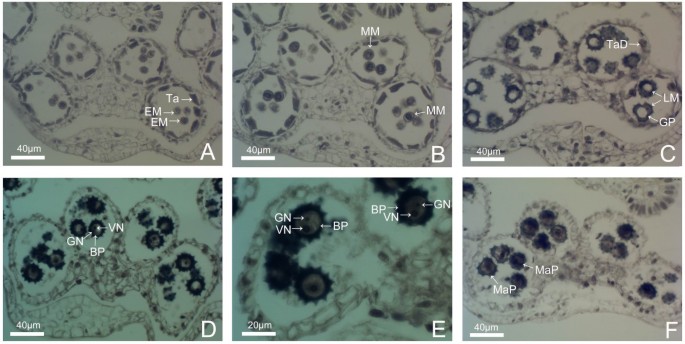
‘Qx-097’、‘Noa’、‘Qx-115’和‘翠鸟’每花序的花盘小花数分别为196.4、175.4、144.2和202.81).四个品种每朵小花的花药数量相同。但4个品种在花药花粉量和花序上存在显著差异1;数字1).以Qx-097为例,其花药和花序的花粉粒数最多,分别为819粒和80万粒以上,花药开裂后柱头上的花粉粒数也进一步支持了这一点(图2)1).然而,'翠鸟的花序不含任何花粉颗粒,因为它的花药不能产生花粉颗粒。这些结果表明,每花粉量的花粉量是影响每次喷雾切割菊花的花粉量的主要因素,而每花序的盘小花数几乎没有对每花序的花粉量影响不大。
每花序花粉分散
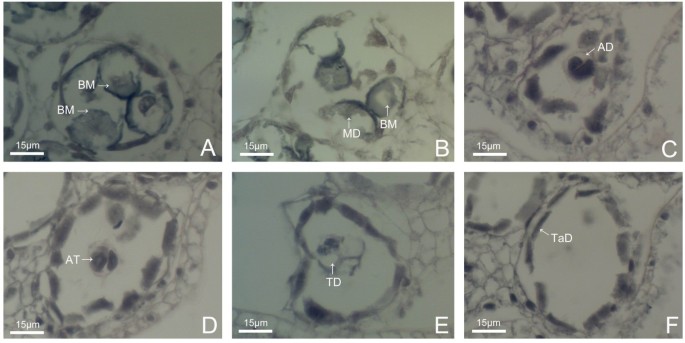
表观花粉量是一种形态学参数,其粗糙地表明在喷雾切割菊花的花药裂开期间聚集在耻骨上的花粉颗粒的量。换句话说,该参数是花粉分散量的直观反映,或者可以被视为评估菊花花粉分散的容量的标准。例如,在花药裂开期间'QX-097'的耻辱的质量清晰明显且大容量大(图1A-D),因此'QX-097'是一种具有大量花粉分散的品种。在花药裂开的“NOA”中也有大量的花粉颗粒在“NOA”中,但花粉质量与“QX-097”(图)相比较小1E-H)。因此,'NOA'被认为是具有少量花粉分散的菊花品种。'QX-115'在花药裂开期间不会分散花粉,并且在其柱头上没有任何花粉颗粒(图1I-L)。因此,'QX-115'被认为是没有花粉分散的品种,尽管它每花药每花粉219花粉,每花序近160,000(表1).“翠鸟”在花药开裂期间根本不传播花粉(图1M-P),因为其花药或花序不含任何花粉(表1),属非分散花粉品种。
'QX-097'的微孢子发生和花粉发育
Because ‘Qx-097’ is a cultivar with high quantity of pollen dispersal, thus the detailed reproductive processes of microsporogenesis and pollen development were presented here, which will provide some useful information for revealing the reason of its high quantity of pollen dispersal from reproductive aspect.
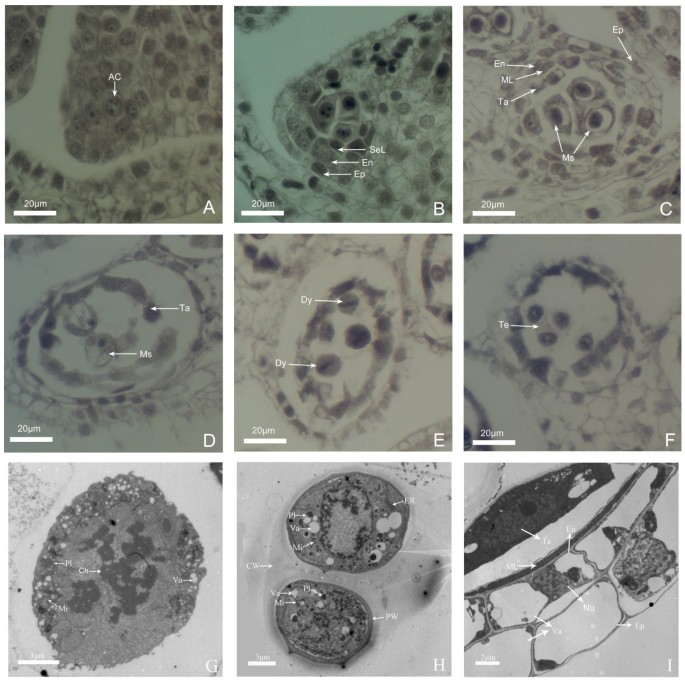
小孢子发生包括原孢子细胞分化到四分体形成的过程(图)2).在发育初期,花药横切面呈梯形,原孢细胞在花药的四角分化(图)2A).随着发育的进行,原孢子细胞通过周分裂首先发育成初生孢子生细胞和初生壁细胞层,初生壁细胞继续分裂成初生壁细胞层和内皮(图)2b)。之后,次级顶叶细胞分为翅膀和中间层。同时,主要孢子源细胞也在一系列分化中,最终形成微孔母细胞和整个花药壁(图2C)。微孔母细胞互连,其特征在于大型中心定位的核。花药墙由来自内层的四层组成:Tapetum,中间层,内皮和表皮。随着花药的进一步发展,微孔母细胞接受了减数分裂并达到了大世代的预言。此时,微孔母细胞的细胞核显示色素肿瘤和突出的核仁(图2d)。此外,微孔母细胞含有大量的电子密集细胞质,大量线粒体和塑性,以及靠近质膜附近的许多液泡(图2G)。微孔母细胞产生四面体四倍体的四倍体孢子(图2F)经历中期I和二分体期后(图2e)。微孢子细胞含有丰富的核糖体和内质网,线粒体,塑性体以及真空,和微孔壁或花粉壁可以在晚期阶段观察(图2H)。同时,中间层细胞已经开始降解,内皮细胞和表皮细胞的细胞质几乎消失,但胶质细胞中的细胞质凝结并染色非常黑(图2一世)。
TEM和石蜡截面法的“QX-097”孢子。(一)分化朝向细胞。(B)小孢子细胞形成阶段,表现为小孢子母细胞和3个花药壁(由内到外分别为次生壁细胞层、内壁和表皮)的分化。(C)微麦纤维素细胞形成阶段,显示微孔母细胞紧密邻接和四个完整的花药壁。(D)微孔母细胞在MeIosis的Praphase I,显示微孔母细胞,椭圆形,细胞和突出的核仁。(e)在第一个减数分子中脱发的微微孢子,在中期板上排列染色体。(F)Tetrad和凝胶层的凝聚细胞质。(G)粗线期小孢子母细胞,有线粒体、质体和大量液泡。(H)四分体时期,线粒体、质体、内质网、液泡增大、胼胝质壁和细胞壁开始发育。(一世)小孢子母细胞减数分裂时期花药壁内膜层、表皮层和绒毡层细胞细胞质液泡化,核大核仁明显的绒毡层细胞细胞质浓缩,中间层降解。AC:孢子细胞的细胞;Ch:染色质;连续波:胼胝质壁;Dy:一对;En:内层;Ep:表皮;呃:内质网;心肌梗死:线粒体;ML:中间层; Ms: Microspore mother cell; Nu: Nucleus; Pl: Plastid; PW: Pollen wall; SeL: Secondary parietal cell layer; Ta: Tapetum; Te: Tetrad; Va: Vacuole.
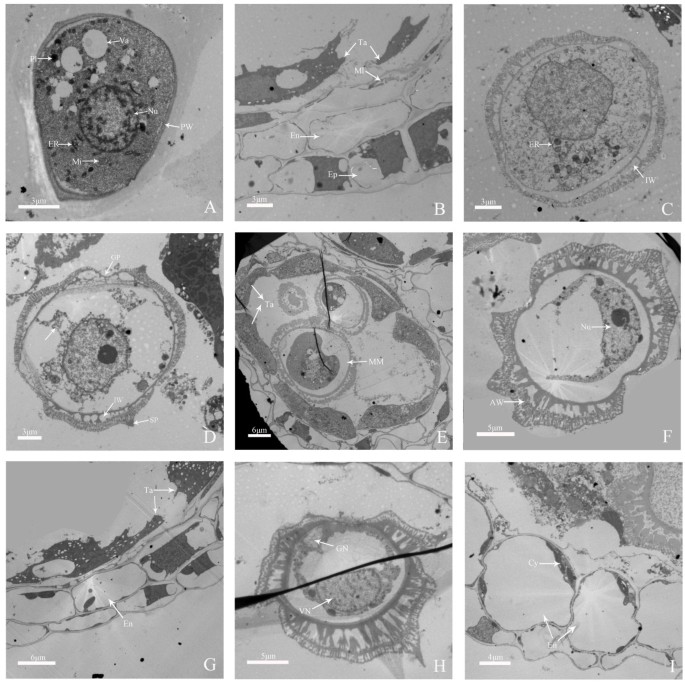
四分体释放出单倍体小孢子后,小孢子开始有丝分裂,最终形成双细胞花粉(图)3.和4).在小孢子早期,幼小的小孢子有一个明显的位于中心位置的核,稠密的细胞质,薄的细胞壁,大量的核糖体内质网,线粒体,质体和一些正在生长的液泡(图)3.A和4一种)。此外,中间层细胞几乎已退化,内皮细胞变为空虚(图3.b)。在中间微孔阶段,可以观察到细胞壁和细胞孔,尖刺突起出现在细胞壁的外表面上,核糖体,线粒体和塑性的数量降低,而形成几种空隙并占据了太多空间(图3.C, D和4b)。Tapetal细胞薄,但含有丰富的细胞细胞器,例如内质网,线粒体和塑性(图3.e)。在晚期微孔阶段,核和细胞质被一个大型中心液泡挤压,并从中心朝向细胞周边迁移,细胞壁厚度增加(图3.F和4C)。Tapetal细胞是山丘形的,它们的内切壁几乎劣化,中间层细胞几乎消失(图3.G)。在早期的双细胞花粉阶段,微孔核分为形成大型营养细胞和一个小的生成细胞对外壁,塔皮特细胞几乎消失,内皮细胞的体积增大(图3.h,我和4d)。之后,生成细胞远离墙壁移动并开始在营养细胞附近移动;淀粉等含量开始积聚在细胞质中,但可以观察到两个核,并且液泡逐渐消失(图4e)。当花粉晶粒成熟时,淀粉等内容物在花粉晶粒中几乎填充了整个细胞质,并且很难观察细胞质中的液泡(图4F)。
' Qx-097 '花粉发育的透射电镜研究(一)早期微孔,微孔细胞具有均匀和致密的细胞质,丰富的内质网,线粒体,塑性,一些生长的空泡和细胞中央的核。(B)小孢子早期花药壁,绒毡层细胞质液泡化增加,中层细胞进一步降解。(c - d)中间微孔显示开始发展的内壁,尖刺的突起出现在壁的外侧,可识别的胚芽孔,液泡的扩大,偏心核和降解细胞质和核糖体密度的数量,线粒体和塑性的数量降低。(e)小孢子中期绒毡层细胞细胞器丰富,细胞质致密。(F)小孢子后期,小孢子细胞壁,特别是内壁增厚,中央形成大液泡,使细胞质和细胞核紧贴细胞壁。(G)晚期微孔阶段,塔皮层细胞是山形和内切壁的完全几乎劣化,中间层几乎消失,只有几个残留物。(H)早期双细胞花粉期,有发育的内壁,由原毛霉素沉积形成外壁,再由孢粉素沉积形成外壁,由大的中央营养细胞和小的生殖细胞组成,小孢子核向外分裂形成。(一世)早双细胞花粉期,绒毡层几乎消失,内膜层细胞体积明显增大。Cy:细胞质;En:内层;Ep:表皮;呃:内质网;GN:生殖细胞核;医生:生殖孔;IW:细胞内壁;心肌梗死:线粒体;Ml:中间层; MM: Middle microspore; Nu: Nucleus; Pl: Plastid; PW: Pollen wall; SP: Spiked protuberance; Ta: Tapetum; Va: Vacuole; VN: Vegetative nucleus.
石蜡切片法对“QX-097”的花粉开发。(一)早期的幼儿孢子,胶质层细胞冷凝。(B)小孢子中期,显示胚芽孔,细胞壁增厚,绒毡层细胞径向变薄。(C)晚幼儿孢子阶段,显示单核微量孢子对花药壁和绦虫层的降解。(D)早期的双细胞花粉阶段,显示核突出术术形成大型中枢营养核和小生成核,胶质细胞仅具有残留物和内皮层细胞的体积增大。(e)双胞花粉晚期,淀粉等物质开始在细胞质中积累,但仍能看到两个核,液泡逐渐消失。(F)成熟花粉期,淀粉等物质充满整个细胞,细胞核难以观察到。英国石油(BP):双细胞的花粉;新兴市场:小孢子早期;GN:生殖细胞核;医生:生殖孔;LM:小孢子晚期;地图:成熟的花粉;MM:中间小孢子;助教:毯;泰德:毯碎片; VN: Vegetative nucleus.
‘Noa’、‘Qx-115’和‘Kingfisher’的小孢子发生和花粉发育
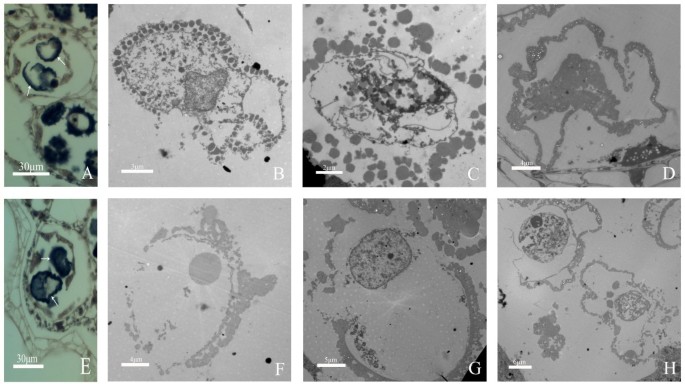
“NOA”,“QX-115”和“翠鸟”的微生物发生和花粉发育类似于“QX-097”。在“QX-097”的微孢子发生和花粉发育期间很少观察到异常,但“NOA”,“QX-115”和“翠鸟”的异常百分比高(图5和6;表格2).对于‘Noa’,四分体释放小孢子后,许多花粉粒夭折(图5啊)。同样,在'QX-115'的中间微孔阶段,花药中有许多破碎,不完全的花粉颗粒(图6A),小孢子后期完整花粉粒少(图6b)。因此,高比例花粉颗粒的退化可能是“NOA”和“QX-115”的花粉量低于“QX-097”(表)的主要原因1).对于‘翠鸟’来说,小孢子细胞减数分裂时期出现异常的比例很高,这是导致该品种花药中没有花粉粒的主要原因。例如,在二分体或四分体时期,花药小孢子囊内仅观察到少量二分体或四分体,大部分呈退化状态(图)6一部)。随后,在花药小孢子囊内未观察到花粉粒(图6F)。这里提出的结果表明,喷雾切割菊花的花粉量与微孢子发生和花粉发育期间的异常程度密切相关。
' Qx-097 '、' Noa '和' Qx-115 '花药开裂期间的雄蕊解剖
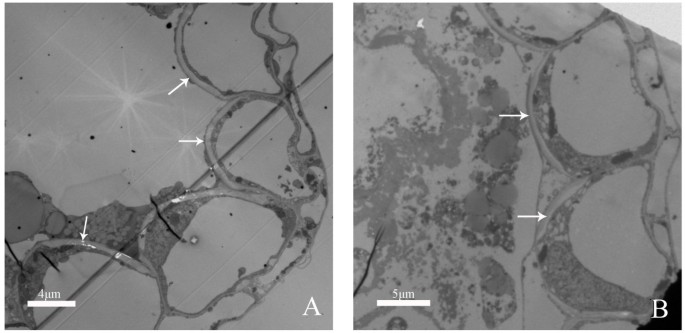
' Qx-097 '、' Noa '和' Qx-115 '的花粉散布能力差异很大(图5)7光学;表格2).‘Qx-097’主要在3个品种中具有最高的花粉散布能力,在花粉完全散布阶段花药小孢子囊内没有花粉粒残留(图)7‘Noa’具有较强的花粉传播能力,但其花粉传播能力不如‘Qx-097’,因为在花粉传播的全部阶段,仍有部分花粉粒残留在花药小孢子囊内(图1)7D-F,L&M)。'QX-115'没有花粉分散的能力,因为它未能分散任何花粉颗粒和花粉量,在整个开花过程中,花药的微孢子囊中没有太大变化(图7G-I, N & O), 3个品种的花粉扩散能力与花药开裂程度有关。花药开裂程度最高的是‘Qx-097’,其次是‘Noa’,而‘Qx-115’花药在花期后期不开裂且枯萎(图)7此外,透射电镜图像显示,在花粉发育后期,' Qx-097 '和' Noa '的内膜层细胞壁增厚,呈u形,开口向外切向壁方向(图)8A和B),可能是花药开裂的结构基础,并促进花药开裂。因此,花药开裂程度通过控制花粉扩散能力,是影响喷切菊花粉扩散量的主要因素之一。也就是说,花药开裂的程度与花粉的散布量呈正相关。例如,‘Qx-097’被认为是花粉传播能力强的品种,主要原因之一是该品种在开裂时花药开裂程度非常高(图)1G和H;表格1).“QX-115”是每花序超过一千千花粉的品种,但在花药期间不会分散任何花粉颗粒。主要原因是“QX-115”的麻木在裂开期间未能破裂并保持完整(图1K&L;表格1).
讨论
花粉是由植物雄蕊,花的雄性生殖器官生产,对开花植物的性繁殖非常重要[15,16].然而,花粉在花卉生产中往往是不受欢迎的,因为包括菊花在内的许多花卉的观赏价值通常会随着花粉散布量的增加而迅速下降[17,18].此外,花粉还可以在人们中产生各种过敏反应[5,6,19,20.].在本研究中,四个喷切花菊花品种在花粉散布量上存在很大差异。‘Qx-115’和‘翠鸟’是不分散花粉的品种,‘Qx-097’是花粉分散量高的品种,‘Noa’是花粉分散量少的品种(图)1、表1).呈现的结果表明,四个菊花品种中花粉分散量的大量差异主要是由于每次花序的两个因素,花粉量和花粉分散的能力。换句话说,花粉分散量通常与每花序的花粉量和花粉分散的能力呈正成比例。
喷切菊每花序花粉量由每花药花粉量和每花序花盘小花数共同决定,但每花药花粉量是主要影响因素。由于每个花序的花盘小花数量通常在100 - 200之间,而每个花药的花粉数量的范围更广,通常在0-1000之间1).有许多影响每种花粉量的因素。例如,花粉量在花粉中受到花粉囊的大小,微微孢子的母细胞,气候和营养条件的数量,以及培养和管理水平[15,21,22].刘等.[23]和晒黑等.[24]思想,花盆中的花粉数量还取决于花药是否正常地发展。在本研究中,我们对不同量的花粉分散进行了对4种品种的微生物发生和花粉发育,发现在“翠鸟”,“QX-115”和“NOA”中经常发生异常。例如,几乎所有的母细胞母细胞都在微孢子细胞减少阶段和不对称的二元阶段和鸟类的“翠鸟”中的母细胞,这是该品种花药的主要原因是不含任何花粉的主要原因。然而,在“QX-097”中,在“QX-097”中有很多在花粉中的花粉颗粒很少观察到异常的现象。因此,四个菊花品种花粉量差异的原因主要归因于微孢子发生和花粉发育期间发生的不同程度的异常。不同水平异常的可能原因是菊花的长期营养繁殖,主要是切割,导致染色体结构变异和异常分裂。在百合中也观察到类似的现象[25,26].
花粉散布能力是影响菊花花粉散布量的另一个重要因素,与花药开裂的速度和程度密切相关。花药开裂的速度是单位时间内花药开裂的程度。假设花药开裂程度越高,其花粉扩散能力越强。我们的结果证实了这一假设(表)1).例如,“QX-097”在四种品种之间具有最高程度的花药裂缝,并且其在花药中的花粉颗粒完全分散。“QX-115”不会分散任何花粉,因为它的花药根本不会破裂,尽管它的花粉包含了大量的花粉。'QX-115'中的花药异常破裂的原因可能是花粉流产引起的花药萎缩,该品种的花药壁没有适合于花药裂缝的特殊结构。对于'QX-097'和'NOA',内皮层中的细胞壁是'U'形状和增厚,但是可以促进花药裂开的裂缝,尽管两种品种之间的花药程度差异仍有进一步研究。
曾经被认为是一种简单的组织干燥过程[27,28].然而,许多研究表明,花药开裂是一个复杂的过程,不同种的调控机制不同[29- - - - - -33].例如,水通道蛋白,碳水化合物和k+已被报道通过调节细胞渗透势引起花药组织脱水而与花药开裂有关[34- - - - - -36].此外,花药开裂也受到茉莉酸等激素的调控[37,38],养蛋白[30.]和乙烯[39,40].主要调节模型是,当花药组织处于茉莉酸等调节时,在适当的时刻,花粉晶粒和隔膜脱水,然后k+和碳水化合物等次级代谢产物进入花粉晶粒并导致他们的快速膨胀,在水通道蛋白的帮助下产生对浮雕的压力。同时,乙烯等激素通过酶水解促进剧剧细胞破裂,以终于裂解花药[29,31,33,41].例如,砂光机et al。[42]和唠叨et al。[43发现花了拟南芥花药开裂缺陷的突变体经外源茉莉酸和生长素处理后能够开放。然而,我们的结果(数据未显示)表明,外源茉莉酸甲酯处理不能加速花药开裂不完全的‘Noa’和花药未开裂的‘Qx-115’的花药开裂,说明茉莉酸可能不是影响菊花花药开裂的主要因素。此外,高温等外部环境因素有时也会降低花药开裂的程度[44,45].
结论
总之,我们在这里进行了系统的研究,以研究具有不同量花粉分散的四种喷雾切割菊花品种花粉分散量的因素。三个研究结果值得注意。首先,喷雾切割菊花中的花粉分散量主要由花粉量和花粉分散的容量决定。其次,四种菊花品种中每个花粉量的显着差异主要是由于在微生物发生和花粉发育过程中发生的异常发生的显着差异。第三,花粉分散能力与花药裂开程度密切相关。这些重要调查结果将为在菊花的未来繁殖项目中较少或没有花粉散,甚至是其他作物的花粉分散,尽管花粉流产和口腔异常破裂的潜在机制仍有进一步调查。
参考
- 1.
李hj:中国的菊花。南京:江苏科技专业;1993年。
- 2.
安德森不:菊花(dendranthema.×GrandifloraTzvelv)。花卉繁殖和遗传学。编辑:安德森没有。荷兰:Springer;2007:389-437。
- 3.
陈丽:国际菊花市场研究与分析。草业学报。2005,8:20-22。
- 4.
李毅,方文,陈FD,陈SM,Shi Cl:不同种植日对夏季生产喷雾切割菊花的磷酸质量和品质的影响。作者:王莹,扬州大学学报(农业科学版)JOURNAL。2009,30(3):80-83。
- 5.
Groenewoud GC,De Jong NW,Burdorf A,De Groot H,VanWÿkRG:荷兰温室的山脉花粉的职业过热普遍存在。过敏。2002,57(9):835-840。10.1034 / J.1398-9995.2002.23725.x。
- 6。
李永文,崔淑英,李立宏,孙宗辉,朴jw,洪洪志:菊科植物蒿属花粉的交叉过敏原性研究,dendranthema grandiflorum和蒲公英officinale.陈建平,王志强,王志强,等。10.1016 / s1081 - 1206(10) 60382 - 1。
- 7。
杨宇强,郭志林:家用花卉对室内空气污染的正、负影响。环境科学与管理,2009,34(5):31-33。42
- 8。
Chan Ryc,Oppenheimer JJ:由秘鲁百合引起的职业过敏(陌生统计学).陈建平。过敏性哮喘病的免疫学研究进展[j] .中华结核和呼吸杂志,2002,28(6):638-639。10.1016 / s1081 - 1206(10) 61897 - 2。
- 9。
Hoidn C,Puchner E,Pertl H,Holztrattner E,Obermeyer G:Nondiffusional释放花粉粒的过敏原Artemisia寻常型和百合longiflorum这主要取决于过敏原的类型。国际过敏症免疫杂志。2005,37(3):27-36。
- 10.
李XX,易MF:百合雄性不育的研究进展。西宁:中国对花灯泡的年度审查;2010年。
- 11.
孙长青,黄志忠,王玉玲,陈福德,滕乃杰,方文敏,刘志林:利用特殊授粉技术克服菊花宽交受精前的障碍。植物学报,2011,33(4):457 - 461。10.1007 / s10681 - 010 - 0297 - 6。
- 12.
滕妮,王烨,孙CQ,方武器,陈FD:影响水莲花实验十字架繁殖力的因素(莲属椰子盖恩。)品种。BMC植物BIOL。2012,12:82-10.1186 / 1471-2229-12-82。
- 13.
滕妮,王家,陈涛,吴昕,王毅,林爵士:升高有限公司2诱导植物叶片的生理生化和结构变化拟南芥蒂利亚纳.新植物。2006,172:92-103。10.1111 / J.1469-8137.2006.01818.X。
- 14.
金波,王丽,王杰,姜克忠,王勇,姜晓星,倪春英,王玉兰,滕乃杰:试验增温对小麦叶片功能性状、叶片结构和生物化学的影响拟南芥蒂利亚纳.植物营养与肥料学报。2011,11:35-10.1186/1471-2229-11-35。
- 15.
胡思远:被子植物的生殖生物学。北京:高等教育出版社;2005。
- 16。
Franklin-Tong VE:开花植物中的自我兼容 - 进化,多样性和机制。柏林海德堡:斯普林克 - 威尔拉格州;2008年。
- 17。
陈杰:中国花卉品种分类系统。北京:ChinaForestry Press;2001:218-231。
- 18。
金B,王L,王J,腾NJ,他XD,MU XJ,王YL:无菌花的结构和角色荚虫猕猴F。keteleeri(亚昔昔糖)。植物BIOL。2010,12:853-862。10.1111 / J.1438-8677.2009.00298.x。
- 19。
Ziello C,火花,爱丝特雷娜N, Belmonte J,伯格曼KC,布赫E, Brighetti MA Damialis, Detandt M•C,伽R, Grewling L,古铁雷斯Bustillo, Hallsdottir M, Kockhans-Bieda MC,利纳雷斯CD, Myszkowska D, Paldy,桑切斯,史密斯M, Thibaudon M, Travaglini, Uruska, Valencia-Barrera RM, Vokou D,韦希特尔R,门泽尔:欧洲空气中花粉计数的变化。PLoS ONE。acta physica sinica, 2012, 32(4): 489 - 494。
- 20。
德容NW, Vermeulen AM, Gerth van Wijk R, de Groot H:花卉引起的职业性过敏。中国生物医学工程学报。1998,53(2):204-209。10.1111 / j.1398-9995.1998.tb03872.x。
- 21.
孟JL:植物生殖遗传学。北京:科学出版社;1997。
- 22.
中GB,方WM,佳SZ,陈FD:调查花粉粒量和花粉在体外萌发特征李春万.上海农业学报,2007,23:42-46。
- 23.
刘振华,何茂明,钟飞:梨花粉量的测定与分析。甘肃林业科技。2003,28:34-35。54.
- 24.
Tan JM,CEN XF,WEI PX,MA XJ,MO CM:研究不同杂交线的花粉量和发芽能力罗汉果.桂花。2009,29:881-884。
- 25.
李旭,陈明敏,杜军,梁文峰,邢海涛:云南花粉病花粉母细胞减数分裂异常的观察Lilium Davidii.var。单色的.西北植物学报,2003,23:1796-1799。
- 26.
张CX,明J,Liu C,Li BS:在东方杂交种百合西伯利亚花粉母细胞减数分子行为异常现象的分析与观察。公牛生物学。2010年,45:45-48。
- 27.
Keijzer CJ:花药裂开和花粉分散的过程。I.纵向裂缝的观点的开放机制。新植物。1987,105:487-498。10.1111 / j.1469-8137.1987.tb00886.x。
- 28。
BONNER JL,DICKINSON HG:花药裂开Lycopersicon esculentum磨。I.结构方面。新植物。1989,113:97-115。10.1111 / J.1469-8137.1989.TB02399.x。
- 29。
华SJ,孟赫伯,王XD,江吕克:植物特性和分子机制的植物花药裂开。Chin J细胞BIOL。2007,29:389-393。
- 30.
Cecchetti V, Altamura MM, Falasca G, Costantino P, cararelli M:生长素调节拟南芥花药裂开,花粉成熟和长丝伸长。植物细胞。2008,20(7):1760-1774。10.1105 / TPC.107.057570。
- 31。
杨志强,宋建平,杨志强:花药分裂的调控机制。中国生物医学工程学报。2011,32(5):633- 649。10.1093 / jxb / err014。
- 32。
周SR,王Y,李WC,赵ZG,任YL,王Y,顾SH,林QB,王D, L, N,张X,刘会,Cheng ZJ Lei CL,王莱托,郭XP,吴FQ Ikehashi H,王HY, Wan JM:花粉蛋白质kinesin-1-like semi-sterility1重要男性减数分裂,花药裂开,在水稻生育。acta botanica sinica, 2011, 32(6): 754 - 754。10.1105 / tpc.109.073692。
- 33.
Nelson MR, Band LR, Dyson RJ, Lessinnes T, Wells DM, Yang C, Everitt NM, Jensen OE, Wilson ZA:花药开放的生物力学模型揭示了脱水和二次增厚的作用。植物学报,2012,196(4):1030-1037。10.1111 / j.1469-8137.2012.04329.x。
- 34.
BOTS M,Vergeldt F,Wolters-arts M,Wettersings K,Van-As H,Mariani C:PIP2类的Aquaporins需要在烟草中有效的花药脱落所必需的。植物理性。2005,137:1049-1056。10.1104 / pp.104.056408。
- 35.
Rehman S,Yun SJ:花粉,花药和乳头的K积累的发育调节:花药裂缝,乳头水合和花粉肿胀,导致大麦授粉和施肥(Hordeum Vulgare.L.)受K浓度的变化进行调节吗?J Exp Bot。2006,57:1315-1321。10.1093 / JXB / ERJ106。
- 36.
Castro AJ,ClémentC:在其开发期间,植物中的蔗糖和淀粉分解代谢物:花药壁,小型液和微孔/花粉级分的比较研究。Planta。2007,225(6):1573-1582。10.1007 / s00425-006-0443-5。
- 37.
关键词:拟南芥,同源性蛋白AGAMOUS,茉莉酸生物合成基因,雄蕊发育植物学报。2007,19(11):3516-3529。10.1105 / tpc.107.055467。
- 38.
叶青,朱伟,李丽,张树华,尹勇,马辉,王旭:油菜素内酯通过调控拟南芥花药和花粉发育关键基因的表达调控雄性育性。美国国家科学院学报。系统工程理论与实践,2016,35(4):527 - 534。10.1073 / pnas.0912333107。
- 39.
Rieu I,Wolters-Arts M,Derksen J,Mariani C,Wettersings K:乙烯调节烟草中花药裂缝的时机。Planta。2003,217:131-137。
- 40。
王Y,Kumar PP:来自Petunia的两个乙烯受体Phers1和Phetr2的表征:PHET2调节花药裂缝的时序。J Exp Bot。2007,58:533-544。
- 41。
Matsui T,Omasa K,Horie T:水稻花药裂缝机制(栽培稻L.)。Ann Bot。1999,84(4):501-506。10.1006 / anbbo.1999.0943。
- 42。
桑德斯首相,Lee PY, Biesgen C, Boone JD, Beals TP, Weiler EW, Goldberg RB: The拟南芥延迟Dehiscence1基因编码茉莉酸合成途径中的酶。植物细胞。2000,12:1041-1061。
- 43。
Nagpal P,Ellis Cm,Weber H,Ploense Se,Barkawi LS,Guilfoyle TJ,Hagen G,Alonso JM,Cohen JD,Farmer EE,Ecker JR,Reed JW:Auxin响应因子ARF6和ARF8促进茉莉酸生产和花卉成熟。发展。2005,132:4107-4018。10.1242 / dev.01955。
- 44。
Matsui T,Omasa K,Horie T:在开花的高温抑制花粉粒肿胀,在水稻中的脑裂解的驱动力(奥雅萨苜蓿植物科学进展。2000,3:430-434。10.1626 / pps.3.430。
- 45.
李WB,王H,悬挂FS:硅对高温胁迫下水稻花药裂开和花粉的影响。Acta Agron Sin。2005,31:134-136。
确认
非常感谢BMC《植物生物学》杂志指派的两位匿名审稿人对我们的稿件进行了认真的审核,并提出了许多宝贵的建议和意见。我们还要感谢中国科学院植物研究所穆锡金教授在这些实验的早期阶段所作的宝贵讨论。教育部新世纪优秀人才支持计划项目(no . NCET-11-0669);国家自然科学基金项目(no . 31171983);中央高校基本科研业务费专项资金(no . KYZ201308, no . KYZ201147);青年科技创新基金(KJ2011009)。
作者信息
隶属关系
通讯作者
附加信息
相互竞争的利益
作者声明他们没有竞争利益。
作者的贡献
NJT、XGW、FDC、JFJ和WMF设计了实验。NJT、XGW、HBW和YL进行了实验。NJT、XGW、FDC、JFJ分析数据并撰写稿件。NJT和XGW对稿件进行了修改。所有作者阅读并批准了最终的手稿。
作者的原始提交的图像文件
下面是作者提交的原始图片文件的链接。
权利和权限
开放获取本文在“生物资源”中央有限公司的许可下公布了这是一个开放式访问条款,分配根据创意公约归因许可证的条款(https://creativecommons.org/licenses/by/2.0.),允许在任何媒介上无限制地使用、分发和复制,但必须正确引用原作。
关于这篇文章
引用这篇文章
王,xg。,王,hb。,陈,fd。et al。影响喷雾切割菊花花粉分散量的因素(菊花莫瑞菊).BMC植物杂志14,5(2014)。https://doi.org/10.1186/1471-2229-14-5
已收到:
接受:
发表:
关键字
- 花粉开发
- 花粉传播
- Tapetal Cell.
- 花瓶的生活
- 小孢子母细胞