摘要
背景
大豆是最重要的油料作物之一。与石油积累有关的调控基因在很大程度上还不清楚。我们开始研究,以确定调节这一过程的基因。
结果
一个MYB-type基因GmMYB73通过微阵列分析发现其在大豆不同发育阶段种子中的表达存在差异,并进一步研究其在脂质积累中的作用。GmMYB73是一个具有单一MYB重复序列的小蛋白,与拟南芥中的CPC-like MYB蛋白有相似之处。GmMYB73与GL3和EGL3相互作用后被抑制GL2,是油积累的负调节因子。GmMYB73转基因拟南芥种子和叶片的脂质含量均有显著提高。种子长度和千粒重也有促进作用。GmMYB73拟南芥引种试着中国共产党双突变体挽救了总脂质、种子大小和千粒重。GmMYB73转基因莲花的种子和叶片以及转基因大豆毛状根中的脂质水平也有所升高。GmMYB73提升骑士α1其启动子可被GL2结合和抑制。骑士α1突变使拟南芥种子中三酰甘油含量轻度降低,但在叶片中显著降低。
结论
GmMYB73可能会减少GL2,然后释放抑制gl2骑士α1脂质堆积表达。操纵GmMYB73可能潜在地提高豆科作物的油料产量。
背景
大豆油作为一种重要的油料作物,为满足日益增长的需求,提供食用、工业和新能源用油[1,2].不同品种大豆种子含油量一般在13% - 22%之间,与大多数其他油籽作物相比,含油量相对较低[3.].因此,大豆种子含油量高是很有必要的,也是育种和基因工程的主要目标。
大多数种子的贮藏化合物由碳水化合物、油和贮藏蛋白质组成,这些化合物占种子干重的90%或更多。脂肪酸以三酰甘油(TAGs)的形式储存在种子中[4,5].TAG代谢的调控涉及两个机制。一种是基于底物有效性、变构效应剂和/或酶修饰的短期调节。另一种调节脂质生物合成的方法是通过控制酶的合成和周转率。这些目标是通过直接修饰脂肪酸生物合成酶来改变特定天然脂肪酸的相对数量,以生产新的脂肪酸或设计脂肪酸链的长度[6- - - - - -9].几份报告揭示了关键酶,如乙酰辅酶a羧化酶(ACCase)和双甘油酯酰基转移酶(DGAT)的过表达或修饰会改变种子油的积累[10- - - - - -13].
除了在脂质代谢途径的关键酶和主要步骤上的调控外,脂肪酸和脂质的积累也在转录水平上受到调控。通过对拟南芥突变体的筛选,发现了一些转录因子是种子油含量的主要调控因子LEC1, LEC2而且WRI1[14- - - - - -17].调控转录因子可调节脂肪酸生物合成中的基因表达,改变脂肪酸/油的水平[18- - - - - -23].其他种子特异性转录因子也可能在调节油脂积累中起作用[24- - - - - -26].储存的脂质积累可能被新的转录因子、激酶/磷酸酶和/或参与RNA调节的蛋白质进一步调节[27- - - - - -31].此外,新策略已被开发出来,通过过量生产用于油生物合成的WRI1,同时减少淀粉生物合成,以增加油的含量[32].
MYB蛋白在植物生长、发育以及对生物和非生物因子的响应等多个方面发挥着重要作用[33- - - - - -36].MYB蛋白可分为三种类型:具有两个重复序列的r2r3型MYB,具有三个重复序列的r1r2r3型MYB,以及在植物中通常含有单重复或非典型重复的第三种类型。中国共产党例如(反复无常)基因家族编码具有单一MYB基序的小蛋白,并负调控植物毛状体的发育拟南芥.7个cpc样蛋白已被鉴定拟南芥,包括中国共产党[37),试一试[38].
之前,我们研究了大豆转录因子,并分析了它们在非生物胁迫耐受中的作用[35,39- - - - - -42].三个MYB基因GmMYB76,GmMYB92而且GmMYB177已发现在转基因植物的抗胁迫能力中发挥不同的作用[35].我们还发现了两个大豆转录因子基因GmDof4而且GmDof11通过直接与启动子区结合,上调脂类生物合成相关基因,下调存储蛋白基因,从而提高转基因拟南芥植物种子中的脂类含量[43].可能有更多的因子参与大豆植物脂质合成的调控。
为了寻找可能调控种子发育过程中脂肪酸积累的新基因,利用大豆发育过程中不同阶段和一系列差异表达的种子rna进行了微阵列分析MYB选择基因并对其功能进行表征[44].在九MYB基因分析,只GmMYB73,一个编码单一MYB重复序列蛋白质的基因改变了转基因拟南芥种子中的脂质含量[44].由于该基因具有增加脂质水平的潜在能力,因此对其进行了详细的研究。过度的GmMYB73提高了转基因拟南芥和转基因莲藕种子和叶片的含油量,提高了转基因大豆毛状根的含油量。这些功能可能是通过GmMYB73与GL3/EGL3相互作用,抑制GL2和激活的骑士α1.
结果
GmMYB73基因表达
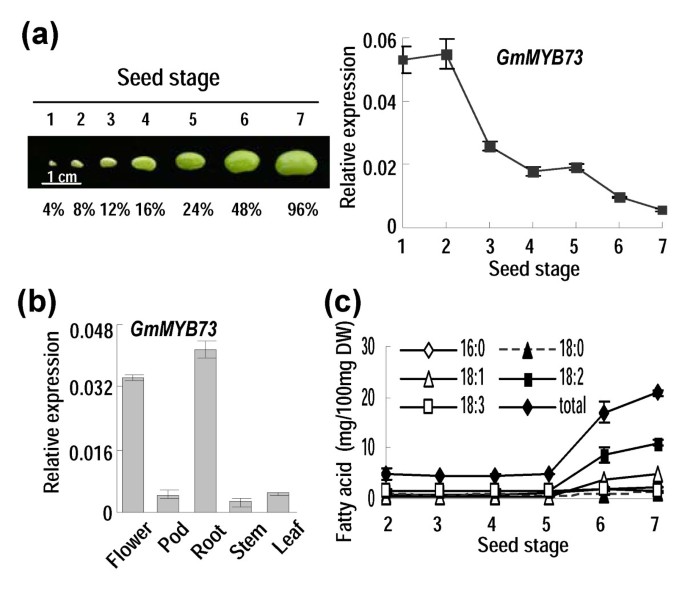
将发育中的大豆种子从授粉到成熟分为7个阶段,与未脱水的正常种子相比,每个阶段的相对种子重在4% ~ 96%之间(图1)1一个,左面板)。的表达GmMYB73用定量PCR方法对该阶段种子中编码73个MYB重复序列的蛋白(DQ822927)进行了分析。的GmMYB73基因最初是通过微阵列分析从不同发育阶段的种子中提取的rna识别出来的[44].GmMYB73在种子发育的第二阶段之后,表达量急剧下降,当种子接近完全大小时,表达量达到最低水平(图1)1一个,右面板)。的GmMYB73在大豆的不同器官中也检测到了表达,在花和根中观察到相对较高的表达水平,而在荚果(第5期)、茎或叶中没有(图1b)。
测定了发育中的大豆种子的脂肪酸水平,在第五个阶段之后,总脂肪酸和组成发生了显著变化(图1c)。
转基因拟南芥过表达植株的表型GmMYB73
研究GmMYB73功能,我们生成了构造港GmMYB73通过CaMV 35S启动子控制pPROK II载体,并利用农杆菌介导的花浸转化方法将该基因转化到拟南芥植株中。GmMYB73表达式被检查(附加文件1对纯合子转基因株系(OE-1、2、5、7和10)和植株表型进行了研究。
所有转基因系表达GmMYB73与Col-0相比,几乎没有毛状体(附加文件1),这表明GmMYB73抑制毛状体的形成。进行了系统发育分析,比较GmMYB73与其他拟南芥MYB蛋白参与毛状体形成的关系1).GmMYB73与拟南芥中具有单一MYB重复序列的7个CAPRICE (CPC)样蛋白聚类,包括CPC [37], [38, TCL1, TCL2, ETC1, ETC2和CPL3。的GmMYB73过表达线OE-5被交叉试着中国共产党双突变体,具有明显的簇状毛体(附加文件1) [45].毛状体的形成试着中国共产党含有纯合子的突变体GmMYB73转基因产品(尝试cpc / GmMYB73)在叶和茎中均被抑制,与GmMYB73 -过度表达的植物(附加文件1).这些结果表明,GmMYB73是CPC和TRY的同源物,参与了毛状体的形成。GmMYB172 (DQ822946)和GmMYB363 (FJ555058)是大豆中GmMYB73的近亲同系物1).
GmMYB73与GL3和EGL3结合并抑制GL2表达式
在拟南芥中,中国共产党-如R3 MYB蛋白(如TRY和CPC)是转录激活因子的阻遏因子,并与GL1 (R2R3-MYB因子)竞争与GL3和EGL3结合,两者都是bHLH因子[46,47].当与GL3和EGL3结合时,GL3/EGL3/GL1/TTG1 (WD40蛋白)转录复合体的形成被阻断,从而GL2同源域转录因子的转录被抑制。最后,毛状体的形成受到抑制。38,46,47].GL2突变导致拟南芥种子中油脂积累增强[18,23].我们还发现,在酵母双杂交试验中,GL3和EGL3都可以与GmMYB73相互作用(图2a).此外,通过BiFC检测在拟南芥原生质体中确认了这些相互作用,如细胞核和细胞质中的黄色荧光所示(图2b).这些结果表明GmMYB73可以与GL3和EGL3相互作用。
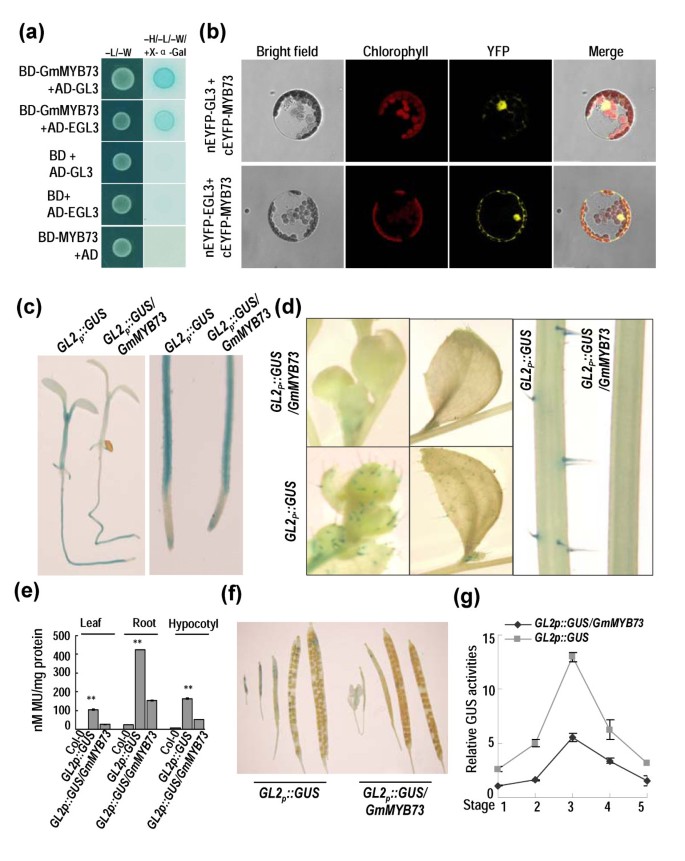
GmMYB73与GL3和EGL3相互作用并抑制GL2表达式。(一)酵母双杂交试验中GmMYB73与GL3和EGL3的相互作用。酵母转化菌在对照SD/ -Leu / -Trp(左列)和选择培养基SD/ -Ade / -His / -Leu / -Trp(右列)和X-a-Gal和Aureobasidin A(右列)中培养。细胞生长和选择培养基上的蓝色表明细胞间存在正相互作用。其他组合作为阴性对照。(b)利用BiFC检测拟南芥原生质体中GmMYB73与GL3或EGL3的相互作用。YFP中的黄色荧光表示正相互作用。(c)GL2启动子活性被抑制GmMYB73在地上部分,但在根部分被抑制。左:全苗GUS染色;右图:根内GUS染色。(d)cGmMYB73镇压GL2花芽萼片(左)、叶片(中)和茎(右)上的启动子活性和毛状体的形成。(e)GL2转基因植物的叶片、根系和下胚轴中的GUS活性表明GmMYB73抑制了启动子活性。**表示与Col-0水平有显著差异(P < 0.01)。(f)GmMYB73抑制GL2GUS染色显示,启动子在角果发育过程中的活性。(g)GmMYB73抑制GL2启动子活性,从相对GUS活性显示。第1阶段的GUS活性GL2p:格斯/ GmMBY73设置为1,并将所有其他值与之进行比较。这5个阶段与植株的角果表型相对应(f)分别。
确定GmMYB73是否影响GL2表达,转基因拟南芥植物港湾GL2发起人::格斯(GL2p::格斯) [48]与过度表达的转基因植物杂交GmMYB73(OE-5)植株,并在纯合子中进行GUS染色GL2p::格斯/ GmMYB73转基因植物。在GL2p::格斯植物,在花芽、叶和茎的下胚轴、根、茎尖和毛状体中观察到GUS染色2c, d)。GmMYB73对下胚轴和茎尖GUS染色有强烈抑制作用GL2p::格斯/ GmMYB73植物(图2c).这些植物的花蕾、叶和茎中几乎检测不到毛状体和GUS染色(图2d).根中GUS染色仅部分被抑制GL2p::格斯/ GmMYB73植物(图2c).在上述转基因植物的叶片、下胚轴和根中也定量检测了GUS活性,其水平与GUS染色结果一致(图2c, d, e)。这些结果表明,GmMYB73通过与GL3和EGL3相互作用来抑制表毛体的形成GL2转基因拟南芥植物的转录。
角果发育的五个阶段GL2p::格斯而且GL2p::格斯/ GmMYB73我们发现,在发育中的角果中,GUS染色逐渐减少GL2p::格斯植物(图2f)。GmMYB73部分抑制了水稻角果的GUS染色和GUS活性GL2p::格斯/ GmMYB73植物(图2f, g)。这些结果表明,GmMYB73抑制GL2发育中的角果启动子活性。
过度的GmMYB73提高种子大小和千粒重
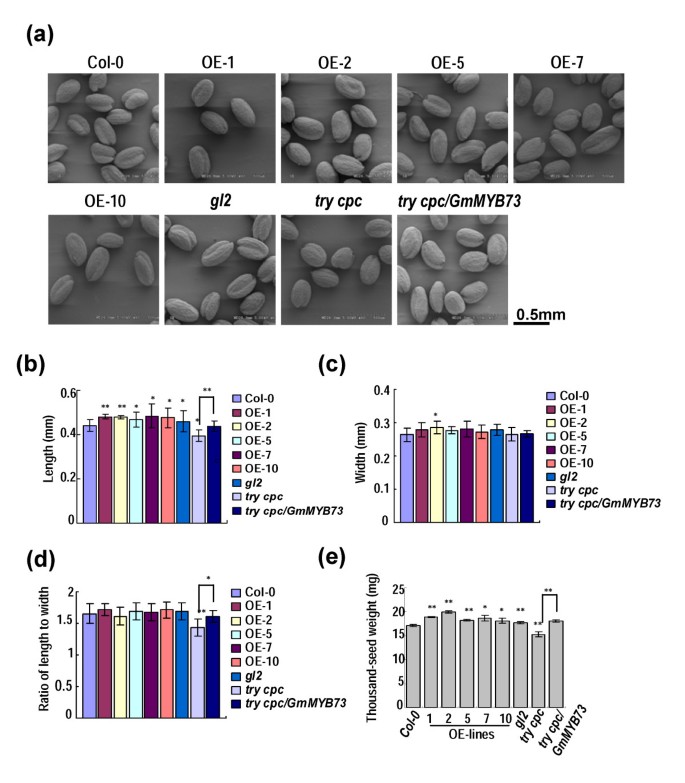
GmMYB73表达在大豆种子发育的不同阶段发生变化(图1)和影响GL2在转基因植物角果中的表达(图2f, g)。然后我们检测种子大小是否在GmMYB73-overexpressing植物。在扫描电子显微镜下,我们发现试着中国共产党与Col-0相比,双突变体的种子更小GmMYB73转基因植物和gl2-2突变体似乎有更大的种子(图3.a).进一步测量种子大小显示,种子长度,而不是种子宽度,显著增加GmMYB73-overexpressing植物和gl2与Col-0相比突变(图3.b, c)。这些植物的种子长宽比没有显著变化(图3.d).种子长度和长宽比显著降低,而种子宽度不显著降低试着中国共产党与Col-0相比是双突变体(图3.b, c, d).介绍GmMYB73变成双突变体试着中国共产党拯救了种子的长度和长宽比(图3.b, d).这些结果表明GmMYB73可能还有它的同系物试一试而且中国共产党影响种子发育和种子大小。
GmMYB73过表达控制转基因拟南芥种子大小和千粒重。(一)拟南芥种子的扫描电镜形态。的种子GmMYB73-过表达拟南芥植物(OE),gl2-2,试着中国共产党和尝试cpc / GmMYB73行。(b)不同植物种子长度的比较。误差条表示SD (n = 20 ~ 30)。的值尝试cpc / GmMYB73线只是与来自的比较试着中国共产党突变体。列上方的' ** '和' * '分别表示与Col-0或在P < 0.01和P < 0.05时差异显著。(c)拟南芥不同品系种子宽度的比较。其他的则是(b).(d)种子长宽比的比较。其他的则是(b).(e)拟南芥各株系千粒重比较。误差条表示SD (n = 4)。其他的则是(b).
还测量了数千粒种子的重量GmMYB73-过表达系的千粒重明显高于Col-0(图1)3.e)。gl2种子的这一参数水平也略高,但显著高于其他种子3.相比之下,e)。试着中国共产党双突变体的千粒重明显低于Col和引种GmMYB73恢复的水平尝试cpc / GmMYB73植物(图3.e).这些结果表明,GmMYB73及其同系物TRY、CPC和GL2调控种子发育。
GmMYB73增加转基因拟南芥和莲藕种子和叶片的脂质含量,以及大豆转基因毛状根的脂质含量
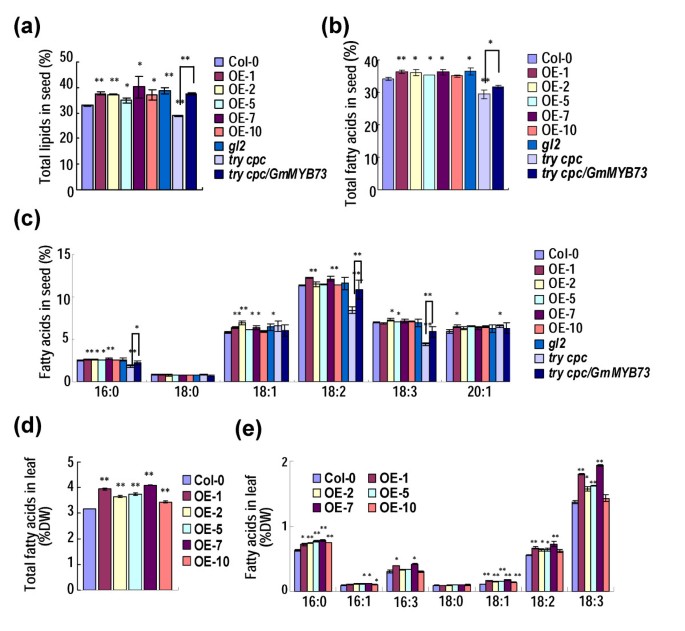
col0种子总脂质含量,GmMYB73-过表达系(OE-1, -2, -5, -7和-10)和各种突变系测定。所有五个GmMYB73转基因线和gl2突变体的总脂质水平高于Col-0,增加范围为5.9% ~ 17.9%(图4一个)。试着中国共产党突变体的脂质含量低于col0和col0GmMYB73转化增加了脂质含量尝试cpc / GmMYB73植株与双突变体的比较(图4a).总脂肪酸含量GmMYB73 -转基因线和gl2突变体与Col-0相比也有所增加(图4b).总脂肪酸试着中国共产党对突变体进行了还原和导入GmMYB73在突变体中,总脂肪酸含量基本恢复到WT水平(图4b).在脂肪酸组成方面,除18:0外,其余脂肪酸的含量略有增加或无显著变化GmMYB73转基因线和gl2与Col-0相比突变(图4c)。试着中国共产党突变体种子的3种脂肪酸(16:0,18:2,18:3)含量均较Col-0显著降低,并有部分挽救作用GmMYB73表达式(图4c)。
GmMYB73增加转基因拟南芥植物种子和叶片中的脂质含量。(一)油菜籽粒总脂质含量GmMYB73-转基因植物(OE-1, 2, 5, 7, 10)gl2-2,试着中国共产党,尝试cpc / GmMYB73.误差条表示SD (n = 4),数值为种子干重。的值尝试cpc / GmMYB73线只是与那些从试着中国共产党突变体。星号表示与Col-0或两组间差异显著(*P < 0.05和**P < 0.01)。(b)各种植物种子中总脂肪酸的含量。误差条表示SD (n = 4)。其他的则是(一).(c)各种植物种子中脂肪酸的组成。误差条表示SD (n = 4)。其他的则是(一).(d)植物叶片中的总脂肪酸。误差条表示SD (n = 4),数值为干重。其他的则是(一).(e)植物叶片中脂肪酸的组成。误差条表示SD (n = 4),数值为干重。其他的则是(一).
测定了不同植物品系叶片中的脂肪酸含量。GmMYB73-过表达系叶片总脂肪酸含量显著高于col04d).除18:0外,转基因株系中各脂肪酸组分的含量均较Col-0显著或略有增加(图1)4e).这些结果表明GmMYB73转基因拟南芥种子和叶片中总脂类和总脂肪酸含量增加。
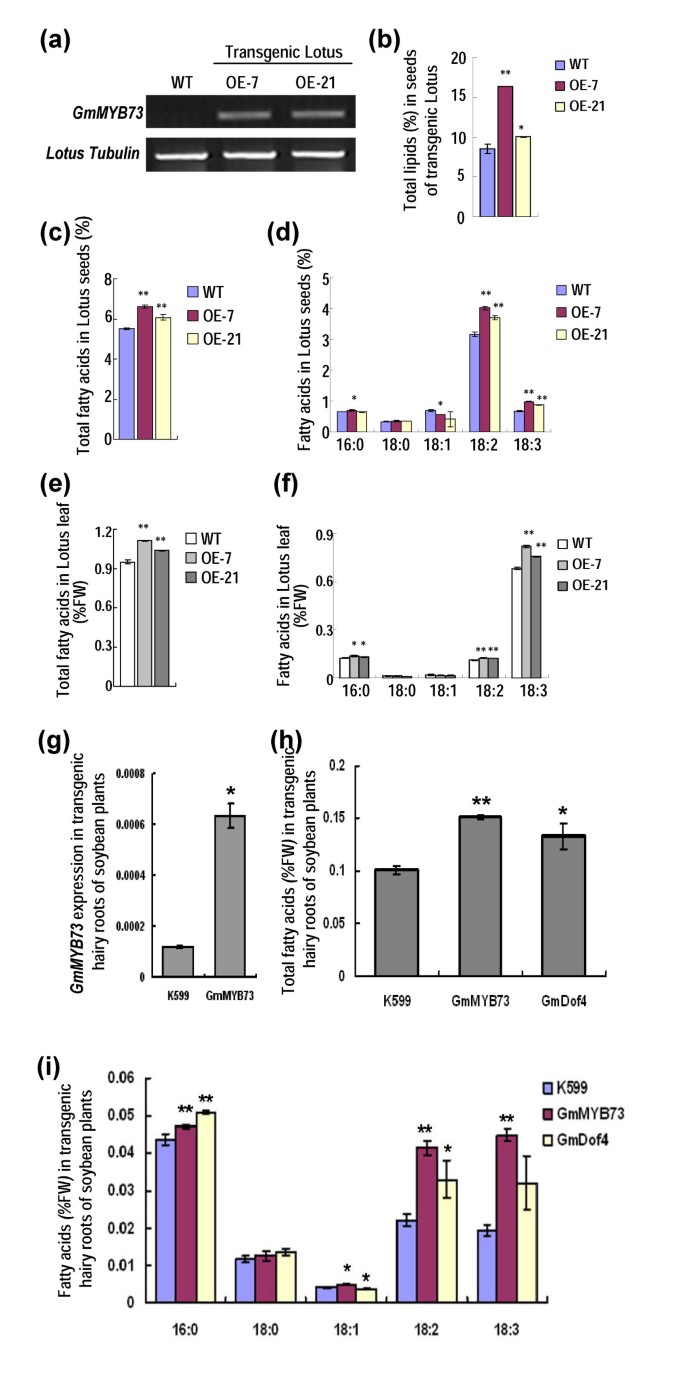
大豆是一种豆科植物,我们进一步改造GmMYB73变成豆科植物莲藕(Leo)。鉴定出两个转基因系,并均进行了展示GmMYB73与WT的比较(图5a).与WT相比,两个品系种子中总脂和总脂肪酸显著增加(图5b, c)。在脂肪酸组成方面,只有两种脂肪酸(18:2和18:3)在转基因种子中显著增加(图5d).我们还检测了转基因植株叶片中的脂肪酸水平,发现总脂肪酸和3种脂肪酸(16:0、18:2和18:3)明显增强(图5e, f).这些结果表明GmMYB73增加莲子转基因植株种子和叶片中总脂和总脂肪酸的含量。
GmMYB73提高转基因莲藕种子和叶片的脂质含量,以及大豆转基因毛状根的脂质含量。(一)GmMYB73在转基因莲花植株叶片中的表达。使用了OE-7和OE-21两条线。微管蛋白基因扩增作为对照。(b)转基因种子中总脂含量与WT的比较。误差条为SD (n = 4),数值为干重。星号表示与WT相比差异显著(**P < 0.01, *P < 0.05)。(c)转基因种子中总脂肪酸含量。误差条表示SD (n = 4),其他为(b).(d)转基因种子中各脂肪酸组成的含量。其他的则是(b).(e)转基因莲花植株叶片总脂肪酸含量的研究。数值以鲜重计算。其他如(b)。(f)转基因莲花植株叶片中各脂肪酸含量。数值以鲜重计算。其他的则是(b).(g)GmMYB73大豆转基因毛状根的表达。K599:控制的根源。GmMYB73:GmMYB73转基因毛状根。误差条表示SD (n = 4)。星号表示与对照K599差异显著(*P < 0.05)。(h)总脂肪酸水平GmMYB73转基因毛状根。K599:控制的根源。GmMYB73:GmMYB73转基因毛状根。GmDof4:GmDof4-转基因毛状根作为脂质积累的阳性对照。误差条表示SD (n = 4)。数值以鲜重计算。星号表示与对照K599比较差异显著(**P < 0.01, *P < 0.05)。(我)每一种脂肪酸成分的含量GmMYB73转基因毛状根。数值以鲜重计算。其他迹象如(h).
考虑到GmMYB73进一步研究了GmMYB73是否能提高转基因大豆植株毛状根中的脂质积累。的GmMYB73将-过表达载体转染到发根农杆菌菌株K599中,用该菌株通过注射感染大豆幼苗下胚轴。GmMYB73表达要高得多GmMYB73-转基因毛状根(GmMYB73)比K599再生根(K599)要好(图5g).总脂肪酸和三种脂肪酸(16:0,18:2和18:3)的水平在GmMYB73-转基因毛状根与对照K599根的比较(图5h, i)。GmDof4,在我们之前的研究中,该基因增强了转基因拟南芥植物的脂质水平[43],还能增加转基因大豆植物毛状根中的脂肪酸含量(图5h, i)。
GmMYB73增强了骑士α1哪些启动子可以被GL2结合
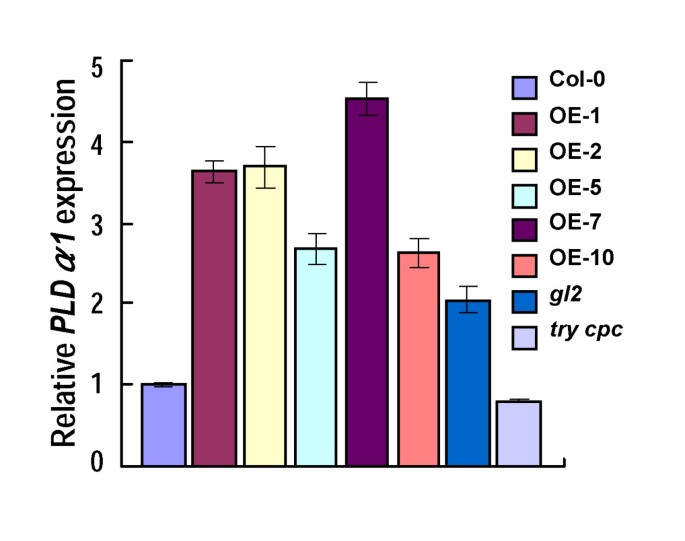
GmMYB73抑制GL2表达式(图2).的种子GmMYB73-overexpressing植物和gl2突变体积累了更多的脂类和脂肪酸(图4).我们检测了GmMYB73是否通过抑制GL2.GL2突变导致种子含油量增加[18].GL2抑制磷脂酶D ζ相1 (PLDZ1)基因表达[49].pld影响脂质组成[50- - - - - -52].然而,种子含油量的增加gl2变种是不因的PLDZ1或PLDZ2表达式[23].我们发现骑士α1在叶片中上调GmMYB73-overexpressing植物和gl2突变体,但抑制在试着中国共产党与Col-0相比(图6).这些结果表明,GmMYB73可能抑制GL2,从而激活骑士α1表达式。
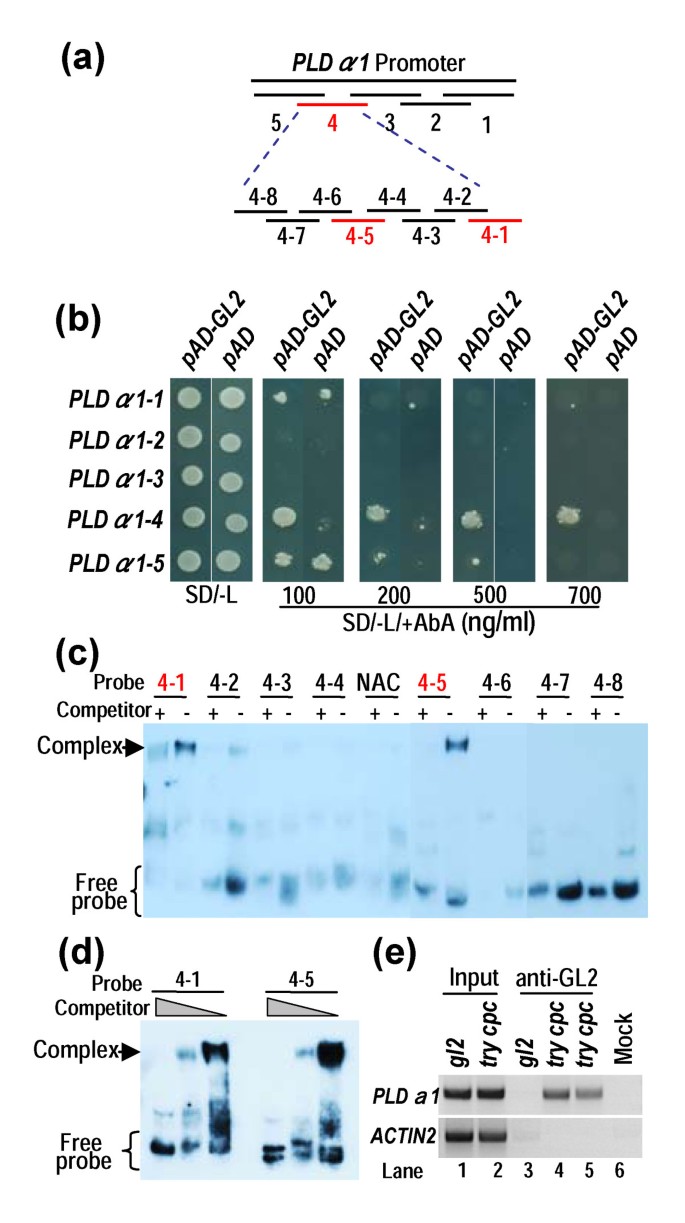
我们进一步研究了骑士α1在酵母单杂交试验中,启动子可被GL2结合。五个重叠的DNA片段(1:-1到-263;2: -246 ~ -492;3: -472到-753;4: -739到-1038;5: -1021 ~ -1328)骑士α1检测GL2结合的启动子(图7)。只有片段骑士α1 - 4是被GL2结合的,这是由含有pAD-GL2和pAbAi-骑士α1 - 4在选择介质SD/-Leu/+AbA(图7b)。骑士α1 - 4又被划分为八个地区(图7c;额外的文件2),并使用凝胶位移分析进一步测试这些小区域是否与GL2结合。GL2特异性结合于两个区域骑士α1 - 4(4-1和4-57c).增加非标记竞争对手的浓度显著降低了dna -蛋白质复合物的条带强度,表明GL2与这些元素的结合是特异性的(图7d).使用NAC蛋白结合元件(NAC)作为GL2结合的阴性对照(图7c).这些结果表明GL2特异性地结合于骑士α1启动子区域。
GL2结合到骑士α1启动子。(一)图骑士α1启动子区域。启动子被分成五个片段。第四个碎片被进一步分成八个小碎片。红色的片段表示与GL2结合。(b)GL2绑定到骑士α1 - 4地区。不同的区域骑士α1将启动子克隆到pAbAi载体中,与pAD-GL2共转染酵母Y1HGold细胞。转染酵母细胞在AbA培养基上的生长表明GL2与相应的元素结合。(c)凝胶移位法检测GL2在细胞中的4-1和4-5段结合骑士α1启动子。在存在(+)或不存在(-)200倍摩尔多余的未标记竞争对手的情况下,用标记探针孵育蛋白质。添加NAC结合序列作为阴性对照。箭头表示蛋白质/DNA复合体。(d)GL2结合的4-1和4-5段骑士α1启动子存在标记探针加上500倍,200倍和0倍摩尔多余的未标记竞争对手(分别从左到右车道)。(e)GL2绑定骑士α1 - 4染色质免疫沉淀(ChIP)法。ChIP与试着中国共产党(根在4道,叶在5道)和gl2-2植株(lane 3)使用抗gl2抗体。引物集特定于的区域骑士α1 - 4用于PCR反应。ACTIN2被放大作为对照。用第二抗体(抗小鼠IgG)孵育的超声染色质作为模拟对照(巷6)gl2-2而且试着中国共产党作为输入控制(1、2车道)。
采用染色质免疫沉淀(ChIP)法测定GL2与骑士α1直接启动子。使用特异性引物进行扩增骑士α1 - 41,骑士α1 - 4-5个片段,经测序证实。GL2结合到的启动子区域骑士α1在试着中国共产党双突变体;但是,没有GL2 /骑士α1检测到启动子复合物gl2突变体(图7e)。ACTIN2作为阴性对照。ChIP结果与骑士α1表达式(数据6而且7e).这些结果表明GL2与骑士α1启动子负调控骑士α1表达式.
骑士α1基因突变影响脂质积累
自骑士α1表达增强GmMYB73-转基因拟南芥植物,我们检测是否骑士α1突变会影响脂质积累。拟南芥种子总脂含量变化不显著骑士α1与Col-0相比突变(图8a).与Col-0相比,突变体种子中总脂肪酸含量和亚油酸水平略有降低(图1)8b, c)。在叶片中,突变体总脂肪酸和3个组成(16:3,18:2和18:3)的含量较Col-0显著降低(图1)8d, e)。
我们进一步研究了各种脂肪种类的变化GmMYB73转基因拟南芥植物,骑士α1和其他突变体。在种子中,与Col-0相比,三酰基甘油(TAG)的水平显著提高GmMYB73-转基因系(OE-1, 2, 5, 7, 10),gl2,尝试cpc / GmMYB73植物,但略有减少试着中国共产党而且骑士α1突变体(表1).二酰基甘油(DAG)水平明显升高GmMYB73转基因线,gl2,尝试cpc / GmMYB73植物。肝脏中磷脂酰胆碱(PC)水平有所降低GmMYB73转基因线和gl2。磷脂酸(PA)水平在所有比较的植物中没有显著变化(表1).叶片中TAG、DAG和PA水平平均轻度升高GmMYB73-转基因植株,而PC水平在这些植株中略有降低(表2).在骑士α1与Col-0相比,突变体叶片的TAG和PA水平显著降低,而PC水平略有升高(表5)2).这些结果表明,GmMYB73、GL2和PLDα1可能通过同一途径调节脂质积累。
讨论
GmMYB73该基因在大豆种子发育过程中具有不同的表达水平,并促进转基因拟南芥中的脂质积累。GmMYB73对脂质积累的影响可能是通过降低脂质积累的负调控因子GL2的表达,然后释放受GL2抑制的脂质积累骑士α1表达式。
过度的GmMYB73拟南芥转基因植株种子大小和千粒重的增强(图3.e)。GmMYB73还拯救了种子的表型和千粒重试着中国共产党双突变体(图3.).这些结果表明GmMYB73或其在拟南芥中的同系物除了控制表毛体的形成外,还调节种子的发育。参与调控毛状体形成的其他几个基因也影响种子的发育。这些包括透明的外种皮GLABRA2[53),透明的外种皮GLABRA1[54种皮分化;gl2突变体不产生可释放的黏液[23];GL3,EGL3,TTG1调节种皮原花青素的生物合成[55,56].其中一些基因还在种子大小控制和千粒重调节中发挥作用[57].应该提到的是gl2-1与WT相比,Ler生态型种子的千粒重没有变化[57].相比之下,现在gl2-2(Col生态型)与对照相比,千粒重略有但显著增加(图3.e).这种差异可能源于使用的生态类型不同和/或种子的储存时间不同。还有其他基因调节种子发育和植物生长发育的各个方面。乙烯受体基因的抑制OsETR2在水稻中表达导致千粒重增加和花期提前[58].突变的MHZ7 / OsEIN2影响晶粒形状和衰老[59].乙烯和盐诱导的nima相关激酶NEK6促进拟南芥植株生长和种子产量但千粒重和种子宽度减小[60].最近,两个景深基因DOF4.2而且DOF4.4已发现在拟南芥中促进芽的分枝,但影响种子/角果的发育[61].其他参与调节种子大小和/或发育的基因在[62].
GmMYB73过表达促进了转基因拟南芥和转基因莲花植物中脂肪酸的积累4而且5).该基因还完全挽救了小鼠的总脂质水平和部分挽救了小鼠的总脂肪酸水平试着中国共产党双突变体(图4),表示GmMYB73参与了脂肪酸积累的上调。值得注意的是,在种子中总脂肪酸水平的增加GmMYB73-转基因拟南芥植株很可能不是由于任何特定脂肪酸的增加,而是由于每一种脂肪酸水平的整体增加(图4b, c)。然而,在转基因植物的叶片中,总脂肪酸的增加是由于亚麻酸的增加(18:3)(图4d, e).种子和叶片组织中脂肪酸积累模式的差异可能是由于这两个器官生理代谢的差异,其中种子是一个汇器官,而叶片是一个源器官。在GmMYB73-转基因莲花植株,叶片中总脂肪酸的增加主要是由于亚麻酸的增加(18:3)(图5f),与拟南芥转基因植物叶片的情况类似(图4e).然而,与转基因拟南芥种子相比,转基因莲花种子的脂肪酸组成发生了不同的变化,总脂肪酸的增加归因于亚麻酸(18:2)和/或亚麻酸(18:3)的增加(图)5).转基因拟南芥和转基因莲藕种子中脂肪酸组成的不同积累模式表明,这些植物的脂质积累可能受到一些不同的机制的影响。
针对大豆植株转化困难的问题,采用了一种大豆转基因毛状根的生成方法。GmMYB73大豆转基因毛状根的过表达增加了总脂肪酸水平,这可能是由于亚油酸(18:2)和亚麻酸(18:3)水平的增加(图)5h, i)。需要指出的是,转基因大豆毛状根中脂肪酸组成的变化与转基因拟南芥植物叶片中脂肪酸组成的变化非常相似(图4e和5i),表明在拟南芥和大豆的营养器官中可能存在类似的机制。有可能GmMYB73会促进大豆种子中的脂质积累,就像在拟南芥种子中一样,尽管还需要进一步的研究来证实这一点。
GmMYB73减少GL2表达式(图2),并且发现GL2参与了种子中油脂的积累。沈等.[18的基因突变GL2与野生型相比,基因导致种子含油量增加。过度的BnaC。GL2.b在拟南芥中影响种子油积累[63].最近,施等.[23]发现PLDZ1/2基因,GL2的靶点[49],不参与种子油的积累。然而,阻塞MUM4,GL2的另一个下游靶标,被发现可以减少粘液的生物合成,这可能与种子油产量的增加有关[23].不久,我们就发现了GmMYB73-过表达植物和拟南芥gl2-2突变体有更高的骑士α1,由于抑制GL2表达的GmMYB73(图2而且6).GL2已被证明与骑士α1启动子和抑制骑士α1表达式(图7).因此,GmMYB73可能通过抑制促进脂质积累GL2表达,从而增强骑士α1表达式。
PLD水解磷脂酰胆碱(PC)的P-O键生成磷脂酰酸(PA)和胆碱。PA被转化为1,2-sn-二酰基甘油(DAG) [64在PA磷酸酶的作用下,DAG可以酰化生成三酰甘油(TAG)。在大豆种子发育过程中,TAG形成的主要途径是PC转化为DAG, DAG酰化产生TAG [65].最近,李等.[51,52的研究报告指出,脂质分布是通过抑制骑士α在新鲜种子中,总脂质和TAG信号有降低的趋势骑士α-可拆卸的大豆。现在,我们发现了骑士α1拟南芥的突变大大降低了种子和叶片中的TAG水平1而且2).相比之下,GmMYB73-与Col-0相比,转基因拟南芥植物在种子和叶片中含有更多的TAG1而且2).值得注意的是,在种子中,大部分的脂质是TAG,而在叶子中,主要的脂质种类是PC和PA1而且2).两种植物叶片中PA与PC含量呈大致负相关GmMYB73转基因植物和骑士α1突变体(表1而且2)提示GmMYB73可能最终通过PLDα1功能的PC转化促进PA和可能的DAG和TAG的积累。类似的情况可能在中国发生GmMYB73-转基因种子虽然PA水平不高,可能是由于有效转化为DAG和TAG。所有这些数据表明,GmMYB73可能增加脂质积累至少部分通过抑制GL2和促进骑士α1.其他下游基因(例如,MUM4)也可能参与此过程[23].应该提到的是GmMYB73过表达的拟南芥植物没有毛状体或毛状体很少。考虑到毛状体含有多种蜡成分,并能分泌脂质[66],缺乏毛状体可能节省转基因植物种子和叶片等其他器官脂质生物合成的总能量和资源。最近,骑士α1人们发现过表达可以提高种子的耐旱性并增加种子产量[67,为我们目前的研究提供了支持。
值得注意的是,尽管GmMYB73提高了转基因种子中的脂质含量,但它在大豆种子发育过程中的表达与这些阶段脂肪酸的积累模式并不一致(图1)1).这种差异可能是由于GmMYB73是一个上游调控因子,因此在种子发育早期表达,以调控下游基因,包括GL2,骑士可能还有其他基因。在后期,GmMYB73降低,下游因子和脂质生物合成基因被激活,脂质积累。另一个基因GmbZIP123,在大豆种子发育过程中表达量增加,通过激活蔗糖转运体基因和细胞壁转化酶基因促进糖易位,从而增加转基因拟南芥植物种子中的脂质含量[68].
结论
综上所述,我们发现GmMYB73促进了转基因植物中的脂质积累,可能是通过抑制GL2抑制gl2的释放骑士α1表达式。种子大小和千粒重也提高了GmMYB73在转基因拟南芥植物中的表达。操纵GmMYB73或者同源物可以提高豆科作物的产油量。
方法
植物材料
大豆植物(大豆。L, HN44)田间种植,收集不同发育阶段种子进行RNA分析。从三周大的植物中提取不同的器官进行RNA分离。拟南芥gl2-2(Col生态型)和GL2::GUS系[48,69]被用于这项研究。双突变体试着中国共产党是由T-DNA插入突变体产生的中国共产党(CS6399)和试一试(CS6518)在哥伦比亚(Col)生态型背景下使用。的试着中国共产党/GmMYB73线是通过交叉产生的试着中国共产党与GmMYB73 -OE-5 overexpressing线。GL2:格斯/ GmMYB73通过将GL2::GUS线与GmMYB73 -overexpressing OE-5。按照所述进行GUS染色和活性测定[59].的骑士α1变种人是由王雪明教授(密苏里大学)提供的。拟南芥植株在标准条件下生长[60].
GmMYB73基因克隆与植物转化
GmMYB73利用带有BamHI和KpnI限制位点的基因特异性引物(5 ' -GGATCCATGGCTGACATAGATC-3 ')和5 ' -GGTACCTTGGCTAGT CGAAAATC-3 ')从叶片cdna中扩增出基因,并克隆到pPROKII中。pPROKII -GmMYB73转染农杆菌农杆菌GV3101,用花浸法导入拟南芥[70].用纯合子拟南芥转基因株系进行进一步分析。该结构也用于转化莲花(Lotus japonicus, Leo)植物[44],收集T1转基因植株的种子,进行总脂和脂肪酸分析。的GmMYB73-载体也被引入到根际农杆菌菌株K599中,转染的细菌通过注射大豆(科丰1号)下胚轴进行根感染,并基于之前和我们自己的方案[42,71].感染后14 d在感染部位产生发状根,浸泡3 d后去除原有的主根。将转基因毛状根的幼苗在水中培养7 d,然后收集根系进行基因表达和脂肪酸分析。
基因表达分析
用TRNzol试剂(天根)提取总RNA,用于第一链cDNA合成。利用SYBR Green Master Mix对这些cdna进行实时定量PCR。所有引物的使用浓度均为10 μM。GmMYB73,骑士α1而且GmDof4采用实时荧光定量PCR检测转基因植株的表达。qPCR在Roche LightCycle 480 II系统中进行,预循环步骤为95°C 2 min,然后依次为95°C 15秒,58°C 20秒,72°C 30秒,循环40次。AtACTIN2(NM_112764.3)和GmTubulin(XM_003520891)分别作为拟南芥和大豆的内参基因。
总脂类和脂肪酸分析
从纯合子转基因拟南芥株系中提取种子(10 mg)或从杂合子转基因莲花株系中提取叶片(100 mg鲜重),如所述[72].根据描述提取拟南芥叶片(20 mg干重)的脂肪酸[73].大豆转基因毛状根(100 mg)也进行了类似的分析。采用己烷萃取法定量种子总脂质[18].从每个品系中提取4个生物重复样品进行总脂质和脂肪酸分析。采用气相色谱法(GC2014, SHIMADZU)分析脂肪酸。采用30 m(长度)× 0.32 mm(内径)× 0.25 μm(液膜厚度)色谱柱(Cat。不。12498年,RESTEK)。初始温度保持在170℃,持续5分钟,然后增加2℃-1到210°C。试验结束后,利用FAME分析标准(Cat。不。18920 - 1 - amp, Supelco)。每个样品的浓度与内部对照的七烷酸甲酯归一化。使用不同批次和/或不同代的材料进行脂质分析,结果一致。给出了一组结果。
酵母双杂交和单杂交试验
载体和酵母菌株均来自Clontech (Matchmake Gold双杂交系统)。GmMYB73融合到pGBKT7中编码GAL4 dna结合域的序列上。GL3而且EGL3与pGADT7中编码GAL4激活域的序列融合。蛋白质相互作用通过转化子的生长和在缺乏必需氨基酸和含有额外的补充物Aureobasidin A和X-a-Gal作为底物的培养基上的蓝色显示。
在单杂交酵母中,将编码GL2 HD-ZIP结构域(氨基酸1 ~ 236)的序列克隆到pGADT7 (pAD)中,生成pAD-GL2。5个DNA片段(1,-1 ~ -263 bp;2、-246 ~ -492 bp;3、-472 ~ -753 bp;4、-739 ~ -1038 bp;5、拟南芥-1021 ~ -1328 bp)骑士α1分别将启动子构建到pAbAi中。将这些pAbAi载体转化为Y1HGold酵母菌株,得到诱饵酵母菌株,并将这些诱饵细胞进一步转染pAD-GL2。转化子在SD/-Leu/+AbA上生长表明GL2与DNA片段结合。NAC核结合位点作为阴性对照[42].
BiFC检测和亚细胞定位
pSAT1-cEYFP和pSAT1-nEYFP矢量[74]用于BiFC分析。GmMYB73融合了nEYFP;GL3而且EGL3融合了cEYPF.每个质粒取10 μg进行原生质体转化。用莱卡TCS SP5共聚焦显微镜观察EYFP在黑暗中孵育16 h后的荧光。
扫描电子显微镜
拟南芥开花植物种子、叶片和茎用2%戊二醛固定于磷酸盐缓冲液中,用醇系脱水,用醋酸异戊酯浸泡过夜。在临界点干燥机(HCP-2)中去除醋酸异戊酯液后,用日立S-3000 N扫描样品。
种子大小和千粒重的测量
对20 ~ 30粒种子在扫描电镜下拍照,用ImageJ程序测定种子的长度和宽度。利用上述数据计算种子长宽比。千粒重来自三个样品,每个样品的重量为1000粒。
凝胶迁移率漂移试验
含有HD-ZIP结构域的截断的GL2蛋白(氨基酸1 ~ 236)被纯化为GL2- his融合蛋白。atpldt1 -4(-739 ~ -1038)的DNA区被分离成8个片段(附加文件2).对互补寡核苷酸进行退火处理,并用Dig-UTP在标记缓冲液中标记双链寡核苷酸。标记的寡核苷酸与0.5 μg GL2蛋白孵育30 min,同时加入未标记的寡核苷酸作为竞争物。蛋白质/DNA复合物被分离并暴露在x射线胶片中。
染色质免疫沉淀(ChIP)法
按照Wang的方法进行芯片分析等.[75].10日龄约2克试着中国共产党双突变体(分离根和叶)和gl2-2用1%甲醛溶液交联突变苗。可溶性染色质经抗gl2抗体或无抗体ChIP处理,4℃旋转平台孵育过夜。在鲑鱼精子DNA/蛋白a -琼脂糖(Millipore)上收集染色质-抗体复合物。DNA-蛋白质交联在65°C下逆转4 h,纯化DNA用于PCR反应。引物对(AGCCCTACACGTTTTTAGTTTCAC和GTCGGGCGCACGATTTGGAT)用于扩增AtPLDа1 - 4。ACTIN2也被放大作为对照。
质谱分析
种子样品粉末在900 μL氯仿:甲醇(1:1)中,4℃,1200 rpm,恒温器中提取过夜。用500 μL去离子H2加入O和300 μL氯仿。样品进行涡旋,然后在4℃下以10 000 rpm离心2分钟。萃取下层有机相并转移到新管中。第二和第三次萃取分别是在剩余的水相中加入500 μL的氯仿,然后分别在4℃、1200 rpm的温度下孵育4 h。
叶片样品在450 μL氯仿:甲醇(1:2)+ 50 μL去离子H中均质2再用450 μL氯仿:甲醇(1:2)+ 50 μL去离子H漂洗2O.样品在4℃、1200转/分的恒温器中孵育30分钟2加入O和300 μL氯仿。样品被旋涡化,然后在4°C下以10 000 rpm离心5分钟。萃取下层有机相并转移到新管中。在剩余的水相中加入500 μL的氯仿进行第二次萃取。
使用SpeedValco将萃取物组合并干燥。干燥的脂质提取物保存在-80°C,直到进一步的质谱分析。所有用于提取的溶剂都是冰镇的。每个品系提取3个生物重复样品进行脂质含量分析。
脂质分析使用Agilent 1260高效液相色谱系统与三重四极子/离子阱质谱计(4500 Qtrap;应用生物系统公司)。采用Phenomenex Luna 3 μm-二氧化硅色谱柱(内径150 × 2.0 mm),在流动相a(氯仿:甲醇:氢氧化铵,89.5:10:5 .5)和流动相B(氯仿:甲醇:氢氧化铵:水,55:39:0.5:5.5)的条件下,用正相(NP)-HPLC分离极性脂类中的各个脂类。甘油脂类[二酰甘油酯和三酰甘油酯]采用前面描述的改进版反相(RP)-HPLC/ESI/MS/MS进行分析[76].简单地说,上述脂类的分离是在Phenomenex Kinetex 2.6 μm-C18色谱柱(即4.6 × 100 mm)上进行的,使用等分流动相氯仿:甲醇:0.1 M醋酸铵(100:100:4),流速为150 μL/min,持续18 min。通过使用多重反应监测(MRM)过渡参考加标的内部标准,对单个脂类进行定量[76].
统计分析
数据采用方差分析或Student 's分析t-使用SPSS 11.5 (SPSS Inc., USA)进行测试。
支持数据的可用性
支持本文结果的数据集包含在本文及其附加文件中。
缩写
- ACCase:
-
乙酰辅酶a羧化酶
- DAG:
-
甘油二酯
- DGAT:
-
甘油二酯酰基转移酶
- PA:
-
磷脂酸
- PC:
-
磷脂酰胆碱
- 骑士:
-
磷脂酶D。
- 标签:
-
三酰甘油。
参考文献
- 1.
张志强,张志强,张志强,等。植物三酰甘油在生物燃料生产中的应用。植物学报,2008,32(5):563 - 566。10.1111 / j.1365 - 313 x.2008.03442.x。
- 2.
Clemente TE, Cahoon EB:大豆油:功能和总含量修饰的遗传方法。植物生理学报,2009,29(4):379 - 379。10.1104 / pp.109.146282。
- 3.
辛格RJ, Hymowitz T:大豆遗传资源与作物改良。中国生物技术学报,1999,42:605-616。10.1139 /可以- 039。
- 4.
Beisson F、Koo AJ、Ruuska S、Schwender J、Pollard M、Thelen JJ、Paddock T、Salas JJ、Savage L、Milcamps A、Mhaske VB、Cho Y、Ohlrogge JB:拟南芥酰脂代谢相关基因。2003年的候选人普查,器官表达序列标签分布的研究,以及基于网络的数据库。植物生理学报,2004,24(3):381 - 381。10.1104 / pp.103.022988。
- 5.
植物中三酰甘油积累的分离。中国生物医学工程学报,2012,29(4):378 - 378。10.1074 / jbc.R111.290072。
- 6.
Kinney AJ, Knowlton S:设计师油:高油酸大豆。食品工业中的基因改造。编辑:Roller S, Harlander S. 1998,美国:施普林格
- 7.
植物脂肪酸生物合成的代谢工程。环境工程学报,2002,4:12-21。10.1006 / mben.2001.0204。
- 8.
Jaworski J, Cahoon EB:来自转基因植物的工业油。植物学报,2003,6:178-184。10.1016 / s1369 - 5266 (03) 00013 - x。
- 9.
Damude HG, Kinney AJ:工程油籽生产营养脂肪酸。植物工程学报,2008,32(4):371 - 371。
- 10.
王晓燕,王晓燕,王晓燕,等。拟南芥同源性乙酰辅酶A羧化酶对油菜质体的靶向作用。植物生理学报,1997,15(4):381 - 381。10.1104 / pp.113.1.75。
- 11.
Weselake RJ, Shah S, Tang M, Quant PA, Snyder CL, Furukawa-Stoffer TL, Zhu W, Taylor DC, Zou J, Kumar A, Hall L, Laroche A, Rakow G, Raney P, Moloney MM, Harwood JL:代谢控制分析有助于对油菜(Brassica napus)进行遗传调控以提高种子含油量。中国生物医学工程学报,2008,29(5):369 - 369。10.1093 / jxb / ern206。
- 12.
郑萍,Allen WB, Roesler K, Williams ME, Zhang S, Li J, Glassman K, Ranch J, Nubel D, Solawetz W, Bhattramakki D, Llaca V, Deschamps S, Zhong GY, Tarczynski MC, Shen B: DGAT中的苯丙氨酸是玉米含油量和组成的关键决定因素。中国生物技术学报,2008,30(4):367-372。10.1038 / ng.85。
- 13.
李瑞,畑中田,于凯,吴燕,福泽海,希尔德伯兰D:大豆油生物合成中双酰基甘油酰基转移酶的作用。功能整合基因组学,2013,13:99-113。10.1007 / s10142 - 012 - 0306 - z。
- 14.
Cernac A, Benning C: wrinkle 1编码一个AP2/EREB结构域蛋白,参与控制拟南芥贮藏化合物的生物合成。植物学报,2004,30(4):576 - 576。10.1111 / j.1365 - 313 x.2004.02235.x。
- 15.
Baud S, Mendoza MS, To A, Harscoet E, Lepiniec L, Bubreucq B:皱纹1指定了在拟南芥种子成熟过程中叶子叶don2对脂肪酸代谢的调节作用。植物学报,2007,30(5):527 - 527。10.1111 / j.1365 - 313 x.2007.03092.x。
- 16.
Baud S, Wuilleme S, To A, Rochat C, Lepiniec L:皱纹1在拟南芥糖酵解和脂肪酸生物合成基因转录调控中的作用。植物学报,2009,29(3):369 - 369。10.1111 / j.1365 - 313 x.2009.04011.x。
- 17.
Santos-Mendoza M, Dubreucq B, Baud S, Parcy F, Caboche M, Lepiniec L:破译控制拟南芥种子发育和成熟的基因调控网络。植物学报,2008,32(4):366 - 366。10.1111 / j.1365 - 313 x.2008.03461.x。
- 18.
沈b, Sinkevicius KW, Selinger DA, Tarczynski MC:同源盒基因GLABRA2对拟南芥种子含油量的影响。植物生物学杂志,2006,30(4):387 -387。10.1007 / s11103 - 005 - 4110 - 1。
- 19.
穆娇,谭辉,郑强,付芳,梁勇,张军,杨旭,王涛,冲科,王旭军,左俊:叶状子叶don1是拟南芥脂肪酸生物合成的关键调控因子。植物生理学报,2008,29(4):347 - 347。10.1104 / pp.108.126342。
- 20.
谭辉,杨旭,张峰,郑鑫,曲晨,穆军,付峰,李娟,关锐,张宏,王刚,左娟:条件表达甘蓝型油菜叶状子叶don1和LEC1-LIKE促进油菜种子产油。植物生理学报,2011,29(4):379 - 379。10.1104 / pp.111.175000。
- 21.
陈明,王铮,朱颖,李铮,Hussain N,宣林,郭伟,张刚,蒋玲:透明TESTA2对拟南芥幼苗建立过程中种子脂肪酸生物合成及环境胁迫耐受性的影响。植物生理学报,2012,29(4):366 - 366。10.1104 / pp.112.202945。
- 22.
Gupta M、Dekelver RC、Palta A、Clifford C、Gopalan S、Miller JC、Novak S、Desloover D、Gachotte D、Connell J、Flook J、Patterson T、Robbins K、Rebar EJ、Gregory PD、Urnov FD、Petolino JF:工程锌指蛋白转录因子对油菜β-酮脂基acp合成酶II的转录激活作用植物生态学报,2012,32(4):369 - 369。10.1111 / j.1467-7652.2012.00695.x。
- 23.
Shi L, Katavic V, Yu Y, Kunst L, howhn G:黏质生物合成缺乏的拟南芥glabra2突变体种子产生更多的油。植物学报,2012,29(4):447 - 447。10.1111 / j.1365 - 313 x.2011.04768.x。
- 24.
Verdier J, Kakar K, Gallardo K, Le Signor C, Aubert G, Schlereth A, Town CD, Udvardi MK, Thompson RD: M. truncatula转录因子的基因表达谱确定了籽粒豆科植物种子灌浆的可能调控因子。植物生物学杂志,2008,37(4):366 - 366。10.1007 / s11103 - 008 - 9320 - x。
- 25.
Le BH, Cheng C, Bui AQ, Wagmaister JA, Henry KF, Pelletier J, Kwong L, Belmonte M, Kirkbride R, Horvath S, Drews GN, Fischer RL, Okamuro JK, Harada JJ, Goldberg RB:拟南芥种子发育过程中基因活性的全局分析及种子特异性转录因子的鉴定。中国生物医学工程学报,2010,29(3):366 - 366。10.1073 / pnas.1003530107。
- 26.
Agarwal P, Kapoor S, Tyagi AK:调控单子叶和双子叶种子发育进程的转录因子。生物学报,2011,33:189-202。10.1002 / bies.201000107。
- 27.
Bocher V, Pineda-Torra I, Fruchart JC, Staels B: PPARs:控制脂质和脂蛋白代谢的转录因子。中国科学院学报,2002,29(4):371 - 371。
- 28.
腺苷酸活化蛋白激酶对脂肪酸合成和氧化的调节。生物化学学报,2002,30:1064-1070。
- 29.
Eberle D, Hegarty B, Bossard P, Ferre P, Foufelle F: SREBP转录因子:脂质稳态的主调节因子。生物化学学报,2004,36(4):339 - 348。10.1016 / j.biochi.2004.09.018。
- 30.
Andre C, Froehlich JE, Moll MR, Benning C:一种参与拟南芥种子油生物合成的异聚体可塑性丙酮酸激酶复合物。《植物细胞》2007,19:2006-2022。10.1105 / tpc.106.048629。
- 31.
Moellering ER, Benning C:拟南芥中脂质生物合成的磷酸盐调控与线粒体外膜DGS1复合体无关。植物生理学报,2010,32(5):561 - 561。10.1104 / pp.110.153262。
- 32.
桑java, Durrett TP, Weise SE, Benning C:转基因拟南芥通过将淀粉合成的碳转移到油的生物合成来提高营养组织的能量密度。植物生态学报,2011,29(3):366 - 366。10.1111 / j.1467-7652.2011.00599.x。
- 33.
金海林,Martin C:植物myb基因家族的多功能性和多样性。植物生物学杂志,1999,41:577-585。10.1023 /: 1006319732410。
- 34.
Araki S, Ito M, Soyano T, Nishihama R, Machida Y:有丝分裂周期素刺激烟草中c- myb样因子的活性,从而激活G2/M期特异性基因。中国生物医学工程学报,2004,29(4):359 - 359。10.1074 / jbc.M403171200。
- 35.
廖颖,邹洪峰,王华伟,张伟坤,马斌,张建军,陈淑云:转基因拟南芥大豆GmMYB76、GmMYB92和GmMYB177基因的抗逆性。Cell Res. 2008, 18: 1047-1060。10.1038 / cr.2008.280。
- 36.
μRL,曹年,刘YF, Lei G,邹高频,廖Y,王HW,张周,马B, Du生理改变,元M,张JS,陈SY: R2R3-type AtMYB59调节转录因子基因在拟南芥根生长和细胞周期进展。Cell Res. 2009, 19: 1291-1304。10.1038 / cr.2009.83。
- 37.
和田T,立花T,志村Y,冈田K:用Myb同源物CPC测定拟南芥表皮细胞分化。科学学报,1997,27(4):513 - 516。10.1126 / science.277.5329.1113。
- 38.
Schellmann S, Schnittger A, Kirik V, Wada T, Okada K, Beermann A, Thumfahrt J, Jurgens G, Hulskamp M: TRIPTYCHON和CAPRICE介导拟南芥毛体和根毛模式的侧抑制。中国生物医学工程学报,2004,24(3):366 - 366。10.1093 / emboj / cdf524。
- 39.
周庆云,田亚光,邹洪峰,谢志明,雷刚,黄俊,王春明,王华伟,张建军,陈淑云:大豆wrky型转录因子基因GmWRKY13、GmWRKY21和GmWRKY54在转基因拟南芥植株中具有不同的非生物胁迫耐磨性。植物生态学报,2008,26(6):476 - 476。10.1111 / j.1467-7652.2008.00336.x。
- 40.
魏伟,黄娟,郝玉军,邹洪峰,王华伟,赵建勇,刘晓燕,张伟坤,马斌,张建军,陈淑云:转基因拟南芥大豆gmphd型转录调控因子提高耐胁迫能力年代植物。科学通报,2009,4:e7209-10.1371/journal.pone.0007209。
- 41.
谢志明,邹洪峰,雷刚,魏伟,周启勇,牛秋芳,廖颖,田ag,马斌,张伟坤,张建军,陈淑云:转基因拟南芥大豆三螺旋转录因子GmGT-2A和GmGT-2B提高植物对非生物胁迫的耐耐性。科学通报,2009,4:e6898-10.1371/journal.pone.0006898。
- 42.
郝玉军,魏伟,宋秋霞,陈华伟,张玉强,王芳,邹慧峰,雷刚,田银,张伟坤,马斌,张建军,陈永春:大豆NAC转录因子促进转基因植株的非生物胁迫耐受力和侧根形成。植物学报,2011,29(3):366 - 366。10.1111 / j.1365 - 313 x.2011.04687.x。
- 43.
王华伟,张斌,郝玉军,黄军,田银银,廖莹,张建军,陈玉云:大豆多夫型转录因子基因GmDof4和GmDof11可提高转基因拟南芥种子中的脂质含量。植物学报,2007,38(5):716-729。10.1111 / j.1365 - 313 x.2007.03268.x。
- 44.
刘艳芳:大豆GmMYB73基因的功能分析。博士论文。2011,北京100101:中国科学院遗传与发育生物学研究所
- 45.
Kirik V, Simon M, Huelskamp M, Schiefelbein J: TRY和CPC1基因增强子在拟南芥表毛和根毛细胞模式中与TRIPTYCHON和CAPRICE起冗余作用。中国生物医学工程学报,2004,29(4):447 - 447。10.1016 / j.ydbio.2003.12.037。
- 46.
拟南芥毛状体和根毛起始过程中二维模式从头生成。中华检验医学杂志,2004,14:422-427。10.1016 / j.gde.2004.06.007。
- 47.
Ishida T, Kurata T, Okada K, Wada T:毛状体和根毛发育的遗传调节网络。植物生态学报,2008,29(5):364 - 364。10.1146 / annurev.arplant.59.032607.092949。
- 48.
Lee MM, Schiefelbein J:狼人蛋白是拟南芥中myb相关蛋白,是一种表皮细胞模式的位置依赖性调节蛋白。细胞学报,1999,99:473-483。10.1016 / s0092 - 8674(00) 81536 - 6。
- 49.
Ohashi Y, Oka A, rodriguez - pousada R, Possenti M, Ruberti I, Morelli G, Aoyama T: GLABRA2对根毛模式形成中磷脂信号的调控。科学通报,2003,30(3):327 - 327。10.1126 / science.1083695。
- 50.
李敏,洪艳,王鑫:磷脂酶D-和磷脂酸介导的植物信号转导。生物化学学报2009,1791:927-935。10.1016 / j.bbalip.2009.02.017。
- 51.
Lee J, Welti R, Schapaugh WT, Trick HN: PLD抑制对大豆种子磷脂和三酰甘油谱的影响。植物生态学报,2011,29(3):359-372。10.1111 / j.1467-7652.2010.00562.x。
- 52.
李J, Welti R,罗斯M, Schapaugh WT,李J,技巧HN:增强种子活力和脂质成分改变在自然老化通过抑制磷脂酶Dα大豆种子。植物生态学报,2012,30(4):366 - 366。10.1111 / j.1467-7652.2011.00650.x。
- 53.
Johnson CS, Kolevski B, Smyth DR:透明TESTA GLABRA2是拟南芥表毛体和种皮发育基因,编码WRKY转录因子。植物学报,2002,14:1359-1375。10.1105 / tpc.001404。
- 54.
张峰,赵茂珍,张晓燕,张晓燕:拟南芥ttg1依赖通路中冗余bHLH蛋白网络的研究。《科学进展》,2003,30(3):359 - 369。10.1242 / dev.00681。
- 55.
Gonzalez A, Mendenhall J, Huo Y, Lloyd A: TTG1复合物myb, MYB5和TT2控制外种皮分化。生物工程学报,2009,29(4):412-421。10.1016 / j.ydbio.2008.10.005。
- 56.
Li SF, Milliken ON, Pham H, Seyit R, Napoli R, Preston J, Koltunow AM, Parish RW:拟南芥MYB5转录因子调控黏液合成、种皮发育和毛状体形态发生。植物学报,2009,21:72-89。10.1105 / tpc.108.063503。
- 57.
张丽娟,张丽娟,张丽娟。拟南芥种壳对种子休眠、萌发和寿命的影响。植物生理学报,2004,24(3):366 - 366。10.1104 / pp.122.2.403。
- 58.
五日阳汉华、张斌、曹文华、马斌、雷刚、刘艳芳、魏伟、吴海军、陈立军、陈华伟、曹逸尔、何世杰、张伟坤、王新军、陈少春、张建军:乙烯受体ETR2延缓水稻花的转变并影响淀粉积累。植物学报,2009,21:1473-1494。10.1105 / tpc.108.065391。
- 59.
马斌,何淑娟,段克新,尹长青,陈红,杨超,熊强,宋秋霞,陆晓,陈红伟,张伟坤,陆大刚,陈思思,张建军:水稻乙烯响应突变体的鉴定与鉴定MHZ7 / OsEIN2在乙烯响应和产率性状调控上有明显差异。植物学报,2013,6:1830-1848。10.1093 / mp / sst087。
- 60.
张斌,陈华伟,穆瑞林,张伟坤,赵爱梅,魏伟,王芳,于浩,雷刚,邹慧峰,马斌,陈世思,张建军:nima相关激酶NEK6对拟南芥植物生长和胁迫响应的影响。植物生态学报,2011,29(4):447 - 447。10.1111 / j.1365 - 313 x.2011.04733.x。
- 61.
邹洪峰、张永强、魏伟、陈华伟、宋秋霞、刘永峰、赵爱梅、王芳、张炳、林青、詹伟科、马斌、周永华、张建军、陈淑霞:转录因子AtDOF4.2调控植物芽分枝和种皮形成拟南芥.中国生物医学工程学报,2013,38(3):369 - 369。10.1042 / BJ20110060。
- 62.
Kesavan M, Song JT, Seo HS:种子大小:谷类作物的优先性状。植物工程学报,2013,37(4):369 - 369。10.1111 / j.1399-3054.2012.01664.x。
- 63.
柴刚,白铮,魏峰,王光杰,石磊,董超,陈红,刘珊:芸苔属GLABRA2基因:籽油含量相关功能分析及功能标记的开发。中国生物工程学报,2010,30(4):359 - 361。10.1007 / s00122 - 010 - 1279 - 8。
- 64.
Dahlqvist A, Stahl U, Lenman M, Banas A, Lee M, Sandager L, Ronne H, Stymne H:磷脂:二酰基甘油酰基转移酶:一种在酵母和植物中催化不依赖于酰基辅酶A的三酰基甘油形成的酶。中国生物医学工程学报,2000,29(4):381 - 381。10.1073 / pnas.120067297。
- 65.
贝茨PD,杜雷特TP, Ohlrogge JB, Pollard M:大豆胚胎中三酰甘油合成的多途径酰基通量分析。植物生理学报,2009,30(4):447 - 447。10.1104 / pp.109.137737。
- 66.
Choi YE, Lim S, Kim HJ, Han JY, Lee MH, Yang Y, Kim JA, Kim YS:烟草NtLTP1是一种腺体特异性脂质转移蛋白,是腺体毛状体分泌脂质所必需的。植物学报,2012,29(4):489 - 489。10.1111 / j.1365 - 313 x.2011.04886.x。
- 67.
吕松,巴恩SC,曲刚,秦浩,洪勇,徐强,周勇,洪勇,王鑫:干旱胁迫下甘蓝型油菜保护细胞磷脂酶Dα1表达增加,水分流失减少,种子产量提高。植物生态学报,2013,31(4):389 -389。10.1111 / pbi.12028。
- 68.
宋秋霞、李启涛、刘艳芳、张丰兴、马斌、张伟坤、满WQ、杜文华、王德光、陈思思、张建军:大豆GmbZIP123该基因提高了转基因拟南芥植物种子中的脂质含量。中国生物医学工程学报,2013,32(4):359 - 359。10.1093 / jxb / ert238。
- 69.
王松,Barron C, Schiefelbein J,陈景刚:拟南芥GLABRA2与单重复序列R3 MYB转录因子调控毛表体和根毛模式的显著关系。植物学报,2010,38(4):387- 396。10.1111 / j.1469-8137.2009.03067.x。
- 70.
Clough SJ, Bent AF:花浸渍:农杆菌介导的拟南芥转化的简化方法。植物学报,1998,16:735-743。10.1046 / j.1365 - 313 x.1998.00343.x。
- 71.
李东,李德华,李德华,李德华,李德华,李德华,李德华,李德华,李德华,李德华,李德华,李德华,李德华,李德华,李德华:根际农杆菌介导的大豆根生物学研究。通信学报,2007,27(2):449 - 452。10.1038 / nprot.2007.141。
- 72.
Poirier Y, Ventre G, Caldelari D:在发育中缺乏双酰基甘油酰基转移酶活性或合成中链长脂肪酸的拟南芥种子中,脂肪酸流向β -氧化的增加。植物生理学报,2004,24(3):369 - 369。10.1104 / pp.121.4.1359。
- 73.
Browse J, McCourt PJ, Somerville CR:联合消化后叶脂的脂肪酸组成和新鲜组织脂肪酸甲酯的形成。中国生物化学杂志,1998,26(4):381 - 381。10.1016 / 0003 - 2697(86) 90132 - 6。
- 74.
Citovsky V, Lee LY, Vyas S, Glick E, Chen MH, Vainstein A, Gafni Y, Gelvin SB, Tzfira T:植物中相互作用蛋白的双分子荧光互补亚细胞定位。中华分子生物学杂志,2006,32(4):369 - 369。10.1016 / j.jmb.2006.08.017。
- 75.
王松,郭世胜,曾强,Ellis BE,陈晓霞,Schiefelbein J,陈建刚:拟南芥中毛状体无毛蛋白1通过抑制GLABRA1调控毛状体模式。《科学进展》,2007,34(4):369 - 369。10.1242 / dev.009597。
- 76.
Lam SM, Tong L, Duan X, Petznick A, Wenk MR, Shui G:使用不同技术收集的人类泪液的广泛表征揭示了新型脂质两亲性物质的存在。中国生物医学工程学报,2014,38(5):559 - 561。10.1194 / jlr.M044826。
致谢
我们感谢ABRC试一试而且中国共产党突变体种子。我们也感谢博士。Martin Huelskamp John Schiefelbein和Xueming Wang提供了变异种子。基金资助:国家基础研究计划项目(2010CB125903, 2013CB835201, 2011CB109300);国家转基因研究计划项目(2014ZX0800926B, 2014ZX08004003-005, 2013ZX08009-003-004, 2013ZX08009-004)。
作者信息
从属关系
相应的作者
额外的信息
相互竞争的利益
作者声明他们没有竞争利益。
作者的贡献
YFL进行了实验并起草了最初的手稿。QTL重复并增加新的实验。XL、QXS、WKZ、BM和QL有助于数据分析。WQM和WGD提供大豆原料。SML和GHS对质谱分析有贡献。JSZ和SYC构思了这项研究,获得了资金,分析了数据,完成了最终的手稿。所有作者阅读并批准了最终稿件。
刘云峰、李青田对这项工作也有贡献。
电子辅料
转基因拟南芥过表达植株的表型
额外的文件1:GmMYB73相比之下试着中国共产党双突变体。(PDF 371 KB)
香港八个小地区
额外的文件2:AtPLDа1 - 4用于GL2结合分析。(PDF 29 KB)
权利和权限
开放获取本文由BioMed Central Ltd.授权发布。这是一篇开放获取文章,根据创作共用授权协议(https://creativecommons.org/licenses/by/2.0),它允许在任何媒体上不受限制地使用、分发和复制,只要原始作品的名称正确。创作共用公共领域奉献放弃书(https://creativecommons.org/publicdomain/zero/1.0/)除另有说明外,适用于本条提供的资料。
关于这篇文章
引用这篇文章
刘、YF。,Li, QT., Lu, X.et al。大豆GmMYB73促进转基因植物的脂质积累。BMC植物杂志14,73(2014)。https://doi.org/10.1186/1471-2229-14-73
收到了:
接受:
发表:
关键字
- 脂肪酸
- GmMYB73
- 种子大小
- 大豆
- 脂质
- Thousand-seed重量