抽象的
背景
所有生物都能自发地发出低强度的生物发光,这种发光在应激反应中会增加。成像这种超弱发光的方法以前一直受到所使用探测系统的灵敏度的限制。
结果
我们开发了一种新型的冷却电荷耦合器件(CCD),用于生物材料光发射的二维成像。在本研究中,我们对植物叶片的光子发射进行了成像。该设备允许较短的图像采集集成时间,提供关于生物发光的高分辨率空间和时间信息。我们能够对全叶延迟叶绿素荧光和局限于组织损伤部位的低水平伤致发光进行时间过程成像。我们发现,伤口诱导的发光是叶绿素依赖的,在较高的温度下增强。
结论
收集在植物生物发光上的数据说明了这里描述的设备代表了二维发光成像技术的改进。使用该系统,我们将叶绿素鉴定为叶片的伤口引起的发光的起源。
背景
有充分的记录,基本上所有的生活系统都自发地产生并发出了非常低的光水平(在[1])。这种超弱的生物发光通常以光子(有时称为“生物光子”)的发射强度小于10为特征-14年W.CM.-2(<1000 photon.sec-1疲倦-2).这与来自显着发光的动物的动物更广泛的已知生物发光相反,例如使用荧光蛋白质和/或荧光素酶的某些种类的水母和甲虫,以催化导致化学发光的反应的荧光蛋白和甲虫的动物。通常认为超弱生物发光通常由细胞内发生的氧化化学产生[1,2[但在大多数情况下,尚未确定观察到的排放来源。然而,在许多系统中观察到,在许多系统中观察到响应应力 - 特别是氧化应激的发射水平的变化 - 或者包括细菌[3.], 植物 (如.[2,4- - - - - -6])和动物[7,8].因此,超弱生物发光的测量可以是用于监测对细胞活性的快速扰动和早期检测患病和受损细胞的有用的非侵入性技术。
在植物中,已经响应于病原体感染而观察到自发低水平发光的增加[5],盐胁迫[9,渗透压力[10]和机械损伤或伤害[2,4,6,11].这表明,发光是由单线态氧和由脂质过氧化反应产生的激发态羰基产生的[2,11].受伤和病原体感染的植物组织中的脂质过氧化是ROS的常见后果,其也充当诱导植物防御反应的信号[12].
通常使用敏感的光电倍增管作为光子计数装置获得这种超弱光子发射的定量测量。然而,最近,二维光电倍增管和冷却的电荷耦合器件(CCD)相机也被采用作为成像从患病和受损植物组织的光发射的空间分布的手段[2- - - - - -6,9].最清晰的图像是通过陈获得的等, (2,利用微通道板与冷却的CCD耦合,对通过透镜捕获的光进行成像。然而,获取一个相对较弱的信号所需的时间是1小时,这阻止了对应激诱导的生物发光进行详细的时间研究。
在这里,我们介绍了一种冷却CCD的新颖配置,其能够具有高分辨率,高分辨率二维成像,具有短积分时间。我们证明了系统对图像的效用,并量化了植物叶片的延迟叶绿素荧光和伤口诱导的发光。
结果与讨论
施工意见成像仪
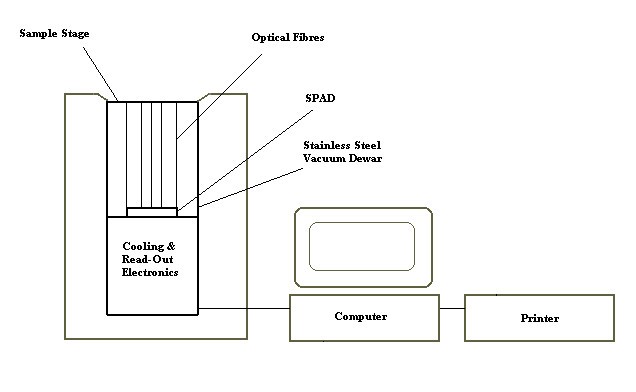
实验成像设置如图所示1,基本上由耦合到具有光纤的冷却CCD的玻璃样品阶段组成。该配置通过避免与基于透镜的系统相关联的不可避免的光分散,可以最大地捕获从阶段的平坦样品的一侧发射的光。该系统可用于从诸如植物叶片或细胞的平面样本中成像生物发光,所述植物叶子或细胞生长透明培养容器或诸如显微镜载玻片或膜的固体载体。通过分析从CCD捕获的数据,可以估计在非常宽的动态范围内每单位面积检测到的光子的数量。我们在1000光子/秒/ mm的区域中常规测量排放水平2来自受伤的叶子(见下文)。除了高灵敏度之外,成像仪比基于光电倍增管的设备昂贵。
延迟成像叶绿素荧光
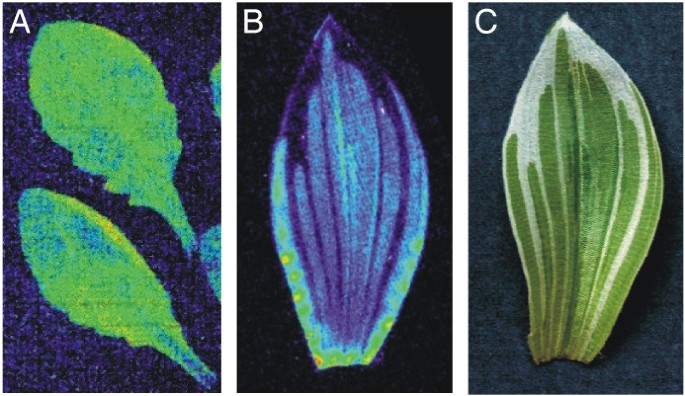
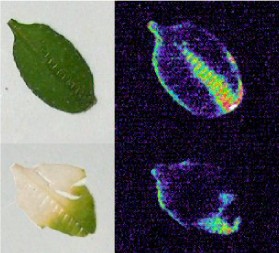
延迟叶绿素荧光是众所周知的现象,其是从叶片转移到黑暗后的激发叶绿素分子的光子发射的结果。它通常使用诸如光电倍增管的装置和原则上测量,可以通过现有的基于透镜的CCD成像系统来检测。我们首先通过从叶子上成像延迟叶绿素荧光来测试我们系统的空间和时间分辨率拟南芥蒂利亚纳和Tradescantia albiflora(图2).叶子的图像从vieiegatedT.Baliflora.植物清楚地表明依赖于叶绿素发生的叶绿素,因为叶子的白色,非着色区域不会发光(比较数字2 b和2摄氏度).1-5分钟的曝光时间相对较短,即可获得明亮的图像。延迟叶绿素荧光在转入黑暗后5 ~ 10分钟迅速消退。叶绿素荧光延迟的绝对水平拟南芥叶子大大变化,一般出现在当天晚些时候下降。
伤叶超弱发光的时空分辨率
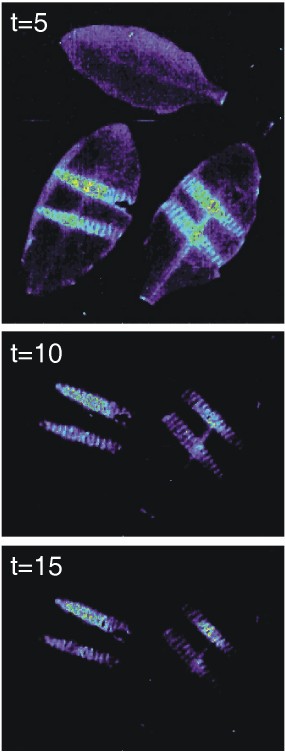
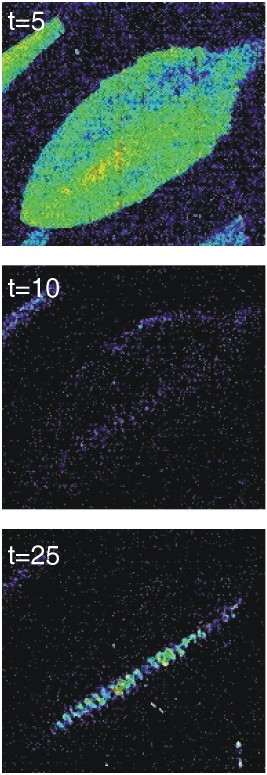
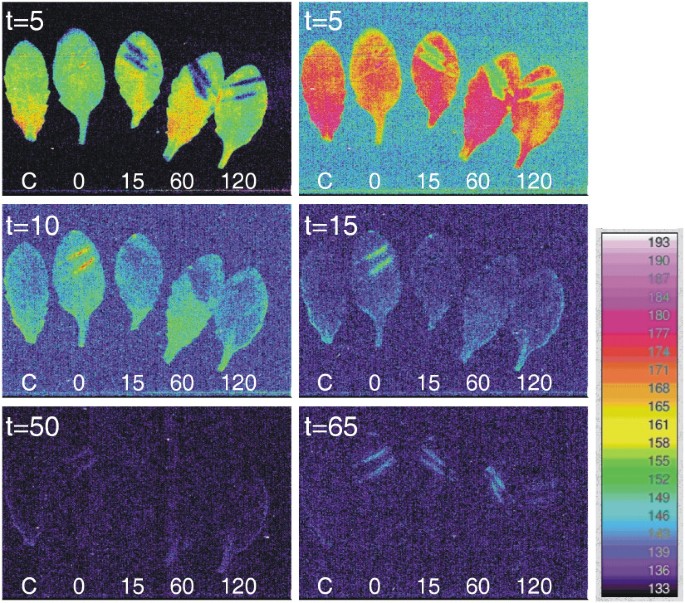
与典型的超弱生物发光水平相比,延迟叶绿素荧光产生相对强烈的发光。为了测试设备的灵敏度,我们想尝试以映像这些较低级别的排放量。以前的几份报告表明,机械伤口增加了来自植物叶子的超弱发光,但是对这种现象的时间和空间性质有限的研究。我们使用了一个僵局来造成伤口拟南芥在一段时间内,通过连续5分钟的曝光对它们进行成像。在许多实验中,由于被延迟的叶绿素荧光掩盖,在转移到成像仪后的前5分钟内看不到伤致发光。然而,在最初的阶段之后,受伤组织周围的光子发射更加强烈。在其他实验中,延迟叶绿素荧光较低,即使在第一次暴露中也能看到信号。实验结果如图所示3.并在伴随的扩展动画(附加文件1).在第一图像中,其包括未经涂抹的控制叶和两个叶片,每个叶片在椎板上伤害两次,可以看出突出的叶绿素荧光的一般背景上方的伤口诱导的发光(图3).在后续5分钟的曝光中,叶绿素荧光已经消退,而伤口诱导的发光仍然很高(图3 b, c).止血器表面的锯齿状图案清晰地反映在叶片的发光图案上,损伤较大的区域表现出最大的光子发射。总的来说,我们观察到,诱导发光在受伤后立即最强,然后在一小时或更长时间内逐渐衰减。
伤口诱导的发光的起源
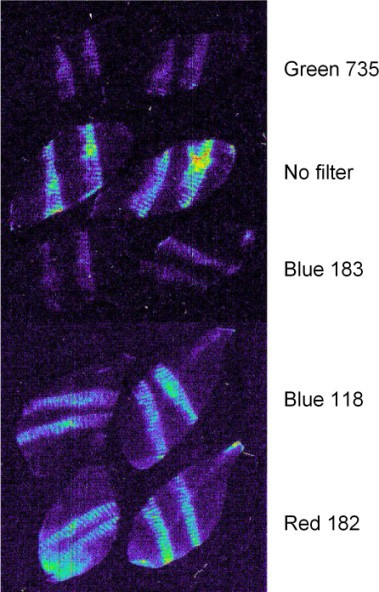
为了了解更多关于受伤叶子发出的发光的起源,我们使用彩色过滤器来研究其光谱特性。结果如图所示4.红色滤光片(LEE 182)能穿透波长大于600 nm的可见光,对伤口发出的光有效透明,而蓝色和绿色滤光片(LEE 183和LEE 735)能吸收550 ~ 750 nm的光,当放置在受伤叶片和样品阶段之间时,导致到达检测器的信号显著减少。有趣的是,另一种蓝色滤光片(LEE 118)通过700 nm以上的光,对发光没有显著影响(图)4).这些结果表明,伤员排放的光拟南芥叶子的波长在700到750 nm之间,即.可见光谱的红色区域。这与来自叶绿素(730nm)的典型荧光一致。为了测试叶绿素是否可能是伤口引起的光子发射的来源,我们使用类胡萝卜素生物合成抑制剂Norflurazon,产生缺乏叶绿素的光漂白叶子[13].与来自对照植物的当量叶相比,这些白色叶片未能在伤口后未能发光,除了剩余的含叶绿素的区域(图5).总之,这些结果表明,受伤叶片的光发射是依赖叶绿素的。由于发光发生在黑暗中,并延长时间远远超过延迟叶绿素荧光,我们得出的结论是,某些创伤诱导过程产生的激发能量转移到叶绿素并以光的形式发射。这种能量的一个可能来源可能是氧化损伤的产物,如脂质过氧化过程中产生的激发态三联体羰基[14].
伤口诱导的发光的温度依赖性
延迟叶绿素荧光表现出在几个系统中显示出温度依赖性[15].由于我们确定叶绿素是受伤叶片的主要光源来源,我们研究了伤口诱导的发光是否可能受到温度的影响。通过箔加热器在样品室的盖子中施加热量在样品室中的应用显着增加了测试温度范围内的发光强度。如果没有施加的热量,则当仅检测到低水平的发光时,样品阶段的温度约为7℃。在加热器的激活时发光显着增加,导致样品阶段的温度增加到20℃的区域。这种现象在图中示出6,并在附带的扩展动画中(请参阅附加文件2).
此外,我们发现加热可以在成像前3小时损伤的叶子中的发光。例如,图7展示了一系列实验的图像,在成像之前,树叶在不同的时间被损伤。没有暖气,只有叶受伤前成像显示检测wound-induced发光,这20分钟内放射衰变到非常低的水平。在45分钟后,加热应用于样品室,并在10分钟,伤口立即应用,开始前15分钟,1小时成像清晰可见,成像开始前2小时,叶子上的伤口也能检测到微弱的辐射(因此这里显示的图像(t = 65)是在这片叶子受伤后3小时拍摄的)。这种现象使人想起热释光法测量的光发射[14].热致发光是在高温下观察到的叶绿素依赖性发光(在70-90℃和120-140℃),如超弱生物发光,归因于氧化过程中脂质过氧化的单线氧和三重态羰基。压力 [14].与上述结果相结合,这些数据表明,温度增加了激发三重态羰基的衰减率,并且释放的能量转移到叶绿素并作为光发射。对于来自激发叶绿素的光发射的速率,也可以存在另外的温度依赖性组分,如延迟荧光所观察到的[15].
结论
我们在本研究中使用的冷却CCD的新配置,以捕获植物叶片的二维图像,为生物材料中的生物材料中的生物发光/化学发光过程提供了优异的时间和空间分辨率,这是各种形式的压力和疾病的重要标记。使用该系统,我们能够从植物作为叶绿素中造成伤口诱导的发光的起源,并表明这通过氧化应激产生的激发三重羰基的温度依赖性释放能量。
方法
植物材料
植物的拟南芥蒂利亚纳,哥伦比亚生态型,在22℃下在玻璃盆中种植,具有16小时的光周期。通过用止血液破碎叶子进行伤害。生成缺乏叶绿素的叶子,拟南芥在16小时光/ 8小时黑暗中生长3周的植物,用0.1mm Norflurazon(Sigma Aldrich PS1044)浇水,并在120μmol/ m的恒定照射下生长2/秒。在这些条件下,新出现的叶片组织是白色的。在Norflurazon治疗开始后15天留下了白色区域的叶子,并用于发光成像。
二维发光成象装置
使用的成像仪是一个二维成像系统基于慢扫科学品位的硅照片Area-Detector (SPAD) (SPAD集成成像系统1 - PiXx * l形,Biolumonics有限公司),它包含一个冷却敏感区域内打光检测器不锈钢真空容器和相关图像采集电子产品。输入图像通过光纤(数值孔径= 1)耦合到探测器上。探测器包含222,336像素,在这里给出的实验中,在-58°C的工作温度下运行。结合专有的低读出噪声电子、探测器的冷却和光纤耦合,形成了一个灵敏的成像系统,能够以高分辨率(根据样品的几何形状和积分时间,40 μm到200 μm)记录最微弱的发光。SPAD的光谱吸收响应范围从近紫外到红外,包括整个可见光谱,直到硅的带隙能垒(1.1 eV)。即.大约1100 nm;但是,对于最终敏感性,检测器输出是单色,即.本仪器没有波长选择性。Michel floro - henry, Biolumonics Ltd.可获得更多信息。
过滤器
彩色滤镜来自Lee filters (Andover, UK)。我们使用了光效果滤镜LEE 182 -“淡红”,LEE 118 -“淡蓝”,LEE 183 -“月光蓝”和LEE 735 -“丝绒绿”。滤光片的光谱特性可在http://www.leefilters.com.尽管读者应注意,随着滤波器提供的透射率谱覆盖300-800nm的范围,而不是在网站上显示的400-700nm光谱的范围。在成像之前,将过滤器置于叶片和样品阶段之间。
参考
- 1.
Devaraj B,USA M,Inaba H:BioPophotons:来自生活系统的UltraWeak光发射。CurrOpar固态垫SCI。1997年,2:188-193。10.1016 / s1359-0286(97)80064-2。
- 2.
陈WL,兴D,TAN SC,唐耶,他YH:造成伤口萌发大豆的超弱生物发光和单次氧气发射的成像。发光。2003,18:37-41。10.1002 / BIO.703。
- 3.
macarone M, Finazzi AA, Rosato N:超弱光发射是细菌细胞对物理化学压力的一种常见反应。中国生物化学杂志。1998,13:287-293。10.1002 / (SICI) 1099 - 1271 (1998090) 13:5 < 287:: AID-BIO489 > 3.3.CO; 2。
- 4。
Suzuki S, Usa M, Nagoshi T, Kobayashi M, Watanabe N, Watanabe H, Inaba H:植物幼苗超弱辐射模式的二维成像和计数。光化学与光化学,1998,16(1):1- 7。10.1016 / 1011 - 1344(91) 80153 - 9。
- 5。
作者:田春梅,田春梅,田春梅,平松,田春梅:甘薯和枯萎病菌相互作用产生的超弱发光与防御反应。光化学与光化学。
- 6。
利用高灵敏度CCD相机对大豆种子萌发过程中超弱光子辐射进行二维成像。光化学与光化学。
- 7。
Amano T,Kobayashi M,Devaraj B,USA M,Inaba H:移植膀胱癌的Ultrafeak Biophoton发射成像。Urol Res。1995年,23:315-318。10.1007 / BF00300020。
- 8.
Kobayashi M,Takeda M,Sato T,Yamazaki Y,Kineko K,Ito K,Kato H,Inaba H:在大鼠脑中的自发超广差光子发射的体内成像与脑能量代谢和氧化应激相关。Neurosci Res。1999,34:103-113。10.1016 / s0168-0102(99)00040-1。
- 9.
黄志强,黄志强,黄志强:盐胁迫对红豆幼苗生长的影响。应用物理学报。2000,39(4):593 - 598。10.1143 / JJAP.39.3696。
- 10。
OHYA T,Oikawa N,Kawabata R,Okabe H,Kai S:Adzuki Bean Roote的渗透胁迫诱导的生物光源排放。JPN J APPL PHY。2003,42:7625-7628。10.1143 / JJAP.42.7625。[http://jjap.ipap.jp/link?jjap/42/7625]
- 11.
Salin ML, Quince KL, Hunter DJ:机械损伤大豆根组织的化学发光。光化学学报。2003,21(4):457 - 461。
- 12.
Mittlle R:氧化应激,抗氧化剂和应力耐受性。趋势植物SCI。2002,7:405-410。10.1016 / s1360-1385(02)02312-9。
- 13.
Jung S:叶绿素还原的影响拟南芥蒂利亚纳通过甲基己酸酯或Norflurazon抗氧化系统。植物理性生物化学。2004,42:225-231。10.1016 / J.Plaphy.2004.01.001。
- 14.
Havaux M:自发性和热诱导的光子发射:用于检测和定量植物中氧化应激的新方法。趋势植物SCI。2003,8:409-413。10.1016 / S1360-1385(03)00185-7。
- 15.
张志强,王志强,王志强,等。叶绿素荧光在植物模型中的应用。光合作用。1994,30:1-24。
作者信息
隶属关系
通讯作者
额外的信息
作者的贡献
MF-H设计了PiXx*ell 1A发光成像仪。MF-H和MRR构思了本研究,参与了本研究的设计和协调,进行了实验并撰写了论文。MF-H进行数据分析。TCM进行了去氟拉松实验,TCM和GLdB都参与了一些实验设计和执行。所有作者阅读并批准了最终的手稿。
Michel Flor-Henry和Michael R Roberts同样为这项工作贡献。
电子辅料
12870 _2004_43_moesm1_esm.gif
附加文件1:动画GIF文件,显示从五个序贯5分钟的一个控制叶(底部)和四个伤员的图像拟南芥树叶。(GIF 89 KB)
12870_2004_43_moesm2_esm.gif.
附加文件2:动画GIF文件,显示来自两个控制叶(底部)和四个受伤的七个顺序5分钟曝光的图像拟南芥树叶。最初在冷成像阶段的样品中捕获图像,但是当指示时,打开样品级的盖子中的加热器。(GIF 629 KB)
作者的原始提交的图像文件
权利和权限
关于这篇文章
引用这篇文章
Flor-Henry,M.,Mccabe,T.C.,De Bruxelles,G.L.等等。使用高度敏感的二维发光成像系统来监测植物叶中的内源性生物发光。BMC植物BIOL.4,19(2004)。https://doi.org/10.1186/1471-2229-4-19
已收到:
接受:
发表:
关键词
- 叶绿素
- 发光成像
- Norflurazon
- 受伤的叶子
- 短集成时间