摘要
背景
质体基因组含量和蛋白质序列在陆生植物及其近亲藻类中高度保守。寄生植物通过依附于寄主植物而获得部分或全部营养,这通常是一个显著的例外。异养可导致部分质体基因约束放松,甚至全部基因丢失。我们对寄生属的两个物种的质体基因组进行了测序五角和它的非寄生亲戚一起,番薯紫竹,以研究质体基因组的变化,可能导致过渡到寄生的生活方式。
结果
除了失去一切ndh的基因,五角exaltata保留在强选择约束下进化的光合和光呼吸基因。五角obtusiflora它的质体基因组发生了更大的变化,包括失去了质体编码的RNA聚合酶的所有基因。尽管基因含量发生了广泛的变化,整体核苷酸取代率大大提高,c . obtusiflora也保留了所有的光合作用和光呼吸基因,只有一个小例外。
结论
虽然Epifagus virginiana到目前为止,它是唯一一种具有质体基因组测序的寄生植物,已经失去了大量重叠的转移rna和核糖体基因五角在美国,它已经失去了所有与光合作用有关的基因,只保留了一组最不同的基因五角.分析表明,光合作用基因是在任何基因的质体基因组最高的约束五角这表明RuBisCo和通过光系统的电子传递的功能仍然是这些物种质体基因组保留的主要原因。
背景
寄生植物为研究基因组进化的变化提供了极好的机会,这些变化伴随着从自养生活方式到异养生活方式的转变,这种转变在进化过程中发生过多次。在被子植物中,通过直接依附于寄主植物来获取营养的能力已经进化了至少十几倍。1]还有许多植物通过特定的真菌营养相互作用获得大部分或全部营养的例子[2,3.].在叶绿体进化过程中,大约90%参与光合作用的基因已经转移到核基因组,因为它们与自由生活的蓝藻有亲缘关系[4],这些核基因通常很难在非模式生物中进行研究。广泛的基因和基因组重复常常使核基因间的同源性推断变得困难,而一些寄生植物核糖体位点的速率加速表明,核基因序列可能过于分散,无法通过标准PCR进行扩增[5].相比之下,保留在质体染色体上的基因比核基因进化得更慢,它们作为单个的、易于识别的同源体存在于每个质体质体组中,尽管质体染色体本身每个细胞的拷贝数很高[6].
许多种类的寄生植物保留了光合作用的能力,除了与寄主的根有补充联系外,在习性上与完全自养的植物相似[7].然而,另一些则表现出对寄主的依赖性增加,往往达到完全异养和非光合作用的程度。这样的植物通常被认为是“全息寄生虫”,其中一个物种,Epifagus virginiana(Beechdrops, Orobanchaceae)是迄今为止唯一完成全质体基因组测序的寄生植物[8].由于普遍存在的基因缺失,包括所有的光合和光呼吸基因、部分核糖体蛋白基因、许多tRNA基因和质体编码聚合酶基因,使其质体基因组缩小到正常被子植物的一半以下[8,9].尽管发生了如此剧烈的变化,质体转录和内含子剪接仍在发生[9,10],可能是为了产生其余四种与转录或翻译无关的蛋白质。较小规模的研究表明,相关物种的基因组减少类似或更少[11- - - - - -14].对于某些全寄生系而言,功能性质体基因组的存在仍有待证实,尽管初步证据表明,在巴兰科、胞苔科、水螅科和锁蟹科中可能存在极其不同的质体基因组[15,16].
大量关于质体功能的研究已涉及寄生属的成员五角,来源于牵牛花科(旋花科,茄目,菊科)。不同类群间质体超微结构和基因含量差异较大[17],在这个广泛分布和可辨认的属中有超过150种[18].不像Epifagus和其他根寄生科,五角是缠绕的藤蔓,成熟时没有根。相反,它把它的芽像进食器官,吸器,直接进入宿主的茎,侵入脉管系统,获得所有必要的水和其他营养物质。叶子退化成退化的鳞片。尽管有义务依赖他们的主人,许多五角物种显示一些绿色,至少在他们的花序,特别是在成熟的胚珠。Machado和Zetsche证明了RuBisCo、叶绿素和低水平的碳固定的存在五角reflexa亚属的一个成员Monogyna[19].此外,虽然所有的NADH脱氢酶(ndh)基因要么无法检测到,要么没有功能[20.],其他与光合作用有关的基因则以功能形式出现[21].在这个物种中,正常功能的绿色质体定位于茎髓和皮层之间的细胞环,这些细胞环是从大气气体交换中分离出来的,这表明光合作用可能发生在这个物种中,利用循环的呼吸CO2[22]尽管其捕光复合体中的叶黄素循环发生了改变[23].
用poly-A选择的RNA进行点印迹c . reflexa在烟草中101个烟草基因中的一些也显示阳性杂交,尽管这些结果实际上是质体基因的核转录副本、多聚腺苷化质体转录本,还是通过cDNA生成步骤泄漏非多聚腺苷化质体转录本尚不清楚[24].存在不同的情况五角pentagona(亚属Grammica),这种植物缺乏在植物茎中观察到的光合细胞环c . reflexa,但在幼苗和成年植物的绿色组织的质体内的适当位置,具有具有光合作用能力的质体,具有免疫可检测的RuBisCo、光系统和光收获蛋白[25].亚属内的其他种Grammica显示一系列:转录水平,从低到无[17],并且该亚属的样本成员缺乏质体编码聚合酶上游的启动子rrn16而且:基因,虽然转录:在这两种情况下,仍然发生在核编码聚合酶启动子位点[26].存在相互矛盾的证据五角欧洲公司(亚属五角),被描述为缺乏叶绿素和可检测:蛋白质(19],但仍具有绿色和更典型的质体序列,包括:,而不是亚属的成员Grammica[27].其他微小的变化已被检测在质体基因组五角sandwichiana,如删除内含子内部ycf3,收缩反向重复排除rpl2,rpl23,trnI,损失trnV-UAC,尺寸减小ycf2;结尾略有改动atpB,尺寸减小trnL内含子和删除rpl2内含子与其他非寄生的旋花科植物共享,在旋花科植物寄生进化之前就已出现五角[28].
在这项研究中,我们测试了质体基因组的显著变化是否发生在寄生进化之前,如果先前发表的质体基因组进化的观察五角适用于本属其他成员,如果叶绿素含量和分布之间的差异五角物种间质体基因组含量平行差异,质体基因是否保留于五角在强烈的净化选择下仍在进化,质体基因的保留和选择约束是否表明该寄生属的质体具有光合作用。为此,我们测序了两个物种的全质体基因组五角作为近亲的光合作用,番薯紫竹(牵牛花)。番薯是旋花亚纲的一员,旋花亚纲被认为是最有可能的姐妹类群五角在多项研究中[27,29- - - - - -31].五角exaltata亚属的一个成员Monogyna可见叶绿素分布在整个茎和花序五角obtusiflora亚属的一个成员Grammica通常只在花序、果实、饥饿的幼苗和受压的茎尖表现出绿色色素,被选择来代表五角.我们通过比较所有质体基因的同义和非同义替代率,以及功能定义的基因类别,检查了选择性约束的总体替代率和变化,以确定光合基因是否仍然是质体基因组中最保守的基因,以及在该谱系中寄生进化前后,功能约束的放松是否先于基因损失。我们还测试了转移RNA损失的模式、基因间区域的变化和替代率是否与完全非光合作用的情况相似Epifagus virginiana.最后,我们利用光合定位、特定基因丢失和特定基因的强功能约束的累积证据,提出了与卡尔文周期无关的质体基因组的光合功能五角也许还有其他的寄生植物。
结果与讨论
质体基因组大小与反向重复结构
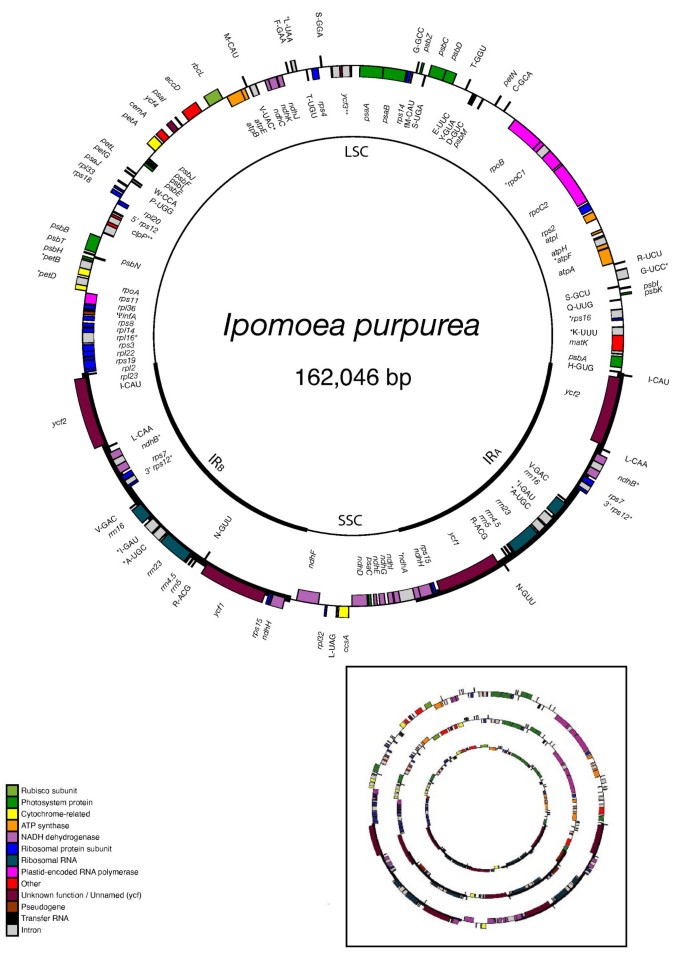
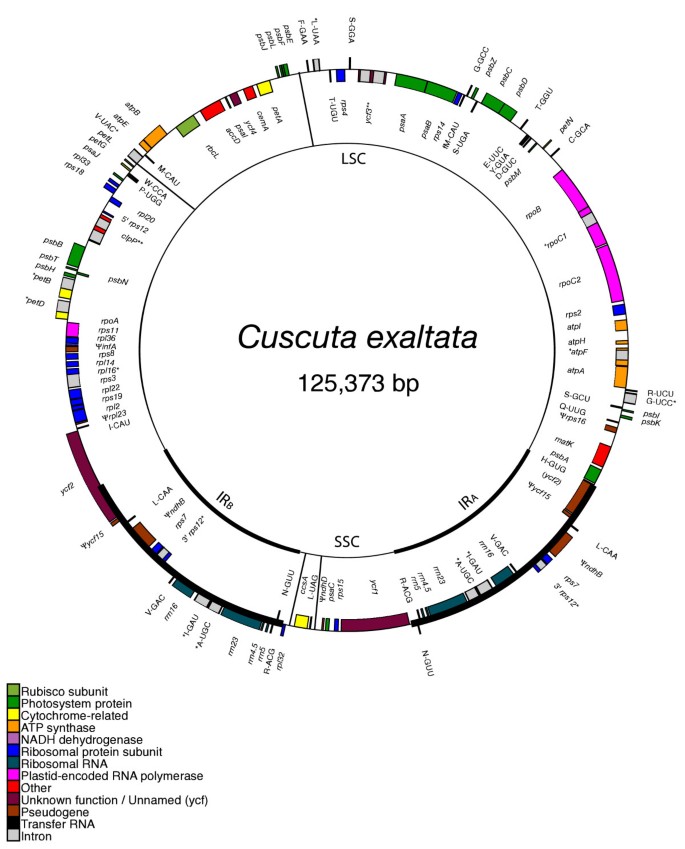
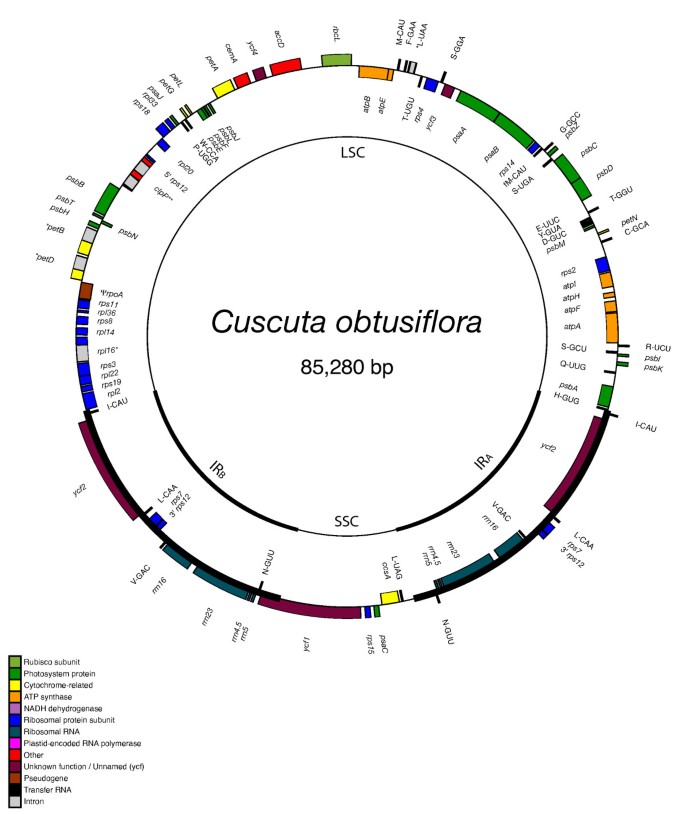
这里介绍的三个质体基因组都有一对大的、倒置的、相同的重复序列(IR),两端由一个大的单拷贝区和一个小的单拷贝区(LSC和SSC)彼此分开,几乎所有植物质体基因组都是如此[32].然而,这三个质体基因组序列之间存在相当大的长度差异,其中最小的基因组,五角obtusiflora在美国,只有一半的面积番薯紫竹(85,280个碱基对对162,046个bp)。五角exaltata中等大小,为125,373 bp(见图。1,2,3.).质体基因组番薯比的略大烟草(155,939 bp),主要是通过IR区域扩展到SSC区域(图。1).而IR烟草几乎没有延伸到ycf1,的IR番薯包括整个ycf1的基因,rps15,ndhH的第一外显子的一小段片段ndhA.相比之下,红外的LSC端略有收缩,不包括rpl2而且rpl23就像在烟草.此前,利用Southern blots以烟草质体片段为探针,根据限制片段的相对大小估计旋花科的质体基因组大小,结果显示,从非寄生虫到旋花科的质体基因组大小也有类似的逐步减小的趋势五角亚属Monogyna对其他各种物种[24].在那项研究中,旋花科的一个非寄生成员关系非常密切番薯,旋花植物薄荷,给出的质体基因组大小估计比我们的大24 KBP番薯紫竹序列(186 KB vs. 162 KB)。相当大的差异可能是由于红外尺寸的更大的增加旋花植物相对于烟草的番薯,或者它可能只是反映了无法使用该研究中使用的粗略限制片段分析正确检测IR边界。五角reflexa在该研究中给出的质体基因组大小估计为122 KBP,这与我们测序的125 KB大小很匹配五角exaltata,也在亚属Monogyna.其他估计五角种类从81 KBP到104 KBP不等,尽管该研究中一些物种的明显错误识别使进一步的系统发育比较变得困难[33].
质体基因含量
基因含量番薯肯定是相似的吗烟草而且Atropa.这三个类群,还有两个五角种,缺一种完整infA[34],表明该基因的丢失可能发生在茄科从旋花科分化之前,两者都属于茄科。这并不奇怪,因为infA在被子植物进化中多次从质体中丢失[35].第二个基因,ycf15,在本研究测序的旋花科类群中缺失,但在茄科和外类群中存在[34,36,37].然而,该基因的功能尚不清楚,其缺失对旋花科植物的影响也难以解释。第三个基因,rpl23,显然是一个假基因Cusucta exaltata完全沉浸在c . obtusiflora,但不清楚它是否在番薯.虽然一个完整的长度开放阅读框存在番薯为rpl23,它包含两个移码突变和3'端延伸。基因似乎也不是在纯化选择性约束下进化的烟草(见图。4),进一步表明它可能是一个假基因,尽管需要进行表达测试来证实这一点。尽管是质体翻译装置的组成部分,这种核糖体蛋白基因亚基在其质体位置的消耗性是由其从质体基因组的损失所支持的菠菜也[37].迄今为止只在茄科成员中发现的基因,sprA[34],在旋花科的所有测序基因组中都没有发现,表明该基因在叶绿体组中的存在仅限于茄科。
令人惊讶的是,在旋花科的三个质体基因组中都发现了一个基因ycf1,一个功能未知的大基因,此前报道为缺失五角和其他三种旋花科[38].该研究使用Southern Blot杂交技术筛查基因存在;ycf1仍然是质体基因组中第二大的开放阅读框,但两者之间的大小变化极大五角种类和大大拉长番薯这些因素可能解释了先前观察到的负杂交现象。尽管它是最不保守的基因之一五角而且番薯作为一个功能基因,它显然仍在选择性约束下进化。情况也是如此ycf15然而,要解释该基因在旋花科中极端分化的后果,还需要充分了解其功能。
基因损失在两者中更为突出五角物种比番薯.所有基因都丢失了c . exaltata也迷失在c . obtusiflora,并且被最朴素地认为是在两个物种的共同祖先中丢失的。这些损失中最引人注目的是ndh基因,所有这些都从质体中完全丢失或者是假基因五角.这证实了所收集的PCR和blot数据五角reflexa这意味着ndh该物种的基因缺失、高度改变或易位[21],以及其他物种的PCR和序列阴性结果[28].所有ndh基因也从质体中丢失Epifagus[9],表明寄生的进化可能促进这些基因的丢失或向核基因组的移动。虽然ndh基因保留在大多数光合植物中,它们也从叶绿体基因组中丢失松果体[39],表明即使在完全自养的植物中,它们在质体基因组中的存在也不是光合作用所必需的。这两个五角物种也缺乏功能性rps16尽管是质体中的基因c . exaltata含有一个假基因,外显子和II组内含子的部分存在于它们之间。最后的基因损失五角也有报道c . reflexa是损失trnK下面部分(40].情况也是如此Epifagus,c . exaltata保留开放的阅读框,matK,包含在该tRNA的内含子内。中的删除trnV-CAU内含子也在c . reflexa[21],与Orobanche小,可能会破坏其剪接[13],但由于两个外显子在这些物种中都保持完整,我们不愿将其称为假基因C.exaltata没有实验证据。除了这些基因的损失,质体基因组的含量c . exaltata和里面的一样吗番薯并且包含了光合作用所必需的一整套基因。
质体基因组重排
在结构上,质体基因组c . exaltata经历了一些变化相对番薯而且烟草.IR的LSC端在两者中都受到限制五角物种,但它显然已经重新扩展到包括一些核苷酸trnH-GUG(4核苷酸在c . exaltata, 6英寸c . obtusiflora).就像在番薯,第一个完整基因在IR的LSC端c . obtusiflora是trnI标出。然而,红外收缩在c . exaltata,rpl2,trnI,超过一半ycf2落在IR之外(图;2).这些基因的假定损失C.reflexaPCR检测[40]很可能是这种收缩的产物,而不是缺失,因为该研究中使用的引物也会显示类似的结果c . exaltata并没有放大相反的LSC/IR连接,而这些基因实际上存在于这个连接上。IR并没有实质性地延伸到SSC五角就像在番薯.事实上,c . exaltata有点收缩相对烟草的开始密码子稍早结束ycf1.就像烟草,的IRc . obtusiflora包含5'末端的一部分ycf1.观测到两个节段反转事件c . exaltata.一个反转发生在trnVuac,psbE在LSC区域,另一个在SSC中只有两个基因,ccsA而且trnLuag。这两种反转都与曾经包含ndh基因。广泛的非编码假基因序列可能有助于改善重复序列的积累,从而促进反转。也许不是巧合,唯一观测到的反转Epifagus是trnL- SSC中的uag [8].
质体基因组变化c . obtusiflora
质体基因组五角obtusiflora令人惊讶的是,相对于烟草而且番薯.不像c . exaltata,c . obtusiflora缺乏广泛的假基因序列,可能已经在有利于反转事件的序列基序有时间发展之前从其质体中清除了这些未使用的DNA。另一方面,基因丢失在体内更为猖獗c . obtusiflora(表1).除了之前讨论过的基因c . exaltata,c . obtusiflora失去了第三个核糖体蛋白基因,rpl32,以及另外5个tRNAs。同样丢失的还有质体编码的RNA聚合酶的所有亚基(rpo)和内含子成熟酶matK,其损失也与基因组中所有IIA组内含子的损失平行,如先前报道的[41].印迹和PCR阴性结果提示质体丢失rpo亚属内其他物种的基因Grammica也[26,28],虽然rrn基因簇和:至少在某些物种中,基因似乎仍然由核编码聚合酶转录[42].尽管从质体中丢失了大量的基因,c . obtusiflora保留叶绿体内直接参与光合作用的所有质体基因,包括所有三磷酸腺苷基因,所有宠物的基因,:,以及所有psa而且公安局基因,除了psaI.该基因是质体中最小的基因之一(36个密码子或更少),尽管它在陆地植物中高度保守。的损失trnV里面有两个内含子ycf3报告为亚属的另一成员Grammica,五角sandwichiana[28],也出现在五角obtusiflora.
质体基因的选择限制
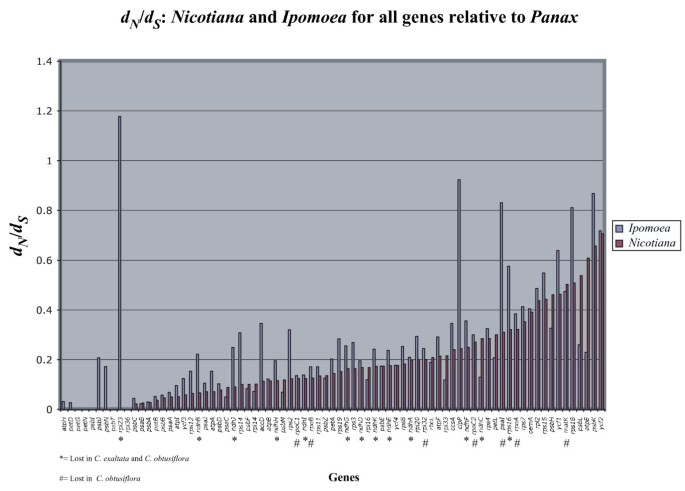
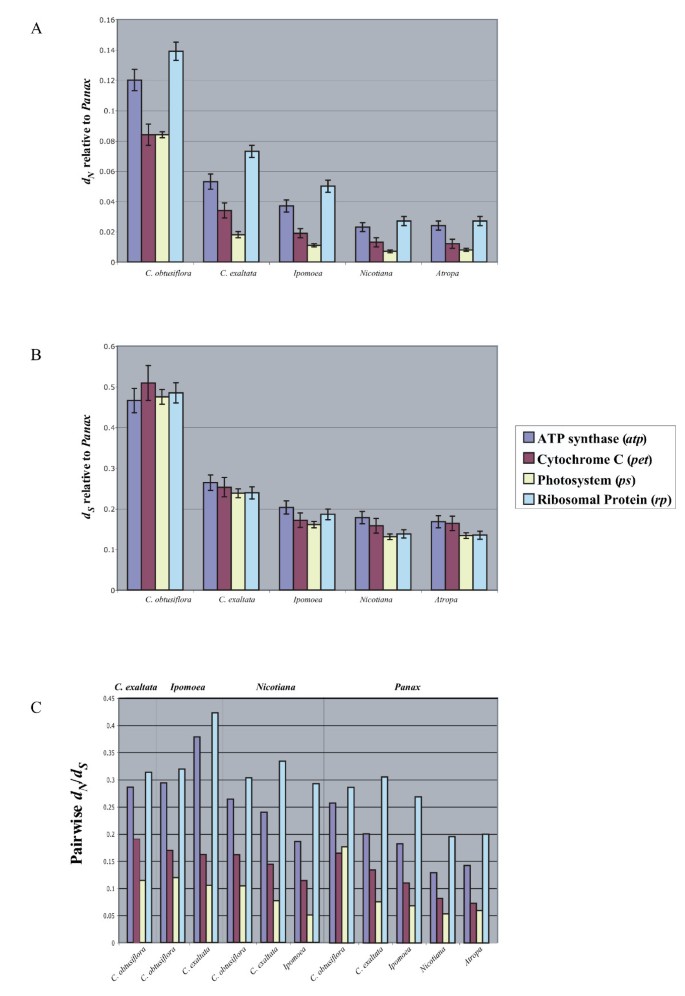
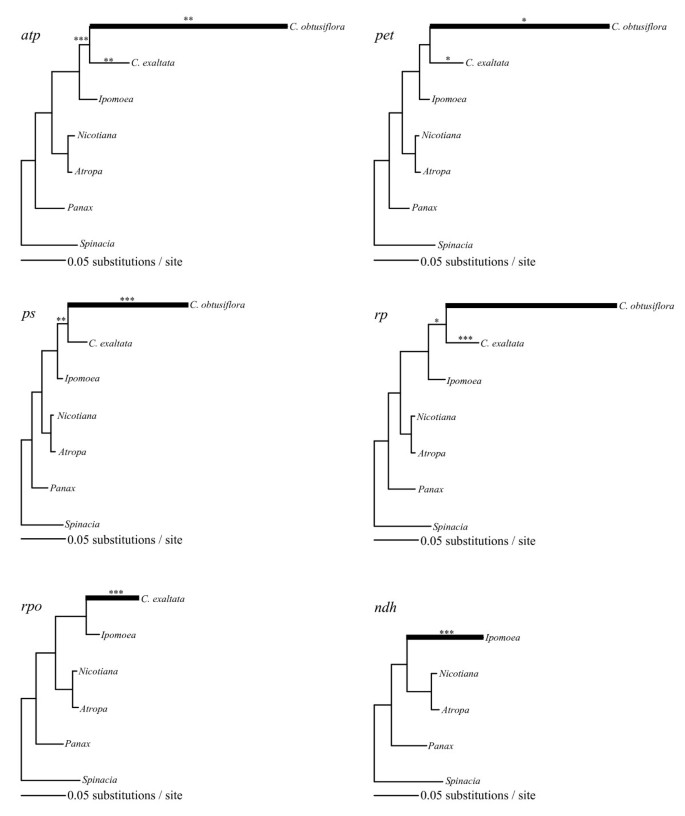
通过这三个新的全质体基因组序列,我们测试了基因的选择压力是否发生了实质性的变化,特别是那些丢失的基因五角,发生在进化之前的寄生在这个世系。计算每个非同义位点的非同义核苷酸取代的校正距离后(dN)和每个同义站点的同义替换(d年代)中所有的基因番薯而且烟草相对于一个普通的外群体,人参在完全自养生物的基因组中,出现了一种有趣的放松选择趋势番薯被揭示(图。4).在这两个类群共有的77个蛋白质编码基因中,有56个(72.7%)的蛋白质编码基因的编码水平较高dN/d年代在番薯比在烟草只有15个基因显示更高dN/d年代在烟草(6个基因不可区分或有dN/d年代两类群均< 0.01)。此外,两者均有12/13的基因丢失五角物种有更高的dN/d年代在番薯表明这些基因可能在旋花科寄生进化之前就已经处于宽松的选择状态。使用似然方法,所有先前定义的基因类别(三磷酸腺苷,宠物,ps,rp,rpo,ndh的例外宠物显示了更大的整体替代率番薯比在烟草在成对相对率测试中使用人参作为一个外组(表2).的组合集分析ndh基因显示,在分枝上,非同义替代率与同义替代率(R)的比值番薯远高于树中通往Solanales的前一个分支,导致在不受约束时,树的可能性存在极其显著的差异(p < 0.0001,表3.),建议放宽选择ndh基因可能在寄生出现之前就开始了。
两两相对比率检验也显示出显著的总体比率差异番薯而且五角exaltata以及两者之间五角所有类型的基因的物种(表2).接下来,我们想测试基因类别之间的整体选择比例是否保持不变五角与自养类群相似。数字5显示了同义和非同义替换的模式如何在取样的茄属分类群之间变化人参用于质体中不同种类的基因。虽然不同基因类之间的同义率有微小的变化,但每个基因类的树拓扑的同义率的相对比率测试没有产生显著的差异(表2).但是,非同义的速率值ps两者的基因明显不同三磷酸腺苷而且rp基因的非同义率和R较低宠物而且ps所有配对比较中的基因(图。5 b而且5度).的趋势五角与其他类群明显对称;所有类别的基因似乎是在强负选择下进化,R远低于1,光系统和宠物基因仍然是最保守的,即使在快速进化的环境中也是如此c . obtusiflora基因组。尽管失去了psaI在c . obtusiflora,两者质体基因组的选择性约束五角物种强烈表明光合作用过程仍然是它们质体基因组的主要目的。
虽然质体基因在五角仍在强烈的负选择下进化,数据表明,与完全自养的亲戚相比,它们有些放松。数字6显示了前面讨论的每个基因类的亲系图,其同义率和R显著增加,由分支上指示的LRTs确定。的整体同义率c . obtusiflora在可研究的四类基因中,其变异为旋花科分支的5到8倍,而C.exaltata几乎完全相同(表3.).这些高度加速的替代率c . obtusiflora这可能是由于更短的世代时间,放松的选择约束允许修复机制受损,或者,也可能是由于较低的生物体或质体基因组种群大小[43].强烈的负选择压力c . obtusiflora,特别是在ps而且宠物尽管核苷酸替代的速度高度加快,但基因的出现进一步支持了这一观点c . obtusiflora一定是利用光合作用基因达到某种对植物很重要的目的。考虑到完全失去质体编码聚合酶,这尤其令人着迷。而Epifagus virginiana已显示在缺乏质体的情况下,核糖体和各种其他蛋白质编码基因的转录rpo基因(9,10],这种现象在任何光合植物中都是未知的。在很大程度上,质体聚合酶在典型的绿色植物中执行光合基因的转录职责,但在植物中似乎发生了戏剧性的转变五角对所有基因导入核聚合酶转录。许多质体基因已知可由这两种聚合酶转录[44],以及是否自养亲戚五角obtusiflora已经具备了用进口核聚合酶转录所有基因的能力,或者新的启动子和转录因子结合位点是否是最近才进化出来的,还有待观察。
质体基因组差异五角与Epifagus virginiana
虽然Epifagus virginiana也经历了类似的质体基因组缩小,它和五角在很多方面都有很大的不同,最明显的是五角保持一组看似有效的光合作用基因Epifagus已经失去了所有这样的基因。失去了rpo在这两个类群的基因中,我们研究了这两个类群是否在基因间区显示了相似的缺失模式,这些区域应该包含质体启动子、转录因子结合位点和其他在核转录质体质体组中不再需要的基序。总的来说,Epifagus蛋白质编码基因少22个,tRNA基因少7个c . obtusiflora.而质体基因组大小Epifagus(70028 bp)比的小了15个碱基以上C.obtusiflora在美国,考虑到整体基因含量的巨大差异,这实际上比预期的要少。在63个非编码基因中,两者的同源功能基因之间的基因间区五角物种,番薯,烟草,c . obtusiflora(11714)经历了49%的总长度相对于烟草(22,996 bp),可能主要是由于质体聚合酶和转录因子结合位点的缺失。c . exaltata在同一地区下降了16%番薯只有1%。共有的16个基因间区域Epifagus,c . obtusiflora下降了33%相对于烟草,而Epifagus下降幅度仅略超过3%(表4).同样,在3个区域中,保守的功能基因与含有同源失效基因的区域可以进行比较Epifagus而且C.obtusiflora,Epifagus显示32%的总减少大小相对于包含功能基因的全长序列烟草,而c . obtusiflora要短85%(表4 b).的IREpifagus与正常被子植物的长度几乎相同,而其SSC和LSC区域几乎是其所有基因丢失的地方。五角obtusiflora在这些区域也有广泛的缺失,但也表现出IR的显著收缩,主要是通过假基因的损失相对于Epifagus.而五角obtusiflora几乎完全缺乏假基因序列,Epifagus保留了相当数量的数据。再加上各种内含子损失,质体基因组c . obtusiflora比的要流线型得多Epifagus.
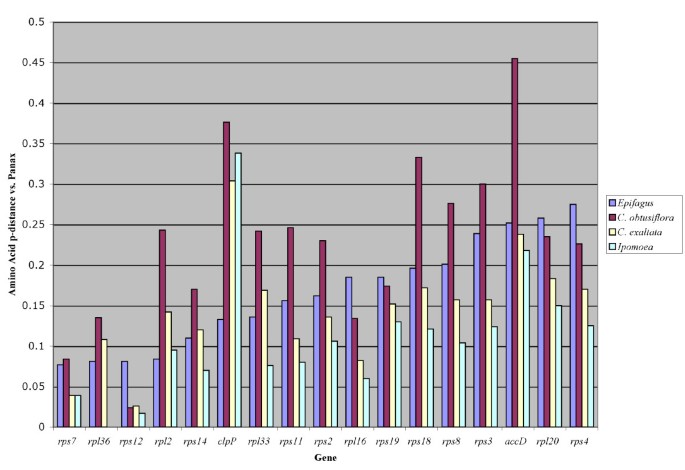
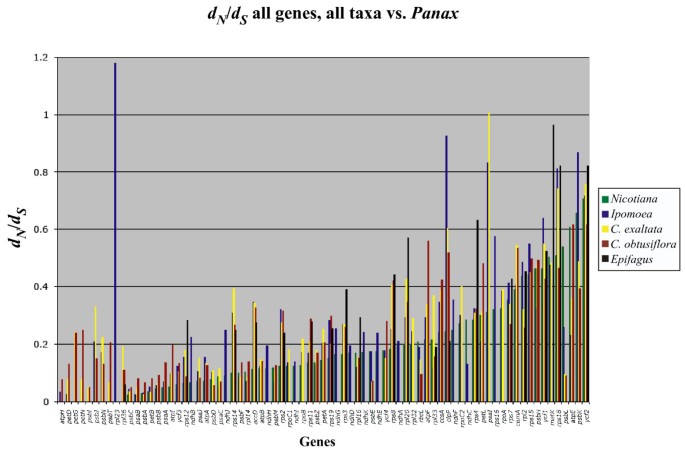
我们还想测试基因是否保留在完全非光合作用的质体中Epifagus受到的限制比假定的光合作用生物要少五角物种。令人惊讶的是,在它们共享的可对齐基因中,C.obtusiflora通常在蛋白质水平上与普通外群更不同,人参(无花果。7).的比较dN/d年代在所有基因中均无明显的变化趋势,其中部分基因受抑制程度较大Epifagus比在c . obtusiflora而其他人则更保守五角(无花果。8).
c . obtusiflora保留了四个蛋白质编码基因Epifagus与转录或翻译无关的,可能是在该物种中保留质体基因组的原因:accD,clpP,ycf1,ycf2[8].accD而且clpP两者都受到较少的限制五角比在Epifagus,在clpP旋花科的三个类群都表现得更高dN/d年代对于两个基因。这对氨基酸分化的影响也是非常明显的。7).clpP对芽的发育至关重要的蛋白酶在体内吗烟草,但它究竟针对哪些蛋白质进行降解仍然未知[45].为什么它在近亲自养生物中如此发散,番薯,也有待推演。的可对齐区域ycf1而且ycf2实际上更低dN/d年代在c . obtusiflora比Epifagus,每个基因的其他区域甚至在蛋白质水平上都是不对齐的五角而Epifagus是相对容易对齐的,整体蛋白质差异实际上要高得多c . obtusiflora比Epifagus在这些基因中。总的来说,除光合基因外,植物的质体基因组五角obtusiflora更精简,约束更少,更发散Epifagus因为他们有共同的基因。这是否意味着更快的整体进化速度c . obtusiflora或者,如果没有精确的年代测定方法和更多的分类单元采样,很难识别在宽松约束下的较长时间的特化寄生虫。
与其他非光合系的比较
尽管在进化模式上存在一些差异,但在生物体内质体基因组的进化过程中存在许多相似之处五角和相关的但独立衍生的寄生谱系Orobanchaceae,包括Epifagus.这两种谱系都显示出总体上核苷酸替代率的增加,选择限制的放松,尽管失去了多个trna,但同义密码子的使用没有任何明显的变化[46)(表5).在两个世系中都观察到大量的基因损失;除了分担所有的损失ndh而且rpo基因与c . obtusiflora,Epifagus从质体基因组中丢失了大量重叠的tRNAs。所有的trna都丢失了C.obtusiflora也迷失在Epifagus除了trnR-ACG,甚至有人认为它是假基因[13].三种核糖体蛋白质丢失c . obtusiflora也有一个子集迷失在六个Epifagus.虽然Epifagus缺乏所有的光合作用基因,其他芒科保留光合作用通常所需的基因,以看似功能的形式。Lathraea clandestina有什么功能:(RuBisCo,大亚基)基因rpo基因也可通过PCR扩增,尽管这种植物显然缺乏叶绿素,除开花期间外,整个生命周期都在地下度过[12].类似地,该属的一些成员Orobanche家族内的其他全息寄生虫也保留了下来:似乎在功能限制下进化的基因[47- - - - - -49].Pholisma是全寄生科莲叶科的一个属,是另一个独立的非光合世系保留的例子:[50].如果没有来自这些植物的完整质体基因组序列,就很难知道它们是否也可能仍然拥有剩余光合作用所需的质体基因的补充五角在这项研究中,它们在任何生命阶段都缺乏明显的叶绿素,并且在它们生命周期的大部分时间里都没有在地面上接触到光。
其他非被子植物中含有质体的寄生虫谱系也表现出质体基因缺失和选择性约束缺失的模式。顶复体的顶质体基因组,被认为是源于质体祖先,更类似于Epifagus比五角因为它们只包含少数不参与转录或翻译的基因,其中没有一个与光合作用有关。然而,没有一个剩余的非转录/翻译基因与之共享Epifagus, RNA聚合酶基因保留在根尖体基因组中[51].裸腺寄生虫不能站立隆也有一个高度减少的质体基因组而喜欢五角保留:[52].非光合藻类质体基因组含量多变;通常在被子植物中发现的唯一不参与转录或翻译的基因是植物的质体基因组Helicosporidium是ycf1而且accD,四个这样的基因中有两个被平行保留Epifagus[53].Prototheca还保留ATP合成酶基因,部分光合装置也保留五角但是迷失在Epifagus[54].虽然存在一些相似之处,但每个独立衍生的寄生虫谱系似乎都遵循着质体基因组减少的独特途径。
脂质生物合成作为光合基因保留的假说五角
虽然有假设,质体基因组必须保留至少最低限度在非光合生物转录trnE,是质体中合成四吡咯的必需产物[55],保持一种保守的光合作用装置五角这表明了质体基因组在这些寄生虫中的另一个重要作用。因为没有大气气体交换发生与叶绿素细胞c . reflexa,呼吸二氧化碳的循环已被提出作为该物种光合作用保留的一种假设,尽管它们的碳水化合物来源显然都来自宿主,但在有光的情况下,确实可以检测到二氧化碳释放的净下降[22].然而,通过卡尔文循环将二氧化碳循环回碳水化合物并不是保持光合作用的唯一潜在原因。另一种可能的解释是光合基因守恒五角以及保留:在其他全息寄生虫中的作用可能在于RuBisCo最近描述的一种涉及脂质生物合成的替代功能,在这种功能中,RuBisCo独立于其先前已知的碳水化合物卡尔文循环生产的作用。在这种替代途径中,多20%的乙酰辅酶a可用于脂肪酸的生物合成,并且减少40%的碳以二氧化碳的形式在绿色种子中损失芸苔属植物显著.这一途径仍然在很大程度上依赖于光合作用光反应过程中产生的ATP和NADPH,尽管RuBisCo在脂质合成中发挥主导作用所需的卡尔文循环所需的ATP和NADPH不足15% [56].这个过程不需要大气中的二氧化碳,这也可以解释在光照下呼吸损失较少的现象[22]时,反应所需的ATP和NADPH就会产生。叶绿素在发育中的胚珠和种子中最集中五角obtusiflora亚属中的近亲Grammica就像五角pentagona,在髓和皮质之间缺乏环状的叶绿素细胞[57].因为五角物种在萌发后必须存活足够长的时间来寻找并依附于寄主,利用光合作用的这种替代功能来有效地为种子分配脂质,并在自由生活的幼苗中有效地使用碳,这可能解释了这种寄生谱系中需要完整的光合器官。
使用RuBisCo进行脂质生物合成也可以解释保留:在其他全寄生被子植物质体和寄生裸腺中不能站立.质体基因质体基因组被转录的少数基因之一Epifagus而且Helicosporidium,accD,是乙酰co-A羧化酶的一个亚基,这表明脂质生物合成在这些物种中仍然是质体的重要功能。在许多非光合非被子植物中,脂质生物合成已被实验证明是顶质体和质体的主要功能[58,59].植物光合组织的未来生理学研究五角以及其他的寄生植物,它们的质体基因组可能在很大程度上(如果不是完全的话)失去了主要的光合作用,这应该有助于更好地理解质体基因组在寄生植物和自养植物中可能的替代作用。
结论
通过对该属两种寄生被子植物的全质体基因组进行测序五角它是一种非寄生的近亲,番薯,我们已经能够更好地理解异养生物中质体基因组的定向缩小,因为对光合作用产生碳水化合物的依赖减少。与寄生被子植物已有的基因组相比,这些基因组得到了极大的补充Epifagus virginiana;通过研究这两种寄生谱系之间的异同,我们更清楚地揭示了在向异养过渡的过程中,质体基因组的哪些变化可能发生,哪些可能是缺乏叶绿素的植物所特有的,哪些可能是特有的谱系五角.我们发现ndh在向寄生转变的过程中,基因是唯一失去功能的基因五角而编码材料和非编码材料更广泛的丢失则发生在最近。尽管质体在基因组中大量减少五角在美国,最保守的基因仍然是那些直接参与光合作用的基因,而那些与完全非光合作用的基因共享Epifagus是最不保守的物种之一。我们假设,对剩余光合基因的高度限制可能表明这些基因产物在脂质生物合成中发挥重要作用,而不是通过卡尔文循环产生碳水化合物。
方法
质体基因组测序、组装与注释
所有三个物种的种子都在宾夕法尼亚州立大学生物温室中发芽和生长。的一种传家宝品种番薯紫竹“Ott爷爷的”,用于降低样本内异质性的可能性。用1克幼叶组织进行DNA分离番薯.从自育亲本植物中收集的非常绿色的幼苗中提取一克组织用于五角exaltata, 1克茎尖组织用于五角obtusiflora.使用CopyControl fosmid文库生产试剂盒(epiccentre, Madison, WI)从提取的DNA构建部分fosmid文库。根据McNeal等人[60].为每个物种选择覆盖整个质体基因组的克隆子集,并根据前面描述的方法对克隆进行鸟枪测序和组装reads [61].基因组注释使用DOGMA完成[62]结合之前从可用的相关物种注释的基因的手动序列比对。序列存入Genbank,登录号EU118126 (番薯), eu189132 (c . exaltata)及EU189133 (c . obtusiflora).
分子进化分析
在PAUP*4.0b10中构建各基因的系统发育关系[63]在各种最大简约性、邻居连接和最大似然标准下,包括以下相关类群,其完整质体基因组序列公开可用:烟草(Genbank加入NC 001879)和Atropa belladona(茄科,茄科,茄科),人参(NC 006290)(五瓣科,蜂科,菊科),和菠菜oleracea(NC 002202)(石龙科)为外群。所有测序的基因看起来都是同源的,与预期的系统发育只有微小的、方法依赖的畸变,这可能是由于类群之间的极端速率异质性[64].在一般时间可逆模型下进行的最大似然分析在从数据中获得预期的系统发育方面最为准确,该模型具有位点间变异的伽玛分布(GTR+gamma)和从数据中估计的模型参数,并用于组合基因数据集的后续系统发育重建。
每个同义站点的同义替换的两两估计(d年代)和每个非同义位点的非同义核苷酸取代(dN)和标准误差采用MEGA 2.1的Kumar方法计算[65为每个基因以及一起编码较大蛋白质亚单位的基因类别。ATP合成酶基因,6个基因,4344个对齐字符(三磷酸腺苷);细胞色素b6/f复合亚基,6个基因,2622个排列特征(宠物);光系统I和II蛋白亚基,19个基因,11730个排列特征(psa而且公安局=ps);大小核糖体蛋白亚基,17个基因,7686个排列特征(rpl而且RPS = rp);质体编码RNA聚合酶4个基因,11958个排列特征(rpo);nadh -脱氢酶,11个基因,10653个对齐字符(ndh)是预先确定的基因类别。成对d年代,dN,并计算氨基酸之间的p距离Epifagus virginiana而且人参这是最接近它和的可用外群五角.
在HYPHY .99beta包中的MG94 × HKY 3 × 4密码子模型下,计算了组合基因数据集系统发生的每个分支的同义替代率的最大似然估计和非同义与同义率的比值(R) [66].HYPHY还用于在具有普遍约束同义率的树之间进行似然比检验(LRTs),以及R与各参数在一个分支上不受约束的树之间进行似然比检验。旋花科的分支(番薯+两个五角物种),五角,而每个人五角用这种方法测试物种的显著p值。此外,对每个基因类进行了成对相对率检验,使用不同的分类群组合,所有参数受约束为原假设,所有参数不受约束为备用假设。在HYPHY中,以同义或非同义距离约束为零假设的组合数据集之间进行成对相对比值检验,以确定两种基因类别之间是否存在显著异质性。对每个分支的参数进行独立估计。最后,GCUA [67]用于确定每个基因组的所有编码序列中相对同义密码子的使用,以确定可能伴随tRNA丢失或光合作用选择放松的密码子偏误的任何变化。
证明说明
两个额外的五角质体基因组序列被公布(Funk et al.;BMC植物生物学2007年,7当前位置在我们审稿的后期。虽然在我们的手稿数据的分析表明很少重叠,质体基因组结构和含量五角reflexa手稿中与我们的数据非常相似五角exaltata.同样,的序列五角gronovii显示类似的结构和基因含量五角obtusiflora.
参考文献
- 1.
Barkman TJ, McNeal JR, s.l, Coat G, Croom HB, Young ND, dePamphilis CW:线粒体DNA提示被子植物寄生的12个起源,并暗示寄生植物是水平基因转移的载体。将提交给美国国家科学院院刊。
- 2.
Bidartondo MI, Bruns TD:寄生单对虾科(Ericaceae)的极端特异性:广泛的系统发育和地理结构。生态学报,2001,30(4):357 - 357。
- 3.
Bidartondo MI, Redecker D, Hijri I, Wiemken A, Bruns TD, Dominguez L, Sersic A, Leake JR, Read DJ:以丛枝菌根真菌为特征的寄生植物。自然科学,2002,29(4):389-392。
- 4.
Martin W, Herrmann RG:基因从细胞器转移到细胞核:多少,发生了什么,为什么?植物生理学报,1998,18(3):344 - 344。
- 5.
Nickrent DL, Starr EM:全寄生开花植物中核小亚基(18S) rDNA的高核苷酸替代率。分子进化学报,1994,39:62-70。
- 6.
Wolfe KH, Li WH, Sharp PM:植物线粒体、叶绿体和核dna的核苷酸替代率差异很大。美国国家科学院学报,1987,84:9054-9058。
- 7.
寄生开花植物生物学。伯克利和洛杉矶,加州大学出版社1969年。
- 8.
王晓明,王晓明,王晓明:非光合寄生植物最小质体基因组的功能和进化。美国国家科学院学报,1992,89:10648-10652。
- 9.
dePamphilis CW, Palmer JD:寄生开花植物质体基因组光合和氯呼吸基因的损失。自然学报,2000,28(3):337-339。
- 10.
Ems SC, Morden CW, Dixon CK, Wolfe KH, dePamphilis CW, Palmer JD:非光合植物Epifagus virginia质体rna的转录、剪接和编辑。植物学报,2004,26(3):349 - 349。
- 11.
Delavault P, Sakanyan V, Thalouarn P: rbcL和atpB两个质体基因在非光合寄生植物中的发散进化。植物学报,2004,27(3):379 - 379。
- 12.
Delavault PM, Russo NM, Lusson NA, Thalouarn PA:一种叶绿素寄生植物——密地草的还原质体基因组的组织。植物生理学报,1996,16(3):344 - 344。
- 13.
Lohan AJ, Wolfe KH:非绿色植物质体DNA中保守tRNA基因的一个子集。遗传学报,1998,15(4):425-433。
- 14.
Wimpee CF, Morgan R, Wrobel RL:寄生植物中质体16S-23S核糖体rna基因间隔的转移rna基因丢失。《现代遗传学》,1992,21:417-422。
- 15.
Nickrent DL, Yan OY, Duff RJ, dePamphilis CW:非小行星全寄生开花植物有质体基因组吗?植物学报,1997,34:717-729。
- 16.
Nickrent DL, Duff RJ, Konings DAM:全寄生被子植物中质体来源的16S rrna的结构分析。植物学报,1997,33(3):344 - 344。
- 17.
van der Kooij TAW, Krause K, Dorr I, Krupinska K:寄生开花植物菟丝子属质体的分子、功能和超微结构特征。植物学报,2000,29(3):357 - 357。
- 18.
Yunker TG:菟丝子属。陶里植物俱乐部回忆录,1932,18:113-331。
- 19.
马查多,马泽哲,王晓明:全寄生虫cucuta reflexa和cucuta europaea质体的结构、功能和分子分析。植物学报,1998,18(3):344 - 344。
- 20.
Haberhausen G, Zetsche K:全寄生开花植物cucuta reflexa质体基因组中ndh基因的功能缺失。植物学报,2004,27(3):357 - 357。
- 21.
黄志刚,张志刚,张志刚:全寄生开花植物菟丝子(cucuta reflexa)叶绿体基因组光合基因的结构和序列。中国生物医学工程学报,2002,23(3):344 - 344。
- 22.
Hibberd JM, Bungard RA, Press MC, Jeschke WD, Scholes JD, Quick WP:寄生被子植物cucuta reflexa光合代谢的定位。植物学报,1998,29(4):528 - 528。
- 23.
Bungard RA, Ruban AV, Hibberd JM, Press MC, Horton P, Scholes JD:植物中不同寻常的类胡萝卜素组成和一种新型叶黄素循环。美国国家科学院学报,1999,96:1135-1139。
- 24.
李志刚,李志刚,李志刚:寄生性植物菟丝子(cucuta)叶绿体基因组结构与光合能力的丧失。实验植物学杂志,2005,26(3):344 - 344。
- 25.
谢尔曼TD, Pettigrew WT, Vaughn KC:菟丝子叶绿体的结构和免疫特性。植物生理学报,1999,30(4):344 - 344。
- 26.
Krause K, Berg S, Krupinska K:全寄生植物cucuta属的质体转录:rn16 pep启动子和编码质体编码RNA聚合酶的rpoA和rpoB基因的平行缺失。植物学报,2003,26(3):344 - 344。
- 27.
Stefanovic S, Krueger L, Olmstead RG:旋花科植物的单系性及其基于多叶绿体位点DNA序列的主要世系界限。植物学报,2002,29(4):531 - 531。
- 28.
李文杰,李文杰:旋花科植物质体基因组进化的滑坡效应。中国生物工程学报,2005,29(3):344 - 344。
- 29.
Stefanovic S, Austin DF, Olmstead RG:旋花科的分类:系统发育方法。系统植物学,2003,28:791-806。
- 30.
Stefanovic S, Olmstead RG:检测寄生植物(菟丝子科,旋花科,菊科)的系统发育位置:贝叶斯推断和从三个基因组中提取数据的参数引导。中国生物工程学报,2004,29(3):344 - 344。
- 31.
Neyland R:从大的核糖体亚基(26S) rDNA序列推断,Cuscuta是旋花科的派生成员。《中国科学》,2001,29(4):344 - 344。
- 32.
Palmer JD:叶绿体基因组的比较组织。杨文杰,2005,30(4):344 - 344。
- 33.
McNeal JR:寄生植物菟丝子属(菟丝子属)的系统分类和质体基因组进化第五章:“隐光合寄生植物菟丝子属(旋花科)的系统分类和质体基因组进化”。生物系。宾夕法尼亚州立大学,2005年。
- 34.
Schmitz-Linneweber C, Regel R, Du TG, Hupfer H, Herrmann RG, Maier RM:茄属质体染色体及其与烟草的比较:RNA编辑在植物物种形成过程中产生分化的作用。分子生物学与进化,2002,19:1602-1612。
- 35.
Millen RS, Olmstead RG, Adams KL, Palmer JD, Lao NT, Heggie L, Kavanagh TA, Hibberd JM, Giray JC, Morden CW, Calie PJ, Jermiin LS, Wolfe KH:被子植物进化过程中叶绿体DNA中多个因子的平行损失,并多次独立转移到细胞核。植物学报,2001,13:645-658。
- 36.
金kj,李海林:高丽参叶绿体全基因组序列及17种维管植物的序列进化比较分析。中国生物医学工程学报,2004,30(4):344 - 344。
- 37.
Schmitz-Linneweber C, Maier RM, Alcaraz JP, Cottet A, Herrmann RG, Mache R:菠菜质体染色体:完整的核苷酸序列和基因组织。植物学报,2001,30(4):357 - 357。
- 38.
杜尼·SR,帕尔默·JD:叶绿体DNA重排在植物系统发育重建中的应用。植物分子系统学“,”编辑:Soltis DE, Soltis PS和Doyle JJ。1992年,英国伦敦,查普曼和霍尔,14-35。
- 39.
Wakasugi T, Tsudzuki J, Ito S, Nakashima K, Tsudzuki T, Sugiura M:通过对黑松松(Black Pine us thunbergii)整个叶绿体基因组测序确定所有ndh基因的丢失。美国国家科学院学报,1994,91:9794-9798。
- 40.
庞默D, Haberhausen G, Zetsche K:全寄生开花植物cucuta reflexa的质体DNA中两个核糖体蛋白(rpl2, rpl23),一个转移rna (trnI)和orf2280同源物的大量缺失。中国生物医学工程学报,1993,24:171-176。
- 41.
McNeal JR:寄生植物菟穗子属的系统学和分子进化中“内含子的消失促进适应性变化和高度保守的成熟酶的丢失”。生物学系,2004年,宾夕法尼亚州立大学帕克分校
- 42.
Berg S, Krause K, Krupinska K:两种铜属植物C. groonovii和C. subinclusa的rbcL基因由核编码质体RNA聚合酶(NEP)转录。植物学报,2004,29(4):344 - 344。
- 43.
Mogensen HL:植物细胞质遗传的方式和原因。中国植物学报,2004,27(3):344 - 344。
- 44.
Liere K, Maliga P:光合作用的调控。2001,多德雷赫特,波士顿,伦敦,克鲁威学术出版社,11:29-49。高等植物中的质体RNA聚合酶,Aro E和Andersson B,光合作用和呼吸的进展,
- 45.
Kuroda H, Maliga P:质体clpP1蛋白酶基因对植物发育至关重要。自然科学学报,2003,29(2):344 - 344。
- 46.
Morden CW, Wolfe KH, Depamphilis CW, Palmer JD:非光合植物中的质体翻译和转录基因-完整,缺失和伪基因。中国机械工程学报,2001,30(4):388 - 388。
- 47.
李本,李志强,李志强,李志强:洞穴小龙虾和非光合植物系选择性约束丧失试验的功率分析。分子生物学与进化,2002,19:1292-1302。
- 48.
Wolfe AD, dePamphilis CW:放松功能约束对光合和非光合寄生植物光合基因rbcL的影响。分子生物学与进化,1998,15:1243-1258。
- 49.
Wolfe AD, dePamphilis CW: Orobanche四种非光合物种光合基因rbcL的交替进化路径。植物学报,1997,33:965- 966。
- 50.
Bremer B, Bremer K, Heidari N, Erixon P, Olmstead RG, Anderberg AA, Kallersjo M, Barkhordarian E:基于3个编码和3个非编码叶绿体DNA标记的小行星系统发育及非编码DNA在更高分类水平的应用。分子系统发育与进化,2002,24:274-301。
- 51.
Wilson rpm, Denny PW, Preiser PR, Rangachari K, Roberts K, Roy A, Whyte A, Strath M, Moore DJ, Moore PW, Williamson DH:疟原虫恶性疟原虫质体样DNA的完整质体基因图谱。分子生物学杂志,1996,26(3):344 - 344。
- 52.
Gockel G, Hachtel W, Melkonian M:非光合裸鳃鞭毛虫质体基因组的完整基因图谱。生物工程学报,2002,23(3):357 - 357。
- 53.
deKoning AP, Keeling PJ:寄生绿藻Helicosporidium sp.的完整质体基因组序列高度还原和结构。生物工程学报,2006,4:
- 54.
Knauf U, Hachtel W:编码ATP合成酶亚基的基因在异养藻原膜藻(Prototheca wickerhamii)的还原质体基因组中是保守的。分子遗传学与基因组学研究,2002,26(4):492-497。
- 55.
李志刚,李志刚:质体基因组在非光合生物中的保留机理。植物科学进展,2006,11:101-108。
- 56.
Schwender J, Goffman F, Ohlrogge JB, Shachar-Hill Y: Rubisco去除Calvin循环可提高绿色种子的碳效率。自然科学学报,2004,29(3):344 - 344。
- 57.
谢尔曼TD, Pettigrew WT, Vaughn KC:菟丝子l -叶绿体的结构和免疫特性。植物生理学报,1999,30(4):344 - 344。
- 58.
Waller RF, Keeling PJ, Donald RGK, Striepen B, Handman E, langunnasch N, Cowman A, Besra GS, Roos DS, McFadden GI:弓形虫和恶性疟原虫的核编码蛋白靶质体。中国生物医学工程学报,2004,27(3):357 - 357。
- 59.
李丽娟,李丽娟,李丽娟:绿藻原乳藻非光合质体的多重代谢作用。中国生物医学工程学报,2005,30(4):344 - 344。
- 60.
McNeal JR, Leebens-Mack JH, Arumuganathan K, Kuehl JV, Boore JL, dePamphilis CW:利用部分基因组fosmid文库测序完整的细胞器基因组。生物技术,2006,41:69-73。
- 61.
Jansen RK, Raubeson LA, Boore JL, dePamphilis CW, Chumley TW, Haberle RC, Wyman SK, Alverson AJ, Peery R, Herman SJ, Fourcade HM, Kuehl JV, McNeal JR, Leebens-Mack J, Cui L:获取和分析全叶绿体基因组序列的方法。酶学研究进展。2005,34(3):348- 348。
- 62.
杨晓明,杨晓明,杨晓明,等:基于DOGMA的细胞器基因组自动注释。生物信息学,2004,20:352 - 355。
- 63.
Swofford DL: PAUP*。利用简约(*和其他方法)的系统发育分析。2002年,马萨诸塞州桑德兰,辛瑙尔协会,4.0b10版
- 64.
Felsenstein J:在这种情况下,简约和兼容方法会产生积极的误导。系统动物学,1978,27:401-410。
- 65.
库马尔,田村K, Jakobsen I, Nei M:分子进化遗传学分析(MEGA) 2.1版。2000
- 66.
Kosakovsky-Pond SL, Frost SDW, Muse SV: HyPhy:使用系统发育的假设检验。生物信息学,2004,bti079。
- 67.
McInerney JO: GCUA(通用密码子使用分析)。生物信息学,1998,14:372-373。
确认
我们要感谢Mauricio Bonifacino和Daniel Austin为研究获取植物材料提供的帮助,感谢Tony Omeis的温室援助,感谢Tim Chumley的技术支持,感谢Robert Jansen的一般支持和鼓励,感谢David Geiser、Stephen Schaeffer、Andrew Stephenson和Kai Müeller对手稿的批判性审查。我们也感谢宾夕法尼亚州立大学生物系的支持,包括授予JRM的Henry W. Popp奖学金。本研究由美国国家科学基金会DEB-0206659和DEB-0120709资助,部分在美国能源部科学、生物和环境研究项目办公室的赞助下进行,由加州大学劳伦斯伯克利国家实验室根据合同编号进行。DE-AC02-05CH11231。
作者信息
从属关系
相应的作者
额外的信息
相互竞争的利益
作者声明不存在相互竞争的利益。
作者的贡献
JRM对植物进行栽培,制作和筛选部分基因组fosmid文库,批注和分析质体基因组,并撰写稿件。JVK对选定的fosmid克隆进行亚克隆、测序和组装。JLB和CWD帮助构思、设计和协调研究,并对手稿编辑做出了巨大贡献。所有作者都阅读并批准了最终的手稿。
权利和权限
本文由BioMed Central Ltd授权发布。这是一篇开放获取文章,根据创作共用属性许可协议(http://creativecommons.org/licenses/by/2.0),允许在任何媒介上不受限制地使用、传播和复制,前提是正确地引用原始作品。
关于本文
引用本文
麦克尼尔,j。r。库尔,j。vet al。完整的质体基因组序列表明寄生植物属中光合基因的保留有很强的选择作用五角.BMC植物生物学7,57(2007)。https://doi.org/10.1186/1471-2229-7-57
收到了:
接受:
发表:
关键字
- :
- 番薯
- 质体基因组
- 选择性约束
- 寄生植物