摘要
背景
第一个植物基因组测序显示,细胞色素P450已经进化成为二次代谢中最大的酶家族。然而,具有特征生化功能的P450酶的比例非常小。如果P450的多样化反映了化学多样性的进化,这表明人们对植物代谢的理解出乎意料地贫乏。我们假设对基因表达的广泛分析可能会引导P450酶的功能,并强调植物代谢中被忽视的方面。
结果
我们创建了一个全面的数据库“CYPedia”,描述了P450基因在四个数据集中的表达:器官和组织、应激反应、激素反应和突变体拟南芥,基于公开Affymetrix ATH1微阵列表达数据。然后将P450的表达与4,130个重新注释的基因的表达结合起来进行共表达分析,这些基因被预测在植物代谢中起作用。基于不同途径注释数据库中共表达基因的注释,确定了共表达途径。对大多数具有已知功能的p450进行了预测验证。举例来说,p450的共表达结果与质体功能/光合作用以及苯丙素、三萜和茉莉酸代谢有关。
结论
本文提出的大规模假设生成工具为植物代谢中的许多p450提供了新的途径、意想不到的功能和调控网络。这些现在可以被社区利用,通过反向遗传学、生物化学和代谢谱实验来验证所提出的功能。
背景
细胞色素P450单加氧酶在植物代谢中催化底物、区域和立体特异性的氧合步骤,已经发展成为一个巨大的酶超家族。植物基因组测序计划最近揭示了39个全长P450基因衣藻reinhartii在青苔中Physcomitrella金属盘, 246英寸拟南芥米356英寸,米312英寸杨树trichocarpa(1]。然而,根据最近的一项调查[2]中,246个编码序列中只有41个答:芥基因组与特定的生化功能有关。P450超家族的高度复杂性,相对于单个P450酶功能的相对稀缺的可用信息,是第一次测序植物基因组的惊喜之一[3.- - - - - -5]。假设植物中P450的数量和多样性反映了化学、生态和生物多样性的进化,这表明即使在模式植物中,人们对次生代谢的理解也出乎意料地贫乏。这使我们假设,对P450基因表达的广泛分析实际上可能用于识别代谢网络,突出被忽视的植物代谢方面,并揭示“孤儿”P450酶的功能。
对已测序的生物体(包括植物)中P450基因的广泛和持续的注释正在进行中,并已在由David Nelson维护的田纳西大学网站上公开发布(表1)1)。注释的答:芥P450基因也被不同的组织在其他数据库中进行了整理和整理(表1)1)。它们包括基因组,cDNA和蛋白质序列,遗传图谱,系统发育,功能,可用突变体和基于精品P450基因微阵列的组织特异性基因表达的评论。另一方面,个体P450基因的表达信息可以从大规模的数字基因表达数据库中获得。还有一些大规模的共表达工具可用于将感兴趣的基因的表达谱与单个基因或微阵列上可用的所有基因进行比较[6- - - - - -10)(表1)。
这些资源被用作创建综合数据库“CYPedia”(参见URL的可用性和需求部分)的起点,该数据库将大规模的P450(共)表达式数据与功能注释结合在一起。第一步,从公开可用的实验中提取Affymetrix ATH1微阵列数据,生成所有p450的综合基因表达矩阵。在第二步中,每个P450基因的表达与4,130个经过精心重新注释的植物代谢基因的表达之间的相关性进行了检测。这种比较分析揭示了大多数P450的高度复杂和分化的表达模式,并为P450的功能、相关通路和相应的调控网络提供了新的线索。本文介绍了该数据库的结构、内容,并提供了一些可以从中提取的一般信息和更具体的信息的示例。
结果与讨论
P450基因家族信息及表达数据
共有271辆p450从答:芥已列入PlaCe拟南芥P450数据库[11]。使用相应的位点标识符(Atxgxxxxx),发现227个基因在由216个探针集代表的Affymetrix ATH1微阵列上表示(详见方法)。所有P450基因的列表,相关的AGI位点,以及使用的探针集可以在附加文件中找到1以及“CYPedia”的主页。还提供了对其生化功能的描述(如果已知),并链接到相关出版物以及外部数据库中的信息,例如“MAtDB”,“TAIR”或“SIGnAL”(表1)1)。我们从“genevestiator Digital Northern”工具中检索了所选探针组的标准化基因表达数据[10],覆盖了1800多个微阵列。经过背景校正后,将每个实验的重复平均强度比分为以下四类:i)野生型植物的器官和组织样本(与背景水平相比),ii)野生型植物的胁迫处理(与未处理的对照相比),iii)激素、营养(剥夺)和其他处理(与对照相比),iv)突变植物(与野生型样本相比)。
器官和组织特异性表达
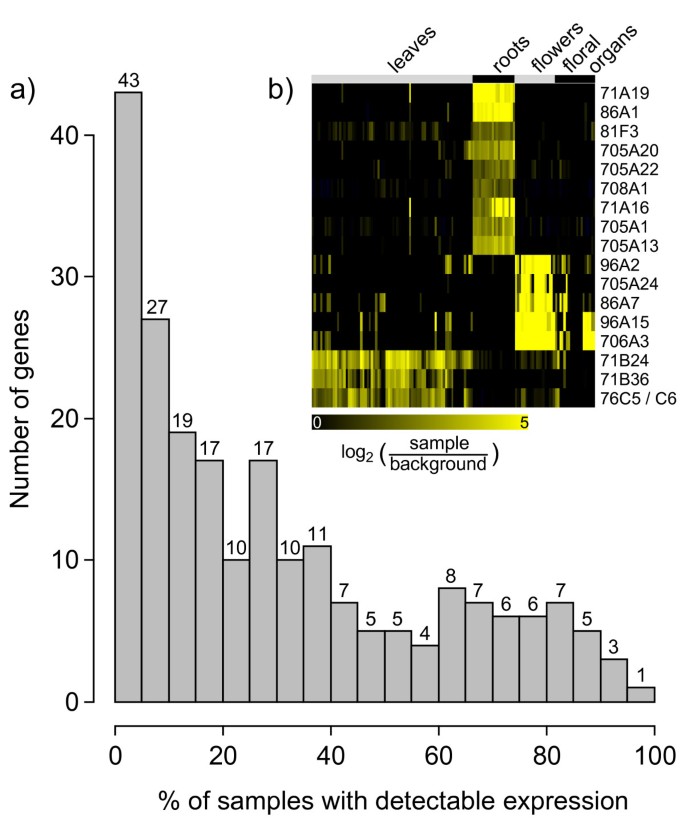
在整个器官和组织数据集中,只有7个P450基因(由6个探针组表示)在任何样本中表达不超过背景的两倍。另外6个基因(由5个探针组表示)仅在一个样品中表达,两个基因仅在两个样品中表达(附加文件)1)。因此,这些可能被认为是在器官样本集中无法检测到的表达。该组包括Affymetrix阵列上表示的所有假定的假基因。相反,93个探针组在两个以上的实验中确实表现出表达,但在277个器官和组织样本中不到20%(附加文件)1;对应于图中的前四个箱子1),表明阵列上43%的P450基因高度特化表达。花、根或叶特定的p450群是明显的。例如,56个探针组在超过80%的所有根样本中表现出表达(背景以上两倍)(23次实验);其中,有9个在不到20%的其他样本中表达(图2)1 b)。利用相同的定义,我们还鉴定出5种花特异性和4种叶特异性p450。这些代表了最特异表达的基因(图2)1 b)。另一方面,只有16个探针组表明在超过80%的组织和器官样本中表达(附加文件)1),相应的18个P450基因可以被认为是组成性表达基因或管家基因(图中最后四个格子)1)。完整的P450器官和组织表达矩阵可以在“CYPedia”网页上的“查看矩阵”链接中找到。
器官和组织数据集中的表达。微阵列数据从genevestiator数据库中检索。每个探针集的背景被定义为所有样本的平均强度,探针集被称为“缺失”(不显著高于用相应的错配探针集观察到的信号(p < 0.06))。a)描述P450基因在器官和组织数据集中表达频率分布的直方图。在277个器官和组织杂交实验中,给出了在0% ~ 5%、5% ~ 10%等范围内表达高于背景两倍以上的P450基因的探针组数,最高可达95% ~ 100%。每个箱中的基因数量在每个箱的顶部给出。b)选择在超过80%的根、全花或叶片样本(大于背景的两倍)中表达的基因,而在所有其他样本(总共277个样本)中表达的基因不超过20%。如上所示,这些基因在叶、根和花样品中的表达数据。将表达强度与背景(定义为所有被称为“缺席”的样本的平均强度)进行比较。
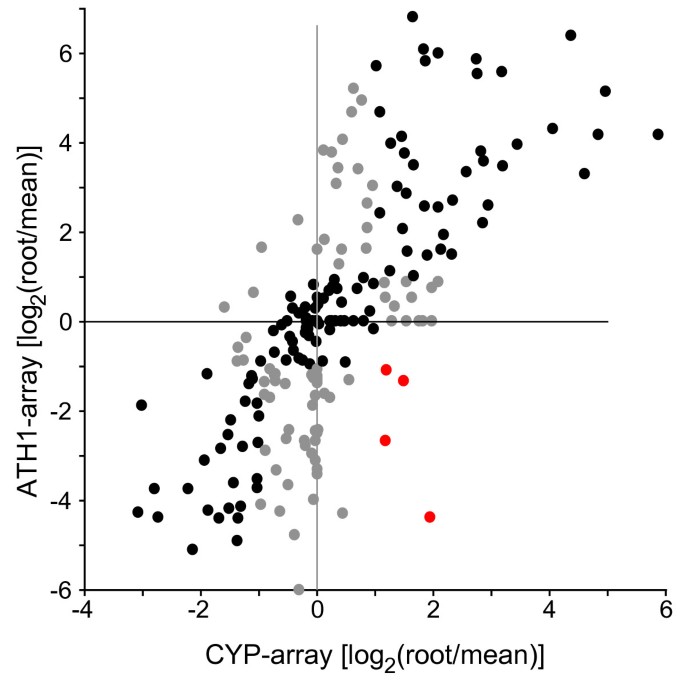
我们将高特异性基因的表达与通过定位基因特异性PCR产物生成的专用P450阵列生成的表达数据进行了比较[2]。这里鉴定的大多数器官特异性基因在使用精品阵列的各自器官中也显示出显性或排他性表达(未示出)。同样在更大的范围内,用ATH1阵列观察到的表达谱与精品阵列的结果非常吻合(图2)2)。我们从Affymetrix器官数据集中选择了与精品阵列相似的样本,并与所有分析器官的平均表达相比,从根中生成了平均中心表达比。大多数p450在两个具有R的阵列平台上都遵循相同的趋势2-值为0.508的线性回归(图2)。另一组是模棱两可的,因为它的表达与使用一个平台的平均表达不同(超过两倍),而另一组则表示接近平均表达。在两个平台的比较中,只有4个基因得到相反的结果。虽然在其他器官比较中相关性不太明显(数据未显示),但它们也表明不同方法之间存在很好的一致性,特别是考虑到所使用的生物材料的巨大差异。然而,目前的分析得益于更大规模的实验。
平台间表达数据比较。使用覆盖基因特异性PCR产物的斑点微阵列(cypp阵列)生成的P450表达数据从“拟南芥P450s功能基因组学”网页中检索(表1)。在本分析中,通过与“通用RNA”样本进行比较,产生了1周幼苗根系中的信号强度[2]。与“通用控制”相比,不可检测强度被人为设置为0.05的比率2-转化表达数据以实验平均值为中心。已发表的Affymetrix ATH1阵列杂交的表达数据按方法处理。选取17个幼根试验的平均强度。为了生成一个类似于“通用RNA”的对照,我们计算并记录了69个覆盖相似样本的实验的平均强度2比率被生成。所示为2 × 2图,比较平均中心表达比[log]2(样本/平均值)],使用两种阵列类型上表示的所有P450基因的数据。遵循相同趋势的数据点以黑色表示,与一个平台的平均表达差异超过两倍,但在另一个平台的差异小于两倍的数据点以灰色表示。红点表示在两个平台上表达相反的基因
应激反应
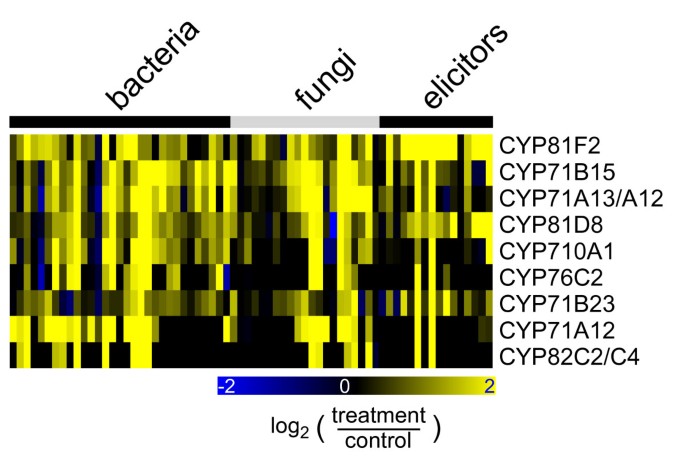
在239个应力处理实验中,一大群p450对一个或几个应力有反应。上调的基因比下调的多。虽然在20多个实验中有38个探针组显示出诱导作用,但在20多个处理中只有两个基因被抑制。所有p450的完整应力响应矩阵可以在“CYPedia”网页上的“查看矩阵”链接中找到。为了突出p450的应力诱导,我们选择了49个探针组,代表53个p450,在至少30%的实验中,在至少一个处理组中表现出两倍以上的上调(附加文件)2)。一组代表11个p450的9个探针组被细菌和真菌病原体强烈诱导(图2)3.)。这些基因在不相容的相互作用中被迅速诱导答:芥和两,而在兼容相互作用中的诱导相对较慢,因为在许多防御相关基因中都观察到这一点[12,13]。它们也可由激发子和一些非生物胁迫(包括氧化、渗透和紫外线胁迫)诱导3.、附加文件2)。在这些基因中,CYP71B15已被证明对病原体有反应,并编码一种酶参与camalexin生物合成的最后一步,主要的答:芥植物抗毒素(14,15]。最近,CYP71A13被证明催化camalexin形成的早期步骤[16]。以前也被描述为在相容和不相容的相互作用和衰老中受到差异调节CYP76C2(17],尽管在这种情况下,蛋白质的功能尚未阐明。相反,CYP710A1没有涉及防御反应,但被证明参与了豆甾醇的生物合成[18]。到目前为止,还没有对这组基因的其他功能或防御作用进行描述。
另一个不同的星团是由一组13个p450定义的(从CYP74A附加文件2)。这些基因对病原体没有(或弱)反应,但受到几种非生物胁迫的诱导,特别是损伤、氧化应激(如百草枯、臭氧或H2O2)、遗传毒性胁迫(博来霉素施加)、渗透胁迫和盐胁迫(分别用甘露醇和NaCl处理)。在这一组中有表征良好的氧化亚烯合成酶(AOS, CYP74A)和氢过氧化物裂解酶(HPL, CYP74B2) [19]。这两种酶都参与了导致茉莉酸盐和其他氧化脂类衍生物参与应激信号的生物合成的氧脂素途径。在这个组里还有CYP86A2它编码一种ω-羟化脂肪酸的酶,并参与角质层的氧脂代谢[20.,21]。
激素的反应
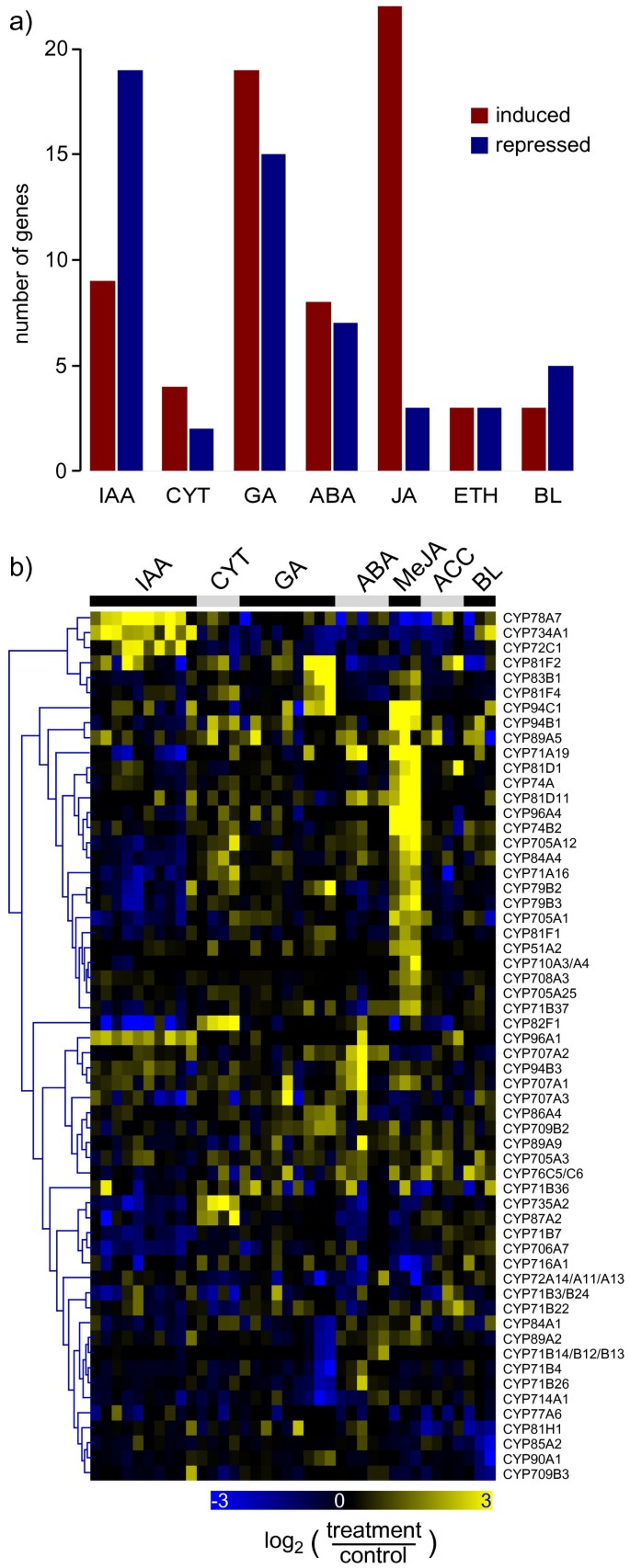
许多p450似乎是由茉莉酸甲酯(MeJ)诱导的(图2)4)。在所有MeJ处理实验中,超过30%诱导了22个p450,但只有3个p450被抑制(图3)4)。前者中又有CYP74A和CYP74B2参与脂肪酸氢过氧化物的代谢[19],众所周知,这是由茉莉酸盐诱导的,但也有大量额外的p450(图2)4 b)。并不是所有这些基因都与氧脂素代谢有关,但这组基因可能包括与茉莉酸调节的其他途径有关的基因。这适用于CYP79B3,它将色氨酸转化为相应的肟,从而导致吲哚硫代葡萄糖苷、camalexin和生长素的生物合成[22- - - - - -24]。注意到这一点很有趣CYP79B3在吲哚乙酸(IAA)处理下抑制。其他明显的类群包括IAA处理强烈诱导的p450(图上)4 b),或被种子中的赤霉素酸(GA)抑制(图下半部分)4 b,从…开始CYP84A1)。总的来说,不同激素反应之间的广泛串扰是明显的:在每个激素组至少三个治疗实验中,11个p450对一种以上的激素有反应(>两倍)。单个p450在IAA和GA、MeJ和IAA以及细胞分裂素和IAA之间的拮抗转录反应是明显的(图2)4 b)。引人注目的是,大多数激素应答p450,当它们的功能被确定时,它们本身就参与激素的生物合成或分解代谢:例如CYP734A1 (BAS1)和CYP72C1 (SOB7)都参与油菜素内酯的分解代谢[25,26], CYP735A2起催化作用反式-玉米素形成[27], CYP79B2参与IAA的生物合成[24,28]。因此,其他一些功能未知的激素反应性p450也可能参与激素代谢网络。
突变型野生型比较
突变体中P450表达的定位通常突出了在分离突变体或突变体组中非常特定的反应。只有在少数情况下,十个或更多基因的亚群在响应一个或几个突变时被共同调节。这种协调反应提供了如下所示的代谢途径。该数据集揭示的最显著的特征是参与应激反应的P450基因组的激活与LEAFY基因的激活之间存在非常强的正相关[29]。完整的P450突变反应矩阵可以在“CYPedia”网页上的“查看矩阵”链接中找到。
总之,表达矩阵鉴定了在植物发育过程中具有特定功能或在植物防御和信号网络中发挥作用的基因群。这些可能会指导进一步研究这个大基因家族的个体成员的功能,包括精细表达分析,突变表型描述和组织靶向代谢谱。明显的激素网络和串扰可能有助于识别参与激素稳态的其他酶,并突出新的和迄今为止被忽视的信号通路。
Co-expression分析
p450在植物次生代谢的所有分支中催化缓慢且不可逆的步骤。CYPedia方法的基本假设是,在相同生化途径中起作用的基因是共表达的。当其功能已知时,p450通常与同一分支通路中的其他酶共同调节[6,30.]。假设这可能也适用于尚未表征的P450,我们进行了全面的共表达分析,将每个P450的表达与4130个选定的与P450相关的基因的表达进行了比较答:芥新陈代谢。这些数据来自不同的数据库,包括“KEGG”,“AraCyc”,“acyl脂质”,“BioPathAt”,以及专门用于注释次级代谢途径的出版物(Litpath) [30.- - - - - -35]。所有途径和相关基因的列表可以在“CYPedia”页面的“浏览途径”链接下找到。对于这些基因,我们随后添加了来自'MatDB'的'功能目录'的注释[36]并从“TAIR”中手动整理“GeneOntology”术语[37],以及来自“TAIR”的基因描述(表1)1)。基于对综合注释和文献综述的人工评估,每个基因被给予一个反映注释准确性的注释分数(详见方法)。
每个基因的注释信息与上述P450基因的表达数据相结合。以每个P450的4个表达载体为诱饵,计算了所选4130个基因的Pearson相关系数(r值),共为3.78 × 106在贝奥武夫计算机集群上进行计算。对于每个P450,保留相似表达基因(r > 0.5)。根据共表达基因的数量和注释分数,确定每个P450和表达数据集的共表达途径。每个P450的共表达途径列表可以在“CYPedia”主页上的“途径图”链接中找到。从那里,可以找到各个热图的链接,这些热图描绘了四个数据集中每个数据集中所有共表达基因的表达概况和详细信息。
途径预测的验证:以苯丙素代谢为例
在大多数情况下,基于得分最高的共表达途径预测的功能与表征的p450的实际功能吻合得很好3.)。对于已知功能的43个p450中的27个,使用该方法预测了正确的途径(63%的成功率)。对于另外4个p450,未发现共表达途径。在大多数情况下,这是因为基因在任何实验中都没有表达到可检测的水平。在基于共表达分析预测错误通路的11个p450中,有3个在10个得分最高的通路中存在正确通路。剩下的8个基因没有正确的识别途径(19%的错误识别率)。其中大部分与激素代谢有关。
在正确预测的p450中,所有三种羟化酶都参与了苯丙素途径的木质素部分[38]。例如,当使用CYP73A5编码肉桂酸4-羟化酶(C4H)作为诱饵,在器官和应激数据集中,所有其他表征在一般苯丙氨酸途径中起作用的基因的r值均大于0.5(附加文件)4)。在其余两个数据集中相关性不太明显,但注释通路“苯丙素代谢”(BioPath)和“木质素生物合成”(AraCyc)是根据CYP73A5的实际生化功能在所有四个数据集中发现的得分最高的通路[39]。不仅是下游苯丙素途径不同分支的基因,还包括莽草酸途径所有上游步骤的同种异构体[30.]导致苯丙氨酸生物合成的基因共表达,从而重建了完整的途径(附加文件)4)。
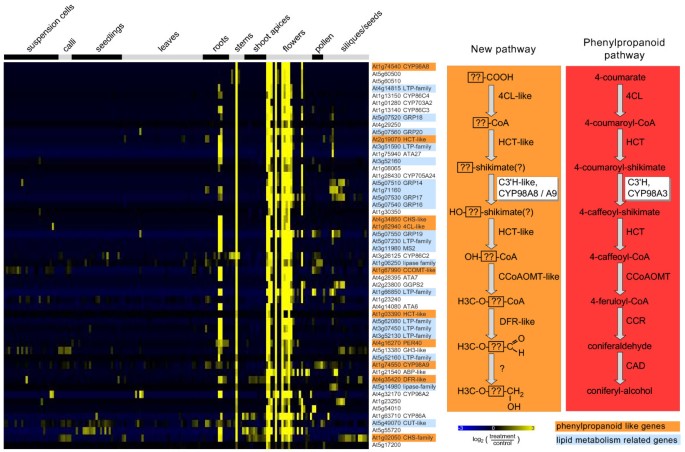
值得注意的是,相当大比例的p450可能在尚未阐明的生化途径中起作用,并可能产生从未被描述过的天然化合物。显然,这些未知通路中的基因尚未被注释,因此不可能使用共表达方法来预测这些通路。然而,即使在这种情况下,也可以通过仔细检查共表达基因获得有价值的信息。这可以用CYP98家族来举例说明。CYP98A3编码p-香豆素莽草酸酯/喹酸酯3'-羟化酶(C3'H),参与单脂醇的生物合成[40,41]。该基因紧密共表达C4H和大多数其他特征基因参与一般苯丙素途径(附加文件)4)。同一家族的另外两个基因(CYP98A8和CYP98A9)具有广泛的序列相似性CYP98A3,但不编码C3'H [41]。这两个CYP98A8和CYP98A9共享重叠的表达模式,这是非常不同的C3'H,主要在花组织中表达(图2)5&附加文件5)。在器官数据集中,这两个基因的得分最高的共表达途径出现为“杂酰基脂质代谢”(acyl脂质),这是由于大量假定和已知的与脂肪酸代谢相关的基因,这些基因可能参与花粉外壳/壁的发育。然而,与苯丙素途径相关的几个基因也与CYP98A8和CYP98A9(在图中以橙色突出显示)5)。总之,它们编码具有未知功能的“类苯丙烷”酶,与特征的类苯丙烷酶具有序列相似性[30.,32,35]。因此,这种共表达组似乎是由于苯丙素途径的至少一部分重复以及随后的新的花特异性途径的募集(图2)5)。鉴定任何这些酶的底物都应该导致这种“类苯丙烷途径”的阐明。
以CYP98A8为诱饵进行表达分析。已发表的Affymetrix微阵列数据代表167个器官和组织样本,从genevinvestigator数据库中检索[10]。背景校正和比率日志2-比率生成方法见方法。的表达向量CYP98A8使用“expression angler”算法将其与不同数据库中注释的4119个参与任何代谢途径的基因进行比较[9]。相关系数大于0.6的共表达基因的表达谱用热图表示。在热图的顶部显示了样品组。以平均为中心的信号强度比用颜色编码,如热图底部所示。与苯丙素途径酶相似的基因以橙色突出显示。与脂质代谢相关的基因以蓝色突出显示。有关共表达基因和样品的详细信息可在附加文件中找到5。右侧的苯丙素途径部分用红色表示,基于CYP98A8共表达分析的假设的复制途径用橙色表示。
综上所述,这些例子表明,共表达分析结合共表达基因的途径定位是鉴定在同一生化途径中作用的酶的编码基因的有力工具。作为概念证明,大多数已知的p450被放置在预期的路径上。但这种方法也为大量孤儿p450提供了新的途径。
与质体活性相关的p450(叶绿素/类胡萝卜素途径)
共表达分析揭示的最显著的特征之一是P450基因的一个意想不到的大子集被映射到被确定为“质体异戊二烯类”(BioPath),“光系统”(BioPath),“光合作用”(KEGG或FunCat)和“叶绿体的生物发生”(FunCat)的途径上。在“CYPedia”主页上,点击“浏览路径”和“CYP =>路径”链接,进入相应的数据库获取详细信息。他们的路径预测得分通常远高于500,是整个分析中最高的。其中包括CYP97A3和CYP97C1它们最近被证明与类胡萝卜素β-和ε-环的羟基化有关[42,43],但还有多达79个其他仍然是孤儿的P450基因。
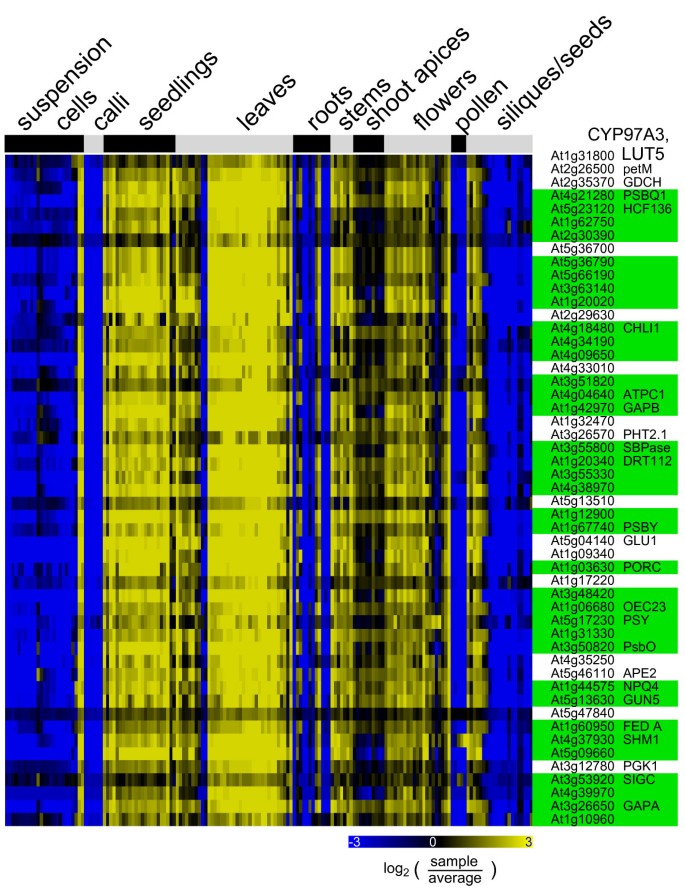
所有这些基因表现出非常相似的表达模式,如图所示6(另见附加文件6)CYP97A3,在所有绿色组织中都有很高的表达。它们也经常在叶片组织中表现出对病原体攻击的下调(未示出)。根据ChloroP预测,其中11个具有质体定位。基于人工评估,Schuler和同事确定了11个p450可能定位于质体[2];其中7个是预测到可塑性活性的群体。这可能表明P450加氧酶在类胡萝卜素、叶绿素假基、生育酚、phyllo- and plasoquinones等质体萜类衍生物代谢中的作用一直被忽视。这也可能表明许多植物P450酶具有与初级光合代谢有关的功能,用于合成抗氧化剂、质体结构成分、与能量代谢或光感知相关的信号分子。后一种情况由CYP90A1显示图中所示的典型表达式模式6。CYP90A1催化油菜素内酯生物合成中的23-羟基化步骤[44],而最近有报道说,它们受到昼间依赖光线的控制[45]。另一方面,该组中的一些P450可能具有看家功能或参与本构天然产物的生物合成,这些本构天然产物在空间和时间上与能量产生和植物活性生长耦合。CYP86A2最近被描述为参与角质层脂质的生物合成[21],可能是后一类的代表。
与plastidial活性相关的P450: CYP97A3的共表达分析。从genevinvestigator数据库中检索微阵列表达数据,并按照方法中描述的方法进行处理。的器官表达载体CYP97A3作为共表达分析的诱饵,如图4所示。诱饵的表达载体CYP97A3(第一行)显示167个器官和组织样本。后列共表达基因50个,相关系数r > 0.84。生成的热图按指示用颜色编码。绿色突出显示的是来自“质体异戊二烯类”(BioPath)、“光系统”(BioPath)、“光合作用”(KEGG或FunCat)和“叶绿体生物发生”(FunCat)类别的基因。有关共表达基因和样品的详细信息可在附加文件中找到6。在CYPedia分析中,多达80个p450具有相似的表达谱和通路预测。
作用于三萜化合物的候选p450
萜类化合物是由C5异戊二烯衍生的化合物,是种类最多、种类最多的一类天然产物。在植物中,它们通过激素和抗氧化剂在发育和适应中发挥重要作用,但大多数是与其他生物拮抗或有益相互作用的介质,如防御病原体或吸引传粉昆虫[qh]46]。其中,2,3-氧化二烯由13个基因(包括甾醇环化酶CAS和LAS)编码的三萜合成酶(TTPS)合成三萜答:芥(47]。每个TTPS产生一组独特的萜类化合物,这些萜类化合物可以被p450进一步调节,例如羟基化,从而产生大量修饰的三萜化合物。虽然很多ttp但目前只鉴定出一个参与三萜修饰的P450 [48]。我们的通路定位方法确定了63个p450与“三萜、甾醇和油菜素类固醇代谢”(LitPath)类别的基因共表达,其中27个属于“三萜生物合成”类别(从“CYPedia”主页点击链接“浏览途径”和“通路=> CYP”到“LitPath”)。为了进一步识别单个对ttp和P450对于每个表达数据集,我们计算了可能协同作用的基因,比较了每个表达载体的相关系数ttp每个P450。其中7个ttp共表达的p450基因多达6个(r > 0.75)2)。共有20个p450(由18个探针组表示)与至少一个共表达ttp在至少一个数据集中。到目前为止,这些p450都没有特征。其中七个属于CYP705而没有其他家族有两个以上的共表达基因,这表明该家族在三萜调节中具有特殊作用,这可能是由CYP705/ttp联合进化。
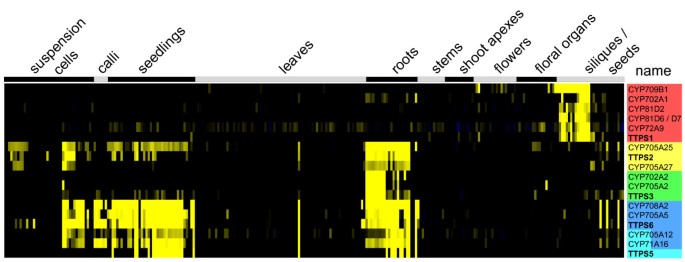
相关性最强的是TTPS6和TTPS5(MRN1)。TTPS6 (thalalianol合成酶)催化2,3-环氧喹啉环化生成三环三萜thalalianol [49],而MRN1则催化非典型环氧烯环化成单环环烯三萜,命名为marneral [50]。产品和进一步的代谢物尚未确定在足底。相关的环烯三萜在鸢尾科。MRN1和TTPS6在所有数据集中,尽管在器官数据中最明显,但与同一组4个p450共享重叠的表达模式(图2)7、附加文件7)。它们在根、幼苗(可能是其根部分)和一些细胞培养物中高度表达。在集群中,CYP705A5和CYP708A2表达得更相似吗TTPS6,而CYP705A12和CYP71A16有更相似的器官模式MRN1,主要在较成熟的根样中表达(图2)7)。同样,该基因集在激素数据集中形成一个单独的簇,在细胞分裂素(玉米素)和MeJ处理下诱导表达,再次具有相同的亚簇(附加文件)7)。MRN1没有应激反应(因此在应激数据集中没有共表达的p450),但是TTPS6,CYP705A5和CYP708A2虽然r值相对较低,但在伤害、干旱和其他一些胁迫条件下,它们在根中形成一个明显的表达簇(表1)2、附加文件7)。整个群体在具有典型表达模式的突变数据集中再次形成一个强簇。它在det2和ga1突变体(附加文件7),它们分别在油菜素内酯和赤霉素酸的生物合成中受阻[51,52]。由此看来,阻断TTPS作用上游分支的激素通路也会导致这些通路的下调。
总之,鉴定了两个强共调控基因亚群。其中,CYP705A5和CYP708A2是催化进一步修饰的良好候选者,可能是顺序羟基化,形成胁迫响应的根特异性三萜。虽然这篇论文还在评估中,但Fields和Osbourn对thalalianol通路的功能表征充分证实了这一预测[53]。他们对这一途径的表征是由共同表达基因的操纵子样物理聚类指导的。另一方面,CYP705A12和CYP71A1则更有可能参与到marneral的修饰中,形成三萜环烯醚衍生物,类似于迄今为止被认为具有特征的多羟基环烯醚萜类化合物鸢尾科(54]。从TTPS1、TTPS2和TTPS3启动的三萜途径相关的其他p450的聚类分析中也获得了同样一致的线索。
与植物激素生物合成有关的p450
细胞色素p450在各类植物激素的代谢中起核心作用[4]。我们的共表达方法在十八烷酸途径导致茉莉酸盐和其他氧化脂质的生物合成的情况下特别成功。茉莉酸盐是一种特性良好的应激反应信号,在雄蕊和花粉发育过程中也发挥激素作用[qh]55]。这两种p450都参与了这一途径,烯氧化物合酶(先进的,CYP74A)和氢过氧化物裂解酶(HPL1,CYP74B2) [19],分别被正确地放置在“茉莉酸生物合成”(TAIR-GO)和“脂氧合酶途径”(AraCyc)中。然而,额外的p450可能参与茉莉酸的代谢(如催化茉莉酸的羟基化)和其他氧化脂类。此外,参与防御或植物发育的基因子集预计会被茉莉酸级联选择性激活。事实上,还有多达10个p450与茉莉酸信号相关基因共表达(即被归类为“茉莉酸生物合成”[AraCyc]、“茉莉酸生物合成”[TAIR-GO]或“对茉莉酸刺激的反应”[TAIR-GO])。表格3.列出p450与茉莉酸盐相关基因的相关系数,p450至少在两个数据集中共表达基因,p450至少在一个数据集中有五个以上共表达基因。四种迄今未被鉴定的p450与许多茉莉酸相关基因具有共同的激素反应谱(表上)3.),这是由于甲基茉莉酸盐处理后的强烈和特异性诱导。这些基因与其他数据集中的茉莉酸盐相关基因也有共同的特征(表1)3.)。发展史,在体外功能分析预测其中大部分(cyp94、CYP96A4)参与氧化脂类代谢[56]。对于第二组基因,与茉莉酸途径相关的表达在器官数据集中尤为突出(表底部)3.)。那些已知或预测参与光感知/质体活性(CYP97B3, CYP90A1[44], CYP72A11),或硫代葡萄糖苷的生物合成(CYP83B1 [57】,CYP71B7)。有趣的是,在12-氧二烯酸还原酶的情况下,OPR3与大多数p450共表达(包括先进的和HPL1),而OPR2仅在器官数据集中与p450有相似的表达。
不同的P450亚群与各种其他激素通路相关(未显示)。然而,与茉莉酸相关基因相比,r值通常较低,并且在各自的途径中,共表达仅限于较少的基因。这可能是由于这些激素的代谢特征较少,或者更有可能是由于这些激素通路中涉及的大多数基因的相对较低和细胞/组织特异性表达。
总之,共表达方法将p450组与特定的激素通路联系起来。然而,与控制植物发育的低浓度激素相比,该分析在涉及强烈反应的胁迫信号的情况下提供了更多的信息。因此,预计主要支持表征新的应激信号通路。
结论
大量公开可用的微阵列表达数据提供了迄今为止仅被很少利用的惊人数量的信息。基因表达与其生物/生化作用之间的相关性是必要的,当基因编码在相同途径中起作用的代谢酶时,它们有望被共同调节。这里提供的涵盖已知途径的数据在很大程度上证实了这些假设。基于P450超家族的共表达分析答:芥我们已经提出了关于生物化学和生物学功能的新假设,涉及大量的个体基因或基因群共同途径。引人注目的是,根据我们的数据预测的新途径的第一次验证是在对这篇论文的评估期间独立发表的[53],从而进一步证实了这种方法的潜力。在越来越多的特征基因功能的支持下,更多的线索将在未来几年从这一分析中出现。新的假设现在可以通过利用不断扩大的反向遗传学工具箱来实验解决,例如插入突变与靶向代谢分析相结合,以及利用重组蛋白集合和底物集合的中等通量筛选进行反向生物化学[58]。同样的方法也可以扩展到其他基因家族,包括转录因子,因此有可能大大加快对植物天然产物代谢网络和调控的分子理解。
材料与方法
探针集P450基因的选择和表达数据
所有细胞色素P450的集合答:芥(截至2005年4月271个基因)和相应的AGI(拟南芥基因组计划)位点标识符(Atxgxxxxx)从“PlaCe拟南芥P450数据库”中检索(表)2)。在PlaCe注释的21个P450基因中,没有AGI位点相关。其中包括18个带注释的假基因。两对P450基因与同一agi位点相关(CYP71A27P和CYP71A28: At4g20240;CYP71A23和CYP71A24编号:At3g48290),总共留下248个AGI位点。使用“genevestiator”探针选择工具,这些探针用于识别Affymetrix ATH1微阵列上相应的探针集[10]。21个基因未在阵列上显示。其余227个基因共有229个探针集代表,其中26个基因有多个探针集代表,32个探针集代表多个基因。使用“genevinvestigator”探针选择工具,我们确定了这些探针集识别的所有基因,如果一个给定基因存在多个探针集,我们为该基因选择一个单一的,特定的(如果可用)探针集。这导致216个选定的探针集;其中191个识别单个P450基因,21个识别两个基因,3个探针组可以与3个基因杂交,1个探针组可以识别4个基因,总共227个代表P450基因,3个非P450基因(也被探针组识别的侧翼基因)。使用的探针集和这些探针集识别的基因可以在“CYPedia”主页上找到。
然后,我们从“genevestiator Digital Northern”工具中检索这些探针集的规范化表达数据[10]。数据于2005年5月下载(数据集1),涵盖1823个微阵列实验,并于2006年4月下载(数据集2,包括数据集1的更新),涵盖2202个微阵列。对于每个探头集,背景被定义为所有被Affymetrix软件称为“缺席”的探头的平均信号强度,所有缺席的探头被设置为这个背景值。如果有重复序列,则确定所有重复的平均强度。每个试验分为以下四类:i)野生型植物的器官和组织样品,ii)野生型植物的胁迫处理,iii)野生型植物的激素、营养(剥夺)和其他处理,iv)与野生型样品相比,同样处理的突变植物(如果适用)。然后将来自器官和组织样本的信号强度与背景强度进行比较,从而产生对数2-背景比率。将两个治疗组的信号强度与相应对照样本的信号强度进行比较2-处理与对照比较的比率,以及突变体样本的强度与同样处理的野生型样本的强度进行比较,从而生成log2-突变体与野生型的比值。每个数据集使用K-means聚类分为30个表达组,所有聚类的综合热图可以在“CYPedia”主页上的“视图矩阵”链接中找到。在“生物阵列资源”(BAR)上的“HeatMapper”工具可使表达式矩阵可视化[9],并将得到的热图合并到常用的电子表格格式(Adobe PDF、Microsoft Excel和OpenOffice Calc)中。
代谢基因的选择
检索所有基因,生成与植物代谢各方面相关的基因列表(途径数据库)答:芥基因,在以下数据库中进行了注释:i)KEGG Orthology (KO) -拟南芥(KEGG) [59], ii)“拟南芥信息资源”(AraCyc)的“代谢途径”[60];iii)“拟南芥脂质基因数据库”(acyl脂质)[61], iv)“生化途径知识数据库”(BioPathAt) [34], v)专门注释次级代谢途径的出版物(Litpath) [30.- - - - - -33,35,62]。将所有数据库的信息合并到一个数据矩阵中,并为上述独特基因集选择Affymetrix探针集,得到4,129个独特探针集。对于这组基因,添加了来自“慕尼黑蛋白质序列信息中心”(MIPS-FunCat)的“功能目录”的注释[36]和人工从TAIR中整理的“GeneOntology”术语[63(即有证据代码IDA[从直接分析推断],IMP[从突变表型推断]和/或TAS[可追溯的作者声明]。
每个基因都被赋予一个通路注释分数:生物化学特征基因的10分(即在“acyl脂质”或“BioPath”中注释为“功能性”,或在文献综述中确定);在TAIR-GO中描述为IDA的具有直接生化功能的基因得9分,在“acyl脂质”、“BioPath”或文献中注释为“功能性(?)”或“从突变表型推断”的基因得8分;TAIR-GO证据编码为IMP的基因得7分;具有描述的突变表型但分子功能不明确的基因得6分;高相似性基因5分(WU-BLAST e < 10)-50年)转化为具有特征的植物基因;与另一种植物基因高度相似,但该基因的功能未得到验证的基因得4分;相似基因3分(WU-BLAST 10)-10年E < 10-50年)转化为具有特征的植物基因;低相似性基因2分(WU-BLAST e > 10)-10年)转化为具有特征的植物基因;相似度低的大基因家族成员1分(WU-BLAST e > 10)-10年)转化为具有特征的植物基因。
共表达分析和通路定位
检索所选4129个探针集的Affymetrix表达数据,对p450进行如上处理,并合并表达矩阵。如前所述进行共表达分析[9]。简而言之,表达载体以均值为中心,计算每个P450的表达载体与“池塘”中4129个基因的表达载体之间的Pearson相关系数(r值)。随后的操作使用R环境执行[64]。对每个P450和数据集检索r > 0.5的共表达基因,并从途径数据库中提取相应的生化途径(见上文)。对于每个通路,计算共表达基因的数量,并计算注释分数之和(见上文)。只有当列表中至少有一个基因具有6个以上的注释点时,该通路才被保留。将给定通路中共表达基因的数量和得分与该通路中所有基因的总数和得分进行比较。基于尾部超几何分布分析,只保留了共表达基因组中过度代表的通路(p [hyper] < 0.005)。随后,鉴定了所有四个数据集中鉴定的途径,并对每个数据集中发现的基因的数量和分数进行了汇总。结果表根据得分进行排序,并导入到OpenOffice Calc (OpenOffice.org)模板和实际表达式热图的缩略图中,这些热图是使用'BAR'中的'Heatmapper plus'工具生成的[9],并以HTML格式保存。每个P450的结果可以在每个P450的“通路图”网页上找到。将共表达基因的表达数据和通路信息数据(最多50个基因r > 0.5)进行合并,并按r值排序。使用“BAR”中的“Heatmapper plus”工具对表达式表进行颜色编码,并保存为链接到相应路径图的静态网页。
阵列平台比较
使用覆盖基因特异性PCR产物的斑点微阵列生成的P450表达数据从“拟南芥P450s功能基因组学”网页检索(表1)1)。利用这种双通道平台(cyp -阵列),通过与“通用RNA”样本进行比较,产生了1周龄幼苗(和其他四个器官)根系中的信号强度。这种“通用RNA”由来自幼苗和叶子的根和芽、成熟植物的茎和花的RNA混合而成[2]。为了从公共ATH1微阵列中产生类似的“通用对照”,我们从处理过的器官数据集中选择了14个幼苗芽样本、9个成熟植物叶片样本、17个幼苗根系样本、19个整花样本和10个茎样本(见上文)。然后我们计算平均对数2所有样本的背景强度,并将其与根样本的平均强度进行比较,从而创建根/“通用控制”比率,类似于来自cep阵列的比率。对于后者,与通用对照相比,将不可检测强度人为设置为0.05的比率,并对比率进行对数计算2改变了。在两个平台上表示的基因的表达数据在整个实验中平均居中。基于线性回归模型比较了两个数据集的R2计算值。
可用性和需求
参考文献
从苔藓到杨树的植物细胞色素p450。植物化学,2006,5:193-204。10.1007 / s11101 - 006 - 9015 - 3。
舒勒M,段华,Bilgin M, Ali S:拟南芥细胞色素P450s在植物生物化学中的应用。植物化学,2006,5:205-237。10.1007 / s11101 - 006 - 9035 - z。
Werck-Reichhart D:细胞色素P450。《拟南芥》。编辑:Somerville C和Meyerowitz E. 2002, Rockville医学博士,美国植物生物学家协会,Rockville医学博士,[http://www.bioone.org/perlserv/?request=get-document&issn=1543-8120&volume=2&issue=1&page=1]
舒勒马,Werck-Reichhart D: p450的功能基因组学。植物学报,2003,35(4):629-667。10.1146 / annurev.arplant.54.031902.134840。
Nelson DR, Schuler MA, Paquette SM, Werck-Reichhart D, Bak S:水稻和拟南芥的比较基因组学。单子叶和双子叶727个细胞色素P450基因及假基因分析。植物生理学报,2004,35(5):756-772。10.1104 / pp.104.039826。
黄青木,杨志刚,柴田,等。植物基因共表达网络的实用信息提取方法。植物生理学报,2007,28(4):381- 391。10.1093 /卡式肺囊虫肺炎/ pcm013。
Barrett T, Troup DB, Wilhite SE, Ledoux P, Rudnev D, Evangelista C, Kim IF, Soboleva A, Tomashevsky M, Edgar R: NCBI GEO:数千万个表达谱的挖掘-数据库和工具更新。中国生物医学工程学报,2007,35(5):769 - 769。10.1093 / nar / gkl887。
帕金森H, Kapushesky M, Shojatalab M, Abeygunawardena N, Coulson R, Farne A, Holloway E, Kolesnykov N, Lilja P, Lukk M, Mani R, Rayner T, Sharma A, William E, Sarkans U, Brazma A: ArrayExpress-微阵列实验和基因表达谱的公共数据库。中国生物医学工程学报,2007,35(5):774 - 775。10.1093 / nar / gkl995。
张建军,张建军,张建军,张建军,张建军。植物基因序列的基因表达分析。植物科学与技术,2005,33(4):559 - 561。10.1111 / j.1365 - 313 x.2005.02437.x。
刘建军,刘建军,刘建军,等。拟南芥微阵列数据库和分析工具箱。植物生理学报,2004,31(2):369 - 369。10.1104 / pp.104.046367。
彭建军,李建军,李建军,等。拟南芥细胞色素P450基因超家族的结构与系统发育。中国生物医学工程学报,2003,19(3):387 - 387。10.1089 / 10445490050021221。
防御基因表达调控的全球视角——一个高度互联的信号网络。植物学报,2004,7(5):559 - 561。10.1016 / j.pbi.2004.07.013。
陶勇,谢忠,陈伟,Glazebrook J,常洪生,韩波,朱婷,邹刚,Katagiri F:拟南芥与丁香假单胞菌亲和和不亲和互作反应的定量性质。植物学报,2003,15(5):317-330。10.1105 / tpc.007591。
Schuhegger R, Nafisi M, Mansourova M, Petersen BL, Olsen CE, Svatos A, Halkier BA, gllawischnig E: CYP71B15 (PAD3)催化camalexin生物合成的最后一步。植物生理学报,2006,41(1):1248-1254。10.1104 / pp.106.082024。
周宁,张志强,张志强,等。拟南芥细胞色素P450单加氧酶基因的克隆与表达。植物学报,1999,11:2419-2428。10.1105 / tpc.11.12.2419。
王晓明,王晓明,王晓明,等。拟南芥细胞色素P450单加氧酶71A13的合成及其酶活性研究。植物学报,2007,19:2039-2052。10.1105 / tpc.107.051383。
Godiard L, Sauviac L, Dalbin N, Liaubet L, Callard D, Czernic P, Marco Y:拟南芥细胞色素P450基因CYP76C2在发育性细胞死亡中的表达。生物医学工程学报,1998,38(4):245-249。10.1016 / s0014 - 5793 (98) 01309 - x。
Morikawa T, Mizutani M, Aoki N, Watanabe B, Saga H, Saito S, Oikawa A, Suzuki H, Sakurai N, Shibata D, Wadano A, Sakata K, Ohta D:拟南芥和番茄细胞色素P450 CYP710A编码甾醇C-22去饱和酶。植物学报,2006,18:1008-1022。10.1105 / tpc.105.036012。
Chehab EW, Perea JV, Gopalan B, Theg S, Dehesh K:水稻和拟南芥的氧脂素途径。植物遗传学报,2009,29(1):1 - 4。10.1111 / j.1744-7909.2006.00405.x。
段华,马舒勒:拟南芥CYP86A亚家族的差异表达和进化。植物生理学报,2005,37(3):1067-1081。10.1104 / pp.104.055715。
肖峰,Goodwin SM,肖勇,孙志,Baker D,唐鑫,Jenks MA,周建民:拟南芥中CYP86A2基因抑制丁香假单胞菌III型基因,是角质层发育所必需的。中华生物医学工程学报,2004,23(3):2903-2913。10.1038 / sj.emboj.7600290。
细胞色素P450酶在camalexin生物合成中的作用。生物化学学报,2006,34(4):1186 - 1186。10.1042 / BST0341206。
Mikkelsen MD, Petersen BL, gllawischnig E, Jensen AB, Andreasson E, Halkier BA:拟南芥防御信号通路对CYP79基因和硫代葡萄糖苷谱的调节。植物生理学报,2003,31(4):398 - 398。10.1104 / pp.011015。
赵Y,船体AK,古普塔NR,戈斯KA,阿隆索J,艾克尔JR norman J, Chory J, Celenza杰:Trp-dependent生长素生物合成在拟南芥:参与细胞色素p450 CYP79B2 CYP79B3。中国生物医学工程学报,2002,32(4):391 - 391。10.1101 / gad.1035402。
黄春华,黄春华,黄春华,黄春华,黄春华,黄春华,黄春华,黄春华,黄春华,黄春华,黄春华,黄春华。植物生理学报,2009,33(2):444 - 444。10.1104 / pp.103.030882。
Turk EM, Fujioka S, Seto H, Shimada Y, Takatsuto S, Yoshida S, Wang H, Torres QI, Ward JM, Murthy G, Zhang J, Walker JC, Neff MM: BAS1和SOB7通过独特的油菜素内酯失活机制调控拟南芥光形态发生。植物学报,2005,42(2):393 - 398。10.1111 / j.1365 - 313 x.2005.02358.x。
taki K, Yamaya T, Sakakibara H:拟南芥CYP735A1和CYP735A2编码细胞分裂素羟化酶,催化反式玉米蛋白的生物合成。生物化学学报,2004,29(4):488 - 488。10.1074 / jbc.M406337200。
Mikkelsen MD, Hansen CH, Wittstock U, Halkier BA:拟南芥细胞色素P450 CYP79B2催化色氨酸转化为吲哚-3-乙酰氧肟,吲哚-3-葡萄糖苷和吲哚-3-乙酸的前体。中国生物医学工程学报,2009,25(3):377 - 377。10.1074 / jbc.M001667200。
李建军,李建军,李建军,李建军,李建军,李建军,等。科学通报,2004,29(3):379 - 379。10.1073 / pnas.0307842100。
李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,李志刚,Douglas CJ:拟南芥木质素合成和纤维分化的转录因子分析。植物学报,2005,42(2):618- 664。10.1111 / j.1365 - 313 x.2005.02403.x。
王晓明,王晓明,王晓明,等。拟南芥萜类合成酶(AtTPS)基因家族的基因组分析。中国生物医学工程学报,2002,26(3):369 - 369。10.1007 / s00438 - 002 - 0709 - y。
Costa MA, Collins RE, Anterola AM, Cochrane FC, Davin LB, Lewis NG:拟南芥苯丙素途径代谢网络的基因功能和组织及其局限性的计算机评估。植物化学,2003,64:1097-1112。10.1016 / s0031 - 9422 (03) 00517 - x。
王晓明,王晓明,王晓明,等。芥子酸-芥子酸酶系统的研究进展。植物学报,2005,28(4):564 - 571。10.1016 / j.pbi.2005.03.002。
Lange BM, Ghassemian M:整合生化通路图的综合后基因组数据分析方法。植物化学学报,2005,25(6):413-451。10.1016 / j.phytochem.2004.12.020。(http://www.sciencedirect.com/science?_ob=ArticleURL&_udi=B6TH7-4FC8V01-2&_user=113008&_coverDate=02%2F01%2F2005&_rdoc=3&_fmt=summary&_orig=browse&_srch=doc-info (% 23 toc % 235275% 232005% 23999339995 % 23999339995体积% 23佛罗里达州% 23显示% 23)&_cdi = 5275 &_sort = d&_docanchor =视图= c&_ct = 11 &_acct = C000008898&_version = 1 &_urlversion = 0 &_userid = 113008 md5 = 113008 fc8e852b4d3210b60d0aadf9b]
李建军,李建军,李建军,李建军。拟南芥木质化工具箱的全基因组分析。植物生理学报,2009,32(3):591 - 591。10.1104 / pp.103.026484。
Ruepp A, Zollner A, Maier D, Albermann K, Hani J, Mokrejs M, Tetko I, Guldener U, Mannhaupt G, Munsterkotter M, Mewes HW:全基因组蛋白质系统分类的功能注释方案。中国生物医学工程学报,2004,32(2):539- 545。10.1093 / nar / gkh894。
Berardini TZ, Mundodi S, Reiser L, Huala E, Garcia-Hernandez M, Zhang P, Mueller LA, Yoon J, Doyle A, Lander G, Moseyko N, Yoo D, Xu I, Zoeckler B, Montoya M, Miller N, Weems D, Rhee SY:拟南芥基因组控制词的功能注释。植物生理学报,2004,35(5):745-755。10.1104 / pp.104.040071。
王晓明,王晓明,王晓明,等。细胞色素P450在生物代谢中的作用。植物化学,2006,5(5):239-270。10.1007 / s11101 - 006 - 9025 - 1。
Urban P, Mignotte C, Kazmaier M, Delorme F, Pompon D:两个亲缘关系较远的拟南芥nadph -细胞色素P450还原酶与P450 CYP73A5偶联的克隆、酵母表达和特性。中国生物医学工程学报,2009,27(2):391 - 391。10.1074 / jbc.272.31.19176。
Franke R, Humphreys JM, Hemm MR, Denault JW, Ruegger MO, Cusumano, Chapple C:拟南芥中苯丙素代谢3-羟化酶基因的表达。植物学报,2002,30(3):394 - 394。10.1046 / j.1365 - 313 x.2002.01266.x。
Schoch G, Goepfert S, Morant M, Hehn A, Meyer D, Ullmann P, Werck-Reichhart D:拟南芥(Arabidopsis thaliana)中酚酯的3'-羟化酶,这是苯丙素途径缺失的一个环节。中国生物医学工程学报,2001,31(2):369 - 369。10.1074 / jbc.M104047200。
王晓明,王晓明,王晓明,等。拟南芥类胡萝卜素b环羟化酶CYP97A3在植物叶黄素合成中的作用。美国国家科学促进会。[j] .中国科学:地球科学。10.1073 / pnas.0511207103。
Tian L, Musetti V, Kim J, magallane - lundback M, DellaPenna D:拟南芥LUT1基因座编码类胡萝卜素e-环羟基化活性所需的细胞色素P450家族成员。美国国家科学促进会。[j] .中国科学:地球科学。10.1073 / pnas.2237237100。
王晓明,王晓明,王晓明,王晓明,王晓明,王晓明。油菜素内酯对拟南芥细胞色素P450基因表达的影响。细胞学报,1996,35(5):171-182。10.1016 / s0092 - 8674(00) 81094 - 6。
Bancos S, Szatmari AM, Castle J, Kozma-Bognar L, Shibata K, Yokota T, Bishop GJ, Nagy F, Szekeres M:拟南芥油菜素类固醇生物合成CPD基因的日调节。植物生理学报,2006,31(1):369 - 369。10.1104 / pp.106.079145。
陈建军,陈建军,陈建军,等。萜烯类天然产物的研究进展。生物化学学报,2007,32(3):444 - 444。10.1038 / nchembio.2007.5。
Lodeiro S,熊强,Wilson WK, Kolesnikova MD, Onak CS, Matsuda SPT:氧化角鲨烯环化酶通过多种机制合成多种产物:对三萜生物合成概念的挑战。生物化学学报,2007,29(2):1122 -1122。10.1021 / ja073133u。
Shibuya M, Hoshino M, Katsube Y, Hayashi H, Kushiro T, Ebizuka Y: β -amyrin和sophoradiol 24-羟化酶的表达序列标记挖掘和功能表达分析。中国生物医学工程学报,2006,27(3):948-959。10.1111 / j.1742-4658.2006.05120.x。
王志强,徐锐,张春华,等。植物三萜的基因组挖掘。生物化学学报,2004,26(6):578 - 579。10.1021 / ja0318784。
熊强,王志强,张志强,张志强。拟南芥氧化角鲨烯环化酶在环化过程中对虹膜骨架形成的催化作用。化学与工程学报,2006,35(4):1285-1288。10.1002 / anie.200503420。
Fujioka S, Li J, Choi YH, Seto H, Takatsuto S, Noguchi T, Watanabe T, Kuriyama H, Yokota T, Chory J, Sakurai A:拟南芥油菜素内酯生物合成早期阻断突变体。植物学报,1997,9:551 - 562。10.1105 / tpc.9.11.1951。
孙平平,Kamiya Y:拟南芥GA1基因座编码赤霉素生物合成环化酶戊烯合成酶A。植物学报,1994,6:1509-1518。10.1105 / tpc.6.10.1509。
田野B,奥斯本AE:代谢多样化-植物操纵子样基因簇的独立组装。科学通报,2008,32(3):543- 547。10.1126 / science.1154990。
方荣,霍顿PJ,罗超,Hylands PJ:鸢尾中三萜的分离及结构分析。植物化学学报,2007,32(2):442 - 447。10.1016 / j.phytochem.2007.02.018。
Wasternack C: Jasmonates:生物合成、信号转导及其在植物逆境响应和生长发育中的作用研究进展安·伯特(朗德)。2007
黄海伟,黄海伟,黄海伟,黄海伟,黄海伟,黄海伟。拟南芥脂肪酸-欧米茄羟化酶的进化关系及底物特异性。植物科学,2006,17(2):326-338。10.1016 / j.plantsci.2005.08.028。
Naur P, Petersen BL, Mikkelsen MD, Bak S, Rasmussen H, Olsen CE, Halkier BA: CYP83A1和CYP83B1,两个非多余的细胞色素P450酶代谢硫代葡萄糖苷的生物合成。植物生理学报,2003,33(3):693 - 693。10.1104 / pp.102.019240。
Olry A, Schneider-Belhaddad F, Heintz D, Werck-Reichhart D:中通量筛选法测定耗氧酶的催化活性:细胞色素P450和其他加氧酶功能表征的新工具。植物学报,2007,51(1):331- 334。10.1111 / j.1365 - 313 x.2007.03140.x。
毛翔,蔡涛,Olyarchuk JG,魏磊:基于KEGG同源词的基因组自动标注与通路识别。生物信息学,2005,21(1):387 - 393。10.1093 /生物信息学/ bti430。
张萍,Foerster H, Tissier CP, Mueller L, Paley S, Karp PD, Rhee SY: MetaCyc和AraCyc。植物代谢途径数据库研究。植物生理学报,2005,38(3):779 - 779。10.1104 / pp.105.060376。
Beisson F, Koo AJ, Ruuska S, Schwender J, Pollard M, Thelen JJ, Paddock T, Salas JJ, Savage L, Milcamps A, Mhaske VB, Cho Y, Ohlrogge JB:拟南芥酰基脂代谢相关基因。2003年候选人口普查,器官中表达序列标签分布的研究,以及基于网络的数据库。植物生理学报,2003,32(2):681-697。10.1104 / pp.103.022988。
Lange M, Ghassemian M:拟南芥基因组组织:涉及类异戊二烯和叶绿素代谢的基因调查。植物生理学报,2003,25(5):925-948。10.1023 /: 1023005504702。
Rhee SY, Beavis W, Berardini TZ, Chen G, Dixon D, Doyle A, Garcia-Hernandez M, Huala E, Lander G, Montoya M, Miller N, Mueller LA, Mundodi S, Reiser L, Tacklind J, Weems DC,吴毅,徐毅,Yoo D, Yoon J,张平:拟南芥信息资源(TAIR):一个集中、有组织的拟南芥生物学、研究资料和社区门户。中国生物医学工程学报,2003,31(1):394 - 398。10.1093 / nar / gkg076。
团队RDC: R:统计计算的语言和环境。2006,维也纳,奥地利,R基金会统计计算,[http://www.R-project.org]
致谢
这项工作得到了欧盟对乙脑的国际重返社会补助金(MIRG-CT-2006-036537)的支持。VS和AO感谢拜耳作物科学的支持,VS感谢法国国家技术研究署对CIFRE资金的支持。JFG由人类前沿项目RGP0065/2005-C资助。我们要感谢弗朗索瓦·伯尼尔对手稿的批判性阅读,以及弗兰克·皮诺和休伯特·夏勒进行的大量有益的讨论。
作者信息
从属关系
相应的作者
额外的信息
作者的贡献
JE对微阵列数据进行分析,设计并构建CYPedia数据库。VS和AO帮助构建了web界面。JFG参与了数据库的更新。NJP进行共表达分析。DWR和JE构思了这个项目。DWR指导了这项研究,并帮助解释了数据。JE和DWR撰写了手稿。所有作者都阅读并批准了最终的手稿。
电子补充资料
12870 _2008_255_moesm1_esm.xls
附加文件1:p450基因座和探针组信息。给出了用于细胞色素P450的Affymetrix AtH1微阵列探针组,以及这些探针组识别的名称和AGI位点。此外,给出了各自数据集中表达可检测的实验次数(与对照组相差两倍以上),以及表达可检测的样本比例。在器官数据集中,每个探针组的控制被定义为阵列上的平均信号强度,该探针组被Affymetrix软件称为“缺席”。在压力和激素数据集中,控制被定义为未经处理的控制样本的信号强度。在突变数据集中,控制被定义为对应野生型样本中的信号强度。(xl68kb)
12870 _2008_255_moesm2_esm.xls
附加文件2:P450s的应激反应性表达。从genevinvestigator数据库中检索微阵列表达数据,并按照方法中描述的方法进行处理。如上图所示,只有在至少一个治疗组中超过30%上调(>两倍)的基因被选中。背景校正后的表达强度与未处理的对照实验和log进行比较2-比率用于具有完全联系的层次聚类分析。生成的热图用颜色编码,如表1(概述)中的概述图像所示。单个样本的详细信息可在此电子表格的Sheet2(详细信息)中找到。(xls 664 kb)
12870 _2008_255_moesm3_esm.pdf
附加文件3:基于已知功能的p450共表达分析的通路预测。得分最高的p450共表达途径具有特征性的生化功能。(pdf 31kb)
12870 _2008_255_moesm4_esm.xls
附加文件4:以编码肉桂酸4-羟化酶的CYP73A5为诱饵进行共表达分析。已发表的Affymetrix微阵列数据(代表a) 167个器官和组织样本,b) 243个应激相关处理)从genevinvestigator数据库中检索[10]。按照方法进行背景校正和比率log2-比率生成。使用“expression angler”算法将CYP73A5的表达载体与不同数据库中注释的4,119个参与任何代谢途径的基因进行比较[9]。相关系数大于0.5的共表达基因的表达谱用热图表示。在热图的顶部显示了样品组。平均中心信号强度比在每个热图的底部用颜色编码。编码苯丙素和莽草酸途径酶的基因分别以红色和绿色突出显示。表1为总览图,有关共表达基因和样本的详细信息可在本文件表2(器官)和表3(压力)中找到。(xl2mb)
12870 _2008_255_moesm7_esm.xls
附加文件7:三萜合成酶(TTPS)和p450的聚类分析。从genevinvestigator数据库中检索微阵列表达数据,并按照方法中描述的方法进行处理。所有12个TTPS基因的4个数据集的表达载体来自答:芥作为共表达分析的诱饵,将其与所有P450基因的表达进行比较。我们保留了7个TTPS基因,这些基因在四个表达数据集中的至少一个和相应的P450中至少与一个P450共表达(r > 0.75)2)。这组基因被用于分层聚类,在a)器官表达数据集和b)突变数据集中有完整的链接,如表1的概述图所示。具有高相关系数的TTPS和P450基因簇用颜色编码。有关共表达基因和样本的详细信息可在本文件的表2(器官)、3(应激)、4(激素)和5(突变)中找到。括号内的数字是来自genevestiator数据库的实验ID。(xl1mb)
权利和权限
开放获取本文由BioMed Central Ltd.授权发表。这是一篇开放获取的文章,在知识共享署名许可(https://creativecommons.org/licenses/by/2.0),允许在任何媒体上不受限制地使用、分发和复制,前提是正确引用原创作品。
关于本文
引用本文
J.埃尔廷,V.索维潘,A.奥利。et al。细胞色素P450超家族的广泛(共)表达分析工具拟南芥。BMC Plant Biol8日,47(2008)。https://doi.org/10.1186/1471-2229-8-47
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/1471-2229-8-47
关键字
- P450基因
- 吲哚乙酸
- 茉莉酸生物合成
- 注释的分数
- 识别失误率