摘要
背景
隐植物是高度区室化的生物,除细胞核、线粒体和质体外,在核形态及其周围的残余细胞质中表达一个二级最小化的真核生物基因组。由于核胚编码蛋白质组的成员可能有助于基本的细胞通路,阐明核胚编码的功能是最感兴趣的。不幸的是,到目前为止,隐生植物还不能进行遗传转化。因此,核胚编码蛋白的功能必须通过在遗传可达生物中应用方法间接阐明。
结果
Orf222是隐生植物中未鉴定的核胚特异性开放阅读框之一Guillardiaθ,显示同源单反1649集胞藻属sp. PCC 6803。最近从聚球藻属sp. PCC 7002编码藻蓝蛋白-β155-胆素裂解酶。这里我们通过插入诱变来证明集胞藻属sp. PCC 6803单反1649编码蛋白也作为胆素裂解酶,并有助于连接子附着和/或藻胆体的稳定性。最后,我们的结果表明藻蓝蛋白-β155-bilin裂解酶集胞藻属sp. PCC 6803可以补充在活的有机体内通过核胚编码的开放阅读框羊痘疮222.
结论
我们的数据表明,藻蓝蛋白裂解酶功能的丧失会导致多效性效应集胞藻属PCC 6803,表明从一个共同的祖先蛋白中分离出藻红菊酯裂解酶Guillardiaθ保留了胆素基团与其他藻胆蛋白偶联的能力。这是进一步的,意想不到的例子的普遍性藻胆蛋白裂解酶。
背景
藻胆蛋白是大多数蓝藻和红藻的主要附属光收获复合物(LHC)的亚基,也存在于隐生植物的类囊体腔中。与蛋白质共价相连的是发色团,即藻胆素[1,2].这些开放的四吡咯环通过硫醚键与保守的半胱氨酸残基耦合,是光收集和高效能量流动所必需的[3.].各种藻胆蛋白,即异藻蓝蛋白、藻蓝蛋白、藻红菊酯、藻红蓝蛋白,都含有不同数量的胆素基团。
胆素与藻胆蛋白的附着是一种酶催化反应,也是自发发生的,但效率较低[4].几种双素附着裂解酶被描述。编码的二聚体酶之一中国共产党E和中国共产党F基因连接发色团与藻蓝蛋白α-亚基[4,5].压电陶瓷E和压电陶瓷F基因编码第二种已知的裂解酶,特异于phycoer红红素α-亚基[6- - - - - -8].最近,赵和他的同事们发现了cpes样蛋白作为phycocyanobilin-半胱氨酸-beta84裂解酶的功能淡水藻类的一种sp. PCC 7120,这是第一个被鉴定为藻钴蛋白β亚基的裂解酶[9].Shen等人发现了另一种特定于藻胆蛋白β亚基的裂解酶。10].他们鉴定出的基因产物cpcT被认为是Cys-β153-phycocyanobilin裂解酶聚球藻属sp. PCC 7002。此外,Zhao等人报道了淡水藻类的一种sp. PCC 7120 CpeS1作为蓝藻藻胆蛋白中半胱氨酸-84结合位点的“近乎通用”裂解酶[11,12].
在大多数蓝藻和红藻中,藻胆蛋白以多聚体复合体的形式组织,称为藻胆体[13- - - - - -15].它们的天线结构位于类囊体膜的细胞质表面,由各种连接多肽和藻胆蛋白组成。每个藻胆体本身是一个多聚体复合体,由一个核心和几个杆状结构组成。藻胆体可根据其结构进行细分。蓝藻中最常见的类型是半镰状的,由一个三圆柱形的核心和六根杆状组成。
同种藻蓝蛋白(AP, λ马克斯= 650 nm)形成核心结构,通过连接蛋白将藻胆体连接到类囊体膜。杆状细胞可以由三种不同的藻胆蛋白组成:藻蓝蛋白(PC, λ马克斯= 617 nm)位于核心近端,而藻红菊酯(PE, λ马克斯= 560 nm)和phycoerythrocyanin (PEC, λ马克斯= 575 nm)位于核的远端[16,17].每种生物的藻胆体杆的藻胆蛋白组成不同。集胞藻属sp. PCC 6803含有半鳞状藻胆体。PC是这种生物中唯一的棒状结构的胆蛋白,由α-和β-亚基组成。这些亚基二聚成异质二聚体,组装成六聚体(αβ)6随后,它们相互偶联,并通过连接蛋白与ap -核心偶联[18,19].根据它们的位置(在核心或棒)和它们的分子质量,连接蛋白被分为四组[20.,21].除了介导藻胆体的组装和稳定的主要功能外,连接蛋白还促进向反应中心的能量转移[20.].
Guillardiaθ是一种以藻红菊酯为藻胆蛋白的隐植植物。β亚基编码在质体基因组上[22],而藻红菊酯α-亚基由一个位于核的基因家族编码。在后一种情况下,基因编码的前蛋白包含一个三方地形信号,负责跨五个生物膜的易位[23].由于这种单细胞光养生物存在广泛的基因组数据,现有的知识可以用来重建这些生物的生物化学。的核形态基因组中由开放阅读框编码的蛋白质功能的阐明Guillardiaθ是特别有趣的,因为这个基因组是最小化的,因此应该只编码必需的蛋白质。在分析核形基因组数据后,Orf222被鉴定为与包括Slr1649在内的许多蛋白质同源集胞藻属sp. PCC 6803和CpcT聚球藻属sp. PCC 7002。因为隐生植物无法通过基因操作,我们创造了一个单反1649-功能丧失的菌株集胞藻属PCC 6803,并用核胚编码的orf修饰该菌株。
生成的Slr1649功能缺失突变体通常具有Shen等人描述的acpcT淘汰赛中聚球藻属sp. PCC 7002 [10].然而,额外的影响单反1649敲除突变体集胞藻属sp. PCC 6803被鉴定为突变体藻胆体内的连接蛋白。互补的单反1649年的核胚特异性羊痘疮222表明,隐植蛋白虽然起源于以藻红菊酯为辅助色素的生物,但在蓝藻中藻蓝蛋白的Cys-β155位置上附着一个胆素。
结果
在网上分析
在分析了隐生植物的核形态基因组后Guillardiaθ,我们确定了一个开放阅读框(羊痘疮222),与蓝藻的基因高度相似(表1),编码具有DUF1001结构域的可溶性蛋白质。隐菌序列与蓝藻序列的比对表明羊痘疮222应该编码一个额外的转运肽,如n端延伸所示。与同源的进一步的orfs羊痘疮222和蓝藻同源物另外存在于红藻的核基因组中[24].在高等植物中,即。拟南芥,也有一些相似的orfs [25].甚至是噬菌体S-PM2,它会感染聚球藻属的同系物进行编码羊痘疮222年(26)(表1).
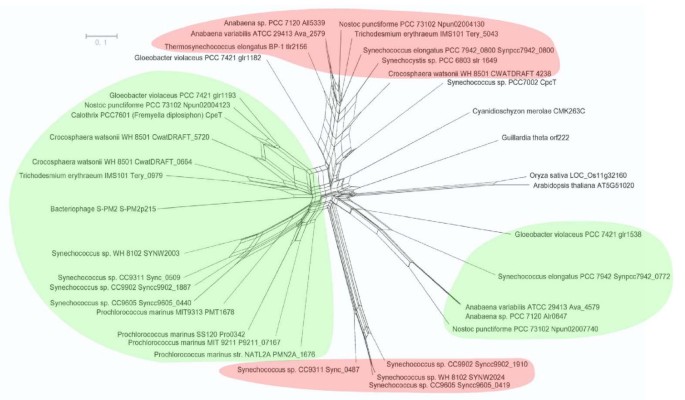
蓝藻中Orf222同源物的数量在几个物种中有所不同,与藻胆蛋白的数量无关。然而,在杆状体中含有多种藻胆蛋白的生物体中,Orf222同源物表达超过一种的强烈趋势(表2)1).根据氨基酸序列比对和系统发育网络,可以划分出四个单系类群。1).其中两个类似于cpet样蛋白(phycoerythrin operon protein);另外两组含有slr1649型的成员。无论是Guillardiaθ序列或任何其他真核生物序列都不能归属于四个单系群中的任何一个。
NeighborNet (NNet)对41个类群进行图分割.蛋白质序列与MUSCLE排列。初始比对包含307个位点,其中191个缺口位点被排除在分析之外,剩下116个氨基酸位点用于对数行列式(LogDet)距离估计,并使用LDDist程序去除不变位点。由此构建了一个邻网分割图,它是用Splitstree4可视化的。突出显示的是四个单系类群:其中两个类群类似于cpet样(phycolyythrin operon protein)蛋白质(绿色突出显示),两个类群含有slr1649样类型的成员(红色突出显示)。未显示:的序列聚球藻属elongatusPCC 7942 Synpcc7942_0800和聚球藻属elongatusPCC 6301 Syc0738_d和的序列相同聚球藻属elongatusPCC 7942 Synpcc7942_0772和聚球藻属elongatusPCC 6301 Syc0764_d的序列原绿球藻SS120 Pro0342和原绿球藻CCMP1375 orf195。
此外,明确的从属关系Gloeobacter violaceusPCC 7421 (glr1182)和聚球藻属sp.PCC 7002 (CpcT)序列不能外推。除了Prochlorococcus在迄今为止所研究的所有蓝藻中,至少有一个slr1649样群的成员存在。cpet样蛋白仅在编码藻红素和/或藻红素的蓝藻细菌中检测到。尽管两组蛋白质似乎具有相同的功能,但进一步研究基因组环境中相关的相应基因,发现了明显的差异。不像基因cpeT组,单反1649-组在其基因组定位上远没有那么保守(表1).除了念珠藻属第PCC 7120号淡水藻类的一种摘要ATCC 29413和束毛藻属erythraeumIMS 101,同源基因的定位总是在下游cp.在少数情况下,它后面是cp.另一方面,基因单反1649-组在所研究的蓝藻菌基因组中相当随机地分布(表1).
一代slr1649淘汰赛压力
我们使用集胞藻属sp. PCC 6803作为模式生物,并创造了第一个单反1649敲除菌株(Δslr1649),将卡那霉素抗药盒插入单反1649开放阅读框通过同源重组。生成的纯合敲除突变体具有Shen等人描述的相同特征。[10].就像有特征的cpcT突变体中聚球藻属sp. PCC 7002,我们的敲除突变体含有减少水平高达60%的藻蓝蛋白和由此产生的淡绿色表型。敲除细胞产生更小的藻胆体,这可能是与野生型藻胆体相比,它们在蔗糖密度梯度中的不同迁移行为的原因。此外,分离出的藻胆体在SDS-PAGE上显示出红移吸光度最大值和藻蓝蛋白β亚基的表观分子质量略小(数据未显示)。在用甲酸消化纯化藻蓝蛋白和藻蓝胆素添加测定后,Shen等人在消化后得出结论中国共产党T基因Synechocccussp. PCC 7002编码一种胆素裂解酶,该酶负责将藻蓝蛋白附着在藻蓝蛋白β亚基的Cys-153上[10].同样的情况很可能也适用于集胞藻属由于两个敲除突变体之间的高同源性和相似的表型,同源Slr1649。因此,Slr1649被认为在β-藻蓝蛋白的同源位置Cys-155上附着一个胆素基团集胞藻属sp.PCC 6803。
藻胆体的分离与分析
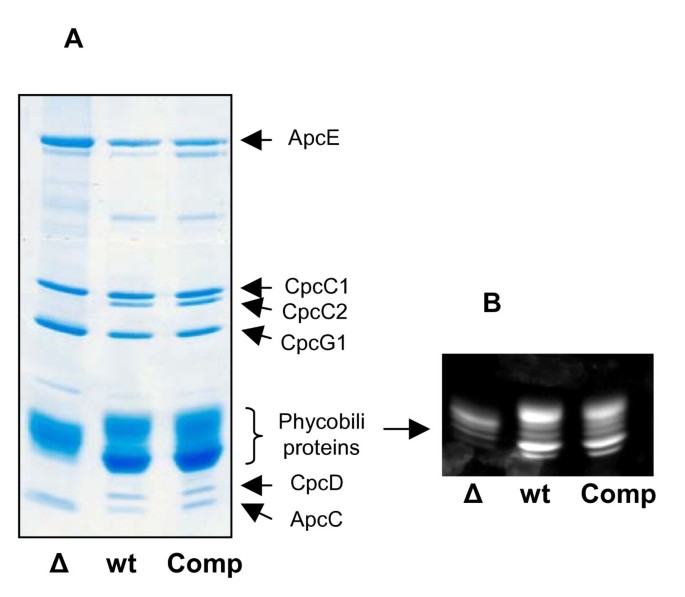
通过从我们的敲除突变体中分离和分析藻胆体,我们观察到一个额外的特征聚球藻属sp. PCC 7002同源物。如图所示。2由基因编码的两个连接多肽CpcC2和CpcDcpcC2而且cpcD分别在突变体的分离藻胆体中缺失,但在野生型中可以通过质谱分析识别。另一个连接多肽CpcC1 (cpcC1), CpcG1 (cpcG1)、ApcC (")及ApcE (apcE)在两种菌株中都存在。
经过进一步的研究,连接蛋白的缺失被证明不是转录效应。在反转录实验中cpcC2,相同的存在cpcC2通过对获得的RT-PCR产物进行测序(数据未显示),证实突变株和野生型菌株均存在转录产物。
互补
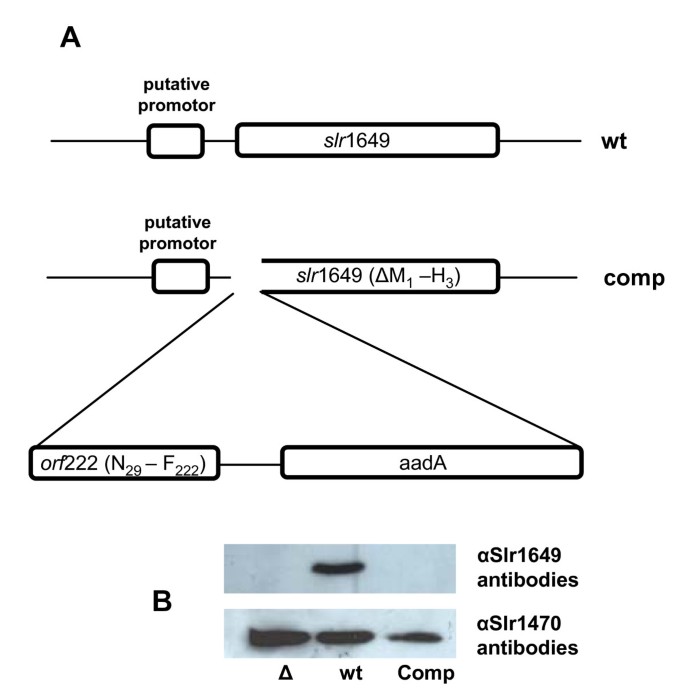
为了研究核胚特异性阅读框羊痘疮222来自隐生植物Guillardiaθ能起到补药的作用吗单反1649年的功能丧失,我们整合了这个潜在的基因没有其假定的转运肽到蓝藻基因组集胞藻属sp. PCC 6803。这同时影响了阅读框单反1649年及其独联体-作用的上游信号(图;3).在互补菌株中,单反1649从其自然上游区域分离,产生一个无启动子的截断基因,其中翻译启动子和接下来的两个密码子不再出现在阅读框中。失去了单反使用针对Slr1649产生的多克隆抗体进行免疫印迹实验,显示了1649基因产物和突变的完全分离。3 b).在这里,抗体的交叉反应显示存在于野生型,但不存在于突变株提取物中。对补充菌株进行RT-PCR分析和序列分析,结果表明该菌株为完整的隐性真菌羊痘疮222是转录的(数据未显示)。
互补菌株的表征
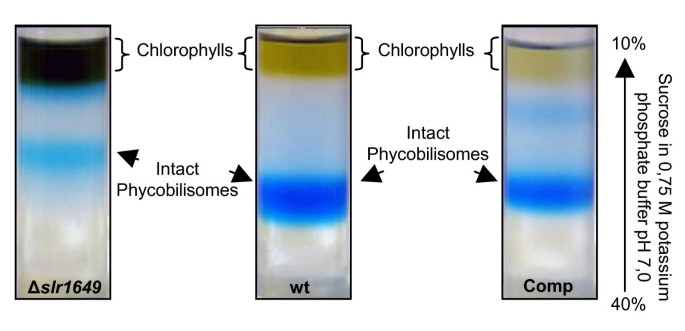
有趣的是,补充菌株的表型与野生型菌株相似,如培养物的绿色所示(数据未显示)。在从补充菌株中分离出藻胆体的蔗糖密度梯度分离过程中,我们注意到,相对于野生型菌株,突出条带的迁移行为与敲除突变体的迁移行为没有差异(图2)。4).这表明在两个菌株中藻胆体的大小是相同的,并且确实可以通过蛋白质组和质谱分析来确认。这里我们展示了缺失的连接蛋白单反互补菌株中有1649个敲除菌株(图;2).SDS-PAGE显示补充菌株藻蓝蛋白β亚基分子质量无明显变化。进一步分析发现,在基因敲除突变体中,Cys-β153和Cys-β155位置缺失的发色团群聚球藻属sp. PCC 7002和集胞藻属PCC 6803,极有可能在互补菌株中再次出现2 +SDS-PAGE分离的藻胆体染色显示野生型和补充菌株的藻胆蛋白信号强度相等(图2)。2 b).
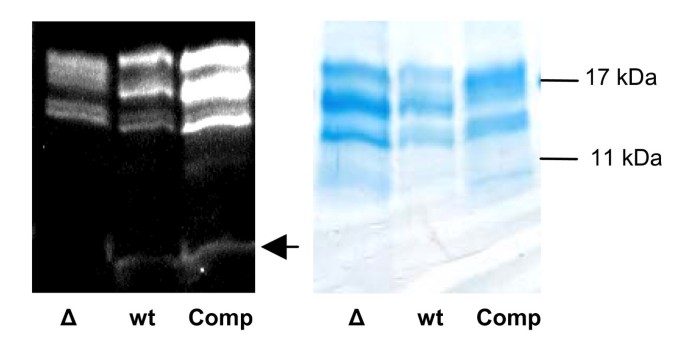
为了澄清这一点,我们用甲酸消化分离的藻胆蛋白。在此过程中,CpcB在单个位点被裂解,而所有其他藻胆蛋白不受影响。Cys-β84发色团荧光片段的预期尺寸为15.36 kDa, Cys-β155发色团荧光片段的预期尺寸为2.78 kDa。如图所示5,得到了这些期望的片段。除了15.36 kDa的信号外,在含有野生型菌株蛋白和补充菌株蛋白的通道中检测到2.78 kDa的信号,但在含有Δ的通道中没有检测到slr1649蛋白质。这些数据证实了缺失在敲除突变体中的发色团存在于互补中。这与补充菌株中连接蛋白谱的鉴定表明其为野生型藻胆体结构。
讨论
隐生植物之所以重要,有几个原因。在细胞生物学方面,它们复杂的区室化是主要的兴趣点,因为在这些生物中存在多种等离子体和基因组,可以追溯到原核生物或真核生物[27].隐生植物的标志之一是第二核的残余物,这是由一个被吞噬的光养真核生物的细胞核被另一个真核细胞还原而产生的[28].这种腔室,即核形态,在其编码能力和表达方面是最小化的Guillardiaθ的十分之一大肠杆菌K12基因组[29].编码能力的降低导致了基因仍然存在于可能编码重要功能的核形态的印象。因此,我们对解决由核形态编码的蛋白质的功能感兴趣。然而,由于缺乏转染隐植体的方法,我们正在研究遗传可达生物中核形基因及其编码蛋白的同源性,以间接识别隐植蛋白的功能。蓝藻是研究得最好、遗传上最容易获得的细菌之一集胞藻属sp. PCC 6803。
Orf222是一种未鉴定的核胚特异性开放阅读框,其同源物存在于许多蓝藻中。分析该基因在不同生物体内的贡献,表明两者之间存在明显的相关性羊痘疮222个同源基因和藻胆蛋白存在,因为至少有一个羊痘疮222同源体编码在所有表达藻胆蛋白的生物中,包括红藻。系统发育研究表明,同源羊痘疮222基因可分为以下4类(图;1): Slr1649-like a, Slr1649-like b, CpeT-like a和CpeT-like b。因为我们研究中的网络构建和采样方法与最近提出的系统发育学不同[10),因此解决了略有不同的从属关系也就不足为奇了。然而,我们的网络纠正了错误的隶属关系,并指出了基础分组的不确定性。这可以从噬菌体序列的位置上看出来,噬菌体序列在图中所示的网络中,与它们所感染的细菌相邻,而不是与隐植序列在同一分支中。
尽管具有高度的同源性,但Slr1649-like和CpeT-like类群的成员在相应基因的基因组环境中存在差异(表1)1).CpeT基团的成员主要定位于藻红菊酯相关的连接子蛋白操纵子[30.,31]在…旁边cp基因。在某些情况下,甚至cp基因直接定位于下游cpeT.由于操纵子结构在许多情况下连接功能相关的基因,CpeT可能是藻胆体的结构或功能部分,它已被证明负责从β-藻蓝蛋白将胆素基团附着到特定位点[10].值得注意的是,slr1649组成员的一致分布是不可见的,因为这些基因似乎在不同的基因组中随机定位。有趣的是,单反1649-同源体存在于一些高等植物中,如栽培稻而且拟南芥(无花果。1).这些陆生植物的编码蛋白也具有DUF1001结构域的特征,但显然具有副同源功能拟南芥同源体似乎是质体分裂所必需的[25].在植物细胞分化和细胞分裂平面调控中也有重要作用[25].同样的情况也适用于噬菌体S-PM2的复制,但似乎不太可能,因为这种噬菌体感染不同的病毒聚球藻属菌株及其同源物的资源可能是一种选择优势的结果。
纯合敲除突变体Δslr1649在集胞藻属sp. PCC 6803表现出与a .相同的特征cpcT敲除突变体聚球藻属Shen等人描述的PCC 7002 [10].在这里,同样的淡绿色表型和减少的藻蓝蛋白含量,导致一个缺失的胆素组在藻胆体,是通过敲除中国共产党T,等价于单反这个蓝藻中的1649同源物。这表明该蛋白的同源蛋白裂解酶的功能聚球藻属sp. PCC 7002和集胞藻属sp. PCC 6803具有可比性。
然而,我们获得了一个额外的,没有描述的特征集胞藻属sp. PCC 6803敲除突变体。在敲除突变体Δ中,两个连接蛋白CpcC2和CpcD在藻胆体中缺失slr1649.CpcD是一个小的连接器(10 kDa),位于棒的远端尖端,可能作为棒的终止因子[32].CpcC2棒连接器(30 kDa)连接最远端的藻蓝蛋白盘[33].这两个基因都位于藻蓝蛋白操纵子中,它们与藻蓝蛋白亚基和藻蓝蛋白操纵子共转录cpcC1连接基因[33].导致连接蛋白丢失的转录效应似乎不太可能,因为α-亚基、β-亚基和CpcC1连接子都存在,尽管CpcD和CpcC2连接子同时不存在。这表明了我们的发现cpcC2逆转录实验表明,基因确实在突变体中转录(数据未显示)。因此,突变藻胆体中两个连接蛋白的缺失是一种转录后效应。然而,我们不能排除β-藻蓝蛋白改变导致藻胆体稳定性下降可能是我们的制剂中缺乏这两种连接蛋白的原因。在任何情况下,连接蛋白的缺乏都是裂解酶功能丧失的分子标记,这可能是值得研究的聚球藻属sp. PCC 7002 [10也一样。
Guillardiaθ,我们主要关注的隐生植物表达了同源的单反1649年与藻红菊酯有关。藻胆蛋白位于类囊体腔内,在隐生植物的藻胆体中显然没有组织。因为隐生植物Guillardiaθ使用藻红菊酯而不是藻蓝蛋白作为光合作用的辅助色素,人们可能不会想到假定的隐化裂解酶能够补充光合作用集胞藻属sp. PCC 6803。令人惊讶的是,补充菌株显示出野生型藻胆体结构,其发色团和连接蛋白谱均正确附着。因此,来自隐生植物的Orf222能够补充Slr1649的功能缺失,这表明隐生植物的藻红蛋白裂解酶仍然保留了将胆素基团与β-藻蓝蛋白耦合的能力,即使这两类蛋白质的前体进化为明显的同源蛋白。然而,一种胆蛋白裂解酶的多效性功能与藻胆素特异性:半胱氨酸-84最近被证实在体外for CpeS1 from淡水藻类的一种pcc7120 [11],这意味着多种蛋白质,如隐生藻胆素:半胱氨酸-β155裂解酶,具有将胆素偶联到多种藻胆蛋白中的同源位置的能力。
结论
胆素裂解酶功能的丧失导致藻胆体结构的各种影响。这已经在a中展示过了cpcT突变体中聚球藻属sp. PCC 7002,并可通过生成a单反1649年突变体被淘汰集胞藻属sp. PCC 6803,同源物cpcT.另一个特征是缺乏两个远端连接蛋白,这与已知的藻胆体结构改变相吻合,可能是缺少胆素裂解酶的突变体藻蓝蛋白含量降低的原因。
Slr1649的缺失得到补充在活的有机体内由同源物Orf222编码,Orf222由来自隐生植物的真核内共生的微小残留核编码Guillardiaθ.因此,Orf222可能是隐生植物中的藻红菊酯-胆素裂解酶。尽管这种蛋白起源于一种使用藻红菊酯作为辅助色素的生物,但它仍然具有将发色团与藻蓝蛋白的β亚基偶联的能力,一方面表明了胆素裂解酶的功能普遍性,另一方面证明了核胚编码的细胞功能的重要性。
方法
细胞培养
集胞藻属sp. PCC 6803株,野生型,Δslr1649和补充菌株,在含有BG-11培养基的Erlenmeyer烧瓶中30°C生长[34]在标准光条件(70 μE)和大气CO下,产生轻微的旋流2的水平。为了在平板上生长,在BG-11培养基中添加1%琼脂。培养皿在与液体培养相同的条件下孵育。
建设Δslr1649突变体
使用两对引物扩增敲除了结构体的侧翼区域:1649a_f (5'-GGT TAC TGC TCG AGG CGC ATC A-3')和1649a_r (5'-GGA CGG CAA GGG ATC CTA TCT GG-3')生成片段slr1649a, 1649b_f (5'-GGA CGG CAA GGG ATC CTA TCT GG-3')和1649b_r (5'-CAG AAA TTG CCG CGG CCA ATC TC-3')片段1649b。两者都被连接到pGEM-T载体(Promega, Mannheim),并在序列验证后转移到pBluescript II SK (Stratagene, Amsterdam)载体。大肠杆菌以菌株MRF' XL-1 blue为质粒宿主进行克隆。
使用BamHI限制位点(引物1649a-r和1649b_f插入),在两个片段之间克隆出卡那霉素抗性基因,得到质粒pΔ1649。转化为野生型后集胞藻属在添加卡那霉素(起始浓度为5 μg/ml)的BG-11琼脂板上选择含有该质粒的PCC 6803细胞进行转化。将耐卡那霉素克隆转入BG-11液体培养基。增加卡那霉素浓度(最终浓度为50 μg/ml)可获得纯合子培养。通过Southern blot分析确认完全敲除。
互补系的构造
核苷酸序列羊痘疮222从Guillardiaθ通过引物222komp2_f (5'-CAT ATG AAT TAA AAC CAA TCC TTA ATT G -3')和222komp_r (5'-GTT AAA ATT AAA TGA ATT CTA ATA A-3')得到不含推测转运肽的DNA。使用两对引物扩增侧翼区域:1649a_f (5'-GGT TAC TGC TCG AGG CGC ATC A-3')和1649kompa1_r (5'-CAA TAA CTA CAT ATG TCC CAT TCC-3')生成Compa片段,其中包括上游区域单反1649, 1649kompa2_f (5'- ttt ATG TCG AAT TCC ACT GAT C-3')和1649b_r (5'- GAG ATT GGC CGC GGC AAT TTC TG-3')生成的片段Compb。所有三个片段都被连接到pGEM-T载体(Promega, Mannheim)中,并在序列验证后,使用引物插入的不同限制性边转移到pBluescript II SK (Stratagene, Amsterdam)载体中,从而形成前体结构。通过使用生态在RI限制位点上,在Compa/两个片段之间克隆了一个大霉素盒羊痘疮222和Compb合成质粒pComp222 Δ单反1649.改造后集胞藻属利用该质粒在添加大霉素(起始浓度为5 μg/ml)的BG-11琼脂板上筛选转化菌株PCC 6803。将大观霉素耐药克隆转入BG-11液体培养基。增大大霉素浓度(终浓度30 μg/ml)可获得纯合子培养。
核酸分析
集胞藻属PCC 6803细胞用5 ml细胞培养液,3200 × g离心收集,在pH 7.0的400 μl TE缓冲液中重悬,分离DNA。加入破碎缓冲液(10%十二烷基磺酸钠(w/v)、5%月桂基磺酸钠(w/v))、200 μl玻璃微珠(直径0.2 mm)和400 μl苯酚,漩涡溶解3次,持续10 s。然后将悬浮液以12 000 × g离心,得到的上相转移到新的杯中。样品经苯酚-氯仿-异戊醇(25:24:1)处理2次,离心。通过加入1/10 Vol. NaAc pH 4.8和2 Vol. 96%乙醇,DNA在-20°C下沉淀1小时。然后,用70%乙醇进行额外的洗涤步骤。将颗粒干燥后在H中重悬2O。
RNA是从集胞藻属细胞与Trizol©(Invitrogen, Karlsruhe)根据制造商协议。根据标准方案(Sambrook)进行Northern Blot和Southern Blot分析。探针使用PCR DIG探针合成试剂盒(Roche, Mannheim)构建。
抗体的生成和纯化
为了产生抗Slr1649的抗体,我们使用引物ex1649_f (5'-GGA TCC TTA TGT CCC ATT CCA CTG-3')和ex1649_r (5'-CTC GAG GCT GGC TAA AAA CTA ACT-3')来扩增单反1649基因,最终在pGEX-5X-3载体中克隆(GE Healthcare Biosciences)。Slr1649 GST融合蛋白过表达纯化后,由Eurogentec公司(Seraing)执行免疫步骤。
IgG部分通过蛋白A琼脂糖珠从血清中纯化(GE Healthcare Biosciences)。
藻胆体的分离
根据Gray等人的方法进行藻胆体分离[35].在室温下以5000转/分离心10分钟收集细胞。在用BG-11培养基进行额外的洗涤步骤后,将细胞重悬于0.75 M pH 7.0的磷酸钾缓冲液(PPB)中,其中含有蛋白酶抑制剂鸡尾酒(PIC, 2mg /ml Antipain, 5mg /ml Chymostatin, 2mg /ml抑肽酶,5mg /ml胰蛋白酶抑制剂,2mg /ml Pepstatin, 5mg /ml Leupeptin, 1mg /ml Elastatinal和2mg /ml Na)2EDTA在HEPES/KOH中。最终浓度为200 μg/ml的抑制剂),然后在124 MPa的压力下通过法压机(Aminco)破碎两次。裂解物用Triton X-100(2%)在室温下孵育15分钟,随后在20 000 rpm下离心1小时,将未破碎的细胞和膜碎片制成颗粒。立即将上清液加载在10%-40%蔗糖线性梯度上,在PPB中溶解,在15°C下以18 000 rpm离心16 h。
sds - page
标准SDS-PAGE使用Hoefer SE 250仪器(83 mm × 101 mm, 0,75 mm厚)或使用Laemmli缓冲系统的定制系统(250 mm × 150 mm, 1,0 mm厚)[36].分离凝胶中聚丙烯酰胺含量梯度为10% ~ 15%。堆积凝胶中含有6%的聚丙烯酰胺。为了获得质量小于15 kDa的多肽的更好分辨率,使用SDS-Tricine凝胶体系[37].凝胶染色一般用考马斯亮蓝G-250溶解于A溶液(2%磷酸v/v, 10% NH4)2所以4W /v)和甲醇(40:9:1)。为了使携带胆素的蛋白形成化,凝胶在0.2 M ZnSO中孵育4解决方案(38,39]并在透光器(Bio-Rad)中使用紫外线进行高亮。
甲酸裂解
用甲醇/氯仿沉淀藻胆体[40]并重新悬浮在解理缓冲液中。根据Piszkiewicz等人的方法进行裂解[41].30 μg藻胆体在37°C和70%甲酸中孵育16 h,然后加入SDS样品缓冲液,在17%聚丙烯酰胺凝胶上用Tricine SDS- page分析。
植物蛋白质提取物的分离集胞藻属sp. PCC 6803
集胞藻属sp. PCC 6803细胞按上述方法培养和收获。细胞颗粒在TEN100缓冲液中重悬[42],包含PIC。如上所述进行细胞裂解。
MALDI-TOF质谱分析
如前所述,在质谱分析之前,对蛋白质斑点进行凝胶胰蛋白酶消化[43].来自胰蛋白酶消化物的肽混合物使用由反向色谱树脂Poros和Oligo R3制成的ZipTips™柱进行脱盐和浓缩(应用生物系统公司)。结合肽用0.5%甲酸溶液洗涤,用1 μl 33% (v/v)乙腈/0.1%三氟乙酸饱和α-氰基-4-羟基肉桂酸(Bruker Daltonics)溶液从色谱柱中洗脱,直接在MALDI靶板上风干,然后在质谱仪中分析。质谱测量在Ultraflex-TOF TOF串联质谱计(Bruker Daltonics)上进行。使用大约100次激光脉冲提取,在反射器正模式下获得肽质量指纹谱。光谱是在使用参考肽(Peptide mixture II Bruker Daltonics)进行外部校准后获得的。以胰蛋白酶自溶峰为内标(8425.100,2211.1046 Da)进一步对所获得的光谱进行内部校准。单同位素质量使用Biotools™和FlexAnalysis™软件(Bruker Daltonics)进行分配和处理,然后提交给Mascot计划[44]用于在非冗余NCBI数据库上进行搜索。吉祥物肽批量指纹搜索的参数如下:集胞藻属;搜索所有的分子质量和等电点;允许一个缺失的蛋白水解裂解位点和50 ppm的肽质量耐受性。在所有的研究中,蛋氨酸氧化被认为是一种可选的修饰,半胱氨酸氨基甲基化被认为是一种固定的修饰。比赛集胞藻属当概率得分显著且p值< 0.05时,当至少有5个肽且序列覆盖率大于20%时,蛋白质被认为是明确的。对于每种蛋白质,通过所选多肽的串联质谱分析进一步验证其特性。
在网上分析
Blast搜索分析采用NCBI蛋白-蛋白Blast [45](见附加文件1).该程序还用于保守域预测。使用TMHMM server v. 2.0预测跨膜结构域[46]和SOSUI蛋白质预测服务器[47].基因组数据集胞藻属sp. PCC 6803由CyanoBase [48].在网上通过PeptideMass进行裂解[49].
网络建设
41个序列用MUSCLE [5016次迭代。输出格式设置为标准ClustalW格式[51].该序列包含307个位点,其中191个位点被排除在分析之外。在其余116个地点,用LDDist 1.3.2估计logdet距离[52].这些距离被用来构造一个邻网分割图[53用SplitsTree4可视化[54].
参考文献
- 1.
Bishop JE, Rapoport H, Klotz CV, Chan CF, Glazer AN, Füglistaller P, Zuber H:藻红素中的色肽:三个胆素基团的结构和连接。化学学报,2007,29(3):379 - 379。10.1021 / ja00237a039。
- 2.
藻胆蛋白:发色团组成和含量的测定。植物化学学报,1995,6:457 - 457。10.1002 / pca.2800060602。
- 3.
藻胆蛋白触角的结构、功能关系和能量转移。中国生物医学工程学报,2001,29(3):344 - 344。10.1111 / j.1399-3054.1991.tb00129.x。
- 4.
赵娟,周娟,赵俊杰,李志强,李志强,李志刚:藻蓝蛋白裂解酶的研究进展。美国国家科学研究院。1992, 89: 7017-7021。10.1073 / pnas.89.15.7017。
- 5.
Fairchild CD, Glazer AN:藻蓝蛋白α亚基藻蓝糖苷裂解酶的寡聚结构,酶动力学和底物特异性。中国生物医学工程学报,2004,26(4):344 - 344。
- 6.
郑丽娟,陈晓明,陈晓明:藻红素α亚基裂解酶的候选基因。pecE和pecF介子突变体的生化分析。中国生物医学工程学报,2004,27(4):457 - 457。
- 7.
赵赫,邓mg,郑明,周明,Parbel A, Storf M, Meyer M, Strohmann B, Scheer H:一种藻胆蛋白裂解酶的新活性:藻紫胆素的附着和与藻紫胆素的异构化都是由藻红素操纵子编码的PecE和PecF蛋白催化的。中国生物医学工程学报,2000,29(2):344 - 344。10.1016 / s0014 - 5793 (00) 01245 - x。
- 8.
Storf M, Parbel A, Meyer M, Strohmann B, Scheer H,邓mg,郑敏,周敏,赵赫:藻红素光活性3(1)- cyys -alpha 84-phycoviolobilin发色团与胆蛋白的粘附:PecE/PecF的特异性生物化学,2001,40:12444-12456。10.1021 / bi010776s。
- 9.
赵克红,苏萍,李娟,涂建民,周敏,Bubenzer C, Scheer H:藻胆蛋白β亚基的发色团附着:藻胆蛋白样蛋白半胱氨酸-beta84裂解酶活性。中国生物医学工程学报,2006,26(3):344 - 344。10.1074 / jbc.M513796200。
- 10.
沈g, Saunee NA, Williams SR, Gallo EF, Schluchter WM, Bryant DA:一种新型胆素裂解酶的鉴定与鉴定:cpcT基因编码了一种胆素裂解酶,该酶可将藻蓝酶附着在聚球菌PCC 7002藻蓝蛋白β亚基的Cys-153上。中国生物医学工程学报,2006,29(2):344 - 344。10.1074 / jbc.M602563200。
- 11.
赵浩,苏鹏,涂建民,王霞,刘红,Ploscher M, Eichacker L,杨波,周敏,Scheer H: Phycobilin:半胱氨酸-84胆蛋白裂解酶,一种蓝藻藻胆蛋白中半胱氨酸-84结合位点的近乎通用的裂解酶。美国国家科学研究院。2007, 40(4): 344 - 344。10.1073 / pnas.0706209104。
- 12.
赵克红,张洁,涂建明,Bohm S, Ploscher M, Eichacker L, Bubenzer C, Scheer H,王欣,周敏:藻红蛋白和藻蓝蛋白β亚基结合位点的序列重构及其裂解酶活性。中国生物医学工程学报,2007,28(3):341 -341。10.1074 / jbc.M703038200。
- 13.
Glazer AN:光导。光合天线中的定向能量转移。中国生物医学工程学报,1998,26(4):344 - 344。
- 14.
Apt KE, Collier JL, Grossman AR:藻胆蛋白的进化。中华生物医学杂志,1995,26(3):489 - 497。10.1006 / jmbi.1995.0203。
- 15.
MacColl R:蓝藻藻胆体。中国生物医学工程学报,2004,24(3):344 - 344。10.1006 / jsbi.1998.4062。
- 16.
王志强,王志强,王志强,等:细菌主要胆道蛋白的结构特性。中国生物医学工程学报,2003,26(3):344 - 344。10.1007 / BF00416970。
- 17.
藻胆蛋白。方法生物化学学报,1998,17(3):349 - 349。
- 18.
德马萨克NT, Cohen-Bazire G:蓝藻藻胆体的分子组成。美国国家科学研究院。1977, 74: 1635-1639。10.1073 / pnas.74.4.1635。
- 19.
伦德尔DJ,威廉姆斯RC,格雷泽AN:光收集天线的分子结构。聚球菌6301藻胆体棒亚结构的体外组装。中国生物医学工程学报,2001,26(3):366 - 366。
- 20.
刘丽宁,陈晓林,张永珍,周长波:蓝藻和红藻藻胆体中连接蛋白多肽的表征、结构和功能研究综述。生物化学学报,2005,27(3):344 - 344。10.1016 / j.bbabio.2005.04.001。
- 21.
格雷泽AN:通过藻胆体收集光。生物化学学报,1998,15(4):457 - 457。10.1146 / annurev.bb.14.060185.000403。
- 22.
Douglas SE, Penny SL:隐藻Guillardia theta的质体基因组:完整的序列和保守的同构群证实了它与红藻的共同祖先。中华药理学杂志,1999,30(4):344 - 344。10.1007 / PL00006462。
- 23.
Gould SB, Fan E, Hempel F, Maier UG, Klosgen RB:藻红菊酯α亚基跨五种生物膜的易位。中国生物医学工程学报,2007,28(3):339 - 339。10.1074 / jbc.M701869200。
- 24.
阿松崎M,三角,胫骨,Maruyama年代,中田英寿,M, Miyagishima SY, Mori T, Nishida K, Yagisawa F,吉田Y, Y西村,地震区,小林T,桃山Y,这个T, Minoda,佐米,野本H, Oishi K, Hayashi H,太F, Nishizaka年代,哈加年代,三浦年代,Morishita T, Kabeya Y, Terasawa K,铃木Y, Ishii Y,川年代,Takano H,太N,小H,田中K,清水N, Sugano年代,佐藤N, Nozaki H,小笠原群岛N, Kohara Y,小智老师:超小单细胞红藻Cyanidioschyzon merolae 10D的基因组序列。自然科学学报,2004,29(3):344 - 344。10.1038 / nature02398。
- 25.
Asano T, Yoshioka Y, Kurei S, Sakamoto W, Machida Y:拟南芥中编码质体外膜蛋白的CRUMPLED LEAF基因突变影响细胞分裂、细胞分化和质体分裂模式。植物学报,2004,38:448-459。10.1111 / j.1365 - 313 x.2004.02057.x。
- 26.
Mann NH, Clokie MR, Millard A, Cook A, Wilson WH, Wheatley PJ, Letarov A, Krisch HM: S-PM2的基因组,S-PM2是一种“光合作用”t4型噬菌体,感染海洋聚球菌菌株。中华微生物学杂志,2005,27(3):388 - 388。10.1128 / jb.187.9.3188 - 3200.2005。
- 27.
Cavalier-Smith T: Nucleomorphs:被奴役的藻类核。中华微生物学杂志,2002,5:612-619。10.1016 / s1369 - 5274(02) 00373 - 9。
- 28.
Maier UG, Douglas SE, Cavalier-Smith T:隐生植物和氯蜘蛛植物的核形态基因组。生物工程学报,2000,15(3):344 - 344。10.1078 / 1434-4610-00011。
- 29.
Douglas S, Zauner S, Fraunholz M, Beaton M, Penny S, Deng LT, Wu X, Reith M, Cavalier-Smith T, Maier UG:奴役藻核的高度简化基因组。自然科学,2001,42(3):344 - 344。10.1038 / 35074092。
- 30.
Federspiel NA, Grossman AR:从蓝藻Fremyella diplosiphon编码藻红蛋白相关连接蛋白的光调控操纵子的特征。中国生物医学工程学报,2000,29(4):457 - 457。
- 31.
Federspiel NA, Scott L:从蓝藻Fremyella diplosiphon中编码一种新的藻红菊酯相关连接蛋白的光调控基因的特征。中国生物医学工程学报,2003,26(4):344 - 344。
- 32.
de Lorimier R, Bryant DA, Stevens SE: 9 kDa藻蓝蛋白相关连接物多肽的遗传分析。生物化学学报,2000,19(4):529 - 531。10.1016 / 0005 - 2728 (90) 90121 - j。
- 33.
Ughy B, Ajlani G: Synechocystis sp.菌株PCC6803藻胆体杆突变体。微生物学学报,2004,30(3):344 - 344。10.1099 / mic.0.27498-0。
- 34.
李志刚,李志刚,李志刚,李志刚,李志刚:蓝藻菌种分布、菌种历史及特性的研究。中华微生物学杂志,1997,33(3):344 - 344。
- 35.
Gray BH, Lipschultz CA, Gantt E:一种蓝绿色藻类藻胆体。中国生物医学工程学报,2003,26(4):457 - 457。
- 36.
英国Laemmli:在T4噬菌体头部组装过程中结构蛋白的切割。自然学报,1997,27(3):366 - 366。10.1038 / 227680 a0。
- 37.
Schagger H, von Jagow G:用于分离蛋白质的三辛-十二烷基硫酸钠-聚丙烯酰胺凝胶电泳,范围从1到100 kDa。中国生物化学杂志,1997,27(3):366 - 366。10.1016 / 0003 - 2697(87) 90587 - 2。
- 38.
Berkelman TR, Lagarias JC:聚丙烯酰胺凝胶中胆素链接肽和蛋白质的可视化。中华生物医学杂志,1998,26(3):344 - 344。10.1016 / 0003 - 2697(86) 90173 - 9。
- 39.
Zolla L, Bianchetti M:高效液相色谱-电喷雾质谱联用同时分离和鉴定Synechocystis PCC 6803藻胆体蛋白。中国生物医学工程学报,2001,26(3):349 - 349。10.1016 / s0021 - 9673(01) 00532 - 5。
- 40.
Wessel D, Flugge UI:在洗涤剂和脂类存在的稀溶液中定量回收蛋白质的方法。中国生物化学杂志,2004,29(4):344 - 344。10.1016 / 0003 - 2697(84) 90782 - 6。
- 41.
李志强,李志强,李志强:氨基酸序列测定过程中天冬氨酸-脯氨酸肽键的异常裂解。生物化学与生物物理学报,2000,30(4):344 - 344。10.1016 / 0006 - 291 x(70) 90918 - 6。
- 42.
Frangioni JV, Neel BG:酶活性谷胱甘肽s转移酶(pGEX)融合蛋白的增溶和纯化。中华生物医学杂志,1998,29(3):349 - 349。10.1006 / abio.1993.1170。
- 43.
王晓明,王晓明,王晓明,王晓明,等:氨基酸序列分析中蛋白质结构的研究进展。中国生物医学工程学报,1995,26(4):357 - 357。10.1006 / abio.1995.1070。
- 44.
吉祥物的程序。[http://www.matrixscience.com]
- 45.
NCBI蛋白-蛋白爆炸。[http://www.ncbi.nlm.nih.gov/BLAST]
- 46.
TMHMM服务器v. 2.0。[http://www.cbs.dtu.dk/services/TMHMM-2.0]
- 47.
SOSUI蛋白质预测服务器。[http://bp.nuap.nagoya-u.ac.jp/sosui/]
- 48.
CyanoBase。[http://bacteria.kazusa.or.jp/cyanobase]
- 49.
PeptideMass。[http://www.expasy.ch/tools/peptide-mass.html]
- 50.
Edgar RC: MUSCLE:多序列比对,高精度,高通量。中国生物医学工程学报,2004,29(4):344 - 344。10.1093 / nar / gkh340。
- 51.
Thompson JD, Higgins DG, Gibson TJ: CLUSTAL W:通过序列加权、位置特定间隙惩罚和权重矩阵选择提高渐进式多序列对齐的灵敏度。中国生物医学工程学报,1994,22(4):344 - 344。10.1093 / nar / 22.22.4673。
- 52.
LDDist:一个Perl模块,用于计算蛋白质和核苷酸序列的LogDet成对距离。生物信息学,2004,20:416-418。10.1093 /生物信息学/ btg422。
- 53.
Bryant D, Moulton V:邻居网:一种构造系统发育网络的凝聚方法。中国生物医学工程学报,2004,21(4):457 - 457。10.1093 / molbev / msh018。
- 54.
胡森DH,布莱恩特D:系统发生网络在进化研究中的应用。分子生物学杂志,2006,23:254-267。10.1093 / molbev / msj030。
确认
我们感谢Andrew Bozarth对手稿的评论。这项工作得到了德国科学研究院(SFB-TR1, TP A7)的支持。
作者信息
从属关系
相应的作者
额外的信息
作者的贡献
KB, OK和JP进行了除系统发育NG和MALDI-TOF分析外的实验,JN, UGM发起了该项目并担任主管。所有作者都贡献的手稿由KB、OK和UGM设计和撰写,所有作者都阅读并批准了手稿的最终版本。
Kathrin Bolte, Oliver Kawach, Julia Prechtl对这项工作做出了同样的贡献。
权利和权限
开放获取本文由BioMed Central Ltd授权发布。这是一篇开放获取文章,根据创作共用归属许可协议(https://creativecommons.org/licenses/by/2.0),允许在任何媒介上不受限制地使用、传播和复制,前提是正确地引用原始作品。
关于本文
引用本文
博尔特,K.,卡瓦奇,O.,普雷希特,J.。et al。一种藻蓝素-胆素裂解酶的互补集胞藻属sp. PCC 6803具有核胚编码的开放阅读框Guillardiaθ.BMC植物生物学8,56(2008)。https://doi.org/10.1186/1471-2229-8-56
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/1471-2229-8-56
关键字
- 链接器的蛋白质
- 发色团集团
- 比邻
- 藻青素
- 链接器多肽