摘要
背景
促进植物生长的根际细菌正日益被视为补充农业系统中传统投入的一种方式。对其寄主植物的影响是多样的,包括挥发性物质介导的生长增强。本研究旨在评估细菌挥发物对模式草生物产量和根系结构的影响短足(L.)Beauv。
结果
一体外通过不进行任何物理接触的植物-细菌相互作用贯穿气相的实验,筛选了19种菌株在10天共培养期间的促生长能力。根据它们对生物量和根系结构的共同影响,定义了五组细菌,并对其进行了表征。观察到的影响从没有变化到显著增加生物量加上增加根长和分枝。只有挥发性化合物的释放才能增加主根的长度肠杆菌属下水道JM22和短小芽孢杆菌T4。总的来说,最显著的结果是枯草芽孢杆菌总生物量增加81%,总根长、次生根长和不定根长分别增加88.5%、201.5%和474.5%。
结论
本研究首次报道了细菌挥发物对禾本科植物生长的促进作用。观察了生物量生产与根系结构变化的对比调节。大多数增加植物总生物量的菌株也调节了不定根的生长。在我们的筛选条件下,除了初生根长度外,总生物量的产生与根系组成部分的长度和分枝密切相关。目前正在对细菌挥发性化合物的排放动力学进行分析,从而确定对观察到的促生长效果负责的化合物。在我们的内在特征的背景下体外系统,本文识别下一个关键实验步骤,并从基本和应用的角度讨论它们。
背景
在作物环境中,根际(地下)和叶际(地上)细菌对植物生长都有很大的影响[1.–3.].因此,自由生植物,生物膜形成和根殖民化无根瘤菌被认为是可能的占植物,用于增加植物生产率并提高营养利用效率[4.,5.].
植物根际促生菌(PGPR)对其宿主植物具有复杂的作用。其基本机制包括;(1)根系构型(RSA)在吲哚-3-乙酸、细胞分裂素、赤霉素、水杨酸、乙烯和油菜素内酯等介导下对地上部生长的调节作用;(2)磷酸盐溶液化;(3)游离固氮;(4)抑制有害微生物;(5)诱导系统抗性;(6)诱导对非生物约束的系统耐受[1.–4.,6.,7.].
在这些相互作用机制中,细菌挥发性有机化合物(VOCs)的释放对植物生长具有促进作用[6.[Voc介导的植物生长调制现在被广泛认为是一个重要机制[8.]. 除了CO等无机分子2.,co,h2.,n2.,n2.哦,不,没有2.,新罕布什尔州3., H2.S和HCN,微生物能够释放VOCs [5.,9–11.].这些包括酸、醇、酮、醛、酯、萜类、芳香族、含氮和含硫化合物和乙烯[7.,12.,13.].在这些化合物中,尽管已经确定了300种候选分子,但尚未识别出对观察到的植物生长的变化负责[8.,9]主要是因为细菌挥发物可以作为单独的化合物或混合物[13.].
细菌挥发性接触可导致植物生物量增加(多达六倍)或接触21天后植物死亡拟南芥(l)海宁对细菌挥发物[8.,11.]. 总的来说,细菌挥发性有机化合物对植物生长的正面影响比负面影响少[8.,14.]. 在阳性方面,8种细菌挥发物(2,3-丁二醇、3-羟基-2-丁酮、2-戊基呋喃、N,N-二甲基十六胺、CO2.,已经显示了13-四烷基二烯-1-醇,2-丁酮和2-甲基-N-1-三十六烯促进植物生长[6.,8.,15.–19.]. 在模型植物上观察到的短期促生长效应,A. Thaliana.,暴露于枯草芽孢杆菌GB03挥发物包括:(1)细胞分裂素的调节[6.],乙烯[20.,21.]、生长素、水杨酸、油菜素类固醇、赤霉素[4.]、脱落酸和茉莉酸[21.信号通路;(2)较高的光合能力、叶绿体数量、叶绿素含量、淀粉积累和铁吸收[22.];(3)通过在植物组织中积累胆碱和甘氨酸甜菜碱的积累来增加渗透,盐和干旱胁迫的耐受性[23.,24.]; (4) 降低疾病症状的严重程度(5) 活性氧敏感性降低[25.]; 对病原菌的抗性增强[13.]. 类似的长期影响也被描述过[26.]以及其他植物物种,如烟草卡雷尔码头[27.,28.]以及Agrostis Stolonifera.l . (11.,29.].
另一方面,已经在植物,真菌和病原体细菌上注意到了流离虫挥发物的中性或负面影响[14.,30.]. 氰化氢,由少量细菌产生,包括假单胞菌[10.]以及发色菌可能是它们对小麦产生负面影响的原因。互补的是,负面影响Serratia.物种A. Thaliana.已经归因于二甲基二甲基,β-苯基 - 乙醇和无机挥发性NH3.[8.,13.,18.,31.].
尽管进行了这些研究,但仍有几个问题没有得到解答,需要加以解决。到目前为止,仅有两篇关于根际细菌挥发物对草生长影响的研究发表。观察到的影响是负面的[32.或非显着的[30.].因此,到目前为止,细菌挥发物对生长没有明显的促进作用Poaceae.已被证明。草科成员的根系发育在整体结构和个体根的解剖上是不同的[33.],这可能导致与已知的那些不同的挥发效应A. Thaliana.(单科科镜vs双子叶植物)。
关于RSA测量,大多数体外研究使用水平培养皿,根生长在琼脂培养皿中,从而限制其暴露于水溶性挥发性化合物。此外,很少有研究利用专门的实验装置来描述微生物挥发性物质介导的RSA修饰[7.,13.,18.,34.].存在的结果表明细菌VOC能够调节根系形态发生过程,并且这些RSA修改可能与生物质生产有关[7.,13.].
本研究旨在探讨细菌挥发性化合物对小麦生物量的影响短足(L.)博夫(Bd21行),基于10天体外co-cultivation。属毛花瓣在系统发育上接近温带谷类属Triticum,Hordeum和阿韦纳犬足亚科[35.,36.],现在被认为是研究谷物根系发育及其对植物产量影响的一个很有前途的模式属[37.,38.].在这项研究中,我们寻求回答以下问题:细菌挥发物诱导的主要植物表型是什么?根据生物量生产和RSA导致我们的筛查系统,菌株的效果最大?观察到的效果如何与诸如的二象植物报告的效果不同A. Thaliana.? 结果是讨论的背景下的潜力和限制的问题体外研究中使用的系统。
结果
产品特点体外共育系统
为了暴露b . distachyonBd21植株对细菌挥发物的抑制作用及其对生物产量的影响在测定RSA参数的同时,建立了一个近垂直共培养系统(图。1.).细菌生长介质是基于[15.]它的组成是一个折衷的最低限度的媒体和营养之一。这些植物生长在含有霍格兰德培养基的琼脂平板上,霍格兰德培养基与细菌在物理上分离,但环境相同。试管苗可在22℃下保存10天。叶和根生长在琼脂平板的顶部,因此暴露于细菌挥发物中,无论它们在琼脂中的极性或溶解度如何。植株可能产生三种根:初生根(PR)、次生根(SR,PR的分枝)和不定根(AR,Fig。1.).这三种类型的根对应于“主要开放轴根”,“分支根”和“植物精神病源”(“植物精神性节奏根”)定义为[39.]. 这个实验装置没有诱导任何梯度效应,因为所有的植株都位于离挥发性化合物来源相同的距离。
体外co-cultivation系统。b . distachyonBd21植株在接近垂直生长10天后拍摄,没有(左侧)或(右侧)暴露于BsuGB03挥发物。细菌室里有一个法拉格等。[15.]培养基和植物舱含有Hoagland琼脂板。两种越来越多的培养基都是物理分离的,这将植物细菌与挥发物交换限制相互作用。秤杆长1.75厘米。箭头指向不定根(AR),二次根(SR)和主要根(PR)位置
主成分分析(PCA)和应变聚类
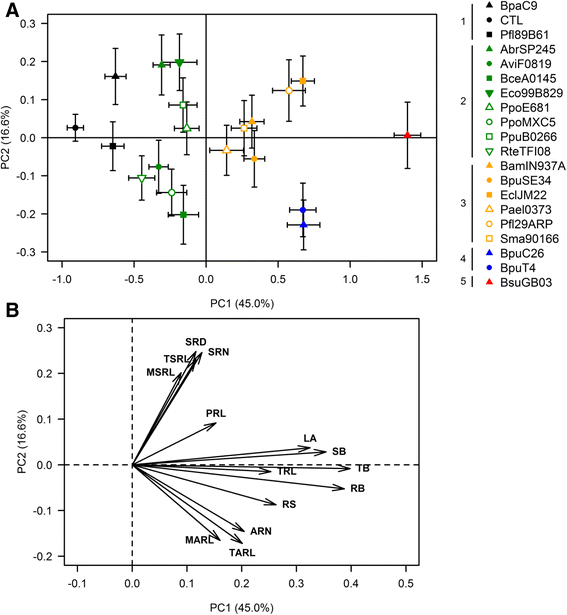
测量了十四变量b . distachyon与19种细菌菌株进行10天挥发性化合物相互作用后的植株(图。4.和5.,附加文件1.:图S1)。为了在其生长调制能力方面对菌株进行分组,基于加权和降低的变量对数据集进行PCA(图。2.).这种处理使我们能够为生物量或rsa相关的变量类分配相同的重量。在每个类中,每个变量具有相同的权重,不管其数量级如何。然后利用14个主成分(PCs)作为输入变量,基于欧氏距离和Ward算法对菌株进行聚类。
轴1和轴2占总方差的61.6%。轴1与菌株的总生物量(TB)、根生物量(RB)、地上部生物量(SB)、叶面积(LA)和总根长(TRL)值呈正相关(图。2B.). 相反,轴2与RSA调制有关,并且与次根生长(次根数(SRN)、总次根长(TSRL)、平均次根长(MSRL)和次根密度(初生根每厘米的次根数,与不定根生长(不定根数、总不定根长和平均不定根长)呈负相关。
基于PC值,聚类算法允许我们定义5个菌株簇,诱导植株表型的一致变化(图。3.).与对照相比,聚类1中包含的菌株对植物表型没有显著影响。只有3株2型菌株的生物量略有增加,但总体效果不显著。簇2菌株对根分枝过程的影响是可变的。3组和4组菌株显著增加了生物量,但对RSA的影响不同。簇5中只包含一个菌株,其促生能力最强(图5)。3A).
簇组成(图。2A)
除对照(无细菌生长培养基)外,簇1还含有BpaC9和Pfl89B61。聚类2有8株菌株,隶属于7个种,分为2个亚群:(1)AbrSP245、Eco99B829、PpoE681、PpuB0266,PC2阳性;和(2)具有负PC2值的AviF0819、BceA0145、PpoMXC5和RteTFI08。在第3群的菌株中,大多数菌株(BamIN937A、BpuSE34、EclJM22、PaeI0373、Pfl29ARP和Sma90166)的PC1阳性值较低。BpuC26和BpuT4定义了第4簇,属于第5簇的菌株只有BsuGB03。
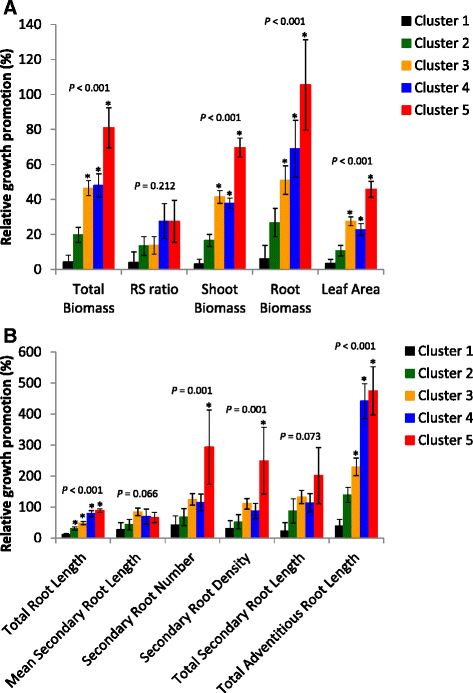
进一步根据其对生物质和RSA变量的相对生长促进效应来表征每个簇(图。3A和B分别)。对于每个变量,聚类效应表示为在给定的聚类内的菌株的重复与没有细菌的对照之间的相对差异的平均值。
主要挥发性化合物介导的生物质生产调节(图。3A)
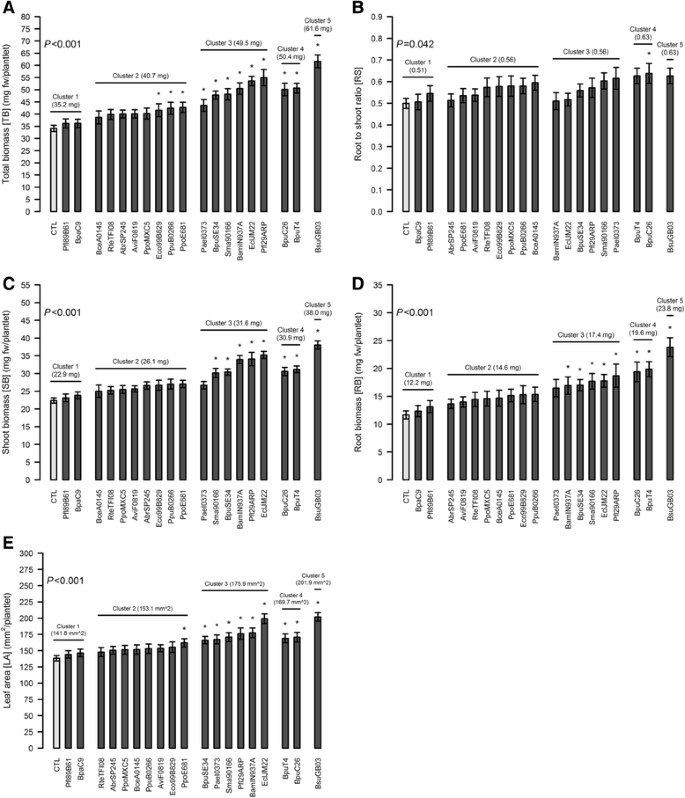
在生物量生产方面,对照植株的TB为34.1 mg,根冠比(RS)为0.50(图。4A).与对照相比,暴露于聚类1菌株释放的挥发物的植株在所有测量参数中均没有显著增加(RB最大增加6.2%)。集群2菌株对结核分枝杆菌(TB)的总体增加(+ 19.7%)不显著,主要是促进了根系生长(+ 26.8%)。簇3和簇4中TB的增幅较高(分别为+46.5和+ 48%),但这些簇的植株生物量分配存在差异。事实上,4组菌株诱导了RB的更高增长(+ 69%)。集群5的生物量产量增幅最高(+ 80.9%),其RS位移(+ 27.5%)与集群4的值非常相似。值得注意的是,第5组RB产量为对照水平的205.5%(+ 105.5%,图。3A). 最后,在聚类5中,LA增加了45.8%,这一性状与所有已定义聚类的SB产量成正比。
单个菌株的生物量调节潜力
除了鉴定受细菌挥发物暴露调节的主要草植物表型外,本研究还试图筛选单个菌株的生长促进能力(图。4.).
结核病受到细菌挥发物的显著调节(P < 0.001). 在19个菌株中,12个菌株诱导了结核产量的显著增加(图。4A),范围从41.6 mg (Eco99B829)到61.6 mg (BsuGB03)。如前所述,Pfl89B61和BpaC9(聚类1株)没有显著影响,所有考虑的变量也是如此。
八分之三的2类菌株诱导了结核产量的显著增加:Eco99B829、PpuB0266和PpoE681。所有三个都属于同一亚组,其特征是PC2值为正值。除了一个菌株的LA外,所有其他与生物量相关的性状在这个聚类中都没有受到影响(PpoE681,图。4E). 由于其狭窄的PC1定位(图。2.)聚类2表明,无论变量是什么,生物量生产的聚类内变异性都很低。
相比之下,第3类菌株在PC1轴上分布更广,因此表现出更大的异质性,TB范围为43.6 mg(PaeI0373)到54.9 mg(Pfl29ARP)。所有6个菌株都表现出显著的增加TB和LA的能力,只有那些暴露于PaeI0373挥发物的植株在SB和RB中没有表现出任何显著的变化(图。4C和D分别)。如簇2菌株所观察到的,单个RS值仍然统计上不受所有六种菌株的影响(图。4B.).
聚类4株(BpuC26和BpuT4)对生物量产生的影响相似,均增加了TB、SB、RB和LA。与聚类1、2和3相比,这些菌株诱导的RB产量更高,平均RS值更高(0.63),但BpuC26是19个菌株中唯一能够显著改变RS的菌株。集群5单枯草芽孢杆菌与对照相比,菌株(BsuGB03)诱导的TB、SB和RB产量最高(分别为61.6mg、38.0mg和23.8mg),对RS值无显著影响。
根系结构的主要挥发介导的介导的调制(RSA)
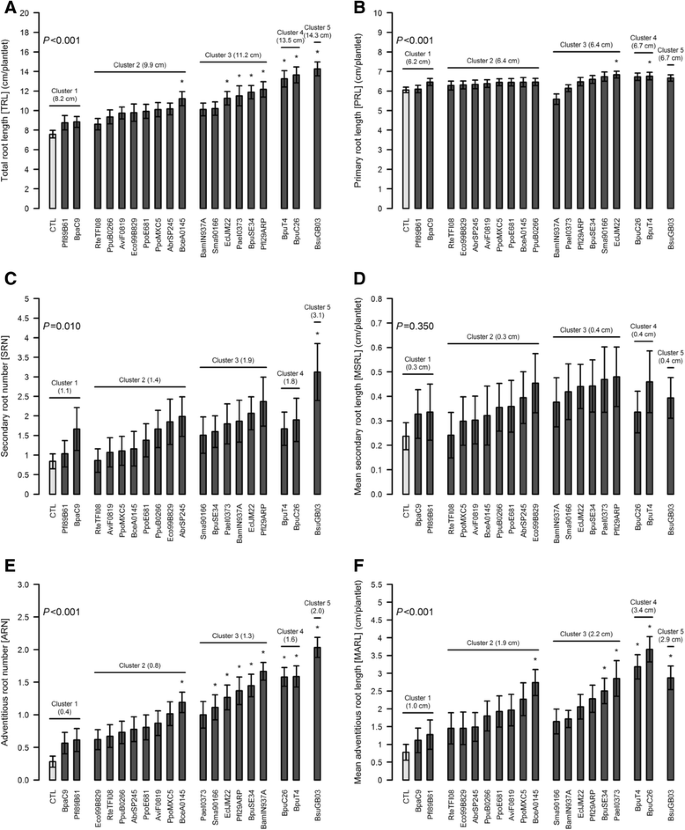
关于RSA,选择到PC1和PC2的最相关的变量以表征每个应变组(图。3B.). 对照植株TRL为7.6cm,次生代谢有限(SRN公司= 0.8;TSRL. = 0.5cm)或不定根产生(TARL = 1厘米)。因此,SRD限制在0.1个次生根cm−1.原代根源(图。5.,附加文件1.:图S1)。群集1在生物质生产或RSA参数中显示出没有显着增加。与生物质生产不同,群体2株能够诱导TRL的总体增加30.8%。簇3和4的RSA调制能力与它们各自的RS值一致。两种群集都促进了总生物质生产,但簇3的TRL增加限制为48.4%,而组合4的增加率为78.7%。簇4(+ 441.5%)比簇3更高(+ 441.5%)(+229.7%)。Cluster 5在TRL(+ 88.5%)的增加最高,由于没有细菌的对照,TARL(+ 474.5%)和SRN(+293%)几乎完全增加。MSRL增加(+65.9%)并不重要。
单个菌株对根体系结构(RSA)的调节
总的来说,除了TRL和原子根长度(PRL,图3)之外,RSA参数的可变性高于生物质变量的变量(PRL,5.). 没有一个集群1菌株引起RSA变量的显著变化。
对于第2类菌株,只有BceA0145引起TRL、ARN和MARL的显著变化(图。5,E和F). 因此,它主要负责上述整个集群2 TRL的重大变化。这些菌株对PRL、SRN或MSRL均无显著影响(图。5 b,C和D). 值得注意的是,PC2阳性菌株的SRN和MSRL最高。除RteTFI08外,PC2阴性的ARN和泥灰岩也是如此。六分之四的菌株在集群3中增加了TRL。相比之下,BamIN937A和Sma90166没有引起TRL的显著变化,并且给出了最低的MSRL和MARL值。此外,与对照组(6.1cm)相比,BamIN937A挥发物似乎稍微降低了PRL(5.6cm)。BamIN937A挥发物对PRL的这种负效应被平均SRN(1.9)和高ARN(1.7)所平衡。唯一增加PRL的第3群菌株是EclJM22(6.8cm)。在第3组水平上,SRN和MSRL没有统计学意义的影响。除PaeI0373外,所有3类菌株的ARN均升高。该菌株与BpuSE34一起诱导产生显著更长的不定根(图。5 f).ARN和MARL均显示出高的簇内变异性,范围为1.0至1.7,从1.6到2.9厘米的小植物−1., 分别。
第4群菌株增加了TRL、ARN和MARL,但对SRN和MSRL无显著影响。平均而言,与次生根性状相反,第4类菌株比第3类菌株更有效地促进了不定根的生长。只有BpuT4显著增强PRL(6.8cm)。如图所示。5 bRSA参数是受细菌挥发物影响最小的性状之一。
群集5菌株(BSugb03)对大多数RSA参数的显着影响,除了PRL和MSRL。它引起最高的TR1(14.3cm),主要由高Srn和Arn值解释(分别为3.1和2.0,vs对于没有细菌的对照,分别为0.8和0.3)。
生物产量与根系构型(RSA)性状的相关性研究
在我们的实验中,结核病的产生主要与TRL、SRN、ARN和SRD相关,与R值范围从0.82到0.89,以及TSRL和TARL的程度较小R值分别为0.72和0.75。PRL是RSA参数中相关性最小的(R = 0.41),与其他RSA参数均无显著正相关(促进根系生长)或负相关(初生根与次生根或不定根生长之间的代偿效应)。
讨论
细菌挥发物对模式草的早期发育有重要影响
如图1所示。1.,受到Bsugb03挥发物的代表性植物达到3-叶阶段(第13阶段,[40),而对照植株只有两个展开的叶片(第12期)。这一观察结果与[41.]表明PGPR可以诱导植物生长速率的显着变化。这也可以解释观察到的RSA差异,因为b . distachyon据了解,在第13期,小苗最多可产生两个胚芽结不定根[39.]. 在我们的在在离体系统中,TB的产生与次生根和不定根生长相关的性状密切相关。结核产量与PRL的相关性较弱。肺结核与PRL以及TSRL之间的相关结果相似A. Thaliana.由(7.],表明分枝的根系表型似乎与增加的SB生产相关联。
除了BPUC26,Plantlet的生物质分配(RS)没有受细菌挥发物的显着影响。因此,观察到的生长促进效果似乎没有由于用于增加根生长而不是拍摄发展的能量。
对比生物量和根系结构(RSA)的调节定义了五组细菌菌株
在这项研究中使用的细菌挥发物导致五组表型被定义。
第1组菌株(BPAC9和PFL89B61)在植物生物质生产或RSA中10天后不会导致任何显着变化。
第2组8株菌株中有3株(Eco99B829、PpuB0266和PpoE681)能显著提高植株总生物量。这反映了以较高的SRN和MSRL为特征的改变的根分枝。
组3的特征是生物质产量高,但对TRL的影响较小。该组含有BamIN937A、BpuSE34、EclJM22、PaeI0373、Pfl29ARP和Sma90166,均能显著促进植物生长。
类群4中有两株属于同一种的菌株BpuC26和BpuT4具有较高的促生长潜力。两者均诱导了RB和TRL的大量增加,显著影响了BpuC26的生物量分配。
簇5中的单个菌株BsuGB03的生物量最高,RB为对照的205.5%。BsuGB03诱导的TRL增加最多(+ 88.5%),几乎完全是由于TARL(+ 474.5%)和SRN(+293 %)的增加,对主根的生长没有显著影响。
研究了BsuGB03、BamIN937A、EclJM22、BpaC9、Pfl89B61和Pfl89B61对植物生长的调控能力洋葱伯克霍尔德菌与[6.]和[11.] 上A. Thaliana.. Sma90166,BpuT4,Eco99B829,铜绿假单胞菌和假单胞菌putida不过,情况有所改善b . distachyon对生物质产量无任何显著影响A. Thaliana.生长 [6.,11.].观察到的差异可能是由于接收植物种类或技术限制(例如,细菌和植物培养基组成,培养皿体积或倾角),导致不同的挥发性浓度和感知在密封系统。
可变性一直存在到种内级别,与分类无关
我们的结果与现有文献一致,他们认为特定菌株的促生长作用是特异的[7.,41.].具有细菌挥发性排放型材,不同于属,物种和菌株水平[11.,42.,它们的挥发性物质介导的生长促进能力可能会有所不同。属于同一种的菌株可以诱导相当一致的植物生长促进(例如,短小芽孢杆菌和多粘菌拟杆菌菌株)或对生物量生产和RSA有更多可变影响(例如。,假单胞菌荧光菌株)。
以往对PGPR的研究主要集中在革兰氏阴性菌上[7.,43.,44.].最近,芽孢杆菌这些菌株已经过促生长能力的测试[7.]. 在本研究中,我们的菌株选择包括革兰氏阳性菌和革兰氏阴性菌(表1)1.).从生理来看,大多数革兰氏阴性细菌都无法形成孢子[45.]. 这可能会影响它们在自然不利条件下或在使用前的配方或储存期间的存活率[43.].在我们的筛查条件下,针对革兰氏阳性和革兰氏阴性菌株观察到生长促进,这与获得的结果一致A. Thaliana.for BsuGB03 and EclJM22 [6.].虽然群集4和5株属于革兰氏阳性芽孢杆菌结果表明,革兰氏阳性菌具有较高的促生长能力。强调这一点的是:(1)集群3和2菌株组成(2) 存在芽孢杆菌阴性对照群中的菌株(BpaC9);(3)基于革兰氏染色结果的细菌群的多系性[46.,47.].
对比效果表明细菌挥发性生产中的一些异质性
诱导植株表型的变化从一个集群到另一个集群有很大的差异。因此,我们假设,细菌排放的挥发性混合物在数量(挥发浓度)和质量(挥发特性)上都符合这一观察结果。这一假设必须基于本研究中使用的菌株的挥发性释放动力学的全面分析来评估。在公认的生物活性挥发物中,细菌释放的最重要和突出的无机挥发物是氨(特别是在富含蛋白质的介质中)、二氧化碳和HCN。此外,2,3-丁二醇及其前体acetoin很可能在含蔗糖、低pH的Murashige & Skoog培养基上产生[8.,15.].微生物同时生产2,3-丁二醇和CO2.丙酮酸通过发酵过程合成挥发性前体3-羟基-2-丁酮(乙酰)[30.].体外因此,所观察到的挥发物介导的生长促进效应可能至少部分地与CO有关2.排放(13.,48.].CO的显着增加2.然而,在我们的实验中,由于细菌排放而导致的浓度不太可能,因为它是由CO密封的2.-permableparafilm®[11.].测试该假设的实验可以通过吸收CO来进行2.带Ba(OH)2.,测量CO2.在反应容器中或进行实验时不加任何密封。关于其他具有生物活性的细菌挥发物[8.,16.–19.,它们在促进生长中的作用b . distachyon仍有待调查。更具体地,应研究促进靶向过程的挥发性影响,驾驶主要,次要(横向)和不定(冠部)根系开发。实际上,众所周知,细菌挥发物能够调节主要荷尔蒙途径[4.,6.,20.,21.]并且,特定和共享的荷尔蒙途径都参与了后后根发育[49.–51.].
从体外田间条件
这个体外本研究中使用的共培养系统使我们能够在10天共培养期内筛选19种细菌菌株以获得挥发介导的植物生长促进能力。这个b . distachyon试管苗在接近垂直的琼脂平板上生长,同时在添加蔗糖和胰蛋白酶大豆琼脂的Murashige&Skoog培养基上接种细菌[15.]. 以往的研究表明,VOC的分布和细菌挥发物的促生长作用可能与接种量和培养基组成有关[11.].由于这19种菌悬液过夜生长的技术限制,我们的接种量限制在2*106.菌落形成单位(20 μl的一个108.菌落毫升−1.细胞悬液),低于[6.]和[7.]. 介质[15.]在这项研究中使用的是一种基于Murashige&Skoog的培养基,它允许所有19个菌株生长,同时释放出少量的挥发性有机化合物(Farag M.,pers)。com.)。值得注意的是,当在其他研究中使用营养不良的培养基如Murashige&Skoog或Angle培养基时,接种剂量不影响结果[11.].此外,促进植物生长的作用是由芽孢杆菌只有使用Murashige&Skoog培养基培养细菌和植物时,才能观察到挥发物[8.].因此,所观察到的不同细菌挥发物对植物生长的影响必须符合培养基依赖性的要求。本研究的结果也是如此。
将获得的结果转换到现场条件并不简单,仍然具有挑战性[52.]. 部分原因是技术限制(例如,培养皿的大小和体积,近垂直共培养系统)限制了植物培养过程的持续时间,从而限制了本研究的范围到早期发育阶段。在田间,为了在农艺条件下优化资源利用效率,根系主要觅食区最好位于土壤资源丰富的区域[53.]. 在本研究中,观察到的RSA调制可能有助于提高对短暂或长期干旱胁迫的耐受性,因为土壤上层的根系分枝增加(表土觅食),或者在较小程度上,主根更长(深层土壤觅食)。这样的根系表型也可以帮助植物有效地获取相对固定的(P,K)或流动的(N)养分[53.–55.].此外,各种限制(例如,内源土壤微生物种群、土壤组成、孔隙度和通气、根际沉积等)可能影响细菌的生长和挥发性物质的释放,从而调节田间条件下挥发性物质介导的植物-细菌相互作用的结果。
未来前景
现在表征了一整套菌株的挥发性排放动力学,以鉴定促进的挥发性化合物/混合物b . distachyon增长。SuperScent公共数据库中有770多种细菌挥发性有机化合物(http://bioinf-applied.charite.de/superscent/index.php? site1/4home.,[9,13.])和“MVOC”数据库中的350个细菌和80种真菌物种约1000个微生物VOC(http://bioinformatics.charite.de/mvoc/,[5.,56.])。一旦确定了活性化合物,就应该进行更接近田间条件的实验。一方面,b . distachyon试管苗可以暴露于细菌挥发性混合物的基础上例体外设置类似于[48.] 或者 [19.].这可以使植物(1)在不直接将整个植物暴露于挥发性混合物的情况下感知到根系中的挥发性特征;(2)达到成熟RSA对应的较早的发育阶段。另一方面,挥发性有机化合物的缓释制剂,如用于综合防治病虫害的制剂[57.可用于将根系暴露于受控的VOC浓度,并评估其在真实土壤条件下的影响。实际上,来自释放点的VOC扩散速率可能受到它们的极性和土壤基质的物理化学特性的影响[12.,13.].
结论
据我们所知,这项研究是第一次报告细菌挥发物介导的生长促进草植物。使用体外近垂直筛选设置,五组菌株诱导一个特征变化b . distachyon定义了表型。观察到与RSA的变化相结合的生物质产生的对比调节。大多数植物生物量增加的菌株也调节不定根生长。在我们的筛查条件下,除了原始根长度之外,总生物质产生与根系组件的长度和分支强烈相关。无论是否考虑过的表型变量,枯草芽孢杆菌GB03的挥发性化合物引起的变化最为显著。考虑到细菌挥发物产生的多样性,需要进一步的实验来描述这些细菌菌株的无机和有机挥发物释放动力学,以便确定对所观察到的促生长效应负责的候选菌株,并评估它们在农业土壤条件下对植物生长的影响。
方法
植物材料
短足(BD21线)由Philippe Vain博士从John Innes Center(诺维奇,英国)博士提供友情,并在2009年在温室条件下宣传。
细菌菌株
本研究中使用的细菌菌株是根据其潜在的PGPR特性和/或其在氮循环中的作用选择的(表1)1.).解淀粉芽孢杆菌In937A(BamIN937A),巴氏芽孢杆菌C9(BpaC9),短小芽孢杆菌T4(BpuT4),短小芽孢杆菌SE34(BpuSE34),枯草芽孢杆菌GB03 (BsuGB03),肠杆菌属下水道JM22(ECLJM22),大肠杆菌DH5α99B829(Eco99B829),多粘菌拟杆菌E681(PpoE681),假单胞菌荧光89b61(pfl89b61)和粘质沙雷氏菌90166(Sma90166)由Paul W。帕尔和John McInroy博士(德克萨斯理工大学,卢博克,TX,美国)。假单胞菌荧光29ARP(PFL29ARP)由Alain Sarniguet博士提供(Institut National de La Recherche Agrormique,Rennes,法国)。Azospirillum brasilenseSP245(AbrSP245),Azotobacter vinelandii.F0819.(AVIF0819),短小芽孢杆菌C26(BpuC26),洋葱伯克霍尔德菌A01-45(BCEA0145),多粘菌拟杆菌MXC5 (PpoMXC5),铜绿假单胞菌I03-73(PAEI0373),假单胞菌putidaKT2440-B0266 (PpuB0266)和Raoultella terrigenaTfi08 (RteTFI08)来自鲁汶大学(Leuven,比利时)收藏。
这些菌株的主要特征,包括研究中使用的缩写词、革兰氏类型和分类位置,见表11..
体外筛选
短足植株和菌株共培养体外在22°C条件下,在一个12 cm方形培养皿(植物室)与3.5 cm圆形培养皿(细菌室)底部相结合的系统中培养10天,以便仅允许整个气相的相互作用(图。1.).
肉阜表面消毒,如[58.]和[59.]. 在室温下蒸馏水中培养2h后,去除外稃并将籽粒储存在蒸馏水中。然后在70%v/v乙醇中连续培养30s,在无菌蒸馏水中冲洗一次,在手动搅拌下在1.4%v/v次氯酸钠溶液中表面灭菌4min,然后用无菌蒸馏水冲洗三次。在0.8%w/v植物琼脂(Duchefa Biochemie B.v.,Haarlem,荷兰)平板上,含1×Hoagland培养基(6 mM KNO)的培养基,在4°C的条件下,将颖果在黑暗中分层2天3.,4毫米Ca(无3.)2.,2毫米MgSO4., 1mm NH4.H2.人事军官4.,17.97μM酒石酸铁.2H2.O、 46.25μM小时3.薄熙来3.,9.15μM MnCl2..4H2.O、 0.77μM氧化锌4.0.7小时2.o,0.32μmcuso4.0.5小时2.o,0.11μmnamoo4..2H2.o,参考。30630037-1,PlantMedia,Dublin,OH,USA),在94μmolm下在22°C下转移24小时之前−2.S−1.在具有20-H Photopheriod的PAR(LED照明)中,符合BrachyTag培养方案[58.,59.].颖果被放置在琼脂板上,胚胎面对培养皿盖。培养皿以65°的角度倾斜,以确保根部在琼脂皿上正常生长[7.].
在共培养的开始前一周,将每种细菌菌株从其20%V / V甘油储存悬浮液中贮藏在-80℃下。将所有上述菌株均在4%w / v胰蛋白酶琼脂(Sigma-Aldrich,Saint-Louis,Mo,USA)上铺板,除了(1)pfl29ARP和AVIF0819,在2.5%w / v溶酶体肉汤(Sigma-Aldrich)含有1.5%w / v琼脂的微生物学(Sigma-Aldrich)和(2)ABRSP245和BCEA0145,其在补充有2.5mM CaCl的改性溶酶体肉汤中生长2.和2.5毫米MgSO4..24小时前,将菌株再次镀于相应的培养基上,然后开始在液体培养基([15.]1×Murashige&Skoog培养基[Duchefa Biochemie B.V.],添加1.5%蔗糖和0.4%胰蛋白酶大豆肉汤[Sigma-Aldrich])。随后将每个菌株浓度调整为108.菌落毫升−1.在共培养步骤开始之前。
在22℃下发芽24小时后,两个b . distachyon将小植物转移到含有45ml的Hoagland的培养基(Plantmedia)的每个平方12厘米培养皿中。然后将20μl的每个细菌悬浮液移液在含有3ml的细菌室中[15.]培养基(1×Murashige&Skoog培养基,添加1.5%w/v微生物琼脂[Sigma-Aldrich]、1.5%蔗糖和0.4%胰蛋白酶大豆琼脂[Sigma-Aldrich])。在用Parafilm®(美国伊利诺伊州芝加哥市Pechiney塑料包装公司)密封12 cm培养皿之前,在层流下干燥细菌悬浮液滴[6.])。由此产生的共培养菜肴使植株在22℃下在94μmolm下的细菌存在下超过10天的生长−2.S−1.在具有20-H Photopheriod的PAR(LED照明)中。进行了四种独立的实验重复。在每个实验中,考虑每种菌株的16种植体,32种植物用于对照的对照,没有细菌,只包含[15.] 中等的。在共培养过程结束时,记录了Tb,Sb,Rb,Rs,La和九个RSA参数。
叶面积(LA)测量
共培养10天后,打开培养皿除去冷凝水,准备根和叶进行数据收集。每个培养皿用一个1000万像素的Finepix HS10相机(日本东京富士胶片控股公司)拍摄。根据制造商的说明,使用MVHimage软件v8(Global Systems Science,Boston,MA,USA)测量每个植株的预计LA。
根系统架构(RSA)分析
每个根系系统用针手动未解开,以便在HP ScanJet G4010 A4扫描仪(Hewlett-Packard,CA,USA)上扫描200DPI之前分离混合的侧根。用Ez-Rhizo软件分析所得到的图像[60],符合制造商的说明。每个输出文件都进行了手动检查和编辑,以纠正根自动检测中的错误。小于1mm的次生根和不定根被丢弃,RSA参数的计算和多元分析不考虑。对每株植株进行PRL、SRN、MSRL、TSRL、SRD(每cm主根次生根数)、ARN、MARL、TARL和TRL记录。
统计分析
用r3.0.3软件进行多因素和单因素统计分析[61]运行FactoMineR包1.25[62].使用14个测量变量,PCA对加权,居中并缩放到零均值和单位方差的数据进行。这种方法为生物量和RSA变量类分配了相同的总重量,并限制了与录制的RSA参数的数量相比的生物量相关变量的数量相关的偏差(5vs9,分别)。在每类变量中,每个测量的参数具有相同的权重,而不管其数量级。然后基于欧几里德距离和病房算法用作基于欧几里德距离的分层聚类的输入变量。
基于正态Q-Q(正态性检验)和尺度定位(方差相等检验)图对总体应用条件进行验证后,以各菌株为固定因子,对各变量进行双向方差分析(ANOVA)。以四个实验重复为随机因子,以它们的相互作用为比较基础。当应变对某一特定变量的影响显著(p < 0.05)时,采用Dunnett’s检验分离平均值。在这些图表中,与对照组显著不同的平均值(α= 5%)用星号(*)标记。
支持数据的可用性
支持本文结果的数据集包含在文章和其附加文件中。
缩写
- 方差分析:
-
方差分析
- ar:
-
不定根
- 阿恩:
-
不定根根数
- 拉:
-
叶面积
- 泥灰岩:
-
平均不定根根
- MSRL:
-
平均次根长
- 个人电脑:
-
主要成分
- PCA:
-
主要成分分析
- PGPR公司:
-
植物生长促进relizobacteria
- PR:
-
初生根
- 光杆载荷:
-
主要根长
- RB:
-
根系生物量
- 卢比:
-
根到拍比
- RSA:
-
根系统架构
- SB:
-
射击生物量
- 销售代表:
-
二次根
- SRD公司:
-
次生根密度
- SRN编号:
-
二次根数
- TARL:
-
总不定根长度
- 结核病:
-
总生物量
- TRL:
-
总根长
- TSRL编号:
-
总二次根长度
- VOC:
-
挥发性有机化合物
参考
- 1。
Bulgarelli D、Schlaeppi K、Spaepen S、Ver Loren van Themaat E、Schulze Lefert P。植物细菌群落的结构和功能。植物生物学年鉴。2013;64:807–38.
- 2。
Prashar P,Kapoor N,Sachdeva S.根际:其结构,细菌多样性和意义。Rev Environ Sci Biotechnol。2014; 13:63-77。
- 3.
Pii Y, Mimmo T, Tomasi N, Terzano R, Cesco S, Crecchio C:根际微生物相互作用:促进植物生长的根际细菌对养分获取过程的有益影响。复习一下。生物肥料土壤2015,DOI 10.100。
- 4.
Ryu C-M,Hu C-H,Locy Rd,Kloepper JW。拟南芥植物根瘤菌引发植物生长促进机制研究。植物土壤。2005; 268:285-92。
- 5。
Peñuelas J, Asensio D, Tholl D, Wenke K, Rosenkranz M, Piechulla B, et al.;土壤中的生物挥发性排放物。植物细胞环境。2014,37:1866 - 91。
- 6.
Farag MA,胡,C-HH,Reddy MS,卫H-X,PAR等,Arabidopsis细菌挥发物促进生长。美国国家科学院学报。2003;100:4927–32.
- 7.
Gutiérrez-luna fm,alpez-bucioj,altamirano-hernándezj,瓦伦西亚-cerero e,Cruz Hr,Macías-RodríguezL.植物生长促进relizobacteria通过挥发性有机复合发射来调节拟南芥拟南芥的根系结构。共生。2010; 51:75-83。
- 8.
Bailly A,Weisskopf L。细菌挥发物对植物生长的调节作用。当前知识和未来挑战。电厂信号行为。2012;7(一月):1–7。
- 9.
Schulz S, Dickschat JS。细菌挥发物:微生物的气味。Nat Prod rep 2007; 24:814-42。
- 10.
Blom D、Fabbri C、Eberl L、Weisskopf L。挥发性物质介导的细菌杀灭拟南芥主要是由于氰化氢。应用环境微生物学。2011;77:1000–8.
- 11.
Blom D,Fabbri C,Connor EC,Schiestl FP,Klauser DR,Boller T等。植物生长调节挥发物的产生在根际细菌中广泛存在,并且强烈依赖于培养条件。环境微生物。2011;13:3047–58.
- 12.
Wenke K,Kai M,Piechulla B.以下地下挥发物促进植物根系与土壤生物之间的相互作用。Planta。2010; 231:499-506。
- 13。
文可K,魏世泰,华科R,瓦尔弗德C,万科D,凯M,等。植物的生物通讯。编辑:Witzany G,Baluška F。植物中的信号和通信。第14卷,柏林,海德堡:施普林格-柏林-海德堡;2012.电厂信号和通信。
- 14。
Vespermann A,Kai M,Piechulla B.流离虫挥发物影响真菌和拟南芥的生长。申请环境微生物。2007; 73:5639-41。
- 15.
Farag M,吕C-M,Sumner LW,帕尔PW。根际细菌挥发物的GC-MS-SPME分析揭示了植物促生长和诱导系统抗性的潜在诱导因子。植物化学。2006;67:2262–8.
- 16。
Zou C,Li Z,Yu D.芽孢杆菌菌株XTBG34通过生产2-戊基呋喃来促进植物生长。J microbiol。2010; 48:460-6。
- 17.
通过对节肢杆菌(Arthrobacter agilis)中二甲基十六烷基胺(dimethylhexadecylamine)的分析,发现二甲基十六烷基胺(dimethylhexadecylamine)对细菌生长和紫花苜蓿(Medicago sativa)形态形成具有调节作用。土壤植物。2011;339:329-40。
- 18.
魏斯T,凯M,皮埃丘拉B。细菌氨对植物生长有明显的抑制作用。公共科学图书馆一号。2013;8:e63538。
- 19.
研究结果表明,荧光假单胞菌SS101通过挥发性有机化合物促进植物生长。生物化学与生物物理通讯,2015,在出版社:1-5。
- 20
Ryu C,Farag Ma,Hu C,Reddy Ms,Kloepper JW,Pare PW。细菌挥发物在拟南芥中诱导全身性抗性。植物理性。2004; 134(3月):1017-26。
- 21
Cho Sm,kang br,han sh,安德森Aj,Park J,Lee Y等。2R,3R-丁二醇,由假单胞菌氯吡咯o6产生的细菌挥发性,参与拟计拟南芥干旱的全身耐受性。Mol植物微生物相互作用。2008; 21:1067-75。
- 22
张辉,孙勇,谢欣,Kim M-S, Dowd SE, Paré PW。一种土壤细菌通过缺铁诱导机制调节植物获得铁。植物j . 2009; 58:568 - 77。
- 23
Farag M,张H,Ryu C-M。通过空气传递植物和细菌之间的动态化学通信:细菌挥发物诱导抗性。J Chem Ecol。2013; 39:1007-18。
- 24
Vacheron J、Desbroses G、Bouffaud M-L、Touraine B、Moënne Loccoz Y、Muller D等。植物生长促进根际细菌和根系功能。前植物科学。2013;4(9月):356。
- 25
Kwon YS,Ryu C-M,Lee S,Park HB,Han KS,Lee JH,等。拟南芥幼苗暴露于细菌挥发物的蛋白质组分析。足底。2010;232:1355–70.
- 26
谢X,张H,ParéPW。拟南芥的持续增长促进,长期暴露于有益土壤菌枯草芽孢杆菌(GB03)。植物信号表现。2009; 4:948-53。
- 27
Ryu C, Farag MA, Paré PW, Kloepper JW。来自地下的隐形信号:细菌挥发物诱导植物生长促进和诱导系统抗性。植物病理学杂志2005;21:7-12。
- 28
比较苯并噻二唑、(2R,3R)丁二醇和异石蜡混合物对本氏烟炭疽的诱导抗性。植物病理学研究。2010;59:643-53。
- 29.
Cortes Barco A,Hsiang T,Goodwin PH.用(2R,3R)-丁二醇或异烷烃混合物诱导匍匐茎农杆菌对三种叶面病害的系统抗性。安应用生物学。2010;157:179–89.
- 30.
D'Alessandro M、Erb M、Ton J、Brandenburg A、Karlen D、Zopfi J等。土传内生细菌产生的挥发物增加了植物对病原菌的抗性,并影响了三营养相互作用。植物细胞环境。2014;37:813–26.
- 31.
Kai M,Crespo E,Cristescu Sm,Harren FJM,Francke W,Piechulla B. Serratia Odorifera:挥发性化合物对拟南芥挥发性的发射和生物学影响分析。苹果microbiol biotechnol。2010; 88:965-76。
- 32.
阿斯特罗姆B,格哈德森B。小麦品种对有害根际细菌的反应。种植土壤。1989;117:157–65.
- 33.
Hochshedinger F,Park WJ,Sauer M,Woll K.从杂草到作物:谷物根系发育的遗传分析。趋势植物SCI。2004; 9:42-8。
- 34.
Ditengou FA、Müller A、Rosenkranz M、Felten J、Lasok H、van Doorn MM等。外生菌根真菌倍半萜的挥发性信号重新编程根结构。自然公社。2015;6:6279.
- 35。
Opanowicz M, Vain P, Draper J, Parker D, Doonan JH。二穗草:用野草做干草。植物科学学报,2008;
- 36。
Mochida K,Shinozaki K.解锁Triticeae基因组学可持续地养活未来。植物细胞生理。2013; 54:1931-50。
- 37。
caralan P, Chalhoub B, Chochois V, Garvin DF, Hasterok R, Manzaneda AJ等。短柄草基因组学和基础生物学研究进展。国际短领奖台倡议(IBI)。植物生态学报,2014;
- 38。
Girin T, David LC, Chardin C, Sibout R, Krapp A, Ferrario-Mery S等。短穗木:模式种和谷物之间有希望的枢纽。实验机器人。2014;65:5683-96。
- 39。
瓦特M,Schneebeli K,Dong P,Wilson Iw。颅卷曲的枝条和根系生长及其作为小麦和其他谷物作物模型的潜力。Funct植物Biol。2009; 36:960。
- 40。
Hong S-Y、Park J-H、Cho S-H、Yang M-S、Park C-M。短足亚种物候生长阶段的编码和描述。杂草研究,2011年;51:612–20.
- 41。
Schwachtje J, Karojet S, Kunz S, Brouwer S, van Dongen J。不同生态型拟南芥根际细菌对植物生长的促进作用不同。植物信号行为研究,2012;
- 42
关键词:番茄根核侵染菌,病原菌,挥发性物质,番茄根核侵染菌拱Microbiol。2007;187:351-60。
- 43
Bashan Y、de Bashan LE、Prabhu SR、Hernandez J-P。植物生长促进菌剂技术进展:配方和实用前景(1998-2013)。种植土壤。2013;378:1–33.
- 44
阿赫玛德M,基布雷特M。植物促根细菌的促生机理及应用研究现状。金沙特大学理学杂志。2014;26:1–20.
- 45
Tocheva EI, Dekas AE, McGlynn SE, Morris D, Orphan VJ, Jensen GJ。在革兰氏阴性菌长丙酮杆菌产孢过程中,聚磷酸盐的储存。J Bacteriol。2013;195(6):3940 - 6。
- 46
细菌进化背景。微生物学回顾。1987;51:221–71.
- 47
陈建平。真核生物与古细菌的进化关系。中国生物医学工程学报。微生物学报1998;62:1435-91。
- 48
根际细菌挥发物促进植物生长——CO2效应?2月。2009;583:3473-7。
- 49
Orman-Ligeza B,Parizot B,Gantet PP,Beeckman T,Bennett MJ,Draye X.谷物中的胚胎根系组织组织:从模型植物中分支。趋势植物SCI。2013; 18:459-67。
- 50.
Pérez-Montaño F, Alías-Villegas C, Bellogín RA, del Cerro P, Espuny MR, Jiménez-Guerrero I等。谷类和豆科农业重要植物的植物生长促进:从微生物能力到作物生产。Microbiol杂志2013;169:325-36。
- 51.
植物根系结构:拟南芥和谷类作物的研究。中国生物医学工程学报,2012;
- 52.
Meister R、Rajani MS、Ruzicka D、Schachtman DP。农业作物根系性状改良的挑战。植物科学趋势。2014;19:779–88.
- 53.
林基jp。陡峭,廉价和深:一种玉米根系系统优化水和N采集的意识式。Ann Bot。2013; 112:347-57。
- 54.
Pacheco-Villalobos D,Hardtke CS。从拟南芥到颅骨的根系结构自然遗传变化:朝向自适应价值。Philos Trans R SoC Lond B Biol Sci。2012; 367:1552-8。
- 55.
田X,多纳P。根资源觅食:有关系吗?前植物科学。2013;4(八月):303。
- 56.
Piechulla B,Degenhardt J。微生物挥发性有机化合物的重要性。植物细胞环境。2014;37:811–2.
- 57.
Heuskin S、Verheggen FJ、Haubruge E、Wathelet J。信息化学缓释装置在害虫综合治理策略中的应用。生物技术农业社会环境。2011;15:459–70.
- 58.
Vain P, Worland B, Thole V, McKenzie N, Alves SC, Opanowicz M,等。农杆菌介导二穗短柄草(Bd21) T-DNA插入突变的研究植物生物技术2008;6:36 - 45。
- 59。
Alvès S, Worland B, Thole V, Snape J, Bevan M, Vain P. A农杆菌介导的二穗短柄草群落标准线Bd21的转化方法。Nat Protoc。2009;4:638-49。
- 60
Armengaud P, Zambaux K, Hills A, Sulpice R, Pattison RJ, Blatt MR等。EZ-Rhizo:快速准确测量根系结构的集成软件。植物j . 2009; 57:945-56。
- 61
R:统计计算的语言和环境。统计计算基础,维也纳,奥地利。统一资源定位地址http://www.r-project.org/[http://www.r-project.org/]
- 62。
关键词:多元探索性数据分析,数据挖掘,数据挖掘http://cran.r-project.org/package=factominer.. 2013
- 63。
Kennedy IR,Choudhury ATMA,Kecskès ML.作物耕作系统中的非共生细菌重氮营养体:它们促进植物生长的潜力能否得到更好的利用?土壤生物化学。2004;36:1229–44.
- 64。
德弗雷塔斯JR,格米达JJ。研究冬小麦根际细菌相互作用的根组织培养体系。应用微生物生物技术。1990;33:589–95.
- 65。
张H,Kim M-S,Krishnamachari V,Payton P,Sun Y,Grimson M等。根瘤菌挥发性排放调节拟南芥的生长稳态和细胞扩张。Planta。2007; 226:839-51。
- 66
张H,谢X,Kim M-S,Kornyeyev Da,Holaday S,ParéPW。土壤细菌通过降低植物葡萄糖感应和脱落酸水平来增强拟南芥光合作用。植物J. 2008; 56:264-73。
- 67
Zhang H、基姆、S、Y、Dowd SE、Shi H、帕尔普。土壤细菌通过对钠转运蛋白HKT1的组织特异性调控,赋予植物耐盐性。植物与微生物相互作用。2008;21:737–44.
- 68
Walley FL,Germida JJ。春小麦(Triticum aestivum)对伪霉素物种和灵芝NT 4的相互作用的反应。1997年; 24:365-71。
致谢
作者感谢PaulParé(德克萨斯科技大学,Lubbock,TX,USA),理查德SIBOUT(Institut National de La Recherche Agrormique,凡尔赛,法国)和Micheline Vandenbol和Marc Ongena(Gembloux Agro-Bio Tech,Gembloux,Belgium)为他们富有成效的讨论。作者还感谢Adeline Blondiaux,以便在建立方面的优秀技术援助体外共栽培系统和生产分析数据集。我们也感谢Gerry Cambier编辑这篇文章的英文作文。这项工作得到了比利时科学研究基金会(FRFC项目2.4.591.10)的财政支持。F和博士后资助CTP 1808458)。Delory B.M.(研究员)是由比利时国家科学研究基金(frrs - fnrs)资助的。
作者信息
从属关系
相应的作者
附加信息
利益争夺
作者们宣称他们没有相互竞争的利益。
作者的贡献
构思和设计实验:Pd,SV。进行实验:CB,MM,PD,SV。分析数据:BD,CB,MM,PD,YB。供助试剂/材料/细菌菌株/分析工具:BD,SS,PDJ,YB。写了论文:PD。修订了论文:BD,CB,MM,PDJ,SS,SV,YB。所有作者阅读并认可的终稿。
附加文件
附加文件1:图S1。
不同菌株挥发物对次生根总长度(A)、不定根总长度(B)和次生根密度(C)的影响。菌株根据前面定义的聚类(基于PC)进行分组。在每个聚类中,菌株按平均值升序排列。给出的数值是四个实验重复(64或128个生物重复)的平均值+/− 置信区间(α= 5%))。与无细菌对照相比,显著变化用星号(*)标记。多克斯(374 kb)
权利和权限
开放访问本文根据知识共享署名4.0国际许可的条款分发(http://creativecommons.org/licenses/by/4.0/),允许在任何介质中不受限制地使用、分发和复制,前提是您给予原始作者和来源适当的信任,提供到知识共享许可证的链接,并说明是否进行了更改。知识共享公共领域放弃(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条提供的数据,除非另有说明。
关于这篇文章
引用这篇文章
Delaplace, P, Delory, b.m., Baudson, C。等。根际细菌挥发物对模式草根系构型及生物量产生与分配的影响短足(L.)P。博夫。。BMC植物BIOL.15,195(2015)。https://doi.org/10.1186/s12870-015-0585-3
收到了:
认可的:
发表:
关键词
- 生物质生产
- 不定根
- 总根长
- 短小芽孢杆菌
- 根系统架构