抽象的
背景
拟南芥根生长受到刺激piriformospora indica.磷酸限制和WRKY6转录因子的失活。这些因素的组合导致了根和地上部生长、根系结构和根系基因表达谱的意外改变。
结果
结果表明了这一点P印度在PI限制下促进磷酸盐摄取和根部发育wrky6公司变种人。这与刺激磷酸盐1表达和乙烯生产。从根源的表达概况wrky6公司幼苗发现参与激素代谢,运输,分生,细胞和塑性增殖的基因,以及生长调控。在这些根部也上调了25 miRNA。我们在此生成并讨论了在生长根中调节的常见基因列表,这对于本研究中研究的所有三种生长刺激是常见的。
结论
自根的发育wrky6公司植物暴露于P印度在磷酸盐限制下,强烈促进,我们提出响应所有三种生长刺激的常见基因是控制根生长和建筑的核心。可以测试它们以优化模型和农业植物的根生长。
背景
磷是植物生长发育所必需的大量营养元素,占植物干物质的0.2%。P参与生物体内许多关键代谢途径的调节,包括能量生成、核酸和膜合成、蛋白质磷酸化和氧化还原反应[1-3.]. 植物以无机磷的形式从土壤中吸收磷。由于低可用性和低流动性[4.那5.]土壤溶液中PI的浓度通常为约10μm,低于作物和植物最佳性能所需的临界水平[6.].据估计,〜5.7亿公顷的土地缺乏通过施用肥料来减轻的p。PI施肥会导致生态问题,如富营养化或有毒藻类盛开[7.]. 土壤中的可溶性Pi也与钙、镁、铝或铁等阳离子形成复合物,这些阳离子不易被植物吸收。尽管促进植物生长的根际细菌和真菌[例如丛枝菌根(AM)真菌]促进了植物根系对Pi的吸收,但微生物和杂草也会与植物竞争Pi,或将其转化为无法支持植物生长的有机形式[8.那9.].
为了应对PI限制,植物已经进化了复杂的适应性反应,包括形态学和生理修饰,以改善PI采集或重新繁殖通过各种Pi转运蛋白基因的差异表达[10那11].根系结构的重塑,抑制原药长度,根发密度和长度的增加,以及与AM或AM样真菌的关联是对低PI的典型发育反应[2那12].AM共生在增强土壤中获得磷的作用是众所周知的[13].
piriformospora indica.,一种肌菌皮菌,可增强单焦点和奇特的生长[14-16].真菌改善了土壤中的营养吸收到主体根部[17那18]还包括PI转移通过真菌菌丝通过高亲和力pi转运蛋白pipt定位于外部菌丝[19]. PiPT与酿酒酵母高亲和力PI转运蛋白PHO84和植物PI转运蛋白(CF. [20])。除了刺激pi新陈代谢外,P印度还增强了硝酸硝酸还原酶基因的表达和拟南芥根系中的淀粉降解酶葡聚糖 - 水直立通酶[17]表明真菌对植物初级代谢有很强的影响。在多大程度上,这是植物与植物共生互动的好处所在P印度还不清楚。除了增加植物的生物量[21-23]增强了生物和非生物胁迫的抗性[24那25],诱导系统性和局部阻力[26那27]和刺激次生代谢物积累[28]已经有报道了。这就需要一种高度平衡的共生关系,在这种共生关系中,植物似乎控制着根系的定殖程度[29那30].
WRKYs是植物信号网络中重要的转录因子,调控植物对生物和非生物刺激的多种响应,但这些转录因子也参与协调发育过程的内部信号响应。它们与DNA和非DNA结合蛋白质相互作用[31]根据其相互作用伙伴和靶基因,用作基因表达的激活剂和阻遏物的作用[32那33].WRKY6、WRKY42和WRKY75在Pi剥夺过程中被诱导[34-36]. Chen等人[34]表明WRKY6通过调控调控参与了对低pi胁迫的响应磷酸盐1(磷化氢) 表达。低Pi处理降低了WRKY6与细胞的结合磷化氢启动子,这表明磷化氢WRKY6的调节是PI依赖性的,低PI水平可防止抑制磷化氢表达。植物特异性Wrky75是编码磷酸酶的几种PI饥饿诱导基因的活化剂,MT4 / TPS1样蛋白或高亲和力PI转运蛋白[36].抑制WRKY75通过RNAI沉默的表达诱导应力响应,例如花青素积累[35].
我们注意到了wrky6公司在存在的情况下暴露于PI限制的幼苗和植物P印度与WT控制相比。P印度WRKY6还能促进植物对磷的吸收和转运,而这些过程受到WRKY6的限制。对根的发育有很强的促进作用wrky6公司植物暴露于P印度在Pi限制条件下,我们进行了比较表达谱的研究,以确定基因、蛋白质以及代谢和信号通路,从而优化根系发育,特别是在Pi限制条件下。
结果
wt和wt的根表型wrky6公司不同PI浓度下的幼苗
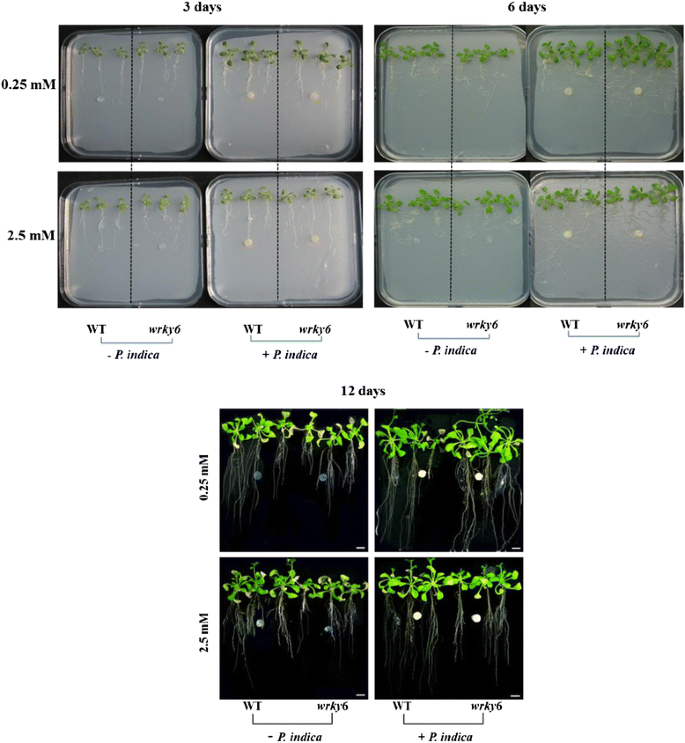
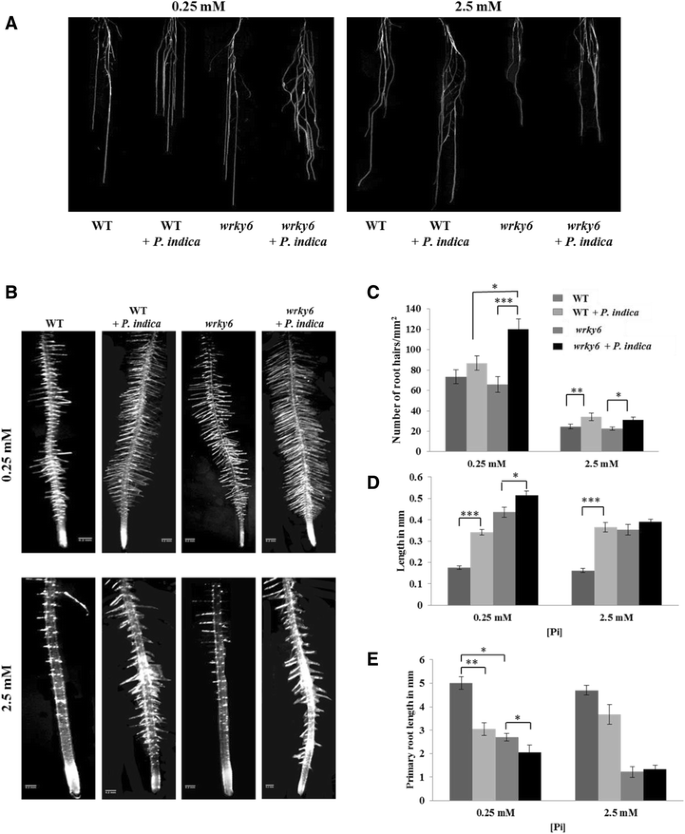
WT和wrky6公司幼苗(图。1)和/没有P印度在含有2.5或0.25 mM Pi的垂直PNM板上放置3、6和12天。真菌对幼苗生长的促进作用在培养3天后开始显现,并且随着培养基中Pi浓度的降低而增强。特别是野生型和野生型的根系生长wrky6公司随着Pi浓度的降低,幼苗得到促进,并进一步受到真菌的刺激(图。1和2).仔细检查显示,在存在的情况下,根部是更密集和灌木丛P印度因为两个侧根的数量和长度(图。1和2a级)以及根毛(图。2b级-D.)增加了。此外,刺激根系生长P印度在WT的WT下,PI限制受到WRKY6的限制。这对于在0.25mm Pi上生长的幼苗特别突出(图。1和2):生长刺激效果P印度更强的是wrky6公司根比WT根(图。2b级-D.). 最后,与AM定殖后根系发育的文献一致[2],WT的主要根长度和wrky6公司在Pi限制条件下,幼苗较短(图。2个). 这些结果表明WRKY6对根结构有很强的影响,并且wrky6公司两种植物的反应均优于WT植物P印度和pi限制。
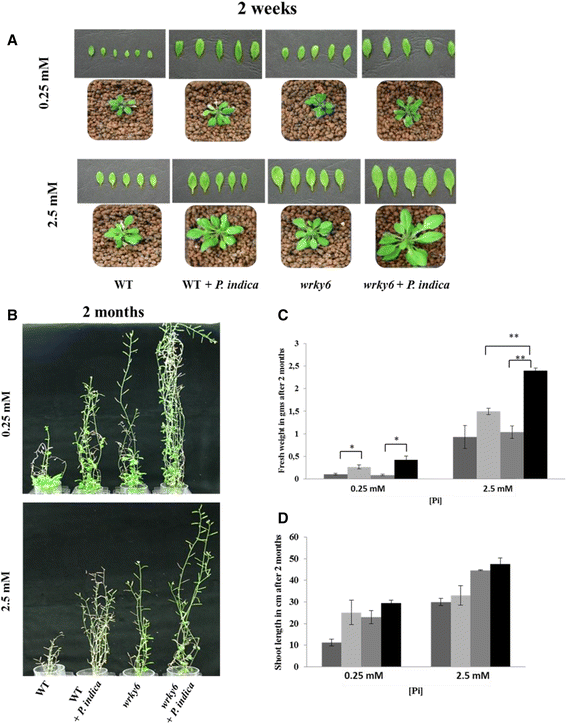
在扩展粘土中的共生长期相互作用后,表型差异变得更加明显。在培养皿中的14天培养后,P印度-殖民或模拟处理WT和wrky6公司在NP(2.5mm,正常Pi)或LP(0.25mm,低Pi)培养基上生长的幼苗转移到膨胀粘土中。2周后,在叶片的大小、形状和面积上首次观察到差异(图。3a级).P印度- 批评wrky6公司与垂直琼脂平板上的幼苗相比,幼苗在两种Pi浓度下较大。虽然所有植物在LP条件下呈现了PI胁迫症状2个月,但是wrky6公司系比WT表现得更好,而且在存在P印度. 特别是2个月后,鲜重显著增加(图。3b级那C)和拍摄长度(图。三维)被观察到P印度-Treated.wrky6公司与未经处理的对照和WT相比,WRKY6对幼苗(在NP培养基上生长)具有限制作用P印度介导促进增长。
低pi增强P印度WT幼苗的殖民化
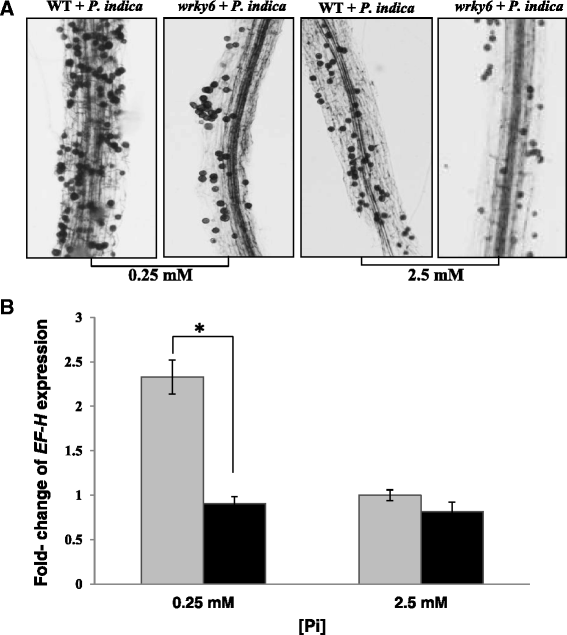
为了评价Pi对拟南芥根系定殖的影响,用台盼蓝对拟南芥根系相关真菌孢子进行染色。图。4a级结果表明,在LP条件下,与WT根相关的孢子数高于NP条件下的孢子数wrky6公司幼苗。殖民地P印度并用定量RT-PCR方法证实P印度- 特异性标记基因ef-h.,相对于植物GAPDH基因(图。4b级).这些结果突出了在LP条件下生长的WT幼苗根系定子的强烈效果(CF.讨论).
P印度刺激LP-生长的乙烯(ET)生产wrky6公司幼苗
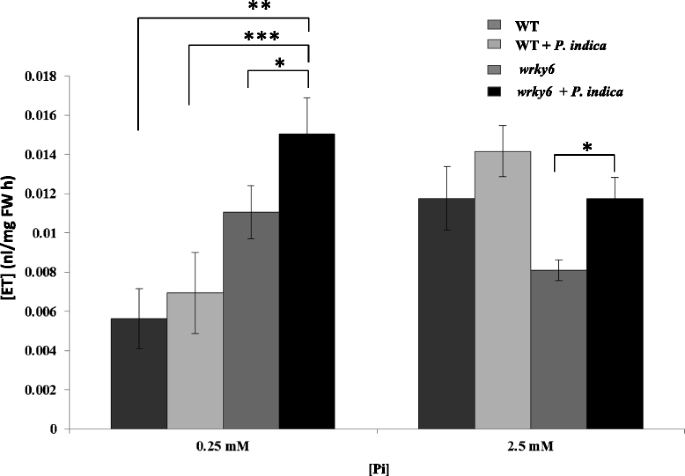
ET在Pi胁迫下幼苗初生根生长和根毛形成中起重要作用[37]对菌丝生长、分枝和根系定殖有很大影响[38]. 如图。5.对野生型幼苗释放的ET进行了研究 > LP条件下比NP条件下低2倍。未克隆ET的生产wrky6公司两种磷浓度下的幼苗具有可比性。在所有情况下,P印度刺激内皮素的产生,但显著的刺激只观察到wrky6公司幼苗。LP-,但不是NP生长的突变幼苗而不是重量〜2倍,而不管幼苗是否暴露于真菌。更高的ET生产wrky6公司与野生型相比,LP条件下的幼苗可能有助于改变突变体的根系结构和较低的根系定殖(37–38,cf。讨论).
P印度促进磷酸盐1(磷化氢)Pi限制下的表达式
PHO1是主要在根中表达的高亲和力PI转运蛋白,并且基因在低PI条件下上调[39].我们观察到~3.8倍的刺激磷化氢表达者P印度在wrky6公司根在Pi限制下,但不是在NP条件下(图。6.).这证实了以前的观察,即Wrky6充当阻遏物磷化氢在NP条件下表达。强烈的效果P印度在根本发展中,由上调反映磷化氢在π的限制。
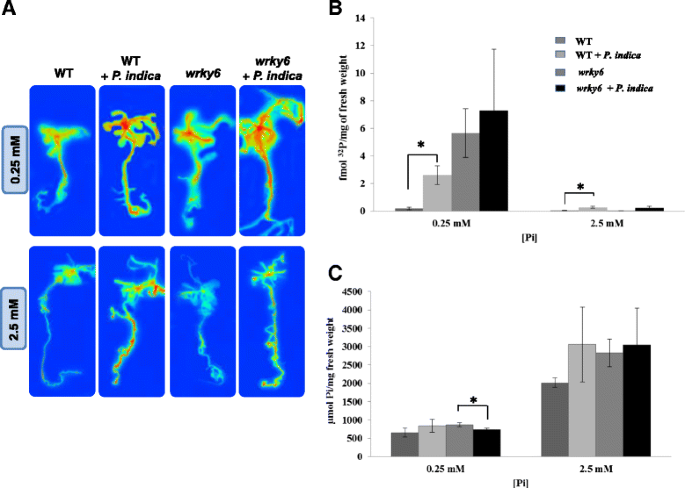
32磷吸收与无机磷含量
数字7个表明所有部分中的放射性P印度- 无论是否在NP或LP条件下都会繁殖,散装幼苗高于非殖民植物,我们观察到〜2倍的刺激32野生型和野生型真菌对磷的吸收wrky6公司幼苗(图。第7b条).PI吸收的可比刺激P印度在两种基因型中均显示出较强的真菌诱导的生长变化wrky6公司突变体不是由更有效的PI吸收引起的。此外,幼苗中PI的总量不能解释真菌诱导的表型差异wrky6公司和WT(无花果。7摄氏度). 正如预期的那样,幼苗中的总Pi含量取决于培养基中的Pi浓度,并且在LP条件下生长的幼苗比在NP条件下生长的幼苗含有更少的Pi。然而,对于培养基中给定的Pi浓度,我们没有观察到两种基因型幼苗中总Pi含量的显著差异,也没有观察到真菌的存在或不存在(图。7摄氏度).因此,定殖和非定殖野生型中Pi的可比性wrky6公司幼苗无法解释在LP条件下种植的幼苗中观察到的根系结构的差异(CF.讨论).
PI-稳压基因P印度- 批评wrky6公司根
当NP-生长时,观察到对根生长的最强刺激P印度- 批评wrky6公司与LP (Figs。1和2).因此,我们首先确定了受P印度只有在wrky6公司根(不在WT中)并且仅在Pi限制下(附加文件1:表S1)。Mapman分类显示9个生长素相关基因编码小生长素up rna(SAURs)。其他编码生长素外排调节因子、生长素反应因子(如ARF12)、生长素调节TFs(如叶子叶2)或生长素靶点(如扩张素、细胞壁生物合成酶)。下调IAA34型,编码ARFs的阻遏子[40那41]进一步支持生长素代谢被激活。两个基因([九-CIS-环氧碳酸二恶英酶4[42] 和HVA22[43])参与ABA功能。赤霉素(GA)生物合成的关键是GA需求1、GA 20-氧化酶3和GA 2-氧化酶7[44那45].
许多转运过程受到刺激,如p-和v-atp酶、碳水化合物、氨基酸、脂质、核苷酸、Pi、硝酸盐和金属转运蛋白、ABC和代谢物转运蛋白以及水通道蛋白的基因调控。
根系结构的重新组织也反映了初级(例如葡萄糖)和次级(例如胁迫)代谢,发育过程,细胞组织,细胞周期,囊泡转运,生长调节剂和早期信号化合物的基因的刺激。后一组是化合物(如CA.2+- 嵌入钙调蛋白样37和受体激酶)尚未在根中分析。这突出了很多人P印度- WT3中的对LP应激的反应受到WRKY6的限制。
有趣的是,在较大的根中有25个miRNAs被调控,其中10个是已知的,15个是未知的。miR156G那miR169F公司那miR395B和mir399c.回应PI饥饿[46那47].miR394B针对SKP1-CULLIN / CDC53-F盒式综合体的F箱蛋白的mRNA,并参与疾病响应[48].miR169F公司以NF-Y TF复合物的A亚基mRNA为靶点,从而控制初生根和侧根的起始[49]. 此外,烯基羟烷基产品2参与硫代葡萄糖苷的生物合成并被预测为米尔826和miR5090两种mirna都是在Pi饥饿时诱导表达的[50].所有这些miRNA都受到监管P印度在LP-exposedwrky6公司,但不是wt根。这突出了TF在PI限制下对根部开发的限制的重要性。
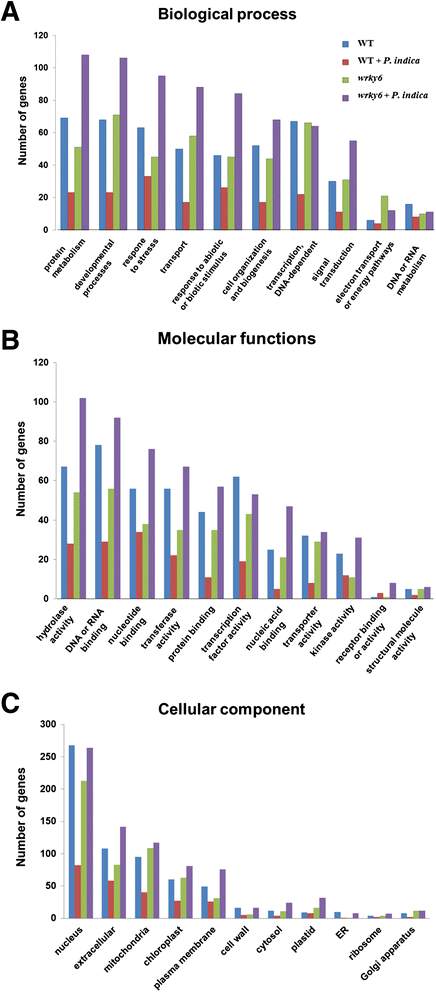
基因的功能分类基于A)参与“生物过程”,b)参与“分子功能”,c)参与“细胞成分”,并根据A对LP的反应调节超过2倍。拟南芥基因本体(TAIR's GO注释)如(图。8.).
提出的综合基因列表涉及根生长促进
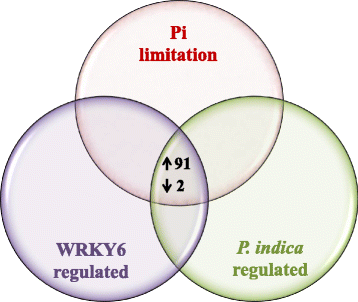
维恩图(图。9.)由Mapman软件鉴定的基因产生,其由LP调节(但不是P印度或wrky6),通过P印度(但不是lp或wrky6),以及wrky6(但不是P印度或lp)。这三种数据集中的常见基因对三种刺激之一没有特异性,因此应该代表更多涉及促进根生长和发育的一般基因(图。9.). 然后根据所有数据集中的平均折叠调节排列这些基因(表1)1,4倍;附加文件2:表S2)。基因在列表中排名越高,似乎越重要似乎是他们在根生长期间的要求。
91个基因的调节超过4倍2 > 2) in all 3 datasets and only 2 of them are down-regulated (Table1).对于其中28次,我们找不到足够的信息来预测其产品的功能。此外,对于59个基因产品,我们没有找到功能分析数据或根系预测。
根系生长似乎与缺水(At1g26850)和对糖的高需求(At5g62850)有关。SWEET5似乎在提供光同化物方面起主要作用通过韧皮对根部和真菌,因为它的信息是甜蔗糖流出转运蛋白基因的唯一一个[51]在列表中。生长素/细胞素素比对于根/芽比对于根本来说很重要。涉及蟾蜍素和细胞素新代谢的3个基因在列表中:参与细胞膨胀的Saur2,一种生长素诱导的无表特征幼亮的重复蛋白(AT1G24650)[52]预测的TF At5g27140通过组氨酸-天冬氨酸光解回路对细胞分裂素产生反应[53].有趣的是,其他与激素相关的基因在普通基因中排名并不高。
在已知参与细胞壁延伸的蛋白质中,如木葡聚糖内转糖酶水解酶、扩张酶、聚半乳糖醛酸酶或过氧化物酶,未确定特征的果胶甲基酯酶At1g69940和At1g11590似乎是重要的。细胞生长需要胞排作用的增加,这反映在高排名SNF7.名单上有吉恩。SNF7参与了血管前腔室内囊泡的形成[54]. 基因家族的特定成员(如外囊70家族的At1g07725)参与刺激生长细胞的输出。对脂质需求的增加反映在参与脂质代谢的基因上(At4g33355;At1g21540)。控制氧化还原电位(At3g45880,At2g33270)和特定质体功能,如导入细胞器(At5g07930),似乎很重要。对发育变化的快速反应与PUMILIO蛋白(At5g56510)介导的转录后过程有关[55].仔细检查基因调节> 4折使用TAIR和NCBI数据库显示,额外的蛋白质可能与根或细胞生长有可能与细胞生长相关,但这需要进一步研究。此外,通过将阈值水平降低到所有三个条件中的阈值水平至2倍的调节(附加文件)来扩展基因列表(附加文件2:表S2,2倍)未覆盖额外的〜100蛋白,具有预测的生长相关功能(TAIR主页),如生殖分泌物1,生长调节因子4,扩展蛋白23,RMIC样柴蛋白AT1G03890,组蛋白乙酰化酶18,CA2+-依赖性蛋白激酶14、LIFEGUARD1和SYNAPTOTAGMIN2等等。最后,还需要分析HVA22J样蛋白强下调的功能。
综上所述,本研究中分析的三种根生长刺激因子对大多数基因的反应信息非常有限。
讨论
低PI是植物的主要压力。因此,植物具有进化的复杂机制,用于获取,重新动员和再循环PI以维持细胞中的P宿剑。时空分子,生理和生物化学PI缺乏响应是局部和系统性传感的结果和信号传导途径的激活。它们刺激PI代谢,还会启动发展重新编程,导致根系结构的变化[56]. 在拟南芥的74个WRKY成员中,WRKY6,−42和−75个与LP应力有关[34那35]. 在这里进行的研究中,我们观察到当WRKY6基因灭活。因此,在更多细节中研究了这种衣物蛋白质。此外,P印度帮助植物适应各种胁迫条件,并提供包括促进根系生长的Pi在内的营养物质[14那16]. 有趣的是,Müller等人[57]对缺Pi的拟南芥叶片进行微阵列分析。他们的73个基因也在我们的基因芯片与野生型根调控。当幼苗在空气中生长时,数量减少到37个P印度(比较Müller等。[57])。这证实了真菌降低了拟南芥根系的PI应激反应。在这里,我们证明了三个无关的因素“存在P印度“Pi限制”和“WRKY6缺失”强烈影响植物生长,尤其是根系结构。WRKY6限制了真菌的刺激作用和Pi限制。在NP条件下,响应的差异P印度在两个基因型中小于LP条件下(图。1和2). 这些效应不仅在幼苗水平上可见,而且在将幼苗移入膨胀粘土后仍然存在(图。3.). 根毛密度和根毛长度的增加是由于P印度在里面wrky6突变体与LP条件下的WT相比(图。2b级-D.)而初生根的长度减少(图。2个). Chen等人[34]还观察到WT和WT之间的表型差异wrky6公司LP条件下的植物,但没有详细分析根系结构。Robatzek和Somssich [58]没有观察到之间的差异wrky6公司而WT,但它们的成长条件与我们的成长条件和陈等人的成长条件不同。[34].在殖民化之后发生响应LP的根系结构中的类似改变[59-61),在P印度-大白菜定植苗[16那62那63].大白菜表现出较强的反应P印度比拟南芥。相互作用导致浓密的根表型,与我们的观察结果相当wrky6个幼苗(图。2).
PHO1参与了Pi从根表皮和皮层细胞向木质部的转移[39]. 这可以解释为什么飞机的空中部分性能更好P印度- Pi限制下的定植突变体。低Pi处理降低了WRKY6与细胞的结合磷化氢启动子(34]. 此外,在一种CT.ivation ofWRKY6刺激磷化氢表达者P印度在LP条件下,而不是NP条件下(图。6.).这表明存在一种独立于wrky6的调控机制来刺激磷化氢LP下的信号表达P印度.菌根共生还增强了各种PI转运蛋白基因的表达OSPT11在水稻[64] 和MTPT4.在Medicago trunculata.[65].P印度也刺激其他Pi转运体基因的表达,包括Pht1;5.在LP中生长wrky6公司幼苗。这个Pht1;5.促销员包含W盒[34那35]这是腕表TFS的推定结合位点。自从Pht1;5.在这些条件下,WRKY6在野生型幼苗中没有上调,因此WRKY6可能作为该基因的转录抑制子发挥作用(数据未显示)。此外,与以往的观察结果一致[18那19那66]我们发现存在的PI吸收增加P印度在低PI条件下,WT和WT之间没有区别wrky6公司幼苗(图。7.).刺激pi的吸收P印度可能会建立当地PI梯度,可能导致局部PI应力反应改变,以及根系发展计划的重新编程。这些计划由PI限制启动并进一步促进P印度以及缺少WRKY6。菌根真菌联合是一个众所周知的策略,提高植物吸收磷[61那67].尽管存在更有效的PI吸收P印度定殖或未定殖野生型和wrky6公司虽然在Pi限制条件下生长的幼苗比在NP条件下生长的幼苗含有更少的Pi,但幼苗没有什么不同(图。7.).这再次符合PI可用性在根系结构中诱导增长和改变的局限性的想法一致。P印度要么降低Pi限制,要么干扰激活Pi应激反应的信号事件。在Pi限制下生长的植物利用自身的Pi库来维持细胞内的Pi稳态[68]同时刺激Pi摄取机制[69那70].在根生长期间在mRNA水平上上调的RMIC样杯蛋白(附加档案1:表S1,附加文件2:已经提出了表S2)具有营养储层活性,并且是用于控制PI可用性的候选者。
在LP条件下,ET是抑制初生根生长和促进侧根伸长的重要因子[2那37].植物衍生的ET还刺激孢子萌发和杂质菌的菌丝生长[38那71]. 如图。5.,定殖和非定殖突变幼苗产生的ET是WT幼苗的2倍。由于ET产量较少的WT植物比wrky6公司无论根环境中的Pi水平如何(图。4.), ET可限制根系定植。因此,这种激素可能对平衡微生物的生长、由此对宿主的益处以及宿主防御基因激活的程度具有重要意义。在我们的生长条件下,较高的ET水平wrky6公司植物可刺激侧根发育、孢子萌发和菌丝生长,这与较好的性能是一致的wrky6公司根。Khatabi和Schäfer也证明了ET和ET信号成分在皮脂目与不同植物物种的互惠互动中的重要作用[30],Mavehl等人。[72和Barazani等人[23].一起携带WRKY6是控制根系发展的重要球员P印度和pi限制。
微阵列分析
由于观察到最强的增长促进效果和根系形态的变化P印度- 批评wrky6公司在LP中,我们使用这些幼苗的根来识别导致这种表型的基因(图。2). 许多具有已知生长相关功能的基因被鉴定出来(附加文件1:表S1,附加文件2:表S2)。这包括参与初级代谢(例如生成富含能量的成分)、细胞壁代谢(例如甲基果胶酶、扩张蛋白)、激素生物合成和信号传导(涉及生长素-、赤霉素-、ET-、茉莉酸-、油菜素内酯和独角醇内酯相关过程的蛋白质)的基因,或者是次级代谢(例如压力或防御化合物或抗氧化剂)。
在这些根中,发育过程的各种特征良好的基因被特异性地上调,如生长调节剂4 (At3g52910)基因,用于细胞调控、离子、多肽、寡核苷酸或其他小分子的转运。之前描述的蛋白质参与P印度/拟南芥相互作用被检测到:例如参与蛋白质分选的成分(cf. [73])细胞骨架重排(cf[21])和含数学域的蛋白质[74]. 然而,大多数基因在根中还没有或很少被鉴定或研究。
WRKY6限制了WT(CF)中的生长素介导的生长反应75])。在鉴定的基因中是有助于细胞膨胀和胸腺炎毒素运输的Saur21 [76]. 索尔,−6.−7.−17, −27, −49, −64和−65参与根系发育的各个方面(TAIR主页)。生长素反应因子(ARF)12在水稻Pi稳态中的作用[77]并且通过在拟南芥中保持毒素运输机械的正确极化来对根本生长至关重要[78]. expansin10、B1、B3和A5参与细胞扩张和根表皮细胞分化[79那80]. 只有四个与细胞壁生物合成有关的酶基因在这个列表中:与根尖生长有关的纤维素合成酶样D4[81],纤维素合酶10和纤维素合酶样D6和-G3。杨等人。[82]证明茉莉酸通过干扰GA信号级联将防御优先于生长。与这一观点一致,我们观察到3个关键的GA生物合成酶基因的上调,而参与防御反应的基因相对较少,其中许多基因在体内甚至下调P印度- 批评wrky6公司LP中的幼苗(附加文件1:表S1)。
miRNAs在植物微生物与固氮根瘤菌共生中的作用[83],AM真菌[16那84那85]以及在生物和非生物胁迫下生长的植物[86那87是有充分证据证明的。一些arf家族的mi/ sirna靶成员参与了生长素稳态和信号传导,假设他们参与了根发育的关键阶段[88].Ye等人[16]报告P印度-介导的几种mirna的诱导,最终导致文柄兰的生长促进和旺盛的根系发育。与大量的出版物一致,似乎根发育的控制涉及具有各种功能和靶标的miRNAs (Li和Zhang [89])。理解在根生长期促进期间对新鉴定的miRNA的功能进行特别有趣。一起服用,这些基因的组合对于PI限制下的重编程根部发育至关重要,并且存在P印度在wrky6.
一般基因
所有三种相当多样化的生长刺激调节的基因应该代码根生长的常见组分。具有较高优先级的基因应表现出响应于三种刺激而不是较低的三种刺激。桌子1和附加文件2:表S2提出了具有多种功能的基因,但它们可能突出了那些需要激活以促进根系生长和发育的细胞和分子过程。有趣的是,一项文献和数据库调查发现,对于大多数基因产物来说,关于它们在根系生长调控中的作用的信息非常有限或没有。其中最强大的上调基因是研究充分的SNF7.编码转运(ESCRT)-III亚单位所需的内质体分类复合物的相互作用蛋白。它调节前房室腔内小泡的形成[54]. 另一个受强烈调控的基因是SWEET5,蔗糖韧皮部转运蛋白家族的成员[51].Sweet5在这种情况下的特定作用是未知的。此外,有趣的是指出,只有多蛋白蛋白复合物的一个特定蛋白质的特定成员或多蛋白复合物的一个特定蛋白质的基因对所有三种刺激作用。基因列表未覆盖代谢和信号通路,其限制了根生长促进。假设这些基因/基因产物的特定组合是合理的,这些基因/基因产物很重要,现在可以通过实验测试。
结论
我们的结论是三个不相关的因素P印度“Pi限制”和“WRKY6缺失”的影响A.拟南芥增长尤其是根系结构,并提出响应所有三种生长刺激的常见基因是控制根生长和建筑的核心。可以测试这些基因以优化模型和农业植物的根生长。
方法
植物和真菌的生长条件
拟南芥WT和wrky6公司种子是表面灭菌并放在含有MS的培养皿上[90.]营养培养基。在4°C下冷处理48小时后,将培养板在22°C下在连续光照(100μmol/L)下培养10天-2S.-1).P印度如前所述培养,如曲霉最小培养基[91.].
纯合子的产生wrky6公司线
salk012997(N661529;利用T-DNA左缘引物和基因特异性引物的组合,对欧洲拟南芥砧木中心株系进行了PCR鉴定WRKY6右边框引物(附加文件1:表S1)。使用两种不同的T-DNA左边界引物,LBA1(TGGTTCACGTAGTGCTGCATCG)和LBA1.3(ATTTTTGCCGATTTCGGAAC)。进行另外的PCR以使用基因特异性引物LP和RP鉴定插入的纯合幼苗(附加文件2:表S3)。
共培养实验
Co-cultivation的A.拟南芥(重量和wrky6公司)用真菌P印度是在体外尼龙膜的培养条件放在溶解的PNM介质上的顶部[91.]. 正方形培养皿被分成两等份和一等份P印度磁盘放在每个部分上,并生长10天。在48小时的冷处理和如上所述的10天的生长后,相等尺寸的幼苗用于共培养测定。对于PI应力处理,使用具有两种不同PI浓度的PNM培养基[2.5mm(正常pi-np)和0.25mm(低pi-lp)]。对于每种PI浓度,比较4种处理:WT,WT + P印度那wrky6公司和wrky6公司 + P印度.在22°C和70 - 80%的湿度条件下,16 h光照/8 h暗循环,在上述两种不同浓度的Pi下维持幼苗3、5、6、12或14天。根和芽分别收获并冷冻在液氮中以供进一步分析。只有根被用于基因表达分析。采用Kaefer培养基(KM)盘进行模拟处理。以2.5 mM NP模拟处理的幼苗为对照。
膨胀粘土的试验研究
与植物共培养后P印度或在PNM板上模拟处理14天,将幼苗转移到含有高压灭菌膨胀粘土的洋红色盒子中(每盒一株)。每周一次向幼苗提供含有两种不同Pi浓度的30ml液体PNM培养基。植物生长在温度(22°C)和湿度控制的室内,顶部有光线(80°C) ± 10μmol m-2S.-1)在短日条件下(8小时光和16小时的黑暗)。每周监测光强度。每周监测幼苗的尺寸并在摄影后量化。
定量实时PCR
如Sun等人所述,在培养3天后(dpi),从根组织中分离出RNA [92.].所有反应均由3个生物重复和3个技术重复进行。每个cDNA探针的mRNA水平与植物甘油醛-3- pi脱氢酶(GAPDH)mRNA水平,这已被证实是一个参考基因的根接种P印度([92.],以及其中的参考文献)。用Pfaffl的ΔΔCP方程计算目的基因的折叠诱导值[93.],与NP模拟处理根的靶基因mRNA水平相关,定义为1.0。本研究中使用的引物对在附加文件中给出2:表S3。
根殖民化
在14dpi的共培养后收获来自平板的根,并在RNA提取之前用蒸馏水进行强烈洗涤。P印度用引物对伸长因子1(PiEF-H)mRNA。细胞的mRNA水平PiEF-H被植物正常化GAPDHmRNA水平。光镜检查前用台盼蓝(0.05%)对菌丝和孢子进行染色[91.].
PI内容分析
如上所述,幼苗在两种不同的Pi条件下生长12dpi。地上部和根系分别取样。在样品在105℃烘箱中干燥过夜之前,测量新鲜质量。对于Pi含量分析,样品与2 ml 65%HNO混合3.并在160℃下保存一小时。将最终体积调节至10 ml,并将pH值调节至3.0–4.0。最后,将样品与抗坏血酸试剂和钼酸铵试剂(din38405)混合,用UV-160A分光光度计通过磷钼蓝反应分析Pi含量。总Pi浓度以μmol/g干重表示。实验用独立材料重复3次。
32P上压测定
WT和wrky6公司与/不与突变体共培养P印度在PNM培养基上用上述两种不同的Pi浓度培养5天。5 dpi、2.5μCi或25 nM32每株添加p -邻位磷(1株/板),再培养3天。根和芽分别收获,在na -柠檬酸缓冲液(10 mM, pH 6.0)中洗涤几次。将根和芽在70°C的烘箱中干燥,用组织增溶剂(Rotiszint®-eco plus)称重并消化。采用液体闪烁计数法(LS 6500),采用标准的全通道程序进行单同位素实验。
测定根毛密度、长度和主根长度
拟南芥幼苗在方形的培养皿上生长,垂直保持。共同种植P印度如上文所述进行了一些修改:(a)对于PNM培养基,使用Gellite代替琼脂,(b)不使用膜来增强根系的可见性。14dpi后,在体视显微镜(leicamz6)下拍摄根系图像,并用imagej1.47v(NIH)手工追踪数字图像。最后将像素转换成适当的度量等价物。为了测定初生根的长度,幼苗生长在液体培养基上P印度孢子在不同Pi条件下培养14d,台盼蓝染色5min后置于玻片上。幼苗的照片用600 dpi的台式扫描仪扫描。利用imagej1.47v(NIH)对扫描图像进行进一步分析。
微阵列分析
来自殖民化WT的根部的RNA和wrky6公司在3DPI下收获来自NP和LP条件下的3个独立生物实验的突变体。来自嘲弄治疗的wt的根源的RNA和wrky6公司突变体作为对照。根据安吉伦公司的单色微阵列基因表达分析(OAK Lab GmBH, Hennigdorf, Germany),对于每个处理,从三个独立的生物复制中提取相同数量的RNA进行标记和杂交。使用Nanodrop 2000分光光度计(Thermo Scientific)检测RNA样品的质量,然后在琼脂糖凝胶(2%)上进行分析,并使用2100生物分析仪(Agilent Technologies, CA)确定RNA完整性和排除潜在污染物。在验证RNA质量后,使用低输入快速Amp标记试剂盒(Agilent Technologies)生成荧光互补RNA (cRNA)。根据制造商的协议,使用花菁3-CTP (Cye-3)标记的oligo-dT引物扩增默认的crna。cye -3标记探针与8 × 60 k定制安捷伦微阵列芯片杂交。使用基因表达杂交试剂盒(Agilent Technologies)进行杂交。杂交玻片分别用SureScan微阵列扫描仪(Agilent Technologies)在3 μm分辨率下进行清洗和扫描,生成20位TIFF文件。
微阵列数据分析
使用安捷伦的特征提取软件版本11从图像中提取数据。使用安捷伦的DirectArray版本2.1软件分析提取的特征数据。根据Bolstad等人的研究,数据的标准化是通过DirectArray使用排名的中位数进行的[94.].识别显着差分表达的基因日志2- 计算和学生的更改T.-进行试验。总之,原始数据按秩中位数标准化,重复探针的强度值取平均值,对数2-处理与学生的比率计算T.- 应用于测试意义的学习。基因带有日志2-fold change <−1或> 1和P.-value < 0.05为显著差异。利用MapMan (http://mapman.gabipd.org/web/guest/mapman)和A.拟南芥基因本体软件(TAIR的GO注解)[95.].
如前所述,微阵列数据通过三个独立的生物实验和三个技术复制品(附加文件)通过qRT PCR进行验证2:表S4)。微阵列数据已提交给NCBI(GEO),注册号为GSE63500(https://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=gse63500.).
量化等
为了测量ET,从每个处理中收集100 mg的注射材料到4ml小瓶中(Roth,德国)。累积3小时ET后,按照Bhattacharya和Baldwin的描述,使用ETD-300 ET检测器(Sensor Sense B.V., Nijmegen, the Netherlands)进行测量[96.]和Sun等人。[92.].
统计分析
上面已经描述了微阵列数据的统计分析。所有额外的统计分析都是使用Excel(2010)进行学生配对进行的T.-双尾分布检验。
支持数据的可用性
支持本文结果的数据集包含在本文及其附加文件中。该微阵列数据已以GSE63500的加入号提交给NCBI (GEO)。
缩写
- PI.:
-
piriformospora indica.
- 病人:
-
磷
- 圆周率:
-
磷酸盐
- 是:
-
丛枝菌根
- TFs:
-
转录因子
- PHO1:
-
磷酸盐1
- 名词短语:
-
正常磷酸盐
- LP:
-
低磷
- 新闻部:
-
孵化后天
- 等:
-
乙烯
- 重量:
-
野生型
参考
- 1.
梁C,王家,赵家,田J,廖H。磷稳态通过作物基因调控控制。CurrOp植物BIOL。2014; 21:59-66。
- 2.
Fusconi公司。丛枝菌根根系形态发生的调控:真菌分泌物、磷酸盐、糖和激素在侧根形成中起什么作用?安·博特。2014;113:19–33.
- 3.
Péret B, Clément M, Nussaume L, Desnos T.根系发育适应磷酸盐饥饿:安全比遗憾好。植物科学,2011;16:42 - 50。
- 4.
NIU YF,柴RS,JIN GL,王H,唐CX,张YS。根系结构发展对低磷可用性的回应:综述。Ann Bot。2013; 112:391-408。
- 5.
德尼鸟P.磷酸盐饥饿信号传导:三人组对照Systemic P(i)稳态。CurrOp植物BIOL。2008; 11:536-40。
- 6.
Batjes nh。粮农组织联合国教科文组织土壤单位用于全球建模的世界数据集。土壤使用管理。1997年; 13:9-16。
- 7.
唐宁JA,Watson SB,McCauley E.预测湖泊中的蓝杆菌优势。可以j fish aquat sci。2001; 58:1905-8。
- 8.
胡b,zhu c,li f,唐j,王y,林a等。叶尖坏死1在水稻中多次磷酸盐饥饿反应的调节中起着枢转作用。植物理性。2011; 156:1101-15。
- 9。
Lambers H,Finnegan PM,Laliberte E,Pearse SJ,Ryan MH,Shane Mw等。Proteaceae在严重磷贫困土壤中的磷营养:有没有课程才能为未来的作物学习?植物理性。2011; 156:1058-66。
- 10
Vance CP,Uhde-Stone C,Allan DL。磷习得和用途:植物确保不可再生资源的批判性调整。新植物。2003; 157:423-47。
- 11
Lambers H, Shane MW, Cramer MD, Pearse SJ, Veneklaas EJ。有效获取磷的根系结构和功能:形态和生理特性的匹配。安机器人。2006;98:693 - 713。
- 12
丛枝管进口磷酸盐:只是一种营养物质吗?植物微生物学报。2011;24:1296-9。
- 13
Balzergue C, Puech-Pagès V, Bécard G, Rochange SF。磷酸盐对豌豆丛枝菌根共生的调控涉及早期和系统信号事件。实验机器人。2011;62:1049-60。
- 14
Camehl i,Drzewiecki C,Vadassery J,Shahollari B,Sherameti I,Forzani C,等。oxi1激酶途径介质piriformospora indica.- 拟南芥的生长促进。PLOS POAROG。2011; 7,E1002051。
- 15
Jogawat A、Saha S、Bakshi M、Dayaman V、Kumar M、Dua M等。piriformospora indica.高盐胁迫期间拯救水稻幼苗的生长减少。植物信号表现。2013; 8,E26891。
- 16
YE W,Shen Ch,Lin Y,Chen PJ,Xu X,OelmüllerR,等。生长促进相关的miRNA在内生真菌殖民殖民的植物兰花根中piriformospora indica..Plos一个。2014; 9,E84920。
- 17
谢拉梅蒂一世、沙霍拉里B、维纳斯Y、阿尔特施密德L、瓦尔马A、奥尔穆勒R。内生真菌piriformospora indica.通过在其启动子中与保守的基序结合的同源域转录因子刺激硝酸还原酶和淀粉降解酶葡聚糖水直立通酶的表达。J Biol Chem。2005; 280:26241-7。
- 18
Kumar M, Yadav V, Kumar H, Sharma R, Singh A, Tuteja N等。piriformospora indica.通过转移磷酸盐来增强植物生长。植物信号表现。2011; 6:723-5。
- 19
Yadav V,Kumar M,Deep DK,Kumar H,Sharma R,Tripathi T等。一种来自根内生真菌的磷酸转运蛋白piriformospora indica.在磷酸盐转运到寄主植物中起作用。生物化学杂志。2010;285:26532-44。
- 20.
Pedersen BP、Kumar H、Waight AB、Risenmay AJ、Roe Zurz Z、Chau BH等。真核磷酸盐转运蛋白的晶体结构。自然。2013;496:533–6.
- 21.
维纳斯Y,奥尔穆勒R。拟南芥ROP1和ROP6影响萌发时间、根系形态、F-肌动蛋白束的形成和共生真菌的相互作用。摩尔植物。2013;6:872–86.
- 22.
Vadassery J,Ranf S,Drzewiecki C,Mithofer A,Mazars C,Scheel D,等。一种从植物中提取的细胞壁提取物piriformospora indica.促进拟南芥幼苗的生长,诱导根内钙离子的升高。植物j . 2009; 59:193 - 206。
- 23.
巴拉扎尼O,本德罗斯M,格罗滕K,库勒迈耶C,鲍德温IT。piriformospora indica.和Sebacina vermifera以牺牲草食动物抗性为代价提高生长性能烟草. 食道痛。2005;146:234–43.
- 24。
Waller F,Achatz B,Baltruschat H,Fodor J,Becker K,Fischer M等。内生真菌piriformospora indica.将大麦重新编程为盐胁迫耐受性,抗病性和更高的产量。Proc Natl Acad Sci U S A. 2005; 102:13386-91。
- 25。
Baltruschat H,Fodor J,Harrach BD,Niemczyk E,Barna B,Gullner G等.根内生菌诱导大麦耐盐性的研究piriformospora indica.与抗氧化剂的大量增加有关。新植物醇。2008;180:501–10.
- 26。
Pedrotti L、Mueller MJ、Waller F。piriformospora indica.根殖民化触发局部和全身根系响应并抑制远端根的二次定殖。Plos一个。2013; 8,E69352。
- 27。
Fakhro A、Andrade Linares DR、von Bargen S、Bandte M、Büttner C、Grosch R等。环境影响piriformospora indica.论番茄生长及与真菌和病毒病原体的相互作用。mycorrhiza。2010; 20:191-200。
- 28。
Das A,Kamal S,Shakil Na,Sherameti I,Oelmüllerr,dua m等。根内食细胞真菌piriformospora indica.导致药用植物开花早,生物量高,次生代谢产物发生改变COSEUS FORSKOHLII..植物信号表现。2012; 7:103-12。
- 29。
Sherameti I,Tripathi S,Varma A,OelmüllerR.根殖民化内心Pirifomospora indica.通过刺激叶片中干旱胁迫相关基因的表达,赋予拟南芥抗旱性。植物与微生物相互作用。2008;21:799–807.
- 30.
Khatabi B,Schäfer P。乙烯在共生共生体中。电厂信号行为。2012;7:1634–8.
- 31
Chi Y,Yang Y,周Y,Zhou J,Fan B,Yu JQ等人。蛋白质 - 蛋白质相互作用在腕骨转录因子的调节中。莫尔植物。2013; 6:287-300。
- 32
WRKY转录因子,Oelmüller R. WRKY转录因子植物信号处理研究,2014;9,e27700。
- 33
Llorca CM、Potschin M、Zentgraf U。bZIPs和WRKYs:两个大的转录因子家族执行两种不同的功能策略。前植物科学。2014;5:169.
- 34
陈一夫,李立群,徐群,孔一赫,王赫,吴华。WRKY6转录因子调节拟南芥低Pi胁迫下磷酸1的表达。植物细胞。2009;21:3554–66.
- 35
Devaiah BN、Karthikeyan AS、Raghothama KG。WRKY75转录因子是拟南芥磷酸获得和根系发育的调节因子。植物生理学。2007;143:1789–90.
- 36
德瓦雅BN, Raghothama KG。WRKY75对Pi饥饿反应的转录调控植物信号行为。2007;2:424-5。
- 37
MA Z,Baskin Ti,Brown Km,Lynch JP。在磷胁迫下对根伸长的调节涉及乙烯反应性的变化。植物理性。2003; 131:1381-90。
- 38
石井一世,石狮一世,松本刚明。乙烯对泡状丛枝菌根真菌生长及枳实根形成的影响。日本社会科学杂志。1996;65:525–9.
- 39
汉堡D,Rezzonico E,PetétotJMC,Somerville C,Poirier Y.鉴定磷酸盐载荷鉴定和表征磷酸盐载荷对木质。植物细胞。2002; 14:889-902。
- 40
在ARF5/MP的转录调控中,Aux/IAA基因的不同亚分支是直接调控ARF5/MP的靶标。新植醇。2014;204:474 - 83。
- 41
Guilfoyle TJ,Hagen G.在负责助长响应因子-IAA蛋白相互作用的域III / IV上得到掌握。植物SCI。2012; 190:82-8。
- 42
Benschop JJ,Millenaar FF,Smeets ME,van Zanten M,Voesenek LA,Peeters AJ。脱落酸拮抗乙烯诱导的拟南芥低鼻生长。植物生理学。2007;143:1013–23.
- 43
CN,CCC,Zentella R,Pan Sm,Ho Thd。Athva22在拟南芥中的基因家族:系统发育关系,ABA和应力调控和组织特异性表达。植物mol biol。2002; 49:631-42。
- 44.
杨F,宋y,杨h,刘z,zhu z,杨玉。一种生长素响应的内源性肽调节拟南芥的根本发育。J Intent Plant Biol。2014; 56:635-47。
- 45.
关键词:拟南芥,赤霉素生物合成,甘氨酸,rna结合蛋白Mol Biol Rep. 2014; 41:439-45。
- 46.
HSIEH LC,Lin Si,Shih Ac,Chen Jw,Lin Wy,Tseng Cy等。通过深度测序揭示拟南芥磷酸盐缺乏的小RNA介导的反应。植物理性。2009; 151:2120-32。
- 47.
Pant BD,Musialak-Lange M,Nuc P,May P,Buhtz A,Kehr J等人。全面实时聚合酶链反应分析和小RNA测序鉴定营养响应拟南芥和油菜籽微瘤的鉴定。植物理性。2009; 150:1541-55。
- 48。
宋建斌、黄思琦、戴梅、杨志明。microRNA394对叶片形态的调控及其对目标叶片卷曲的响应。植物细胞生理学。2012;53:1283–94.
- 49。
Sorin C,Marie D,AurélieC,托马斯B,林南M,Christine L-B等。MIR169同种型在拟南芥中调节特定的NF-YA目标和根系结构。新植物。2014; 202:1197-11。
- 50。
何浩,梁刚,李勇,王飞,于丹。两个年轻的microrna来源于靶标复制介导的氮饥饿适应通过硫代葡萄糖苷合成的调节拟南芥. 植物生理学。2014;164:853–65.
- 51。
陈立群,曲学群,侯波,索索D,Osorio S,Fernie AR,等。糖蛋白介导的蔗糖外流是韧皮部运输的关键步骤。科学。2012;335:207–11.
- 52。
拟南芥中生长素调控基因与油菜素类固醇激素调控基因的综合比较。植物杂志。2004;134:1555 - 73。
- 53。
Kiba T、Naitou T、Koizumi N、Yamashino T、Sakakibara H、Mizuno T。组合微阵列分析揭示拟南芥基因通过His参与细胞分裂素反应- > Asp磷光电路。植物细胞生理学。2005;466:339–55.
- 54。
蔡奕、庄×、高丙、王×、蒋璐。转运Ⅲ所需的拟南芥内质体分选复合体调控着前胚轴室的内部囊泡形成,是植物发育所必需的。植物生理学。2014;165:1328–43.
- 55
Tam PP、Barrette Ng IH、Simon DM、Tam MW、Ang AL、Muench DG。植物RNA结合蛋白Puf家族:系统发育、结构建模、活性和亚细胞定位。BMC植物生物学。2010;10:44.
- 56
张浩,金女士,Krishnamachari V,Payton P,孙Y,Grimson M,等.根际细菌挥发性物质排放调节拟南芥生长素稳态和细胞扩张。足底。2007;226:839–51.
- 57
Müller R, Morant M, Jarmer H, Nilsson L, Nielsen TH。拟南芥叶片转录组的全基因组分析揭示了磷酸盐和糖代谢的相互作用。植物杂志。2007;143:156 - 71。
- 58
Robatzek S,Somssish Ie。植物衰老和病原体防御期间Atwrky6调节的目标。基因开发。2002; 16:1139-49。
- 59
Sukumar P,LeguéV,VayssièresA,Martin F,托斯康省,Kalluri UC。养肝途径参与在有益植物微生物相互作用中调节根系结构中的调节。植物细胞环境。2013; 36:909-19。
- 60
Mukherjee K,Ane J.发芽孢子从丛枝菌根真菌渗出:植物中的分子和发育反应及其乙烯调控。Mol植物微生物相互作用。2011; 24:260-70。
- 61
López-Arredondo DL, Leyva-Gonzalez MA, Gonzalez-Morales SI, López-Bucio J, Herrera-Estrella L.磷酸盐营养:提高作物低磷耐受性。植物生物学杂志。2014;65:95-123。
- 62
董某,田泽,陈PJ,Senthil Kr,Shen Ch,Cai D等人。成熟区是一个重要的目标piriformospora indica.在大白菜的根部。J实验机器人。2013;64:4529–40.
- 63
李YC,江志强,钱聪,孙聪,蔡德,娄乙,等。大豆对大白菜和拟南芥生长的促进作用piriformospora indica.不受菌丝体合成生长素的刺激。植物与微生物相互作用。2011;24:421–31.
- 64
Glassop D、Godwin RM、Smith SE、Smith FW。与丛枝菌根真菌定殖水稻根系磷吸收相关的水稻磷转运蛋白。植物学。2007;85:644–51.
- 65
哈里森MJ,德沃基,刘家。磷酸盐转运蛋白Medicago Truncatula.参与获得丛枝菌根真菌释放的磷酸盐。植物细胞。2002;14:2413-29。
- 66
Shahollari B,Varma A,Oelmüllerr.拟南芥中受体激酶的表达由蛇肌肌瘤刺激piriformospora indica.蛋白质聚集在tritonx-100不溶性质膜微区。植物生理学杂志。2005;162:945–58.
- 67
Rausch C,Bucher M。植物磷转运的分子机制。足底。2002;216:23–37.
- 68.
Schachtman DP, Reid RJ, Ayling SM。植物对磷的吸收:从土壤到细胞。植物杂志。1998;116:447-53。
- 69.
贾沃特,彭普林,哈里森。MJ。磷酸盐在丛枝菌根共生中的转运特性和调控作用。植物细胞环境。2007;30:31 - 22。
- 70。
AI P,Sun S,Zhao J,Fan X,Xin W,Guo Q等。两种磷酸盐转运蛋白,散氨酸1; 2和散氨酸; 6,具有不同的功能和动力学性质,以摄取和易位。工厂J. 2009; 57:0798-809。
- 71。
林奇j,棕色km。乙烯和植物对营养应激的反应。physiol植物。1997年; 100:613-9。
- 72。
Cameh我,Sharameti I,Venus Y,Bethke G,Varma A,Lee J等。乙烯信号传导和乙烯靶向转录因子需要在内生真菌之间的共生中平衡有益和非联义的性状piriformospora indica.和拟南芥.新植物。2010; 185:1062-73。
- 73。
Peškan-berghöfert,沙尔里拉B,Giong ph,Hehl S,Markert C,Blanke V等人。协会piriformospora indica.具有拟南芥根是一种研究植物与微生物间有益相互作用的新系统,涉及植物内质网和质膜上的早期蛋白质修饰。杂志杆菌。2004;122:465 - 77。
- 74。
Oelmüller R、Peškan Berghöfer T、Shahollari B、Trebicka A、Sherameti I、Varma A。数学结构域蛋白代表了一个新的蛋白质家族拟南芥,并且在植物-微生物相互作用的过程中,至少一个成员在根中被修饰。植物生理学。2005;124:152–66.
- 75。
Vadassery J,Ritter C,Venus Y,Camehl I,Varma A,Shahollari B等人。毒素和细胞素素在拟南芥和互动中的作用piriformospora indica..Mol植物微生物相互作用。2008; 21:1371-83。
- 76。
Spartz AK,Lee SH,Wenger JP,Gonzalez N,Itoh,InzéD等。小生长素RNA基因SAUR19亚家族促进细胞扩张。植物J。2012;70:978–90.
- 77。
王克,张斯,太阳镭射唱片,徐yx,陈y,yu cl,等。养蛋响应因子(Osarf12),一种用于米饭中磷稳态的新型调节剂(栽培稻).新植物。2014; 201:91-103。
- 78。
祁永红,王士科,沈昌杰,张森,陈勇,徐应祥,等。植物生长素应答基因转录激活因子OsARF12调控水稻根系伸长并影响铁的积累(栽培稻). 新植物醇。2012;193:109–20.
- 79
Bruex A,Kainkaryam Rm,Wieckowski Y,Kang Yh,Bernhardt C,夏Y等。拟南芥中根表皮细胞分化的基因调节网络。Plos Genet。2012; 8,E1002446。
- 80。
嗯ys,um jh,金s,金k,park hj,lim js等。拟南芥同源框12(ATHB12)是一种同源结构域亮氨酸拉链蛋白,通过促进细胞扩张和内复制来调节叶片生长。新植物醇。2014;205:316–28.
- 81。
Bernal AJ,Yoo CM,Mutwil M,Jensen JK,Hou G,Blaukopf C,等。顶端生长拟南芥细胞中纤维素合成酶样基因CSLD1,CSLD2和CSLD4的功能分析。植物生理学。2008;148:1238–53.
- 82。
杨德尔,姚杰,梅CS,童Xh,zeng lj,li q等。植物激素茉莉酸酯通过干扰吉伯塞林信号级联来优先考虑对增长的防御。Proc Natl Acad Sci U S A. 2012; 109:E1192-200。
- 83
Simon SA、Meyers BC、Sherrier DJ。豆科根瘤菌共生中的MicroRNAs。植物生理学。2009;151:1002–8.
- 84
顾米,徐克,陈开,朱y,唐g,徐g。表达分析表达分析表明微小磷酸盐和丛枝菌体信号的潜在作用番茄茄.physiol platararum。2010; 138:226-37。
- 85
顾明,刘伟,孟Q,张伟,陈A,孙S,等。6种茄科植物中microRNA的鉴定及其与磷和菌根信号转导的潜在联系。综合植物生物学杂志。2014;56:1164–78.
- 86
hajdarpašia,ruggenthaler p.压力下miRNA表达的分析拟南芥.BOSN J Basic Med Sci。2012; 12:169-76。
- 87
李建平,李永芳。植物微rna在逆境响应中的作用。植物科学,2012;
- 88
Khan GA, Declerck M, Sorin C, Hartmann C, Crespi M, Lelandais BC。MicroRNAs是根发育和结构的调节因子。植物生物学杂志。2011;47:47 - 58。
- 89
李超,张斌。microrna在植物发育中的调控作用。J Cell Physiol. 2016; 231:303-13。
- 90.
一种用于烟草组织培养的快速生长和生物测定的修正培养基。杂志。1962;15:473 - 97。
- 91.
Johnson JM,Sharameti I,Ludwig A,Nongbri Pl,Sun C,Lou B等。协议拟南芥和piriformospora indica.共同栽培 - 研究植物有益特征的模型系统。J Endocyt Cell。2011; 101-13。
- 92.
Sun C,Shao Y,Vahabi K,Lu J,Bhattacharya S,Dong S等人。有益的真菌piriformospora indica.保护拟南芥免受大丽叶黄萎病下调植物防御反应感染。BMC植物BIOL。2014; 14:268。
- 93.
Pfaffl兆瓦。实时荧光定量pcr中相对定量的新数学模型。核酸杂志2001;29,e45。
- 94。
Bolstad BM,Rafael AI,Magnus A,Terence PS.基于方差和偏倚的高密度寡核苷酸阵列数据标准化方法的比较。生物信息学。2003;19:185–93.
- 95。
Berardini Tz,Mundodi S,Reiser L,Huala E,Garcia-Hernandez M,张P等人。拟南芥基因组的功能注释使用受控词汇表。植物理性。2004; 135:745-55。
- 96。
Bhattacharya S,Baldwin。授粉后乙烯爆发和花卉广告的延续是非随机交配选择的先兆尼古利亚娜attenuata..工厂J. 2012; 71:587-601。
致谢
MB由Deutscher Akademischer Austauschdienst(Daad)提供支持。这项工作得到了协作研究中心1127(Deutsche Forschungsgemeinschaft,Project A03),国际Max-Planck研究学校耶拿和耶拿微生物传播学院。Ro和Kwy来自Daad的旅行资助。
作者信息
从属关系
通讯作者
附加信息
相互竞争的利益
作者声明他们没有相互竞争的利益。
作者的贡献
MB设计并进行了所有实验并写了这篇文章。KV帮助微阵列分析。SB做了植物激素分析。是,AV,K-WY,ITB和AKJ为讨论做出了贡献。RO设计了实验,写了这篇文章并监督了该研究。所有作者阅读并认可的终稿。
其他文件
附加文件1:表S1。
基因表达上调超过2倍wrky6公司 + P印度在LP中(日志2价值 ≥ 1或 ≤ −1). (XLS(200 kb)
附加文件2:表S2。
被调控超过2倍的基因(log2值 ≥ 1) 针对Pi限制,P印度和变异的WRKY6.表S3。本研究中使用的引物。表S4。具有实时PCR的微阵列验证。(PDF 563 KB)
权利和权限
开放存取本文根据知识共享署名4.0国际许可的条款分发(http://creativecommons.org/licenses/by/4.0/)如果您向原始作者和源给出适当的信用,则允许在任何介质中进行不受限制的使用,分发和再现,提供指向Creative Commons许可证的链接,并指示是否进行了更改。Creative Commons公共领域奉献豁免(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条提供的数据,除非另有说明。
关于这篇文章
引用本文
Bakshi,M.,Vahabi,K.,Bhattacharya,S。等。WRKY6限制piriformospora indica.- 拟计拟计和磷酸盐诱导的拟南芥根系。BMC植物生物学15,305 (2015). https://doi.org/10.1186/s12870-015-0673-4
收到:
公认:
发表:
关键词
- WRKY6
- piriformospora indica.
- 磷酸盐
- 根系发育
- 表达式档案