摘要
背景
光合作用是植物代谢的重要能量来源,非生物胁迫可能使光合作用效率大大降低。毛竹竹(植被类型),是一种具有重要生态和经济价值的可再生、多用途资源,在自然环境中受到高强度的光胁迫。然而,竹子对强光反应的基因表达谱尚不清楚。
结果
本文首先对毛竹叶片进行了1200 μmol·m强光处理的生理试验-2·年代-1).根据生理结果,选择用高光处理的三个叶片(CK),0.5小时(0.5H)和8小时(8H)处理以进行进一步的高通量RNA测序(RNA-SEQ),分别。然后,转录组结果证明,大多数基因以统计学上显着的值(FPKM≥1)表示,并且通过定量实时PCR验证RNA-SEQ数据。此外,检测到一些显着的基因表达变化。例如,在0.5h中检测到154个差异表达基因vs..CK,在8H内vs..CK是710,429个差异表达基因也以0.5h鉴定出来vs.此外,共完善了47条与光合作用密切相关的基因注释,其中35条注释为light-harvesting叶绿素a/b binding (LHC)蛋白,9条注释为LHC-like蛋白,3条注释为PsbSs。进一步分析了活性氧(ROS)在光合作用中的作用途径。共鉴定出171个与ros清除相关的基因。一些上调的转录因子如NAC、WRKY、AR2/ERF、bHLH主要集中在短期反应中,而C2H2,HSF,BZIP和MYB在很大程度上涉及到高光的短期和中间术语。
结论
通过对毛竹在强光下的基因表达分析,确定了毛竹整体基因表达模式,并对LHC蛋白、LHC样蛋白和PsbS蛋白的注释进行了完善。检测ROS通路,鉴定ROS清除基因和转录因子在调控光合及相关代谢中的作用。这些发现可能为解释毛竹在强光胁迫下光合作用的分子机制提供了一个起点。
背景
在草族Poaceae,Bambusoideae,部落Bambusease的木本竹子被认为是世界上最重要的非木材森林资源之一。近年来,木质竹子在生态和经济方面得到了很多关注,因为它具有多种优势,如快速增长,高强度重量比,强烈氧化的秆,强烈碳固定能力。木质竹是中国亚热带地区碳封存的最佳药物之一,比中国冷杉和松树更有效2至4倍[1].光合作用在提供碳水化合物以展示竹子的特性方面起着至关重要的作用。然而,通过对不同竹类异构体(Lhcb1-3)的光谱特征、形成同型三聚体的能力和结构稳定性的研究表明,尽管存在微小差异,但与其他高等植物具有相似的特征[2]这意味着竹子可能在光利用率和调节过程中具有特殊机制,但它的快速增长虽然它是未知的。
研究竹叶光合作用相关基因表达谱对了解竹叶光合作用的分子基础和响应强光的动态基因表达具有重要意义。高通量RNA测序(RNA- seq)作为下一代测序技术的核心之一,能够揭示RNA存在和数量的快照,从一个基因组在给定的时刻[3.那4.].毛竹基因组序列草图的完成[5.[RNA-SEQ数据将有助于合理地解释基因组的功能元素,并在轻应力下揭示分子组合物。以前的表达谱研究主要集中在不同的组织上[6.-9.].迄今为止,与高光相应的光合作用基因的全基因组表达谱仍然难以实现。
中国特有的竹子品种毛竹(moso bamboo,简称moso bamboo) (植被类型)以进一步的分析为重点。基于光合生理学的分析,三种样品包括高光处理的叶子(1200μmol·m-2·年代-1分别于0 h (CK)、0.5 h (0.5 h)和8 h (8H)进行RNA分离。我们利用Illumina HiSeq 2000测序平台,基于3个样本的RNA-Seq数据,在深度测序池中鉴定了大量表达基因。通过基因聚类分析、基因表达模式分析、差异表达基因分析和转录因子分析,进一步了解强光下的光合作用、活性氧(ROS)和非光化学猝灭(NPQ)。这可能为进一步的实验设计提供了表达谱的来源,也为进一步研究光胁迫下基因的功能和调控网络,特别是参与强光响应的转录因子奠定了基础。
结果与讨论
竹子光合生理分析
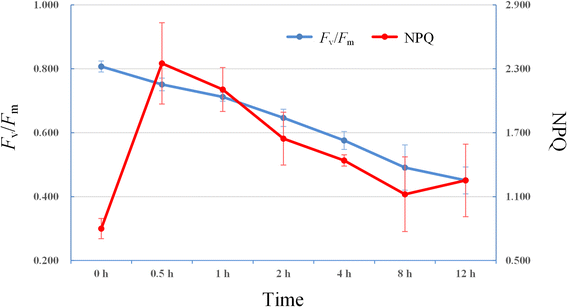
叶绿素荧光动力学技术在植物光合作用的研究中被称为快速和非流体探针。在荧光参数中,NPQ动力学经常用作表征非光化学淬火过程的工具,以及最大光化学效率(FV./Fm)是估计光抑制程度的指数[10.].因此,NPQ动力学和FV./Fm在高光下的莫斯竹叶中研究了(1200μmol·m-2·年代-1),分别持续12小时。因此,图中的结果。1描绘了分布FV./Fm相同光强不同时间处理对毛竹叶片NPQ的影响。最大FV./Fm出现在0小时,然后在高光下的增加的时间几乎线性地降低。的价值FV./Fm结果表明,毛竹叶片在强光下受到光抑制,且随着强光时间的延长,光抑制程度不断增强。同样,NPQ激活的高亮度和迅速增加在第一次0.5 h,然后慢慢下降,最后趋于稳定后8 h。综上所述,我们选择三个代表性样本,包括0 h (CK), 0.5 h(0.5小时)和8 h(8小时),进一步执行一系列的转录组分析。
竹转录组概述QRT-PCR的RNA-SEQ数据验证
鉴于少于8小时的高光线的自然每日压力,在光合生理实验的基础上选择三个RNA文库。构建了这些文库,然后基于Illumina HighSeq-2000对母干测序,以帮助全球理解转录组的全球地图集,以应对高光。在RNA-SEQ的原始数据预处理和质量控制后,清洁读数与竹子基因组数据库的参考基因组序列对齐[11.)(www.bamboogdb.org.(版本1)来估计每个文库中表达基因的轮廓。利用TopHat软件,根据转录组特征和基因组结构设置核心参数。如附加文件所示1,最终获得了3.21亿次(~32 Gb)高质量读,平均每个样本有1.07亿次(~10 Gb)读,全部为干净读。大约75.04%的reads被认为是唯一读,6.76%的reads被认为是多位置读,分别表示映射到参考基因组中具有唯一位置和多位置的读的数量。由于参考基因组的复杂性以及测序和比对方法的局限性,多位置reads最终会随机映射到参考基因组的一个位置,因此在基因表达水平分析中不可避免地存在一定的偏差。因此,在我们的研究中,更多的unique reads和更少的multi-position reads的结果,将有助于产生更可靠的比对数据,以便于后续的表达分析。
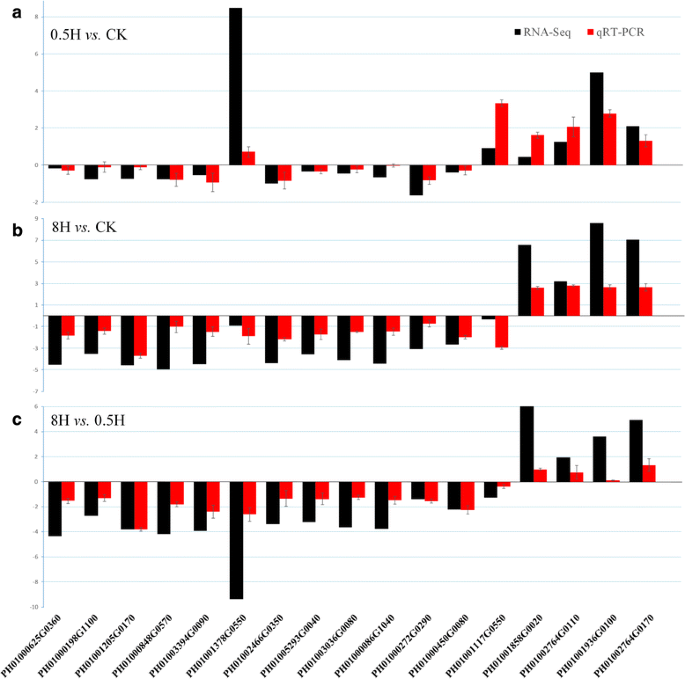
为了适当地验证基于RNA-SEQ的表达的基因,使用独立收集的样品进行QRT-PCR测定,其与用于RNA-SEQ分析的相同的发育阶段。我们从与光合作用相关的更多基因中选择了17个基因。这些含有的14个基因属于叶绿素A / B结合(LHC)蛋白质超家族(10基因编码LHC蛋白和4个基因,编码早期光诱导的蛋白质)和3种Aquaporin蛋白家族,可能涉及气孔数的调节和大小。基于通过QRT-PCR验证RNA-SEQ的子集,图1的比较结果。2RNA-Seq与qRT-PCR表达模式相似,证明RNA-Seq数据的可靠性。详细结果见附加文件2.
竹子中表达基因的分析
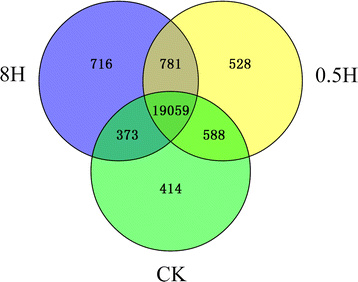
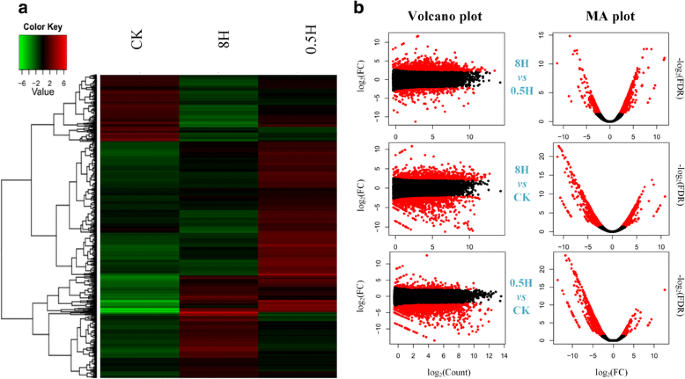
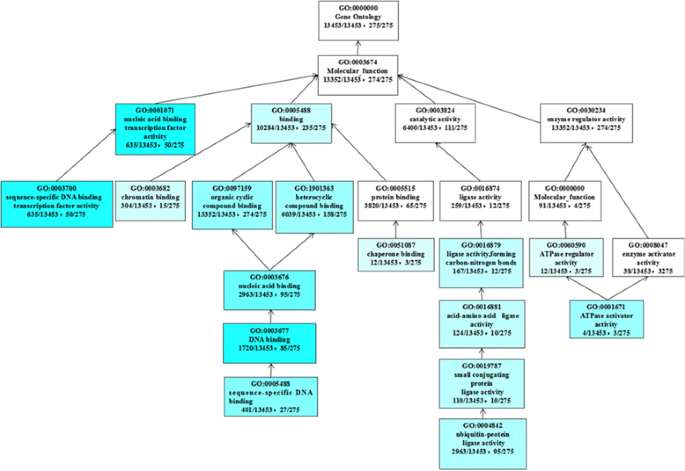
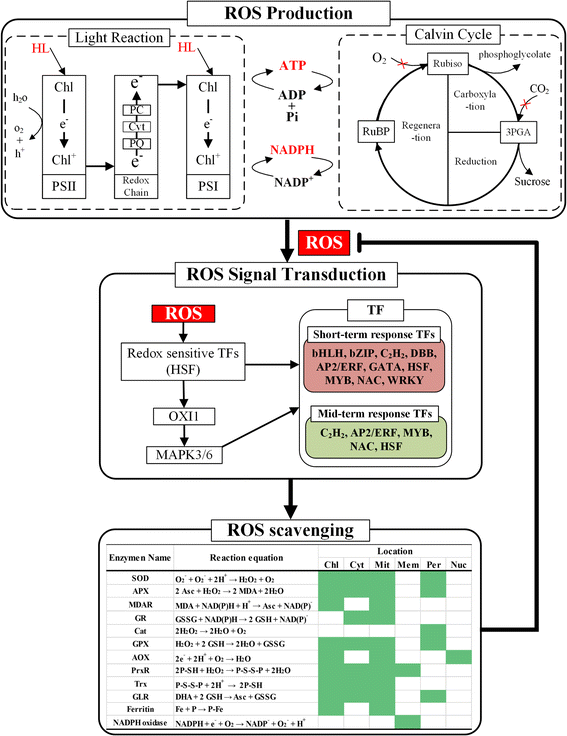
FPKM,也称为每百万覆盖碎片的基因的每千碱基片段,广泛用于RNA-SEQ分析,旨在量化基因表达水平的分析。为了确定在每个样品中表达哪些基因,在三个样品中满足基因表达值分布的统计(图。3.和额外的文件3.).结果表明,毛竹3个文库中所有基因的基因表达分布相似4.).此外,具有FPKM> 0的基因占总注释基因的〜90%基因以及中等表达值(1 3个样本中FPKM≥1表达基因的维恩图。在CK、0.5H和8H中FPKM≥1的表达基因分别为20,434、20,956和20,929个。在三个样本中有19059个表达基因。0.5H ~ 8H表达基因781个。CK ~ 0.5H表达基因588个。CK与8H之间表达基因373个。414个表达基因仅包含在CK中。528个表达基因仅包含在0.5H内。8H包含716个表达基因。维恩图中表达基因的详细信息见附加文件3. 此外,为探究个体样本内(标记为样本内)19059个表达基因的保守生物学功能,以所有竹子基因为背景,进行基因本体(Gene Ontology, GO)术语的富集分析(附加文件)5.).总共131个术语,“生物过程”(80),“分子功能”(22)和“细胞成分”(29)被检测为调整后的重要术语P.值< 0.01。“生物过程”术语的结果表明,这些表达基因在“翻译(GO:0006412)”、“器官氮化合物代谢过程(GO:1901564)”和“小分子代谢过程(GO:0044281)”相关的过程中高度富集。在“分子功能”方面,主要富集了“核糖体结构成分(GO:0003735)”和“RNA结合(GO:0003723)”。最终,在“细胞成分”中富集的GO术语涉及“细胞质(GO:0005737)”、“细胞质部分(GO:0044444)”和“核糖核蛋白复合物(GO:0030529)”。 广泛应用聚类亲和力搜索技术(铸造)以在不同样本期间阐明转录组的动态变化[12.].通过该研究的施放利用的聚类结果显示,样品内的19,059个表达基因聚集成5组,其中基因数范围为337至6564.如图1所示。4.,聚类分析结果显示,5组表达基因的表达模式存在差异。相同的模式包含了相似的表达基因趋势,表明这些基因可能参与了相似或相关的生物学过程。其中,聚类1是最受关注的一组,因为发现了大量与光合作用相关的基因,如叶绿素a/b结合蛋白的26个基因和光系统相关的16个基因。结果表明,集群1中与光合作用相关的基因数量多于其他集群,表明这些基因可能在对强光的响应中起着关键作用。 此外,为了更好地了解和揭示聚类基因的表达特征,采用了对富集的转移术语分析。例如,簇1中的基因表达连续地减小,随着0.5h和8h之间的增加的光处理时间。Go Emichment还示出了“光合作用(GO:0015979)”,“光束(GO:0009521)”和“转运蛋白活动(GO:0005215)”在群体中富集。相反,基因表达连续增加随着光线的增加,0.5h和8h之间。主要重要的GO术语,例如“蛋白分解代谢过程(GO:0030163)”,“RNA结合(GO:003723)”和“核糖体(GO:0030529)”,在群体中是富集的2.与CK相比簇3,类似的表达水平在8小时内出现在0.5h和CK之间的表达水平之前。分子功能的主要重要术语,“核酸结合转录因子活性(GO:0001071)”,“序列特异性DNA结合转录因子(GO:0003700)”和“钙离子结合(GO:0005509)”,表明有些TFS和钙可能会参与这个过程。此外,由于一些数据解决了标准,因此在集群4和5中识别了几个或没有重要的GO术语。每个组中的基因列表和大型GO术语存储在附加文件中6.. 根据样本间的两两比较,利用以下截断点:log,共鉴定出1293个差异表达基因(DEGs)2FC≥2或≤−2,FDR < 0.011).154个基因的数量在0.5H内不同vs..CK,包括132个上调基因和22个下调基因。8小时不同的710个基因的数量vs..由435个上调基因和275个下调基因组成。最终,在0.5H内差异的429个基因中vs..8H,上调基因337个,下调基因92个。因此,为了生动地说明所识别的1293℃的表达谱,图中绘制了热图和plot。5.. 此外,我们完成了GO富集分析,以研究其在差异表达基因中的功能分布7.).结果表明,某些具有相似函数的显著GO项集中在某些数据集中。例如,与转录因子相关的GO术语“核酸结合转录因子活性(GO:0001071)”和“序列特异性DNA结合转录因子活性(GO:0003700)”在0.5H的DGEs数据集中富集vs..CK(无花果。6.).另一个例子是,在8H下调的DGEs数据集中,有17个显著的GO项参与了光系统和相关通路,占总数的50%以上vs..CK,例如“光照00(GO:0009522)”,“光系统(GO:0009521)”,“thylakoid(Go:0009579)和”光合作用(GO:0015979)“。 光合作用为地球上几乎所有生命提供化学能。光合作用中的主要事件涉及从阳光吸收太阳能,在光合系统的外周天线中产生电子激发,并随后将激励转移到反应中心[13.].有效的光收获步骤对于光合作用的成功至关重要。此外,LHC蛋白也称为光收获天线,是真核光合作用的核心,包括LHC家族和几个与phtotopotection相关的家族,例如三螺旋早光诱导蛋白(ELIPS),两个-Helix应激增强蛋白(SEP),单螺旋光诱导蛋白(OHPS)和光系统II亚基S(PSB)[14.那15.].基于基因组的分析,LHC蛋白质和elips拟南芥和栽培稻分析了(16.].然而,LHC蛋白的基因组研究仍然无法在竹子中不可用。在表格基因组分析和RNA-SEQ中,我们在莫斯竹中识别并精制了LHC蛋白质超家族2. 总共有42个在莫斯竹基因组中的基因被注释为大型强子对撞机和大型强子对撞机- 类似的基因,包括38大型强子对撞机基因和4.el基因(11.].在这里,我们对35个、9个和3个基因进行了验证和提炼大型强子对撞机那大型强子对撞机例如,公安局摩尔竹中的基因分别基于(i)互核性最佳基因的序列分析A. Thaliana.和o.苜蓿(ii)二级结构预测,(iii)序列基序,(iv) KEGG结构域搜索,(v)全基因组转录组。例如,对毛竹基因组中5个没有详细注释的基因进行了提炼。PH01002445G0060的精练注释为“单螺旋蛋白1”。PH01000097G0840和PH01000213G0560更新注释为“胁迫增强蛋白1”。PH01003491G0150和PH01000280G1190的精练注释分别为“胁迫增强蛋白2”和“胁迫增强蛋白3”。此外,三个基因注释PH01000004G0130、PH01000293G0420和PH01000845G0420被更新为“非光化学猝灭(NPQ) 4,光系统II亚基”,而不是最初的注释“叶绿素a/b结合蛋白”。 值得注意的是,PH01001205G0190与“叶绿素a/b结合蛋白”的初始注释可能存在问题,这不仅是因为在DNA与蛋白质的序列比较分析中无法得到结果,如NCBI核苷酸收集中的nucleotide BLAST和蛋白域搜索,也因为本研究没有表达价值。此外,PH01001205G0190的表达值在之前的一些毛竹转录组研究中也未检测到[8.那9.那17.].因此,我们认为,由于毛竹中PH01001205G0190的测序和组装的复杂性,最初注释可能存在错误。 毛竹中有35个编码叶绿素a/b结合蛋白的基因,高于毛竹中23个编码叶绿素a/b结合蛋白的基因A. Thaliana.和17个基因o.苜蓿.同样,竹子中也有12个基因编码LHC-like和pbs。那些在A. Thaliana.和o.苜蓿分别为7和11。更多的副本大型强子对撞机基因表明了Moso竹子的快速生长阶段可能需要更多能量。FPKM结果表明了主要的表达大型强子对撞机随着光照时间的增加,基因数量依次减少。同时,表达式值为4el基因出现了很大的崛起,与先前的报道一致,即在早期的紫花状发育和轻应力期间累积的累积。此外,先前的研究还证实,LHC蛋白的主要功能是通过叶绿素激发和吸收能量转移到光化学反应中心的光,而LHC样和PSB家族的成员可能参与应力保护[18.-21]. 高光的照明可能触发到过度光合颜料和电子传输链[22].当它超过正常代谢的要求时,就会在光系统中产生过量的激发能。高能态可由NPQ和/或替代过程(如光呼吸代谢)耗散,并可转移到氧,从而产生有毒活性氧(ROS) [23].为了避免损伤细胞成分甚至氧化细胞的氧化破坏,ROS必须通过ROS-清除途径排毒,该途径含有主要酶,例如超氧化物歧化酶(SOD),抗坏血酸过氧化物酶(APX),过氧化氢酶(猫),谷胱甘肽过氧化物酶(GPX依此类推(附加文件8.).根据竹子的注释和结果,最好的基因与互惠拟南芥和o.苜蓿,在毛竹中发现大量ros -清除酶,且在强光下其表达量增加,其中PH01000083G1490、PH01001010G0010、PH01001942G0260几乎出现在8H。 此外,RNA-Seq数据结果还显示,在强光下,Calvin周期和光呼吸代谢的基因表达均值均下降(Additional file)9.).一个可能的原因是co2光合碳还原循环酶的含量和活性降低可能对卡尔文循环产生不利影响。有限有限公司2因此,同化导致光致血管代谢中的基因表达降低。因此,在高光下抑制了Calvin循环和光呼吸道代谢中表达基因的水平。 ROS信号转导通路在ROS信号检测,接收和交付中实现了基本作用,以调节ROS-清除途径。蒸馏分析结果证实了ROS信号转导途径中的基因在高光下上调。然而,DGE DataSet中的植物热应激转录因子(HSF)在0.5h比8h中更浓缩。在0.5h中检测到高表达基因,例如pH01000000G3800和pH01000546G0840。这些指示的HSF作为ROS信号之一,也许在高光应力的早期阶段起着基本作用。此外,用HSP和HSP20 /α结晶家族蛋白注释的上调基因被检测为浸渍,例如pH01003771G0070,pH01000906G0020,pH01000967G0270等,表明它们不仅与热应力相互作用,而且也是源于热应力,也可以助长ROS信号感应。 此外,ROS信令事件也与CA相关联2+和加利福尼亚州2+结合蛋白(24那25,如钙调素。在0.5H和8H检测到钙调素上调,且0.5H的上调幅度大于8H。此外,Ca2+在0.5H内发现转运蛋白PH01000251G0960表达上调。结合之前对氧化还原敏感的HSF和Ca的研究结果2+,它们的信号可能出现在高光诱导的初步阶段,其中一些转运体可能参与了竹叶ROS信号转导。 作为重要的ROS感测之一,先前报道了丝氨酸/苏氨酸蛋白激酶(OXI1)[26那27[在与CA相关的丝裂原激活蛋白激酶(MAPK)3和6的激活中发挥了核心作用2+.本研究在0.5H和8H中发现了上调的ox1基因,如PH01000015G0230、PH01000016G0280和PH01001215G0410,提示ox1可能在强光下竹子的ROS信号传递中起关键作用。MAPK3/6调控ROS胁迫下不同防御机制相关的不同转录因子的激活,DEG输出中未加入MAPK3/6,但MAPK3/6的FPKM在0.5H和8H表达量较高,且在0.5H出现最大表达量。这可能与强光处理早期MAPK3/6信号增强有关。综上所述,作为ROS信号转导的重要网络,包括对氧化还原敏感的HSF、Ca2+, ox1, MAPK3/6和一些转录因子,这条通路(图。7.)在强光下被激活,在初始阶段出现峰值信号。另一种ROS信号途径是,ROS抑制磷酸酶,然后抑制磷酸酶促进ox1和MAPK3/6的表达[28].随后,MAPK3 / 6激活了许多TFS参与ROS-Scavening。一些下调的磷酸酶基因浓缩,例如脂质磷酸酶基因(pH01000297G0870),具有超家族磷酸酶基因(pH01001136G0170)和磷酸盐转运蛋白基因(pH01000381G0230)。因此,ROS信号途径中的磷酸酶可能在ROS信号在高光处理中在ROS信号中发挥相当大的作用。 竹子活性氧(ROS)途径的广义模型。在光反应中,大量的强光(HL)产生了过量的激发能。一些高能量可能转移到氧,从而产生有毒的ROS。ROS可以通过氧化还原敏感转录因子的机制来检测。磷脂酸和钙2+激活丝氨酸/苏氨酸蛋白激酶(OXI1)。然后,氧气的活化活化激活丝裂原激活蛋白激酶(MAPK)级联(MAPK3 / 6),这些诱导或活化的短/中期反应转录因子调节ROS-清除和相关途径。在ROS-清除,主要ROS酶,反应方程和反应位置在MOSO竹中列出。缩写:HL,高光;Psii,Photosystem II;PSI,PERSICYSTEM I;chl,叶绿素;PC,Plastocyanin;cyt,细胞色素;PQ,塑性醌; 3PGA, 3-phosphoglycerate; RuBP, ribulose-1,5-biphosphate; ROS, reactive oxygen species; SOD, superoxide dismutase; APX, ascorbate peroxidase; MDAR, monodehydroascorbate reductase; GR, glutathione reductase; Cat, catalase; GPX, glutathione peroxidase; AOX, alternative oxidase; PrxR, peroxiredoxin; Trx, thioredoxins; GLR, glutaredoxin; chl, chloroplast; cyt, cytosol; mem, membrane; mit, mitochondria; nuc, nuclei; per, peroxisomes 为了保护细胞并在高光下维持生长,竹子通过发育,生理和生化方式对其环境的不利变化作出反应。这些反应需要响应于轻应激表达的一些基因,这些基因由转录因子网络调节(TFS)[23].在ROS信号网络中,转录因子通过调控基因表达,在应答强光胁迫中发挥关键作用,并通过调控转录因子与ROS结合独联体- 目标基因启动子中存在的元素。 以往的研究表明,许多转录因子可能参与了强光胁迫下的ROS信号网络。首先,HSF作为热休克反应的关键调控因子之一,上调热休克蛋白(HSPs) [29].HSP不仅可以在正常情况下激活和表达,例如细胞生长和发育,还可以由一些应力诱导,例如热休克,感染和重金属[30.].其次,NAC与类黄酮生物合成相关基因的诱导有关,导致花青素在强光胁迫下的积累[31.-41.].第三,MYB在气孔和非气孔响应中发挥重要作用,分别通过调节气孔数量和大小和代谢组分来调节光合作用和相关代谢[42.那43.].第四,AP2 / ERF是一个大型植物特异性TF系列,其调节非生物应激响应基因的表达。最后,作为植物特异性TFS之一,Wrky含有植物中的一个大型监管蛋白质[44.-46.]参与各种生物应激反应和几个发育和生理过程[47.-52.].一些WRKYsA. Thaliana.由h明显增强2O.2,是一种特异性ROS [53.-60.].这些指示的包装可能在氧化应激下进行重要作用。 因此,结合前人的研究和RNA-Seq数据,结果表明,HSF、MYB、bZIP、AR2/ERF、NAC、WRKY等许多竹节tf可能也参与了强光下的ROS信号网络(表)3.)响应于高光,在光合作用过程中调节,适应和调节基因表达的关键作用。此外,基于表达数据和频率的分析,NAC,WRKY,AR2 / ERF和BHLH的TFS可能在短期(0.5h)中满足重要的作用,而C2H2,HSF,BZIP和MYB可能在短期(0.5h)和中期(8H)中的重要角色响应高光。聚类亲和搜索显示三个样本中表达基因的动态变化
分析三个样本的差异表达基因
竹子LHC蛋白家族的鉴定与分析
竹材中活性氧相关基因
TFs在调节ROS中的潜在作用
结论
基于深度测序技术的毛竹叶片基因表达谱和大规模阶段特异性转录组谱的研究,为深入了解毛竹叶片对强光响应的基因和基因调控提供了更准确的视角。共鉴定出1293个差异表达基因,细化了47个毛竹LHC蛋白超家族成员的基因注释。此外,还检测了ROS的信号转导和清除途径。同时鉴定出171个参与ros清除的基因。此外,还发现了一些重要的表达基因和转录因子,它们在强光下的不同调控过程中发挥着重要作用。这些结果可能为进一步研究光胁迫相关蛋白的功能提供了重要的实验资源,并拓展了我们对竹叶光胁迫机制的认识。
方法
植物材料和高光处理
毛竹竹(植被类型在25℃、光照强度为200 μmol·m的长日照条件下(光照16 h /暗8 h),在室内盆栽-2·年代-1.空气相对湿度约为50%。在强光胁迫下,将1年生幼苗从正常光照条件(200 μmol·m)移出-2·年代-1)高光(1200μmol·m-2·年代-1)由凉爽的白色荧光管提供。选择幼苗顶部的第三片叶片分别为0小时,0.5h,1 h,2 h,4 h,8 h和12h高的光处理测量叶绿素荧光参数。
测量叶绿素荧光参数
体内采用Dual PAM-100荧光仪(Walz, Effeltrich, Germany)测定毛竹1年生幼苗叶片的叶绿素荧光参数。计算了PSII的最大量子产率FV./Fm= (Fm-FO.)/FmNPQ的非光化学猝灭计算为(Fm-Fm')/Fm”(10.),FO.是适应黑暗状态下的最小荧光值,Fm和Fm'分别是在饱和光的脉冲(0.6秒)照射时的黑暗适应和光适应的最大荧光。FO.和Fm在20分钟的暗方适应后确定。每次治疗10个重复测量每个参数。使用SPSS软件统计分析所有数据。
RNA分离,cDNA文库结构和RNA测序
在上述材料中,3个样品的毛竹叶片在强光(1200 μmol·m)照射下-2·年代-1)对于0小时(CK),分别收集0.5小时(0.5h)和8小时(8h)。从基因上的至少三个随机选择的竹子中收集每个样品,并且混合束在液氮中迅速冷冻以进行RNA分离。根据制造商的说明,使用Trizol试剂溶液(Invitrogen,Carsbad,CA)从所有选定的竹组织样品中分离出总RNA。将提取的RNA在37℃下用RNase的DNase I处理30分钟以除去残留的DNA。使用Nanodrop 2000分光光度计检测RNA的质量和量。用逆转录系统(USA)进行逆转录(USA)[61.].如前所述进行cDNA文库构建和归一化[62.].然后用Illumina HiSeq对聚合库进行测序TM值2000平台(Illumina,San Diego,CA,USA)。
生物信息学分析
首先,利用Trimmomatic对适配器序列和低质量序列进行裁剪[62.].其次,为了准确对齐清洁到参考竹基因组并探索未爆发的基因,插入cDNA文库的大小和德诺维由Trinity软件组装干净读取[63.].然后从竹基因组数据库下载毛竹基因组序列和注释(版本1)作为参考基因组。www.bamboogdb.org.)[11.].使用TOPHAT2将过滤序列映射到参考竹基因组[64.].随后,对齐后的读文件由Cufflinks处理[65.].reads被组装到转录本后,利用基因外显子序列中每千碱基的reads数量(每百万reads)来估计和标准化它们的丰度[66.].在功能和结构注释分析中,使用ontology进行GO富集[67.].
RNA-SEQ数据的底漆设计和验证
使用Primer3自动设计用于每个独特基因的侧翼序列的引物对(附加文件10.).所有引物在进行实时定量PCR (qRT-PCR)前均用日本TaKaRa公司的rTaq检测。采用Roche LightCycler 480 SYBR Green I Master Kit在Qtower (analyticjena, Germany)上进行qRT-PCR反应。反应体积为10 μL,含5.0 μL 2 × SYBR Green I Master Mix、0.8 μL cDNA、0.2 μL正向引物和反向引物各5 μM、3.8 μL ddH2O.重复所有反应三次。QRT-PCR方法由95℃组成10分钟,50个循环为95℃,10s,60℃。对于每种条件,QRT-PCR实验是生物三份酸盐。用2计算相对基因表达水平-△△CT.方法(68.)使用“挪威通讯社”星期六报导作为参考基因[69.].
加入号码
本文中三个样本的所有序列数据都保存在NCBI数据库的Short Read Archive (SRA)中,登录号如下:SRR2035212、SRR2035263和SRR2035327。
缩写
- APX型:
-
抗坏血酸盐过氧化物酶
- 爆炸:
-
基本的局部对齐搜索工具
- 演员:
-
聚类亲和搜索技术
- 猫:
-
催化剂
- 度:
-
差异表达基因
- elips:
-
早期light-inducible蛋白质
- FPKM:
-
每千碱基的基因片段每百万定位片段
- 去:
-
基因本体论
- GPX:
-
谷胱甘肽过氧化物酶
- HSF:
-
热应激转录因子
- KEGG:
-
Kyoto基因和基因组的百科全书
- LHC:
-
聚光叶绿素a / b-binding
- MAPK:
-
mitogen-activated-protein激酶
- NPQ:
-
non-photochemical淬火
- 形成:
-
单螺旋光诱导蛋白
- 公安局:
-
Photosystem II亚基S.
- QRT-PCR:
-
定量实时PCR
- RNA-SEQ:
-
RNA测序
- ROS:
-
活性氧
- SEPs:
-
应激增强蛋白质
- SOD:
-
超氧化物歧化酶
- TF:
-
转录因子
参考文献
- 1。
周G,吴九,江普。不同管理模型对Phyllostachys Pubescens森林碳储存的影响。J北京林业UNI(中文)。2006; 28(6):51。
- 2.
刘春华,刘志强,杨晨。叶绿素a/b配合物对叶绿素荧光特性的影响。Photosynthetica。2012;50(1):129 - 38。
- 3.
测序技术——下一代。中国科学(d辑:地球科学)2010;11(1):31-46
- 4.
舒斯特SC。下一代测序变换了今天的生物学。NAT方法。2008; 5(1):16-8。
- 5。
彭志鹏,卢勇,李磊,赵强,冯强,高志,等。快速生长的非用材林物种毛竹(Phyllostachys杂环).NAT Genet。2013; 45(4):456-61。
- 6。
彭志鹏,陆涛,李林,刘旭,高志,胡涛,等。基于10608个推测的全长cDNA序列,对最大的草、竹子的全基因组特征进行了分析。BMC Plant Biol. 2010;10:116。
- 7。
高志明,李春林,彭志忠。马竹幼叶归一化cDNA文库表达序列标签的生成与分析麻latiflorus Munro).植物细胞批准。2011; 30(11):2045-57。
- 8。
高军,张勇,张超,齐飞,李旭,穆胜,等。毛竹花部转录组特征(植被类型)通过转录组测序和RNA-SEQ分析的不同开花发育阶段。Plos一个。2014; 9(6),E98910。
- 9.
彭震,张超,张勇,胡涛,穆胜,李旭,等。毛竹速生苗的转录组测序与分析(植被类型).公共科学图书馆。2013;8(11),e78944。
- 10。
麦克斯韦·K,约翰逊叶绿素荧光——实用指南。acta botanica yunshan(云南植物研究)2000;51(345):659-68。
- 11.
赵H,彭Z,Fei B,Li L,Hu T,Gao Z等。Bamboogdb:具有功能性注释和分析平台的竹基因组数据库。数据库(牛津)。2014; 2014:BAU006。
- 12.
李建平,梁伟,李军,等。TM4:一个用于微阵列数据管理和分析的免费、开源系统。生物学技术。2003;34(2):374 - 8。
- 13.
程永昌,陈永明。光合作用的光收获动力学。化学学报。2009;60:241-62。
- 14。
Engelken J,Brinkmann H,Adamska I.扩展LHC的分类分布和起源(光收获复合体)天线蛋白超家族。BMC EVOL BIOL。2010; 10:233。
- 15.
绿色br。是“分子机会主义”的一个因素在不同光合灯收获颜料系统的演变?Proc Natl Acad Sci U S A A. 2001; 98(5):2119-21。
- 16。
苏维尔P.全基因组分析叶绿素A / B结合蛋白的叶绿素A / B系列拟南芥和米饭。植物信号学报。2010;5(12):1537-42。
- 17。
他,崔克,张jg,段ag,zeng yf。基于下一代测序的mRNA和MicroRNA表达分析分析显示涉及在莫斯竹中发育秆的快速生长的途径。BMC植物BIOL。2013; 13:119。
- 18。
Montané M-H, Kloppstech K.光捕获相关蛋白家族(lhc, ELIPs, HLIPs):捕获光是它们的主要功能吗?基因。2000;258(1):1 - 8。
- 19.
原核生物和真核生物类囊体膜中应激蛋白的Elip家族。:对光合作用的调节.施普林格》2001。p . 487 - 505。
- 20.
黄志强,王志强,王志强,等。植物叶绿素a/b结合蛋白的进化与调控。中国科学(d辑:地球科学)1995;92(2):636-40。
- 21.
李晓平,Björkman O,史志强,Grossman AR, Rosenquist M, Jansson S,等。一种色素结合蛋白,对调节光合作用的光收获至关重要。大自然。2000;403(6768):391 - 5。
- 22。
王志强,王志强,王志强。青藏高原生物多样性研究进展。植物生理学杂志。2015;72:13 - 32。
- 23。
陈志强,陈志强,陈志强,等。环境胁迫下植物光合及相关代谢的转录因子及其调控。安机器人。2009;103(4):609 - 23所示。
- 24.
Bowler C,Fluhr R.钙和活性氧的作用作为控制交通的信号。趋势植物SCI。2000; 5(6):241-6。
- 25.
骑士H,骑士先生。非生物应激信号通路:特异性和串扰。趋势植物SCI。2001; 6(6):262-7。
- 26。
植物胁迫信号转导中的MAP激酶途径。植物科学进展。2005;10(7):339-46。
- 27。
Wang H,Ngwenyama N,Liu Y,Walker JC,张S.气孔发育和图案化由环境反应丝裂解性蛋白激酶进行调节拟南芥.植物细胞。2007; 19(1):63-73。
- 28。
李志刚,李志刚,李志刚。植物活性氧基因网络的研究进展。植物科学进展。2004;9(10):490-8。
- 29。
植物热胁迫转录因子(Hsf)家族的结构、功能和进化。生物物理学报。2012;1819(2):104-19。
- 30.
Westerheide SD,Raynes R,Powell C,Xue B,Uversky VN。HSF转录因子家庭,热休克反应和蛋白质内在病症。Curr蛋白Pept Sci。2012; 13(1):86-103。
- 31.
龚伟,沈永平,马立国,潘勇,杜玉龙,王东辉,等。全基因组ORFeome的克隆与分析拟南芥转录因子基因。植物理性。2004; 135(2):773-82。
- 32.
Souer E,Van Houwelingen A,Kloos D,Mol J,Koes R.在胚胎和花中的图案形成需要喇叭花的无顶部分泌基因,并在分生和原始界限中表达。细胞。1996年; 85(2):159-70。
- 33.
关键词:子叶分生组织,子叶细胞,边缘分生组织,子叶分生组织拟南芥.植物细胞。2003; 15(7):1563-77。
- 34。
谢强。拟南芥NAC1在TIR1下游转导生长素信号,促进侧根发育。基因Dev。2000;14(23):3024 - 36。
- 35。
陈兰、中岛康、佐久间、辛普森、藤田康、丸山康等。的分离和功能分析拟南芥干旱胁迫诱导的NAC转录因子独联体-对脱水胁迫的早期反应元素植物细胞。2004;16(9):2481 - 98。
- 36。
Fujita M,Fujita Y,Maruyama K,Seki M,Hiratsu K,Ohme-Takagi M,等。脱水诱导的NAC蛋白RD26参与新的ABA依赖性应力信号通路。工厂J. 2004; 39(6):863-76。
- 37.
Aida M, Ishida T, Fukaki H, Fujisawa H, Tasaka M.参与器官分离的基因拟南芥:杯形子叶突变体的分析。植物细胞。1997年; 9(6):841-57。
- 38。
熊勇,刘涛,田超,孙树华,李军,陈明。水稻单子叶和双子叶转录因子的基因组比较分析。植物学报。2005;59(1):191-203。
- 39。
Morita Y,Saitoh M,Hoshino A,Nitasaka E,Iida S. CDNA分离用于R2R3-MYB,BHLH和WDR转录调节因子和CA和CA衰变的识别日本牵牛花中的白花。植物细胞生理。2006; 47(4):457-70。
- 40.
Feild Ts,Lee DW,Holbrook NM。为什么叶子在秋天变红。花青素在红色奥西尔山茱萸的叶片中的作用。植物理性。2001; 127(2):566-74。
- 41.
Morishita T, Kojima Y, Maruta T, Nishizawa-Yokoi A, Yabuta, Shigeoka S。拟南芥NAC转录因子ANAC078调控强光下类黄酮的生物合成。植物生理学报。2009;50(12):2210-22。
- 42.
辛格k,foley rc,onate-sanchez l.植物防御和压力反应中的转录因子。CurrOp植物BIOL。2002; 5(5):430-6。
- 43.
友敌:拮抗bHLH/bZIP转录因子整合光和活性氧信号拟南芥.植物细胞。2013;25(5):1483。
- 44.
Weigel D. Apetala2结构域与新型DNA结合结构域有关。植物细胞。1995年; 7(4):388。
- 45.
Shigyo M, Hasebe M, Ito M. AP2亚家族的分子进化。基因。2006;366(2):256 - 65。
- 46。
从内切酶到转录因子:植物AP2 DNA结合域的进化。植物细胞。2004;16(9):2265 - 77。
- 47。
植物对非生物胁迫响应的基因调控。生物物理学报。2012;1819(2):85。
- 48。
陈我,宋y,li s,张l,zou c,yu d。腕骨转录因子在植物非生物应激中的作用。Biochim Biophys Acta。2012; 1819(2):120-8。
- 49.
eulgem t,rushton pj,Robatzek S,Somssish Ie。植物转录因子的腕骨超家族。趋势植物SCI。2000; 5(5):199-206。
- 50.
透明的TESTA GLABRA2,一种毛状体和种皮发育基因拟南芥,编码腕表转录因子。植物细胞。2002; 14(6):1359-75。
- 51.
Lagace M, Matton DP。WRKY转录因子在鱼类晚期胚胎中的表达特征茄属植物chacoense.足底。2004;219(1):185 - 9。
- 52.
Pandey SP, somsich IE。WRKY转录因子在植物免疫中的作用。植物杂志。2009;150(4):1648 - 55。
- 53.
黄芪多糖的拮抗作用拟南芥WRKY53和ESR / ESP在叶片衰老中被茉莉和水杨酸平衡调节。植物细胞。2007; 19(3):819-30。
- 54.
周x,江y,yu d. wrky22转录因子介导黑暗诱导的叶片衰老拟南芥.摩尔细胞。2011;31(4):303 - 13所示。
- 55.
陈磊,张磊,于东。损伤诱导的WRKY8参与机体基础防御拟南芥.Mol植物微生物相互作用。2010; 23(5):558-65。
- 56.
Vanderauwera S, Zimmermann P, Rombauts S, Vandenabeele S, Langebartels C, Gruissem W,等。过氧化氢调控基因表达的全基因组分析拟南芥揭示了一个参与花青素生物合成的高光诱导转录簇。植物杂志。2005;139(2):806 - 21所示。
- 57.
Rizhsky L,Davletova S,Liang H,Mittlle R.氧化溶解酶的氧化溶解酶1表达需要锌手指蛋白Zat12.拟南芥.中国生物化学杂志。2004;27(12):11736-43。
- 58。
Davletova S,Schlauch K,Coutu J,Mitture R.锌 - 手指蛋白Zat12在反应性氧和非生物应力信号中起着核心作用拟南芥.植物理性。2005; 139(2):847-56。
- 59。
肖华,唐军,李勇,王伟,李昕,金磊,等。无雄蕊1,编码单个C2H2锌指蛋白,调节水稻花器官的特性。植物j . 2009; 59(5): 789 - 801。
- 60。
王y,dou d,wang x,李a,胜y,hua c等。这PsCZF1编码c的基因2H2锌指蛋白是植物生长发育和发病所必需的疫霉突变.活细胞Pathog。2009;47(2):78 - 86。
- 61.
尼古丁通过上调XIAP和survivin抑制化疗药物诱导的细胞凋亡。中国科学院院刊2006;103(16):6332-7。
- 62.
Severin AJ, Woody JL, Bolon YT, Joseph B, Diers BW, Farmer AD等。Glycine max的RNA-Seq图谱:大豆转录组的指南。BMC Plant Biol. 2010;10:160。
- 63.
Haas BJ, Papanicolaou A, Yassour M, Grabherr M, Blood PD, Bowden J,等。新创利用Trinity平台从RNA-seq中重建转录本序列,进行参考文献的生成和分析。Nat Protoc。2013;8(8):1494 - 512。
- 64.
Trapnell C, Pachter L, Salzberg SL. TopHat:用RNA-Seq发现剪接连接。生物信息学,2009,25(9):1105 - 11所示。
- 65.
Trapnell C,Roberts A,Goff L,Pertea G,Kim D,Kelley Dr,等。TOPHAT和袖扣RNA-SEQ实验的差异基因和转录物表达分析。NAT PROTOC。2012; 7(3):562-78。
- 66.
Mortazavi A,Williams Ba,McCue K,Schaeffer L,Wold B.用RNA-SEQ进行测绘和量化哺乳动物转录om。NAT方法。2008; 5(7):621-8。
- 67.
Bauer S,Grossmann S,Vingron M,Robinson Pn。Ontologizer 2.0 - 用于转入富集分析和数据探索的多功能工具。生物信息学。2008; 24(14):1650-1。
- 68.
Livak KJ, Schmittgen TD。使用实时定量PCR和2−ΔΔCT方法分析相关基因表达数据。方法。2001;25(4):402 - 8。
- 69.
关键词:竹子,实时荧光定量PCR,内参基因植被类型).公共科学图书馆。2013;8(2),e56573。
资金
基金资助:国家“十二五”科技支撑计划子项目(No. 20141201);项目编号:2015BAD04B03, 2015BAD04B01);国家自然科学基金资助项目(1632015008);31400557和31370588]。
作者信息
从属关系
相应的作者
额外的信息
利益争夺
提交人声明他们没有竞争利益。
作者的贡献
HSZ设计了实验,进行了主要的生物信息学分析,起草了手稿。YFL设计并完成了叶绿素荧光参数的测量。HYS参与了本次研究的设计。LCL通过实时荧光定量PCR进行验证实验。LLW进行了统计分析。LLD进行图形装配。ZMG设计了工作台验证,修改了原稿。所有作者阅读并批准了最终的手稿。
附加文件
额外的文件1:
从莫斯竹子隔绝的差动样本用于RNA-SEQ分析。(XLSX 10 KB)
额外的文件2:
RNA-Seq和qRT-PCR在筛选出的17个基因中的相对表达量。(XLSX 12 kb)
额外的文件3:
维恩图中FPKM≥1的表达基因列表。(XLSX 289 KB)
额外的文件4:
样品中基因表达值的分布。(XLSX 10 KB)
额外的文件5:
样本内显著氧化石墨烯项。(XLSX 20 KB)
附加文件6:
基于聚类亲和搜索技术的五组基因列表和重要的GO术语。(XLSX 293 kb)
额外的文件7:
三个样本中差异表达基因的列表。(XLSX 135 kb)
附加文件8:
摩尔竹中活性氧物种清除的基因及表达。(XLSX 29 kb)
附加文件9:
库尔循环循环中基因表达的值和光致血管代谢。(XLSX 12 kb)
附加文件10:
从毛竹中筛选出17个基因,利用qRT-PCR引物。(XLSX 11 KB)
权利和权限
开放获取本文根据创意公约署署署的条款分发了4.0国际许可证(http://creativecommons.org/licenses/by/4.0/),它允许在任何媒体上无限制地使用、分发和复制,前提是你给予原作者和来源适当的荣誉,提供一个到知识共享许可协议的链接,并指出是否作出了更改。创作共用及公共领域专用豁免书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条提供的数据,除非另有说明。
关于这篇文章
引用这篇文章
赵慧,娄烨,孙慧。等等。转录组和比较基因表达分析植被类型响应高光线。BMC植物BIOL.16,34(2016)。https://doi.org/10.1186/s12870-016-0720-9
收到了:
公认:
发表:
关键词
- 毛竹竹
- RNA-Seq
- 光合作用
- 基因表达
- 转录因素