摘要
背景
单根纤维强度是影响棉纤维成纱强度的重要质量指标。由于难以可靠地测量单个棉纤维的强度,纤维强度通常从纤维束中测量。然而,纤维束强度(BFS)并不总是与纱线强度相关,因为除了单个纤维强度外,它还受到纤维束内纤维-纤维相互作用中涉及的多种纤维特性的影响。调控单个纤维强度的分子机制仍然未知。陆地棉近等基因系(NILs), MD52ne和MD90ne显示BFS的变化,为剖析涉及个体纤维强度的调节机制提供了机会。
结果
对NILs的综合纤维性能分析表明,MD52ne纤维优越的束强主要来自于较高的单个纤维强度,而较大的纤维长度对纤维强度的贡献较小。对NILs的转录组比较分析表明,MD52ne纤维束强度的优势可能与两条信号通路有关:一条是乙烯和参与棉纤维伸长的相互连接的植物激素通路,另一条是参与维持细胞壁完整性的受体样激酶(RLKs)信号通路。多个RLKs在MD52ne纤维中差异表达,并定位于包括强度数量性状位点(qtl)的基因组区域。在MD52ne纤维中,随着次生细胞壁的产生,若干参与晶体纤维素组装的候选基因也被上调。
结论
比较表型和转录组分析显示MD52ne和MD90ne发育纤维中涉及晶体纤维素组装、乙烯和RLK信号通路的基因表达差异。乙烯及其植物激素网络可能促进MD52ne纤维的伸长,并通过潜在地改善纤维与纤维的相互作用间接促进束强度。在其他植物中介导细胞伸长和SCW生物合成协调的RLKs可能是调控棉纤维细胞壁组装和强度的候选基因。
背景
棉(Gossypium纤维是纺织工业中最重要的天然纤维[1].物理性质,如强度、长度、成熟度(厚度)和细度,决定了棉纤维及其纺成纱的价值和质量。随着现代高速纺纱机械的出现,它以经济有效的方式生产出高质量的纱线,在竞争激烈的全球纺织市场上,对更强纤维的需求增加了。在过去的20年里,美国棉花的纤维强度通过育种逐渐提高[2],然而,由于我们对纤维强度发展的知识有限,改进的速度受到了限制。
棉花生产商和加工商通常通过由数千根单独纤维组成的一束纤维来测量纤维强度。强度只是指折断纤维所需的力[1,3.].束纤维强度(BFS),也称为纤维强度,是由自动化大容量仪器(HVI)测量的,该仪器旨在高效快速地测量棉纤维的市场价值。目前,美国农业部(USDA)的农业营销服务局(AMS)根据HVI测量的BFS值,将棉纤维分为从最低(23.0 g/tex或以下)到最高(31.0 g/tex或以上)的不同等级。一种stelometer用于测量相对少量纤维的BFS值[1,3.- - - - - -5].由于一个纤维束内纤维之间的内在可变性,相同重量的两个纤维束的纤维数量不相同。因此,实际BFS以克/tex (g/tex)为单位,其中破碎力(g)由线性密度或细度(tex = g/km)标准化。因此,通过增加破碎力(g)或降低细度值(tex)可获得较高的BFS (g/ tex)。
棉花工业一直使用HVI和高级纤维信息系统(AFIS)确定的纤维特性作为预测纱线质量的参数,并选择正确的原棉材料来生产不同质量的纱线。然而,一些纺织论文报道了棉纤维的BFS数据不足以预测纱线强度,因为棉花BFS与纱线强度之间的相关性不显著[4,6,7].BFS值受固有纤维强度和其他影响纤维束内纤维间相互作用的纤维特性的调节[1,3.,4,8- - - - - -10].促进纤维束内纤维相互作用的纤维长度值会影响BFS值[11].与纤维厚度相关的特性,包括马克隆值(MIC)、成熟度比(MR)和细度值(tex),也影响棉纤维束的强度,因为它们决定了纤维束中单个纤维的数量[9].
固有纤维断裂力值与纱线强度相关,可通过Mantis或Favimat仪器从单个纤维中测量[1,3.,8,9,11].从几百根单个纤维中获得的平均断裂力(cN)不受其他束状纤维性能的影响,据报道是决定由这些纤维纺成的纱线强度的最重要因素之一[4,12,13].尽管对单个纤维的特性很有用,但需要费力处理的Mantis和Favimat仪器以前还没有用于棉花遗传学和基因组学研究。
陆地棉通过回交育种获得了NILs、MD52ne和MD90ne种质[14].MD90ne是循环父结点,MD52ne是BC结点6high-BFS选择。MD52ne的BFS值比NIL高10%,短纤维减少22%,纤维长度增加7%,MD90ne [15].MD52ne较强的BFS性状可能由少数(≤2个)基因控制[15].利用棉花表达序列标签(ESTs)开发的棉花寡核苷酸芯片原型[16],我们之前观察到MD52ne纤维从纤维伸长过渡到次生细胞壁(SCW)生物合成的过程中,次级细胞壁(SCW)生物发生基因较MD90ne有短暂性上调[17].另一组研究人员还认为,SCW生物成因相关基因可能有助于纤维强度g .分子携带染色体片段的染色体渐渗系(CSILs)g .取得谁的纤维比它们的亲本更长、更强、更细g .分子TM-1 [18].的g .分子CSILs用于识别潜在的负责纤维长度的基因[19]除了纤维强度外[18].由于影响束内纤维间相互作用的纤维长度和细度可调节棉花NILs的BFS值[17]及CSILs [18],目前尚不清楚SCW生物发生相关基因是否参与调节单个纤维断裂力和/或其他束状纤维特性。事实上,相同的SCW生物发生相关基因被鉴定为差异表达基因(DEGs),可能参与控制纤维长度的分子机制[19]和纤维厚度相关特性[20.,21]除BFS外[17,18].因此,哪些候选基因真正参与了单个纤维断裂力,从而影响了纱线强度,仍有待回答。
在本研究中,我们测量了MD52ne、MD90ne的成熟纤维和发育纤维的纤维性能2使用新方法和传统方法,包括Favimat,横截面图像分析显微镜,衰减全反射傅里叶变换红外光谱(ATR-FTIR), HVI, Stelometer, AFIS和重量细度方法。拉伸纤维性能分析表明,MD52ne纤维的优良断裂力主要来自于较高的单个纤维断裂力,而纤维长度的增加对断裂力的贡献较小。对NILs的转录组比较分析表明,MD52ne纤维的优良BFS可能与乙烯通路导向的纤维伸长和由于受体样激酶(RLK)信号通路的活性而增强的细胞壁完整性有关。
结果
MD52ne和MD90ne成熟纤维束纤维性能的比较
HVI纤维性能分析表明,成熟MD52ne纤维的BFS明显大于在两个地理位置和环境条件有很大差异的单独种植的MD90ne纤维(表2)(19 ~ 25%)1).此外,MD52ne纤维上半段平均长度(UHML)较长(5 ~ 6%)。MD52ne的平均纤维伸长值低于MD90ne,但仅在一处有统计学意义。在两个地区生长的MD52ne和MD90ne之间MIC值无显著差异。
束状纤维强度与其他纤维性能的相关性
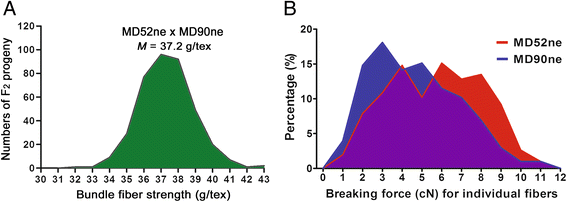
为了确定NILs的BFS值是如何受到纤维-纤维相互作用中涉及的其他物理性质的影响,我们开发了F2由MD52ne和MD90ne杂交获得的384个子代植物群体。在F中2后代的BFS值呈宽范围的高斯分布(31.99和42.66 g/tex)(图。1).HVI和AFIS测定的纤维UHML长度(27.82 ~ 32.48 mm)、伸长率(4.78 ~ 6.45%)、MIC(4.39 ~ 5.78)、成熟度比(0.979 ~ 1.078)和细度(172.0 ~ 215.0 mtex)均呈高斯分布2因此我们能够确定BFS与其他纤维物理性能的相关性。
表格2HVI测定的纤维长度(UHML, mm)和马克隆值(MIC), AFIS测定的成熟度比(MR)和细度(mtex)对NILs的BFS值有影响。相关系数值(r)用皮尔逊的方法[22]显示,BFS值与UHML、MIC、MR、细度呈正相关,而与FE无显著相关。的R2结果表明,BFS方差受UHML影响较小(12.9%),而与纤维厚度相关的特性如MIC(1.2%)、MR(2.9%)和细度(1.2%)影响较小。
成熟MD52n和MD90ne纤维各纤维性能的比较
为了尽量减少其他物理纤维性能对纤维强度的影响,我们首先筛选除BFS值外纤维性能相似的NIL植物。在BFS值有显著差异(24%)的棉花中,我们发现MD52ne和MD90ne的MIC值几乎相同(4.931),这代表了纤维成熟度比和细度的组合。除了HVI外,AFIS测量的纤维性能证实,所选NILs之间的纤维长度有显著差异(5%,UHML),但与纤维厚度相关的性能(MIC, MR和细度)没有显著差异(表2)3.).单根MD52ne纤维的平均断裂力显著大于单根MD90ne纤维的平均断裂力(22.4%)3.).从断裂力分布曲线可以看出,各空纤维中单根纤维的断裂力变化较大,MD52ne单根纤维(0.93 ~ 11.25 cN)与MD90ne单根纤维(0.62 ~ 11.27 cN)的断裂力分布范围相似。1 b).与MD90ne相比,MD52ne中cN值较高的纤维更强。
研制中的MD52ne和MD90ne纤维性能比较
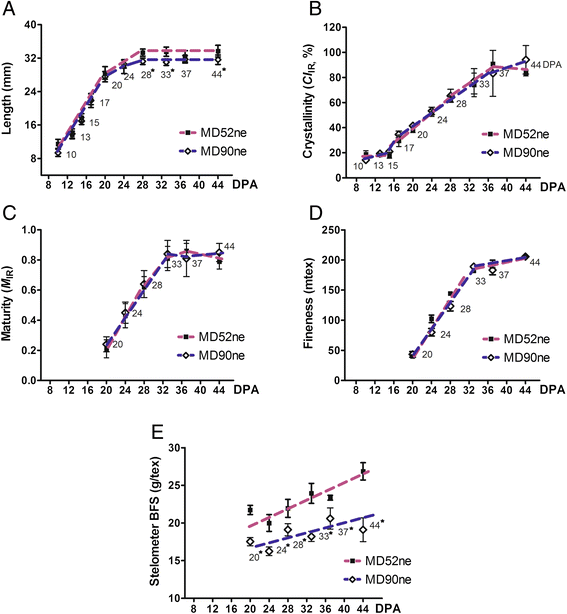
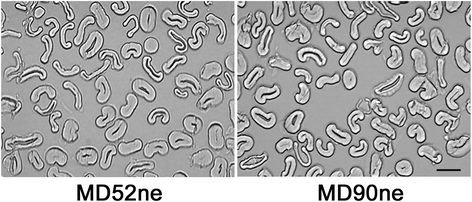
为了确定两种NILs在棉纤维发育过程中发生纤维性能变化的时间,我们测量了10个不同发育时间点(10、13、15、17、20、24、28、33、37和44 DPA)发育纤维的物理性能,涵盖整个发育阶段(图。2).主动伸长MD52ne和MD90ne纤维的生长速率在20dpa时下降(图2)。2).统计分析t结果表明,NILs之间小于24dpa的发育纤维的平均长度没有显著差异。28 DPA及以上发育MD52ne纤维的平均纤维长度显著延长(p值,0.0012)高于相应时间点显影MD90ne纤维。在15 DPA左右,纤维进入了一个过渡阶段,同时伴有SCW纤维素生物合成和纤维伸长(图2)。2 b).利用ATR-FTIR光谱及其相应算法对显影MD52ne和MD90ne纤维的结晶度进行了测量[23,24].比较图显示结晶度低(CI红外)在10 ~ 15 DPA之间。的CI红外值迅速增加至17 DPA,在37 DPA时达到峰值(图2)。2 b).观察结果表明,在10、13和15 DPA发育的纤维主要由低结晶度的原代细胞壁(PCW)组成,从延伸到SCW生物合成的转变发生在15到17 DPA。结晶度高的SCW沉积在两个NILs的显影纤维上,直到37dpa。差异无统计学意义CI红外在整个发育阶段,两个NILs之间的发育纤维的值(图。2 b).铃完全发育,在大约42 DPA时开始开铃。成熟纤维在44 DPA下开裂。纤维成熟率或壁厚度(米红外)还通过ATR-FTIR光谱对MD52ne和MD90ne纤维进行了评估。2摄氏度) [23,24].在17 DPA及以下的发育纤维中,SCW纤维素含量很少,而SCW纤维素是纤维成熟的主要原因[25].的米红外结果表明,在20 DPA及以上的发育纤维由SCW纤维素组成。在两种NIL纤维的SCW生物合成阶段(20 - 33dpa),均能得到较好的效果米红外值同样增加(图;2摄氏度).完全成熟的MD 52ne和90ne纤维的横切面图像及其计算的MR显示了NILs之间的相似性(图2)。3.).从20 DPA到44 DPA, MD52ne纤维的细度值(40.0到205.6 mtex)的增加模式与MD90ne纤维的细度值(43.3到205.6 mtex)在相应时间点几乎相同(图。二维).MD52ne纤维在20 DPA及以上时发育显著(p-value < 0.0008)比在相应dpa处显影的MD90ne纤维更强(图。2 e).当显影纤维达到20 DPA时,MD52ne (21.7 g/tex)和MD90ne (17.5 g/tex)的BFS差异明显。用直径计测量显影纤维束强度,其所需纤维量比HVI少。无论是stelometer还是HVI都不能测量小于20dpa的发育纤维的BFS值,因为含糖和粘性的发育纤维不能个体化。
研制MD52ne和MD90ne纤维性能的比较。在9个不同发育时间点(10、13、15、17、20、24、28、33和37 DPA)发育的纤维和44 DPA完全发育的纤维收集自2013年在洛杉矶新奥尔良的复制田中并排生长的NILs。时间点旁边的星号表示统计显著性。一个纤维长度。计算了30个重复不同dpa下发丝纤维的平均长度。b结晶度。平均结晶度(CI红外)从6个重复的ATR-FTIR光谱中确定。c成熟。平均纤维成熟度(米红外)采用ATR-FTIR从6个重复中测定。d细度。300根长度为15毫米的纤维用于重量细度分析的每个重复。计算3个重复的平均细度值。e束纤维强度。用Stelometer测量了三个重复的显影纤维束的平均强度
通过RNA-seq分析MD52ne和MD90ne之间发育纤维的转录组
为了研究MD52ne优于MD90ne的纤维强度的分子基础,采用MD52ne和MD90ne之间发育纤维中提取的总rna进行全基因组比较转录组分析。根据从开发纤维中获得的纤维性能数据(图。2),在两个不同的发育时间点,15个DPA主要含有PCW, 20个DPA同时含有PCW和SCW,在两个生物重复的NILs之间进行比较。
通过Illumina配对测序获得的每个库的平均原始reads数在32.80 ~ 33.49,000,000 reads之间4).在两个时间点上,MD52ne的平均原始读取数略高于MD90ne。在原始reads中,每个文库80.83 - 84.35%的reads被映射到草图基因组中的注释蛋白编码基因g .,TM-1 [26].在陆地棉基因组中,四个文库共绘制了61263个基因的图谱1).表达基因用拟南芥Tair 10同源基因进行注释。每个文库的reads per kilo-base per million reads (RPKM) >1的基因比例为71.61 ~ 79.22%。我们选择RPKM阈值为1,以与之前使用该基因组草案的工作一致[26].
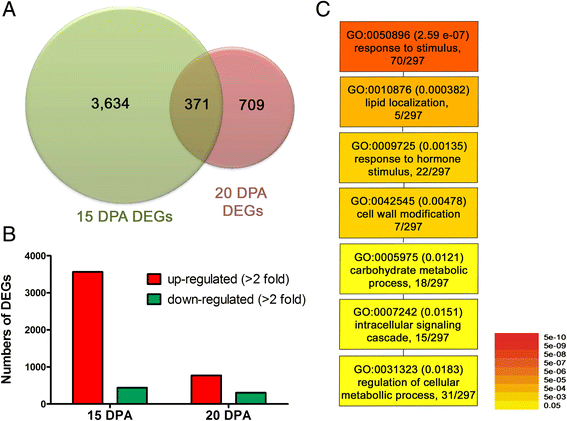
利用各自时间点的RPKM值进一步评估两个NILs之间表达的映射基因。将误发现率(FDR)设置为5%,确定的阈值p价值在多个测试和分析。判断基因表达差异的显著性,进行调整p≤0.05,log的绝对值2以比值≥1为阈值[27].在37675个表达基因中,分别有4005个和1080个独特基因在15和20 DPA时表达显著差异。4,其他文件2而且3.).在4005个差异表达基因中,3565个和440个独特基因在MD52ne中分别在15 DPA时表达上调和下调,而在1080个基因中,774个和306个差异表达基因在MD52ne中分别在20 DPA时表达上调和下调(图。4 b,其他文件4,5,6而且7).
MD52ne纤维中DEGs的注释及基因本体分析
agriGo对标注DEGs的GO富集分析[28]表明,在15和20 DPA时MD52ne纤维发育过程中,参与刺激和植物激素反应、细胞内信号、细胞代谢过程、细胞壁修饰、脂质定位和碳水化合物代谢过程的DEGs通常被识别出来(图2)。4摄氏度和表5).许多受生长素、乙烯和赤霉素(GA)等促生长植物激素调控的转录因子在发育中的MD52ne纤维中差异表达(表2)5).其中,1-氨基环丙烷-1-羧酸合酶6 (ACC6)和1-氨基环丙烷-1-羧酸氧化酶4 (ACO4)是合成乙烯的关键酶,可促进纤维伸长[29,30.),而ein3结合F盒蛋白1(EBF1)参与乙烯信号传导[31]在15和20 DPA上调。GAST1GA促生长酶编码[32]在MD52ne中高度上调。我们还分别使用15和20 DPA的deg进行了氧化石墨烯富集分析(附加文件)8).
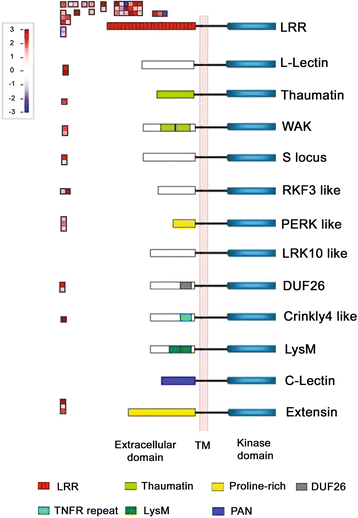
有趣的是,多个受体激酶(RLKs)在MD52ne发育纤维中表达差异于MD90ne。在图中描述的各种类型的rlk中。5其中,富含亮氨酸重复序列(LRR)的RLKs包含三个结构域(LRR配体结合基序、跨膜区域和激酶结构域)。LRR RLKs最近被认为是调节植物细胞壁完整性维护的一种新的信号通路[33]和拟南芥中的纤维素沉积[34,35].一个远程雷达RLK(Gh_D08G0203)是在MD52ne纤维发育过程中,在15 DPA(377倍)和20 DPA(702倍)时表达上调最多的deg之一(附加文件)9).
的微分表达式受体激酶(RLKs)在15 DPA下显影MD52ne纤维。通过MapMan生成不同类别rlk的微分表达式。红色和紫色分别代表上下规则。rlk包含三个结构域,包括胞外结构域、跨膜结构域(TM)和细胞质侧的激酶结构域。c -凝集素,具有凝集素样基序的RLKs;Crinkly4-like,具有Crinkly4-like结构域的rlk;DUF26,未知函数域26;Extensin,含有Extensin motif的RLK;l -凝集素,具有凝集素结合域的RLKs;LRK 10-like, Lr10位点上的RLK基因; LRR, leucine-rich repeats; LysM, RLKs with lysine motif; PERK-like, proline-rich extensin-like kinase; RKF3-like, receptor-like kinase in flowers 3; S-locus, RLK with S-domain; Thaumatin, RLK-like thaumatin protein; WAK, wall-associated kinase
棉花扩增素基因[36,37],果胶甲基酯酶[38],以及木葡聚糖内转葡萄糖酶/水解酶(XET) [39在MD52ne纤维发育过程中,拉伸PCW所需的]均呈上调趋势。五个棒曲霉素(Gh_D13G0786, Gh_A11G2917, Gh_A04G0707, Gh_A12G1619, Gh_A12G1619),三个中外职业s (Gh_A05G1180, Gh_D06G0865和Gh_D07G0145),以及5个XETs (Gh_A03G1432, Gh_D02G1891, Gh_D05G0764, Gh_A11G0768, Gh_D13G0290)在MD52ne纤维中表达量较高(表25).四个Sus(Gh_A07G0665, Gh_A08G1031, Gh_D08G1309, Gh_D11G0438)和参与纤维发育的多种脂质转移蛋白[29,40,41]在积极伸长MD52ne纤维中共表达。
类眼镜蛇蛋白2,其序列与拟南芥相似眼镜蛇式蛋白质拟南芥中纤维素微原纤维定向的研究[42),而几丁质酶/Chitinase-like(气/ CTL),与拟南芥相似CTL2负责拟南芥晶体纤维素含量[43],在MD52ne的SCW期(20 DPA)特异性上调。几种转录因子包括南汽(没有顶端分生组织),bHLH(基本helix-loop-helix),COL5(CONSTANS-like 5),WRKY,锌指家族蛋白在15和20 DPA下MD52ne纤维发育中均有差异表达,而MYB 26而且46种转录因子同源于拟南芥MYB26(AT3G13890)和46(AT5G12870)参与SCW生物合成[44,45]在15 DPA时MD52ne纤维发育中明显上调(表25).
MD52ne纤维中deg的验证
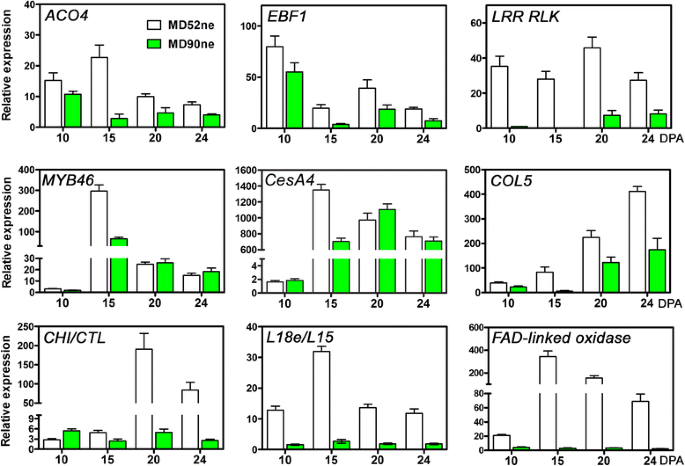
通过实时定量PCR (RT-qPCR)分析两株NILs RNA-seq数据鉴定的DEGs的表达模式。在GO富集分析的基础上,利用发育纤维在10、15、20和24 DPA下的rna进行RT-qPCR,筛选出32个在RNA-seq中表现不同表达模式的deg。通过RT-qPCR和RNA-seq获得的所有32个DEGs的比较转录水平在附加文件中显示10, 9个关键deg的RT-qPCR结果如图所示。6.RT-qPCR和RNA-seq中所有被测DEG的表达模式相同,表明测序和DEG过滤过程的可靠性。
纤维发育过程中与细胞壁活性相关基因的RT-qPCR验证。在4个纤维发育阶段(10、15和24 DPA)进行3次生物复制和3次技术复制,用于RT-qPCR分析。1-氨基环丙烷-1-羧酸氧化酶或乙烯形成酶(Gh_A07G0774);EBF1,ein3结合F盒蛋白1(Gh_A05G0085);远程雷达RLK,富亮氨酸重复受体样激酶(Gh_D08G0203);MBY46转录因子(Gh_A09G1074);纤维素合成酶催化亚基A4(Gh_A08G0421);COL5,CONSTANS喜欢5(Gh_D08G0923);气/ CTL,Basic-Chitinase / Chitinase-like(Gh_D06G0439);L18e/L15,核糖体L18e/L15蛋白(Gh_D02G1619);FAD-linked氧化酶(Gh_D02G1214)
ACO4而且EBF1,它们都参与乙烯信号通路[29,30.],在PCW生物合成(10 DPA)、过渡(15 DPA)和SCW生物合成(20和24 DPA)的各个阶段,MD52ne的表达量均高于MD90ne(图2)。6).在所有发育阶段中最显著的上调是在远程雷达RLK这是细胞壁完整性的一个新的信号通路[33].一个转录因子显示出与拟南芥的序列相似性MYB 46调节纤维素、半纤维素和木质素的生物合成[44,46]在MD52ne中比MD90ne中表达更丰富,特别是在PCW和SCW生物合成之间的过渡阶段(15 DPA)(图。6).一致,c纤维素合酶催化亚基A4(CesA4),参与棉纤维的SCW生物合成[47]显示了相同的表达模式MYB46转录因子.锌指蛋白的表达模式COL5参与细胞代谢过程的MD52ne在所有测试的dpa中也高度丰富。一个气/气(Gh_D06G0479)对其他植物中晶体纤维素含量的影响[43,48]与MD90ne相比,MD52ne中表达高度上调。在活性SCW生物合成阶段(20-24 DPA),转录水平气/气MD52ne纤维比MD90ne纤维高30倍。一个FAD-linked氧化酶和一个核糖体L18e/L15蛋白(L18e /课时)在所有发育阶段MD52ne的表达均高于MD90ne。
在束强度和纤维长度的QTL区域发现了deg
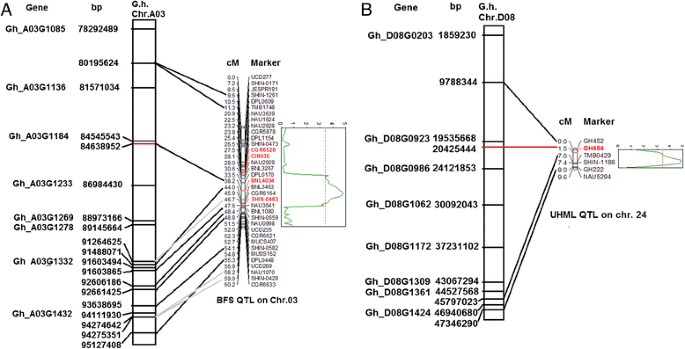
之前,我们使用F - pcr方法鉴定了与BFS和纤维长度相关的稳定数量性状位点(qtl)2MD52ne和MD90ne的杂交衍生的种群[49].与BFS和UHML相关的qtl分别与位于3号染色体(A03)和24号染色体(D08)上的简单序列重复标记BNL4034和GH454连接。我们将QTL区域和deg与植物的物理图谱进行比对g .分子TM-1基因组[26,50].共有75个基因在15和20 DPA的QTL区域差异表达。根据GO分析,在75个DEGs中,有17个基因(BFS QTL中9个DEGs, UHML QTL中8个DEGs)在MD52ne中上调超过2倍,参与细胞壁修饰(附加文件)11).三个远程雷达RLKs,两个NAC转录因子,COL5,MADS-box转录因子,WRKY转录因子参与植物激素和RLK信号通路的QTL均位于QTL区域(图;7).海藻糖-磷酸合酶9、XET9、Sus3和芽蛋白样蛋白参与细胞壁生物合成或细胞壁碳水化合物代谢的QTL位点附近也有发现。两个核糖体L18e/L15蛋白QTL位点也位于染色体A03上。其中,核糖体L18e/L15蛋白(Gh_D02G1619)远程雷达RLK位于D08 QTL附近的(Gh_D08G0203)是在所有发育阶段中表达最多的DEGs(图8)。6).
的物理图中deg的对齐陆地棉TM-1基因组和与束纤维强度(A)和UHML纤维长度(B)相关的QTL区域,MD52ne纤维中相应基因的丰度高于MD90ne。基因图谱位置[49]显示在厘摩(cM)和物理位置显示在碱基对(英国石油公司)。红色标记与qtl连接。一个A03 QTL中的DEGs。Gh_A03G1085 (MADS-box转录因子), Gh_A03G1136 (响应调节器)、Gh_A03G1184及Gh_D02G1619 (核糖体蛋白L18e/L15), Gh_A03G1233 (海藻糖磷酸酶/合成酶), Gh_A03G1269 (远程雷达RLK), Gh_A03G1278 (膜脂蛋白), Gh_A03G1332 (南京83), Gh_A03G1432 (XET 9).bD08 QTL中的DEGs。Gh_D08G0203 (远程雷达RLK), Gh_D08G0923 (COL5), Gh_D08G0986 (远程雷达RLK), Gh_D08G1062 (蛋白激酶), Gh_D08G1172 (南汽), Gh_D08G1309 (Sus 3), Gh_D08G1361 (细菌蛋白喜欢蛋白质10), Gh_D08G1424 (WRKY)
讨论
断断MD52ne的单根纤维所需的力比断断MD90ne的空纤维更大
BFS值被广泛应用于评价纤维束的断裂力,即纤维强度。除了断裂力外,BFS还受到不同纤维特性的影响,如长度、细度、成熟度和纤维-纤维相互作用中涉及的MIC。从384f纤维性能的相关性分析2MD52ne和MD90ne杂交的后代表明,NILs的BFS变化主要由断裂力决定,与纤维-纤维相互作用相关的可变纤维性能影响较小(表5)2).不同NILs之间5 - 6%的纤维长度差异对NILs之间的BFS差异有轻微影响(12.9%),而不同NILs之间差异不显著的纤维厚度相关特性对NILs的BFS差异几乎没有影响(表2)1而且2).由于NILs的BFS方差主要由断裂力驱动,因此NILs之间的束强度之比预计与不受纤维-纤维相互作用影响的单个纤维强度之比相似。正如预测的那样,来自MD52的纤维束强度(24%)和单个纤维强度(22%)同样高于来自MD90ne的纤维束强度(表9)1而且3.).综上所述,MD52ne纤维的高束强主要得益于断裂力,较长的纤维对其贡献较小。与用于研究纤维强度的棉花CSIL品系相比,尽管由于CSIL品系之间的显著差异,纤维长度和厚度相关特性有很大的潜在影响[18,19], MD52ne和MD90ne是分析固有纤维强度分子机制的更理想的棉花NILs,因为它们的BFS方差主要受断裂力的影响,而最小限度地受纤维束中涉及纤维-纤维相互作用的其他纤维特性的调节。
基于结晶度从15到17 DPA迅速增加的发展纤维的纤维性质分析(图。3 b),我们确定从PCW到SCW生物合成阶段的过渡开始于大约15 DPA。因此,我们比较了MD52ne和MD90ne纤维在两个不同时间点的转录本丰度:15 DPA时,活跃伸长纤维主要由低结晶度的PCW组成(MD52ne, 18.1%;MD90ne, 20.9%)和20 DPA,其中SCW增稠纤维由高结晶度的PCW和SCW组成(MD52ne, 38.4%;MD90ne, 41.5%)。在过渡阶段的纤维发育过程中,会沉积一层新的细胞壁层,称为缠绕层[51].通过观察由最小SCW缠绕层组成的显影纤维(21dpa)的高纤维强度[8],缠绕层被推测为纤维强度的潜在来源[17,52].为了确定缠绕层是否以及如何影响纤维束和单个纤维的强度,可能需要进一步的综合研究,因为发展中的纤维的单个纤维强度之前是由Instron拉伸测试仪测量的,该测试仪是测量单个纤维强度的原型[8]并导致高度的可变性和不一致性[53].在我们的研究中,在NILs的过渡阶段(20 DPA)也检测到NILs的高BFS值(图2)。3 e).显像MD52ne纤维(21.73 g/tex, 20 DPA)的BFS显著(p值,0.0027)高于发展中的MD90ne纤维(17.52 g/tex, 20 DPA)。
乙烯及其网络植物激素通路可能参与了MD52ne优越的纤维长度发育
比较转录组分析表明,MD52ne中乙烯及其网络生长素和促进纤维伸长的GA信号通路相关转录本高度丰富(表2)5和无花果。4摄氏度).乙烯气体是一种主要的促进纤维伸长的植物激素[54].乙烯合成基因如ACC和ACO的上调以及乙烯信号基因如EBF的上调对纤维活性伸长至关重要[29- - - - - -31].与之前的发现一致,Acc6, aco4, ebf1,ERF1参与乙烯生物合成和纤维伸长所需要的信号通路在MD52ne纤维中高度表达,其长度(UHML)大于其长度(NIL), MD90ne(表5和无花果。6).此外,成绩单(辅助/ IAA,生长素反应GH3蛋白,GAST1)参与生长素和GA对纤维的分化和伸长是必需的[41,55].用于促进纤维伸长,倍数棒曲霉素参与了细胞壁的松动脂质转移蛋白参与纤维伸长[29]的表达也在MD52ne纤维中上调(表5和无花果。8).一大组基因(XET,中外,Sus)参与木葡聚糖和果胶的生物合成和需要棉纤维伸长的碳水化合物代谢[56]也富集在拉伸的MD52ne纤维中(表56 .答案AXET(Gh_A03G1432)和aSus(Gh_D08G1309)与BFS和UHML相关的qtl链接(图2)。7).
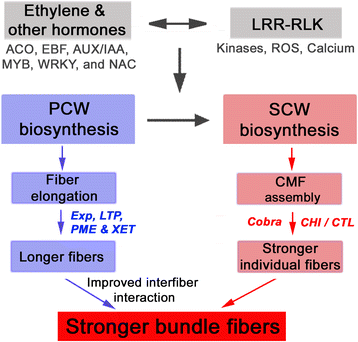
提出了MD52ne中高纤维束强度和单个纤维断裂力的机理模型。该模型的缩写为:LRR RLK, Leucine rich repeat receptor-like kinase;PCW,原代细胞壁;SCW,次生细胞壁;CME,纤维素微原纤维;1-氨基环丙烷-1-羧酸氧化酶;EBF, ein3结合F盒蛋白;AUX/IAA, AUX/IAA转录因子;MYB、MYB转录因子:WRKY、WRKY转录因子;NAC, NAC转录因子; Exp, Expensin; LTP, Lipid transfer protein; PME, Pectin methylesterase; XET, Xyloglucan endotransglucosylase; Cobra, Cobra like protein; CHI/CTL, Chitinase/Chitinase-like protein; ROS, Reactive oxygen species
受体样激酶信号通路调节纤维素沉积和维持细胞壁完整性可能参与MD52ne纤维强度的发展
除了控制植物生长发育的植物激素和转录网络外,受体样激酶(RLKs)也被发现是植物发育和胁迫反应的新型调节因子[33,57].在图中描述的各种RLK类中。5,含有富亮氨酸重复序列(LRR)的rlk最常从发育中的MD52ne纤维中识别出来。在与BFS和长度相关的两个qtl中也发现了3个LRR RLKs(表5,数据6而且7).在拟南芥伸长根尖和种子中,有报道称两个名为FEI 1和2的LRR RLKs在拟南芥伸长根尖的纤维素沉积中发挥作用[34]和种皮[35].ACC(1-氨基环丙烷-1-羧酸)是乙烯信号必不可少的分子,已被认为是FEI 1和2的信号分子[58],因此乙烯和LRR RLK信号很可能都参与了拉长组织中的纤维素沉积(图。8).其他配体未知的LRR RLKs被报道为拟南芥SCW形成的调节因子[59]和常见的树木[60].据报道,一种位于质膜的名为GhRLK1的棉花LRR RLK在活性SCW合成阶段被诱导[61].因此,LRR RLK信号通路可能参与介导棉纤维发育过程中细胞伸长和SCW生物合成的协调,这与其他植物的研究结果一致[57,58].
MD52ne纤维二级壁生物合成阶段晶体纤维素组装相关基因的时间调控
编码眼镜蛇样蛋白的三个基因(Gh_D12G0298、Gh_A13G0320和Gh_D13G0359)在MD52ne纤维SCW生物合成阶段被特异性上调(表2)5).类眼镜蛇蛋白2,gpi锚定的类cobra家族成员,最近被发现在拟南芥种皮的晶体纤维素沉积中发挥作用[62].当脆性秆m1水稻突变体中眼镜蛇样蛋白缺失时[63]或脆茎玉米突变体[64]时,杆的机械强度降低。一种与纤维素相互作用的类眼镜蛇蛋白调节水稻中的纤维素组装[42].因此,三个眼镜蛇式蛋白质在MD52ne纤维SCW阶段上调的基因可能是促成MD52ne超强强度的候选基因(图。8).
四个气/ CTLGh_D06G0479、Gh_A06G0439、Gh_A10G1271、Gh_D09G2016等基因在MD52ne纤维SCW期特异性上调,其序列与几丁质酶(气),几丁质酶样蛋白(细胞毒性t淋巴细胞)。CTL2是拟南芥中晶体纤维素含量的主要原因[43),而气是水稻和玉米中响应生物胁迫的致病相关基因[65,66].由此可见,的真正功能气/ CTL从MD52ne中鉴定出的基因仍有待确定。
MD52ne纤维过渡阶段基因的时间调控
我们之前报道了MD52ne纤维中从PCW到SCW阶段转变时SCW生物合成相关基因的短暂上调,基于第一代棉花寡核苷酸微阵列的转录组谱[16,17].目前的转录组分析采用RNA-seq和g .分子基因组序列在MD52ne纤维中鉴定出更多的DEGs(附加文件12)比之前的微阵列分析[17].RNA-seq分析还显示一些与SCW生物合成相关的基因,如MYB26,MYB46,CesA4[44,45,47]均在15 DPA时上调(表5和无花果。6).相比之下,其他26个中国极限运动协会RNA-seq鉴定的s在过渡阶段没有出现暂时性上调。为了进一步分析SCW生物合成相关基因的时间调控,我们从PlaNet [67]这些基因在拟南芥SCW生物合成过程中在时间和空间上共同表达。在与181个拟南芥scw相关基因同源的MD52ne基因中,有64个基因(35.4%)在15个发育MD52纤维的DPA中出现时间上调(附加文件)13),而其他基因则没有表现出时间上的上调。除了MD52ne比MD90ne中上调的SCW基因数量有限外,NILs之间的结晶性水平相同(图。2 b)可能意味着与SCW纤维素组装和壁完整性相关的基因相比,与SCW纤维素生物合成相关的基因较少参与MD52ne优越的纤维强度。
结论
随着现代高速纺纱技术的出现,对高纤维强度的要求急剧提高。棉花研究人员试图改善这一特性g .分子遗传背景。MD52ne被证明具有比NIL MD90ne更高的纤维强度。本研究利用RNA-seq技术,揭示了MD52ne中优良单根纤维强度(与纱线强度相关)形成背后的分子机制。MD52ne纤维的束强主要取决于单个纤维强度与纤维长度的结合。对比NILs的转录组分析表明,MD52ne纤维的超强强度可能与两种信号通路有关(图2)。8):一种是乙烯及其相互连接的植物激素通路,参与纤维伸长和纤维间相互作用;另一种是RLKs信号通路,参与调节细胞壁完整性,并可能介导细胞伸长和SCW生物合成的协调。几种次生细胞壁生物发生相关基因和转录因子等眼镜蛇式蛋白质,气/ CTL,NAC, WRKY, COL5,锌指家族蛋白而且MYBMD52ne发育纤维上调。MD52ne纤维的优良BFS可能是由于较高的单个纤维强度,较长的纤维长度对其贡献较小。较长的纤维可能会增加纤维间的相互作用,这可能是某些PCW相关基因差异调节的结果。MD52ne个体纤维强度的提高可能与调节细胞壁完整性的途径有关。
方法
植物材料
棉花NILs MD52ne和MD90ne是由USDA-ARS-SEA的William Meredith博士培育和提供的14) [14,15].这两种NILs分别在两个不同的土地上生长了两个生长季节,在温室里生长了一个生长季节。为了比较两种无尼尔纤维的物理特性,并确定每种无尼尔植物的变化,2012年,每种无尼尔在位于马萨诸塞州斯通维尔的一块田地中种植了10株单株。斯通维尔的土壤类型为博斯克特细砂壤土。成熟的纤维采自每株野牡丹。为了进行转录组比较分析,在每个发育时间点(10、13、15、17、20、24、28、33、37、44和48 DPA)从两种NILs的50株植物中收集了3个生物复制(每个复制大约40个棉铃),这些植物于2013年生长在洛杉矶新奥尔良的一个领域。新奥尔良的土壤类型是在一个高架位置的冲积层上疏浚的Aquent,以提供足够的排水。纤维样品从384f2从MD90ne和MD52ne的杂交中获得的子代植物于2012年在美国MS的Stoneville收集,如Islam等人所述。[49].所有自然开放的铃都是人工从F2植物。人工从胚珠中收集发育纤维(10-37 DPA),成熟纤维(44 DPA)使用实验室轧辊轧棉机轧皮。收集的纤维立即用液氮冷冻用于RNA提取或在40°C培养箱中干燥用于物性分析。为了提取额外的rna用于验证转录组结果,在每个发育时间点(10-44 DPA)从两个NILs中收集了3个棉纤维的生物复制,这些NILs在位于洛杉矶新奥尔良的温室中使用Metro-Mix 360在5加仑花盆中生长。在从种植、标记、收获和轧轧的所有过程中,两个并排生长的NILs被等效地处理。
纤维性能测量
为了测量棉纤维的纤维特性,在21±1°C下,在65±2%的湿度下预平衡纤维48小时。所有纤维特性都是通过根据制造商说明书正确校准的仪器获得的,标准棉纤维来自USDA-AMS。
两种NILs成熟纤维的BFS (g/tex)、UHML (inch)、FE(%)和MIC值由HVI (USTER Technologies Inc., Knoxville, TN)测量的5个重复获得。为了从显影纤维中确定BFS,使用了一个stelometer (SDL Atlas, Stockport, England)对纤维样品进行了三个重复。BFS给出的强度,表示为千牛顿米每千克,是打破一束具有特定重量线性密度的纤维所需的力。根据Delhom等人的研究,为了测量单个纤维的断裂力,使用了Favimat (Textechno, Mönchengladbach,德国)与303根单个纤维和一个13毫米的长度计。[68].
使用Uster®AFIS- pro (Uster Technologies Inc.,诺克斯维尔,田纳西州)测量AFIS成熟度比和细度。AFIS纤维数据平均来自5个重复,每个重复5000根纤维。
用于测量重量细度(mtex, mg km−1),对300根纤维进行梳理,在顶部和底部切割,使它们长15毫米,并用微量天平测量[69].平均重量细度由三次测量计算。
表征纤维细胞壁厚度程度的圆度(θ)是直接从横切面纤维的光镜图像中测量的[70].平均细胞壁面积(A),不包括纤维截面的管腔和周长(P),根据Xu和Huang [71].由方程θ = 4πA/P得到圆度2[72]用公式MR = θ / 0.577 [73].
ATR-FTIR光谱采集和数据分析
所有光谱使用FTS 3000MX FTIR光谱仪(Varian Instruments, Randolph, MA)收集,并配有陶瓷源、KBr分束器和氘化硫酸三甘氨酸(DTGS)探测器。ATR采样装置采用DuraSamplIR单通道金刚石涂层内反射附件(Smiths Detection, Danbury, CT),并通过不锈钢棒和电子负载显示器施加一致的接触压力。在4000-600厘米范围内,在不同位置对单个样品至少进行了6次测量−1身高4厘米−1和16个共同添加的扫描。所有的光谱都以吸光度单位给出,没有应用ATR校正。在GRAMS /AI(版本9.1,Thermo Fisher Scientific, Waltham, MA)中导入GRAMS IQ应用后,使用Savitzky-Golay函数(多项式= 2,点= 11)平滑光谱。然后,将光谱集加载到Microsoft Excel 2000中,使用先前提出的算法分析来评估棉花的结晶度和成熟度[23,24].在最初的概念评估纤维素成熟度(M红外)和结晶度指数(CI红外)源自红外测量[22- - - - - -24],识别关键波长,然后采用两种算法(R1和R2)用于棉花纤维素M红外和CI红外通过表示R1和R2值。两类品种之间的比较采用每种纤维样品的均值和标准差。
RNA提取,文库制备和测序
使用Sigma Spectrum™植物总RNA试剂盒(Sigma- aldrich, St. Louis, MO)从发育中的棉纤维(10、15、20和24 DPA)中提取总RNA,并根据制造商的协议进行DNase1消化。使用NanoDrop 2000分光光度计(NanoDrop Technologies Inc., Wilmington, DE)和Agilent生物分析仪2100 (Agilent Technologies Inc., Santa Clara, CA)测定总RNA的质量和数量。来自两种NIL纤维的两个不同发育阶段(15和20 DPA)的两个生物复制RNA样本被送往Data2Bio LLC (Ames, Iowa)进行文库制备,并根据先前描述的方法进行后续配对端Illumina mRNA测序[74].
RNA-seq数据处理
原始RNA-seq reads用镰刀(https://github.com/najoshi/sickle),使用20分的质量分值。然后,RNA-seq读取与陆地棉基因组草图[26]使用GSNAP软件程序[75].用Bedtools软件计算每个注释基因的Reads [76].
鉴别差异表达基因
通过EdgeR软件的负二项式方法计算差异基因表达,并使用离散度的tagwise估计[77].RPKM用于估计计算的基因表达水平:RPKM = [109/问] C,其中C代表可以映射到目标单基因的读取数,N表示可以映射到至少一个单基因的读取数,L表示目标单基因的长度。FDR修正了试验结果的准确性。在本研究中,FDR < 0.05和对数的绝对值2使用ratio(其中“ratio”指的是目标单基因在文库中的表达倍数变化)来选择DEGs。
RT-qPCR验证RNA-seq结果
RT-qPCR相关实验流程及数据分析依据定量实时PCR实验发布的最低信息指南[70].采用4个纤维发育阶段(10、15、20和24 DPA)进行RT-qPCR分析,验证所选基因的RNA-seq结果。cDNA制备、qPCR及计算的详细描述已有报道[20.].从32个deg中设计特异性引物对以验证RNA-seq。RT-qPCR反应使用的内源内参基因为18S rRNA (U42827)和α-微管蛋白4 (AF106570)。参考基因和目标基因引物序列见附加文件15.RT-qPCR每个时间点分别进行3次生物学重复和3次技术重复。
基因注释分析
从两个NILs的15和20根DPA纤维中获得的RNA-seq数据首先使用BioVenn进行Venn分析[78]以确定在两个时间点之间哪些deg是常见的。为协助识别数据中所代表的生物过程,氧化石墨烯富集分析采用agriGO奇异富集分析[28].统计学检验方法为Fisher精确检验(显著性水平0.05)。代谢分析,MapMan软件[79]用于识别和说明细胞壁相关分子的代谢概况。
伦理批准并同意参与
不适用。
支持数据的可用性
所有支持数据都可以在手稿及其附加文件中找到。生物序列存放在美国国家生物技术信息中心(NCBI)的序列阅读档案(SRA)中,登录号为SRS843151、SRS843159、SRS843160和SRS843163。
缩写
- AFIS:
-
先进的光纤信息系统
- 细胞毒性t淋巴细胞:
-
Chitinase-like
- 度:
-
差异表达基因
- 分区:
-
花后天数
- 的边后卫:
-
纤维束强度
- 罗斯福:
-
错误发现率
- 菲:
-
纤维伸长
- 红外光谱:
-
傅里叶变换红外光谱
- 女友:
-
重量细度
- 构建院系:
-
重型仪器
- 走:
-
基因本体论
- 麦克风:
-
麦克隆
- 零:
-
Near-isogenic线
- 物理化学加工:
-
原代细胞壁
- RPKM:
-
每千碱基每百万次读取
- RT-qPCR:
-
逆转录定量聚合酶链反应
- 标准铜线:
-
次级细胞壁
- TF:
-
转录因子
- UHML:
-
上半段平均长度
参考文献
- 1.
Wakelyn PJ, Bertoniere NR, French AD, Thibodeaux DP, Triplett BA, Rousselle M-A,等。棉纤维化学与技术,第17卷。美国纽约:CRC出版社;2010.
- 2.
尼科尔斯·N,马丁·V,迪瓦恩·J,李华,琼斯·D,哈克·K.品种性能:棉花竞争力的关键问题。北卡罗来纳州,罗利:棉花公司;2012.
- 3.
决定纤维结构和用途的生理解剖因素。In:棉花生理学。美国纽约:施普林格;2010.33-47页。
- 4.
Bradow JM, Davidonis GH。纤维质量的定量和棉花生产加工界面:生理学家的观点。棉花学报2000;4:34-64。
- 5.
Frydrych I, Thibodeaux DP。纤维质量评价——棉花纤维质量的现状和未来趋势/内在价值。在:Wakelyn PJ, Chaudhry MR,编辑。棉花:21世纪的技术。华盛顿特区:国际棉花咨询委员会;2010.p . 251 - 96。
- 6.
泰勒RA。强度和延伸率的高速测量。见:第一届世界棉花研究会议:1994;1994年,澳大利亚布里斯班。p . 268 - 73。
- 7.
崔Suh MW, X,萨瑟PE。与MANTIS和HVI数据相关的棉花小束拉伸性能——纱线强度预测之路。见:1996年华盛顿棉花会议进程。田纳西州纳什维尔:国家棉花委员会;1996.p . 1296 - 300。
- 8.
谢永林,李志强,李志强。温室栽培SJ-2型阿卡拉棉单纤维强度的发育研究。文献论文集,1995;26(2):344 - 344。
- 9.
评价纤维加工对棉纤维拉伸性能的影响。美国德克萨斯州拉伯克:德克萨斯理工大学;2014.
- 10.
谢长廷Y-L。棉纤维的结构发育及其与纤维质量的关系。进:Basra AS,编辑。棉纤维发育生物学,质量改进与纺织加工。纽约:霍沃斯出版社;1999.p . 137 - 65。
- 11.
崔晓霞,张志刚,张志刚,张志刚。棉纤维强度测量中纤维长度对棉纤维强度测量的影响。文献综述,2014;34(9):979-88。
- 12.
Munro JM。棉花。第二版。哈洛,英国:朗曼科学技术;1987.
- 13.
佩蒂尔NB,辛格M.适合转子纺纱系统的中等短纤维高强度棉的开发。见:第一届世界棉花会议:1995;1995年,澳大利亚,布里斯班。
- 14.
MD 52ne高纤维优质棉花种质资源和循环亲本MD 90ne的登记。作物科学,2005;
- 15.
回交群体中控制棉纤维强度的最小基因数。作物科学,2005;45(3):1114-9。
- 16.
胡志强,王志强,王志强,等。斑点棉花寡核苷酸微阵列基因表达分析。BMC基因组学。2007;8(1):81。
- 17.
Hinchliffe DJ, Meredith WR, Yeater KM, Kim HJ, Woodward AW,陈志军,等。比较高通量谱分析显示,纤维束强度不同的近等基因棉花种质系在纤维基因表达模式上存在时间差异。应用理论与实践。2010;20(7):1347-66。
- 18.
方琳,田睿,陈娟,王松,李霞,王萍,等。携带不同巴贝多棉染色体段的陆地棉染色体渐渗系纤维强度的转录组学分析。PLoS ONE。2014; 9 (4): e94642。
- 19.
方琳,田睿,李霞,陈杰,王松,王鹏,等。通过不同染色体段渗进的较长纤维系的表达谱分析,揭示了棉纤维伸长网络。BMC基因组学杂志,2014;15(1):838。
- 20.
金海军,唐勇,文海霞,方丹东。棉花未成熟纤维(im)突变体的功能分析推测纤维细胞壁发育与胁迫响应有关。BMC基因组学杂志,2013;14(1):889。
- 21.
王超,吕艳,徐伟,张涛,郭伟。毛棉未成熟纤维(Im)突变体Im基因突变导致纤维细胞壁增厚的异常表型和转录组表达。中国生物医学工程学报,2014;15(1):94。
- 22.
皮尔逊对进化数学理论的贡献。3回归,遗传和混血。科学通报。1895;59(353-358):69-71。
- 23.
刘勇,刘永杰,刘永杰,刘永杰。傅里叶变换红外光谱直接、无损、快速测定棉纤维成熟度的研究进展。文献综述,2011;29(3):357 - 357。
- 24.
刘颖,Thibodeaux D, Gamble G, Bauer P, VanDerveer D.傅立叶变换红外光谱(FT-IR)与x射线衍射(XRD)测定棉纤维结晶度的比较研究。光谱学与光谱学学报,2012;26(3):344 - 344。
- 25.
刘勇,金海杰。使用ATR-FTIR光谱直接,无损,快速评估植物和培养中生长的发育棉纤维。光谱学与光谱学学报,2015;29(3):344 - 344。
- 26.
张涛,胡勇,姜伟,方林,关霞,陈杰,等。同种异体四倍体棉花(Gossypium hirsutum L. acc。TM-1)为光纤改进提供了资源。生物工程学报。2015;33:531-7。
- 27.
Audic S, Claverie J-M。数字基因表达谱的意义。基因组学报,1997;7(10):986-95。
- 28.
杜震,周旭,凌云,张震,苏哲。agriGO:农业社区GO分析工具包。核酸研究,2010;38(Web Server): W64-70。
- 29.
史永华,朱淑文,毛学泽,冯建新,秦玉明,张磊,等。转录组分析、分子生物学和生理学研究揭示了乙烯在棉纤维细胞伸长中的重要作用。植物学报。2006;18(3):651-64。
- 30.
毛李G,孟X,王R, G,汉族L,刘Y, et al。乙烯诱导过程中MPK3/MPK6级联及其下游WRKY转录因子对ACC合酶活性的双水平调控公共科学学报,2012;8(6):e1002767。
- 31.
Binder BM, Walker JM, Gagne JM, Emborg TJ, Hemmann G, Bleecker AB,等。拟南芥EIN3结合F-Box蛋白EBF1和EBF2在乙烯信号传导中具有不同但重叠的作用。植物学报。2007;19(2):509-23。
- 32.
拟南芥富半胱氨酸蛋白GASA4促进GA反应并在细菌和植物中表现出氧化还原活性。植物学报,2010;36(6):344 - 344。
- 33.
植物细胞壁完整性维持机制——细胞壁质膜信号网络的一个案例研究。植物化学。2015;112:100-9。
- 34.
徐世林,王志强,王志强。在拟南芥中,两种富含亮氨酸的重复受体激酶介导信号通路,连接细胞壁生物合成和ACC合成酶。植物学报。2008;20(11):3065-79。
- 35.
Harpaz‐Saad S, McFarlane HE, Xu S, Divi UK, Forward B, Western TL,等。通过FEI2 RLK/SOS5途径和纤维素合成酶5合成纤维素是拟南芥种皮粘液结构所必需的。植物学报,2011;36(6):344 - 344。
- 36.
An C, Saha S, Jenkins JN, Scheffler BE, Wilkins TA, Stelly DM.棉花EXPANSIN基因的转录组分析、序列表征和基于snp的染色体分配。中国生物医学工程学报。2007;27(5):539 - 553。
- 37.
阮艳玲,刘海燕,王晓明,等。棉花单细胞纤维伸长与胞间连丝发育可逆门控的关系及蔗糖、K+转运蛋白和扩张蛋白的协调表达。植物细胞学报,2001;13(1):47-60。
- 38.
刘Q, M Talbot, DJ Llewellyn。两种不同纤维性质的棉属植物纤维壁的果胶甲基酯酶和果胶重构存在差异。PLoS ONE。2013; 8 (6): e65131。
- 39.
李J, Burns TH, Light G, Sun Y, Fokar M, Kasukabe Y,等。棉花木葡聚糖内转糖基酶/水解酶基因及其在纤维伸长中的作用。足底。2010;232(5):1191 - 205。
- 40.
姜艳,郭伟,朱辉,阮玉玲,张涛。GhSusA1过表达可提高植株生物量,提高棉纤维产量和品质。中国生物技术学报,2012;10(3):301-12。
- 41.
Kim HJ, Hinchliffe DJ, Triplett BA,陈志军,Stelly DM, Yeater KM,等。植物激素网络促进棉花花前胚珠的纤维首字母分化。公共科学学报。2015;10(4):e0125046。
- 42.
刘磊,上官K,张波,刘旭,闫敏,张磊,等。脆性Culm1是一种类似眼镜蛇的蛋白质,通过结合纤维素微纤维在纤维素组装中起作用。公共科学图书馆,2013;9(8):15。
- 43.
Sánchez-Rodríguez C, Bauer S, Hématy K, Saxe F, Ibáñez AB, Vodermaier V,等。几丁质酶样1/pom-pom1及其同源物CTL2是葡聚糖相互作用蛋白,对拟南芥纤维素生物合成至关重要。植物学报。2012;24(2):589-607。
- 44.
钟睿,叶振华。MYB46和MYB83结合到SMRE位点,直接激活一系列转录因子和次级壁生物合成基因。植物生理学报。2012;32(2):368-80。
- 45.
杨超,徐震,宋杰,K Conner, Barrena GV, Wilson ZA。拟南芥MYB26/MALE STERILE35调控内胚囊的二次增厚,对花药开裂至关重要。植物学报。2007;19(2):534-48。
- 46.
高建辉,全华威,金卫c,金建勇,韩k - h。MYB46/ myb83介导的转录调节程序是二级细胞壁生物合成的看门人。学报学报。2014;114(6):1099-107。mcu126。
- 47.
金海杰,穆莱N,方达东,Triplett BA。毛棉纤维素合成酶催化亚基4启动子在转基因拟南芥和棉花组织中的功能分析。中国植物科学,2011;18(2):323-32。
- 48.
Mokshina N, Gorshkova T, Deyholos MK.几丁质酶样(CTL)和纤维素合成酶(CESA)基因在亚麻(Linum usitatissimum L.)韧皮胶状纤维壁中的表达。PLoS ONE。2014; 9 (6): e97949。
- 49.
Islam MS,曾磊,Delhom CD,宋旭,金海杰,李鹏,等。利用两个纤维束强度不同的近等基因系的种内杂交鉴定棉纤维品质数量性状位点。分子育种2014:1-12。
- 50.
李峰,范刚,陆超,肖刚,邹超,Kohel RJ,等。陆地棉(Gossypium hirsutum TM-1)基因组序列为人类基因组进化提供了新的视角。中国生物工程学报。2015;33(5):524-30。
- 51.
海鸥RW光碟。细胞骨架参与棉纤维生长发育。微米,1993;24(6):643 - 60。
- 52.
Haigler CH, Betancur L, Stiff MR, Tuttle JR.棉花纤维:细胞壁和纤维素研究的强大单细胞模型。植物科学进展。2012;3:104。
- 53.
Benedict CR, Kohel JR, Lewis HL。棉纤维质量。在:史密斯CW,科罗瑟JT,编辑。棉花的产地、历史、技术和生产。纽约:John Wiley & sons, Inc;1999.p . 269 - 88。
- 54.
金正日HJ。纤维生物。在:方DD,珀西RG,麦迪逊WI,编辑。美国农学学会,美国作物科学学会,美国土壤科学学会2015年第2版。p . 97 - 127。
- 55.
比斯利C,叶婷。植物生长物质对未受精棉花胚珠体外纤维发育的影响。李文杰,2004;
- 56.
张志刚,张志刚,张志刚,张志刚,等。初级细胞壁的特殊外层将拉长的棉纤维连接成组织状的束。植物科学进展。2009;30(2):344 - 344。
- 57.
De Smet I, Voß U, Jürgens G, Beeckman T.受体样激酶塑造植物。中国生物医学工程学报。2009;11(10):1166-73。
- 58.
Yoon GM, Kieber JJ。1-氨基环丙烷-1-羧酸在植物中的信号分子。植物学报。2013;5:plt017。
- 59.
王娟,Kucukoglu M,张玲,陈萍,Decker D, Nilsson O,等。拟南芥LRR-RLK, PXC1,是一个与TDIF-PXY/TDR-WOX4信号通路相关的次生壁形成调控因子。中国生物医学工程学报。2013;13(1):94。
- 60.
宋东,奚伟,沈娟,毕涛,李磊。杨树次生维管分化过程中质膜蛋白和受体样激酶的研究。植物分子生物学杂志,2011;26(1):344 - 344。
- 61.
李永林,孙杰,夏国祥。与棉纤维发育相关的LRR受体样蛋白激酶基因的克隆和特性。中国生物医学工程学报,2005;29(3):344 - 344。
- 62.
Ben-Tov D, Abraham Y, Stav S, Thompson K, Loraine A, Elbaum R,等。COBRA-LIKE 2是gpi锚定的COBRA-LIKE家族的成员,在拟南芥种皮粘液分泌细胞的纤维素沉积中起作用。中国生物医学工程学报,2015;29(3):344 - 344。
- 63.
李勇,钱强,周勇,闫敏,孙林,张敏,等。脆性CULM1编码一种类似眼镜蛇的蛋白质,影响水稻的机械性能。植物学报。2003;15(9):2020-31。
- 64.
陈青,杜嘉佳,阿彭策勒,梅利,TM, Howard RJ,等。脆柄2编码一种假定的糖基磷脂酰肌醇锚定蛋白,通过改变次级细胞壁的组成和结构来影响玉米组织的机械强度。足底。2006;224(5):1174 - 84。
- 65.
Bravo JM, Campo S, Murillo I, Coca M, San Segundo B.真菌和创伤诱导的含有玉米发病相关蛋白4 (PR-4)家族II类几丁质酶mRNA的积累。植物分子生物学杂志,2003;52(4):745-59。
- 66.
中崎T, Tsukiyama T, Okumoto Y, Kageyama D,内藤K,井上K,等。水稻致病相关蛋白-3几丁质酶基因家族的分布、结构、器官特异性表达及系统发育分析基因组。2006;49(6):619 - 30。
- 67.
Mutwil M, Klie S, Tohge T, Giorgi FM, Wilkins O, Campbell MM,等。PlaNet:来自7个物种的植物网络的组合序列和表达比较。植物学报。2011;23(3):895-910。
- 68.
戴宏平,崔晓霞,陈晓明。单纤检测方法。2010:1405-1410。
- 69.
美国测试与材料学会。纺织纤维线密度的标准试验方法。选项A,纤维束称重。在。:一个STM Standard D1577-07. Annu. Book of ASTM Standards. Philadelphia, PA: ASTM; 2012.
- 70.
Boylston EK, Thibodeaux DP, Evans JP。应用显微技术开发棉纤维成熟度的参考方法。纺织工业学报,1993;29(2):344 - 344。
- 71.
徐波,黄云。棉纤维图像分析第二部分:截面测量。文献研究,2004;29(5):516 - 516。
- 72.
Thibodeaux DP, Evans JP。棉纤维成熟度的图像分析。文献文献,1986;56(2):130-9。
- 73.
锡伯多DP, Rajasekaran K.棉纤维成熟度新参考标准的开发。棉花科学,1999;3:188-93。
- 74.
Naoumkina M, Thyssen G, Fang DD, Hinchliffe DJ, Florane C, Yeater KM,等。Li2突变导致异体四倍体棉花(Gossypium hirsutum L.)伸长纤维亚基因组表达偏倚降低。公共科学图书馆,2014;9(3):e90830。
- 75.
吴涛,Nacu S.短读中复杂变异和剪接的快速和耐snp检测。生物信息学,2010,26(7):873 - 81。
- 76.
昆兰AR,霍尔IM。BEDTools:用于比较基因组特征的一套灵活的实用程序。生物信息学,2010,26(6):841 - 2。
- 77.
Robinson MD, McCarthy DJ, Smyth GK。edgeR:用于数字基因表达数据差异表达分析的Bioconductor包。生物信息学,2010,26(1):139 - 40。
- 78.
Hulsen T, de Vlieg J, Alkema W. biovenn -一个使用面积比例维恩图比较和可视化生物列表的web应用程序。BMC基因组学。2008;9(1):488。
- 79.
Thimm O, Bläsing O, Gibon Y, Nagel A, Meyer S, Krüger P,等。mapman:一种用户驱动的工具,可以将基因组学数据集显示在代谢途径和其他生物过程的图表上。植物学报,2004;37(6):914-39。
确认
这项研究要献给已故的美国农业部科学家William R. Meredith Jr.博士,他在MS的Stoneville开发了MD90ne和MD52ne棉花品系,并将其用于目前的研究。我们要感谢美国农业部海洋研究所(USDA-ARS-SEA)的曾凌河博士提供的AFIS数据,感谢李平女士、特雷西·康登(Tracy Condon)和宋先良博士在纤维样品制备过程中的协助,感谢Holly King女士、Jeannine Moraitis和Raisa Moiseyev女士对纤维性质的分析。本文中提及的商品名称或商业产品仅为提供特定信息的目的,并不意味着美国农业部的推荐或认可,农业部是一个平等机会的提供者和雇主。
资金
本项目由USDA-ARS CRIS项目#6054-21000-017-00D和Cotton Incorporated资助#12-199支持。
作者信息
从属关系
相应的作者
额外的信息
相互竞争的利益
这篇手稿中描述的研究部分是由棉花公司资助的。资助者在研究设计、数据收集和分析、发表决定或手稿准备中没有任何作用。这并不会改变作者对共享数据和材料的所有政策的遵守。
作者的贡献
MSI收集纤维样本,提取rna,过滤RNA-seq数据,进行qPCR验证,分析转录组数据,并撰写手稿。DDF构思了这项研究,设计了实验,并修改了手稿。GNT分析了RNA-seq数据并修改了手稿。CDD负责纤维性能的测量。YL使用ATR-FTIR光谱测量纤维性能。HJK设计实验,协调功能和纤维性能分析,分析结果,并撰写稿件。所有作者都阅读并批准了最终的手稿。
附加文件
附加文件1:
中映射基因的名称陆地棉(TM-1)及其拟南芥同源基因的注释。该表包含61263个同源四倍体棉花基因陆地棉(TM-1)基因组草图。用拟南芥同源基因对所映射的基因进行了注释,并对其进行了描述。还提供了每个基因的物理位置,包括染色体名称。第一列有g .分子(TM-1)基因名称后跟拟南芥基因名称,TAIR 10基因描述,g .分子染色体数目,基因的物理位置和链的类型(+/-)。(xlsx3358 kb)
附加文件2:
MD52ne和MD90ne在15 DPA处差异表达基因。该表包含4005个异体四倍体棉花基因,这些基因在15个DPA发育纤维中MD52ne和MD90ne之间显著表达。log的阈值绝对值2比值≥1和p值≤0.05。MD52ne和MD90ne的表达水平比较也包括在fold change中。第一列有g .分子(TM-1)基因名后接拟南芥基因名,TAIR 10基因描述,log2MD52ne和MD90ne之间的每千碱基每百万reads (RPKM)比值对应p值,调整p值和折叠变化(MD52ne除以MD90ne)。(xlsx428kb)
附加文件3:
MD52ne和MD90ne在20 DPA处差异表达基因。该表包含1080个异体四倍体棉花基因,这些基因在20个DPA发育纤维中MD52ne和MD90ne之间显著表达。log的阈值绝对值2比值≥1和p值≤0.05。MD52ne和MD90ne的表达水平比较也包括在fold change中。第一列有g .分子(TM-1)基因名后接拟南芥基因名,TAIR 10基因描述,log2MD52ne和MD90ne之间的每千碱基每百万reads (RPKM)比值对应p值,调整p值和折叠变化(MD52ne除以MD90ne)。(xlsx127 kb)
附加文件4:
MD52ne中15 DPA差异表达上调基因。在MD52ne的15个DPA位点上有3565个差异表达上调的基因包含在这个表中。第一列有g .分子(TM-1)基因名后接拟南芥基因名,TAIR 10基因描述,log2MD52ne和MD90ne之间的每千碱基每百万reads (RPKM)比值对应p值,调整p值和折叠变化(MD52ne除以MD90ne)。(xlsx371 kb)
附加文件5:
MD52ne在15 DPA处差异表达下调基因。在MD90ne的15 DPA位点上有440个差异表达上调的基因包含在这个表中。第一列有g .分子(TM-1)基因名后接拟南芥基因名,TAIR 10基因描述,log2MD52ne和MD90ne之间的每千碱基每百万reads (RPKM)比值对应p值,调整p值和折叠变化(MD52ne除以MD90ne)。(xlsx63 kb)
附加文件6:
MD52ne中20 DPA差异表达上调基因。在MD52ne的20 DPA位点上有774个差异表达上调的基因包含在这个表中。第一列有g .分子(TM-1)基因名后接拟南芥基因名,TAIR 10基因描述,log2MD52ne和MD90ne之间的每千碱基每百万reads (RPKM)比值对应p值,调整p值和折叠变化(MD52ne除以MD90ne)。(xlsx91 kb)
附加文件7:
MD52ne在20 DPA处差异表达下调基因。在MD90ne的15个DPA位点上有306个差异表达上调的基因包含在这个表中。第一列有g .分子(TM-1)基因名后接拟南芥基因名,TAIR 10基因描述,log2MD52ne和MD90ne之间的每千碱基每百万reads (RPKM)比值对应p值,调整p值和折叠变化(MD52ne除以MD90ne)。(xlsx42 kb)
附加文件8:
去分析。采用奇异富集分析来识别在MD52ne发育纤维的15 (A)和20 (B) DPA上差异表达的GO类别。与GO标识符相邻的颜色和数字表示p值。该文件包含了分别在15和20 DPA下使用差异表达基因进行氧化石墨烯富集分析的结果。(docx198kb)
附加文件9:
的微分表达式受体样激酶(RLKs)在20 DPA下显影MD52ne纤维。通过MapMan生成不同类别rlk的微分表达式。红色和紫色分别代表上调和下调。RLKs包含三个结构域,包括胞外结构域、跨膜结构域和细胞质侧的激酶结构域。c -凝集素,具有凝集素样基序的RLKs;Crinkly4-like,具有Crinkly4-like结构域的rlk;DUF26,未知函数域26;Extensin,含有Extensin motif的RLK;l -凝集素,具有凝集素结合域的RLKs;LRK 10-like, Lr10位点上的RLK基因;LRR,富亮氨酸重复序列; LysM, RLKs with lysine motif; PERK-like, proline-rich extensin-like kinase; RKF3-like, receptor-like kinase in flowers 3; S-locus, RLK with S-domain; Thaumatin, RLK-like thaumatin protein; WAK, wall-associated kinase. This file contains the results of MapMan analysis of different RLKs using differentially expressed genes at 20 DPA. (DOCX 135 kb)
附加文件10:
在纤维发育过程中,从RNA-seq数据中选择一些差异表达基因的RT-qPCR验证。本文件包含32个基因的qPCR分析结果和RNA-seq表达数据,这些基因用于比较MD52ne和MD90ne之间的折叠表达水平。4份(10、15、20和24 DPA)显像纤维样品和2份(15和20 DPA)显像纤维样品分别用于RT-qPCR和RNA-seq。RT-qPCR结果校正为Tubilin和18S基因。每个处理组分别对3个生物重复进行3次qPCR检测,然后取平均值。(docx644 kb)
附加文件11:
与棉纤维细胞壁发育相关的重要基因名称位于已鉴定的QTL区域附近。本表包含来自RNA-seq数据的差异表达基因,这些基因位于先前分别报道的位于03号和24号染色体上与BFS和UHML相关的两个qtl附近。2014 [49].(xlsx12kb)
附加文件12:
Hinchliffe等人2010年RNA-seq和微阵列之间恭顺表达基因的比较。这些图比较了本研究的RNA-seq (RNA)结果与Hinchliffe等人报道的微阵列(MA)数据之间差异表达基因的数量。2010 [17].RNA-seq和微阵列数据从15,20和16,20 DPA显影纤维样本中生成。A)两个时间点DE基因总数;B) DE在RNA序列中仅以15 DPA表达,在微阵列数据中仅以16 DPA表达;C) DE在RNA序列和微阵列数据中均仅在20 DPA表达。(docx320 kb)
附加文件13:
棉花MD52ne转录水平与拟南芥次级壁生物发生共表达基因的比较。该表包含64个次生细胞壁(SCW)生物合成相关基因,这些基因来自PlaNet [67]这些基因在拟南芥SCW生物合成过程中在时间和空间上共同表达。这64个基因在MD52ne中表达上调。(docx20kb)
附加文件14:
陆地棉近等亲本MD52ne和MD90ne的杂交方案。该图为取自Islam等人的陆地棉近等基因系MD52ne和MD90ne的杂交方案。2014 [50].括号中R代表循环,D代表各自的亲本。JCPC, DP, MD和FTA是种质资源名称,分别代表John Cotton Poly Cross, Deltapine, Mississippi Delta和ARS品系。
附加文件15:
本研究使用引物名称及其序列进行RT-qPCR验证。该文件包含32个RT-qPCR引物对序列,用于验证RNAseq表达数据。相应的基因名称和描述也包括在这里。(xlsx13kb)
权利和权限
开放获取本文根据创作共用属性4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),允许在任何媒介上不受限制地使用、分发和复制,前提是您对原作者和来源给予适当的赞扬,提供到创作共用许可证的链接,并注明是否进行了更改。创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)除另有说明外,适用于本条所提供的资料。
关于本文
引用本文
Islam, m.s., Fang, d.d., Thyssen, G.N.et al。比较纤维性质和转录组分析揭示了可能与棉花高纤维强度有关的关键基因(陆地棉L.)行MD52ne。BMC植物生物学16日,36(2016)。https://doi.org/10.1186/s12870-016-0727-2
收到了:
接受:
发表:
关键字
- 纤维束强度
- 纤维素组装
- 乙烯
- 陆地棉
- 单个纤维强度
- Near-isogenic线
- 受体激酶