摘要
背景
磷(P)是一种必需的宏量营养素,在土壤中经常受到限制,影响植物的生长和发育。在拟南芥,低磷根(LPR1)及其近paraLPR2编码多铜氧化酶(MCOs)。它们调节根系对磷(Pi)缺乏的分生组织反应。然而,角色LPR水稻基因家族(栽培稻)在维持Pi稳态中的作用尚未阐明。
结果
在此,对同源词进行鉴定和表达分析LPR1/2在大米中进行。五个同系词,以下简称OsLPR1-5在水稻中鉴定到,分布在1号染色体上,范围为65 kb。系统发育分析分组OsLPR1/3/4/5而且OsLPR2分为两个不同的子支系OsLPR3而且5显示距离很近。定量实时RT-PCR (qRT-PCR)分析显示OsLPR3-5而且OsLPR2分别在根和茎上。不同营养元素如磷、氮(N)、钾(K)、镁(Mg)和铁(Fe)的缺乏对各成员的相对表达量产生差异和部分重叠的影响OsLPR家庭。Pi缺乏(- P)导致的相对表达水平显著增加OsLPR3而且5。在相对表达水平上有较强的诱导作用OsLPR3而且5在osphr2提示其转录负调控作用OsPHR2。进一步,表达水平OsLPR3而且5或者减弱了ossiz1而且ospho2或者在水稻过表达中增加OsSPX1。
结论
这项研究的结果为进化扩展和可能的功能分歧提供了见解OsLPR家庭的潜在角色OsLPR3而且5在维持水稻Pi稳态中起重要作用。
背景
磷(P)是人体必需的宏量营养素之一,是多个生化和生理过程所必需的,也是核酸、ATP和膜磷脂等关键大分子的组成部分[1]。磷以磷酸盐(Pi)的形式从根际吸收,由于磷在土壤中的扩散速度缓慢和/或固定为固定的有机磷,植物通常不容易获得磷[2]。有限的Pi可用性对植物的生长发育产生不利影响[3.]。
在拟南芥,缺磷会导致初生根尖的分生组织活性逐渐丧失,从而抑制初生根的生长(PRG) [4]。LPR1(At1g23010)及其近paraLPR2(At1g71040)编码多铜氧化酶(MCOs),是与Pi缺乏介导的PRG抑制相关的主要数量性状位点(qtl) [5,6]。功能丧失突变LPR1而且LPR2影响Pi缺陷介导的PRG抑制[6]。然而,与拟南芥不同的是,缺乏Pi对分类多样性的双子叶和单子叶的PRG没有任何显著影响[7,8]或触发水稻中PRG的增加[9,10]。这些研究表明,磷缺乏介导的PRG抑制并不是在不同植物物种间的全球性反应。这就提出了一个明显的问题,关于同源词的可能作用LPR1/2特别是在水稻等物种中,缺磷对PRG有截然相反的影响。
Nuclear-localizedSIZ1(At5g60410)编码一个小的泛素样修饰子(SUMO) E3 ligase1和sumoylates转录因子(TF)PHR1(At4g28610)在拟南芥中的表达[11]。PHR1在调节Pi 3饥饿响应(PSR)基因的表达中起着关键作用,其启动子富含phr1结合序列(P1BS) motif [12]。PHR1是Pi传感和信号级联的关键上游组件,包括miR399年代,IPS1(At3g09922),PHO2(At2g33770),SPX1(At5g20150), Pi转运体Pht1; 8(At1g20860),Pht1; 9(At1g76430)和其他PSR基因的子集[13- - - - - -15]。有趣的是,两者的推动者LPR1而且LPR2不具有P1BS基序,这表明缺乏对PHR1这些基因的表达。因此,识别tf调节LPR1/2请进一步研究。
水稻是最重要的谷类作物之一,养活了世界上三分之一以上的人口,有时也是卡路里的唯一来源[16,17]。水稻通常在低磷土壤上的雨养系统中种植,这影响了水稻的生长发育,从而影响了产量潜力[16]。因此,破译维持Pi稳态的复杂性,以开发具有更高Pi利用效率的水稻,以实现农业的可持续发展,变得越来越必要。拟南芥和水稻之间Pi饥饿信号转导途径高度保守[17]。在这种情况下,水稻中拟南芥的几个同源物,即,OsPHR2[18,19],OsPHO2[20.,21],OsSPX1而且OsSPX2[22]已被功能表征,是Pi传感和信号级联的关键组成部分[17]。但是,同系词的作用LPR1 /2在水稻体内维持Pi稳态过程中的作用尚未阐明。
在本研究中,鉴定和表达分析OsLPR1-5在大米中进行。系统发育分析显示它们分为两个不同的亚支。这些基因在全磷和缺磷条件下以及其他营养缺乏条件下的差异表达表明它们之间存在功能差异。进一步分析了基因的相对表达量OsLPR3而且OsLPR5在功能丧失突变体中(ossiz1,osphr2而且ospho2)和转基因水稻过表达OsPHR2或OsSPX1揭示了它们在Pi传感和信号级联中的潜在作用。
结果与讨论
比较结构分析lpr在拟南芥和水稻中
以拟南芥LPR1-2蛋白序列为查询对象,在国家生物技术信息中心(NCBI)数据库中进行TBLASTN搜索,在水稻基因组中鉴定出5个同源基因,以下简称为OsLPR1-5。他们的基因座ID, cDNA接入数和蛋白质特征的详细信息列在附加文件中1。OsLPR1-5在1号染色体的短臂上紧密地定位在65kb范围内(附加文件2).采用DNAMAN 7.0程序对其核苷酸和氨基酸进行多序列比对LPR1-2而且OsLPR1-5并确定了它们之间的单位矩阵的百分比(图。1).核苷酸序列同源性(SI)为85%OsLPR3而且OsLPR467.2%介于两者之间OsLPR2而且OsLPR3。氨基酸SI在OsLPR3和OsLPR5之间分别为68.3%和40.9%。分析表明,OsLPR5与OsLPR3相对接近,与OsLPR2相对遥远。核苷酸SILPR1与OsLPR1而且OsLPR4分别为58%和54.1%。氨基酸SI从OsLPR1和LPR1之间的57%到OsLPR5和LPR2之间的44.8%不等。这表明,OsLPR家族的成员在系统发育上彼此之间的关系比与lpr的关系更密切。用于比较分析外显子和内含子的数量和位置lpr从水稻和拟南芥中,它们的全长cDNA序列与相应的基因组DNA序列一致(图2)。1 b).外显子数量从4 (LPR1-2),三个(OsLPR1/2/5)至两个(OsLPR3/4)。在水稻中,最长的外显子长度为1446 bpOsLPR5到1551 bpOsLPR3,两者均为1125 bpLPR1-2。有一个明显的例外OsLPR4的最后一个外显子lpr而且OsLPRs长度54 bp。内含子的数量也有变化,从3个(LPR1-2而且OsLPR5),两个(OsLPR1/2/4)到一(OsLPR3),长度为70 bpLPR2到6123 bpOsLPR2。的5′非翻译区(UTR)OsLPR4/5被内含子破坏了。分析揭示了的散度和守恒LPR拟南芥基因年代和米饭。
的系统发育分析LPR基因
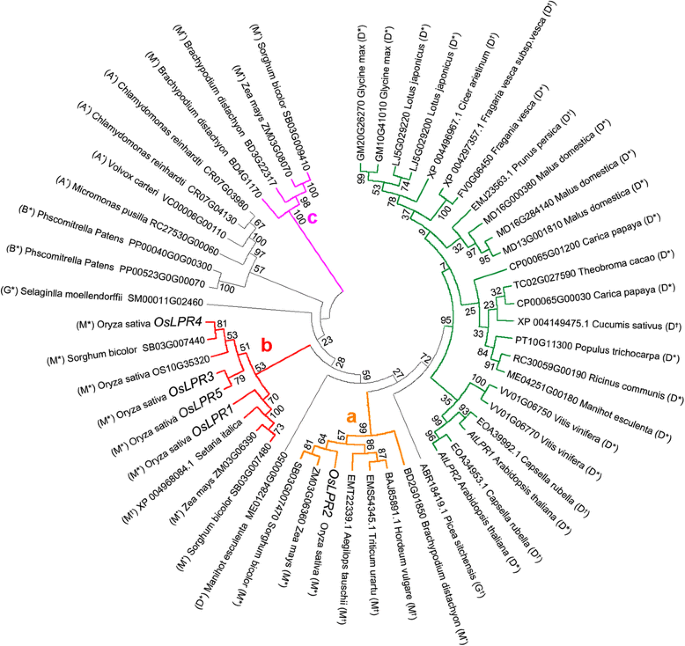
LPR1和LPR2被用作NCBI和PLAZA数据库BLASTP搜索的查询项,该数据库从分类多样性较高的植物(15种双子叶植物、8种单子叶植物和2种裸子植物)和较低的植物(1种苔藓植物和3种藻类植物)中鉴定出53个LPR同源物。利用MEGA 4.0的邻居连接方法重建了所有鉴定同源物的无根系统发育树(图4)。2).单子叶LPR蛋白分为支a、b而且c在系统发育树上分别用黄色、红色和紫色线表示。除了OsLPR2之外,OsLPR1和OsLPR3-5还聚集在一起b与LPRs的进化距离更近高粱二色的(SB03G007440 SB03G007480),Setaria斜体(XP004968084.1)和玉米(ZM03G06390)。OsLPR3和OsLPR5在一个不同的子分支中的分组与它们的高核苷酸和氨基酸SI一致(图。1).在一个子分支中,OsLPR3和OsLPR5是OsLPR1/2/4的内平行子,而不是外平行子。OsLPR2被放在枝中一个以及来自草科成员的lpr,美国二色的(SB03G007470),z梅斯(ZM03G06360),Aegilop stauschii(EMT22339.1),小麦属植物urartu(EMS54345.1),大麦芽(BAJ85891.1)和Brachypodium distachyon(BD2G01850)。在其他单子叶植物中也发现了OsLPR1/2/4的同源物。的进化枝c包括从b . distachyon(BD4G11770 BD3G22317),z梅斯(ZM03G8070)和美国二色的(SB03G009410)表明两个演化支的进化距离都很长一个而且b。虽然所有来自双子叶的LPR都形成了一个不同的分支(绿色),但值得注意的例外是来自双子叶的LPR的位置木薯耐(ME01284G00050)(灰色支)支间一个而且b。AtLPR1和AtLPR2都表现出与LPRs密切的系统发育关系危害风疹(EOA34953.1和EOA39992.1)。裸子植物的LPRs (卷柏moellendorffii)、苔藓植物(Physcomitrella金属盘)和藻类(Micromonas pusilla,Volvox carteri而且衣藻reinhardtii)聚在灰色枝中。从这一系统发育分析可以明显看出,单子叶物种的LPRs密切相关,这表明在单子叶和双子叶分裂之前可能存在重复事件。双子叶植物的LPR平行亲缘关系密切,表明在单子叶和双子叶分裂后发生重复。因此,可以认为OsLPRs的功能可能与其他单子叶植物的直系同源体相似,但与双子叶植物(包括拟南芥)的LPRs不同。总的来说,分析揭示了在分类多样性较高和较低的植物物种中LPRs的保护。
水稻LPR蛋白的cu氧化酶结构域分析
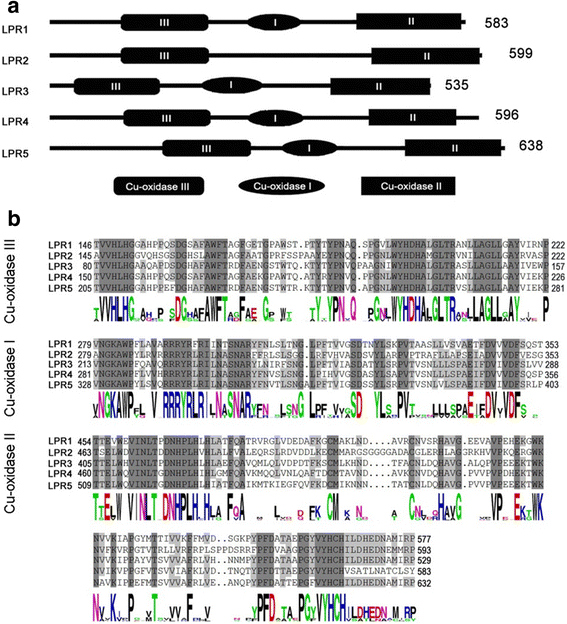
多铜氧化酶(MCO)促进有机或金属离子的氧化,三核铜簇(TNC)参与O的还原2[23]。在拟南芥中,LPR蛋白的MCO活性是在缺磷期间诱导抑制初生根生长的关键[6]。Pfam和NCBI蛋白质数据库(http://pfam.xfam.org/而且http://www.ncbi.nlm.nih.gov/guide/proteins/#databases)用于分析已测序的高等和低等植物LPR蛋白中cu -氧化酶1-3和过氧化物酶的结构域结构(附加文件3.).分析表明,在推测的LPR蛋白中,cu -氧化酶1-3和过氧化物酶结构域的大小和位置存在显著差异b . distachyon(BD4G11770 BD3G22317),z梅斯(ZM03G8070)和美国二色的(SB03G009410)与其他LPR蛋白比较。此外,还分析了OsLPR蛋白中的cu -氧化酶结构域(图。3).在OsLPR1、3、4和5中检测到cu -氧化酶结构域I、II和III,而在OsLPR2中明显缺失cu -氧化酶I结构域。LPR蛋白全长多肽由535 ~ 638个氨基酸组成。使用Clustal X和DNAMAN 7.0程序对OsLPR蛋白的cu -氧化酶I、II和III结构域的氨基酸进行多序列比对(图。3 b).铜氧化酶I、II和III在oslpr中的氨基酸数量分别为74-75、77-78和123-130。分析显示,oslpr中cu -氧化酶的所有三个结构域都具有显著的守恒性,这对于维持其最佳疗效至关重要。通过密歇根州立大学(MSU)水稻数据库(rice.plantbiology.msu.edu/index.shtml)的搜索,确定了另外42个基因(27个漆酶,4个l -抗坏血酸氧化酶和10个单铜氧化酶),这些基因由3个cu -氧化酶域代表。MEGA 4.0用于重建无根树图,揭示这些基因之间的系统发育关系(附加文件)4).分析显示oslpr与单铜氧化酶亚家族的成员相对接近。相反,在拟南芥和水稻中OsLPR蛋白的n端区域显示出相当低的同源性(附加文件)5).
水稻LPR蛋白cu -氧化酶结构域的分析。一个OsLPR蛋白中的cu氧化酶I、II和III结构域分别以椭圆、矩形和圆角矩形表示。编号表示OsLPR蛋白的长度。b水稻LPR蛋白cu -氧化酶I, II和III结构域氨基酸序列的定位。LPR蛋白中相同和相似的氨基酸分别用深灰色和浅灰色背景突出显示。Weblogo确定的共识序列(http://weblogo.berkeley.edu/)显示在底部
组织特异性表达谱OsLPRs
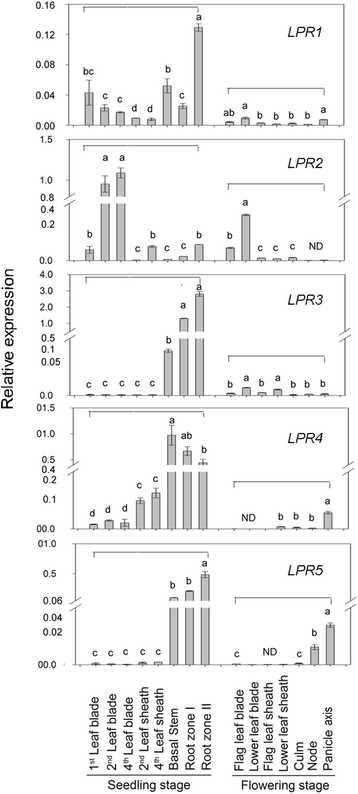
的时空表达模式OsLPRs,分别在苗期(14 d龄)和花期(60 d龄)进行qRT-PCR(图;4).苗期对不同组织(第1、2、4叶片、第2、4叶鞘、基茎和根区I、II区)进行研究。尽管表达OsLPR1在所有被检幼苗组织中均有检测到,其中根区II的含量显著高于其他组织。相反,表达水平OsLPR3而且OsLPR5主要在根区和基茎中表达,在叶片和叶鞘中表达量较低或几乎不表达。的表达OsLPR4基茎区和根区也相对高于叶鞘区和叶片区。高表达水平OsLPR1/3/4/5在根中表明了它们在根际养分获取方面的潜在作用。的表达式OsLPR2在第2和第4叶片显著升高,第1叶片、第4叶鞘和根区II中等,第2叶鞘、基茎和根区i较低OsLPR2在养分的动员下进行射击。在花期,表达模式OsLPRs分别对旗叶片、下叶片、旗叶鞘、下叶鞘、茎、节和穗轴进行了测定。虽然低表达OsLPR1在下叶片和穗轴中可见,在其他组织中几乎不可见。OsLPR2在旗叶和下叶中转录本含量高,在叶鞘(旗叶和下叶)和秆中转录本含量低,在节轴和穗轴中不检测到转录本。的表达式OsLPR3在叶片下部和叶鞘下部相对较高,而OsLPR4穗轴显著高于下叶鞘、茎和节,旗叶、下叶片和旗叶鞘均未发现。在这种情况下OsLPR5,表达模式显示出类似的趋势OsLPR4与其他组织相比,圆锥轴的含量显著升高。Pht1; 1(OsPT1),是13人之一Pht1水稻中的Pi转运蛋白,在根和茎的各种细胞类型中都有丰富的组成性表达(Sun et al., 2012)。因此,OsPT1被用作阳性对照,以确定所有成员的相对表达水平OsLPR21 d龄水稻幼苗不同组织中的科(附加文件)6).总的来说,不同成员的相对表达量OsLPR苗期科数高于花期科数。结果表明,成员可能扮演不同的角色OsLPRs以特定组织和发育的方式。职能上的分歧在各成员之间也很普遍OsPTs(Pi转运体)和OsSPXs(含SPX结构域蛋白)基因家族[17]。
营养缺乏影响基因表达谱OsLPRs
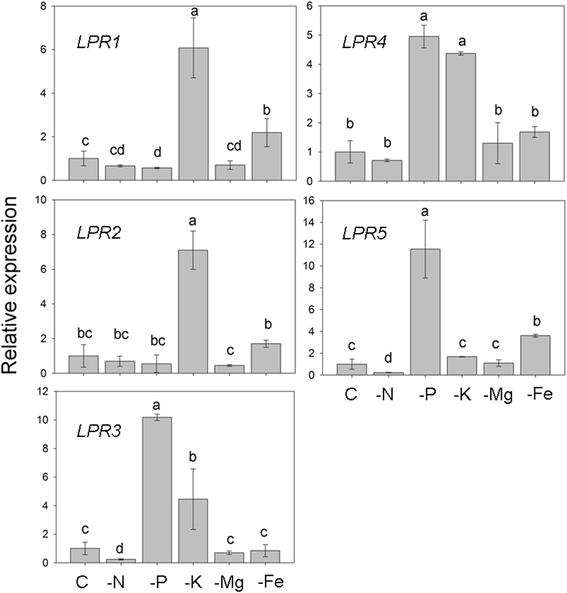
水稻幼苗(14 d龄)分别在完全营养液(C)和不含Pi、氮(N)、钾(K)、镁(Mg)和铁(Fe)的营养液中生长7 d。对这些幼苗的根系进行了相对表达量的测定OsLPRsqRT-PCR(图;5).与C相比,相对表达量OsLPR1在-K和-Fe条件下显著诱导,在-P条件下减弱,在-N和-Mg条件下不受影响。虽然-K引发的相对表达量显著增加OsLPR2,与c相比,其他营养缺乏对其表达水平无显著影响OsLPR3在-P和-K条件下显著诱导,在-N条件下降低,而在-Mg和-Fe条件下不受影响OsLPR4在-P和-K条件下,其表达水平升高,但与c相比,其他营养缺乏对其表达水平无显著影响OsLPR5在-P和-Fe条件下增加,在-N条件下减少,在-K和-Mg条件下与C相当。分析揭示了不同营养缺乏对基因表达水平的可变影响OsLPRs。在不同的营养缺乏症中,磷缺乏症表现出广泛的影响,包括诱导(OsLPR3-5),衰减(OsLPR1)和没有影响(OsLPR2)对这些基因的相对表达量的影响。这提示了它们在调节水稻Pi稳态中潜在的可变和特定的作用。在拟南芥中,LPR1已被证明在抑制初生根生长中发挥关键作用,以响应感知局部Pi剥夺[6,24]。然而,与拟南芥的主根系统不同,水稻具有须根系统[25]而缺乏圆周率会导致其伸长[9,10,26]。这提出了一个相关的问题,关于一个可能的角色,如果有的话,任何pi响应的成员OsLPRs在磷缺乏介导的水稻根系发育反应中。分析其功能缺失突变体可以提供更好的见解,这需要进一步的综合研究。SPX (SYG1/PHO81/XPR1)结构域的基因家族成员也报道了对Pi缺乏的不同反应,这些基因家族成员被指定为OsSPX1-6。在这其中,OsSPX 1、2、3、5而且6对π饥饿有响应[27]。虽然OsSPX4SPX4对Pi缺乏无反应,SPX4与OsPHR2相互作用并负调控Pi信号通路和稳态[28]。在这种情况下,没有响应OsLPR2但不能完全排除其在Pi感测和信号级联中的作用。的相对表达水平增加OsLPR3而且OsLPR4在-P和-K条件下表明这两种营养物质之间有相互作用。在大豆中也观察到P和K之间的类似串扰GmPT年代,Pht1编码Pi转运蛋白的基因家族,均因P和K缺失而上调[29]。在另一项研究中,来自番茄根的1280个基因组成的高密度阵列显示,当缺乏Pi或K时,编码Pi和K转运蛋白的基因协调和共调节[30.]。此外,对拟南芥整体缺磷反应的微阵列分析显示,几个基因的表达水平显著诱导(Kup10, kup11, hak5, kat1而且KEA2)编码不同的K转运蛋白[31]。相对表达中的抑制和诱导OsLPR1分别在-P和-Fe条件下对该基因产生拮抗作用。这一结果与之前的研究一致,即Pi的有效性对水稻铁反应基因的调控有显著影响[26]。此外,铁的有效性也影响了拟南芥中Pi缺乏介导的形态生理和分子反应[31- - - - - -33]。这些研究为水稻和拟南芥中π和Fe的相互作用提供了证据。相反,−N或施加衰减(OsLPR3而且OsLPR5)或无效果(OsLPR1, OsLPR2而且OsLPR4)的相对表达量OsLPRs。的相对表达水平增加OsLPR3而且OsLPR5在-P条件下和-N条件下的抑制表明这两种营养物质在水稻中发生了拮抗串扰。这两种营养物质之间类似的拮抗串音在水稻中很明显,编码硫酸盐转运蛋白1.2 (LOC_Os03g09970)的基因在- p和- n条件下分别上调和下调[34]。拟南芥中P和N信号通路相互作用的证据也越来越多[35- - - - - -37]。总的来说,该研究揭示了不同营养素之间的相互作用,对其产生调节影响OsLPR家庭成员。这与公认的教条是一致的,即缺乏一种营养素会导致其他营养素的不平衡,从而导致它们相关的形态生理和分子反应[38]。相反,各成员的表达水平OsLPRs在缺乏镁期间没有受到影响。
基亚压制OsLPR3/5对水稻缺磷的响应
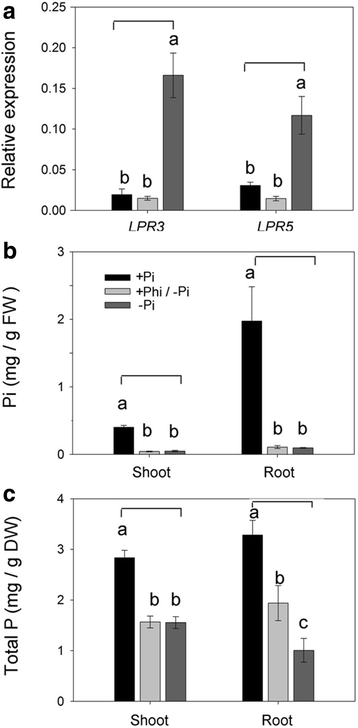
亚磷酸酯(Phi)是Pi的不可代谢类似物。Phi通过Pi转运体被植物吸收,在一定程度上模仿Pi,干扰Pi信号通路,并已被证明在拟南芥中抑制PSR基因的协调表达[39- - - - - -41]。因此,Phi是一个有效的工具,可以确定一个基因是否是控制Pi稳态的传感和信号网络的组成部分。因此,比较Phi和Pi缺乏处理对蛋白相对表达量的影响OsLPR3/5在根部,水稻幼苗(14 d龄)在+ Pi (300 μM Pi)、-Pi (0 μM Pi)和+ Phi/ -Pi (300 μM Phi/ 0 μM Pi)条件下生长3 d(图2)。6).两者的相对表达量均有显著增加OsLPR3/5与+ Pi苗相比,-Pi苗的根含量较高。然而,这些基因在+ Phi/ -Pi根中的相对表达量显著降低,几乎与+ P苗相当。结果提供了证据的参与OsLPR3/5Pi缺乏介导的信号转导。该结果与早期的一项研究一致,该研究报告了饥饿诱导的Pi表达的衰减OsIPS1而且OsIPS2在长期暴露于Phi的大米中[42]。正如预期的那样,与+ Pi苗相比,-Pi苗的根和茎中的Pi和总磷含量显著降低(图2)。6 b, c).+ Phi/ -Pi苗的Pi(茎部和根部)和总磷(茎部)含量也显著降低,与-Pi苗相当。这说明,+ Phi/ -Pi处理和-Pi处理对磷含量和全磷含量的衰减作用相似,但值得注意的是,+ Phi/ -Pi根的全磷含量显著高于+ Pi根和-Pi根。因此,结果提示了Phi在调节Pi稳态的传感和信号级联中的部分影响。
磷缺乏对植物表达谱的短期和长期影响OsLPRs在根部
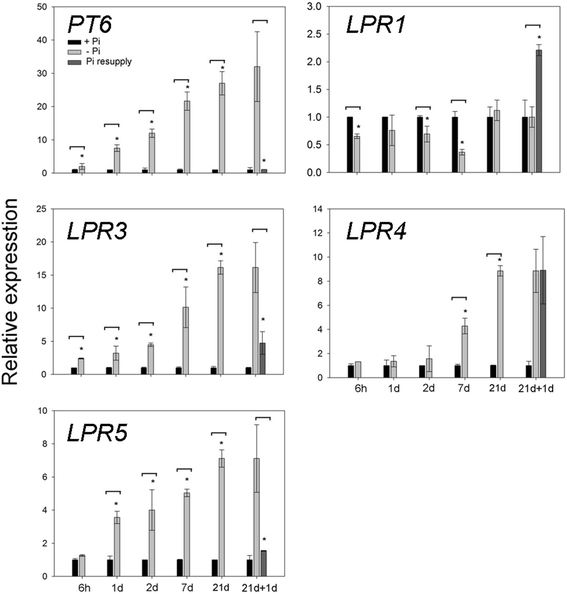
将14 d龄的水稻幼苗分别在+ Pi和-Pi条件下处理6 h、1 d、2 d、7 d和21 d,在-Pi (21 d)处理后再补充+ Pi (1 d)。早先的一项研究报告了-Pi处理21 d后水稻幼苗完全饥饿[43]。高亲和力Pi转运体OsPT6在-Pi处理期间,在根和芽中迅速诱导并维持诱导[44]。因此,OsPT6是验证在+ Pi和-Pi条件下种植水稻幼苗的生长条件保真度的有效基因。采用qRT-PCR法测定基因的相对表达量OsLPRs(1,3.,4而且5),OsPT6在+ Pi和-Pi条件下生长的不同时间间隔和补充+ Pi后的幼苗根部(图。7).相对表达量OsPT6在短期(6 h) -Pi处理期间迅速诱导,在较长时间内相应增强,在向-Pi (21 d)幼苗补充+ Pi (1 d)后迅速减弱。结果为本研究中使用的生长条件的有效性提供了证据,以确定-Pi条件对幼苗相对表达谱的时间影响OsLPRs。与+ Pi相比,的相对表达量OsLPR1在-Pi处理6 h、2 d和7 d时显著减弱,在+ Pi补充后显著诱导。的相对表达量显著增加OsLPR3在短期(6 h) -Pi处理期间,与+ Pi相比,其相对表达水平随着处理时间的增加而增加。虽然相对表达水平OsLPR5短期(6 h) -Pi处理与+ Pi处理相当,但在长期(1d、2d、7 d和21 d) -Pi处理中,其水平显著升高,趋势与+ Pi处理相似OsLPR3。已知许多PSR基因在短期-Pi处理期间被瞬时诱导[45]。相反,诱导在相对表达量上OsLPR3而且5在短期(6 h) -Pi处理过程中,不是短暂的。在拟南芥-Pi响应的全球微阵列分析中,几个参与Pi获取的PSR基因(Pht1; 4;[46])、动员(RNS1;[47])、磷脂替代(SQD2;[48])及根系发育(PLDZ2;[49])也表现出类似的早期和持续诱导模式。两者的相对表达水平均有显著降低OsLPR3而且5在补充+ Pi (1 d)后,在-Pi (21 d)幼苗的根部。这为它们通过Pi有效性的转录调控及其在维持Pi稳态中的潜在作用提供了证据。虽然相对表达量有显著增加OsLPR4在长期(7 d和21 d) -Pi处理中,与+ Pi相比,后续补充+ Pi对其升高的相对表达量没有任何衰减作用。这表明Pi在转录调控中的作用不太可能OsLPR4。总的来说,差异相对表达水平OsLPR1、3、4而且5在短暂的-Pi处理和+ Pi补充后表明它们在Pi感测和信号级联中的特定作用。这并不奇怪,因为一个基因家族的成员通常表现出缺乏功能冗余。例如,Pi转运蛋白家族成员(OsPTs)在-Pi条件下表现出不同的响应,并在维持Pi稳态中发挥不同的作用[44,50- - - - - -53]。
裂根实验揭示了系统Pi感知对相对表达量的影响OsLPR3/5
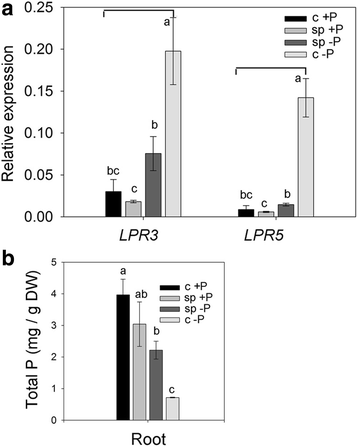
在分根实验中,完整根系的每一半都保持与不同的营养介质接触,这是一种有吸引力的技术,用于确定PSR基因是受外部Pi有效性(局部感知)还是受整个植物的内部Pi状态(系统感知)调控[54]。在拟南芥中,利用该技术鉴定出一系列受局部或全身Pi感测特异性调控的PSR基因[55]。因此,在本研究中,该技术被用于确定局部和全身Pi感知对相对表达水平的影响OsLPR3/5和水稻幼苗根中总磷含量(图;8).在水培系统中,将水稻根系的两半分别浸入+ P (300 μM Pi)或-Pi (0 μM Pi)中,模拟对照植物在均质介质(以下分别称为c + P和c -P)中生长。在另一种设置中,完整根系的每一半分别置于+ P和-Pi营养介质中,分别称为sp + P和sp -P。采用qRT-PCR法测定基因的相对表达量OsLPR3/5在c + P, c -P, sp + P和sp -P条件下生长的幼苗根部(图2)。8).如预期的,相对表达水平OsLPR3/5c -P的根含量显著高于c + P。sp -P根系相对表达量较c -P显著降低,与c + P基本相当。相对表达量OsLPR3/5c + P根和sp + P根具有可比性。这清楚地表明,尽管-Pi培养基中存在sp -P根,但其表达水平OsLPR3/5受全株Pi状态的系统调节。这一结果与早先对拟南芥的研究相反LPR1而且LPR2在PRG的局部Pi传感介导反应中发挥关键作用[6]。这表明功能上的分歧LPR在分类上多样化的拟南芥和水稻科。根组织也分析了总磷含量(图。8 b).全磷含量以c + P和c -P根最高、最低。但有趣的是,sp + P和sp -P的总磷含量差异无统计学意义。根系组织中全磷含量的变化与土壤肥力有关OsLPR3/5表达水平。
OsLPR3/5消极地受到OsPHR2并受到SIZ1 / PHO2 / SPX1-介导的π感应
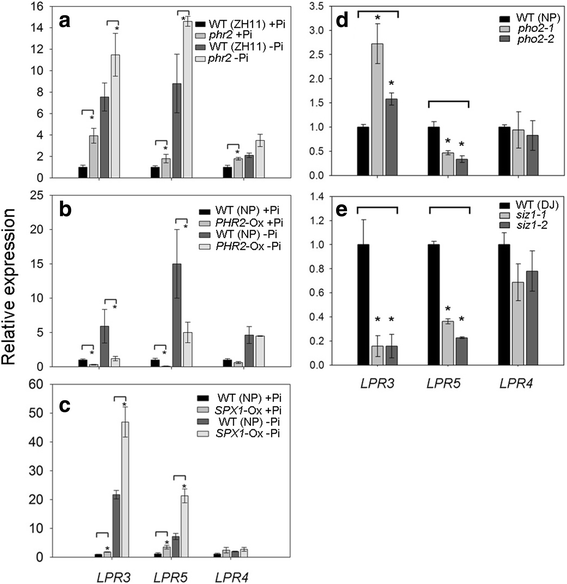
在水稻中,几种转录因子(tf)在PSR基因的转录调控中起着关键作用[3.,17,56]。在这些助教中,OsPHR2是在不同的Pi体制下的本构性表达,并涉及调节Pi信号和稳态[18,19]。以确定是否OsPHR2施加任何监管影响OsLPRs,在野生型(ZH11)和野生型(ZH11)的根中检测其相对表达量osphr2+ P和-P条件下生长的幼苗(图;9).的相对表达量显著增加OsLPR3而且5在根源osphr2在+ P和-P条件下与相应的野生型进行比较。但是,相对表达量有边际但显著增加OsLPR4在根中被检测到osphr2+ P条件下与野生型比较。此外,相对表达水平OsLPR3/4/5的+ P根和-P根比较OsPHR2-牛属植物及其相应的野生类型(图;9 b).虽然相对表达水平OsLPR3而且OsLPR5+ P和-P根均显著减弱OsPHR2-Ox植株与相应野生型相比,在相对表达量上未检测到这种影响OsLPR4。这表明了更明显的负面调控影响OsPHR2关于表达OsLPR3而且5比OsLPR4。有趣的是,的推广者OsLPR4富含P1BS基序,而其他人OsLPRs(1- - - - - -3.)是丰富的W-box主题(附加文件7).在拟南芥Pi缺乏反应的全球微阵列分析中,分析了PSR基因的启动子是否存在P1BS基序[31]。分析显示了几个P1BS基序的PSR基因启动子的富集。此外,我们还发现了一些在-P条件下没有被诱导的基因,尽管存在该基序。例如,紫色酸性磷酸酶基因的启动子(人民行动党)19(At3g46120)和20.(At3g52780)均富集3个P1BS基序,但均未在缺磷过程中表现出诱导作用。在这种情况下,观察到的突变(−P)或过表达(+P和-P)缺乏任何显著影响也就不足为奇了OsPHR2的相对表达水平OsLPR4。的启动子上缺乏P1BS基序OsLPR3/5通过可能调用前馈调控循环(FFRL),表明OsPHR2对它们的负调控。在拟南芥中,tf南/ ATAF1/2 / CUC2016(NAC016;At1g34180)和nac样,ap3 / pi激活(午睡;At1g69490)抑制转录脱落酸响应元件结合蛋白1(AREB1;At1g45249)通过FFRL [57]。的启动子中存在两个W-boxOsLPR3(附加文件7)暗示WRKY tf可能对监管产生影响。在水稻中,WRKY TF超家族有109个成员[58]。最近的研究表明OsWRKY74调节Pi稳态的作用[59]。因此,研究是否OsWRKY74和OsPHR2调节OsLPR3在FFRL中,这值得进一步研究。
转录水平OsSPX1在-P根和茎中诱导OsPHR2-牛属植物表明前者位于后者的下游[60]。另一项研究表明OsSPX1以pi依赖的方式抑制OsPHR2的活性[22]。这些研究共同表明了一个负反馈循环调节OsPHR2通过OsSPX1。的相对表达水平OsLPR3而且OsLPR5显著增加了osphr2+ P和-P条件下(图;9),预期会有相似的表达模式SPX1牛。与这一假设一致,的相对表达水平显著增加OsLPR3而且OsLPR5观察到SPX1+ P和-P条件下的-Ox与相应的野生型相比(图2)。9 c).相反,相对表达量OsLPR4在SPX1-Ox (+P和-P)与野生型相当。这表明OsLPR3而且OsLPR5都是OsPHR2-OsSPX1-介导的Pi稳态调节。
OsPHO2、下游的信号组件OsPHR2,在调控的表达中起关键作用OsPTs和多重磷饥饿反应,从而影响水稻对磷的利用[20.,21]。因此,调节的影响OsPHO2在OsLPR3-5进行调查(图;9 d).的相对表达量显著增加OsLPR3在pho2-1而且pho2-2与野生型相比。增加的表达OsSPX1在根源pho2突变体提示负调控影响OsPHO2在其下游OsSPX1[60]。的相对表达量加重OsLPR3在SPX1牛(无花果。9 c),pho2-1而且pho2-2(无花果。9 d)从而表明它是…的下游OsPHR2-OsPHO2-OsSPX1途径。相反,显著降低而对相对表达量无影响OsLPR5而且OsLPR4,分别在pho2-1而且pho2-2与野生型相比(图;9 d)强调了各成员的不同角色OsLPR家庭OsPHR2-OsPHO2-OsSPX1 -介导的Pi感应。
素酰化是一种关键的翻译后修饰,涉及蛋白质-蛋白质相互作用、转录激活和蛋白质定位[61]。OsSIZ1而且OsSIZ2,拟南芥的同源SIZ1在水稻中,部分补充了形态表型siz1-2拟南芥[62]。此外,参与Pi感知和信号传递的几个基因被调节ossiz1[63]。因此,效果OsSIZ1关于监管OsLPR3-5,进行分析(图;9 e).的相对表达量显著降低OsLPR3而且OsLPR5在这两个siz1-1而且siz1-2与野生型相比。虽然在表达水平上有边际的降低OsLPR4在这些突变体中也有检测,差异无统计学意义。这表明翻译后调节的影响OsSIZ1在OsLPR3而且OsLPR5。然而,目前还不知道是否OsSIZ1对…施加直接的监管影响OsLPR3而且OsLPR5通过sumoylating他们或通过一个靶标介导,这是尚未确定的。功能表征OsLPRs可以深入了解它们在维持Pi稳态中的具体作用,因此值得进一步研究。
结论
本研究对水稻LPR家族成员的基因结构、系统进化和组织特异性表达模式进行了详细的全基因组分析(OsLPR1——OsLPR5).系统发育分析显示它们分为两个不同的亚支。这些基因在缺磷和其他营养物质下的差异表达表明它们之间缺乏功能冗余。进一步深入了解可能的作用OsLPR3而且OsLPR5通过检测其在功能缺失突变体中的相对表达水平(ossiz1, osphr2而且ospho2)和转基因水稻过表达OsPHR2或OsSPX1。因此,本研究的结果为进一步详细的不同成员的功能表征提供了基础OsLPR以阐明它们在缺乏Pi和/或其他营养物质时维持体内平衡的具体作用。
方法
数据库检索,序列比对和系统发育分析
完整的基因组序列和转录本OsLPR1-5检索自密歇根州立大学(MSU)水稻基因组注释项目汇编(v7) (http://rice.plantbiology.msu.edu/).的识别LPR使用tBLASTn程序和PLAZA1.0数据库(http://bioinformatics.psb.ugent.be/plaza/).LPR同源词在双字型中被发现(拟南芥,风疹,番木瓜,西葫芦,黄瓜,牛毛藤,大豆,莲叶,海棠,木薯耐,杨树trichocarpa,碧桃,萝藦,茄属植物lycopersicum,Theobroma可可而且葡萄)、单子叶(长柄剑,短柄剑,大柄剑,水稻,狗尾草,高粱双色,乌拉尔小麦而且玉米)、裸子植物(云杉sitchensis而且卷柏moellendorffii)、苔藓植物(Physcomitrella金属盘)和绿藻(Volvox carteri而且衣藻reinhardtii).的无根系统发育树LPR采用邻域连接法生成同源物,并用MEGA4.0程序进行显示。
植物材料和生长条件
在本研究中,野生型水稻(栽培稻ssp。粳稻品种(Nipponbare、ZH11和Dongjin)、T-DNA插入突变体(ospho2-1/2[21],ossiz1-1/2[63],osphr2[64],分别在Nipponbare、Dongjin和ZH11的背景下表达)和两个纯合过表达子(OsSPX1 -牛(60),OsPHR2 -Ox [Gu未发表的作品]在日本的背景)被使用。为OsPHR2的ORFOsPHR2使用来自日本裸cDNA的特异性引物进行扩增。PCR产物按所述连接到pTCK303载体[44]。通过电穿孔,将结构物转移到根癌土壤杆菌菌株EHA105转化为Nipponbare [65]。在水培实验中,水稻种子用75%乙醇(v/v)表面消毒1分钟,用稀释的(1:3,v/v) NaClO表面消毒30分钟,然后用去离子水彻底冲洗30分钟。种子在25℃的黑暗条件下发芽3 d。水培实验在光周期为16 h(30℃)/8 h(22℃)的生长室内进行,相对湿度保持在70%左右。均匀生长的幼苗(7 d龄)转移到含1.25 mM NH的完整营养液中4没有3., 300 μm kh2阿宝4, 0.35 mM K2所以4, 1mm CaCl2h·22O, 1mm MgSO4h·72O, 0.5 mM Na2SiO3.h·92O, 20 μM Fe-EDTA, 20 μM H3.薄3., 9 μM MnCl2h·42O, 0.32 μM CuSO4h·52O, 0.77 μM ZnSO4h·72O和0.39 μM Na2MoO4h·22O.对于+ P(控制)和-P介质,KH2阿宝4浓度分别为300 μM和0 μM。为了在+ P和-P介质中保持K的等摩尔浓度,KH2阿宝4在+ P介质中用K代替2所以4在-P介质中。对于+ K(对照)和-K介质,300 μM KH2阿宝4和300 μM NaH2阿宝4分别使用。对于+ Mg(对照)和-Mg介质,1 mM MgSO4h·72O和1mm Na2所以4h·72O分别被使用。对-Fe介质,从+ Fe(对照)介质中剔除20 μM Fe- edta;实验全程使用去离子水,并将所有营养液的pH调至5.0。在所有实验中,水培装置中的营养液每3 d更新一次。Pi分根实验中,准备好幼苗,在完整的营养液中生长14 d,然后转移到分根容器中,持续14 d。将单株根系分成相等的两部分,分别放置在不同的容器中,其中一半接受300 μM Pi,另一半不接受任何Pi。对照包括分根处理,根的两半都受到+ Pi (300 μM Pi)和-P (0 μM Pi)的影响。对于Phi处理,幼苗在-Pi (0 μM Pi)中生长21 d。然后均匀生长的幼苗转移到+ Pi (300 μM Pi)、-Pi (0 μM Pi)和+ Phi/ -Pi (300 μM Phi, 0 μM Pi)溶液中培养3 d。
中存在
用Trizol试剂(Invitrogen)从不同组织中分离总rna,用oligo (dT)-18引物和逆转录酶合成第一链cDNA。OsActin(加入。qRT-PCR分析以AB047313)为内对照。qRT-PCR分析使用SYBR green master mix (Vazyme)和ABI StepOnePlus序列检测系统(Applied Biosystems)从生物三拷贝中进行。用于qRT-PCR的引物列在附加文件中8。
测量植物中Pi和总磷浓度
为了测量植物中的Pi浓度,使用约0.5 g Fresh样品定量植物中的Pi浓度,如所述[18]。用H消化干样(0.05 g)测定总磷浓度2所以4- h2O2在280°C,然后用钼蓝测定,如所述[66]。
统计分析
采用SPSS 13程序对数据进行方差分析(ANOVA)。突变体与WT直方图上的不同字母或星号和/或不同处理在Duncan多重极差检验中表示差异有统计学意义P< 0.05。
缩写
AREB1,脱落酸响应元件结合蛋白1;铁、铁;FFRL,前馈调节回路;钾、钾;LTN1,叶尖坏死1;LPR1,低磷根t1;Lpsi,局部磷酸盐感知受损;镁、镁;MCOs,多铜氧化酶;MSU,密歇根州立大学;N,氮;NAC016、南/ ATAF1/2 / CUC2016;打盹,nac样,ap3 / pi激活;国家生物技术信息中心;牛,overexpressing;磷、磷;π,磷酸;φ,亚磷酸盐;−P,缺Pi;P1BS, phr1结合序列;PSR, Pi饥饿响应;PRG,初生根生长; PAP, purple acid phosphatase; SUMO, small ubiquitin-like modifier; qRT-PCR, quantitative real-time PCR; QTLs, quantitative trait loci; SI, sequence identity; TF, transcription factor; TNC, trinuclear Cu cluster; UTR, untranslated region
参考文献
- 1.
Raghothama公斤。磷酸的收购。植物化学学报,1999;50:366 - 366。
- 2.
Veneklaas EJ, Lambers H, Bragg J, Finnegan PM, Lovelock CE, Plaxton WC, Price CA, Scheible WR, Shane MW, White PJ,等。提高农作物磷利用效率的机会。新植物,2012;195:306-20。
- 3.
López-Arredondo DL, Leyva-González MA, González-Morales SI, López-Bucio J, Herrera-Estrella .磷营养:提高作物的低磷耐受性。植物科学进展。2014;
- 4.
Sánchez-Calderón L, López-Bucio J, Chacón-López A, Cruz-Ramírez A, nietojacobo F, Dubrovsky JG, herrira - estrella L.磷酸盐饥饿诱导植物根系发育的决定程序拟南芥。植物物理学报,2005;26(4):344 - 344。
- 5.
李志刚,李志刚,李志刚,李志刚,等。磷素胁迫下水稻根系生长的QTL鉴定拟南芥。植物细胞环境学报。2006;29:115-25。
- 6.
Svistoonoff S, Creff A, Reymond M, sigoilot - claude C, Ricaud L, Blanchet A, Laurent Nussaume L, Thierry DT。根尖与低磷介质接触会改变植物的根结构。Nat Genet, 2007; 39:792-6。
- 7.
李志强,李志强,李志强,等。缺磷对植物根系形态的影响。在:Scaife A,编辑。植物营养学,第2卷。Slough:联邦农业局;1982.412 - 7页。
- 8.
缺磷对玉米根系生长发育的影响。中国科学(d辑),1999;
- 9.
Shimizu A, Yanagihara S, Kawasaki S, Ikehashi H.水稻缺磷诱导根系伸长及其QTL (栽培稻l .)。应用理论,2004;109:1361-8。
- 10.
易克坤,吴志春,周娟,杜丽明,郭伯林,吴玉玲,吴平。水稻耐磷饥饿转录因子OsPTF1的研究进展。植物科学学报,2005;
- 11.
Miura K, Rus A, Sharkhuu A, Yokoi S, Karthikeyan AS, Raghothama KG, Baek D, Koo YD, Jin JB, Bressan RA,等。拟南芥SUMO E3连接酶SIZ1控制磷酸盐缺乏反应。中华自然科学杂志,2005;42(2):366 - 366。
- 12.
Rubio V, Linhares F, Solano R, Martin AC, Iglesias J, Leyva A, Paz-Ares J.在维管植物和单细胞藻类中参与磷酸饥饿信号的MYB转录因子。Gene Dev. 2001; 15:2122-33。
- 13.
Bari R, Pant BD, Stitt M, Scheible WR。PHO2、microRNA399和PHR1定义了植物中的磷酸盐信号通路。植物物理学报。2006;41:988 - 99。
- 14.
Franco-Zorrilla JM, Valli A, Todesco M, Mateos I, Puga MI, Rubio-Somoza I, Leyva A, Weigel D, García JA, Javier Paz-Ares J.靶标拟态为microRNA活性调控提供了一种新的机制。Nat Genet, 2007; 39:1033-7。
- 15.
Puga MI, Mateosa I, Charukesi R, Wang ZY, Franco-Zorrilla JM, de Lorenzo L, Irigoyen ML, Masiero S, Bustos R, Rodríguez J,等。SPX1是拟南芥中磷酸盐饥饿反应的磷酸盐依赖抑制剂1。中国科学院学报(自然科学版),2014;
- 16.
Gamuyao R, Chin JH, Pariasca-Tanaka J, Pesaresi P, Catausan S, Dalid C, Slamet-Loedin I, Tecson-Mendoza EM, Wissuwa M, Heuer S。大自然。2012;488:535-9。
- 17.
吴鹏,寿海霞,徐国华,连小明。在了解磷信号和稳态的基础上提高水稻磷效率。中国植物学报,2013;16(3):344 - 344。
- 18.
周杰,焦长峰,吴志才,李友友,王晓明,何新伟,钟文琴,吴萍。OsPHR2参与植物幼苗磷饥饿信号传导和过量磷酸盐积累。植物物理学报。2008;46:1673 - 86。
- 19.
郭明敏,阮文伟,李春春,黄福龙,曾敏,刘友友,于燕,丁小明,吴yr,吴志才,等。磷酸盐反应1亚家族在水稻磷酸盐信号转导和稳态中作用的综合比较。植物科学进展。2015;
- 20.
胡斌,朱清泉,李峰,唐建勇,王永强,林阿华,刘立龙,车荣荣,褚成昌。叶尖NECROSIS1在水稻多重磷饥饿反应调控中起关键作用。植物学报。2011;156:1101-15。
- 21.
曹颖,闫颖,张峰,王海德,顾敏,吴晓荣,孙珊珊,徐国华。对OsPHO2基因敲除突变体的精细鉴定揭示了其在水稻Pi利用中的关键作用。中国生物医学工程学报。2014;
- 22.
王志智,阮文伟,史俊,张磊,向东,杨超,李春春,吴志才,刘勇,于亚,等。水稻SPX1和SPX2通过与PHR2相互作用,以磷酸盐依赖的方式抑制磷酸盐饥饿反应。中国科学院学报(自然科学版),2014;
- 23.
王永明,王永明,王永明2还原成H2通过多铜氧化酶。Dalton Trans. 2008; 30:3921-32。
- 24.
Müller J, Toev T, Heisters M, Teller J, Moore KL, Hause G, Dinesh DC, Bürstenbinder K, Abel S.铁依赖性胼胝质沉积调节根分生组织维持与磷素有效性。生物工程学报。2015;33:216-30。
- 25.
杨晓明,杨晓明,杨晓明,杨晓明。水稻根系发育的遗传控制研究。植物科学进展,2010;15:219-26。
- 26.
郑玲,黄峰,纳赛,吴娟,吉罗,何峰,程林,王芳,吴萍,惠兰,等。水稻幼苗铁磷相互作用的生理和转录组分析。植物科学进展。2009;
- 27.
王震,胡辉,黄海军,段凯,吴志才,吴鹏。OsSPX1和OsSPX3对水稻OsSPX结构域基因表达及pi饥饿信号的调控。中国生物工程学报,2009;
- 28.
吕启东,钟玉杰,王毅刚,王泽宇,张磊,史杰,吴志春,刘勇,毛长志,易克坤,吴萍。水稻SPX4通过与PHR2相互作用负向调控磷酸盐信号通路和稳态。植物学报。2014;26:1586-97。
- 29.
秦玲,郭艳霞,陈丽丽,梁荣科,顾明,徐国华,赵娟,Walk T,廖慧。酵母14个Pht1家族基因的功能表征及其在大豆营养饥饿响应中的表达。科学通报。2012;7,e47726。
- 30.
王永华,Garvin DF, Kochian LV。番茄根系磷、钾和铁缺乏时快速诱导调节和转运基因:相声和根/根际介导信号的证据。植物科学学报,2002;30(2):366 - 366。
- 31.
Misson J, Raghothama KG, Jain A, Jouhet J, Block MA, Bligny R, Ortet P, Creff A, Somerville S, Rolland N,等。全基因组转录分析使用拟南芥Affymetrix基因芯片确定了植物对磷酸盐剥夺的反应。中国科学院学报(自然科学版)2005;
- 32.
沃德JT,兰纳B,雅库波娃E,索尔特DE,拉戈塔马KG。缺磷时期铁对拟南芥初生根伸长的影响。植物学报。2008;147:1181-91。
- 33.
Rai V, Sanagala R, Sinilal B, Yadav S, Sarkar AK, Dantu PK, Jain A.铁的有效性影响磷酸盐缺乏介导的反应,以及与生长素和锌的交叉作用的证据。中国生物医学工程学报,2015;
- 34.
蔡慧敏,谢文文,连小明。氮磷胁迫下水稻差异表达基因的比较分析。植物生物学杂志2013;31:160-73。
- 35.
康德,彭,罗斯坦。NLA和MicroRNA827对拟南芥维持硝酸盐依赖性磷酸盐稳态的遗传调控PLoS Genet, 2011;7, e1002021。
- 36.
杨晓明,李志刚,李志刚。氮磷相互作用与细胞分裂素的关系拟南芥和pdr1突变体。植物科学进展(英文版);
- 37.
AtNIGT1/HRS1在拟南芥根尖整合硝酸盐和磷酸盐信号。AtNIGT1/HRS1整合硝酸盐和磷酸盐信号。国家公共,2015;6:6274-84。
- 38.
Schachtman DP, Shin R.营养传感和信号:NPKS。植物生物学,2007;58:47-69。
- 39.
亚磷酸酯对拟南芥磷素饥饿反应的抑制。植物物理学报2001;127:963-72。
- 40.
Varadarajan DK, Karthikeyan AS, Matilda PD, Raghothama KG。亚磷酸酯是磷酸盐的类似物,在磷酸盐饥饿的情况下抑制基因的协调表达。植物科学学报,2002;29(4):344 - 344。
- 41.
Jost R, Pharmawati M, Lapis-Gaza HR, Rossig C, Berkowitz O, Lambers H, Finnegan PM。区分磷依赖和磷不依赖的系统性磷饥饿反应网络拟南芥通过亚磷酸酯的应用。中国科学(d辑),2015;
- 42.
侯晓玲,吴鹏,焦长峰,贾庆军,陈红梅,于军,宋晓文,易建坤。的表达规则OsIPS1而且OsIPS2通过系统和局部的Pi信号和激素植物学报。2005;28:353-64。
- 43.
吴鹏,李志刚,李志刚,李志刚,李志刚。水稻根、芽对磷胁迫响应的时空转录谱分析。《植物科学》2013;
- 44.
艾晓辉,孙珊珊,赵金娟,范晓荣,辛文杰,郭强,于林,沈绍荣,吴萍,Miller AJ,等。两种水稻磷酸盐转运蛋白OsPht1;2和OsPht1;6在吸收和转运过程中具有不同的功能和动力学性质。植物学报(英文版);
- 45.
Hammond JP, Bennett MJ, Bowen HC, Broadley MR, Eastwood DC, May ST, Rahn C, Swarup R, Woolaway KE, White PJ。拟南芥幼苗在磷酸盐饥饿过程中基因表达的变化及培育智能植物的潜力。植物学报。2003;32:578 - 96。
- 46.
申H,申HS, Dewbre GR, Harrison MJ。拟南芥中的磷酸盐转运:Pht1;1和Pht1;4在低磷和高磷环境下的磷酸盐获取中都起主要作用。植物J. 2004; 39:629-42。
- 47.
巴里奥拉PA,霍华德CJ,泰勒CB, Verburg MT,亚格兰VD,格林PJ。拟南芥核糖核酸酶基因RNS1在磷酸盐限制下受到严格控制。植物J. 1994; 6:673-85。
- 48.
于波,徐春春,本宁。拟南芥亚砜合成酶SQD2编码中断对磷酸限制生长的影响。自然科学学报(英文版)2002;
- 49.
Cruz-Ramírez A, Oropeza-Aburto A, Razo-Hernández F, Ramírez-Chávez E, Herrera-Estrella L.磷脂酶DZ2在拟南芥根的塑外半乳糖生物合成和磷酸盐循环中发挥重要作用。中国科学院学报(自然科学版),2006;
- 50.
孙珊珊,顾敏,曹颖,黄雪鹏,张旭,艾伟辉,赵金娟,范小荣,徐国华。一种本构表达的磷酸盐转运蛋白OsPht1;1可调节全磷水稻的磷酸盐摄取和转运。植物科学学报。2012;39(2):344 - 344。
- 51.
王晓峰,王玉峰,Piñeros MA,王铮,王伟,李春,吴铮,Kochian LV,吴萍。磷酸盐转运蛋白OsPHT1;9和OsPHT1;10参与水稻的磷酸盐吸收。植物生态学报。2014;37:1159-70。
- 52.
李奕婷,张静,张旭,范宏明,顾敏,曲海燕,徐国华。水稻中磷转运体OsPht1;8在磷从源器官到库器官的再分配以及种子胚和胚乳之间的分配中起着重要作用。植物科学通报2015;230:23-32。
- 53.
张峰,孙玉峰,裴文祥,贾恩阿,孙锐,曹勇,吴晓荣,姜涛,张磊,范晓荣,等。OsPht1;4参与磷酸盐的获取和动员促进水稻胚胎发育。植物学报(英文版);
- 54.
Burleigh SH, Harrison MJ。的下调Mt4样基因通过磷肥系统发生,并涉及到磷酸盐向芽的转运。植物科学学报,1999;19(3):344 - 344。
- 55.
Thibaud MC, Arrighi JF, Bayle V, Chiarenza S, Creff A, Bustos R, Paz-Ares J, Poirier Y, Nussaume L.拟南芥对磷酸盐饥饿的局部和全系统转录反应解剖。植物J. 2010; 64:775-89。
- 56.
Jain A, Nagarajan VK, Raghothama KG。高等植物获取磷酸盐的转录调控。中国生物医学工程学报(自然科学版)2012;
- 57.
樱叶勇,金玉生,韩胜,李伟德,白忠忠。拟南芥转录因子NAC016通过抑制促进干旱胁迫响应AREB1通过涉及NAP的三叉前馈调控环进行转录。植物学报。2015;27:17 - 87。
- 58.
刘勇,沈庆杰。的WRKY水稻基因家族。中国植物学报。2007;49:827-42。
- 59.
戴晓霞,王友友,张文辉。WRKY转录因子OsWRKY74调控水稻抗磷饥饿能力。中国机械工程学报,2015;
- 60.
王超,应生,黄海军,李凯,吴鹏,寿海霞。OsSPX1参与水稻磷酸盐稳态的研究。植物学报(英文版);2009;
- 61.
三浦K,长谷川总理。植物中的素酰化和其他泛素样翻译后修饰。细胞生物学,2010;20:223-32。
- 62.
Park HC, Kim H, Koo SC, Park HJ, Cheong MS, Hong H, Baek D, Chung WS, Kim DH, Bressan RA,等。水稻中SIZ/ pias型SUMO E3连接酶、OsSIZ1和OsSIZ2的功能表征植物细胞环境。2010;33:23 23 - 34。
- 63.
王海德,孙锐,曹勇,裴文祥,孙玉峰,周辉,吴晓宁,张峰,罗林,沈清海,等。OsSIZ1是一个SUMO E3连接酶基因,参与调控水稻对磷和氮的反应。中国生物医学工程学报,2015;
- 64.
陈建勇,刘颖,倪娟,王玉峰,白玉华,史军,甘军,吴志成,吴萍。OsPHF1调控水稻低亲和和高亲和无机磷酸盐转运蛋白的质膜定位,并决定水稻无机磷酸盐的吸收和转运。植物物理学报。2011;157:269-78。
- 65.
Upadhyaya NM, Surin B, Ramm K, Gaudron J, Schunmann PHD, Taylor W, Waterhouse PM, Wang MB。农杆菌属利用改良的启动子和可选择标记对澳大利亚水稻品种Jarrah和Amaroo进行介导转化。植物学报。2000;27:201-10。
- 66.
贾海峰,任海燕,顾敏,赵金娟,孙素生,张旭,陈建勇,吴鹏,徐国华。磷酸盐转运体基因OsPht1;8参与水稻的磷酸盐稳态。植物学报。2011;156:1164-75。
致谢
国家自然科学基金项目(31172014)、国家转基因植物研发计划项目(2014ZX08 009-003-005、2014ZX0800931B、2016ZX08009-003-005)、江苏省自然科学基金项目(BK20141367)、教育部创新科研团队发展计划项目(IRT1256)和111项目(编号12009)资助。我们也感谢印度政府科技部生物技术部授予A.J. Ramalingaswamy奖学金[BT/HRD/35/02/26/2009]。我们也感谢Viswanathan Satheesh在准备和修改本手稿期间提出的宝贵建议和纠正。
数据和材料的可用性
所有支持目前发现的数据都包含在手稿中。
作者的贡献
YC参与了实验的策划和实施,进行了生物信息学分析,并帮助撰写了手稿。HA进行了一些实验。AJ参与了数据的分析,并帮助撰写了稿件。XW, LZ和WP参与了不同的实验。AC有助于生物信息学分析。GX参与了这项研究的规划。SS构思了这项研究,参与了数据的规划和分析,并帮助撰写了手稿。所有作者都阅读并批准了最终的手稿。
相互竞争的利益
作者宣称他们之间没有利益冲突。
发表同意书
不适用。
伦理批准并同意参与
不适用。
作者信息
从属关系
相应的作者
附加文件
附加文件1:
各成员的基因座ID、cDNA接入数和蛋白质特征的详细信息OsLPR基因家族。(dok33kb)
附加文件2:
示意图显示的位置OsLPR1-5水稻染色体1上。(DOC 84kb)
附加文件3:
的域结构分析lpr在不同的植物种类中。(DOC 101kb)
附加文件4:
水稻MCO家族成员的系统发育分析。(DOC 288kb)
附加文件5:
水稻和拟南芥LPR蛋白氨基酸序列的比对。(DOC 390kb)
附加文件6:
OsLPRs表现出组织特异性表达。(DOC 75kb)
附加文件7:
独联体的启动子中的元素OsLPRs。(DOC 78 kb)
附加文件8:
qRT-PCR分析所用引物OsLPR沙子OsPT6。(DOC 32kb)
权利和权限
开放获取本文根据创作共用属性4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),允许在任何媒介上不受限制地使用、分发和复制,前提是您对原作者和来源给予适当的赞扬,提供到创作共用许可证的链接,并注明是否进行了更改。创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)除另有说明外,适用于本条所提供的资料。
关于本文
引用本文
曹,Y, Ai, H, Jain, A。et al。的鉴定和表达分析OsLPR家庭揭示了潜在的作用OsLPR3而且5维持水稻中磷酸盐的稳态。BMC植物生物学16日,210(2016)。https://doi.org/10.1186/s12870-016-0853-x
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12870-016-0853-x
关键字
- 大米
- 缺磷
- OsLPR家庭
- OsLPR3
- OsLPR5
- 磷酸体内平衡