摘要
背景
鳄梨(Persea美国磨坊)是全球重要的商业水果作物。生产的主要限制是卵菌疫霉、肉桂它会导致根腐病,导致树枝枯萎和树木死亡。果园的衰败感染了p、肉桂当遇到洪水时,即使洪水只是短暂的,也会发生得更快。淹水是一种多因子胁迫,由多个个体胁迫综合而成,使耐涝品种的选育具有挑战性。随着越来越多的种植园出现在灌溉和排水不完善的边缘地区,了解鳄梨对这些压力的反应对该行业来说非常重要。
结果
通过糖酵解相关转录本的上调和乙醇发酵相关转录本的诱导,我们发现能量生产的维持是对洪水反应的核心。能量密集型过程通常被下调,与次级细胞壁生物合成以及防御相关转录本等过程相关的转录本受到抑制就是明证。研究发现,暴露在洪水中的牛油果根部水通道蛋白下调,表明在这些条件下水分吸收减少。
结论
牛油果对洪水和水的转录组反应p、肉桂采用微阵列分析进行研究。与洪水引起的转录组扰动相比,病原体存在引起的转录组差异很小。鳄梨对洪水的转录组反应揭示了几个物种对洪水的保守反应。这些数据可以提供关键信息,可用于改进鳄梨产业中耐胁迫砧木的选择。
背景
洪水是一种复杂的压力,可由自然洪水、大量降雨、过度灌溉或地下水位过高引起[1]。它包括几个单独的压力,包括缺氧、土壤pH值的变化和病原体活性的增加,所有这些都有助于植物所经历的整体压力[2]。这导致光合作用减少,气孔关闭,根系导水能力下降,导致生长和产量下降[3.,4]。洪水胁迫的多因素特性使具有重要商业价值的作物耐受性品种的开发具有挑战性。5]。一般来说,天然耐水植物要么利用一种机制使淹水组织重新通气,要么在淹水消退后保存能量以恢复生长。6- - - - - -8]。在淹水条件下,缺氧是制约植物正常生长的主要因素。氧可用性降低限制了线粒体呼吸,导致糖酵解产生的ATP需求增加[4,9]。在这些条件下,发酵可使NAD再生+为了维持糖酵解,从而产生能量。然而,通过发酵产生的ATP(每摩尔葡萄糖2 mol ATP)比线粒体呼吸产生的ATP(每摩尔葡萄糖38 mol ATP)少得多。这导致了植物的能量短缺,需要更高水平的发酵来维持能量平衡[10]。事实上,在一些物种中,糖酵解酶编码基因的诱导率更高,以应对洪水,包括拟南芥、水稻及杨树[11]。与此同时,与线粒体呼吸相关的转录本也受到抑制。糖酵解通量的增加代表了一种补偿机制,目的是在限氧条件下增加ATP的产量[12]。然而,糖酵解和发酵的压力增加会导致对碳水化合物的需求增加和储备的消耗('巴斯德效应')[4]。在这些条件下,光合作用的下降加剧了这种情况[13]。植物通过发酵维持能量平衡的能力是耐水植物的特征[4]。
在水淹期间,一些物种的气孔导度下降,而水力导度的降低被认为是导致这些下降的原因,因为根系吸水和随后向嫩枝的输送受到了水淹的影响[14]。这些减少通常是早期的反应[15]并且在易受洪水影响的植物中更为明显。根系水力导度降低,高度依赖于环境条件[16],可能是由于根系受损或水通道膜蛋白水通道蛋白活性或表达降低[4,17]。这些是多功能蛋白质,可运输水、气体、硼、硅和活性氧(ROS) [16]。这些蛋白质促进土壤水分的吸收,并可大大提高根系的水力传导率(> 60%)[16,17]而降低这些基因的表达可能会限制水通道蛋白的功能[18]。洪水期间,水分吸收的中断会对植物的生长和生存产生不利影响。
鳄梨(Persea美国Mill.)因其富含石油的果实而在世界各地种植。但易受水浸影响[19,20.],即使是短暂的洪水也会造成严重的破坏。对鳄梨生产的最大威胁是由卵菌病原体引起的疫霉、肉桂兰德。这种病原体攻击鳄梨植物的喂食根,导致根腐病(PRR),导致树枝枯死,最终导致树木死亡。洪水加剧了PRR的疾病进展,造成树木更快的衰退和更大的产量损失[21,22]。目前,商业生产者利用与商业接穗嫁接的耐PRR砧木,以最大限度地减少由PRR引起的损害p、肉桂.虽然这些砧木在排水良好的土壤中是有效的,但在经历短暂洪水的地区,它们不一定表现良好。对浸水的耐受性似乎是由砧木决定的,而不是接穗。23,24]。选择对洪水和洪水有耐性的砧木p、肉桂将极大地造福于该行业,但目前的PRR耐受性选择方案并没有考虑对洪水的耐受性。
评估牛油果对洪水反应的分子研究是有限的,没有大规模的表达研究。本研究的目的是研究一种耐PRR砧木的转录组反应,该砧木以前被证明易受洪水影响。的影响p、肉桂研究人员还调查了洪水之前土壤中的存在,以确定这是否会导致被洪水淹没的鳄梨树更快地衰退。在这项工作中,使用定制的鳄梨安捷伦阵列进行了基因表达的全局分析。
方法
植物材料和RNA分离
在南非比勒陀利亚大学林业和农业生物技术研究所(南纬25°45' 19.63",东经28°14' 7.75",比勒陀利亚大学)的温室(平均最高温度24.9°C,平均最低温度13.7°C)中,在2升容器中培养1年无性系‘Dusa™’植株(威斯特法利技术服务公司,南非Tzaneen)。植物每周浇水3-4次,并补充Hoagland的溶液[25每周一次。治疗分为四组;对照植物(C)、侵染植物(I)、淹水植物(F)和淹水和侵染混合暴露植物(FI)。试验采用随机区组设计,每个处理在每个时间点进行三个生物重复,每个生物重复由两株植物组成。疫霉、肉桂被隔离在南非林波波岛的Tzaneen的牛油果果园的商业街区。进行了评估疾病发展的预试验,以确认分离株的致病性。接种与p、肉桂使用2.5 × 104先前报道的游动孢子/ml [26]。为了使侵染建立,植物在侵染后7天被淹。通过将植物浸泡在装满自来水的塑料水库中,使其低于盆栽介质1厘米。通过重新分离病原体和随后使用物种特异性LPV3引物证实感染[27]。根系样本分别在淹水开始的6个时间点(0、8、22、48、96 h和7天)收获,并立即在-80°C下储存。提取并纯化总RNA [26]。总RNA浓度和完整性使用NanoDrop®ND-1000 (NanoDrop Technologies Inc., Montchanin, USA)分光光度计和非变性2% TAE琼脂糖凝胶以及Bio-Rad Experion™自动电泳系统(Bio-Rad, CA, USA)进行评估。
微阵列分析
会议纪要新创牛油果根部转录组在洪水和p、肉桂感染(26]用于探针设计。从这些数据中,选择了6141个带注释的contig和1987个单例Persea美国.另外还包括516个未注释contigs的双向序列。因此,根据Reeksting 2014年的描述,总共选择了9160份牛油果转录本用于探针设计。数组上表示的唯一转录本总数为9625,其中包括465p、肉桂基因。这些病原基因是根据其在致病性中的作用而选择的。序列被上传到安捷伦eArray (https://earray.chem.agilent.com/earray/)网站FASTA格式,使用SurePrint HD格式载片(8x15K)与60多聚寡核苷酸设计探针。特征布局随机化,空特征填充随机重复探针。安捷伦连接器序列包括在每个探针的3 '端。从每个治疗和时间点提取2 μg RNA,形成一个共同的参考池。4 ~ 6 μg RNA用于第一链cDNA合成。使用Superscript™III逆转录酶(Invitrogen)按说明书合成单链cDNA,总体积为30 μl。第一链合成用随机非分子(N9(Inqaba Biotec, Sunnyside,南非)和oligo(dT) (dT23VN, Inqaba)引物。cDNA清除使用RNA清除试剂盒(Qiagen RNeasy®MinElute™)去除水解RNA。使用Nanodrop®ND-1000测定cDNA的浓度和纯度。样品干燥在真空内(SpeediVac)在50°C。球团再次溶解在100 mM NaHCO中3.缓冲液(0.2 M Na2有限公司3., 0.2 M NaHCO3.样品用Cy5标记,参比用Cy3标记(CyDye后标记活性染料包,GE Healthcare Life Sciences)。用3m NaOAc (pH 5.2)终止反应。根据制造商的说明,使用RNeasy®MinElute™cleanup kit (Qiagen)去除多余的染料。标记cDNA用30 μl RNase-free H洗脱2阿水。根据基于双色微阵列的基因表达分析方案(Agilent)计算产量和比活性,并进行杂交。使用Axon GenePix 4000B扫描仪(Molecular Devices, CA, USA)扫描微阵列载片,并使用Axon GenePix 6.0软件(Molecular Devices)进行图像评估。GenePix Array List (GAL)文件由Agilent生成并加载到GenePix中,链接每个打印点的信息以分析结果。在使用软件进行自动点位检测后,进行手动特征比对以验证点位的发现。特征的标记基于饱和度和信噪比(SNR)。两个通道中信噪比< 2的特征被排除,前景饱和度> 20%的特征也被排除。本研究的数据集可从NCBI的基因表达Omnibus通过GEO系列登录号GSE81297 (http://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE81297)根据MIAME指南。
统计分析
微阵列数据线性模型,www.bioconductor.com)包在R版本3.1.0环境中使用(R基础统计计算,http://www.R-project.org),对微阵列数据进行统计分析。背景校正使用LIMMA中的' normexp '函数,偏移量为50 [28]。采用鲁棒样条归一化方法进行阵列内归一化。Gquantile归一化用于数组之间的归一化。通过拟合LIMMA中每个基因的线性模型(lmFit)来估计折叠变化和标准误差。对标准误差(eBayes)进行经验贝叶斯平滑。最后,P-值使用错误发现率(FDR)校正进行多次测试。标准的成对皮尔逊相关(r)使用归一化m值来确定生物重复之间的一致性。目标被定义为不同的表达,如果日志2比值大于等于1或小于等于-1 (log2比值≥1,log2比例≤-1)和调整后的P-value小于或等于0.05 (P≤0.05)。
功能注释、聚类和路径分析
利用台式cDNA annotation System (dCAS)软件(v 1.4.3)对微阵列上的靶标进行功能标注[29]。描述生物过程、分子功能和细胞成分的基因本体(GO)术语使用Blast2GO软件(B2G;http://www.blast2go.com).使用默认参数,截断FDR为0.05。维恩图是用Venny (http://bioinfogp.cnb.csic.es/tools/venny/index.html).使用Multi Experiment Viewer (MeV) 4.8.1版本,通过平均链接进行分层聚类[30.]。
RT-qPCR
利用RT-qPCR对微阵列分析得到的基因表达水平进行验证。根据制造商说明书(Promega Corporation, Madison, USA),使用ImProm-II™单链cDNA系统合成单链cDNA。随机六聚体(0.5 μg, Invitrogen Life Technologies, California, USA)用于第一链合成。内含子黄酮-3-羟化酶(F3H)引物F3H F 5 ' -TCTGATTTCGGAGATGACTCGC-3 '和F3H R 5 ' -TGTAGACTTGGGCCACCTCTTT-3 ' (Inqaba Biotec)用于评估基因组DNA (gDNA)污染。研究了9个鳄梨基因的表达。三个内源性控制基因(肌动蛋白,18岁,α-1微管蛋白)用于正常化。内源控制基因和九个鳄梨基因的引物序列和退火温度在附加文件中给出1:表S1。PerlPrimer v1.1.21 (http://perlprimer.sourceforge.net引物由Integrated DNA Technologies公司(IA, USA)合成。引物的特异性最初通过常规PCR检测,RT-qPCR中出现单一熔点曲线证实。通过生成每个引物组的标准曲线(1:5、1:10、1:20、1:50、1:100、1:500、1:500、1:500、1:500、1:100、1:100)来确定最佳稀释度。反应在96孔板中进行,RT-qPCR使用Bio-Rad CFX96™实时PCR检测系统,使用Sensimix™SYBR No-ROX (Bioline Ltd, London, UK)。每个治疗时间点分别进行3次生物试验,所有反应均重复3次。使用Bio-Rad CFX管理软件进行数据分析。数据的统计显著性是由单向方差分析,然后是学生的t-使用JMP®10.0.0版本软件进行测试(http://www.jmp.com/SAS Institute, Inc.)。在P< 0.05。数据采用GraphPad Prism®version 6.03 (www.graphpad.com).
结果与讨论
鳄梨的转录组反应
使用淹水后22和48 h的根样本进行微阵列分析,并使用RT-qPCR验证结果(附加文件)2:表S2)。研究发现,洪水对鳄梨的转录组有深远的影响,导致超过1000个转录本的诱导(Log2FC > 1, Adj;P-value < 0.05),有相似的数字被抑制(表1).将受感染的淹水处理(FI)与未受感染的淹水处理(F)进行比较,两种处理之间的基因表达没有显著变化。这表明,在对感染的反应中发生的更微妙的转录组变化可能被对洪水的反应所掩盖。在未遭受洪水侵袭的侵染植物(I)和未侵染植物(C)之间,转录本表达的差异支持了这一结论。在淹水后22 h (hpf,侵染后8天),感染株(I)和未淹水的对照株(C)之间的基因表达只有很小的差异(表2)1).诱导转录本包括同源转录本乙醇脱氢酶从链霉菌属sp。(Pa_Sin_GI32N0T02IWOXV,日志2fc = 1.23),β-1,3.-葡聚糖酶(Pa_Contig00542日志2FC = 1.95296) from葡萄,以及一个与任何已知序列没有显著同源性的contig (Pa_NA_RC_Contig07628, log . log)2fc = 2.46)。在对感染的反应中,几种与防御相关的转录本被发现在48 hpf上调(I),包括β-1,3.-葡聚糖酶,细胞色素P450(Pa_Contig07667),chitotriosidase(Pa_Contig00472),几丁质酶(Pa_Contig01014),致病源-相关的蛋白质-就像(Pa_Contig01063),GDSL酯酶/脂肪酶(Pa_Contig00520)和germin-像蛋白质(附加文件3.:表S3)。β-1,3-葡聚糖酶是已知的致病相关蛋白[31]。Pa_Contig00542,β-1,3.-葡聚糖酶可见,在22 hpf诱导,也上调(log2FC = 1.72) 48 hpf(感染后9天)。细胞色素P450已被证明在植物防御中发挥作用[32],chitoriosidase是一种几丁质酶,这些蛋白也属于致病相关蛋白[33], GDSL酯酶/脂肪酶已被描述为在植物发育、次生代谢产物合成和防御反应的调节中发挥作用[34],而发芽样蛋白质则参与植物的发育和防御[35]。
Pearson相关性分析表明,淹水植物(FI和F)与未淹水植物(C和I)之间的表达模式有很强的相似性。事实上,在22 hpf时,FI和F之间没有显著的基因表达差异。在淹水条件下,22 hpf的上调转录本与下调转录本的比值通常高于之后的时间点,这表明随着淹水的持续,更多的基因受到了抑制。在同一处理下,在不同时间点上的表达也有很强的正相关,而在淹水处理和非淹水处理之间则有负相关(表2)1).
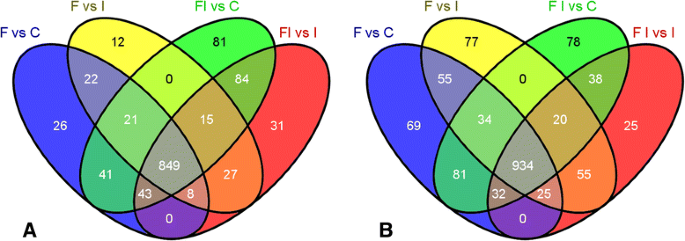
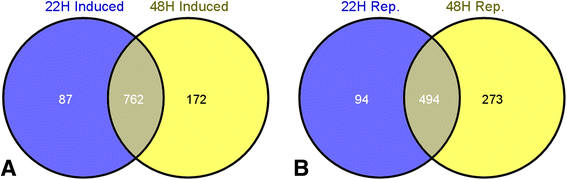
大多数在洪水诱导下的差异表达转录本(900)在感染处理和未感染处理之间共享(图2)。1).这表明无论病原体是否存在,对洪水的反应都是保守的。在被抑制的转录本中也看到了类似的趋势(附加文件4:图S1)。尽管存在一些时间点特异性基因,但许多在22 hpf时表达改变的基因在48 hpf时仍保持这种变化(图2)。2).
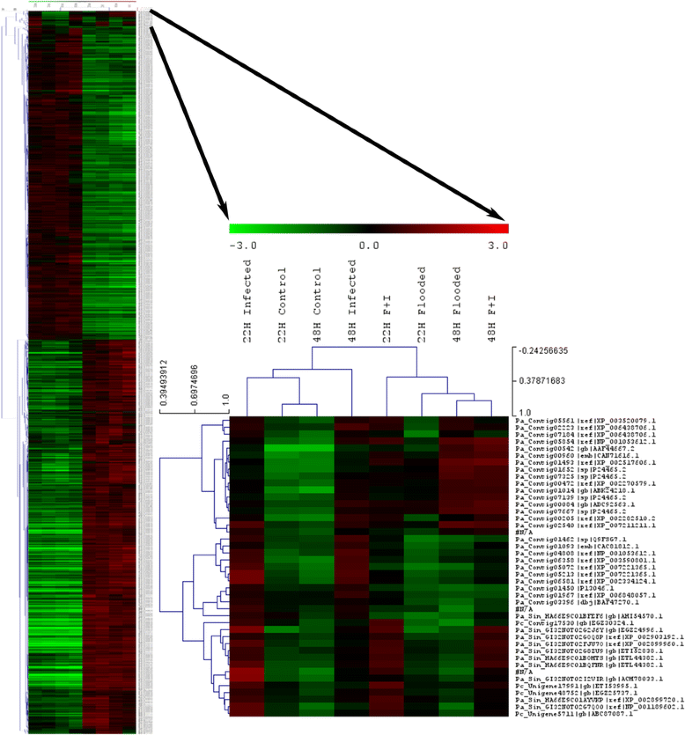
使用平均连锁的层次聚类(HCL)对所有相对于非淹水比较中显著诱导或抑制的转录本进行。3.).淹水处理之间表现出相似的表达模式,而非淹水处理之间表现出相似的表达模式,无论它们是否被感染。淹水处理和非淹水处理之间存在明显的负相关(-0.71,Pearson),表明淹水胁迫引起了转录组的巨大变化。这在图中可以清楚地看到。3.图中,非淹水处理(左侧)与淹水处理(右侧)的基因表达模式明显相反。随后将这两组按时间点进行划分,感染状态在治疗之间仅引起微妙的转录组变化。在非淹水处理中,由病原体存在引起的差异更为明显(图2)。3.).
碳代谢的影响
对显示显著(log2FC > 1或< -1,adj。P-value < 0.05)差分表达式。在淹水与非淹水的比较中,许多在22 hpf水平上调转录本的类别被过度代表,这与对缺氧的反应有关(附加文件5:图S2)。这包括辅因子结合、辅酶结合、氧化还原酶活性、氧化还原过程、糖酵解、双加氧酶活性和对缺氧的反应。在48小时的所有比较中,转移酶活性和氧化还原过程是转录物上调的最具代表性的类别6:图S3)。超过23%的序列与转移酶活性相关。其他在淹水处理中比例过高的类别通常涉及酶的功能,如“辅因子结合”或其他与能量相关的过程[36],如氧化还原酶,催化电子转移,并可能参与NAD的再生+以进一步推动糖酵解反应。双加氧酶活性和对缺氧的反应也是淹水植物的丰富种类,具有广泛的生物学作用。应激诱导的血红蛋白可能具有双加氧酶的功能,解毒缺氧时产生的一氧化氮(NO) [37]。钙离子结合在某些比较(FI vs C)中也被过度代表,钙已被认为在植物内部氧胁迫信号中具有关键作用,并已被发现是诱导乙醇脱氢酶在玉米和拟南芥[38]。
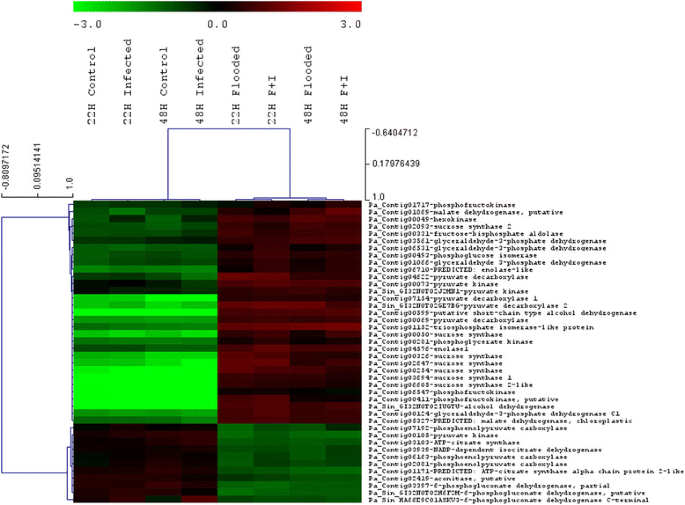
糖酵解通量增加[17],与糖酵解相关基因表达增加相结合,在低氧条件下发生,以补偿与呼吸抑制相关的ATP生成减少[12]。在牛油果中可以看到糖酵解酶的诱导反应,其中糖酵解途径中的10种酶中有9种表达增加。这些措施包括己糖激酶,phosphoglucose异构酶,phosphofructose激酶,果糖-酮糖醛缩酶,triosephosphate异构酶,甘油醛3-磷酸脱氢酶,磷酸甘油酸酯激酶,烯醇酶,丙酮酸激酶(表2).只有磷酸甘油酸酯变位酶表达量没有明显增加。糖酵解基因的诱导已经在一些物种中被发现,以应对洪水,比较两个不同的橡树品种对洪水的耐受性,发现在更耐涝的品种中糖酵解基因的诱导更强[39]。
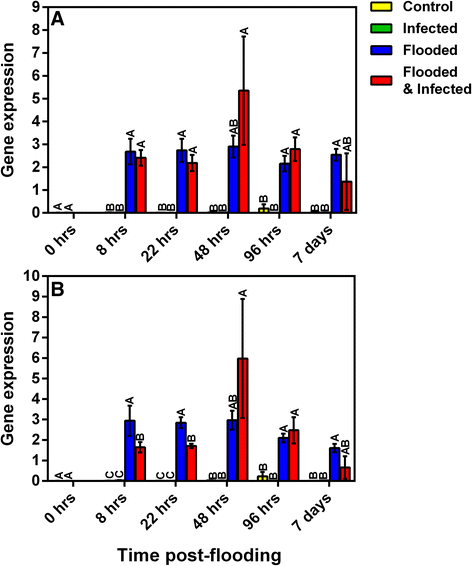
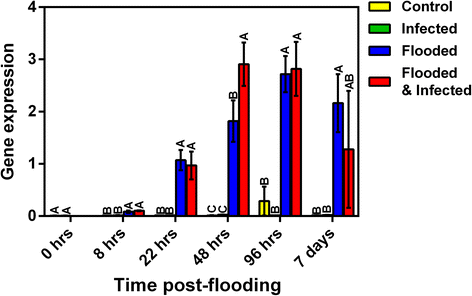
糖酵解之后是低氧条件下的厌氧发酵,所有物种都能诱导发酵,而不管它们对水浸的耐受程度如何[11]。丙酮酸经乳酸脱氢酶(LDH)发酵成乳酸,一般先经丙酮酸脱羧酶(PDC)和酒精脱氢酶(ADH)发酵成酒精[9,19]。然而,这会导致细胞质酸化并刺激ADH同时抑制LDH活性[9,19]。在我们的数据集中没有看到代表LDH的转录本的增加。LDH的诱导可能发生在缺氧的早期阶段,可能已经下降了22 hpf,类似于杨树,淹水5小时后LDH水平上升,之后下降[18]。表达增加抗利尿激素在鳄梨8 hpf(图;4)表明此时已经诱导了酒精发酵。以乙醛为中间体,通过PDC和ADH发酵丙酮酸制乙醇。河畔+通过厌氧发酵产生两个ATP分子,糖酵解反应持续进行。抗利尿激素,PDC,焦磷酸-果糖-6-磷酸盐1-磷酸转移酶是本研究中所有淹水处理中最常见的高度诱导转录本。抗利尿激素在22和48 hpf时表达增加超过40倍。的表达PDC(Contig 00088)在淹水处理中早在8 hpf时就被诱导(图。4 b).此外,未受感染的淹水植物比淹水侵染植物有明显更高的该转录本表达(图2)。4 b).在实验期间,相对于非淹水植物,淹水植物中该转录本的表达增加。类似的归纳抗利尿激素和PDC在淹水条件下的灰杨树中可见,相应酶的酶活性也有所提高[18]。此外,对淹水诱导转录本的富集分析表明,在淹水后22和48小时,与PDC相关的术语在比较中过度代表(附加文件5:图S2和附加文件6:图S3)。在牛油果中,与发酵代谢相关的基因在应对洪水时的诱导很明显,其他物种也已注意到这一点[40]。这些糖酵解酶和发酵相关酶在低氧条件下的协同表达可能表明存在一种共同的调节机制,调节这些基因的表达,如玉米中的厌氧反应元件(ARE)拟南芥[9]。
在淹水处理和非淹水处理的比较中,发现与蔗糖合酶活性相关的术语在两个时间点上都过度代表。此外,7个与蔗糖合酶相同的转录本与糖酵解酶和柠檬酸循环酶(TCA)聚在一起,所有7个转录本都被发现在淹水处理中相对于非淹水处理中被诱导(图2)。5).蔗糖的裂解产生葡萄糖和果糖,用于糖酵解,并由转化酶或蔗糖合酶催化[8]。在低氧条件下,蔗糖通过蔗糖合酶裂解被认为是有利的,因为在这个反应中消耗的ATP比由转化酶催化的反应要少[8,11,18]。RT-qPCR证实了该转录本在洪水反应中的上调(数据未显示)。蔗糖代谢的这种变化可能与维持糖酵解所需的碳水化合物需求增加有关[18]。
显示与糖酵解、TCA循环和磷酸戊糖途径(PPP)相关酶同源的转录本随后被聚类,以确定其在不同条件和时间点的表达模式。与水稻,杨树和拟南芥[11],在鳄梨中发现属于TCA和电子传递链的转录本表达减少(图。5).其中包括两份同源基因柠檬酸合成酶,一个被分配为顺乌头酸酶,一为异柠檬酸脱氢酶,三个代表丙酮酸羧化酶.只有一份笔录,被认定是推定的苹果酸脱氢酶,在淹水处理中表达增加。TCA循环和电子传递链构成了有氧呼吸的一部分,并负责产生额外的36个ATP分子[19]。从PPP中有三个转录本表现出差异表达。这三种酶都对应于PPP的氧化部分的一种酶,6-磷酸葡萄糖酸脱氢酶,并且在淹水处理中表达下降(图2)。5).
我们选择了30个最受诱导和30个最受抑制的转录本,并对其进行筛选,以确定处理之间常见的高度调控转录本(表2)3.和4).这些转录本在22或48 hpf或两个时间点都存在。在所有淹水处理中,发现有27个转录本被诱导,其中13个在两个时间点都被诱导3.).这13个转录本中有7个代表假设的、未特征的或未知的蛋白质。这些常用诱导转录本的基因本体分类显示,以转运(13.4%)、催化活性(13.4%)、结合(9%)、转运体活性(7.5%)、水解酶活性(6%)和细胞活性(6%)所占比例最大。醇脱氢酶家族蛋白(Pa_Contig00297,表3.)的平均折叠变化为41.19 (log2FC = 5.36)在22 hpf的比较中,平均折叠变化为50.18 (log2FC = 5.64)在48 hpf。不同时间点间表达差异无统计学意义。
在22 hpf的所有比较中,有9个转录本通常被诱导(表3.).其中三个代表未知或假设的蛋白质。有趣的是,这两个丙酮酸脱羧酶(Pa_Contig00088)和乙醇脱氢酶(Pa_Sin_GI32N0T02IUGTU)在此时淹水处理中强烈诱导。丙酮酸脱羧酶显示了一个平均对数2对比的FC为4.89,对应的折叠变化为29.55。在48小时,该转录本的表达仍被显著诱导(平均对数2FC = 4.83, fold-change = 28.49)。同样的,乙醇脱氢酶(Pa_Sin_GI32N0T02IUGTU)表达量平均增加29.11个fold-change (log2FC = 4.86)在22 hpf和34.51折叠变化(log2FC = 5.10)在48 hpf。丙酮酸脱羧酶和乙醇脱氢酶都参与丙酮酸酒精发酵。一个预测:焦磷酸-果糖6-磷酸盐1-磷酸转移酶亚基(Pa_Contig07556)在22 h时的所有比较中均发现3.),表达量平均增加27.19 fold-change (log .2FC = 4.76)在22 hpf和17.67折叠变化(log2FC = 4.13)在48 hpf。表达量从22 hpf显著降低至48 hpf (fold-change = -2.00, log2FC = -0.99)。该组中GO术语代表的三个主要类别是催化活性(29.4%)、结合(23.5%)和代谢(11.8%)。
在48 hpf的比较中,有5个转录本是最容易诱导的转录本,其中3个代表未知或假设的蛋白质(表2)3.).另外两份笔录对应的是假定的多药耐药蛋白(Pa_Contig06346)和a预测:甘露糖-特异性凝集素3-像蛋白质(Pa_Contig00627)。Pa_Contig06346的平均增加折叠变化为17.67 (log2FC = 4.13)。在较早的时间点,该转录本的表达也有所增加(平均折叠变化= 27.19,log2fc = 4.76)。多药耐药蛋白(MRPs)在植物中有多种作用,包括解毒、气孔调节[41,42]并且被认为在可能导致细胞损伤的活性代谢物的隔离和排除细胞质中起作用。表达增加多药耐药蛋白,2(06346)在淹水处理8小时后明显增加。6).当淹水处理与非淹水处理相比,该转录本的表达差异在22 h时变得更大,在48 h时达到峰值。在48小时时,接种的牛油果之间也有差异p、肉桂而那些没有接种的植株表达量最高。这种差异在96小时不再明显,在所有淹水处理中表达水平相似。6).表达的趋势一直维持到第7天,此时差异不再显著。笔录注释为甘露糖-特异性凝集素3-像蛋白质(Pa_Contig00627)表达量显著增加(Average fold-change = 51.85, log2在48 hpf下,淹水处理与未淹水处理相比FC = 5.66)。虽然这个转录本也显示了增加的表达(平均折叠变化= 11.91,log2FC = 3.54)在22 hpf时,表达似乎在较晚的时间点达到峰值。甘露糖特异性凝集素蛋白被认为通过识别甘露糖型聚糖参与了对外来微生物的识别[43]。
抑制能量消耗
在缺氧条件下,使用过多能量的过程,如细胞壁生物合成和木质素生产,会减少植物的生长[18]。与液泡、外质体、细胞壁和胞间连丝有关的术语都被发现在下调转录本中富集。与国防相关的转录下调也被认为是对洪水的反应(表4).国防相关的文字记录,如查耳酮合酶(Pa_Contig and Pa_Contig00619),过氧化物酶(Pa_Sin_FZ03KKT01A7ZOH),谷胱甘肽S-转移酶(Pa_Contig02129)就是其中之一。其中一些与防御相关的转录本参与了ROS的产生,以应对病原体的入侵。这包括氧化物酶[44],它们被发现在牛油果中受到洪水的反应时被高度抑制。此外,与防御相关的转录本在48小时也显示出显著的减少,与查耳酮合酶(Pa_Contig05744, Average fold-change = -13.27, log2FC = -3.70)和谷胱甘肽S-转移酶(Pa_Contig01208, Average fold-change = -11.42, log2FC = -3.51)在这个时间点被显著抑制。感应的查耳酮合酶被认为是对紫外线、细菌或真菌感染等应激条件的反应,是类黄酮生物合成途径中的关键酶[45]。的表达查耳酮合酶导致植物抗毒素的积累,并在水杨酸防御途径中发挥作用[45]。苯丙氨酸氨-裂合酶(朋友,平均折叠变化= -11.90,log2FC = -3.55在22小时和平均折叠变化= -11.88,log2FC = -3.56 (48h)是所有淹水处理中最受抑制的转录产物之一。PAL参与类黄酮、苯丙类化合物和木质素的生物合成,是苯丙类化合物途径的第一步[46]。这种酶在受到伤害、病原体、温度和其他一些外界刺激时被诱导[46]。这可能表明,通常分配给防御反应的能量被重新定向到对洪水条件下的生存更重要的其他过程中,这可能解释了对病原体,特别是与洪水条件有关的根腐烂的易感性增加。在水淹处理中被下调的其他过程代表了在这些胁迫条件下不优先考虑的过程,例如对镉(一种环境污染物)的反应,对盐的反应,激素刺激,对水剥夺的反应和对温度刺激的反应。此外,一些显示显著抑制的转录本代表未知或假设的蛋白质序列(表4).
水通道蛋白在洪水响应中的作用
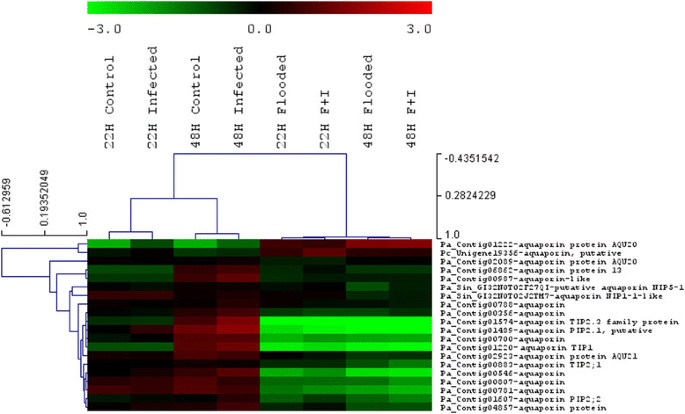
水通道蛋白(Aquaporins)是一种水通道蛋白,属于质膜固有蛋白(PIP)家族,有助于调节植物根系的导水能力拟南芥[17]。非生物胁迫可干扰水通道蛋白基因的表达[47]而洪水已导致一些树木的表达能力下降[18,39]。对下调的牛油果转录本的富集分析表明,在22 hpf和48 hpf下,大多数序列与水淹处理中的质膜(GO:0005886)相关。几种水通道蛋白家族蛋白也被认为是最受抑制的转录本(表4).水通道蛋白PIP2.1(Pa_Contig01489, average fold-change = -8.23, log2FC = -3.01在22小时和平均折叠变化= -24.36,log2在48小时时FC = -4.59)和提示蛋白质(Pa_Contig01574, average fold-change = -7.64, log2FC = -2.93)在22小时和平均折叠变化= -32.60,log2FC = -4.97(48小时)是22 hpf和48 hpf最受抑制的30个转录本之一。一个额外的水通道蛋白,一定要(Pa_Contig01220, average fold-change = -3.42, log222小时时FC = -1.77,平均折叠变化= -16.88,log2FC = -4.07(48小时)是在48小时表现出最大抑制的转录本之一。该转录本在22小时时间点也被抑制,这表明抑制发生相对较早。研究了所有20个与水通道蛋白同源的转录本的表达,大多数转录本在洪水反应中要么不表达,要么表达降低(图2)。7).只有一种牛油果水通道蛋白表达增加。以前的研究已经注意到,不同的水通道蛋白在应对特定压力时,可以在基因表达上表现出相反的趋势。本文认为水通道蛋白在水淹条件下对牛油果根系导水能力的调节中起重要作用。降低根部的导水性最终会导致鳄梨的气孔关闭,这在鳄梨中已经被发现是对洪水的反应[48]。
使用qRT-PCR进一步研究了两种水通道蛋白的表达,并评估了延长时间过程中的表达(图。8).的表达质膜内禀蛋白(Contig 00546)受到洪水的不利影响,与非洪水处理相比,这些处理的水平有所降低。在22 hpf淹水的植物中,可以看到该转录水平的降低,暴露在胁迫组合下的植物表达显著降低(图2)。8).有趣的是,与淹水处理相比,在无淹水条件下感染的植物在22 hpf时表达水平增加,在48 hpf时相对于所有处理均显著增加。淹水处理显示该水通道蛋白的表达显著降低96 hpf(图。8).这一趋势在淹水后7天仍保持不变,尽管感染植株再次表现出略高于对照植株的表达水平,显著高于淹水处理观察到的水平。与contig 00546类似,表达的减少膜通道蛋白(contig 01220)诱导22 hpf,联合治疗显著降低(图2)。8 b).水通道蛋白在48 hpf感染植株中表达量最高。在96 hpf下,非淹水处理的contig 01220转录本的表达量高于淹水处理(图2)。8 b).淹水7 d后,contig 01220在联合处理中的表达量与contig 00546相似。淹水处理的转录水平仍然很低(图2)。8).两种不同的水通道蛋白在感染反应中的表达增加是有趣的,这表明这可能作为一种一般的应激反应来改变水传导能力。
结论
这项研究是第一次大规模的基因表达分析,评估了鳄梨对洪水和洪水的反应p、肉桂.解开涉及植物对洪水反应的分子机制并生成这种反应的综合模型是具有挑战性的。然而,这将有助于阐明自然洪水易发环境中植物分布和丰度的模式,并有助于选择和开发具有更好的抗洪水能力的作物。这项研究的重点是确定洪水对鳄梨的影响,并确定这是否受到了p、肉桂.此外,鉴定与牛油果对洪水反应相关的基因对于培育出能够耐受洪水条件的砧木很重要。无论植物是否感染洪涝,洪涝都会引起鳄梨转录组的巨大变化p、肉桂与否。这可能是由于洪水引起的巨大代谢中断掩盖了对病原体更微妙的反应。然而,许多受淹植物影响的基因是与防御相关的转录本。这些转录本在淹水条件下通常被抑制,以限制O2-洪水造成的有限条件。这可能会导致被水淹或被水淹的牛油果对p、肉桂.水淹处理诱导了糖酵解酶、参与发酵的酶和蔗糖代谢相关的转录本。这说明在这些条件下,维持能量平衡对鳄梨很重要。水通道蛋白被发现在洪水的施加下被强烈下调,这可能解释了鳄梨气孔导度在洪水的响应下的降低[48]。这些减少的发生是因为水通道蛋白在根的水力传导能力中很重要,最终会影响气孔功能。在牛油果中受到洪水影响的很大一部分基因要么与已知序列没有同源性,要么代表了假设的或预测的蛋白质。这在以前的研究中已经被注意到,并且需要选择候选基因进行功能注释。将这些转录本与已知功能的转录本聚类可能有助于这些未知基因的功能表征。在拟南芥,几种突变熟知的蛋白质导致突变体显示出对淹没的耐受性显著改变,并表明这些特征不佳的蛋白质可能包含丰富的候选蛋白,可用于操纵植物对缺氧的反应[49]。我们的研究已经确定了许多功能尚未明确的基因,这些基因可能有助于牛油果对洪水的耐受性,这需要进一步的研究。值得注意的是,空间信息,例如在同一时间点诱导的基因如何相互关联,并不一定能通过微阵列分析来解决,需要进一步的研究来阐明这一点。
缩写
- 抗利尿激素:
-
乙醇脱氢酶
- 是:
-
厌氧反应元件
- B2G:
-
Blast2GO软件
- C:
-
控制植物
- dca:
-
桌面cDNA注释系统
- F:
-
工厂被淹
- 舰队指挥官:
-
褶皱变化
- 罗斯福:
-
错误发现率
- FI:
-
遭受洪水和感染双重作用的植物
- 加:
-
GenePix数组列表
- gDNA:
-
基因组DNA
- 盐酸:
-
分层聚类
- 高通滤波器:
-
时间成为了
- 我:
-
受感染的植物
- LDH:
-
乳酸脱氢酶
- LIMMA:
-
微阵列数据的线性模型
- 兆电子伏:
-
多重实验查看器
- 可机读护照:
-
多药耐药蛋白
- PDC:
-
丙酮酸脱羧酶
- 皮普:
-
质膜内禀蛋白
- 购买力平价:
-
磷酸戊糖途径
- PRR:
-
疫霉根腐病
- ROS:
-
活性氧
- 信噪比:
-
信噪比
- 柠檬酸:
-
柠檬酸循环
参考文献
- 1.
科兹洛夫TT。木本植物对淹水和盐度的响应。树木生理学专著,1997;1(1):490。
- 2.
杨晓明,王志强,王志强,等。水稻作物对水淹的响应。园艺,1992;13:257-313。
- 3.
多明戈R, Pérez-Pastor A, Ruiz-Sánchez MC.嫁接在不同砧木上的杏树对洪涝胁迫的生理响应。植物营养学报,2002;26(4):344 - 344。
- 4.
家长C, Capelli N, Berger A, Crèvecoeur M, Dat JF。植物对土壤内涝的响应综述。植物胁迫。2008;2(1):20-7。
- 5.
杨晓明,李志强,李志强,等。工程植物抗非生物胁迫的研究进展。生物技术。2005;16(2):123-32。
- 6.
耐淹性:植物在不同环境下的性状组合。植物学报。2009;36(8):665-81。
- 7.
植物对缺氧的反应——生存是一种平衡行为吗?植物科学进展,2004;9(9):449-56。
- 8.
李志强,李志强,李志强,等。水淹胁迫对植物遗传多样性的影响。植物学报。2008;59:313-39。
- 9.
缺氧和根代谢:缺氧和缺氧下的损伤和驯化。植物学报。1997;48(1):223-50。
- 10.
李志强,李志强,李志强,等。水浸对水稻耐水植物C代谢的影响(Quercus栎树)和不宽容(Fagus sylvatica)树种。树物理学报,2012;32(2):135-45。tps009。
- 11.
王丽娟,王丽娟,王丽娟,王丽娟。植物对缺氧的转录和代谢反应的比较分析。生态学报。2011;29(2):379 - 379。
- 12.
李志强,李志强,李志强,等。树木对涝渍胁迫的分子和生理响应。植物细胞环境学报。2014;37(10):2245-59。
- 13.
Gérard B, Alaoui-Sossé B, Badot P-M。淹水对两种橡树生长初期淀粉分配的影响。树木。2009;23(2):373 - 80。
- 14.
黑水湿地植物水分关系和叶片气体交换对洪水的响应。植物生态学报。2015;26(6):342 - 342。
- 15.
张伟,张文生。低氧效应2浓度和叠氮化物对小麦根系皮层细胞导水性和渗透容量的影响。植物学报。1991;18(6):603-13。
- 16.
莫雷尔C,布尔西克Y, Luu D-T, Santoni V, Shahzad Z, Verdoucq L.植物水通道蛋白。中国生物医学工程学报,2015;29(4):344 - 344。
- 17.
Tournaire-Roux C, Sutka M, Javot H, Gout E, Gerbeau P, Luu DT, Bligny R, Maurel C.胞质pH通过水通道蛋白门通调节缺氧胁迫下根系水分运输。大自然。2003;425(6956):393 - 7。
- 18.
Kreuzwieser J, Hauberg J, Howell KA, Carroll A, Rennenberg H, Millar AH, Whelan J.灰色杨树叶片和根系在低氧胁迫下的差异响应。植物科学进展。2009;29(1):466 - 466。
- 19.
土壤缺氧对牛油果的影响(Persea美国机)树。智利:Seminario International: Manejo del Riego和Suelo en el culo del Palto La Cruz;2006.
- 20.
谢伟强,李志强,李志强。亚热带和热带果树对钙质土壤洪水的响应。HortScience。41 2006;(3): 549 - 55。
- 21.
洪涝和疫霉根腐病对牛油果光合特性的影响。在:佛罗里达州园艺学会会议;1987.290 - 94页。
- 22.
洪涝和疫霉根腐病对牛油果净气体交换和生长的影响。植物病理学。1989;79(2):204 - 8。
- 23.
吴志刚,叶连泽。柑橘树对土壤水淹的光合响应。植物科学。1991;81(1):7-14。
- 24.
彭勇,董勇,涂斌,周忠,郑波,罗林,石春,杜凯。互接研究表明,根系在杨树抗洪性中起着重要作用。中国植物学报。2013;26(8):489 - 497。
- 25.
Hoagland DR, Arnon DI。无土壤种植植物的水栽培方法。伯克利:环形加州农业实验站;1950: 347(第二次编辑)。
- 26.
李国强,李国强,李国强,李国强。新创根转录组的测序、组装和分析Persea美国(米尔)回应疫霉、肉桂和洪水。公共科学图书馆,2014;9(2):e86399。
- 27.
孔鹏,洪昌,理查森。快速检测疫霉、肉桂用LPV假定存储蛋白基因的引物进行PCR检测。植物病理学杂志,2003;52:681-93。
- 28.
里奇ME,西尔弗J,奥什拉克A,霍姆斯M,迪亚加马D,霍洛韦A,史密斯GK。双色微阵列背景校正方法之比较。生物信息学。2007;23(20):2700 - 7。
- 29.
郭艳,李志强,李志强,李志强。cDNA序列注释的一种应用程序。生物信息学,2009,25(9):1195 - 6。
- 30.
Saeed A, Sharov V, White J, Li J, Liang W, Bhagabati N, brasted J, Klapa M, Currier T, Thiagarajan M. TM4:一个免费的、开源的微阵列数据管理和分析系统。生物学技术。2003;34(2):374。
- 31.
Neale AD, Wahleithner JA, Lund M, Bonnett HT, Kelly A, Meeks-Wagner DR, Peacock WJ, Dennis ES。几丁质酶、β - 1,3 -葡聚糖酶、渗透素和延伸素在烟草外植体中表达。《植物科学》1990;2(7):673-84。
- 32.
刘志刚,李志刚,李志刚,李志刚。顺式茉莉素诱导的细胞色素P450 CYP81D11在植物防御中的作用。植物信号行为研究。2011;6(4):563 - 563。
- 33.
植物几丁质酶:遗传多样性和生理作用。植物学报,2012;31(1):57-73。
- 34.
谢皮什科,赖昌平,黄立明,刘建辉,邵建峰。水稻(Oryza sativa L. japonica)基因组中GDSL酯酶/脂肪酶基因家族的多功能性和多样性:生物信息学分析的新见解BMC Genomics. 2012;13(1):309。
- 35.
王涛,陈霞,朱峰,李浩,李玲,杨强,迟霞,余松,梁霞。花生发芽样蛋白和AhGLPs在植物发育和防御中的作用。公共科学图书馆,2013;8(4):e61722。
- 36.
李文杰,李文杰。能量平衡在提高光合生产力中的重要性。中国生物医学工程学报,2011;29(1):344 - 344。
- 37.
杜达斯C,竞争对手J, Hill RD.植物血红蛋白,一氧化氮和低氧胁迫。中华科学技术学报。2003;91(2):173-8。
- 38.
Dat JF, Capelli N, Folzer H, Bourgeade P, Badot P- m。植物洪水期间的传感和信号。植物化学学报。2004;42(4):273-82。
- 39.
Le Provost G, Sulmon C, Frigerio JM, Bodénès C, Kremer A, Plomion C.涝渍反应基因在两种同向橡树种间分化中的作用。树物理学报,2012;32(2):119-34。
- 40.
李志强,李志强,李志强,李志强。利用微阵列技术研究生物反应器厌氧反应拟南芥.学报学报。2005;96(4):661-8。
- 41.
杨晓明,李志强,李志强,等。一种多药耐药相关蛋白在花青素转运中的应用玉米.植物细胞学报。2004;16(7):1812-26。
- 42.
Klein M, Perfus‐Barbeoch L, Frelet A, Gaedeke N, Reinhardt D, Mueller‐Roeber B, Martinoia E, Forestier C.植物多药耐药ABC转运蛋白AtMRP5参与保护细胞激素信号和水分利用。植物学报,2003;33(1):119-29。
- 43.
Peumans WJ, Van Damme EJ。凝集素在植物防御中的作用。组织化学杂志,1995;27(4):253-71。
- 44.
奥布莱恩JA,道迪A,巴特VS博尔威尔GP。活性氧及其在植物防御和细胞壁代谢中的作用。足底。2012;236(3):765 - 79。
- 45.
Dao T, Linthorst H, Verpoorte R.查尔酮合成酶及其在植物抗性中的作用。植物化学学报,2011;10(3):397-412。
- 46.
Giberti S, Bertea CM, Narayana R, Maffei ME, Forlani G.两种苯丙氨酸解氨酶异构体参与了水稻对真菌病原体的诱导反应Magnaporthe oryzae.植物营养学报,2012;29(3):344 - 344。
- 47.
Boursiac Y, Boudet J, Postaire O, Luu DT, Tournaire‐Roux C, Maurel C.刺激诱导的根系水运输下调涉及活性氧激活的细胞信号转导和质膜内征蛋白内化。植物学报,2008;26(2):344 - 344。
- 48.
瑞克斯汀,泰勒,范登伯格,洪泛,Phytophthora、肉桂:不同抗疫霉根腐病抗性的美洲Persea americana (Mill.)非嫁接砧木对光合作用和叶绿素荧光的影响。中国植物学报,2014;
- 49.
李,李。防水作物:有效的洪水生存策略。植物科学进展。2012;
确认
作者要感谢南非国家研究基金会的Hans Merensky基金会和THRIP计划(TP14080787841)的资助。BR由Claude Leon基金会提供的博士后奖学金支持。树木由威斯特法利技术服务公司提供。还要感谢非洲基因技术中心(ACGT)微阵列设施提供的技术援助。
资金
作者要感谢南非国家研究基金会的Hans Merensky基金会和THRIP计划(TP14080787841)的资助。BR由Claude Leon基金会提供的博士后奖学金支持。
数据和材料的可用性
本研究的数据可从NCBI的基因表达Omnibus通过GEO系列登录号GSE81297 (http://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE81297)根据MIAME指南。补充材料可在数据表1中找到。
作者的贡献
BR参与了研究和实验设计,进行了实验工作,进行了数据分析,并起草了手稿。NO为微阵列实验提供技术支持,进行数据分析,并对稿件有贡献。NVDB为研究设计、实验设计、资助和文稿起草做出了贡献。所有作者都对最终稿做出了贡献并通过了。
相互竞争的利益
作者声明,本文的发表不存在任何利益竞争。
发表同意书
不适用。
伦理批准并同意参与
不适用。
作者信息
从属关系
相应的作者
附加文件
附加文件1:表S1。
引物用于微阵列数据的RT-qPCR验证。分配给每个转录本的假定身份列在“基因”列中。(docx22 kb)
附加文件2:表S2。
微阵列数据的RT-qPCR验证。选择用于微阵列验证的代表性阵列。选择了五个转录本以确保微阵列数据与其他表达分析方法具有可比性。值表示基因表达的折叠变化。(docx21 kb)
附加文件3:表S3。
与对照处理(C)相比,在淹水后48 h(感染后8天),感染处理(I)中发现牛油果转录物上调。(docx22 kb)
附加文件4:图S1。
在淹水后22小时(A)和淹水后48小时(B),比较淹水处理与未淹水处理中被抑制的鳄梨转录本。首先对阵列上存在多个探针的转录本的值进行平均,然后对阈值进行分析以确定差异表达。(TIF 3090kb)
附加文件5:图S2。
对22HF和22HI中上调序列进行富集分析后go项的差异分布。与由阵列上所有序列组成的参考集相比,与GO项相关的序列的百分比在22HF和22HI的比较中显示过度表示(FDR < 0.05)。只有转录本显示显著差异表达(log2FC > 1, adj。P-value < 0.05)均纳入分析。(PNG 96kb)
附加文件6:图S3。
48HFI与48HC比较中上调序列富集分析后go项的差异分布。在48HFI vs. 48HC的比较中,与GO项相关的序列的百分比与由阵列上所有序列组成的参考集相比显示过度代表性(FDR < 0.05)。只有转录本显示显著差异表达(log2FC > 1, adj。P-value < 0.05)均纳入分析。(PNG 110kb)
权利和权限
开放获取本文根据创作共用属性4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),允许在任何媒介上不受限制地使用、分发和复制,前提是您对原作者和来源给予适当的赞扬,提供到创作共用许可证的链接,并注明是否进行了更改。创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)除另有说明外,适用于本条所提供的资料。
关于本文
引用本文
Reeksting, b.j., Olivier, N.A. & van den Berg, N.耐疫霉根腐病牛油果的转录组反应(Persea美国)根茎到洪水和疫霉、肉桂.BMC植物生物学16日,205(2016)。https://doi.org/10.1186/s12870-016-0893-2
收到了:
接受:
发表:
关键字
- 鳄梨
- 微阵列
- 缺氧
- 水通道蛋白
- 糖酵解