抽象的
背景
农药导致植物氧化应激及其残留物在植物零件中持续存在,这是环境和人类健康的主要关注点。已知芸苔类固醇(BRS)保护植物免受非生物胁迫条件,包括农药毒性。本研究证明了种子浸泡与24倍氧化物(EBR)对10天老年人的生理反应的影响Brassica Juncea.在吡虫啉(IMI)毒性下种植的幼苗。
结果
在从EBR处理的种子中提出的幼苗并在IMI毒性下生长,过氧化氢的含量(H.2O2)和超氧化物阴离子(o.2-)降低,超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽还原酶(GR)、谷胱甘肽- s -转移酶(GST)、愈创木酚过氧化物酶(POD)活性增强,谷胱甘肽(GSH)含量增加。与对照相比Sod, cat, gr, pod, nadh(NADH-泛烯酮氧化还原酶),cxe.(羧酸酯酶), GSH-S(谷胱甘肽合酶), GSH-T(谷胱甘肽Transporter-1),p450.(细胞色素P450单加氧酶)GST1-3,5-6在从EBR处理的种子中提出的幼苗中得到增强,并在IMI补充的基质中生长。但是,表达了投呼吸爆发氧化酶,负责H2O2经EBR处理的种子和IMI毒性下生长的幼苗产量下降。此外,EBR种子处理降低了IMI残留38%以上B. Juncea.幼苗。
结论
本研究表明,EBR种子浸泡可通过调节基因表达有效降低氧化应激和IMI残基B. Juncea.根据IMI压力。总之,外源EBR应用可以保护植物免受农药植物毒性的影响。
背景
植物易受各种害虫如白蚁,土壤虫,蚜虫和叶料斗的攻击。农药广泛用于控制这些害虫,但这些农药由于其挥发性而在喷射时导致空中污染[1].吡虫啉(IMI)是一种新烟碱类杀虫剂,通过土壤/种子处理系统作用,保护植物免受土壤和空中害虫的侵害,而不会造成任何空中农药污染[2].农药的应用通过产生反应性氧物种使植物氧化应激[3.,4].农药在农药残留的形式植物的部分持续存在[4,5对人类和包括蜜蜂在内的传粉者造成重大威胁[6].由于农药残留的持久性,也通过食物链进入生态系统,对生态系统和环境造成严重威胁[1].植物能够通过三相酶介导的降解过程将农药降解成可溶性和较小的毒性代谢物[7,8].第一阶段涉及细胞色素P450单加氧酶(P450)、过氧化物酶和羧酸酯酶等酶,这些酶参与了农药的激活。在2n相,谷胱甘肽- s -转移酶(GST)和udp -糖基转移酶帮助激活的农药与谷胱甘肽(GSH)和葡萄糖结合,从而形成毒性较小和更可溶性的代谢物。这些代谢物最终储存在液泡或质外体中rd.农药解毒阶段。油菜素内酯(Brassinosteroids, BRs)是一类植物激素,众所周知,它可以保护植物免受包括农药引起的非生物胁迫[9- - - - - -12.].BRS还降低了农药引起的植物中的氧化应激,伴随着增强的抗氧化酶活性[3.]及减少植物内残余除害剂[5,6].据报道,BRS的外源应用增强了编码P450,GST,超氧化物歧化酶(SOD),抗坏血酸过氧化物酶(APOX),过脱落酶(猫),谷胱甘肽还原酶(GR)和GSH合酶的表达,导致农药排毒[3.,5].农药应用通过产生活性氧(ROS)导致植物氧化应激,并持续以农药残留的形式存在。抗氧化和农药排毒酶有助于清除ROS和减少农药残留物。请记住,BRS在促进农药毒性下促进植物的抗氧化防御系统方面的作用,本作出现了本作的24倍氧化物(EBR) - 调节农药解毒机制Brassica Juncea.幼苗。在早期的研究中,研究人员主要通过叶面模式应用BRS,但本研究进行了在10天氧化应激和IMI残留物中获得种子浸泡的效果。B. Juncea.在IMI毒性下生长的幼苗。
方法
植物萌发
的种子B. Juncea.L.品种RLC-1浸泡在0或100 nm ebr l中−1IMI浓度(0、150、200和250 mg IMI L−1将IMI溶于蒸馏水中制备。将3ml IMI溶液倒入每个衬有Whatman#1滤纸的Petri-plate中。浸透了ebr的种子B. Juncea.在含有IMI溶液中的培养皿中发芽并保持在种子萌发剂(25±0.5℃,16小时光周期和175μmolM中−2年代−1光强度)。在播种10天后收获幼苗,分析ROS和GSH的含量,抗氧化酶的活性,基因和IMI残基的表达。所有实验均以三份酶进行。每次复制由一个培养板组成,并从中选择10个幼苗。
活性氧的估计
超氧化物阴离子(o.2-)
超氧阴离子含量根据Wu等估算[13.].将一个G植物组织在含有1%的聚乙烯吡咯烷酮的6ml磷酸盐缓冲液(65mm,pH = 7.8)中均化。将匀浆在4℃下以5000×g离心15分钟。加入0.5ml上清液,加入0.5ml磷酸盐缓冲液(65mm,pH = 7.8)和0.1ml盐酸羟胺(10mM)。将混合物在25℃下孵育30分钟。孵育后,向混合物中加入1ml 3-氨基苯磺酸(58mm)和1ml 1-萘氨基(7mm),然后在25℃下孵育20分钟。在530nm下测量吸光度。为了计算超氧化物含量,使用亚硝酸钠的标准曲线,表示含量为μmolg−1弗兰克-威廉姆斯的幼苗。
过氧化氢(h2O2)
H2O2使用Patterson等人提供的方法评估。[14.].将植物组织(0.5g)粉碎在1ml丙酮中,然后在4℃下以5000×g离心15分钟。向上清液中,加入20μL浓浓HCl中的20%氯化钛。然后加入200μl氨溶液(17μm),然后用丙酮重复洗涤沉淀物。将洗涤的沉淀物溶解在1.5ml H中2所以4(2 n)。吸光度在410nm读取。从H的标准曲线计算过氧化氢的含量2O2表示为μmol g−1弗兰克-威廉姆斯的幼苗。
估计抗氧化酶和谷胱甘肽含量
超氧化物歧化酶(SOD)
根据Kono估计SOD活动[15.]微小修改。将一个G植物组织在3ml碳酸钠缓冲液中均化,然后在4℃下以12,000×g离心20分钟。上清液用作进一步分析的样品。反应混合物由1630μl碳酸钠缓冲液(pH = 10.2),500μl硝基噻唑(24μm),100μl的EDTA(0.1mm),100μl羟胺盐酸盐(1mm),100μlTriton-X-100(0.03%)和70μl样品。在560nm下测量吸光度。
过氧化氢酶(CAT)
根据Aebi估计猫活动[16.略作修改。取3 mL pH 7.0的100 mM磷酸钾缓冲液(PPB)均质1 g新鲜幼苗。匀浆4℃,2000 × g离心20 min,取上清液测定CAT活性。在比色管中,反应混合物由1500 μL PPB (pH = 7.0, 50 mM)、930 μL双氧水(15 mM)和70 μL样品组成。在240 nm处测定吸光度。
愈创木酚过氧化物酶(POD)
POD活性测定采用Putter [17.].1 g幼苗在3 mL PPB (100 mM, pH = 7.0)缓冲液中均质,4℃12,000 × g离心20分钟。上清作为进一步分析的样本。制备70 μL样品、2350 μL PPB (50 mM, pH 7.0)、50 μL愈创木酚溶液(20 mM)和30 μL H2O2 (12 mM)的反应混合物,在436 nm处记录吸光度。
谷胱甘肽还原酶(GR)
GR活性根据Carlberg和Manisorvik确定[18.].1 g新鲜幼苗在3 mL PPB (100 mM, pH = 7.0)缓冲液中均质,4℃12,000 × g离心20分钟。上清作为植物样品测定GR活性。反应混合物中PPB (50 mM, pH 7.0) 1530 μL, EDTA (3.0 mM)、NADPH (0.1 mM)各300 μL,氧化谷胱甘肽(1.0 M)和样品70 μL。在340 nm处记录吸光度。
Glutathione-S-transferase(销售税)
基于Habig和Jacoby量化谷胱甘肽-S-转移酶活性[19.].1 g新鲜幼苗用3 mL PPB (100 mM, pH = 7.5)缓冲液均质,12,000 × g 4℃离心20分钟。上清液作为反应混合物中的样品。反应混合物中样品70 μL, PPB (50 mM, pH 7.5) 1930 μL,还原性谷胱甘肽(10 mM)和1-氯-2,4-二硝基苯(10 mM)各250 μL。在340 nm处测定吸光度。
谷胱甘肽(GSH)
根据Sedlak和Lindsay给出的方案测定谷胱甘肽含量[20.].新鲜植物组织(1 g)在3 mL含有1 mM EDTA的Tris缓冲液(50 mM, pH 10.0)中均质。将匀浆12000 × g离心15 min,取植物提取物上清液测定谷胱甘肽含量。植物提取物的100μL, 1毫升的三羟甲基氨基甲烷缓冲液,50μL Ellman试剂和4毫升无水甲醇添加,并保持在室温下15分钟,然后进行离心3000 g×15分钟。上层清液的吸光度测定指出在412海里。
基因表达分析
根据制造商的指示(Invitrogen),使用Trizol方法从整个幼苗中提取总RNA。总RNA用于用RNA与CDNA试剂盒(Invitrogen)的逆转录转录,含有MULV,作为逆转录酶,DNTP的混合物,随机八氧化物和寡核苷酸(DT)16..Gene-specific引物(表1)根据来自Genbank和Embl数据库的mRNA序列设计的,以及施由于其植物植物营养阶段的高表达稳定性,基因被用作内部控制。使用Stepone TM实时检测系统(Applied Biosystems)和定量实时PCR(QRT-PCR)和权力SYBR®Green PCR Master Mix(三个生物和技术重复)。在每个PCR循环结束时,使用随PCR系统提供的软件生成熔化曲线,验证单个产物被扩增。mRNA定量采用Livak和Schmittgen方法[21].通过减去内部控制的阈值(CT)来获得ΔCt值(施)从兴趣基因的基因。ΔΔCt值由ΔCt值减去未处理对照样品的Ct值得到。表达水平相对于未经处理的样品的fold-changes表示为2——ΔΔCt.
IMI残留分析
AOAC,官方方法2007.01 [22洗涤幼苗提取物用于IMI残留分析。将一个g幼苗在乙腈中粉碎1ml 1%乙酸,200毫克无水MgSO4加入50mg乙酸钠。将混合物摇动2分钟,然后以1500×g离心5分钟。取出0.5ml上层,并进行75毫克无水MgSO4还加入了25mg初级仲胺(PSA)吸附剂。再次离心混合物,然后用0.22μ过滤器过滤上层并在4℃下储存直至分析。
gc - ms分析
GC-MS(QP2010 Plus,Shimadzu,Kyoto,日本)用于分析IMI残留物的幼苗提取物。用作载气作为载气,将初始烘箱柱温度设定在50℃,然后在25℃min时将其增加至125℃−1并在10°C min时提高到300°C−1(保持15分钟)。进样温度设置为250℃,进样方式为分流进样,柱流速为1.70 mL min−1,分析柱为DB-5 ms。离子源温度为200℃,界面温度为280℃。进样量为8 μL。
统计分析
使用自编码软件(MS-Excel 2010)和人工神经网络(ANN)使用统计数据,使用双向ANOVA,Tukey的HSD和多元线性回归分析(MLR)分析结果。在ANN模型中,氧化应激标记物和GSH的含量,抗氧化酶的活性,基因的相对表达和IMI残基(靶标)以使用3神经元,1个隐藏层的施用IMI和EBR(输入)的浓度来回归浓度,塔尼功能从输入到神经元,又从神经元到输出。
结果
EBR对ROS的影响
观察到吡虫啉(IMI)应用增加氧化应激B. Juncea.通过增强H的内容来幼苗2O2和o..2-.100 nM EBR浸种可降低IMI添加Petri-plates培养的幼苗中活性氧(ROS)的含量(见表2)2).采用双向方差分析和Tukey’s HSD对数据进行统计分析,结果表明,黄芪幼苗活性氧含量存在显著差异B. Juncea.植物。多元线性回归(MLR)分析显示,用于种子浸泡的EBR浓度与H的含量之间的部分回归2O2和o..2-生成的消退消退,而IMI对这些RO的产生积极回归。这表明EBR在减少ROS生成时的作用(表2).
EBR对谷胱甘肽含量及抗氧化酶活性的影响
GSH的含量以及SOD,猫,豆荚,GR和GST等抗氧化酶的活性在从EBR处理的种子饲养的幼苗中提高,并在补充有IMI溶液的培养皿中生长(表2).使用双向ANOVA和Tukey的HSD在分析数据后,观察到SOD,CAT,POD,GR和GST活动和GSH内容的显着差异。MLR分析和阳性βEBR.回归系数还显示EBR应用增加了抗氧化酶的GSH含量和活性(表2).
EBR对基因表达的影响
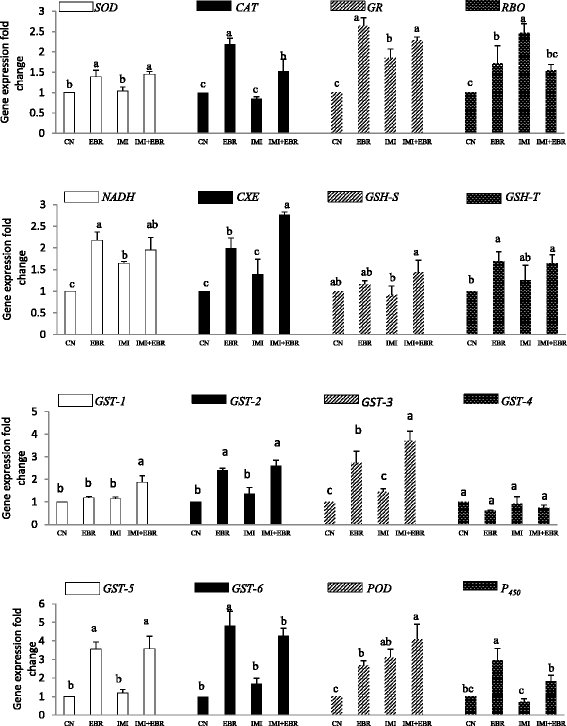
我们观察到种子浸种显著地调节了该基因的表达B. Juncea.在IMI毒性下种植的幼苗(图。1).折叠变化的表达投与未处理和IMI处理相比,ebr处理和IMI处理降低了37.65%。类似比较B. Juncea.树苗,增加了表达草皮(39.42%),猫(78.82%),GR.(23.24%),荚(31.51%),GST1(64.04%),GST2(90.51%),GST3(157.64%),GST5(203.39%),GST6(154.76%),GSH-S(56.52%),GSH-T(32.0%),CXE(99.28%),NADH.(18.18%)和P450.注意(152.78%)注意到(图。1).我们观察到在农药解毒酶的编码基因表达有显著差异B. Juncea.使用双向ANOVA和TUKEY的HSD分析数据后幼苗。正βEBR.从MLR分析中获得的值显示EBR种子浸泡上调所有基因的表达(种群杀虫排毒酶中涉及的编码酶),除外GST-4(桌子3.).
浸种对水稻IMI胁迫改良相关基因相对表达的影响Brassica Juncea.幼苗。数据显示为平均值±标准差(3次生物重复),相同字母的条形表示在p < 0.05 (comparison among treatments of same gene). HSD values for each gene have been mentioned in Table3..(EBR浓度= 100nm和IMI浓度= 200 mg IMI L.−1)
EBR对IMI残留的影响
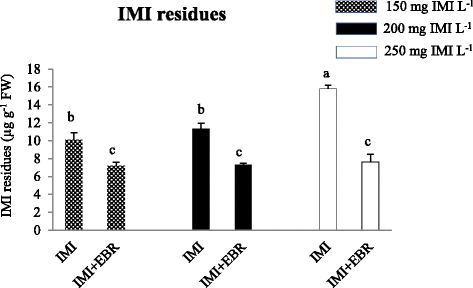
IMI残留量在EBR种子浸渍中提出的幼苗中减少了38%,并在IMI处理的培养皿中发芽(图。2).使用双向方差分析和Tukey的HSD数据分析显示,在IMI残基中存在显著差异B. Juncea.从未处理的种子和EBR处理的种子中提出的幼苗并在IMI毒性下生长。负βEBR.IMI残留物的回归系数也揭示了用EBR浸泡的种子浸泡导致IMI残基(表4).
我们使用ANN的数据分析还表明,实验(目标)和模拟(输出)数据具有高度相关性,这表明ANN模拟在当前实验中进行的生理学研究,其具有非常高的意义(表5).
讨论
在本调查中,ROS的内容包括和o.2-和H.2O2随着IMI的应用而增加。经EBR种子处理后,这些活性氧含量显著降低。产生这些ROS的原因之一可能是由于抗氧化防御系统被破坏而引起的非生物应激条件下的氧化爆发[23].它也被证明了rboh1.(呼吸爆发氧化酶同源物1)负责生产H.2O2在农药压力下的植物中[4].此外,在目前的研究中,我们还观察到表达了投基因(呼吸爆发氧化酶,一种负责H的基因2O2)上调B. Juncea.在IMI毒性下种植的植物。已经观察到o2.-结果表明,施用EBR后,籽粒中O的含量降低,这可能与O的转化有关2.-到H2O2通过超氧化物歧化酶(SOD)的活性和基因表达(SOD)在目前的实验中,在EBR的种子处理后也观察到较高。另外,h的内容2O2还注意到EBR的种子申请下降,并且背后的可能原因可能是H的转换2O2通过抗氧化酶过氧化酶(猫)水和分子氧。在目前的研究中,猫酶的活性和表达的猫在从EBR-浸泡的种子饲养的幼苗中也增加了基因,并在含有IMI的培养皿中生长。而且,表达了投亦已观察到随着EBR申请减少,表明H H的显着减少的另一个原因2O2.Hayat等人进行的研究[24]和Fariduddin等人。[25还表明,BRS在环境压力条件下在植物中的清除中发挥着重要作用。
由于农药毒性引起的氧化应激,抗氧化防御系统被激活,从而有效地清除ROS,最终降低氧化应激[3.].本研究发现,除IMI浓度较高外,外源IMI处理和EBR种子处理均显著增加了GSH含量和SOD、CAT、POD、GR和GST等酶抗氧化剂的活性。SOD和CAT参与将有害的超氧阴离子转化为无毒的水和分子氧。此外,也有报道称,另一个途径,抗坏血酸-谷胱甘肽循环,参与H2O2[26].谷胱甘肽参与H的还原2O2通过抗坏血酸-谷胱甘肽循环进入水中,这也是由GR酶催化的[27].在抗坏血酸-谷胱甘肽循环中,GR还通过维持还原型谷胱甘肽和氧化谷胱甘肽的比例,在降低氧化应激中发挥重要作用。在目前的研究中,GR的比活性也随着IMI的应用而增加,这表明GR积极参与了IMI毒性产生的ROS的解毒。GR活性也有类似的增加豇豆属辐射动物植物在喉毒性下种植[28].本研究中应用EBR种子进一步提高了IMI毒性下各抗氧化酶的活性。这些抗氧化酶活性的变化可能是由于EBR调节蛋白质合成或改变酶动力学[29,30.].此外,在目前的研究中,我们注意到草皮,猫,GR.,荚和GST1-3,5-6在ebr处理的种子和IMI毒性下生长的幼苗中也上调。这说明抗氧化酶基因的表达增加可能是抗氧化酶活性增强的原因之一B. Juncea.由ebr处理的种子在IMI胁迫下生长的植物。
在目前的研究中,观察到IMI残基降低从EBR处理的种子饲养的幼苗,并在IMI毒性下生长。如引言部分所述,三个相序酶介导的排毒系统负责植物中的农药降解[7,8].在目前的研究中,观察到涉及三个相平的农药解毒系统的POD和GST酶的活动,以随着IMI应用以及EBR种子处理增加。另外,相1酶的基因表达即P450、POD、CXE和第二阶段酶GST.随着GSH-S和GSH-T在IMI毒性作用下,随着EBR的施用也会增加。氧化还原酶有助于农药解毒[4]和基因表达NADH.在IMI毒性下EBR种子应用后也被注意到。由于EBR籽浸泡调节基因的表达(参与农药排毒系统的编码酶),因此这可能是减少IMI残基的可能性B. Juncea.从EBR处理的种子中提出的幼苗,并在IMI毒性下生长。
结论
目前的研究表明,随着EBR的种子浸泡增强了IMI解毒,并降低了氧化应激B. Juncea.通过上调幼苗SOD,猫,GR,POD,NADH,CXE,GSH-S,GSH-T,P450和GST1-3,5-6参与酶机农药排毒的基因伴随着下调投基因。与基于FRS的叶面应用的早期研究相比,目前研究的重要点是通过种子处理的单一应用可以通过调制基因表达有效地激活植物防御系统免受农药应激的影响。
缩写
- 方差分析:
-
方差分析
- AOAC:
-
官方分析化学家协会
- 互补脱氧核糖核酸:
-
互补脱氧核糖核酸
- EBR:
-
24-epibrassionolide
- EMBL的:
-
欧洲分子生物学实验室
- FW:
-
鲜重
- HSD:
-
诚实差异
- 高:
-
多元线性回归
- PCR:
-
聚合酶链反应
- PSA:
-
主要二级胺
- RNA:
-
核糖核酸
参考文献
- 1。
Rajendran S.在印度农业中使用的农药环境和健康方面。在:Martin J,Bunch V,Suresh M,Kumaran TV,编辑.第三届环境与健康会议的诉讼程序。约克大学马德拉斯大学地理学系,大学环境研究院;2003.353-373。
- 2.
王志强,王志强,王志强,等。玉米作物对吡虫啉吸收的定量分析。中国农业科学。2005;53:5336-41。
- 3.
外源施用28-同油菜素内酯可调节盐和农药对优质水稻basmati1号的胁迫响应。植物生长规律。2015;34:509-18。
- 4.
周y,xia x,yu g,wang j,wu j等。芸苔类固醇在作物植物中的农药代谢调节中起着关键作用。SCI REP。2015; 5:9018。DOI:10.1038 / srep09018.
- 5.
夏Xj,张y,吴jx,王杰,周耶等。芸苔类固醇促进黄瓜杀虫剂的代谢。JAgric Food Chem。2009; 57:8406-13。
- 6.
Cresswell我。一项新烟碱类杀虫剂(吡虫啉)对蜜蜂影响试验的荟萃分析。Ecotoxicol。2011;20:149-57。
- 7。
科尔曼J,Blake-Kalff M,Davies E.植物疾病的解毒:化学改性和真空舱室。趋势植物SCI。1997年; 2:144-51。
- 8。
Cherian S,Oliveira mm。转基因植物在植物修复:最近的进展和新的可能性。环境科技。2005; 39:9377-90。
- 9。
Krishna P. Brassinosteroid介导的应激反应。J工厂增长调节。2003; 22:289-97。
- 10。
Kanwar Mk,Poonam,Bhardwaj R.砷诱导抗氧化防御系统和芸苔类芸苔豆荚的调节芸苔属juncea L. Ecotoxicol Envice Saf。2015; 115:119-25。
- 11.
Sharma A,Kumar V,Singh R,Thukral Ak,Bhardwaj R.种子预浸皂化与24倍纤维化剂对生长和光合参数的影响Brassica Juncea.吡虫啉土壤中的L.。生态毒理学环境科学。2016;133:195-201。
- 12.
表油菜素内酯-吡虫啉相互作用增强非酶抗氧化活性Brassica Juncea.L. Ind J植物理遗。2016; 21:70-5。
- 13.
吴格,崔j,陶l,杨h. fluroxypyr通过在水稻中产生超氧化物和过氧化氢来触发氧化损伤(栽培稻).生态毒罗。2010; 19:124-32。
- 14.
帕特森BD,Mackae EA,Mackae I.使用钛(IV)植物提取物中过氧化氢的估计。肛门生物化学。1984年; 139:487-92。
- 15.
康诺Y.在羟胺的自氧化过程中产生超氧化物的产生和超氧化物歧化酶的测定。拱生物志法生物学。1978年; 186:189-95。
- 16.
过氧化氢酶的体外培养。方法Enzymol。1984;105:121-6。
- 17。
Putter J.过氧化物酶。在:Bergmeyer Hu,编辑。酶促分析方法。纽约:Verlag Chemie-Academic Press;1974年..685-90。
- 18。
大鼠肝脏黄酮酶谷胱甘肽还原酶的纯化与鉴定。中国生物化学杂志。1975;250:5475-80
- 19。
Habig WH,Jakoby WB。谷胱甘肽S-转移酶(大鼠和人)。方法酶。1981; 77:218-31。
- 20。
Sedlak J, Lindsay RHC。用Ellmann试剂估计组织中总巯基、蛋白结合基和非蛋白巯基。学生物化学肛门。1968;25:192 - 205。
- 21。
Livak KJ,Schmittgen TD。使用实时定量PCR和2分析相对基因表达数据-ΔΔct方法。方法。2001; 25:402-8。
- 22。
AOAC官方方法2007.01。硫酸镁,气相色谱/质谱与液相色谱/串联质谱法通过乙腈提取和分配食品中的农药残留。AOAC int。2007年。
- 23。
抗氧化应激、抗氧化剂与应激耐受性。植物科学进展。2002;7:405-10。
- 24。
陈志强,王志强,王志强,等。镉、盐胁迫下28-同油菜素内酯对小麦生长的保护作用。国际生物学杂志。2014;64:130-6。
- 25.
法迪德丁Q,Yusuf M,Ahmad I,Ahmad M. Brassinosteroids及其在植物对非生物胁迫的反应中的作用。Biol Planta。2014; 58:9-17。
- 26.
Asada K,Takahash M.在光合作用中产生和清除活性氧气。在:kyle dj,osmond cb,arntzen cj,编辑。漂亮。阿姆斯特丹:elestvier;1987. p。227-87。
- 27.
咀嚼o,whelan j,millar啊。抗坏血酸 - 谷胱甘肽循环的分子定义拟南芥线粒体揭示植物抗氧化防御的双重靶点。J Biol Chem. 2003; 47:46869-77。
- 28.
TA1 Jan S. Mahmooduzzafar,Fatma T.氧化应激评价豇豆属辐射动物L.对毒死蜱的反应。中国环境科学(英文版),2012;
- 29。
Lascano HR,Gomez Ld,Casano Lm,Trippi Vs.小麦叶片中谷胱甘肽还原酶活性和蛋白质含量的变化和暴露于光氧化应激的叶绿体。植物理性生物化学。1998年; 36:321-9。
- 30.
Thao NP, Tran LS。抗旱大豆基因工程的潜力。生物技术学报2012;32:349-62。
确认
作者对印度科技部向AS提供的INSPIRE奖学金和新德里大学资助委员会提供的先进仪器设备表示诚挚的感谢。感谢Axios Review,两位匿名审稿人和他们的编辑,他们对这份手稿的早期版本提供了有价值的评论。
资金
不适用。
可用性数据和材料
本研究中产生或分析的所有数据均包含在本文中。
作者的贡献
如图所示,ST和VK执行了实验。AS和AKT统计地分析了数据并写了稿件。RB,AKT和AKK设计了实验,监督工作并批判地检查了稿件。所有作者阅读并认可的终稿。
相互竞争的利益
提交人声明他们没有竞争利益。
同意出版
不适用。
伦理批准和同意参与
不适用。
作者信息
隶属关系
相应的作者
权利和权限
开放访问本文遵循知识共享署名4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),它允许在任何媒体上无限制地使用、分发和复制,前提是你给予原作者和来源适当的荣誉,提供一个到知识共享许可协议的链接,并指出是否作出了更改。创作共用及公共领域专用豁免书(http://creativecommons.org/publicdomain/zero/1.0/)除非另有说明,否则适用于本文中提供的数据。
关于这篇文章
引用这篇文章
Sharma,A.,Thakur,S.,Kumar,V.等等。通过调节基因表达,24-呕血素醇促刺激吡虫啉毒品Brassica Juncea.L.BMC植物杂志17,56(2017)。https://doi.org/10.1186/s12870-017-1003-9
已收到:
接受:
发表:
关键词
- Brassica Juncea.
- 吡虫啉毒性
- Brassinosteroids
- 农药残留物