抽象的
背景
棉纤维品质性状,如纤维长度、强度和成熟程度,在棉纤维发育的顺序阶段(细胞伸长、向次级细胞壁构建过渡和纤维素沉积)由基因型和环境决定。棉纤维中薄层在纤维发育过程中对细胞的粘附和分离起着至关重要的作用。为探讨棉纤维品质与棉纤维发育速度的关系,本文对棉纤维特性不同的4个品种进行了结构和组成分析:陆地棉,G. Barbadense.,g . herbaceum和g . arboreum.
结果
棉纤维细胞通过棉纤维中间板(CFML)粘附是一个由基因型决定的发育调控过程。CFML由所有四种产纤维棉花品种中的去酯化高半乳糖醛酸、木聚糖和阿拉伯多糖组成:陆地草,巴巴多斯草,草本草和g . arboreum.明显成对的细胞壁隆起是两种CFML的特征G. Hirsutum从纤维细胞壁脱离开始到次生细胞壁沉积开始的品种。在细胞壁隆起处有丰富的木葡聚糖,在后期这些区域没有果胶阿拉伯糖。
结论
棉纤维的CFML在过渡阶段被重新构造。富含木葡聚糖的成对细胞壁凸起在细胞中更为明显G. Hirsutum品种比其他棉花品种多。
背景
棉花纤维是单细胞,单个纤维作为独立的实体从种子表面开始伸长。然后,纤维在纤维伸长阶段粘附在一起,并在纤维发育的后期再次分离。这使得棉纤维细胞成为研究与胞质分裂无关的植物细胞粘附和细胞分离过程的特殊模型,因为这种过程很少出现在同一发育系统中。棉花纤维细胞发育是一个非常精细的调控过程,从开花当天开始,通常持续50到60天。纤维发育通常分为五个连续和重叠的阶段:起始、伸长、过渡、次生细胞壁合成和干燥(通常被误称为成熟)。
在起始阶段(0至3-5 dpa),表皮细胞由种子表面的某些细胞产生,这些细胞具有纤维首字母和非纤维细胞,比例为1:7 .7 [1].一个种子可以生成约14500纤维屑(长)纤维[2],给出高达1300纤维的纤维密度/ mm2[3.].考虑到花子房包含4到5心皮(小室),通常包含8种子(胚珠)被假定棉纤维成为坚持要求在小腔内的高度拥挤环境空间优化和高膨压维持在协调纤维伸长阶段。在这一阶段,棉纤维获得锥形尖端形状,并以螺旋状的方式在粘连团中拉长[3.,4].
两个粘附的植物细胞之间的聚合物基质称为中间片层,棉花纤维中间片层(CFML)最早由Singh等人描述[4] 在陆地棉它是纤维生产中最商业化的品种之一。CFML是初级细胞壁的一种特殊外层,它介导细胞的粘附并将若干纤维连接成组织样束。因此,CFML并非来自胞质分裂后形成的细胞板,而是来自细胞延伸阶段开始时细胞间的接触。这在发育上与通常认为的植物细胞中间片层不同,后者介导子细胞之间的细胞粘附,并在细胞分裂过程中由细胞板建立[5- - - - - -9].与细胞板衍生的中层板层相似,利用单克隆抗体发现CFML富含木葡聚糖和去酯化的同半乳糖醛酸多糖[4].当纤维伸长时,由于CFML的黏附特性,它们以分组和有序的方式翻转和折叠自己,直到次级细胞壁沉积开始[4].
棉纤维不会突然伸长,但经历过渡阶段,其特征在于纤维素合成率的增加[10]和卷绕层(类似于在木质部导管的S1层)的形成作为第一次生细胞壁层的待沉积内部的初生细胞壁[11]。正是在这个阶段,纤维在次级细胞壁沉积的主要阶段开始时彼此分离。这些发育事件的时间取决于基因型,也受纤维生长期间的温度和环境条件的影响[12- - - - - -15].棉纤维长度是纺织及衍生工业的主要特征。大部分的纤维伸长发生在细胞粘附后,在它们彼此分离和次级细胞壁开始沉积之前。纤维处于延伸阶段的时间在一定程度上决定了纤维的最终长度。因此,了解CFML介导细胞粘附和脱离的机制是重要的知识,有可能用于改善纤维质量。
对CFML的结构和组成的全面了解,以及对不同棉花基因型CFML细胞粘附和脱离过程的发育时间的比较分析等方面还有待进一步研究。这些问题已经在这里得到了解决,在纤维质量非常不同的基因型之间,细胞粘附和细胞分离的不同时间点(纤维质量参数在[16)已确定。此外,CFML的两个不同的细胞壁结构特征G. Hirsutum已鉴定出的品种可能是该物种纤维细胞伸长程度的决定因素。使用免疫化学技术,我们已经鉴定出阿拉伯多糖是CFML的一部分,除了果胶汞和木葡聚糖。综上所述,CFML介导的细胞粘附和细胞脱离的时间在不同基因型之间是不同的,可能会影响纤维品质性状。
方法
植物材料
这项研究中使用的植物及其纤维特性与上述描述相同。16].简而言之,6个驯化自交系(FM966和Coker312 -G. HirsutumJFW15 -g . arboreumKrasnyj -g . herbaceum中国10号和巴西7号G. Barbadense.)播种于土壤堆肥中,每个盆栽中添加30 g的Osmocote®11 N + 11P + 18 K+ 2MgO + TE(工作时间5-6个月),在根特拜耳作物科学种植。除室外光照为>0.25 μmol m外,白天温度设置在24-26°C,随着天气温暖,温度升高至30-35°C,光周期16 h−2年代−1.所有的棉花花在开花当天被标记,以便铃能在期望的dpa收获。其中一种用胚珠培养。棉花卵巢在1或2 dpa下收获,用70%乙醇消毒5分钟,用无菌水清洗。同一子房的所有胚珠在无菌条件下转移到培养皿中。每个培养皿中包含12毫升的媒体(MS培养基4 (M0238)营养素(50毫米硝酸钾作为唯一氮源,KH2PO4 2毫米,2毫米MGSO4)、维生素(4μM烟酸,4μM pyridoxine-HCl 4μM thiamine-HCl 1μM肌醇),pH值5,100毫米葡萄糖,果糖20毫米,10μM IAA和0.5μM3.)胚珠在28°C的黑暗中培养,培养基每3-5天更换一次。
植物材料树脂包埋
采集后,立即从棉铃上仔细地解剖小块纤维组织,使组织破坏最小,并浸泡在4% (v/v) PEM (0.1 M PIPES pH 6.95, 2 mM EGTA, 1 mM MgSO4)缓冲液中的多聚甲醛。固定显影纤维已脱水,树脂包埋,切片如前所述[17].
单克隆抗体(MAB)
本研究中使用的单克隆抗体:LM15 [18],lm25 [19],CCRC-M1 [20.],LM6[21- - - - - -23],LM13 [24,25]和LM19 [26].
显微镜和免疫程序
采用树脂切片免疫荧光法检测细胞壁抗原表位。PBS加5% (w/v)常温下加入牛奶蛋白30 min,以防止非特异性结合。一抗在5%牛奶/PBS中1:5稀释(直接偶联的LM19除外,见下文,其稀释倍数为1:1000)1.5小时。使用抗小鼠或蚁鼠IgG Alexa Fluor488 (Life Technologies)作为二抗,在5%的牛奶/PBS中1:100稀释,样品孵育1小时。在0.02 mg/ml的PBS中使用Calcofluor White (Sigma-Aldrich) 5分钟,以观察细胞壁。使用抗褪色试剂Citifluor glycerol/PBS (Agar Scientific)进行载玻片安装。采用Olympus BX61显微镜(http://www.olympus-global.com/)配备表面荧光照射。显微照片由Hamamatsu ORCA285相机(Hamamastu,http://www.hamamatsu.com.)和珀金埃尔默Volocity软件。所有相关的和比较显微照片使用等效设置捕获,以及相关的显微照片为数据集的发电量相当于方式进行处理。在所有情况下在每个显微照片中示出的区域是代表从一个植物分析至少3个部分看到的纤维组织。的情况下的FM966线显微照片是代表性的3周以上的植物的分析。
结果
棉纤维组织细胞壁/CFML的两个显著特征
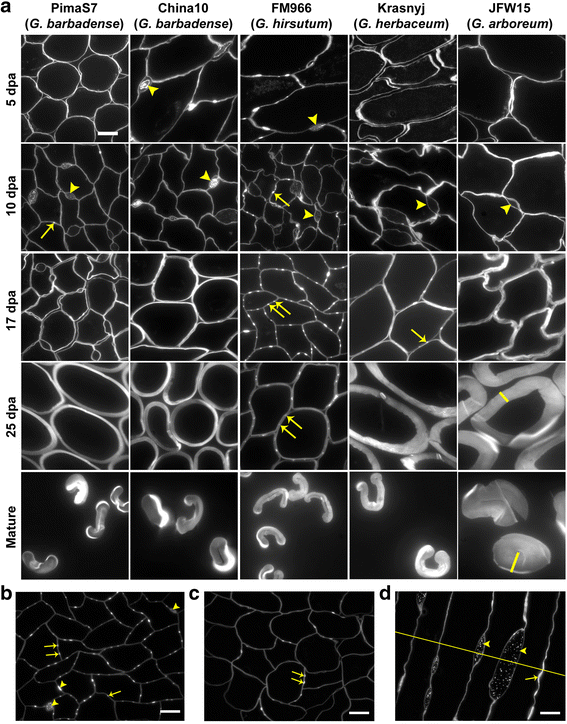
为研究纤维发育过程中细胞壁和中层板层的特征,采用树脂包埋的皮马7 (G. Barbadense.), China10 (G. Barbadense.), FM966 (G. Hirsutum), Krasnyj (g . herbaceum)和JFW15(g . arboreum)用卡尔科弗卢尔白(图进行染色。1)这种染料染色范围广泛的β-聚糖,通常用于揭示解剖结构和细胞壁结构。纤维切片染色显示纤维组织中CFML和细胞壁界面的两个显著特征:扩大的细胞间区域和较小、染色强烈的CFML凸起。细胞壁之间的细胞间隙,其内容物用钙氟白色染色,直径大于2μm,被称为扩大的CFML区域,它们存在于所有分析的棉花品种和品种中,尽管g . arboreum它们较少(图中的箭头)。1a).放大后的CFML区域在同一组织内的大小变化很大,横切面上的长轴通常在2 ~ 10 μm之间(图中的箭头)。1b).此外,横切面G. Hirsutum在纤维组织中观察到,相邻纤维细胞壁的两个高度染色区域位于细胞连接处之间,距离大致相等(图中成对的箭头)。1ab).这些细胞壁特征小,1 μm或更小,重复的配对模式以前似乎没有报道过。FM966表现出大量成对的CFML突起(箭头位于17dpa FM966面板),在10dpa(箭头位于10 dpa FM966面板)和发育后期(箭头位于25 dpa FM966面板)也可以观察到。配对CFML肿胀仅在FM966中明显.虽然其他物种也偶尔显示单个随机分布的CFML凸起(10 DPA PIMAS7面板中的箭头,在17个DPA Krasnyj面板中),它们并不像FM966线那样明显和结构。在Coker312中也经常观察成对的CFML凸起G. Hirsutum线(图。3A),这表明它们是的特征G. Hirsutum物种。
基因型对CFML发育特征的影响。一个PimaS7和China10发育中和成熟棉纤维横截面的钙氟染色(G. Barbadense.), FM966 (G. Hirsutum), Krasnyj (g . herbaceum)和JFW15(g . arboreum).箭头在所有棉线中的CFML放大区域点,箭头点CFML凸起配对仅在G. Hirsutum物种。增厚的次级细胞壁被突出显示黄色的在JFW15线,25 dpa和成熟的面板。b扩大的CFML区域(箭头)显示可变大小而CFML凸起(箭头)均小于1 μm,以成对分布为主G. Hirsutum.c配对CFML膨出也存在于G. Hirsutum体外培养的胚珠。d15 dpa FM966纤维纵切面显示放大的CFML区域的三维结构(箭头),并在CFML凸起的情况下,沿着纤维的纵向条纹(箭头).这些纤维的指示的横截面黄色的线将显示图像相当于B.比例尺=10μm以下。在面板中的所有图像都以相同放大倍率
纤维纵、横截面CFML区域均增大,Calcofluor White染色可见,CFML区域为大的三维结构,呈椭圆形,充满颗粒(如图箭头所示)。1d).另一方面,CFML凸起可以在连续的截面上跟随,这表明每个CFML凸起在纵向截面上沿纤维呈条纹状(图中的箭头)。1d).在从FM966的培养的胚珠中生长的纤维中也存在等效成对的CFML凸起(图。1c),这表明它们的发生不需要显影纤维是一个心室内,此外,该成对的凸出部的安排必须由相邻纤维细胞,而不是由铃的其他营养部分来限定。
棉纤维开发的步伐由棉基因型决定
在相同条件下,棉种间花后5个时间点(5、10、17、25 dpa和成熟纤维)的纤维发育速度存在显著差异,如图所示。1a.这个词发展的步伐是指不同棉系出现共同发育特征,即细胞壁粘附、脱离和次生细胞壁沉积的速度。在中国10和FM966中,5 dpa的纤维细胞粘附很明显,这些细胞系的纤维组织中已经观察到CFML的扩大区域(见箭头5 dpa顶部面板),而在PimaS7、Krasnyj和JFW15中,相同dpa的细胞粘附不完全。在10dpa时,所有细胞系均显示细胞完全粘附,CFML中充满颗粒的放大区域广泛存在于整个组织中,除了JFW15纤维组织,其放大的CFML区域要少得多。在17dpa时,China10、Krasnyj和JFW15的细胞壁脱落开始,而PimaS7和FM966的纤维仍然高度粘连。与其他细胞系相比,FM966细胞系的细胞壁剥离延迟,其他细胞系通过17dpa开始纤维剥离。FM966仅在25dpa时观察到类似的细胞壁脱离。此外,在次级细胞壁沉积的开始和速率上也有明显的差异。在17 dpa时,JFW15细胞株的纤维素沉积较高,而在25 dpa时,FM966纤维细胞壁较其他细胞株更薄,而JFW15和Krasnyj细胞壁增厚。在成熟阶段,JFW15细胞系的纤维素沉积速率较高。而g . arboreum(JFW15)和g . herbaceum(Krasnyj)品种次生细胞壁增厚开始早,纤维素沉积速率高G. HirsutumFM966表现出较长的细胞粘附和特定的CFML模式,纤维素沉积速率较低G. Barbadense.中国10号线和PimaS7号线。在JFW15和Krasnyj品种中,较短的细胞粘附时间和较长的次生细胞壁沉积可能与较低质量的纤维有关。纤维伸长的时间和过渡阶段(这可能与细胞粘附和细胞脱离有关)可能最终影响棉纤维的成熟程度和长度。
CFML动力学和细胞壁聚糖组成在纤维开发期间
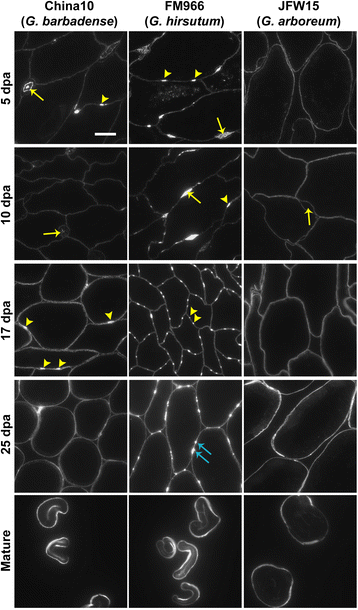
木葡聚糖是CFML的主要成分,可以用木葡聚糖LM25探针进行标记(图)。2).在纤维粘附开始时观察到lm25标记的颗粒,在中国10和FM966品种的纤维伸长期纤维组织中存在的扩大的CFML区域内大量存在(图中5 dpa和10 dpa面板中的箭头)。2),且在JFW15品种中作用较小。在延伸阶段,富木葡聚糖的CFML膨出以单个或成对的形式零星出现(图5和10 dpa图中的箭头)。2).作为纤维的开发的进展,在CFML木葡聚糖降解或重排似乎发生:有利于大多数细胞(箭头之间丰富木葡聚糖凸出部的观察在图17个25 DPA面板在放大CFML区域更少的富含木葡聚糖颗粒。2)在FM966品种中出现最多。
木葡聚糖定向单抗LM25对棉纤维切片的免疫荧光标记。成对的CFML鼓包被限制到G. Hirsutum如在China10在不同发育阶段的纤维组织的横截面标记由木葡聚糖的mAb LM25物种(G. Barbadense.), FM966 (G. Hirsutum)和JFW15(g . arboreum)线。5和10 dpa谱图:放大区域富含LM25表位(箭头)及鼓胀(箭头)在优质品种China10和FM966的纤维组织而从JFW15,低质量的纤维品种缺席CFML的。17个DPA面板:木葡聚糖在单个或成对的凸起结构(箭头),并在FM966细胞脱离时保持作为细胞间的锚定点(蓝色箭头).比例尺=10 μm。图中所有的图像都是同样的放大倍数
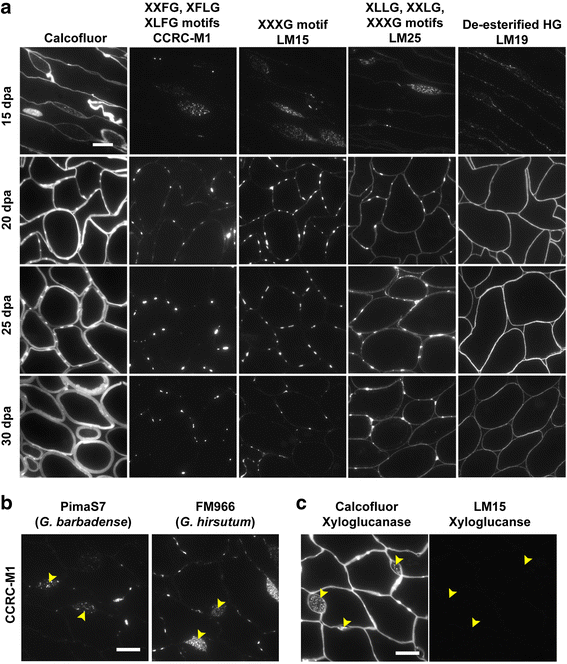
为了进一步探索CFML的成对突起的组成,从另一个纤维组织的横截面G. Hirsutum在15、20、25和30 dpa的品种(Coker312)上标记更广泛的木葡聚糖抗体(图。3a).CCRC-M1和LM15探针以及LM25显示了CFML扩大区域内木葡聚糖含量的颗粒性质,并在20和25 dpa的次级细胞壁沉积开始时与配对的CFML隆起强烈结合。25dpa时,细胞连接处的细胞脱离明显,而CFML隆起仍然是相邻细胞之间的连接点。在晚期的次级细胞壁阶段仍可见残余的CFML突起(图)。3a30 dpa)。它非常感兴趣的是配对的CFML凸起G. Hirsutum在细胞分离前的细胞间隙的开口期间,栽培品种也似乎是细胞之间的锚定点(图。3a, 30 dpa LM25面板和图。2,25 DPA FM966面板)。
CCRC-M1和LM15单克隆抗体识别的木葡聚糖基元对CFML是特异性的。一个所有显微照片都是Coker品种的纤维组织的横截面(G. Hirsutum).钙荧光染色的LM15标记的切片显示在左手边。木糖葡聚糖(CCRC-M1和LM15面板)的岩藻糖基化和XXXG基丝在CFML凸起中突出,而这些棉纤维细胞壁在棉纤维细胞壁中较小,其中半乳糖基化的木葡聚糖出现均匀分布(LM25面板)。在从伸长率到二次电池壁沉积的转变阶段期间的配对CFML凸形不被脱酯化的HG表位(LM19面板)所示。b10 dpa截面G. Barbadense.PimaS7和G. HirsutumFM966品种显示在CFML中存在聚焦木葡聚糖(箭头).c15 DPA横截面G. Hirsutum用木瓜葡聚糖酶处理的FM966品种除去Xyloglucan(箭头在正确的但不影响氟钙白对CFML的染色箭头在左(图)表明存在其他尚未鉴定的β-葡聚糖。比例尺=10 μm。每个面板中的所有图像都是在相同的放大倍数
来自G. Barbadense.品种分析[27],发现其成分与对照组不同G. Hirsutum由于岩藻木聚糖不能被检测到。在我们的手中,发生在CFML中岩藻糖化木葡聚糖G. Barbadense.也在G. Hirsutum采用CCRC-M1探针检测品种[20.]图,如图所示。3b.此外,用木葡聚糖酶处理纤维切片可以有效地去除木葡聚糖LM15表位,但它不能消除钙荧光白染色(图)。3c)提示CFML中存在其他β-聚糖,目前任何探针都无法检测到。
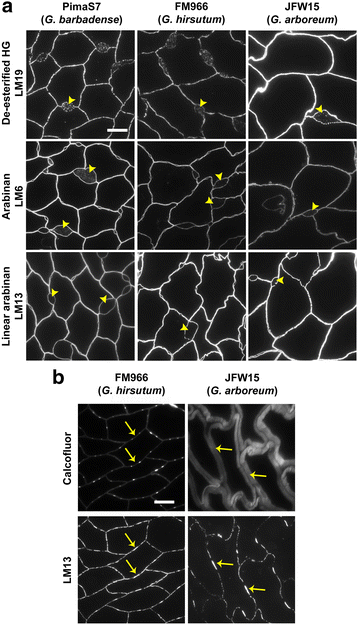
一组扩展的抗体被用来确定CFML(图1的组合物。4).除了木葡聚糖,则LM19去酯化也放大CFML区域(图内检测homogalacturonan表位。4A)在PimaS7 (G. Barbadense.), FM966 (G. Hirsutum)和JFW15(g . arboreum)一般来说,HG LM19探针在扩大的CFML区域内显示出同质标记,这表明含有木聚糖的颗粒可以保存在基于果胶的基质中。与LM19表位类似,LM6阿拉伯多糖表位不仅在纤维细胞壁中检测到,而且在扩大的CFML区域内也检测到(图。4A),主要在PimaS7品种中。另一方面,在扩大的CFML区域未检测到LM13线性阿拉伯多糖表位,但与所有棉花品系的细胞壁紧密结合。此外,FM966中处于过渡阶段(17 dpa)的纤维组织G. Hirsutum当配对的CFML突起明显时,CFML突起周围区域的arabinan LM13表位缺失(图。4B.).有趣的是,在JFW15中的次级细胞壁之间观察到类似的LM13表位的散散检测(图。4B.).这些观察结果可以指示用于阿拉伯聚糖降解为棉纤维细胞壁脱离的一个方面的可能作用。
讨论
棉纤维有一个中间的薄片,它不是起源于细胞板形成后的细胞质分裂,而是在伸长的棉纤维与细胞接触后产生的。CFML将纤维细胞聚集在一起,并帮助它们旋转和折叠,在细胞快速伸长阶段,使细胞在非常有限的棉室体积内进行优化包装。通过对5个棉系在不同dpa条件下的细胞和组织形态的比较,发现细胞粘附的时间、过渡阶段以及纤维素在次生细胞壁沉积的速度是纤维发育过程中主要的形态变量。这项工作揭示了CFML的新特征:颗粒填充的放大区域和CFML凸起(大多成对出现在G. Hirsutum品种)。用对细胞壁多糖的单克隆抗体筛选揭示了几种木糖葡聚糖表位的存在,包括岩藻葡聚糖(CCRC-M1)在两者的扩大的CFML区域中G. Hirsutum和G. Barbadense.除先前报道的去酯化汞外,还有阿拉伯多糖[4].相比之下,只有木葡聚糖在CFML凸起被大量检测。
放大CFML区域颗粒的来源可能是多种细胞壁疏松酶的共同作用,如膨胀素、内切葡聚糖酶和内转糖基酶,它们释放细胞壁碎片,使细胞扩张。xg -纤维素系链的降解在细胞壁松动中是必不可少的,这种降解可以通过木葡聚糖酶和木葡聚糖内转葡萄糖基酶/水解酶(XTH)来完成[28- - - - - -30].有关棉纤维的文献多次报道纤维伸长过程中基因上调和细胞壁重塑酶活性达到峰值,然后在过渡阶段下降[31- - - - - -34].CFML区域中的木葡聚糖可能是细胞壁中广泛的酶活性的结果,这种酶活性消化并释放聚合物到细胞间隙中,以创建一个粘连的中间板层。据报道,在番茄果实中,木葡聚糖参与了果皮薄壁组织的细胞粘附[35].这些观察结果可能表明木葡聚糖和果胶在纤维内聚性控制中的重塑作用。
配对的CFML凸起可能是最佳思想作为线性纵向细胞壁区域,并且是细胞壁异质性的清晰情况。配对凸起的醒目模式在FM966和属于的Coker312品种中的过渡阶段突出G. Hirsutum种细胞如何调节这种特定细胞壁模式的形成以及其目的是什么是一个有趣的问题。似乎成对模式中的CFML组织是特定于G. Hirsutum这些沿着伸长轴的规则结构可能以某种方式参与了维持轴细胞伸长的过程,尽管这在其他物种中并不明显,但对纤维的发育不是必需的。成对的凸起在某种程度上可能与相对较大的延伸率有关G. Hirsutum线或者它们也许有助于在次生细胞壁沉积的阶段开始细胞壁脱离如在一些情况下它们出现标记间空间形成的早期阶段的程度。在此它们都让人联想到玉米叶栅栏细胞的电子致密区域的叶肉空气空间的开发过程中[36].
结论
这项工作首次提供了棉纤维发育过程中与CFML相关的细胞粘附和分离过程的全面的原位生化分析,并确定了与CFML相关的两个细胞壁特征;CFML膨大区和CFML膨大区,后者具有独特的配对模式G. Hirsutum物种。总之,该作品已经确定了细胞壁族聚糖的细胞壁结构域和各方面,所述细胞壁聚糖异质性似乎与可能影响纤维质量的纤维电池粘附和分离过程有关。
参考
- 1.
斯图尔特JM。在棉花胚珠纤维起始(陆地棉).我是J机器人。1975; 62(7):723-30。
- 2.
鲍曼DT,厢式ESbroeck GA,范特霍夫Ĵ,Jividen GM。在现代高地棉花胚珠纤维细胞的数量。Ĵ棉科学。2001; 5(2):81-3。
- 3.
棉纤维发育过程中的自组织现象。中国科学(d辑:地球科学)2004;8(2):127-33。
- 4.
Singh B, Avci U, Eichler Inwood SE, Grimson MJ, Landgraf J, Mohnen D, Sorensen I, Wilkerson CG, Willats WG, Haigler CH.初级细胞壁的一种特殊外层连接棉纤维成为组织样束。植物杂志。2009;150(2):684 - 99。
- 5。
Nishitani K,Demura T.编辑:植物细胞壁的新兴视图作为吻合型智能系统。植物细胞生理。2015; 56(2):177-9。
- 6。
Matar D, Catesson AM。根分生组织中果胶中层片层的细胞板发育和延迟形成。原生质。1988;146(1):10 - 7。结果
- 7。
Albersheim P,Darvill A,Roberts K,Sederoff R,Staehelin A.植物细胞壁。纽约:花环科学;2011年。
- 8。
knox jp。细胞粘附,细胞分离和植物形态发生。植物杂志1992; 2(2):137-41。
- 9。
Daher FB,Braybrook SA.《如何放手:果胶与植物细胞粘附》。前沿植物科学。2015;6:523。
- 10.
Meinert MC, Delmer DP。棉纤维发育过程中细胞壁生化成分的变化。植物杂志。1977;59(6):1088 - 97。
- 11.
弗林特EA.《棉纤维的结构和发展》,《生物学》1950年版;25(4):414-34。
- 12.
芒格P, Bleiholder H, Hack H, Hess M, Stauß R, van den Boom T, Weber E.棉花物候生长阶段(陆地棉L.):根据BBCH量表进行编码和描述。作物学报,1998;180(3):143-9。
- 13
Thaker VS,Saroop S,Vaishnav PP,Singh YD.基因型变异和昼夜温度对棉花纤维发育的影响。1989年《田间作物决议》;22(2):129–41.
- 14
黄建勇,罗国良,黄建勇。循环温度对棉花胚珠纤维代谢的影响。植物杂志。1992;100(2):979 - 86。
- 15
温控温度对棉花产量和纤维性质的影响。中国农业科学。1998;130(04):463-71。
- 16。
Hernandez的-Gomez的MC,Runavot J-L,过X,Bourot S,Benians TAS,Willats WGT,Meulewaeter女,诺克斯JP。Heteromannan和杂木细胞壁多糖显示棉纤维细胞发育的伸长和次生细胞壁沉积阶段期间不同的动态。植物细胞生理。2015; 56(9):1786至1797年。
- 17。
李康德,诺克斯太平绅士。硬组织中植物细胞壁的树脂包埋、切片和免疫细胞化学分析。In:I381;árskýV,CvrčkováF,编辑。植物细胞形态发生,第1080卷。纽约:Humana出版社;2014P41–52.
- 18。
Marcus SE, Verhertbruggen Y, Herve C, ordas - ortiz JJ, Farkas V, Pedersen HL, Willats WG, Knox JP。果胶同半乳糖醛酸在植物细胞壁中掩盖了丰富的木葡聚糖表位。BMC Plant Biol. 2008;8:60。
- 19。
Pedersen HL, Fangel JU, McCleary B, Ruzanski C, Rydahl MG, Ralet M-C, Farkas V, von Schantz L, Marcus SE, Andersen MCF等。用于植物糖生物学和细胞壁研究的多功能高分辨率低聚糖微阵列。中国生物化学杂志。2012;287:39429-38。
- 20.
PuhlmannĴ,Bucheli E,斯温MJ,催款N,Albersheim P,Darvill AG,哈恩MG。对植物细胞壁多糖的单克隆抗体的产生。I.的单克隆抗体的表征给终端-α-(1- - > 2)连接的含有岩藻糖基的表位。植物理性。1994; 104(2):699-710。
- 21.
Jones L, Seymour GB, Knox JP。利用单克隆抗体定位番茄细胞壁中的果胶半乳糖(1[−>]4)-[beta]- d -半乳糖。植物杂志。1997;113(4):1405 - 12所示。
- 22.
Willats WGT, Knox JP果胶多糖的免疫谱分析。学生物化学肛门。1999;268(1):143 - 6。
- 23.
Willats WG,Marcus SE,Knox JP。对(1-> 5)-alpha-l-Arabinan的单克隆抗体的产生。Carboohydr Res。1998; 308(1-2):149-52。
- 24.
Moller I,Marcus Se,Haeger A,Verhertbruggen Y,Verhoef R,Schols H,Ulvskov P,Mikkelsen JD,Knox JP,Willats W.通过其碳水化合物微阵列的分层聚类对植物细胞壁聚糖的单克隆抗体的高通量筛选配置文件。Glycoconj J. 2008; 25(1):37-48。
- 25
关键词:拟南芥多糖,植物细胞壁,发育复杂性,发育机制植物j . 2009; 59(3): 413 - 25所示。
- 26
Verhertbruggen Y, Marcus SE, Haeger A, ordas - ortiz JJ, Knox JP。一组果胶同半乳糖醛酸单克隆抗体。Carbohydr研究》2009;344(14):1858 - 62。
- 27
陈志强,陈志强,陈志强,等。棉花纤维细胞壁的研究进展陆地棉和海岛棉有相关的松散结合的木葡聚糖的差异。Plos一个。2013; 8(2):14。
- 28。
•DJ。植物细胞壁因扩张而松动。大自然。2000;407(6802):321 - 6。
- 29。
Fry Sc,Smith Rc,Renwick Kf,Martin Dj,Hodge Sk,Matthews KJ。Xyloglucan内甲糖苷酶,来自植物的新壁松动酶活性。Biochem J. 1992; 282(PT 3):821-8。
- 30.
陈志强,陈志强。木葡聚糖在植物细胞中的作用。摩尔。2011;4(1):17-24。
- 31.
关键词:棉纤维细胞,细胞壁相关酶,mrna,转录因子植物生理学报。1997;38(3):375-8。
- 32.
Orford SJ, Timmis JN。一个膨化蛋白基因在棉纤维伸长过程中的特异性表达。生物物理学报。1998;1398(3):342-6。
- 33.
Michailidis G, Argiriou A, Darzentas N, Tsaftaris A.异源四倍体木葡聚糖内转糖基化酶/水解酶(XTH)基因分析(陆地棉)及其二倍体祖在纤维伸长过程中表达。acta botanica sinica(云南植物研究),2009;
- 34.
邵明,王新东,倪敏,碧碧N,袁森,马立伟,张惠平,刘应祥,华淑娟。木葡聚糖内转糖基酶/水解酶基因对棉花纤维伸长的调控。中国生物医学工程学报。2011;10(4):3771-82。
- 35.
ordas - ortiz JJ, Marcus SE, Knox JP。细胞壁微观结构分析表明,半纤维素多糖在番茄果皮薄壁组织的细胞粘附中起着重要作用。摩尔。2009;2(5):910 - 21所示。
- 36.
KollöffelC,Linssen PWT。形成豌豆种子的子叶中细胞间隙的形成。原生质。1984; 120(1):12-9。
致谢
我们感谢Sue Marcus提供了本研究中使用的单克隆抗体,感谢Martin Fuller帮助对一些品种进行切片。
资金
这项工作得到了欧盟第七框架计划(FP7 2007-2013)的支持,批准协议No. 263916。本文仅反映作者的观点。欧洲共同体对本网站所载资料的任何用途概不负责。
数据和材料的可用性
在当前研究期间和/或分析的数据集可从相应的作者获得合理的请求。
作者的贡献
MCHG收集棉纤维材料,进行免疫化学测定法,分析和解释数据和写的手稿。JLR收集棉纤维材料,并有助于该数据分析和解释数据。FM提供了这项研究,指导这项工作中使用的棉花植株,并促成了数据的数据分析和解释。JPK指导这项工作,促成了数据的数据分析和解释,并在此稿件的写作的主要贡献者。所有作者阅读并认可的终稿。
相互竞争的利益
提交人声明他们没有竞争利益。
同意出版
不适用。
伦理批准和同意参与
不适用。
出版商的注意
施普林格《自然》杂志对已出版的地图和机构附属机构的管辖权要求保持中立。
作者信息
从属关系
相应的作者
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/)如果您向原始作者和源给出适当的信用,则允许在任何介质中进行不受限制的使用,分发和再现,提供指向Creative Commons许可证的链接,并指示是否进行了更改。Creative Commons公共领域奉献豁免(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条提供的数据,除非另有说明。
关于这篇文章
引用这篇文章
Hernandez-Gomez, m.c., Runavot, JL。Meulewaeter F。et al。不同纤维品质品种棉纤维中间片层的发育特征与细胞粘附和细胞分离的关系。植物生物学17,69(2017)。https://doi.org/10.1186/s12870-017-1017-3
收到了:
接受:
发表:
关键字
- 棉花纤维
- 中胶层
- CFML
- 细胞粘附
- 细胞壁
- Gossypiumspp。
- 多糖