摘要
背景
花期干旱胁迫是玉米减产的主要原因。在产量可持续性方面的遗传和生物技术改进需要理解支撑产量损失的机制。蔗糖缺乏被认为是籽粒败育的原因;然而,基因改良的潜在靶点尚未确定。玉米的田间和温室干旱研究费用昂贵,而且可能难以重现结果;因此,一个在体外籽粒培养法被认为是玉米开花时(授粉后3天)发生干旱胁迫的代理。该方法用于关注干旱对籽粒代谢的影响,以及海藻糖6-磷酸(Tre6P)和蔗糖非发酵-1相关激酶(SnRK1)作为这一反应的潜在调控因子的作用。
结果
在从植株中去除核后的头两个小时内,可以观察到Tre6P的急剧下降,由此产生的转录本丰度变化表明SnRK1被激活,并立即从合成代谢转变为分解代谢。一旦Tre6P水平消耗到1 nmol∙g以下−1无论培养基中是否存在蔗糖,在96 h的实验过程中SnRK1都保持活性。对蔗糖富集培养基的回收可以恢复蔗糖合成和糖酵解过程。生物合成过程包括柠檬酸循环和蛋白质和淀粉的合成被切除抑制,即使重新添加蔗糖也不能恢复。我们还观察到,切除会诱导糖转运体SUT1和SWEET1的转录,蔗糖水解酶细胞壁转化酶2 (INCW2)和蔗糖合成酶1 (SUSY1), II类海藻糖磷酸合成酶(TPS),海藻糖酶(TRE)和海藻糖磷酸磷酸酶(ZmTPPA.3),以前被证明可以增强耐旱性(Nuccio等人,Nat biotechnology(2014年10月):1 - 13,2015)。
结论
耳核切除的影响引发了一连串的事件,从Tre6P水平的急剧下降开始。我们认为,去除Tre6P对SnRK1活性的抑制可能导致SnRK1靶基因的转录和代谢由生物合成向分解代谢过渡。这凸显了Tre6P在饥饿代谢反应中的重要性。我们还提出了糖可以介导SnRK1激活的证据。Tre6P的急剧下降与ZmTPPA转录的大幅增加相对应。3.,indicating that this specific enzyme may be responsible for the de-phosphorylation of Tre6P. The high levels of Tre6P in the immature embryo are likely important for preventing kernel abortion.
背景
花期干旱影响大多数作物,特别是玉米等谷物,渗透胁迫导致的籽粒流产是产量损失的主要原因之一[1- - - - - -5].干旱条件下,籽粒败育与(i)蔗糖消耗和糖含量降低、(ii)蔗糖降解酶活性和转录水平降低、(iii)籽粒淀粉消耗增加有关。下沉组织的淀粉储备有限,可以帮助缓冲饥饿的影响;然而,通常情况下,卵巢的淀粉量不足以维持较长一段时间[6].长期干旱胁迫会改变胚胎的代谢状态,使其无法利用可利用的蔗糖[7],通过激活衰老基因,损伤变得不可逆,导致程序性细胞死亡和核败育[8].
海藻糖(α- d -吡喃葡萄糖基-(1→1)-α- d -吡喃葡萄糖苷)及其前体海藻糖-6-磷酸(Tre6P)被发现具有多种不同的功能,包括储存化学能、保护渗透、防御病原和昆虫以及耐非生物胁迫[9- - - - - -13].海藻糖在细菌、真菌和昆虫体内是一种重要的渗透保护剂,在这些地方它能高浓度积累[14].大多数植物只积累微量的海藻糖,它不太可能起到渗透保护剂的作用。15].在开花植物中,海藻糖的含量通常在皮到纳摩尔范围内,这表明海藻糖及其前体Tre6P可能在植物的源库关系代谢中发挥调节或感知作用[16,17].最近的证据表明,Tre6P在糖感测中起着核心作用[18- - - - - -23],从而提出Tre6P是蔗糖可用性的信号,反过来调节蔗糖的生产和利用[18].也有人提出Tre6P是蔗糖水平的负反馈调控因子[24,25],可能是通过与SnRK1的相互作用[20.,26,27].有大量报道称,海藻糖通路是通过组成性过表达TPS或TPP来工程的[28,29].在某些情况下观察到耐旱性提高,但没有提出任何行动模式[30.- - - - - -32].也许,Tre6P在植物对非生物胁迫的反应中发挥作用的最决定性证据是使用在小穗中异位产生TPP的转基因玉米[33],该研究证明,在水充足的条件下,玉米穗小穗中Tre6P水平的降低可以提高产量,甚至在严重干旱胁迫下更重要。
在体外籽粒栽培被选为干旱胁迫的替代品,为理解干旱条件下对水分亏缺的反应并最终提高作物产量提供了一个模型系统。玉米在体外利用玉米籽粒培养来表征未成熟玉米籽粒(在缺水胁迫期间)的蔗糖饥饿对生长、代谢、能量状态、基因表达和海藻糖通路的影响。之前的研究使用在体外核培养研究了热胁迫的影响[34,激素合成[35,36],碳和氮的利用[37]和授粉效率[38].在本实验中,授粉后3天(DAP)的种子置于无菌培养中,经过48小时的蔗糖饥饿和48小时的恢复。在实验过程中监测生长和能量状态的关键代谢指标,包括Tre6P、SnRK1、糖、糖磷酸和有机酸。对在生长、沉库强度、蔗糖代谢、糖转运、淀粉代谢中起作用的选定基因的表达的详细描述提供了在蔗糖饥饿和恢复期间发生在年轻胚胎中的代谢过程的图像。
结果
玉米内核的文化
玉蜀黍ssp。梅斯品种B73是按照材料和方法中所述的在田间补充浇水的条件下种植的。穗经人工授粉后收获3dap。果仁经解剖取出,表面消毒后置于MS琼脂上。代谢产物和酶的分析如材料和方法所述。在开发这种方法时,籽粒最初培养15天,以评估长期生长在蔗糖、葡萄糖、果糖和糖饥饿的反应(附加文件1:图S1)。在纯ms培养基上籽粒生长不明显;虽然看起来很健康在蔗糖、葡萄糖或果糖上培养的籽粒在15天内质量增加了一倍以上。糖的种类或浓度对生长没有显著影响。在MS盐(饥饿)或MS盐中添加150mm蔗糖培养9天,以评估饥饿对生长的长期影响(附加文件)2:表S1)。在一个单独的实验中,蔗糖、己糖和淀粉在11天的培养过程中被测定,比较纯ms培养基和富蔗糖培养基(150 mM)(附加文件)3.:图S2)。在最初24小时内发生初步变化后,这三种物质的水平都保持不变。
饥饿和恢复对代谢物水平的影响
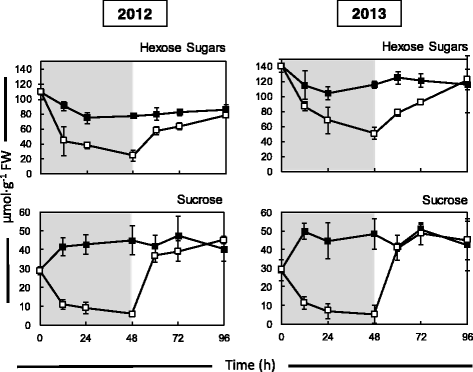
测定了饥饿对籽粒中糖和淀粉水平的影响。将3dap收获的籽粒放置在仅含ms的培养基或富含蔗糖的培养基(150 mM)上48小时。然后将所有籽粒转移到富含蔗糖的培养基上48小时(回收)。在48h饥饿条件下,籽粒中的蔗糖含量在培养的前12小时内迅速下降,而在连续蔗糖条件下,籽粒中的蔗糖含量开始上升,并在培养的前12小时内趋于稳定(图1)。1).饥饿籽粒的蔗糖水平恢复到与连续喂糖籽粒无法区分的水平。所提供的数据来自2012年收获的玉米粒。该实验在2013年再次进行,结果无显著差异(图5)。1).2013年籽粒蔗糖耗损率和恢复率相近,均为3.19 μmol∙g−1h−1和3.55μ摩尔∙g−1h−1分别。尽管植物有补充灌溉,但不同年份的环境条件变化很大4:表S2)。2012年生长季被认为是干旱的一年,有最高的温度和生长度(GDD),而2013年生长季对该地区来说更典型。
饥饿对tre6p和其他代谢物的影响
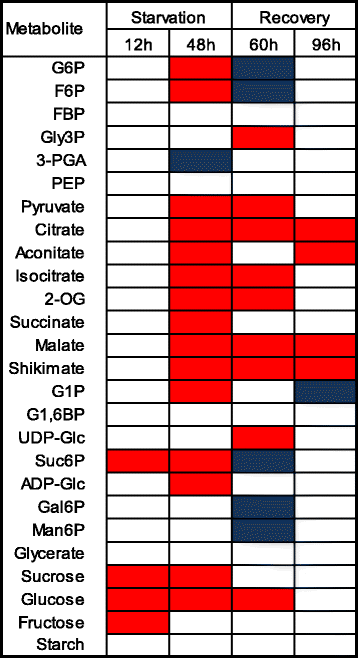
为了评估饥饿和恢复处理对玉米籽粒代谢的影响,对蔗糖和淀粉合成、糖酵解和柠檬酸循环中使用的代谢物进行了分析(图1)。2;额外的文件5:图S3)。剥夺蔗糖48 h可使Glc和Fru降低至极低水平(<10 μmol∙g−1FW),这种下降在很大程度上被培养基中蔗糖的添加所逆转。糖酵解中间体Glc6P、Fru6P(糖酵解、Suc合成和淀粉合成中间体)、果糖1,6-二磷酸(FBP;一种糖酵解的中间体)和甘油3-磷酸(Gly3P;(一种合成甘油脂的中间体)在蔗糖对照中上升,但在饥饿处理中保持不变或仅略有上升,而3PGA和PEP在饥饿处理中比蔗糖对照上升更多。其中许多差异在饥饿48小时时具有统计学意义。丙酮酸在12小时后急剧下降(从150到60纳摩尔∙g−1FW),饥饿处理比对照组下降更明显。许多柠檬酸循环中的中间产物在蔗糖控制下保持较高的含量,但在饥饿处理下下降,包括柠檬酸、联合酸、异柠檬酸、2-氧戊二酸、琥珀酸和苹果酸(图4)。3.).*在从饥饿中恢复的过程中,饥饿的玉米粒中的糖磷酸盐水平恢复到那些持续食用蔗糖的玉米粒的水平。3PGA和PEP仍略高于蔗糖对照组,但不显著。令人惊讶的是,许多有机酸在含蔗糖的培养基上恢复后并没有恢复到初始水平,表明对丙酮酸激酶和/或PEP羧化酶有抑制作用。
蔗糖饥饿对3dap B73籽粒代谢产物水平(以鲜重为基础)的影响(2012季)。如Lunn等人所述,所有代谢物均采用阴离子交换色谱法和质谱联用法测定。[18].对照籽粒在连续蔗糖上用封闭的广场.籽粒饥饿48小时(阴影区域),然后在150 mM蔗糖上恢复48小时开放的广场.平均值采用4个生物重复计算,每个重复3个植物。重要性表示为星号由学生t检验(P< 0.05)
离体籽粒的蔗糖和淀粉代谢也受到饥饿的影响。蔗糖剥夺导致S6P迅速下降,回到富蔗糖培养基后,S6P恢复到对照水平,而在连续喂食的籽粒中,S6P稳定上升。在饥饿的前8小时,S6P的下降比Glc6P和Fru6P更明显,两者在蔗糖和淀粉合成中都很重要(图6)。3.).在蔗糖对照和饥饿处理中,ADPGlc和莽草酯含量均显著降低,表明芳香族氨基酸合成下降,但在蔗糖对照中,莽草酯残留量略高。补加蔗糖后,ADPGlc和莽草酯水平保持在较低水平。
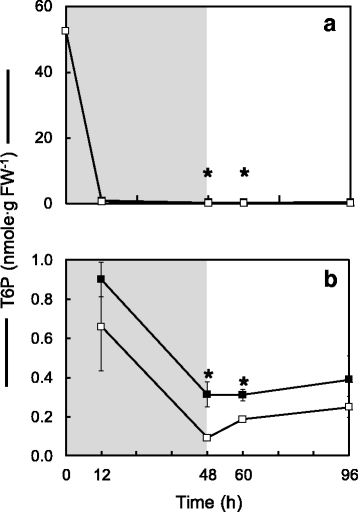
Tre6P水平从54 nmol∙g FW大幅下降−1在培养的前12小时内,在添加蔗糖和不添加蔗糖的样品中都观察到这种情况,并在整个实验期间保持这种情况(图1)。4).*Tre6P已被证明通过激活PEP羧化酶来刺激柠檬酸循环中的通量,因此,被切除的果仁中Tre6P水平低以及再供应蔗糖后缺乏恢复可能会阻止该酶的激活,并解释了被切除的果仁中有机酸的减少以及蔗糖无法恢复这种减少的原因[25].图中没有包含零时间点。4 b因此,Tre6P在最初大幅减少之后的较小后期变化可以更清楚地看到。现在可以看到,在整个实验过程中,蔗糖剥夺会导致果核中Tre6P的进一步减少。
蔗糖饥饿对培养玉米籽粒Tre6P水平的影响(2012季)采用阴离子交换色谱-质谱联用法测定核组织中Tre6P含量[18].一个对照籽粒在连续蔗糖上用封闭的广场.籽粒饥饿48小时(阴影区域),然后在150 mM蔗糖上恢复48小时开放的广场.b扩展了12-96小时的区域。平均值采用4个生物重复计算,每个重复3个植物。重要性表示为星号由学生t检验(P< 0.05)。弗兰克-威廉姆斯,鲜重
饥饿对恢复的影响在体外snrk1活动
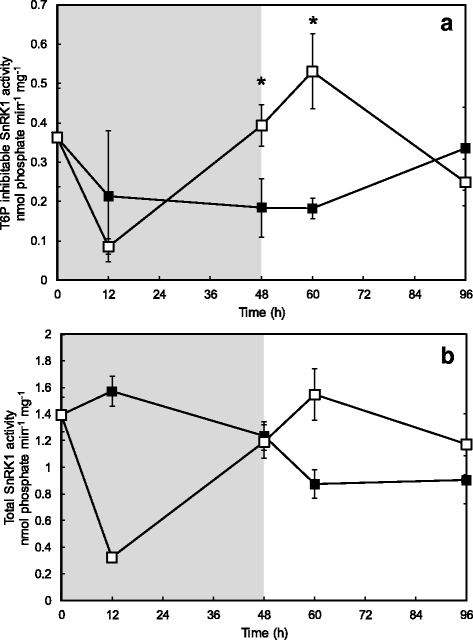
为了评估饥饿和恢复处理对培养玉米籽粒胁迫和蔗糖饥饿传感器SnRK1的影响,在体外测定SnRK1活性。此前已有研究表明,玉米籽粒提取物中的SnRK1活性对Tre6P的抑制高度敏感[39].测定总SnRK1和抑制tre6p (1 mM)的SnRK1活性,并用图形表示为抑制tre6p的活性(图1)。5).对照组和饥饿的籽粒在培养后显示出抑制t6p的SnRK1活性下降,然后在两种处理的96小时恢复到接近初始水平。在连续饲喂的对照组中,这一过程是单调发生的,但在饥饿处理中,抑制tre6p的SnRK1活性在12 - 48小时之间显著上升,并在重新添加蔗糖12小时后继续升高。与对照样品相比,蔗糖缺乏的籽粒在48和60 h时SnRK1活性显著升高。
Tre6P制约在体外SnRK1在对照和缺糖籽粒中的活性(2012季)。在组织提取物中测定SnRK1活性,如[20.].加入外源性Tre6P (1 mM)来测定SnRK1活性对Tre6P抑制敏感的比例。图中阴影区为籽粒饥饿期,无阴影区为恢复期。对照样品用满了广场(黑色的)和饥饿的籽粒用开放的广场(白色).星号表示与对照的显著差异(P< 0.05;n= 3).标准误差显示为垂直的酒吧
饥饿和恢复对基因表达的影响
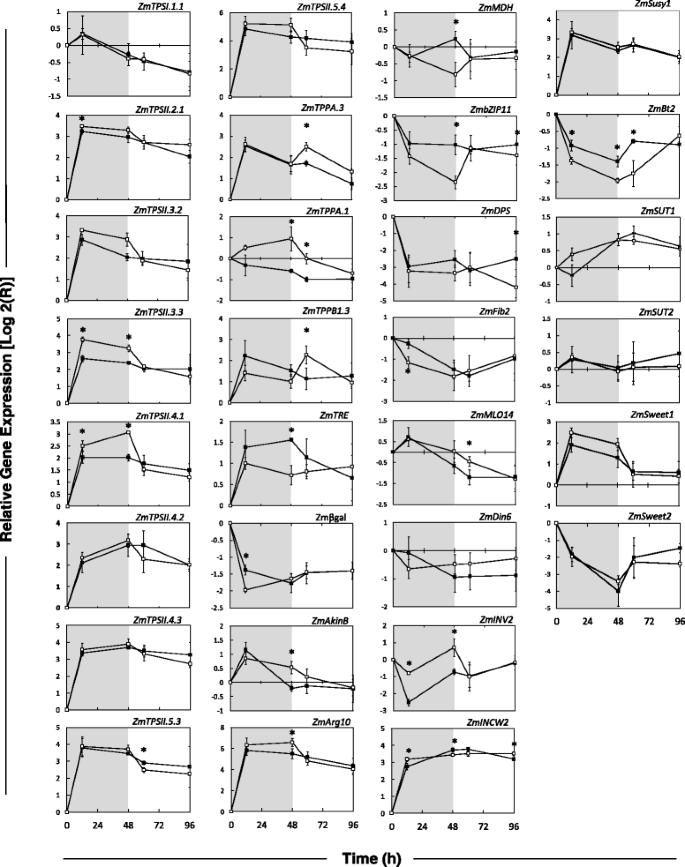
研究了蔗糖剥夺和恢复对基因表达的影响。通过qRT-PCR检测海藻糖通路相关基因(TPS、TPP和TRE)、SnRK1靶基因和糖代谢和转运相关基因的相对基因表达(图1)。6).在TPS基因,编码I类和II类酶的基因对蔗糖缺乏的反应不同。I类基因(ZmTPS1.1),编码具有催化活性的TPS酶,在12 h后逐渐下降,在连续饲喂和不饲喂蔗糖的籽粒之间表达无显著差异。所有的II级TPS研究的基因在蔗糖剥夺的前8小时内被诱导。所有二级班都有一种趋势TPS在缺乏蔗糖的样品中,只有3个(ZmTPSII.2.1,ZmTPSII.3.3而且ZmTPSII.4.1)在12 h和48 h时间点蔗糖缺乏处理与对照之间存在显著差异(Student 's t检验,α = 0.05)。这种效应在重新添加蔗糖后被逆转。
与II类TPS基因相比页基因并没有以这种协调的方式做出反应。为ZmTPPA.3在培养的前8小时,有大量的转录水平诱导。对于该基因,在饥饿的前48小时内,对照和饥饿处理之间没有差异,但在恢复过程中,先前饥饿的籽粒的基因表达高于对照。ZmTPPB.1.3基因表达与ZmTPPA.3,显示在培养的前8小时有相当大的诱导(图。6).缺乏蔗糖的籽粒转录水平对蔗糖恢复的响应程度更大。ZmTPPA.1在蔗糖存在的条件下,转录水平不受影响,但由于饥饿,转录水平有小幅上升。ZmTRE(海藻糖酶)在培养的前8小时出现诱导,在饥饿48小时后被显著抑制。ZmTRE在蔗糖恢复期间,mRNA水平恢复到对照样品。
利用9个推测的SnRK1靶基因的转录水平,评估饥饿和恢复治疗对SnRK1信号通路的影响[27].根据拟南芥玉米同源序列设计引物:5个SnRK1诱导基因(ZmβGal,ZmMOL14和ZmDIN6)和4个SnRK1抑制基因(ZmMDH、ZmbZIP11、ZmDPS和ZmFiB2).选择的SnRK1靶基因对栽培和蔗糖剥夺胁迫均有响应。对于应激特异性SnRK1靶基因,ZmAkinβ已经被证明是诱发的ZmMDH, ZmbZIP11而且ZmFiB2是压抑的27].在推测上调的SnRK1靶点中,有4个相应的反应:ZmAkinβ,ZmArg10, ZmDIN6而且ZmMol14当玉米粒被放入培养液中时。在推测下调的SnRK1靶点中,有5个,Zm评选β加,Zm评选βZIP11,ZmDPS,ZmFib2,ZmMDH,在培养过程中被抑制。然而,只有ZmAkinβ,ZmArg10,ZmMDH,Zm评选βZIP11在处理48小时时,饥饿的籽粒转录物与对照相比有显著差异。假设SnRK1靶基因的表达在饥饿48小时后以Tre6P独立的方式对培养基中添加蔗糖作出反应。这可以从成绩单上看出来ZmAkinβ,ZmArg10 ZmMDH,最显著的是ZmβZIP11.*这种Tre6P对糖的独立反应也可以在所有三个TPP基因中看到(ZmTPPA.3,ZmTPPA.1而且ZmTPPB.1.3).蔗糖恢复后(48-96 h),对照和饥饿处理之间无显著差异ZmDPS在96小时及ZmMol14SnRK1靶基因表达数据进一步证明了SnRK1通路对在体外内核饥饿。
蔗糖代谢关键基因;在液泡转化酶(ZmIVR2)、细胞壁转化酶(ZmINCW2)、蔗糖合酶(ZmSuSy1), AGPase结构域基因BRITTLE2(ZmBT2)和蔗糖转运蛋白(ZmSUT1,ZmSUT2,ZmSWEET1,ZmSWEET2)也评估了他们的表达。ZmIVR2当玉米粒放入培养中,基因表达减少,与推测下调的SnRK1靶基因类似。转录水平;然而,在前48小时内,饥饿籽粒的含量仍显著高于对照(图1)。6).这两个ZmINCW2和ZmSuSy1转录本在培养的前8小时诱导了对照和处理的核,反映出与II类核相同的模式TPS基因和推测上调的SnRK1靶基因。ZmBT2在培养的前8小时转录水平下降,在整个实验过程中,在缺乏蔗糖的籽粒中转录水平保持在较低水平。蔗糖转运蛋白的ZmSUT1而且ZmSWEET1显示饥饿的籽粒mRNA水平较高,接近显著水平(图。6).既不ZmSUT2也不ZmSWEET2对照与饥饿籽粒表达差异。三种糖转运蛋白(ZmSUT1,ZmSUT2,ZmSWEET1,ZmSWEET2)以观察未成熟玉米籽粒对饥饿胁迫的反应。的转录ZmSWEET1而且2糖转运体受收获期饥饿的影响;然而,与其他snrk1调控基因不同的是,转录在96小时内迅速恢复到初始水平。ZmSWEET1当玉米粒被放入培养液中时,mRNA被强烈诱导,但在转移到富含蔗糖的培养基中后,mRNA迅速恢复到初始水平。ZmSWEET2基因表达表现出相反的反应,饥饿时减少,恢复时增加。衰老指示基因ZmDIN6[27]在对照和缺乏蔗糖的籽粒之间没有显著差异。
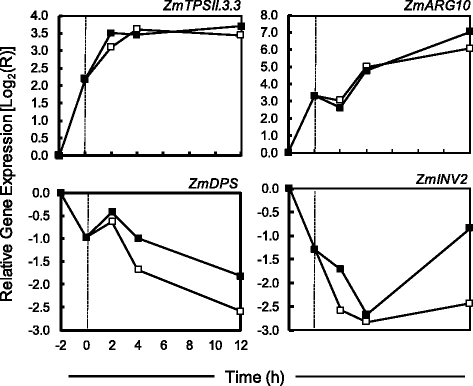
收割和灭菌3dap玉米籽粒的过程带来了不可避免的压力。从籽粒从穗上取下到在营养琼脂上镀膜需要2小时。在这2小时的窗口期内,包括对照在内的所有籽粒都有效地缺乏营养。观察到,切除和灭菌影响了许多参与糖感测、运输和代谢的基因的mRNA水平。这种“切除效应”与培养基中蔗糖的存在无关。为了更好地理解切除效果,我们进行了一个单独的实验,观察切除后最初几个小时内的基因表达(图。7).为了确定籽粒从穗上移除后转录水平的变化速度,我们在−2、0、2、4和12小时采样。−2小时的时间点反映了穗被从植株上移除的时刻,0小时的时间点是籽粒被放置在营养培养基上的时候。用RT-PCR对两个被切除诱导的基因(ZmTPSII.3.3而且ZmARG10)和两个切除抑制基因(ZmDPS而且ZmIVR2).研究发现,这些基因的转录水平在果仁切除、消毒和植盘的两个小时内改变了多达8倍(图1)。7).信使RNA水平继续增加或减少4小时后趋于平稳。3个DAP粒被分为3个周期。Duke和Doehlert [40]观察了5 DAP玉米籽粒中α-的mRNA水平玉米蛋白ß-玉米蛋白,Opaque-2,醛缩酶,Shrunken-1,蜡状,Shrunken-2,Brittle-2在培养0、5、10和15 d时。从0到5天,这些基因的转录都增加了,然后回到最初的水平(25°C)。尽管在他们的论文中没有讨论,但正如在这篇论文中观察到的,这种最初的转录增加可能是在收获期间造成的饥饿的结果。重要的是,对数据的解释要考虑到可能的伤害或切除影响。
讨论
饥饿对糖代谢和转运的影响
糖的吸收对维持籽粒发育至关重要,如果以任何方式中断,即在授粉前后施加干旱,则会导致籽粒流产[41].在这里介绍的工作中,我们选择使用在体外核培养系统(存在或不存在糖)作为一种模拟蔗糖供应中断的方法。然后我们测试了它如何影响糖和淀粉的代谢和糖的感知。在对照籽粒中,蔗糖含量增加而己糖含量只降低了三分之二。这说明在我们的实验体系中,培养基中提供的蔗糖被籽粒很好地吸收了。这也表明蔗糖和己糖的代谢处理是有限度的,并且这种代谢处理与蔗糖水解是平衡的。这与饥饿的籽粒形成对比,在饥饿的籽粒中,蔗糖和己糖都急剧减少,表明它们被分解代谢途径消耗以维持能量状态。这种观察到的代谢过程和转化酶活性之间的平衡已被证明是由激素和已糖信号在反馈调节回路中维持的[42].
在96小时的实验过程中,我们观察到对照和缺乏蔗糖的籽粒之间淀粉水平没有差异。一种可能的解释是淀粉合成在最初2小时的饥饿期中受到了不可逆的抑制。AGPase基因表达的迅速下降(ZmBt2)以及对照和饥饿籽粒中较低水平的淀粉合成中间体ADP-Glc都支持了这一解释。另一种解释是,早期发育的胚胎不在籽粒灌浆阶段,而大部分淀粉是在这个阶段合成的。43].有趣的是,观察到3-PGA水平升高。糖酵解中间体3-PGA,已知可变形活化AGPase(淀粉合成中的调节步骤),通常与淀粉生物合成中导致的高蔗糖利用率相关[44- - - - - -46].然而,在本研究中观察到的恰恰相反。淀粉积累不足,蔗糖水平降低,被抑制ZmBt2mRNA和低淀粉生物合成代谢产物,特别是专用中间体ADPGlc,都表明淀粉生物合成受到抑制。尽管3-PGA在蔗糖缺失的籽粒中含量很高,通常会变形活化AGPase,但AGPase在适应有效碳供应时也会被氧化还原活化[47),蔗糖饥饿最有可能是导致糖尿病的原因ZmBT2即使在3-PGA水平升高的情况下,基因在缺糖籽粒中也有较大程度的关闭。
全植物研究表明,干旱胁迫影响蔗糖代谢,与IVR2和INCW2酶活性及mRNA转录水平呈负相关[31,48,49].这些酶和Susy1一样,负责将蔗糖裂解成己糖,以便被籽粒吸收。在我们的实验中,我们观察到48小时的饥饿诱导了强烈的ZmIVR2成绩单,小幅下降ZmINCW2成绩单,并没有影响ZmSusy1记录。这表明类似于ZmSWEET1而且ZmSUT1,ZmIVR2可能受蔗糖可得性的调节,并在饥饿时诱导,以增加籽粒对糖的吸收。它还表明ZmIVR2可能有比ZmINCW2而且ZmSusy1在回应。这一假设与之前的研究结果相关联,研究表明蔗糖合酶(Susy)在发育后期的蔗糖分解代谢中比在发育早期更重要,因为大部分淀粉合成发生在发育后期[42,43,50].
SWEET转运蛋白是近年来发现的一类新的糖转运蛋白,可使蔗糖或己糖根据糖的浓度梯度在细胞膜上被动扩散。因此,它们被假设为缺失的转运蛋白,使异塑型蔗糖韧皮部卸载和沉质组织通过被动扩散吸收糖[49].然而,关于它们在不同植物组织和物种中的具体功能和定位知之甚少[51,52].与SWEET转运蛋白相反,蔗糖- h+转运体(SUT/SUC)在atp酶产生的质子梯度的驱动下,使蔗糖通过膜的主动转运成为可能(Carpaneto et al. 2005)。SUTs负责源组织中外质体韧皮部的装载,以及包括在籽粒灌浆过程中在内的糖向汇组织的主动吸收[53].这里我们展示的是这两种的转录水平ZmSWEET1而且ZmSUT1易于由切除和体外培养诱导,但也可由12至48小时的蔗糖饥饿诱导。这表明这些转运蛋白可能参与了籽粒对糖的吸收,并可能在转录水平上受到蔗糖有效性的调节。轻微的上升ZmSWEET1而且ZmSUT1饥饿条件下的转录本可能是核的一种补偿性反应,以输入更多的糖,使生存。Ayre审阅的证据[54表明一些蔗糖转运体,如ZmSUT1[55],可能能够根据特定植物组织的需要在导入和导出功能之间切换,允许源和汇组织的单独功能。这是由Aoki等人提出的。[56在非光合作用器官中,可能需要蔗糖转运蛋白向生长组织提供碳水化合物。基于这个假设,在饥饿的籽粒中观察到mRNA的升高ZmSUT1而且ZmSWEET1可能是组织特异性和重要的储备消耗,以提供代谢需要的植物经历蔗糖饥饿。考虑到本研究将发育中的核与其生理来源组织分离,且蔗糖转运蛋白通常是组织特异性的[56],对整个内核样本的分析将产生矛盾的结果也就不足为奇了,因为它同时测量了所有的成分。
Tre6P和海藻糖基因在饥饿反应中的作用
在海藻糖生物合成途径的背景下,结果与已知的该途径基本一致。Tre6P水平已被证明与蔗糖(和Suc6P)浓度高度相关[18,24,57- - - - - -60],并进一步证明抑制发育中的组织中的SnRK1活性[20.,26,27].亚达夫等人。[24和Lunn等人。[18]提出,在一定的条件下,Tre6P与蔗糖的比值保持恒定,因为Tre6P/蔗糖的关系控制着另一个Tre6P/蔗糖的关系,该关系调节着蔗糖的生产、利用和生长中重要的关键代谢过程。研究表明,Tre6P比其他任何一种糖都更接近蔗糖水平。他们还提出,对于特定的组织、发育阶段和环境条件,蔗糖- tre6p关系的敏感性是恒定的,但如果这三个因素中的任何一个发生变化,如施加的压力,蔗糖- tre6p关系的敏感性就会改变[25,57].在这里提供的数据中,蔗糖和Tre6P之间的相关性并不总是正确的。这可能是由于在时间零点到12小时时间点之间,组织的状态或阶段发生了变化。在玉米幼苗的遮荫胁迫中,蔗糖和Tre6P水平之间的类似相互作用已经被观察到[61]和成熟玉米植株的盐胁迫[39].基于Zhang等。[20.他发现在体外在核中发现的浓度下,SnRK1活性被Tre6P抑制,因此可以提出,这种Tre6P的大幅降低将激活对照和饥饿核中的SnRK1,可能是在切割和制备期间(2小时)。*在体外测试中,饥饿后的核具有更高水平的抑制Tre6P的SnRK1活性,这表明另一种机制可能也促进了饥饿切除核中的SnRK1活性。在玉米幼苗的遮荫胁迫中,蔗糖和Tre6P水平之间的类似相互作用已经被观察到[61]和成熟玉米植株的盐胁迫[39].这些发现为Tre6P的多种功能提供了越来越多的证据,并进一步揭示了我们对这种双糖知之甚少,以及进一步探索海藻糖通路的必要性。
本研究的结果与SnRK1靶基因的预期趋势基本一致。Zm评选β加是一个例外,最初被压抑;然而,到48小时,对照和饥饿籽粒之间没有差异。Tre6P与SnRK1靶基因表达的相关性提示Tre6P可抑制SnRK1活性。当Tre6P水平在蔗糖饥饿过程中下降时,与SnRK1下调基因呈正相关,与SnRK1上调基因呈负相关6:表S3)。之间的负相关TPSII类基因和Tre6P是Tre6P参与SnRK1调控的进一步证据,因为它被称为II类TPS基因也是SnRK1的靶标[27].
代谢产物的反应也支持饥饿激活SnRK1,以及海藻糖通路参与发育早期籽粒的碳水化合物代谢。蔗糖合成、淀粉和柠檬酸循环中间产物的减少表明代谢的开关与SnRK1的激活一致,如文献[62- - - - - -64].中间代谢物莽草酸酯通过其在芳香氨基酸合成中的作用成为生长指标。在蔗糖缺乏期间,石草酸盐的水平被耗尽。低石草酸盐可归因于通过抑制关键代谢调节蛋白(14-3-3蛋白)而导致生长停滞的一个指标[65].糖酵解中间体会在糖代谢和分解代谢过程中形成,它们的水平取决于形成速率和利用之间的关系。有趣的是,糖酵解中间产物在蔗糖喂养的籽粒和饥饿籽粒中都很高,并保持相对较高的水平,进一步增加蔗糖的再供给。这与有机酸和莽草酸保持在较低水平形成对比,表明在实验期间饥饿的籽粒的代谢状况继续处于生长停滞状态。也许如果给更多的时间恢复代谢物会回到控制值。另一种解释是,核已开始沿着一条不可逆转的道路走向流产[8,66并且无法恢复。
在饥饿期间,唯一表现出显著增加水平的中间体是3-PGA。此前已有研究表明,在长期遮荫诱导的饥饿中,玉米叶片中的3-PGA水平下降[57,61].当拟南芥幼苗遭受蔗糖饥饿,然后在恢复期喂蔗糖时,幼苗在恢复期的前3天内3- pga水平下降,然后升高[66].他们的研究还显示,蔗糖、己糖、磷酸糖和三磷酸腺苷的含量迅速增加。这一观察结果与核的恢复阶段是一致的。3.).3-PGA在糖酵解和卡尔文循环中都很重要;然而,我们可以推测,未成熟核中的3-PGA大部分来自糖酵解。在糖酵解过程中,3-PGA是己糖氧化为丙酮酸的重要中间体,可用于呼吸作用或生物合成[67].PEP的积累表明丙酮酸激酶和PEP羧化酶对这种代谢物的消耗受到了限制。PEP羧化酶活性低可能是由于被切除的籽粒中Tre6P水平低,考虑到高Tre6P导致该酶的激活[68].通过可逆的烯醇化酶和磷酸甘油酸突变酶反应,PEP的积累也有望导致3-PGA的类似积累,这是PEP和3-PGA在被切除的籽粒中平行增加的原因。
3-PGA的积累可能表明糖酵解中限制的位置可能是碳有效度被抑制导致磷酸甘油酸变化酶活性降低的结果。然而,更可能的解释是,升高的3-PGA浓度可以归因于植物组织中其他来源的甘油可用性的变化。来自线粒体和过氧化物酶体的丝氨酸的分解代谢转化可能是甘油的来源,这会导致蔗糖缺失的籽粒中3-PGA浓度更高[68].
的角色TPS应激反应中的基因家族
在植物中,海藻糖的浓度太低,不能作为一种有效的渗透保护剂;然而,海藻糖通路已被证明在植物中是必不可少的,特别是在有关的活动TPS类基因。I类TPS (TPS1)已被证实在TPS缺乏的酵母突变体中通过互补具有酶活性[69- - - - - -71],并敲出AtTPS1基因在胚胎发育和营养生长中起着至关重要的作用,大量的II类TPSs无法弥补TPS1的缺失[72,73].在我们的实验中,玉米的转录ZmTPSI.1.1在3个DAP的籽粒中发现对蔗糖饥饿无反应。这与我们之前的发现是一致的ZmTPSI.1.13 DAP籽粒对盐胁迫无响应[39].在拟南芥的根和叶组织中也有类似的观察AtTPS1基因表达对干旱、盐、冷、伤和热等广泛的非生物胁迫没有反应[74].这表明,尽管TPS1基因对海藻糖代谢至关重要,但其表达在转录水平上不受调控。考虑到TPS1基因在大多数组织中是组成性转录的,催化活性TPS可能通过翻译后修饰或调控配体的结合进行调控[75,76].
迄今为止,II类TPS蛋白的功能仍不清楚。如前所述,它们不能重复补充酵母TPS1突变,而且到目前为止还没有被证明具有这种功能在体外酶活性(71].不论其功能的不确定性,II类TPSs表现出严格的发育和组织特异性基因调控,强烈的日调节,以及对多种非生物应激的敏感性[39,74,77].玉米ZmTPSII.3.3基因与爆米花籽粒膨大性状相关[78].拟南芥中II类TPS蛋白5、6和7被发现为磷蛋白,在Ser22和Thr49位点磷酸化时与14-3-3蛋白结合[76].不像ZmTPSI.1.1,全部为二类玉米TPS我们所跟踪的基因在核培养的前8小时内在转录水平上被诱导,无论处理如何。二类TPS基因的表现与胁迫诱导的假定SnRK1响应基因在最初2小时饥饿时的表现相似,这表明SnRK1在玉米II类基因的调控中起作用,如之前在拟南芥中所述[64].
Tre6P减弱应激反应
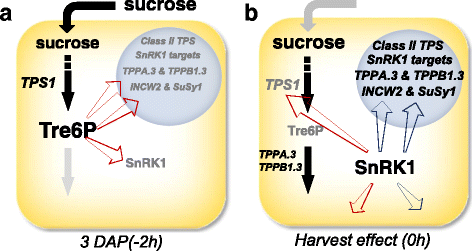
所有的样品在从植株上取下穗子(经过切割和籽粒表面杀菌)到上培养液之间有两个小时的饥饿期。尽管组织碳水化合物储备在这两个小时的饥饿胁迫中没有完全耗尽,但这足以刺激观察到对基因表达的显著影响,特别是对假定的SnRK1靶基因的影响(图1)。8).在整个实验过程中(96小时),无论培养基中是否提供蔗糖,这种对转录水平的影响对大多数基因都是保持不变的,这可能是因为在54 nmol∙g FW的3dap核中,通常减弱SnRK1活性和饥饿响应基因表达的Tre6P从基础水平下降−1小于1 nmol∙g FW−1.尽管从穗轴上切除核后不到12小时,SnRK1靶基因表达发生了显著变化,但总表达和抑制tre6p的表达均无显著变化在体外SnRK1活性为对照核。核切除后SnRK1活性的激活可能是Tre6P水平急剧下降的结果,而不是由于SnRK1蛋白水平的变化。其实总在体外SnRK1的活性在饥饿12小时后显著下降,即使SnRK1仍在继续影响在活的有机体内基因表达;尽管如此,在体外抑制tre6p的SnRK1活性在蔗糖缺乏的籽粒中显著高于对照籽粒(>2倍)。在许多方面,玉米籽粒所受的饥饿胁迫与成熟的小麦籽粒所受的饥饿胁迫相似。58].Tre6P水平急剧下降,SnRK1去抑制,推测的SnRK1靶基因表达,在泛太平洋伙伴关系和类二世TPS观察基因表达。
在饥饿玉米籽粒中观察到的Tre6P水平的下降很可能是因为众多海藻糖磷酸酶之一的激活。所有的十个泛太平洋伙伴关系通过酵母突变体的互补,证实了来自拟南芥的s具有酶活性[17].此外,一种拟南芥叶绿体相关的氧化还原敏感性TPP (AtTPPD)被发现对胁迫耐受性有积极影响[79].盐没有影响泛太平洋伙伴关系基因在3dap玉米籽粒中的表达39].玉米TPP RAMOSA 3基因(ZmTPPB.2.1)被怀疑在顶端分生组织生长和花序发育中起作用[80].RAMOSA 3与玉米的分枝有关,什么时候RAMOSA 3玉米基因组被敲掉,结果往往是不寻常的分支[81].每一个泛太平洋伙伴关系基因对饥饿胁迫的反应不同,可能表明这些基因在组织样本中发现的特定细胞类型中具有不同的功能[61].这是观察到的;然而,饥饿导致了一个大的诱导转录ZmTPPA.3基因。最近,一种大米的同类ZmTPPA.3(OsTPP1)在玉米花梗组织中异位过表达[33].这导致穗小穗(授粉前5天)的Tre6P水平从48到18 nmol∙g FW下降−1蔗糖水平从35 μmol∙g增加到50 μmol∙g−1FW,以及抗旱性的提高。有趣的是,蛋白质编码序列ZmTPPA.3被用来预测其亚细胞定位(Wolf PSORT, Plant-mPLoc和CropPlan),这表明酶很有可能定位于叶绿体(数据未显示)。在光照条件下生长的拟南芥叶片中,Tre6P主要存在于细胞质中,少量存在于叶绿体中[82].这表明Tre6P可能在亚细胞间区之间移动。这与Tre6P转运体系统一致,类似于体内的Glc6P转运体大肠杆菌[83,84和人类的[85].目前尚不清楚TPP是否被翻译后激活。
结论
3 DAP玉米籽粒在富蔗糖培养基上恢复2天后,饥饿48 h对籽粒的影响仍然存在。在田间,这相当于一场降雨无法扭转干旱引起的籽粒流产。未来的工作将检查玉米自交系的遗传变异与籽粒从饥饿中恢复能力的关系。
籽粒切除引起籽粒Tre6P下降50倍,即使在富含蔗糖的培养基上96小时也无法恢复。去除抑制SnRK1活性的Tre6P会导致几个推测的SnRK1靶基因的转录,对代谢物水平的分析揭示了从生物合成到分解代谢的代谢转变。这一观察结果表明了玉米自交系B73对干旱诱导的核败育的敏感性,并强调了Tre6P在饥饿代谢反应中的重要性。我们可以推测,在未成熟的种子中看到极高水平的Tre6P是抑制SnRK1活性所必需的,进一步推测,核败育的途径可能从Tre6P的急剧下降开始,并由此引发SnRK1的激活。
Tre6P的下降与转录的大量增加相对应ZmTPPA.3这表明该特异性酶可能负责Tre6P的去磷酸化,因此是玉米和其他谷物抗旱性遗传和生物技术改进的潜在靶点。
方法
玉米籽粒离体培养
该方法是由[的程序改进而来的。34,35,37,86)(附加文件7:图S4)。为了观察环境条件对籽粒代谢的影响,验证籽粒在培养中继续正常生长发育,并确定该方法作为干旱胁迫替代品的有效性,进行了代谢和基因表达研究。连续两年,玉米自交系B73在相同间距的重复地块上种植,周围有边界,以考虑到平等的竞争和荫蔽。玉米自交系B73于2012年和2013年在重复田块上种植,每周浇水两次,以保持土壤有效含水量在50%以上。2012年和2013年的生长季节明显不同4:表S2)。2012年的生长季被认为是干旱的一年,与所有三年相比,它见证了最高的温度和生长度(GDD)。2012年5月和7月是最热的日子,平均高温分别比20年平均值高15%和11%,gdd分别比20年平均值高28%和17%。此外,2012年的降雨量是最低的,比平均值低54%。2013年的生长季较为温和,温度与平均值相比在4%以内,GDD在7%以内。2013年的降水量比平均水平低16%。每一块地重复种植三次,每一次间隔一周,以确保能够获得足够的花粉。植物每周通过洒水器浇水两次,以减少压力,并确保土壤中有效含水量保持在50%的阈值以上。用芽袋盖住新生的嫩枝,以确保不发生授粉,并用B73花粉对耳朵进行人工授粉。授粉后3天,从最中心位置的4个随机排中每一排收获籽粒,以确保有效的土壤养分和遮阳效果的平等竞争。 Ears were harvested, kept cool and hydrated in a beaker filled with water until preparation was complete (<2 h). Kernels were prepared by hand excision of the center one-third of the ear, and removal of kernels and a small portion of cob tissue. Sufficient cob tissue (cob to kernel ratio of 6:1) was required to permit nutrients to be taken up by the immature kernel [86].将未成熟的籽粒进行灭菌,然后在正方形的培养皿中,在等距的富蔗糖(150 mM蔗糖,1% MS琼脂)或缺乏蔗糖的培养基(1% MS琼脂)中生长,以确保在实验期间,发育中的籽粒之间没有不平等的竞争[34,35,87].胚胎在24°C暗处保存48 h,然后转移到有蔗糖的平板上再保存48 h。每8-12小时取出重复样本,称重后立即在液氮中冷冻2.
碳水化合物和代谢物分析
为了评估蔗糖饥饿的影响,取下的籽粒在无碳源的MS培养基上培养48小时,然后在富蔗糖培养基上恢复48小时。在连续蔗糖培养基上培养96小时的籽粒作为对照处理。冷冻组织(20-100 mg)用组织裂解剂II (Qiagen)研磨成细粉(30-60s)。以乳糖作为内标提取蔗糖、果糖和葡萄糖[18].从提取可溶性糖过程中产生的颗粒中提取淀粉,用淀粉酶水解产生葡萄糖。所有样品采用高压毛细管离子色谱系统(ICS-5000, PA-20柱;ThermoFisher Dionex)使用1 μl注射量和45 mM KOH洗脱液。通过与已知糖的比较确定糖峰,并使用先前描述的核和穗轴L/G比为1/100的公式分析数据[61].T6P和其他磷酸化代谢物通过阴离子交换液相色谱串联质谱法定量[68].
体外SnRK1活性
果仁组织(200毫克)用研钵和杵碾碎,在N液体下2.可溶性蛋白提取于600 μL冰冷匀浆缓冲液(100 mM Tricine-NaOH, pH 8.0, 25 mM NaF, 5 mM二硫苏糖醇,2 mM焦磷酸四钠,0.5 mM EDTA, 0.5 mM EGTA, 1 mM苯甲脒,1 mM苯甲基磺酰氟,1 mM蛋白酶抑制剂鸡尾酒(Sigma P9599),磷酸酶抑制剂(PhosStop;罗氏)和不溶性聚乙烯吡咯烷酮至2% (w/v).匀浆离心(13000 g, 4℃),上清液(250 μL)在用匀浆缓冲液预平衡的Illustra NAP-5柱(GE Healthcare)上脱盐。SnRK1活性的测定如所述[20.].重复样品接受Tre6P至最终浓度为1 mM,以确定Tre6P抑制体外SnRK1活性的百分比。
qRT-PCR分析信使RNA
从玉米组织中分离RNA并进行qRT-PCR,如[61].5 μL cDNA(1/100稀释),最终体积为25 μL,用ZmEF1-1 α引物(适用于:AGA CTC ACA TCA ACA TTG TGG TCA T, Rev.: GTT GTC ACC TTC AAA ACC AGA GAT T)围绕内含子区域设计,采用供应商推荐的GoTaq®DNA聚合酶(Promega, USA),用半定量PCR检测RT质量和基因组DNA污染。对于每个时间点和生物复制,qRT-PCR反应重复3次。试验设3个生物重复。8个内参基因中有3个[39]选择基因表达规范化使用Genorm软件[88].相对基因表达量计算采用[89].采用Pfaffl等人描述的方法确定底漆效率。[90].
缩写
- 3-PGA:
-
3-phosphoglyceraldehyde
- ADP-Glc:
-
二磷酸腺嘌呤葡萄糖苷
- ASI:
-
开花吐丝间隔
- DAA:
-
几天后开花
- 衣冠楚楚的:
-
几天后授粉
- 出口押汇:
-
果糖酮糖
- Fru:
-
果糖
- Fru6P:
-
Fructose-6-phosphate
- GDD:
-
度增长天
- 相关:
-
葡萄糖
- Glc1P:
-
Glucose-1-phosphate
- Glc6P:
-
Glucose-6-phosphate
- Gly3P:
-
Glyceraldehyde-3-phosphate
- HPIC:
-
高压离子色谱法
- HPIC:
-
高压离子色谱法
- SnRK1:
-
蔗糖非发酵相关蛋白激酶1
- 泛太平洋伙伴关系:
-
海藻糖磷酸磷酸酶
- TPS:
-
海藻糖磷酸合酶
- 混乱关系:
-
海藻糖酶
- Tre6P:
-
Trehalose-6-phosphate
- UDPG:
-
尿苷二磷酸葡萄糖
参考文献
Westgate ME, Boyer JS。玉米1号叶片水势低时碳水化合物储备与繁殖发育。作物科学。1985;25:762。
Westgate ME, Boyer JS。玉米1号的低水势繁殖和花粉水势。作物科学。1986;26:951。
Otegui ME, Andrade FH, Suero EE。施丝期干旱玉米的生长、水分利用和籽粒败育。田间作物号1995;40:87-94。
Khorasani S, Mostafavi K, Heidarian A.玉米反应(玉米L.)杂交种和自交系在田间条件下对盐胁迫的抗性。应用科学。2011;2:1-7。
Hiyane R, Hiyane S, Tang AC, Boyer JS。饲喂蔗糖逆转了玉米因荫蔽而导致的籽粒损失。安机器人。2010;106:395 - 403。
McLaughlin JE, Boyer JS。在低水势条件下,玉米籽粒数减少时,葡萄糖在玉米子房中的定位。安机器人。2004;94:75 - 86。
博伊尔MG,博伊尔JS,摩根PW。液体培养基茎部灌注防止玉米低水势繁殖失败。作物科学。1991;31:1246-57。
McLaughlin JE, Boyer JS。低水势下败育玉米子房的糖响应基因表达、转化酶活性和衰老。安机器人。2004;94:675 - 89。
Elbein AD, Pan YT, Pastuszak I, Carroll D.海藻糖的新认识:一种多功能分子。糖生物学。2003;13:17R-27R。
克劳JH,胡克斯特拉FA,克劳LM。低湿休眠。物理学报1992;54:579-99。
桦树GG,海藻糖。碳水化合物化学快报1963;18:201。
Crowe JH。海藻糖作为“化学伴侣”:事实和幻想。中华医学杂志2007;594:143-58。
Brodmann A, Schuller A, Ludwig-Müller J, Aeschbacher RA, Wiemken A, Boller T, Wingler A.海藻糖产生病原菌对拟南芥海藻糖酶的诱导作用Plasmodiophora brassicae.植物-微生物相互作用。2002;15:693-700。
Avonce N, Mendoza-Vargas A, Morett E, Iturriaga G.海藻糖生物合成演化的见解。生物学报。2006;6:109-24。
张燕,张晓燕,张晓燕。海藻糖代谢与信号转导。植物生物学,2008;59:417-41。
Gómez d . S .鲍德,A.吉尔戴,Li Y, IA.格雷厄姆。拟南芥海藻糖-6-磷酸合成酶1突变体胚胎发育延迟与细胞壁结构改变、细胞分裂和淀粉积累减少有关。植物j . 2006; 46:69 - 84。
Vandesteene L, López-Galvis L, Vanneste K, Feil R, Maere S, Lammens W, Rolland F, Lunn JE, Avonce N, Beeckman T, Van Dijck P.拟南芥海藻糖-6-磷酸磷酸酶基因家族的扩展进化。植物杂志。2012;160:884 - 96。
Lunn JE, Feil R, Hendriks JHM, Gibon Y, Morcuende R, Osuna D, Scheible W-R, Carillo P, Hajirezaei M-R, Stitt M.糖诱导的海藻糖6-磷酸增加与adp葡萄糖焦磷酸化酶的氧化还原激活和淀粉合成的更高速率有关拟南芥.j . 2006; 397:139-48。
海藻糖6-磷酸。植物生物学杂志2007;10:303-9。
张Y,普里马维西LF,朱里亚D,安德拉洛jc PJ,米切尔RAC,鲍尔斯SJ,施吕普曼H,德拉特T,温勒A,保罗MJ。海藻糖-6-磷酸对snf1相关蛋白激酶1活性的抑制及代谢途径的调控植物杂志。2009;149:1860 - 71。
张晓燕,张晓燕,张晓燕,等。海藻糖-6-磷酸:植物代谢与发育的关系。植物科学,2011;2:70。
Wingler A, Delatte TL, O 'Hara LE, Primavesi LF, Jhurreea D, Paul MJ, Schluepmann H.海藻糖6-磷酸是与高碳利用率相关的叶片衰老发生的必要条件。植物杂志。2012;158:1241-51。
Wahl V, Ponnu J, Schlereth A, Arrivault S, Langenecker T, Franke A, Feil R, Lunn JE, Stitt M, Schmid M.海藻糖-6-磷酸信号通路对植物开花的调控作用拟南芥.科学。2013;339:704-7。
亚达夫UP, Ivakov A, Feil R, Duan GY, Walther D, Giavalisco P, Piques M, Carillo P, Hubberten H-M, Stitt M, Lunn JE。蔗糖-海藻糖6-磷酸(Tre6P)连接:Tre6P对蔗糖信号的特异性和机制。J Exp Bot。2014;65:1051-68。
Figueroa CM, Lunn JE。一个关于两种糖的故事——海藻糖6-磷酸和蔗糖。植物杂志。2016;172(9月):7-27。
Paul MJ, Jhurreea D, Zhang Y, Primavesi LF, Delatte T, Schluepmann H, Wingler A.海藻糖与生长相关的生物合成过程的上调。植物信号行为学报2010;5:386-92。
Baena-González E,罗兰,张文华,张文华,等。植物胁迫和能量信号转导转录网络的中心集成器。大自然。2007;448:938-42。
海藻糖生物合成在植物中的作用。足底。2002;60:437-40。
李文华,李文华,李文华,等。植物海藻糖代谢的研究进展。植物j . 2014; 49:544 - 67。
Holmström K, Mäntylä E,韦林B,曼达尔a。烟草的抗旱性。大自然。1996;379:683-4。
Garg AK, Kim J-K, Owens TG, Ranwala AP, Choi YD, Kochian LV, Wu RJ。海藻糖在水稻植株中的积累使其对不同的非生物胁迫具有较高的耐受性。中国科学院学报2002;99:15898-903。
Karim S, Aronsson H, Ericson H, Pirhonen M, Leyman B, Welin B, Mäntylä E, Palva ET, Van Dijck P, Holmström K-O。在生产海藻糖的转基因植物中提高了耐旱性而不产生不良副作用。植物分子生物学杂志2007;64:371-86。
Nuccio ML, Wu J, Mowers R,周宏平,Meghji M, Primavesi LF, Paul MJ,陈x,高原,Haque E, Basu SS, Lagrimini LM。在水分充足和干旱条件下,玉米穗中海藻糖-6-磷酸磷酸酶的表达可提高产量。2015;(2014年10月):1-13。
汉福特JM,琼斯RJ。玉米籽粒败育:一、体外诱导败育的玉米籽粒碳水化合物浓度格局及酸性转化酶活性。植物杂志。1986;81:503-10。
Glawischnig E, Tomas A, Eisenreich W, Spiteller P, Bacher A, Gierl A.玉米籽粒生长素的生物合成。植物杂志。2000;123:1109-19。
Hole DJ, Smith JD, Cobb BG。利用脱落酸调控玉米籽粒及相关穗轴组织的胚休眠玉米L.体外培养。植物杂志。1989;91:101-5。
单GW,低于FE。不同碳氮供给条件下体外培养玉米籽粒的生长与组成。植物杂志。1989;89:341-6。
Gengenbach BG。体外授粉玉米颖果的发育。足底。1977;134:91-3。
亨利C,布莱德索SW,格里菲斯CA,科尔曼A,保罗MJ,萨克S,拉格里米尼LM。盐胁迫玉米海藻糖代谢的差异作用。植物杂志。2015;169:1072 - 89。
Duke ER, Doehlert DC。热胁迫对培养发育玉米籽粒酶活性和转录物水平的影响。环境实验机器人。1996;36:199-208。
辛塞尔梅尔C,劳尔M,博伊尔j。扭转干旱引起的粮食产量损失:蔗糖维持玉米胚胎生长。作物科学。1995;35:1390-9。
蔗糖代谢:调控机制和在糖感测和植物发育中的关键作用。植物生物学杂志2004;7:235-46。
早期核发育的激素调节。在:M. Westgate, K. Boote,编辑,玉米的生理和建模内核集,CSSA规范,出版29。CSSA和ASA,麦迪逊,2000年。25-42页。doi:10.2135 / cssaspecpub29.c3.
Stark DM, Timmerman KP, Barry GF, Preiss J, Kishore GM. ADP葡萄糖焦磷酸化酶对植物组织中淀粉量的调控。科学。1992;258:287 - 92。
光合产物分配的对照分析:adp -葡萄糖焦磷酸化酶或质体磷酸葡萄糖酵解酶活性降低对淀粉和蔗糖通量的影响拟南芥(l)Heynh。足底。1990;182:445-54。
淀粉生物合成和降解的调控。植物杂志。1982;33:431-54。
Zeeman SC, Smith S, Smith A.叶片淀粉的日代谢。j . 2007; 401:13-28。
可溶性转化酶的表达是干旱胁迫在玉米幼体卵巢发育的关键、流产敏感期的早期靶点。植物杂志。2002;130:591 - 604。
淀粉与低水势下玉米籽粒数的控制。植物杂志。1999;121:25-36。
Zinselmeier C, Westgate ME, Schussler JR, Jones RJ。低水势破坏玉米碳水化合物代谢(玉米l .)卵巢。植物杂志。1995;107:385 - 91。
陈L-Q。韧皮部运输和病原体营养的甜糖转运蛋白。新植醇。2014;201:1150-5。
陈丽强,曲晓强,侯伯华,Sosso D, Osorio S, Fernie AR, Frommer WB。SWEET蛋白介导的蔗糖外排是韧皮部转运的关键步骤。科学。2012;335:207-11。
Slewinski TL, Garg A, Johal GS, Braun DM.玉米SUT1在韧皮部加载中的作用。植物信号与行为学报2010;5(6):687-90。
艾尔BG。蔗糖的膜运输系统与整株植物碳分配的关系。摩尔。2011;4:377 - 94。
Carpaneto A, Geiger D, Bamberg E, Sauer N, Fromm J, Hedrich R.在蔗糖梯度和质子动力的控制下,皮素定位的质子耦合蔗糖载体ZmSUT1介导蔗糖外流。生物化学杂志2005;280:21437-43。
青木N,广濑T,高桥S,小野K,石丸K,大杉R.玉米蔗糖转运蛋白基因的克隆与表达分析(英文)玉米l .)。植物细胞物理学报1999;40:1072-8。
Czedik-Eysenberg AB, Arrivault S, Lohse MA, Feil R, Krohn N, Encke B, Nunes-Nesi A, Fernie AR, Lunn JE, Sulpice R, Stitt M.玉米生长过程中不同区域碳有效性与生长的相互作用植物杂志。2016;172:943 - 67。
Martínez-Barajas E, Delatte T, Schluepmann H, de Jong GJ, Somsen GW, Nunes C, Primavesi LF, Coello P, Mitchell RA, Paul MJ。小麦籽粒发育的特征是海藻糖6-磷酸的显著积累:组织分布及其与snf1相关蛋白激酶1活性的关系。植物杂志。2011;156:373 - 81。
Schluepmann H, van Dijken A, Aghdasi M, Wobbes B, Paul MJ, Smeekens SC.海藻糖介导的拟南芥幼苗生长抑制是由于海藻糖-6-磷酸盐的积累。植物理疗。2004;135:879 - 90。
Delatte TL, Sedijani P, Kondou Y, Matsui M, de Jong GJ, Somsen GW, Wiese-Klinkenberg A, Primavesi LF, Paul MJ, Schluepmann H.海藻糖-6-磷酸盐抑制生长:SnRK1信号通路控制初级代谢物生长的一个令人意外的案例。植物杂志。2011;157:160 - 74。
Henry C, Bledsoe SW, Siekman A, Kollman A, Waters BM, Feil R, Stitt M, Lagrimini LM。玉米海藻糖途径:对昼夜循环和延长黑暗的保护和基因调控。J Exp Bot 2014; 65:5959-73。
Schluepmann H, Berke L, Sanchez-Perez GF。代谢对生长的控制:海藻糖-6-磷酸盐在植物中的一个例子。J Exp Bot 2011; 63:3379-90。
Delatte TL, Selman MHJ, Schluepmann H, Somsen GW, Smeekens SCM, de Jong GJ。连续萃取-阴离子交换色谱-质谱联用法测定拟南芥幼苗中的海藻糖-6-磷酸盐。学生物化学肛门。2009;389:12-7。
Baena-González E.应激期间基因表达调节中的能量信号。摩尔。2010;3:300-13。
Diaz C, Kusano M, Sulpice R, Araki M, Redestig H, Saito K, Stitt M, Shin R.拟南芥14-3-3蛋白在中枢代谢过程中的新功能。生物医学学报,2011;5:192。
Lauxmann MA, Annunziata MG, Brunoud G, Wahl V, Koczut A, Burgos A, Olas JJ, Maximova E, Abel C, Schlereth A, Soja AM, Bläsing OE, Lunn JE, Vernoux T, Stitt m生殖失败拟南芥在短暂的碳水化合物限制下:花和非常年轻的角果被丢弃,分生组织被保留以允许成功恢复生殖生长。植物细胞环境学报2016;39:745-67。
Plaxton WC。植物糖酵解的组织与调控。植物物理学报1996;47:185-214。
Figueroa CM, Feil R, Ishihara I, Watanabe M, Kölling K, Krause U, Höhne M, Encke B, Plaxton WC, Zeeman SC, Li Z, Schulze WX, Hoefgen R, Stitt M, Lunn JE。海藻糖6 -磷酸盐协调有机和氨基酸代谢与碳利用率。植物j . 2016; 85:410-23。
蒋伟,付福林,张淑珍,吴林,李文春。玉米海藻糖-6-磷酸合酶功能基因的克隆与鉴定。植物生物学杂志2010;53:134-41。
黄文华,张文华,张文华,等。海藻糖-6-磷酸磷酸酶来源:海藻糖-6-磷酸酶拟南芥:通过酵母tps2突变体的功能互补鉴定。植物细胞生物学杂志1998;13:673-83。
臧斌,李宏,李伟,邓晓伟,王旭。海藻糖-6-磷酸合酶(TPS)基因家族分析提示水稻TPS复合物的形成。植物分子生物学,2011;76:507-22。
van Dijken AJH, Schluepmann H, Smeekens SCM。拟南芥海藻糖-6-磷酸合酶1是正常营养生长和向开花过渡所必需的。植物杂志。2004;135:969 - 77。
Gómez LD, Gilday A, Feil R, Lunn JE, Graham IA。attps1介导的海藻糖6-磷酸的合成对于胚胎发育和营养生长以及萌发种子和气孔保护细胞对ABA的响应是必不可少的。植物j . 2010; 64:1-13。
张晓燕,张晓燕。非生物胁迫下海藻糖生物合成的研究。植物生物学杂志,2008;50:1223-9。
海藻糖-6-磷酸合酶基因家族的差异多位点磷酸化拟南芥:一种基于质谱的多平行肽库磷酸化分析过程。分子细胞蛋白质组学。2005;4:1614-25。
Harthill JE, Meek SEM, Morrice N, Peggie MW, Borch J, Wong BHC, Mackintosh C.拟南芥海藻糖-磷酸合酶5对2-脱氧葡萄糖响应的磷酸化和14-3-3结合。植物j . 2006; 47:211-23。
Ramon M, De Smet I, Vandesteene L, Naudts M, Leyman B, Van Dijck P, Rolland F, Beeckman T, Thevelein JM。II类海藻糖代谢蛋白广泛表达调控和缺乏异源酶活性拟南芥.植物细胞环境学报2009;32:1015-32。
Paes GP, Viana JMS, Silva FFE, Mundim GB。玉米品质性状qtl所在染色体区域的连锁不平衡、SNP频率变化及关联映射。中华生物学报2016;39:97-110。
郭志明,张志强,张志强,等。氧化还原敏感叶绿体海藻糖-6-磷酸磷酸酶AtTPPD调节盐胁迫耐受性。抗氧化氧化还原信号。2014;21:1-16。
一种海藻糖代谢酶控制玉米花序结构。大自然。2006;441:227-30。
分支:蔓生途径和草花序形态的演化。植物细胞。2006;18:518-22。
马丁斯MCM,赫贾兹M,费特克J,斯特鲁普M,菲尔R,克劳斯U,阿里沃奇S,沃斯洛D,菲格罗亚CM,伊瓦科夫A,亚达夫UP,皮克斯M,梅茨纳D,斯蒂特M,伦恩JE。海藻糖6-磷酸对拟南芥叶片淀粉降解的反馈抑制植物杂志。2013;163:1142 - 63。
Lloyd AD, Kadner RJ。的拓扑结构大肠杆菌用TnphoA融合分析uhpT糖-磷酸盐转运蛋白。J Bacteriol。1990;172:1688 - 93。
韦斯顿洛杉矶,卡德纳RJ。uhp基因在肿瘤表达中的作用大肠杆菌糖磷酸交通系统。J Bacteriol。1988;170:3375 - 83。
周济阳,曼斯菲尔德。糖-磷酸盐/磷酸盐交换器的SLC37系列,第1版。73卷。爱思唯尔有限公司;2014.
Felker FC。玉米芯组织参与离体培养玉米籽粒对培养基成分的吸收。植物生理学报,1992;139:647-52。
穆希什·乔丹,粉碎RG。玉米泛素(ubiin -1)启动子在玉米发育过程中的调控玉米L.)种子在离体生长的籽粒中瞬时基因表达检测。植物细胞学报1998;17:476-81。
Vandesompele J, De Preter K, Pattyn F, Poppe B, Van Roy N, De Paepe A, Speleman F通过多个内控基因的几何平均实现实时定量RT-PCR数据的精确归一化。基因组医学杂志。2002;3:research0034.1-research0034.11。
Hellemans J, Mortier G, De Paepe A, Speleman F, Vandesompele J. qBase相关定量框架和管理和自动分析实时定量PCR数据的软件。基因组医学杂志。2007;8:R19。
Pfaffl兆瓦。实时RT-PCR中相对定量的新数学模型。核酸条例2001;29:e45。
作者信息
从属关系
相应的作者
附加文件
附加文件1:图S1。
在长期培养(15 d)中,评估收获的3 DAP的果仁在不同浓度的蔗糖、葡萄糖和果糖上的生长情况。杀菌后,将果仁置于MS琼脂上,在24°黑暗中培养c .介质要么只含有MS盐,要么在MS盐中添加100,200或300mm的蔗糖,葡萄糖或果糖作为碳源。在培养第0天和第15天称量单个籽粒的重量。(XLSX 225 kb)
附加文件2:表S1。
研究了长期(9 d)蔗糖饥饿对籽粒生长的影响−1弗兰克-威廉姆斯)。灭菌后,将B73核置于MS琼脂上,24°C暗处培养。对照籽粒连续施蔗糖用SUC (150 mM)表示,缺蔗糖籽粒用NS(不施蔗糖)表示。每天分别从三个不同的穗子中取粒称量,然后再放回培养基中。(XLSX 11 kb)
附加文件3:图S2。
对DAP收获的籽粒进行了长期培养活力的试验。杀菌后,将果仁镀于MS琼脂上,24°C暗处培养。对照籽粒在连续蔗糖(150mm)上用封闭(黑色)方格表示,无蔗糖籽粒用白色(开放)方格表示。用4个生物重复(每个重复3个植物)绘制平均值。(XLSX 24 kb)
附加文件4:表S2。
大田种植玉米的生长条件。月和积温(°C),生长度天数(GDD)(基10°C)玉米),以及2012、2013和2014年生长季内布拉斯加大学-林肯校区地块的降水量(cm)。平均值是根据20年的平均值确定的。(XLSX 15 kb)
附加文件5:图S3。
蔗糖饥饿对在体外培养的果仁(3dap)。授粉后3天,从大田种植的玉米植株中取出玉米粒。杀菌后,将果仁镀于MS琼脂上,24°C暗处培养。对照籽粒在连续蔗糖(150mm)上用封闭(黑色)方格表示,无蔗糖籽粒用白色(开放)方格表示。阴影区域突出了48小时的饥饿期,而非阴影区域表示蔗糖恢复期。平均值使用4个生物重复计算,每个重复包含3个植物,其显著性由学生报告T-test在α = 0.05时。(XLSX 85 kb)
附加文件6:表S3。
Tre6P水平与基因表达之间相关系数的热图。用Pearson比较检验(n4)。正相关用深浅的蓝色表示,负相关用深浅的红色表示。(XLSX 11 kb)
附加文件7:图S4。
玉米内核的文化。通过手工切除3dap穗的中心三分之一(A),去除籽粒和一小部分穗轴组织(B),制备籽粒,保持足够的穗轴组织,以允许营养物质被未成熟的籽粒吸收。消毒和生长在不成熟籽粒蔗糖丰富(150毫米蔗糖、1%琼脂女士),或蔗糖缺乏媒体(1%琼脂女士)在培养皿上相等的间距,以确保有平等竞争营养物质(C),胚胎是保持在24°C在黑暗中48 h,然后转移到盘子与蔗糖48 h。复制样品中每一个8 - 12 h,内核被从穗轴组织(D & E),称重,并立即冻结在液体N2.(XLSX 310 kb)
权利和权限
开放获取本文根据创作共用署名4.0国际许可协议发布(http://creativecommons.org/licenses/by/4.0/),该协议允许在任何媒体上不受限制地使用、分发和复制,前提是您适当地注明原作者和来源,提供创作共用许可的链接,并说明是否有更改。创作共用公共领域奉献放弃书(http://creativecommons.org/publicdomain/zero/1.0/)除另有说明外,适用于本条提供的资料。
关于这篇文章
引用这篇文章
s.w.布莱德索,C·亨利,C·格里菲思et al。Tre6P和SnRK1在玉米早期核发育和胁迫致败核事件中的作用BMC植物杂志17日,74(2017)。https://doi.org/10.1186/s12870-017-1018-2
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12870-017-1018-2
关键字
- 玉米
- 内核的文化
- 干旱
- 饥饿
- 糖代谢
- trehalose-6-phosphate
- SnRK1