- 研究文章
- 开放获取
- 发布:
细胞色素P450单加氧酶CYP71AU87的功能特征表明其在药用植物中的marrubiin生物合成中发挥作用欧夏至草
BMC植物生物学体积19文章编号:114.(2019)
摘要
背景
苦薄荷(欧夏至草)是一种药用植物,其签名的生物活性化合物,marrubiin和相关呋喃二萜内酯,具有用于心血管疾病的治疗中具有潜在的应用和II型糖尿病。缺乏可扩展的植物栽培和复杂的代谢物轮廓M.大麦限制从植物生物量中提取marrubinin。对marrubinin生物合成酶的了解有助于开发用于marrubinin生产的代谢工程平台。我们之前鉴定了两个二萜合成酶,MvCPS1和MvELS,依次作用形成9,13-环氧-labd-14-烯。细胞色素P450单加氧酶(P450)对9,13-环氧-labd-14-烯的转化可以促进关键功能修饰反应形成marrubinin及相关化合物。
结果
挖掘一个M.大麦叶片转录组数据库鉴定了95个全长P450候选基因。选择P450候选人的克隆和功能分析显示高转录丰度显示CYP71家族的一员,CYP71AU87,催化羟基化的9日13-epoxy-labd-14-ene收益率两个异构产品,9日13-epoxy labd-14-ene-18-ol和9,13-epoxy labd-14-ene-19-ol,用气相色谱-质谱和核磁共振分析验证。额外的瞬态尼古利亚娜·宾夕法尼亚州CYP71AU87的共表达测定所建议的不同二萜合酶对那CYP71AU87是特定于所述顺序MvCPS1和Mv13-epoxy-labd-14-ene ELS产品9日。虽然P450产品没有检测到在足底,高水平的CYP71AU87marrubinin积累组织的基因表达支持marrubinin和相关二萜的形成M.大麦.
结论
在与二萜合酶对的顺序反应中MvCPS1和MvELS,CYP71au87形成异构产物9,13-环氧Labd-14-Ene-18/19-Ol在Marrubiin生物合成中的可能中间体。虽然其代谢相关性在足底将需要进一步的基因研究中,CYP71AU87催化活性的鉴定扩大了我们参与专业二萜类代谢植物P450酶的功能景观的知识,可以提供marrubiin及相关生物活性的天然产物的配方的资源。
背景
药用植物和它们的天然产品是丰富的,但没有得到充分利用,源现代疗法,从丰富的传统药物使用知识的茎[1那2].间形成在植物中的无数天然产物,二萜类化合物是超过12000种代谢产物[的一组不同的3.已被证明对药物发现有价值。例如紫杉树自然产生的化学治疗剂紫杉醇®(红豆杉) (4.那5.]中,精神克罗二萜类salvinorin A [6.那7.,甲丁酸ingenol大戟属植物治疗光化性角化症[8.那9.的camp调节器锦紫苏forskohlii[10那11那12].
本研究的重点是药用植物白茯苓(欧夏至草),一种薄荷科(唇形科)的成员,传统上被用来缓解皮肤和呼吸疾病。M.大麦提取物和代谢物已被证明具有治疗II型糖尿病和心血管疾病的潜力[13那14].抗糖尿病疗效M.大麦已归因于Marrubiin,一种呋喃醇二萜内酯代表签名代谢物M.大麦[15那16那17].在体外和体内研究表明,具有潜在的更高的功效高血糖条件下marrubiin刺激胰岛素分泌相比,建立抗糖尿病药物诸如二甲双胍[13那14].Marrubiin积累在M.大麦叶腺毛和花的含量达到每克鲜重4毫克[17].此外,植物化学分析M.大麦密切相关Marrubium种已经揭示了一套结构上相似的半日花烷二萜类化合物的是设有共同呋喃环和19,6内酯官能团[的15那16].这些功能上的修改已经吸引了近几年越来越多的关注[7.那16那18那19那20.],因为类似的呋喃和内酯基团与天然产物的生物活性有关,例如呋喃环对salvinorin A κ-阿片受体激动剂活性的贡献,或倍半萜内酯(如抗疟疾药物青蒿素)的疗效[21那22].
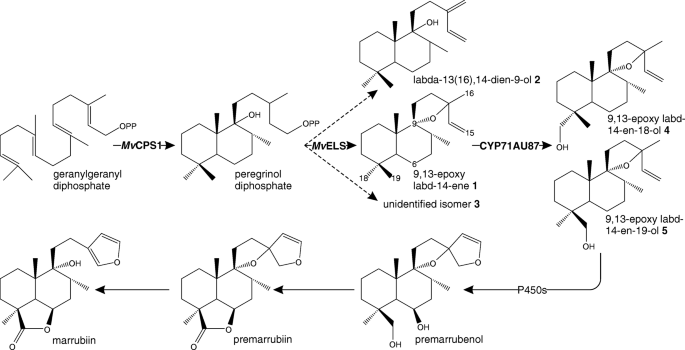
为了阐明在M.大麦,我们之前报道了萜类生物合成候选基因的鉴定M.大麦使用基于基于基于基于基于基于基于基因组的基因发现方法[16那23].一种功能双萜合成酶(diTPSs),指定为PEREGRINOL二磷酸合成酶(MvCPS1)和9,13-环氧- labd -14-烯合成酶(MvELS),被鉴定为在marrubinin生物合成中催化第一个承诺的反应[16].MvCPS1将中心二萜前体香叶基香叶基二磷酸(GGPP)转化为peregrinol二磷酸,这是一种双环戊基二磷酸中间体,具有C-9羟基,主要存在于marrubiin和相关代谢物中(图)。1).在一个由MvELS时,二磷酸基被电离,生成的碳正离子发生重排形成9,13-环氧-14-labd-ene [16].下游由大家族的细胞色素P450单加氧酶的成员催化该中间体,几个氧化反应的(色素P450),估计可能有利于二萜支架,得到marrubiin和结构上相似的生物活性二萜类化合物(图7的功能性的装饰。1).具体而言,羟基化或羧化在C-6和C-19将必须形成特性γ内酯环结构的潜力,羟基化C-16和/或C-15将有利于形成呋喃环的。
提出marrubiin-biosynthetic通路。MvCPS1和MvELS形成二萜合酶对,将中心前体香叶酰香叶酰二磷酸(GGPP)转化为9,13-环氧labd-14-烯1(可能还有其他密切相关的产品,包括labda-13(16),14-dien-9-ol2)通过戊基二磷酸中间体peregrinol二磷酸。假设细胞色素P450单加氧酶催化位置特异性功能修饰,可能通过CYP71AU87产物9,13-环氧labd-14-en-19-ol生成marrubiin5.以及其他途径的中间体,如之前在M.大麦组织。随后内酯生成形成marrubinin前,marrubinin通过酶促或自发开环产生C-9的自由羟基。虚线表示在共表达检测中鉴定的酶产物MvCPS1和MvELS在本研究中
在相关的唇形科物种,所述CYP71和P450的CYP76家庭超家族的成员已被证明在二萜类化合物的代谢位置特异性催化氧化反应[24那25那26那27那28].例如,来自CYP76AH1和CYP76AH4丹参和迷迭香(Rosmarinus officinalis.)催化松香三烯在C-11和/或C-12处氧化生成铁酚和下游丹参酮二萜[29那30.].类似地,CYP76AH24,CYP71BE52和CYP76AK6 / 8中,示出在C-12,C-2或C-20,分别以促进相关半日花烷支架的羟基化和羧化,[26那31].虽然植物色素P450直接参与二萜内酯的形成还没有被报道,在水稻(栽培稻)、CYP99A3和CYP76M8分别催化C-19羧化和C-6羟基化,是生物活性桃内酯二萜内酯环形成的先决条件[32那33].此外,有报道称p450参与呋喃环的形成,包括薄荷中的CYP71A32 (Mentha x piperita.)参与单萜Menthofuran的生物合成[34],以及来自Vitex Agnus-castus羟基化peregrinol在C-16潜在地连接在与结构相似二萜类化合物的生物合成,以marrubiin路线呋喃环闭合[18].
在本研究中,我们将建立的叶片转录组调查与系统发育和基因表达分析相结合,以鉴定CYP71家族成员,Mv1270(CYP71au87),作为Marrubiin生物合成中的功能的可能候选者。CYP71au87的共同表达MvCPS1和Mv船在尼古利亚娜·宾夕法尼亚州和酵母(酿酒酵母)导致的氧化MvELS产物,9,13-epoxy-labd-14-ene, C-18或C-19位,经GC-MS和NMR分析验证。虽然这些同分异构体二萜醇不能被识别在足底采用GC-MS和LC-MS分析,高表达CYP71AU87在聚丸红蛋白组织的转录本M.大麦支持marrubiin生物合成中可能发挥的作用。因此,CYP71AU87的发现对阐明和生产marrubiin的代谢途径工程及相关的天然产品提供了新的资源。
结果
P450基因与生物合成marrubiin可能发挥的作用的转录激活识别
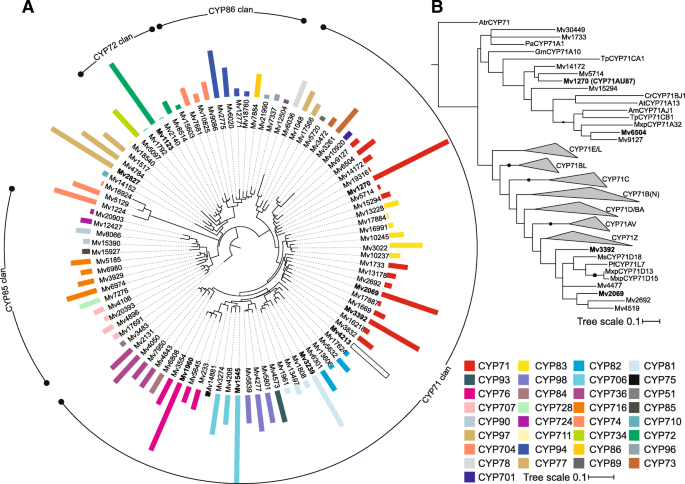
以往的研究表明,marrubiin和相关的二萜类代谢物在叶片和叶毛积累为主M.大麦[16那17].为了识别在marrubinin生物合成中可能具有功能的P450候选蛋白,我们挖掘了一个建立的M.大麦叶转录组(23]与p450特异性蛋白数据库(附加文件1数据文件S1)。Applying a minimal sequence length of 960 bp and anE.-Value截止≤1E.- 50,鉴定了总共95个候选基因与已知的P450酶有显着匹配的候选基因(附加文件2:表S1)。系统发育分析放置这些候选P450到P450 33个家庭与CYP71家族是最代表的(图的成员。2).通过映射获得的原料,以进一步分流高概率P450候选基因表达水平FPKM的基础上评估(片段每千碱基每百万映射转录的读操作)值读取针对组装M.大麦叶子转录组。CYP71成员的转录丰度最高(Mv1270年,Mv2069,Mv3392年,Mv4213),CYP72(Mv1123), CYP76 (Mv1960), CYP81 (Mv3239), CYP706 (Mv1545),和CYP97(Mv(图2827)家庭。2).由于CYP71和CYP76家族的成员已被证明功能在唇形科等植物种类[二萜类化合物代谢26那27那30.那31那35],Mv1270年,Mv3392和Mv追求功能研究4213。尽管广泛的努力,Mv2069和CYP76候选Mv1960年无法成功克隆,防止进一步分析。系统发育分析Mv1270,虽然远缘,成分支也包含CYP71家族的已知的萜类化合物代谢酶,如从薄荷呋喃合酶CYP71A32Mentha x piperita.[34] 和小白菊CYP71CA1和CYP71CB1涉及Costnolide生物合成[36(图。2).另一个降低丰富P450分配给CYP71家庭,Mv6504也位于该分支上,与CYP71A32具有相近的系统发育关系。由于其在呋喃环形成过程中可能具有相似的活性,因此选择其进行功能分析。Mv3392被置于不同的分支中,与CYP71D亚家族成员远亲,该亚家族在薄荷属植物中发挥单萜类生物合成的作用。此外,Mv1545被选为候选酶,因为它代表了所有鉴定的p450中最丰富的转录本,并被归属于CYP706家族,已知其在倍半萜类代谢中有活性[37那38].相似地,Mv4213选择用于进一步的研究中,由于其高转录物丰度和其他仅疏远关系M.大麦P450候选人(图。2).本研究没有进一步研究属于CYP72、CYP97和CYP81家族的剩余丰富的P450转录本,因为这些家族的成员更常见地在油菜素内酯、类胡萝卜素或苯丙素代谢中发挥作用,这在其他植物物种中得到了证实[27那39].
在P450的候选人鉴定欧夏至草叶子转录组。一种P450候选基因的最大似然系统发育树(附加文件2:表S1)M.大麦叶转录组(23].条示出全长P450候选的转录物丰度为基于所计算FPKM(每百万映射转录的片段每千碱基读取)值,和颜色编码,以表示不同的CYP家族。B.最大似然选择系统发育树M.大麦与CYP71酶的功能特征进行比较。双子叶植物的一个CYP71家族成员无油樟trichopoda用于根树。黑点突出引导支持的≥75%(1000次重复)。MV,欧夏至草;Tp,小白菊;通用,大豆;爸爸,Persea美国;在,拟南芥;铬、Catharanthus roseus也叫;点,Ammi majus;Mxp,Mentha x piperita.,ATR,无油樟trichopoda
MvCPS1和MvELS结合活性衍生的反应产物的澄清
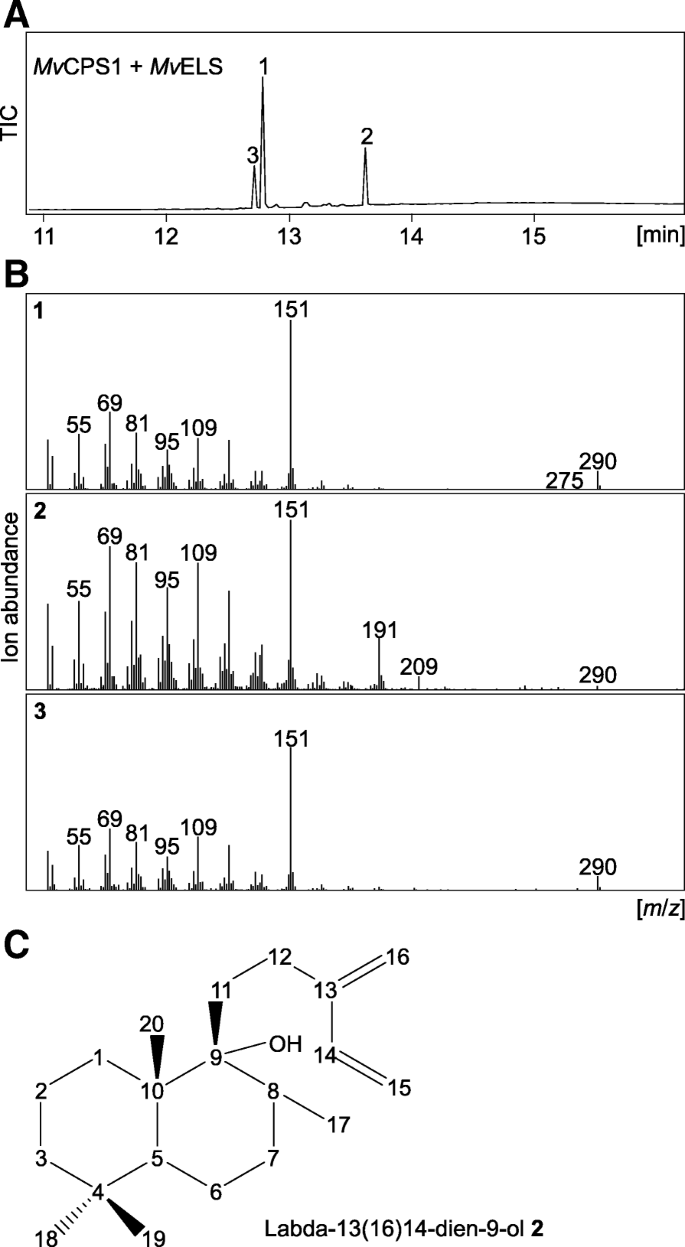
我们之前关于体外配对反应的研究MvELS显示了三种反应产物(化合物)1-3) [16].主要产物(化合物)1)被鉴定为9,13-环氧labd-14-ene,然而,剩余产物丰度低,妨碍了结构分析[16].复合3.可能代表了一个9,13-环氧labd-14-烯的异构体,基于几乎相同的保留时间和碎片模式。相反,化合物的质谱2显示额外丰富的离子m/Z.191和209,指示多个不同的结构(图中。3.).为了澄清的产品概况MvELS,我们进行了大规模的共表达试验MvCPS1和Mv来自冷杉属茅在一个大肠杆菌设计Diterpenoid生产的平台[40].纯化的化合物3.仍然不成功,由于其共洗脱与化合物1.与此相反,化合物的纯化2采用优化的硅胶色谱和半制备高效液相色谱分析方案,使1D1H-NMR和13C-NMR,以及2D NMR实验:COZY,HSQC,HMBC和H2BC(附加文件3.:图S1)。这种方法确定了化合物2如labda-13(16),14-dien-9-ol,其在C-9 (1C, 77.24 ppm)处具有一个自由羟基,而在9,13-环氧labd-14-ene中观察到的9,13-螺醚(1C, 93.8 ppm)(图。3.和额外的文件3.:图S1) [16].化合物中C-13 (1C, 147.54 ppm)和C-16 (1C, 115.43 ppm)以及C-14 (1C, 138.88 ppm)和C-15 (1C, 113.35 ppm)之间存在两个双键,证明了这一点2,而化合物1S.howed one double bond between C-14 (1C, 147.2 ppm) and C-15 (1C, 110.7 ppm), but not between C-13 (1C, 84.6 ppm) and C-16 (1C, 23.5 ppm) (Additional file3.:图S1) [16].
CYP71AU87作为9,13-环氧labd-14-烯羟化酶的生化特性
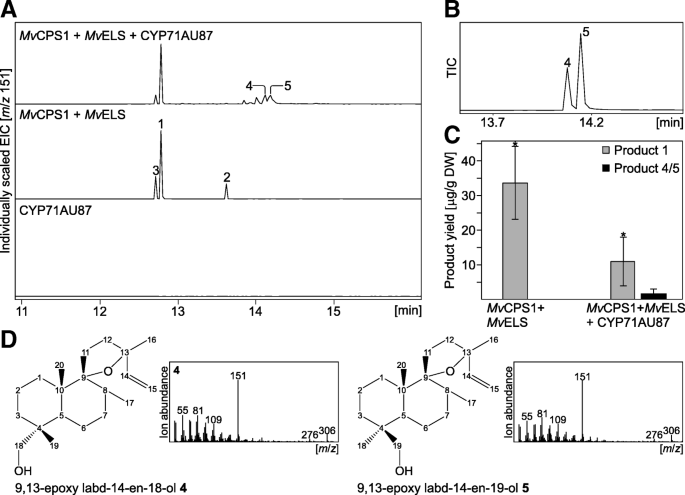
接下来,我们探测所选择的候选P450的活性在转化的反应产物Mv船。的全长序列Mv1270年,Mv3392年,Mv4213,Mv1545年,Mv从制备的cDNA中扩增出6504M.大麦并克隆到pLIFE表达载体中进行构建农杆菌-介导的瞬时共表达检测尼古利亚娜·宾夕法尼亚州[16那23].然后通过每一个候选P450的共表达检测P450的活性MvCPS1和MvELS.As相比化合物1-3.由…的连续活动产生的MvCPS1和Mv单独使用ELS,共表达时未检测到额外的二萜产物Mv1545年,Mv4213,Mv6504或Mv3392(附加文件4.:图S2)。CYP71家族成员共表达Mv1270(以下简称CYP71AU87)与MvCPS1和MvELS产生了两种产物(化合物)4.和5.)with retention times of 14.12 min and 14.19 min, respectively, indicating two closely related structures of higher polarity than the diTPS products (Fig.4.).这两种产品都显示接近该功能的主导相同碎裂模式m / z的质量离子特性,以及附加的质量离子m / z表明有一个额外氧原子的存在(图。4.).虽然只观察到较低的产物量,但cyp71au87催化形成化合物4.和5.伴随着labda-13(16)的接近完全的营业额,14二烯-9-醇2和在丰-9,13-环氧LABD-14烯的3倍的降低1与…的活动相比MvCPS1和Mv只船(图。4.).这种底物丰度的降低基本上与形成的形成一致4.和5.高达4微克g−1DW的转染N. Benthamiana.叶(图4.).
CYP71AU87的功能特征。一种提取离子色谱图(m/Z.由…产生的酶产物农杆菌- 介导的瞬态共同表达MvCPS1,Mv和CYP71AU87在N. Benthamiana..复合19 13-epoxy labd-14-ene;化合物2[1614-dien-9-ol], labda-13 (16);化合物3.,未识别的二萜类密切相关-9,13-环氧LABD -14-烯;化合物4.,9,13-环氧Labd-14-eNE-18-OL(通过NMR分析验证);化合物5.,9,13 - 环氧LABD -14-烯-19-醇(如通过NMR分析验证)。B.CYP71AU87纯化产物的GC-MS总离子色谱(TIC)分析4.和5.通过从〜50的代谢物提取获得 N. Benthamiana.叶子转染MvCPS1,Mv船和CYP71AU87。C9,13-环氧labd-14-烯的气相色谱-质谱分析19、13-epoxy labd-14-ene-18/19-ol4/5(组合量)从单叶中提取N. Benthamiana.co-transformed与MvCPS1,Mv船和CYP71AU87。共表达分析进行三次,误差棒表示一个标准偏差,*表示aP.-value < 0.05使用Tukey’s test。D.9,13-环氧labd-14-烯-18-醇和9,13-环氧labd-14-烯-19-醇的GC-MS质谱和结构基于NMR分析(见附加文件5.:图S3是关于NMR分析的详细信息)
To determine the structure of the CYP71AU87 products, ~ 1 mg of compounds4.和5.were extracted from 150 g of agroinfiltratedN. Benthamiana.然后用硅胶层析和半制备高效液相色谱法进行纯化(图。4.).虽然不能分离这两种化合物,但产品的混合物4.和5.was successfully isolated with > 90% purity. Combining a suite of 1D and 2D NMR analyses identified the products as 9,13-epoxy labd-14-ene-18-ol and 9,13-epoxy labd-14-ene-19-ol (Fig.4.和额外的文件5.:图S3)。Importantly, chemical shifts of C-9 (13C, 92.8 ppm) and C-13 (13C, 83.7) showed the presence of the 9,13-epoxy group rather than a free C-9 hydroxyl function in both CYP71AU87 products (Additional file5.:图S3)。此外,NMR分析表明,CYP71AU87在C-18或C-19处发生羟基化,而C-20、C-17和C-16处存在甲基,可以通过HSQC和HMBC相关性进行验证(Additional file)5.:图S3)。C-18和C-19之间的HMBC相关性分析支持化合物的鉴别4.和5.作为具有C-18或C-19羟基的同分异构体对(附加文件5.:图S3)。确定哪个结构代表化合物4.和5.是否可能根据这些分析,9,13-环氧labd-14-烯-18-醇和9,13-环氧labd-14-烯-19-醇被暂时指定为化合物4.和5., 分别。额外的瞬态N. Benthamiana.co-expression化验的MvCPS1,MvELS和CYP71AU87与Mv3392年,Mv4213,Mv1545或Mv6504没有产生任何新的反应产物,表明这些P450候选化合物利用化合物的能力4.和5.而不是MvELS产品作为基板(附加文件4.:图S2)。
进一步验证CYP71AU87在N. Benthamiana.共表达测定法,我们接下来进行的共表达MvCPS1,Mv温馨的,M.大麦细胞色素P450还原酶(MvCPR)和CYP71AU87在酵母(酿酒酵母).为此目的,构建PESC-HIS:MvCPS /SC.BTS1,PESC色氨酸:Mv目:/Mv生成CPR和pESC-Ura:CYP71AU87,使其共同表达MvCPS1,Mv船,Mv用于提高二萜产量的酵母菌株AM94中的CPR、CYP71AU87和内源性酵母GGPP合成酶BTS1 [41].GC-MS分析结果证实了化合物的生成4.和5.,虽然产品丰度相对较低(附加文件6.:图S4)。值得注意的是,酵母表达Mv单独使用CPS1或与MvELS导致了另外两种化合物的形成,6.和7.,这代表了MvCPS1产品peregrinol6.(即去磷酸化的peregrinol二磷酸)[16]并且可能是其退化产物7.,表示较低的催化活性MvCPS1,MvELS和/或CYP71AU87与在N. Benthamiana..这个观察结果与未转化的GGPP的存在是一致的8.基板上形成的代谢物的提取物。
CYP71AU87表现出底物特异性为-9,13-环氧LABD-14烯和labda-13(16),14-二烯-9-醇
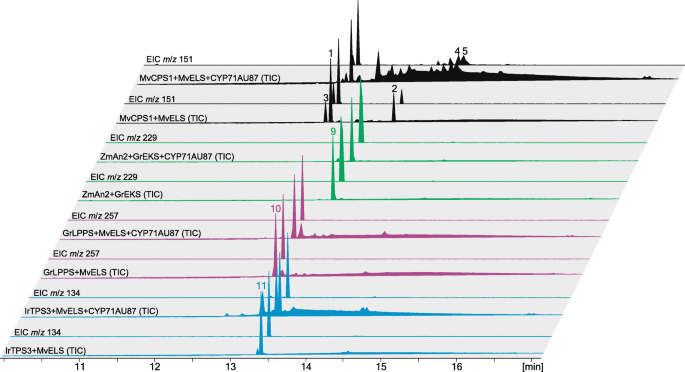
我们早期的研究证明了这一点MvELS是一种多功能diTPS,不仅生产9,13-环氧labd-14-烯作为主要产品,而且还接受II类diTPS产品(+)- copalydiphosphate (CPP)和labda-13-en-8-ol diphosphate (LPP)分别形成miltiradiene和manoyl oxide [16].迄今为止,虽然没有LPP合成酶在本种中被鉴定出来,M.大麦确实含有一个功能性的(+)-CPP合成酶(MvCPS3) [16].因此,我们探讨了CYP71AU87对不同labdane二萜中间体可能的底物杂性。这是通过利用labdane二萜生物合成的天然模块化特性实现的,来自不同物种的diTPSs和p450可以结合形成通向不同产品的活性途径[10那42那43].短暂的N. Benthamiana.通过组合CYP71AU87和COP71au87和CO表达测定MvELS具有不同的II类ditps,包括LPP合成酶Grindelia Robusta(GR牧民联盟)[23生成氧化manoyl(化合物)10)和(+)-CPP合酶Isodon得(IR.TPS3) [44形成米替拉烯(化合物11)(图。5.).此外,瞬态N. Benthamiana.玉米共表达试验(Zea Mays.)耳鼻喉科cpp合酶Zm评选AN2 [45)和G.罗布斯塔ENT-kaurene合酶GReks [23],检测CYP71AU87转化赤霉素前体的能力耳鼻喉科-kaurene(复合9.).CYP71au87的共同表达MvCPS1和MvELS作为阳性对照。CYP71AU87的共表达和diTPS组合Mv船/GRLPP,Mv船/IR.TPS3或Zm评选AN2 /GREKS导致manoyl氧化物,miltiradiene的预期生物合成和耳鼻喉科-kaurene分别(图。5.和额外的文件7.:图S5)。然而,没有检测到cyp71au87催化这些二萜类化合物转化的额外产物。
CYP71AU87的底物特异性。所示为瞬态反应产物的总离子色谱图(TIC)和萃取离子色谱图(EIC)N. Benthamiana.CYP71AU87与不同的II类和diTPSs共表达,产生不同的二萜类支架。被检测的产品包括赤霉素前体耳鼻喉科-kaurene9.由玉米(Zea Mays.)耳鼻喉科cpp合酶Zm评选AN2和耳鼻喉科-kaurene合酶GR的从Grindelia Robusta[45],manoyl氧化物10由LPP合酶产生GR牧民联盟从G.罗布斯塔[23] 和Mv目,miltiradiene11由(+)-CPP合酶形成IR.TPS3从Isodon得[44] 和Mv船。Co-expression的MvCPS1,Mv阳性对照为ELS和CYP71AU87。形成的二萜的质谱和结构在附加文件中给出7.:图S5
植物中CYP71AU87的产物分析
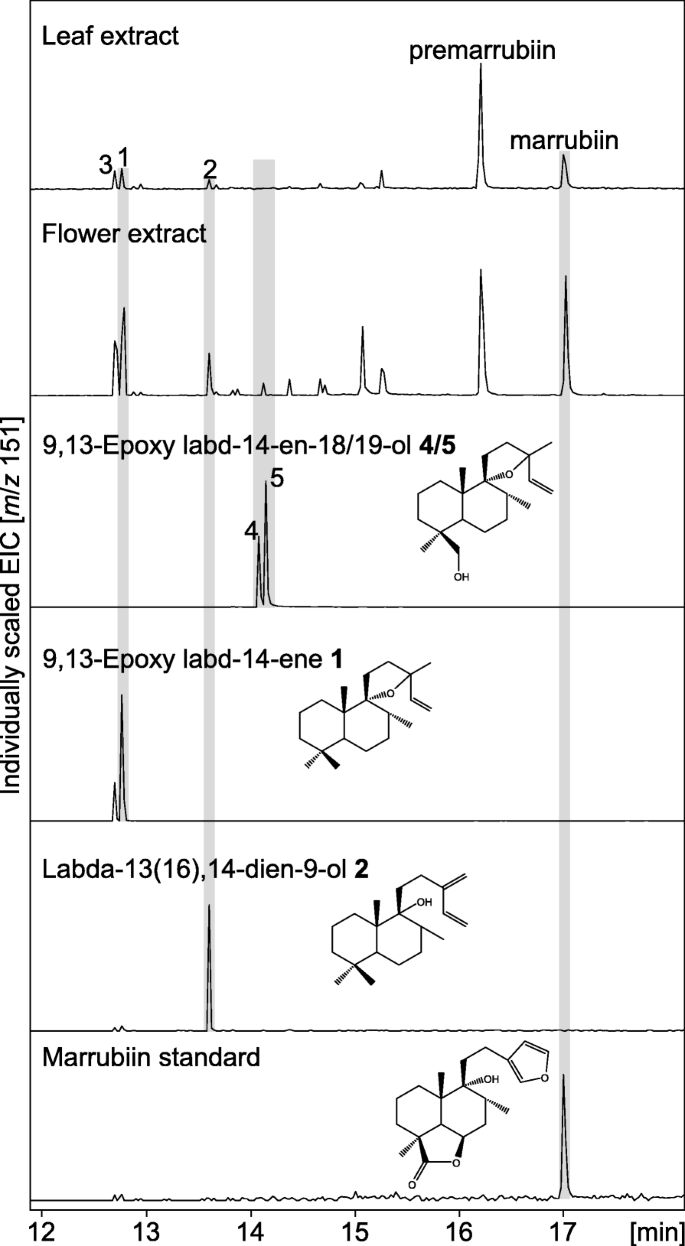
研究CYP71AU87产物9,13-环氧labd-14-烯-18-醇4.9、13-epoxy labd-14-ene-19-ol5.存在在足底的代谢物提取物M.大麦叶和花通过GC-MS分析,因为这些组织已被证明在marrubinin前、marrubinin和相关二萜中含量最多[16].该方法鉴定出marrubinin, pre marrubinin, 9,13-epoxy labd-14-ene1和labda-13(16),14-二烯-9-醇2以及身份不明的人Mv目产品3.而P450两种产物均未检测到(图。6.).为了验证GC-MS分析的结果,代谢物提取物进一步使用UPLC-Q Exactive MS分析(附加文件8.:图S6)。而纯化的CYP71AU87产物可以检测到为铵加合物,亲离子为m/Z.324.2893(单异位质量[m]+m/Z.306.2559)使用这种方法,9,13-环氧labd-14-烯-18-醇和9,13-环氧labd-14-烯-19-醇都不能检测到,从而确认了GC-MS分析的结果(附加文件8.:图S6)。
CYP71AU87转录本在M.大麦叶子和花
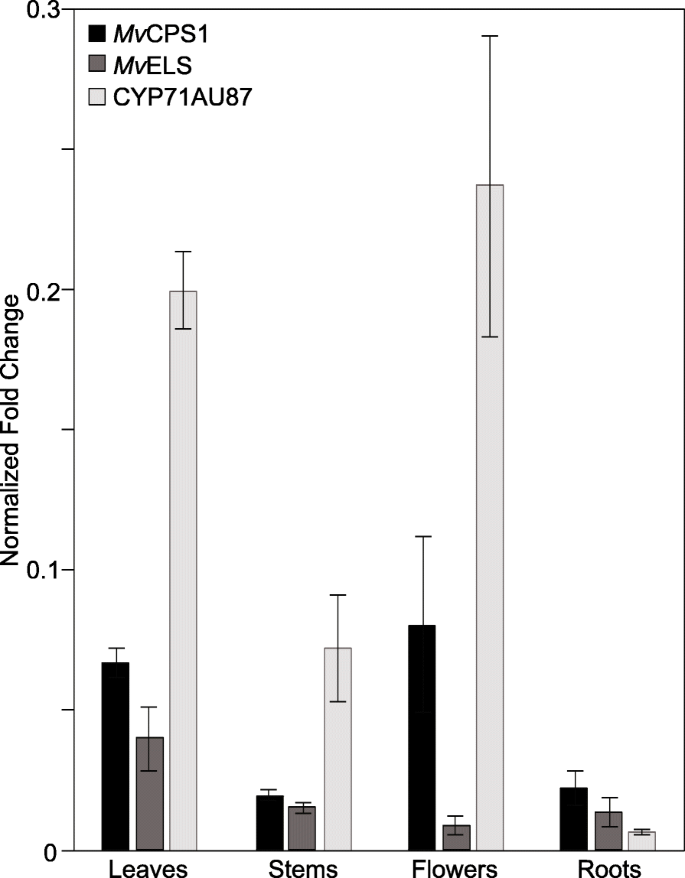
为了进一步研究CYP71AU87在marrubiin或相关二萜类化合物的生物合成,我们接下来进行的引物效率校正定量PCR(qPCR)分析CYP71AU87那mvcps1.和mvel在12周大的叶,茎,花和根中M.大麦植物。与主要丰marrubiin一致[16那17丰富的;丰富的mvel在叶中含量最高,在茎、花和根中也有,尽管总体水平较低(图。7.).相似地,mvcps1.基因在茎和根中表达量低,在叶和花中表达量高。大量的记录CYP71AU87叶和花也是主要的marrubiin积累组织,但茎中含量相对较低,仅在根中检测到微量的marrubiin积累。值得注意的是,基因表达CYP71AU87叶和花分别是?的3.7倍和5.3倍mvcps1.和mvel.
相对转录本丰度CYP71AU87在M.大麦组织。使用基因特异性寡核苷酸通过qPCR检测转录本丰度(附加文件)9.:表S2)和伸长率因子1α (EF1α)M.大麦作为参考。误差棒代表基于三个生物重复的三次测量的标准误差。以效率校正的寡核苷酸为基础计算基因表达量,通过典型产物的解离曲线和序列验证验证反应的特异性
讨论
丸红及相关二萜M.大麦具有潜在的药用价值,因为它们具有抗糖尿病和血管松弛的特性[13那15].进一步的药物开发依赖于生产这些代谢物的可行方法的可用性。从植物生物量中分离生物活性化合物,包括丸红素,往往不足以满足这一需求,这是由于天然生产者的典型复杂化学结构、有限的植物栽培和对地方性野生物种的必要保护。虽然已有报道marrubinin及其选择性衍生物的多步合成路线,但萜类天然产物固有的立体化学复杂性也阻碍了化学合成方法[46那47].随着基因和酶发现的快速进展,利用来自相同甚至不同物种的基因重建途径已成为植物天然产品生产的替代策略,例如抗疟疾药物青蒿素的微生物生产[48].为了实现marrubinin和相关呋喃萜类内酯的代谢工程方法,了解特征呋喃和内酯基团的生物合成是特别有趣的,因为这些功能修饰可能有助于治疗活动,如精神药物复方salvinorin A、抗炎二萜穿心莲内酯和抗疟疾药物青蒿素[49那50那51那52].
所呈现的研究说明结合启用基因组基因的发现和多基因共表达分析,以各种不同P450中识别先前隐藏的功能超家族的效用。CYP71AU87的表征增加了额外的催化剂到组中的CYP71家族的萜类代谢构件。与所述一对diTPS顺序反应,MvCPS1和MvELS、CYP71AU87形成了9,13-环氧labd-14-烯-18-醇和9,13-环氧labd-14-烯-19-醇的同分异构体产物,经GC-MS和NMR分析验证(图2)。4.).C-18和C-19的氧化作用将CYP71AU87与其他CYP71家族成员区分开来,这些成员在labdane二萜代谢中发挥作用,包括来自于labdane的CYP71BE52r . officinalis和鼠尾草pomifera催化铁基酚在C-2的羟基化[26那31],稻CYP71Z6和CYP71Z7促进的C-2氧耳鼻喉科-isokaurene和ent -cassadiene在oryzalide和植物卡桑的生物合成[53和CYP71Z16/18控制玉米中多拉布拉毒素在C-16和C-3上的顺序氧化形成多拉布拉毒素[54].然而,水稻CYP99A2/A3,属于较大的CYP71家族的CYP99亚家族成员,已经被证明催化C-19的顺序氧化syn -海松二烯(55那56].此外,在氧合C-18和C-19半日花烷双萜的已被证明对其他P450家族,如相关的氧化CYP701A家族的成员耳鼻喉科-kaurene在赤霉素生物合成中的作用[35和裸子植物特有的CYP720家族二萜树脂酸代谢[57那58].然而,与cyp71au87催化的羟基化不同,这些酶促进其各自底物的逐步氧化形成相应的酸。因此,p450催化的labdane支架在C-18或C-19处的氧化可能独立进化了几次,进一步的物种特异性多样化催化特异性。
共表达测定N. Benthamiana.而CYP71AU87对C-9-oxygenated的转化具有特异性MvELS产品在这里测试的基质范围内(图。5.),这种酶对C-18或C-19位置的羟基化表现出乱性(图。4.).因为这些产品没有被检测到在足底(无花果。6.),它不是可识别的,如果在形成了该异构体产物对是CYP71AU87的本地功能。Marrubiin和所有描述的结构上相关的二萜类化合物在C-19被官能化,在该位置处支撑的特定区域 - 生物合成反应[15].值得注意的是,已针对CYP720B1描述了类似的催化模式松果体taeda形成C-18-和c -19-羟化的米替拉二烯异构体S. Cerevisiae.[59],而Sitka Spruce的亲密同源物CYP720B4(西加云杉)在C-18中产生Regio选择性产物氧合[57].c -19氧化二萜酸,如该属植物的交联酸和异木栓酸Juniperus和其他针叶树[60那61],也被观察到,但根本代谢酶是未知的。在此背景下,仍有待澄清CYP71AU87是否形成两者的C-18-和C-19羟基化的产品,M.大麦或者更有效的代谢通道在足底仅从C-19异构体就可以形成marrubinin。
在之前的研究中,生物化学特征MvELS所示的三个产品,其中两个表示-9,13-环氧LABD-14烯1并且其身份不明,但密切相关的异构体3.为基于接近相同质谱[16].在这里,核磁共振鉴定出第三个产物为labda-13(16),14-dien-9-ol2,其特征是在C-9上有一个游离羟基,而不是在9,13-环氧labd-14-ene中存在的9,13-螺旋醚功能(图。1).在labda-13(16)的研究过程中,14-dien-9-ol也被报道为diTPS对的产物真空吸尘器TPS1和真空吸尘器TPS6从Vitex Agnus-castus[18,与该属相关的唇形科物种Marrubium产生相关的c -9-氧二萜内酯。早期研究表明,marrubin中特有的游离C-9羟基是由植物物质代谢物提取而非酶解形成的[17那62].这一假设与观察到的CYP71AU87产物仅以9,13螺旋醚形式存在(图。4.).然而,如果9,13环氧化合物的开口和可能的环重新形成是自发的或酶法的,仍有待验证,因为在提取物中都存在labda-13(16),14-dien-9-ol和9,13-环氧labd-14-eneM.大麦(无花果。6.)及在相关物种中观察到的相似代谢物分布[19].
尽管有直接证据表明9,13-环氧labd-14-ene的C-18/19羟基化是CYP71AU87在M.大麦需要进一步的基因研究,同时发生mvcps1.那mvel和CYP71AU87组织中的转录本MvELS产品也存在(图。6.)提示CYP71AU87很容易遇到9,13-环氧labd-14-ene作为底物。底物特异性MvELS产品进一步支持CYP71AU87的marrubiin或相关的二萜类化合物的生物合成中的作用(图5.).在CYP71AU87产品的缺位在足底可能是由于这些功能二萜类化合物的快速转换M.大麦,对于其他在植物组织中无法检测到酶产物的p450,也有类似的建议,如Thapsia garganicaCYP76AE2可能在thapsigargin生物合成中发挥作用[63]和番茄CYP71BN1其催化二萜lycosantalonol的形成[64].
cyp71au87催化生成特别是9,13-环氧labd-14-烯-19-醇,这可能是生物合成前marrubinin和其他二萜类化合物的19,6-内酯环结构的一个反应步骤Marrubium(无花果。1).在一些物种中存在marrubenol和marrubenol,这是一种生物活性的二萜,具有C-19和C-6b的羟基Marrubium支持朝向内酯形成顺序羟基化反应[15那65那66(图。1).在概念上已经描述了类似的途径生物合成木香烃内酯倍半萜类化合物,通过连续氧化C-12和在C-6吉macrene A的羟基化,由一对P450酶促进[20.那67].可替代地,或脱氢酶还原酶可以以进一步氧化作用在-9,13-环氧LABD -14-烯-19-醇的C-19羟基基团,并且与在C-6B P450催化氧化,结果在内酯环的形成为组合类似地提出了水稻二萜稻内酯A和倍半萜青蒿素[33那68那69].前丸红蛋白和相关结构的形成需要进一步通过p450支持的氧化C-15和/或C-16形成呋喃环,并随后闭合环(图)。1).虽然marrubinin生物合成中内酯和呋喃环形成的序列未确定,但来自P450, CYP76BK1五AGNUS-荆,其催化peregrinol的朝向C-16羟基化(peregrinol二磷酸的去磷酸化的衍生物)的预测vitexilactone前体LABD-13Z.-烯-9,15,16-三醇确实是最近被发现的[18].
结论
CYP71AU87的功能表征举例说明相结合的多酶共表达测定转录数据的基因特异性的查询,以确定在非模式植物系统的天然产物途径基因的效用。CYP71AU87增加了额外的催化剂,以二萜类化合物生物合成的P450的目录,并提供资源的酶用于生产marrubiin和相关生物活性二萜内酯。
方法
植物材料
种子欧夏至草购自贝克溪传家宝种子公司种子M.大麦以及尼古利亚娜·宾夕法尼亚州在Conviron TCR120生长室(www.conviron.com在相对湿度60%,光周期16 h, 100 μmol m−2 s−1光照强度,昼夜温度循环为21/18°C。两周后,M.大麦除非另有说明,植物在大学温室里再维持12周。
系统发育和序列分析
使用clustalW2生成蛋白质序列比对,并用Gblocks进行筛选[70].使用PhyML-aBayes版本3.0.1 beta进行最大似然系统发育分析,包括四个比率替代类别、LG替代模型、BIONJ起始树和1000个bootstrap重复[71].使用寿命的交互树(ITOL)V4.3 [72].
将转录组数据映射到候选P450基因
叶特异性转录组资源M.大麦如前所述[23].P450候选蛋白通过查询自定义P450蛋白数据库的转录组清单来识别(附加文件)1数据文件S1)。通过使用BWA版本0.5.9-r16,将适配器修饰的Illumina reads映射回装配的P450转录本,评估P450候选基因的相对转录本丰度。Reads被映射为配对,最大插入尺寸为350 bp,在对齐步骤中允许不匹配的阈值为1。
基因克隆
12周龄叶片总RNAM.大麦利用SuperScript III第一链合成系统(ThermoFisher)将植物转化为cDNA。这CYP71AU87然后使用Phusion-HF聚合酶(新英格兰生物实验室)和基因特异性寡核苷酸进行扩增(附加文件)9.:表S2),并连接到pJET载体(Clontech)进行序列验证。结果扩增子插入pLIFE和pESC:Ura载体中进行表达N. Benthamiana.和S. Cerevisiae., 分别。这Mv以同样的方法克隆了CPR基因,并最终插入到pESC:Trp载体中表达S. Cerevisiae..MvCPS1克隆到含有酵母GGPP合成酶BTS1的载体pESC的第一个多克隆位点。MvELS被克隆到一个已经包含的pESC:Trp载体的第一个多克隆位点MvCPR在第二个多克隆位点。
Terpenoid代谢物的GC-MS分析
提取液从12周龄的叶、茎、花和根中提取,提取量约为150 mgM.大麦植物。组织研磨成在液氮中的细粉末2用1.5 ml己烷在室温下剧烈振荡提取萜类化合物16 h。通过添加无水钠将提取物从残留水中分离出来2所以4.,在氮下干燥2流,并再溶解在己烷中以供进一步分析。GC-MS analysis was performed on an Agilent 7890B GC interfaced with a 5977 Extractor XL MS Detector at 70 eV and 1.2 ml min−1He flow, using a HP5-ms column (30 m, 250 μm i.d., 0.25 μm film) and the following GC parameters: 50 °C for 1 min, 20 °C min−1T.o 300 °C, hold 3 min with pulsed splitless injection at 250 °C and 50 °C oven temperature. MS data from 90 to 600 mass-to-charge ratio (m/Z.)were collected after a 4 min solvent delay. Identification of marrubiin was achieved by comparison to the authentic standard (www.chromadex.com).
萜类化合物的代谢物的LC-MS分析
LC-MS分析:干燥样品用300 μl乙腈:水(80:20;V./ v)。所有测量都是在Q精确HF质谱仪上进行的,该质谱仪配有Vanquish LC系统(Thermo Scientific)。样品体积为5 μl,用Waters Acquity UPLC CSH C进行分离18柱(100 × 2.1 mm;耦合到Acquity UPLC CSH C18VanGuard预柱(5 × 2.1 mm;1.7μm)。柱保持在65°C,流速为0.6 ml min−1.移动相由A:乙腈:水(60:40,v / v)组成,用甲酸铵(10mM)和甲酸(0.1%)和B:2-丙醇:乙腈(90:10,v / v)甲酸铵(10mM)和甲酸(0.1%)。在下面的梯度下进行15分钟的分离:0min 15%B;0-2分钟30%b;2-2.5分钟48%B; 2.5-11分钟82%B;11-11.5分99%b;11.5-12分钟99%b;12-12.1分钟15%b;12.1-15分钟15%B. Orbitrap MS仪器在电喷雾电离(ESI)中以下列参数在电喷雾电离(ESI)中运行:质量范围60-900 m/Z.;喷淋电压3.6 kV,护套气体(氮气)流量60台;辅助气体(氮气)流量25单位,毛细管温度320°C,全扫描MS1质量分辨能力120,000,数据依赖的MSMS (dd-MSMS)每周期扫描4次,dd-MSMS质量分辨能力30,000。使用Thermo Xcalibur 4.0.27.19进行数据采集和分析[73].
瞬时表达尼古利亚娜·宾夕法尼亚州
全长cDNA克隆MvCPS1,Mv船和CYP71AU87在植垢表达载体中单独转化为根癌农杆菌菌株GV3101。Bacterial cultures were grown at 28 °C in Luria-Bertani (LB) medium supplemented with 50 mg l−1卡那霉素,沉淀并重悬至最终OD600在10 mM MES缓冲液中加入10 mM氯化镁2.Following incubation for two hours at 22 °C and gentle shaking, cell suspensions were mixed and syringe-infiltrated into the underside of the leaves of 5-week-oldN. Benthamiana.植物。在所有的实验中,靶基因进一步与植物病毒蛋白p19共同表达以抑制RNA沉默。[23转基因植株保存4天后,用1.5 ml己烷从单个转基因叶片中提取代谢物,如上所述通过GC/LC-MS分析。以结构相关的二萜菌丝膜醇为标准品,采用外标准曲线,通过GC-MS对代谢物进行定量。基于Welch Two Sample计算了烟草共表达检测中代谢物水平之间具有统计学意义的差异T.以及(P.-value < 0.05). Quantification of metabolites via LC-MS in tobacco co-expression assays was calculated using sclareol as internal standard at a concentration of 1 μg ml−1使用Thermo Xcalibur 4.0.27.19软件。
酶在工程酵母中的共表达
生成的结构pESC-HIS:MvCPS /SC.BTS1,PESC色氨酸:Mv目:/MvCPR和PESC浦:CYP71AU87是co-transformed酿酒酵母专为生产二萜而设计的菌株AM94 [59那74].细胞在50毫升相应的选择性辍学培养基(- His, - Trp, - Leu, - Ura, 2%葡萄糖)中生长,30°C至OD600的∼将细胞转移到50 ml相应的含2%半乳糖的选择性dropout培养基中进行诱导。48 h后,用5 ml乙醚中的玻璃微珠涡旋细胞微球提取代谢物,风干后在1 ml己烷中重新悬浮,用于GC-MS分析。
的核磁共振(NMR)分析CYP71AU87产品
大约1毫克CYP71AU87产物从〜50中提取 N. Benthamiana.叶子转染MvCPS1,Mv船和CYP71AU87使用400ml己烷。以乙酸乙酯-正己烷梯度为流动相(100%正己烷,10%乙酸乙酯,20%乙酸乙酯;V./ v)。馏分含有产物的合并,N下干燥2用100%乙腈重悬。进一步的纯化是通过安捷伦1100系列HPLC与安捷伦Zorbax Eclipse Plus C反相高效液相色谱实现的8.色谱柱、G1315B二极管阵列检测器(DAD)和G1364C-1260 FC-AS馏分收集器。流动相由a:水和B:乙腈的混合物组成。产品分离采用以下梯度:0 min 50% B;0-7分钟50% B;7-10分钟75% B;10-20分钟90% B;20-40分钟100% B.将纯化的产品用添加了0.03%四甲基硅烷(TMS)作为内标的氯仿- d混合重悬(Sigma)。用于结构识别CYP71AU87产品1 d (1H,13C、NOE)和2D (COSY、HSQC、HMBC、选择性HSQC、选择性HMBC)光谱在Brucker Avance 800 MHz光谱仪上采集,并配备5 mm CPTCI冷冻探针。
定量PCR (qPCR)
Total RNA was isolated as previously described using approximately 100 mg tissue [75].RNA完整性和浓度使用按照制造商的协议生物分析仪2100 RNA纳米芯片测定(安捷伦)测量。等于RNA量的用于cDNA合成用的Superscript III逆转录酶(赛默飞世)和寡聚(dT)引物。随后的qPCR反应中使用的试剂盒SsoFast(一个Bio-Rad公司CFX96实时系统上进行www.bio-rad.com)和靶特异性寡核苷酸(附加文件9.:表S2)。相对转录本丰度通过效率修正ΔCT计算,该效率是根据每个基因对的引物效率计算产生的扩增效率值(e值)计算的。相对基因表达值计算基于M.大麦延伸因子1α作为内参基因,用3个生物重复进行3次测量。通过对代表性扩增子序列的验证,确定了靶点特异性。
缩写
- CPP:
-
Copalyl二磷酸
- DiTPS:
-
二萜合酶
- GC-MS:
-
气相色谱质谱
- GGPP:
-
Geranylgeranyl二磷酸
- LC-MS:
-
液相色谱质谱
- NMR:
-
核磁共振
- P450酶:
-
细胞色素P450单氧酶
参考文献
- 1。
挖掘植物的生物多样性:一场正在酝酿中的革命。科学。2012;336(6089):1658 - 61。
- 2.
沃泽尔ET,俱知安TM。植物代谢的不同化学组的未来。科学。2016; 353(6305):1232-6。
- 3.
彼得斯rj。所有的两个环:Labdane相关的二萜类化合物。天然产物代表2010; 27(11):1521至1530年。
- 4.
Guerra-Bubb J,Croteau R,Williams Rm。紫杉醇生物合成的早期阶段:关于早期途径代谢产物的合成和鉴定的临时报告。NAT产品批准。2012; 29(6):683-96。
- 5.
关键词:紫杉醇,紫杉醇合成酶,紫杉醇水松黄花细胞悬浮培养物。拱生物化学生物物理学。1997年; 337(2):185-90。
- 6.
Casselman I, Nock CJ, Wohlmuth H, Weatherby RP, Heinrich M.从本地到全球——50年的研究鼠尾草divinorum.J Ethnopharmacol。2014;151(2):768 - 83。
- 7.
Pelot Ka,Mitchell R,Kwon M,Hagelthorn DM,Wardman JF,Chiang A,Bohlmann J,RO DK,Zerbe P.生物合成的精神式植物二萜Salvinorin A:发现和表征的鼠尾草divinorumclerodienyl二磷酸合酶。工厂j . 2017, 89(5): 885 - 97。
- 8.
洛d,Callari R,汉伯格B,Wubshet SG,尼尔森MT,安德森-RanbergĴ,Hallstrom的BM,Cozzi酒店女,海德H,莫勒LB,等。氧化和蓖麻烯环化在大戟的生物合成从成熟种子因子大戟属植物lathyris中国科学(d辑:地球科学)2016;
- 9.
植物二萜代谢在未来生物制药中的应用:前景与挑战。Phytochem启2018;17(1):113 - 30。
- 10。
王志强,王志强,王志强,等。植物二萜合成酶在生物工程中的应用。生物科技趋势》。2015;33(7):419 - 28。
- 11.
Pateraki I,安德森-RanbergĴ,詹森NB,Wubshet SG,Heskes AM,福曼V,Hallstrom的B,汉伯格B,Motawia MS,CE奥尔森等人。从环磷酸腺苷助推器毛喉素的生物合成总锦紫苏forskohlii.Elife。2017; 6:e23001。
- 12.
Nielsen MT, Ranberg JA, Christensen U, Christensen HB, Harrison SJ, Olsen CE, Hamberger B, Møller BL, Nørholm MH. Forskolin前体Manoyl oxide对映体纯形式的微生物合成。应用环境微生物学。2014;80(23):7258-65。
- 13.
好的,Elbagory AM, Ameer F, Hussein AA。Marrubiin。分子。2013;18(8):9049 - 60。
- 14.
Mnonopi N, Levendal RA, Mzilikazi N, Frost CL。Marrubiin,是Leonotis益母草,可缓解糖尿病症状。Phytomed。2012;19(6):488 - 93。
- 15.
马鲁属植物的化学和药理研究进展。医药学报。2010;16(31):3503-18。
- 16.
泽布P,蒋A,Dullat H,O'Neil的约翰逊男,斯塔克斯C,汉伯格B,医药活性二萜类化合物的生物合成系统的Bohlmann J.二萜合酶欧夏至草.植物杂志2014; 79(6):914-27。
- 17.
Roenss W,Reuter B,Zapp J.ApdandeDiterPene marrubiin的生物合成欧夏至草经由非甲羟戊酸途径。生物化学杂志1997; 326(PT 2):449-54。
- 18.
Heskes AM, Sundram TCM, Boughton BA, Jensen NB, Hansen NL, Crocoll C, Cozzi F, Rasmussen S, Hamberger B, Hamberger B,等。药用植物中生物活性二萜的生物合成Vitex Agnus-castus.植物杂志2018; 93(5):943-58。
- 19.
谢大勇,马冬梅,王志强,等。青蒿素的生物合成Artemisia Annua.和代谢工程:问题,挑战和观点。Phytochem Rev. 2016; 15(6):1093-114。
- 20.
池泽N,Gopfert JC,阮DT,金秀,O'Maille PE,春天O,罗DK。莴苣木香合酶(CYP71BL2)和来自向日葵催化不同的区域选择性其同系物(CYP71BL1)和倍半萜内酯代谢立体选择性羟基化。J Biol Chem。2011; 286(24):21601-11。
- 21.
蒙罗TA,Rizzacasa MA,罗斯BL,托特BA,向salvinorin一,强效κ阿片受体激动剂的药效颜F.研究。J Med Chem。2005; 48(2):345-8。
- 22.
埃克斯坦路德维希U,韦伯RJ,凡Goethem ID,东JM,李AG,木村男,奥尼尔PM,布雷PG,沃德SA,克里希纳S.青蒿素目标的恶性疟原虫的SERCA。自然。2003; 424(6951):957-61。
- 23.
陈志刚,陈志刚,陈志刚,陈志刚,陈志刚,陈志刚,陈志刚,陈志刚,陈志刚。非模型系统中模块化二萜代谢的基因发现。植物杂志。2013;162(2):1073 - 91。
- 24.
Teoh KH, Polichuk DR, Reed DW, Nowak G, Covello PS。Artemisia Annua.L.(菊科)毛状体特异性的cDNA揭示CYP71AV1,细胞色素P450在抗疟倍半萜内酯青蒿素生物合成中起关键作用。费用。2006; 580(5):1411-6。
- 25.
郭军,马旭,蔡勇,马勇,詹忠,周永军,刘伟,管明,杨军,崔刚,等。细胞色素P450的混乱导致丹参酮生物合成的分叉途径。新植醇。2016;210(2):525 - 34。
- 26。
Ignea C, Athanasakoglou A, Ioannou E, Georgantea P, Trikka FA, Loupassaki S, Roussis V, Makris AM, Kampranis SC.鼠尾草酸的生物合成。中国科学(d辑:地球科学)2016;
- 27。
植物p450作为物种特异性化学多样性进化的通用驱动程序。中国生物科学(英文版)2013;368(1612):20120426。
- 28。
赵宇军,程qq,苏鹏,陈旭,王学军,高伟,黄立强。细胞色素P450在药用植物萜类生物合成中的作用研究进展中国生物医学工程学报。2014;33(6):369 - 372。
- 29。
郭军,周永军,沈勇,杨丽,王勇,张旭,刘伟,Peters RJ,陈旭,等。CYP76AH1可催化丹参酮生物合成过程中多胺的转化,并可在酵母中异源生产铁酚。中国科学(d辑:地球科学)2013;110(29):12108-13。
- 30.
紫Ĵ,彼得斯RJ。CYP76AH4的表征阐明在唇形科酚二萜的生物合成。Org Biomol Chem。2013; 11(44):7650-2。
- 31.
Bozic医师d,Papaefthimiou d,布鲁克纳K,德沃思RC,Tsoleridis CA,Katsarou d,Papanikolaou A,Pateraki我,Chatzopoulou FM,Dimitriadou E,等人。朝向唇形科阐明鼠尾草酸的生物合成:在途径的三个第一步骤功能表征鼠尾草后和Rosmarinus officinalis..Plos一个。2015; 10(5):e0124106。
- 32。
王Q,Hillwig Ml,冈田K,Yamazaki K,Wu Y,Swaminathan S,Yamane H,Peters RJ。CYP76M5-8的表征表明植物生物合成基因簇内的代谢可塑性。J Biol Chem。2012; 287(9):6159-68。
- 33。
王强,王志强,王志强。CYP99A3:水稻桃内酯生物合成基因簇中二萜氧化酶的功能鉴定。植物j . 2011; 65(1): 87 - 95。
- 34。
Bertea CM,沙尔克男,卡普女,玛菲男,克罗托R.示范该薄荷的薄荷呋喃合酶(薄荷)是细胞色素P450单加氧酶:克隆,功能性表达,和表征负责基因。拱生物化学生物物理学。2001; 390(2):279-86。
- 35。
p450控制植物萜类专门化代谢中的代谢分支。Phytochem启2018;17(1):81 - 111。
- 36.
刘问,marble D, Tanic N,佩斯克米,Bankovic J, Pateraki我Ricard L,费雷尔,德·沃斯·R, van de Krol年代,Bouwmeester h .说明和parthenolide足底重建的生物合成途径。金属底座Eng。2014;23:145-53。
- 37.
Cankar K, van Houwelingen A, Goedbloed M, Renirie R, de Jong RM, Bouwmeester H, Bosch D, Sonke T, Beekwilder J. Valencene oxidase CYP706M1 from Alaska cedar (Callitropsis nootkatensis).2月。2014;588(6):1001 - 7。
- 38.
罗鹏,王玉华,王国栋,Essenberg M,陈小勇。棉花倍半萜生物合成的细胞色素P450单加氧酶(CYP706B1) (+)-delta-cadinene-8-羟化酶的分子克隆及功能鉴定植物j . 2001; 28(1): 95 - 104。
- 39.
追踪细胞色素P450进化路径的进展。生物物理学报。2011;1814(1):14-8。
- 40。
Morrone D, Lowry L, detman MK, Hershey DM, Xu M, Peters RJ。采用模块化代谢工程系统提高二萜产量大肠杆菌: MEV和MEP类异戊二烯前体路径工程的比较。中国生物医学工程学报。2010;32(6):591 - 598。
- 41。
Ignea C,Trikka FA,斯尼古拉迪斯AK,Georgantea P,Ioannou的E,Loupassaki S,Kefalas P,Kanellis AK,Roussis V,Makris AM,Kampranis SC。高效生产双萜酵母中工程Erg20p成香叶基二磷酸合成酶。Metab Eng。2015; 27:65-75。
- 42。
杨斌,吕晓东,杨晓东。合成生物学在阐明植物单、倍半和二萜代谢方面的应用。摩尔。2015;8(1):-。
- 43。
安德森-RanbergĴ,孔斯塔德KT,尼尔森MT,詹森NB,Pateraki I,巴赫SS,汉伯格B,泽布P,斯塔克d,Bohlmann J,等。扩大二萜结构的多样性,通过立体化学景观控制组合生物合成。Angew化学国际版英格兰。2016; 55(6):2142-6。
- 44.
含氧二萜nezukol在药用植物中的生物合成Isodon得由一对二萜合酶催化的。Plos一个。2017; 12(4):e0176507。
- 45.
Harris LJ, Saparno A, Johnston A, Prisic S, Xu M, Allard S, Kathiresan A, Ouellet T, Peters RJ。玉米An2基因是由镰刀攻击和编码耳鼻喉科-copalyl二磷酸合酶。植物学报。2005;59(6):881-94。
- 46.
Mangoni L,Adinolfi M,Caputo R,Laonigro G. marrubiin的合成。四面体。1972; 28(3):611-21。
- 47.
(+)-Marrubiin和(-)-Marrulibacetal的合成。Org。2016;18(14):3430 - 3。
- 48.
Paddon CJ,Westfall PJ,Pitera DJ,Benjamin K,Fisher K,Mcphee D,Leavell MD,Tai A,Main A,Eng D等人。高水平的半合成生产的强化抗疟蒿素。自然。2013; 496(7446):528-32。
- 49.
莱利AP,Groer CE,年轻d,埃瓦尔德AW,Kivell BM,Prisinzano TE。合成和呋喃取代salvinorin一个类似物的κ-阿片样物质受体活性。J Med Chem。2014; 57(24):10464-75。
- 50.
Shul'ts EE, Mironov ME, Kharitonov YV。Labdane系列呋喃二萜:在植物中的出现、全合成、几种转化和生物活性。化学学报。2014;50(1):2-21。
- 51.
廉JC,陈TK,伍DS,Sagineedu SR,StanslasĴ,黄WS。穿心莲内酯及其类似物:打击炎症和癌症通用的生物活性分子。Clin Exp Pharmacol physiol。2012; 39(3):300-10。
- 52.
艾属植物倍半萜内酯的生物活性及分析方法。J Anal Methods Chem. 2015;2015:247685。
- 53.
吴勇,王强,王强。水稻多功能生物合成基因的解析:CYP71Z6和7的生化特性2月。2011;585(21):3446 - 51。
- 54.
马富,丁勇,Murphy KM, Yaacoobi O, Addison JB, Wang Q, Shen Z, Briggs SP, Bohlmann J, Castro-Falcon G, et al。玉米dolabradiene衍生防御的发现、生物合成和胁迫相关积累。植物杂志。2018;176(4):2677 - 90。
- 55.
徐敏。重组表达的优化使得在水稻二萜生物合成中发现新的细胞色素P450活性。应用微生物技术。2015;99(18):7549-58。
- 56。
王强,王强。CYP76M7是一个耳鼻喉科-cassadiene C11alpha羟化酶限定第二多功能二萜的生物合成基因在水稻簇。植物细胞。2009; 21(10):3315-25。
- 57。
二萜代谢的进化:锡特卡云杉CYP720B4催化松柏树树脂酸生物合成的多重氧化。植物杂志。2011;157(4):1677 - 95。
- 58。
松柏二萜树脂酸生物合成的模块化:不同CYP720B分支的P450酶使用不同的底物并聚合在相同的产品上。植物杂志。2016;171(1):152 - 64。
- 59。
关键词:酵母,labdane-type,二萜,生物合成,化学多样性金属底座Eng。2015;28:91 - 103。
- 60。
松柏类植物中二萜树脂酸的研究。植物化学。2006;67(22):2415 - 23所示。
- 61。
巴雷罗AF,Herrador MM,亚加P,亚加JF,亚加AF。COMMUNIC酸:发生,性质和用作chirons用于生物活性化合物的合成。分子。2012; 17(2):1448至1467年。
- 62。
Henderson MS, Mccrindle R. Premarrubiin - a二萜Marrubium Vulgare化学学报(英文版);2014。
- 63。
安德森TB,Martinez的-Swatson KA,Rasmussen的SA,鲍顿BA,乔根森K,安德森-RanbergĴ,Nyberg的N,Christensen的SB,西蒙森HT。本土化和体内表征Thapsia garganicaCYP76AE2在Thapsigargin生物合成中起作用。植物杂志。2017;174(1):56 - 72。
- 64。
松叶Y,紫Ĵ,琼斯AD,彼得斯RJ,的Pichersky E.生物合成的二萜类化合物通过lycosantalonol二磷酸nerylneryl在番茄。Plos一个。2015; 10(3):e0119302。
- 65。
埃尔巴尔达伊S,莫瑞尔N,WIBO男,法布尔N,Llabrés酒店G,Lyoussi B,从marrubenol和marrubiin的Quetin-勒克莱尔J.血管舒张活性欧夏至草.足底医学。2003;69(1):75 - 7。
- 66。
埃尔巴尔达伊S,Hamaide MC,Lyoussi B,Quetin-勒克莱尔Ĵ,莫瑞尔N,WIBO M. Marrubenol与L型钙离子通道的苯基烷基胺结合位点相互作用。EUR J Pharmacol。2004; 492(2-3):269-72。
- 67。
德Kraker JW,Franssen MC,Joerink男,德格鲁特A,Bouwmeester HJ。木香,dihydrocostunolide和leucodin的生物合成。存在于菊苣的倍半萜内酯的内酯环的细胞色素P450催化形成的示范。植物理性。2002; 129(1):257-68。
- 68.
Ikram N, Simonsen HT。植物生物技术生产青蒿素的研究进展。植物学报。2017;8:1966。
- 69.
Shimura K, Okada A, Okada K, Jikumaru Y, Ko KW, Toyomasu T, Sassa T, Hasegawa M, Kodama O, Shibuya N,等。水稻内酯生物合成基因簇的鉴定。中国生物化学杂志。2007;282(47):34013-8。
- 70.
Talavera G,Castresana J.从蛋白质序列比对去除发散和模棱两可的嵌段后改善文学发生。系统中的生物学。2007; 56(4):564-77。
- 71.
Guindon S,Dufayard JF,Lefort V,Anisimova M,Hordijk W,Gascuel O.新算法和估计最大似然性的方法:评估Phyml 3.0的性能。系统中的生物学。2010; 59(3):307-21。
- 72.
交互式生命树(iTOL) v3:用于显示和注释系统发育和其他树的在线工具。44(W1): W242-5。
- 73.
Cajka T, Smilowitz JT, Fiehn O.在9种液相色谱-高分辨率质谱平台上验证定量非靶向脂质组学。肛门化学2017;89(22):12360 - 8。
- 74.
Gietz RD。通过醋酸锂/ SS载体DNA / PEG方法酵母转化。方法Mol Biol。2014; 1163:33-44。
- 75.
Kolosova N, Miller B, Ralph S, Ellis BE, Douglas C, Ritland K, Bohlmann J.从裸子植物和被子植物中分离高质量RNA。生物学技术。36 2004;(5): 821 - 4。
致谢
感谢David Nelson (University of Tennessee)博士对CYP71AU87注释的帮助。
资金
该项目的开发,并完成了财政支助资金启动通过加州大学戴维斯(以P.Z.)大学和加州大学戴维斯分校学术评议教师研究基金(以P.Z.)提供实验支持提供。出版费用由启动资金通过美国加州大学戴维斯分校(以P.Z.)资助。另外,研究生的工资和学费支持由一个NIGMS博士前奖学金(T32 GM007377,以P.S.K.)提供。
数据和材料的可用性
我可以确认我已经在我的手稿的声明部分包含了一份关于数据和材料可用性的声明。本研究报告的核苷酸序列提交美国国家生物技术信息中心(NCBI) GenBankTM/EBI数据库,登录号:CYP71AU87 (MH593587),Mv心肺复苏术(MH593588),Mv1545(MH82416),Mv4213(MH824162),Mv6504 (MH824163),Mv3392 (MH824164)。
作者信息
从属关系
贡献
P.Z.构思了原始研究并监督了数据分析;P.S.K.做了大部分实验;P.D.辅助亚克隆和酶定性实验;T.S.和O.F.进行了LC-MS分析;J.B.A协助进行NMR分析和产品结构验证;P.S.K.和P.Z.撰写了这篇文章,所有作者投稿。所有作者均已阅读并批准本稿件。
通讯作者
道德声明
伦理批准和同意参与
不适用。
同意出版
不适用。
相互竞争的利益
两位作者宣称他们没有相互竞争的利益。
出版商的注意
Springer Nature在发表地图和机构附属机构中的司法管辖权索赔方面仍然是中立的。
附加文件
附加文件1:
数据文件1。本研究使用P450数据库。多克斯(164 kb)
额外的文件2:
表S1。建立的P450候选基因转录本序列列表欧夏至草叶子转录组。(XLSX 79 KB)
额外的文件3:
图S1。NMR分析了labda-13(16),14-dien-9-ol(化合物2)的偶联反应生成MvCPS1和Mv船。(PDF 910 kb)
额外的文件4:
图S2。反应产物的GC-MS分析尼古利亚娜·宾夕法尼亚州co-expression化验的MvCPS1和MvELS的P450候选人Mv1270年,Mv1545年,Mv4213,Mv6504年,Mv3392年,分别。示出的是提取离子色谱(m/Z.二萜化合物9,13-环氧labd-14-烯1、labda-13(16)、14-二烯-9-醇2、未知二萜3,9,13 -环氧labd-14-烯-18-醇4和9,13-环氧labd-14-烯-19-醇5。RNA沉默p19的抑制因子被包括在所有的共表达检测中。(一)Co-expressionMvCPS1,Mv船和Mv的CYP71AU87,(B)的共表达MvCPS1和Mv的ELS,(C-F)的共表达MvCPS1和Mvels与p450Mv1545年,Mv4213,Mv6504年,Mv(G-J)共表达MvCPS1和Mv与ELSMvCYP71AU87和个体P450Mv1545年,Mv4213,Mv6504年,Mv3392年,分别。(K)的表达MvCYP71AU87。(PDF 264 kb)
额外的文件5:
图S3。通过偶联反应形成9,13-环氧-AMD-14-ENE-19-OL(化合物4/5)的NMR分析MvCPS1,Mv船和CYP71AU87。(PDF 1415 kb)
额外的文件6:
图S4。Co-expression的MvCPS1,Mv酵母中ELS和CYP71AU87 (酿酒酵母).示出的是提取离子色谱(m/Z.和共表达的反应产物的质谱MvCPS1,MvELS CYP71AU87,Mv酵母株AM94的CPR与内源性酵母GGPP合成酶BTS1。9,13-环氧labd-14-烯-19-醇2,9,13 -环氧labd-14-烯-18-醇4,9,13 -环氧labd-14-烯-19-醇5,peregrinol(即去磷酸化的peregrinol二磷酸盐)6,未知化合物7,香叶醇(即去磷酸化的GGPP) 8。(PDF 451 kb)
额外的文件7:
图S5。观察到的倍萜的质谱和化学结构N. Benthamiana.共表达检测CYP71AU87底物的杂乱性(见图)。6.).短暂的N. Benthamiana.联合进行共表达测定MvCYP71AU87和Mv具有不同II类ditps的ELS,包括玉米(Zea Mays.)耳鼻喉科cpp合酶Zm评选AN2产生赤霉素前体耳鼻喉科-kaurene(化合物9),从LPP合酶Grindelia Robusta(GRLPPS),以产生manoyl氧化物(化合物10),和一个(+) - CPP合成酶从Isodon得(IR.TPS3),形成咪放射性烯(化合物11)。(PDF 322 kb)
额外的文件8:
图S6。中CYP71AU87产物的LC-MS分析M.大麦树叶和花朵。(A) 12周龄的叶子和花组织M.大麦植物提取量为20% (V./v)乙酸乙酯在正己烷中,然后干燥并在甲醇中重新悬浮。采用Q - Exactive HF质谱联用Vanquish LC系统(Thermo Scientific)对提取物进行LC- ms分析。在Waters Acquity UPLC CSH C上分离体积为5 μl18柱(100 × 2.1 mm;耦合到Acquity UPLC CSH C18VanGuard预柱(5 × 2.1 mm;流速0.6 ml min−1.移动相由A:乙腈:水(60:40,v / v)组成,用甲酸铵(10mM)和甲酸(0.1%)和B:2-丙醇:乙腈(90:10,v / v)甲酸铵(10mM)和甲酸(0.1%)。在下面的梯度下进行15分钟的分离:0min 15%B;0-2分钟30%b;2-2.5分钟48%B; 2.5-11分钟82%B;11-11.5分99%b;11.5-12分钟99%b;12-12.1分钟15%b;12.1-15分钟15%B. Orbitrap MS仪器在电喷雾电离(ESI)中以下列参数在电喷雾电离(ESI)中运行:质量范围60-900 m/Z.;喷淋电压3.6 kV,护套气体(氮气)流量60台;辅助气体(氮气)流量25单位,毛细管温度320°C,全扫描MS1质量分辨能力120,000,数据依赖的MSMS (dd-MSMS)每周期扫描4次,dd-MSMS质量分辨能力30,000。采用Thermo Xcalibur 4.0.27.19进行数据采集和分析。(B) CYP71AU87的结构。(C) CYP71AU87产品在ESI(+) MS模式下可检测到,准确的质量(< 5ppm),保留时间为2.21 min,母代质量为324.2893,与加入铵离子一致(CYP71AU87产品的单同位素质量4/5 = 306.2559)。(PDF 205 kb)
额外的文件9:
表S2。本研究中使用的寡核苷酸。(PDF 111 kb)
权利和权限
开放获取本文根据创意公约署署署的条款分发了4.0国际许可证(http://creativecommons.org/licenses/by/4.0/),它允许在任何媒体上无限制地使用、分发和复制,前提是你给予原作者和来源适当的荣誉,提供一个到知识共享许可协议的链接,并指出是否作出了更改。创作共用及公共领域专用豁免书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条提供的数据,除非另有说明。
关于这篇文章
引用这篇文章
Karunanithi, p.s., Dhanota, P., Addison, J.B.等等。细胞色素P450单加氧酶CYP71AU87的功能特征表明其在药用植物中的marrubiin生物合成中发挥作用欧夏至草.BMC植物杂志19,114(2019)。https://doi.org/10.1186/s12870-019-1702-5
已收到:
公认:
发表:
关键词
- 二萜合酶
- 细胞色素P450单氧酶
- 二萜生物合成
- Marrubiin
- 植物天然产物
- 欧夏至草