- 研究文章
- 开放访问
- 发布:
Oligo-carrageenan Kappa增加葡萄糖,海藻糖和Tor-p,随后刺激参与光合作用的基因的表达,以及基础和次生代谢蓝桉
BMC植物生物学体积19., 文章编号:258.(2019年)
抽象的
背景
先前的研究表明,低聚角叉菜胶(OC) kappa可以促进植物的生长、光合作用以及参与植物基础代谢和次生代谢的酶的活性桉树球状。然而,OC kappa是否能诱导TOR通路的激活,以及参与光合作用的蛋白编码基因以及基础代谢和次级代谢酶的表达增加,目前尚不清楚。
结果
E. Globulus.用水(对照)或OC kappa 1 mg mL喷洒于叶片上- 1,每周一次,总共四次,栽培17周(总共21周)。经过治疗的树木显示比对照的净光合作用较高,从第3周开始,高度较高,在第9周开始,仍然存在于第21周的差异。此外,处理的树木随着周开始的葡萄糖水平的增加显示1,30周1-3的海藻糖,并在第1-2周的Tor-P水平。另一方面,编码参与光合作用的蛋白质的转录物,以及参与葡萄糖积累,C,N和S同化的酶,以及次级代谢物的合成开始于第3-4周,并在第5-6周,8-11周内含有额外的峰,13-14和17-19。因此,OC Kappa诱导葡萄糖,海藻糖和TOR-P水平的初始增加,其次是振荡的型在光合作用蛋白质编码的转录物水平中,以及基础和次生代谢的表明葡萄糖,海藻糖和扭矩的初始增加-P可以触发基因表达的激活。
结论
OC对番茄幼苗生长的刺激作用E. Globulus.至少部分原因是TOR通路的激活,以及光合作用和基础代谢酶编码蛋白的基因表达增加。
背景
现在众所周知,哺乳动物的生长和发育,线虫酵母,植物和藻类是由雷帕霉素(TOR)的激酶靶标的[1,2,3.].Tor是具有丝氨酸/晶蛋白激酶活性的磷酸肌醇相关激酶(PIK),是TOR途径的关键调节激酶[1,2,4].TOR激酶是一种由n端结构域组成的大蛋白H悬挂式,E延长因子3,调节亚基一个PPA2,TOR1(热)域含有几种热重复的域,其由形成两个的37-47个氨基酸构成α.- 涉及蛋白质 - 蛋白质相互作用的螺线管和螺线管结构[5].与HEAT域相邻,为F说唱,一个TM值;T陷阱(脂肪)在大多数PIK中存在的域,并且参与蛋白质 - 蛋白质相互作用[6].在FAT之后,位于FRB FKBP-Rapamycin-Binding (FRB)域,该域与抑制TOR活性的FKBP12-rapamycin复合物结合[7,8].连续地定位与之相互作用的催化结构域(CD)l十六烷醇与年代EC.13蛋白质8(LST8)调节蛋白[9]和猛禽[10,11].在CD之后,位于对氧化还原敏感并与膜结合的c端FAT域(FATC) [12,13].在哺乳动物中,通过细菌产生的大环内酯雷帕霉素的纳米摩尔浓度抑制Tor激酶Streptomyces Hygroscopicus.[14.].相反,Tor激酶对植物中的雷帕霉素进行了适度敏感[15.,16.].在这方面,已经表明,当FKBP12,脯氨酰异构酶过表达或被人或酵母FKBP12取代时拟南芥蒂利亚纳,Tor激酶对雷帕霉素变敏[17.,18.].
在哺乳动物中,通过对应于大约280kDa的大蛋白质的单个基因编码,其通过Treo 2446,Ser 2448,Ser 2481和Ser1261中的磷酸化激活而受到磷酸化活化的[19.,20.].TOR通路由生长因子、促炎细胞因子、胰岛素、葡萄糖、谷氨酰胺、亮氨酸等氨基酸和脂质激活;后者导致合成代谢反应、细胞分裂和生长的增加[2,21.].在哺乳动物中,TOR激酶可以与蛋白质猛杆,LST8和FKBP12相互作用以形成复杂的TORC1,其对雷帕霉素敏感,并且它也可以与RICTOR,LST8和SIN1相互作用,形成TORC2,这对雷帕霉素不敏感,这对雷帕霉素不敏感,这对雷帕霉素不敏感,这对雷帕霉素不敏感,这对雷帕霉素不敏感,这对雷帕霉素不敏感[22.,23.,24.].TORC1调节合成代谢和分解代谢、细胞增殖和暂时生长之间的平衡,而TORC2调节细胞骨架结构、空间细胞生长、细胞极性和凋亡[24.].现在已经明确确定,Torc1由小GTP酶活激活,例如RHEB和RAG,结合TOR的催化位点和LST8 [2]这些GTP酶可以通过激素,生长因子,葡萄糖和一些氨基酸激活[2].
在植物中,TOR是由一个对胚胎后期发育至关重要的单一基因编码的[25.[对应于约250kDa的蛋白质,在其氨基酸序列中与人体转矩相同的39%[2,3.].抗体抗人Tor-P Ser2448识别Ser2424中的磷酸化TOR(TOR-P)拟南芥tor [3.,26.,27.].在植物中,由蔗糖,葡萄糖和果糖喂养激活Tor [28.,29.,30.,31.].此外,葡萄糖在植物中迅速转化为葡萄糖-6-p(g6p)和葡萄糖-1-p(g1p)[31.].此外,海藻糖6-P是海藻糖的前体,T6P的增加导致海藻糖的增加,增强了水稻对非生物胁迫的耐受性[32.].此外,已经证明G1P,G6P和T6P以及核糖6P直接抑制SNRK1 [33.,34.,35.,36.),一种使RAPTOR磷酸化抑制TOR活性的激酶[11].因此,葡萄糖的增加可能导致G1P、G6P和T6P的增加,从而抑制SnRK1激活TOR激酶和TOR通路。最近有研究表明,生长素激活细胞表面的ABP1-TMK生长素感应复合物,进而激活ROP2 GTPase [37.]并且ROP2的激活导致激活TOR,反过来激活S6K和翻译[27.].因此,TOR和SnRK1是能够感知细胞营养状况的激酶,SnRK1对TOR激酶具有拮抗作用。
研究表明,TOR通路在A. Thaliana.导致在合成代谢反应中参与的编码酶的基因表达增加,例如与蛋白质,氨基酸,RNA,DNA和细胞壁相关的那些,以及参与糖酵解的酶的合成,TCA循环和线粒体蛋白质电子传输链[16.,30.,38.].此外,已经表明,使用替代激酶AZD8055的抑制剂的抑制Tar途径导致编码参与光合作用,叶绿素合成和C同化的蛋白质的转录物的减少[39.,40表示Tor途径的激活导致增加光合作用和基础代谢。此外,对蛋白质,氨基酸和脂质合成中参与蛋白质,氨基酸和脂质合成的分解代谢酶的基因表达的激活,以及与淀粉降解,自噬和乙酰甲酸酯循环有关的那些表达。30.].此外,TOR通路的激活也增加了参与次级代谢和防御反应的酶的编码基因的表达,如合成硫代葡萄糖苷的酶[30.].类似地,Tor途径介导苯丙醇丙烷化合物(PPC)和葡萄糖苷水平的增加A. Thaliana.[38.].从这个意义上讲,它已经在酵母中显示,Tor-p可以进入细胞核并结合RNA聚合酶II,导致基因表达的激活[41.].
海藻藻渣 - 角叉菜胶(OCS)增强陆地植物的生长和防御反应[42.,43.,44.].由纯卡拉胶kappa、lambda和iota经酸水解分别得到OCs kappa、lambda和iota,其DP = 20-25 [42.].最初确定ocsκ,λ和iota以1mg ml的浓度施用在植物叶上- 1,每周一次,总共四次,介导在控制条件下培养的烟草植物(Xhanti)中的高度和植物生物质的增加和植物生物质的增加和烟草植物(瓦尔·伯利。伯利。伯利)户外培养四个月[45.].此外,OCs kappa, lambda和iota应用于浓度为1 mg mL- 1,每周一次,总共四次,高度,躯干直径,净光合作用,以及PPC和精油的水平诱导和增加蓝桉在该领域培养三年[46.].另一方面,表明oc kappa介导的还原化合物如NADPH,抗坏血酸(ASC)和谷胱甘肽(GSH)的增加,以及硫氧酮还原酶和硫昔单蛋白的活性增加E. Globulus.树木在户外栽培四个月。此外,癌症增加酶活性涉及基础代谢,C,N和S同化,嘌呤和嘧啶合成,以及克雷斯循环酶的活性E. Globulus.树(47.].此外,癌症增加了促进生长激素,如环蛋白,赤霉素和细胞因素的水平E. Globulus.树(48.]以及松树[49.].此外,oc kappa增加了挥发性萜烯的数量,以及具有潜在的抗致病活动的新萜烯E. Globulus.树(50.].因此,OCκAPA介导净光合作用,基础和次生代谢的增加E. Globulus.树木。
为了分析光合作用的增加以及在基础上观察到的基础和次生代谢E. Globulus.经OC处理的树木,其光合作用蛋白和基础代谢和次级代谢酶的编码基因表达增加,葡萄糖水平升高的酶亚单位的编码基因水平,叶绿素合成酶PSII和PSI的蛋白,并对21周的基础代谢和次级代谢酶进行分析。此外,我们还分析了葡萄糖、海藻糖和TOR-P的水平,以确定这些水平的增加是否先于基因表达的增加,从而可能参与了基因表达的刺激。
结果
OC Kappa诱导的葡萄糖和海藻糖水平的增加,其在光合作用和生长增加之前
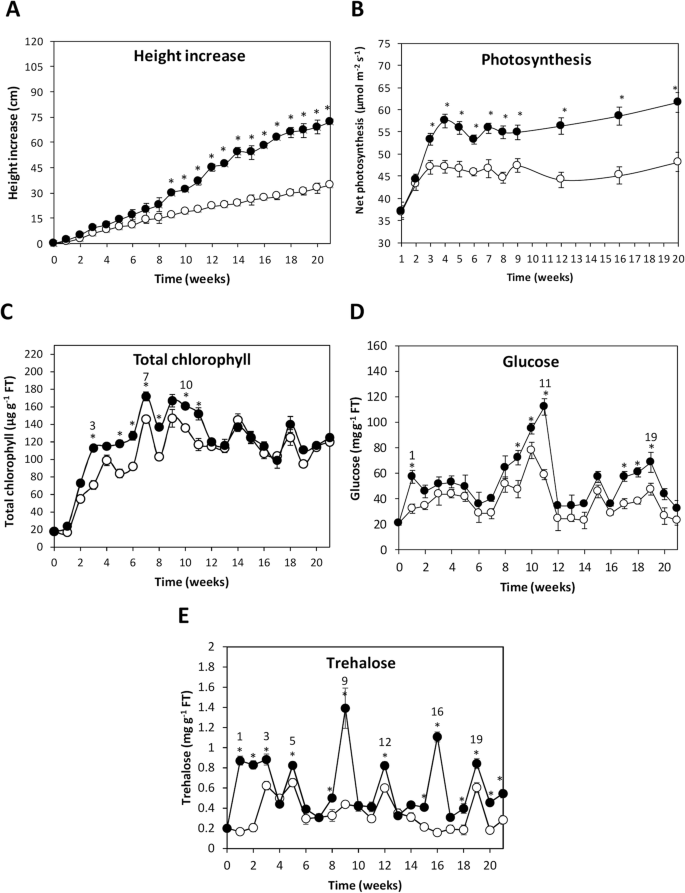
E. Globulus.与OC Kappa治疗的树木与第9周开始的对照相比,高度增加高度增加,并在第21周之前随着时间的时间变得更加明显(图。1一种)。经处理的树木在第21周显示平均高度为72厘米,而控制树显示平均高度为35厘米,表明OC Kappa处理的树木的高度增加105%,相对于对照。此外,用OCκApp治疗的树木在第3周开始呈现净光合作用,其仍然是第21周的第21周,并且比对照更高,33%(图。1b)。此外,在第3周开始的较高水平的总叶绿素和剩余的叶绿素被观察到至第11周的剩余;接下来的一周,总叶绿素的水平降低以达到持续模式的控制水平,直到实验结束(图。1C)。此外,与对照相比,经过普遍的葡萄糖水平均显示出来的树木;这些差异在第1周的第9周和第17页和第17-19周(图。1d)。如果与第1-3,5,8-9,12,15-16和18-21周的最大水平的对照相比,经过处理的树木的趋势较高水平的海藻糖(图。1e)。
ocκA诱导诱导参与葡萄糖积聚的酶的转录物水平
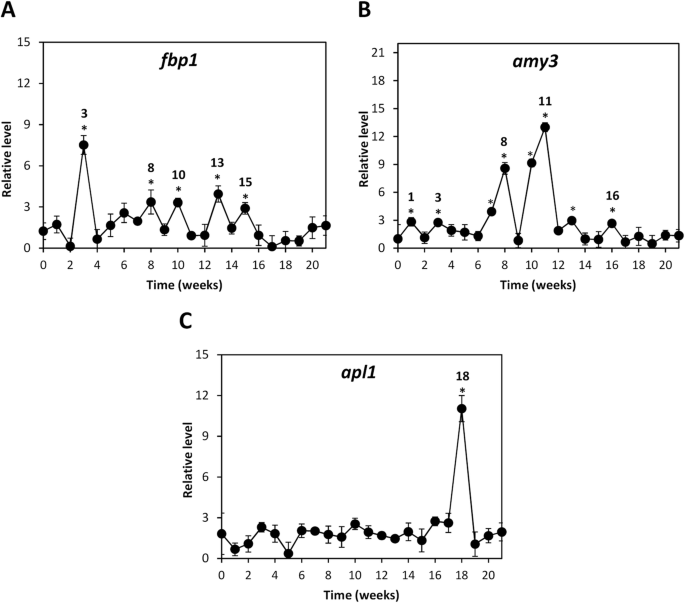
为了分析解释ocκA诱导葡萄糖水平的增加的原因,编码酶果糖-1,6-双磷酸酶参与葡萄糖合成的转录物的程度,fbp1;α-淀粉酶3参与淀粉降解和葡萄糖的生产,amy3;和Adp-葡萄糖酸化酶参与淀粉合成和葡萄糖积累,APL1被检测到。经OC - kappa处理的乔木,叶绿素含量显著增加fbp1在第3,6,8,10,13和15周的转录物相对于对照组(图。2一种)。转录水平amy3与对照组相比,在第1、3、7-8、10-12和16周达到峰值;峰值在第7周和第11周最高。2b)。Apl1转录物仅在第18周增加(图。2C)。
oc kappa引起的tor-p水平增加
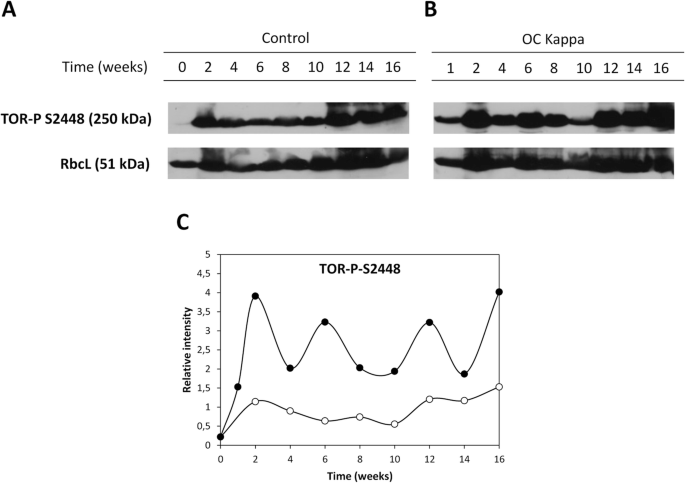
为了分析葡萄糖和/或海藻糖的增加是否可以诱导TOR激酶的活化,在SER2448(TOR-P)中磷酸化的TOR磷酸化水平以及酶核苷酸-1的大亚基(RBCL)的水平使用特异性抗体检测5-二磷酸羧酶/氧酶(Rubisco)(图。3.一种)。使用RBCL的水平标准化有源TOR的水平(图。3.b). OC kappa处理的树木在第1周至试验结束(第21周)表现出较高的TOR-P相对水平,并在第1、2、6、12和16周有所增加(图2)。3.a - c)。
OC - kappa诱导了参与光系统和叶绿素合成的转录本编码蛋白水平的增加
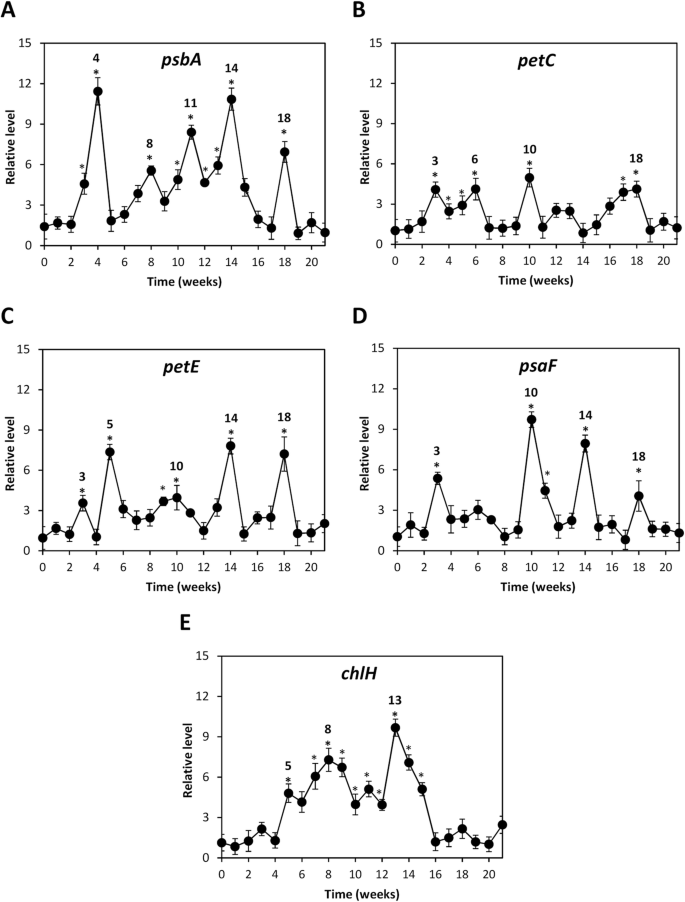
为了分析解释净光合作用增加的原因,编码照相(PS)II的亚基的转录物的水平(PS)II,PSBA.;细胞色素B6F的Rieske亚基,petC;Plastocyanin,皮特;PSI的亚基,PSAF.;和酶参与叶绿素合成的酶镁螯合酶,CHLH.,分析了。用OC Kappa治疗的树木表现出显着增加的水平PSBA.3-4周、8周、10-14周和18周的成绩单(图4)4一种)。峰值petC观察到表达在3-6,10和17-18周内显着(图。4故选c皮特转录物在第3周3,5,9-10,14和18周(图。4C)。表达式PSAF.在第3周、10-11周、14周和18周显著升高。4d)。最后,CHLH.从第5周到第15周,转录本显著增加(图5)。4e)。
OC Kappa诱导的增加涉及基础代谢酶的转录物水平的增加
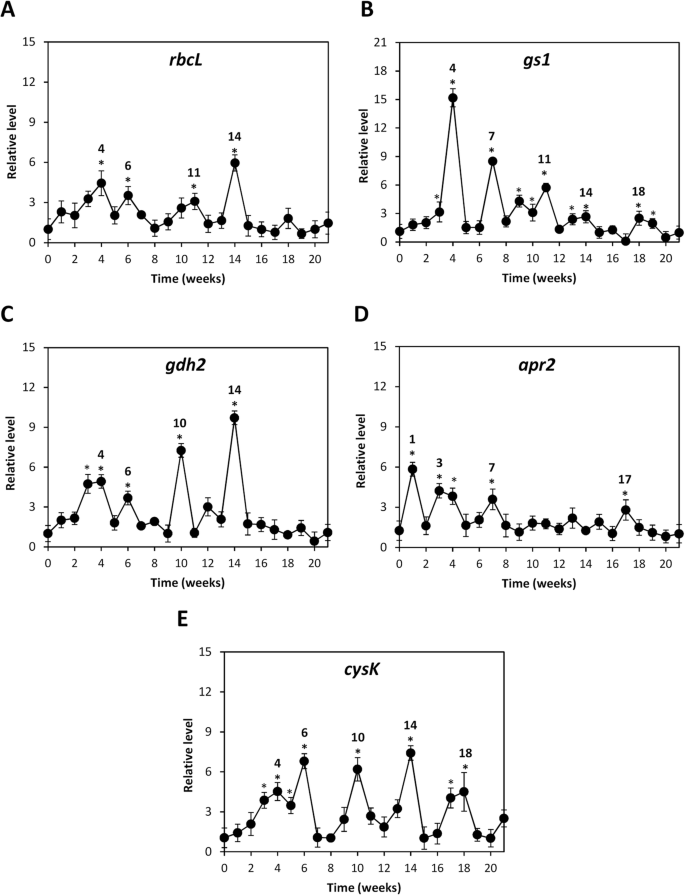
为了分析前人研究中涉及C、N、S同化的酶活性增加的原因,研究了编码C同化的酶rubisco大亚基的转录水平,rbcl.;谷氨酰胺合成酶(GlnS)参与N同化,GS1.;参与N同化的酶谷氨酸脱氢酶(GDH),GDH2.;5 ' -腺苷酰硫酸盐还原酶(APR)参与S同化,4月,以及涉及S同化的酶O-乙酰丝氨酸硫醇酶(O-ASTL),Cysk.被检测到。处理后的树木在rbcl.在第4,6,11,11和14周的转录物(图。5a),在GS1.在第3-4,7,9-11,13-14和18-19周(图。5b),在GDH2.第3-4周、第6周、第10周和第14周。5c),4月第1、3-4、7和17周。5d)和Cysk.在第3-6,10,14和17-18周(图。5e)。
OC kappa诱导参与次级代谢的转录酶的水平增加
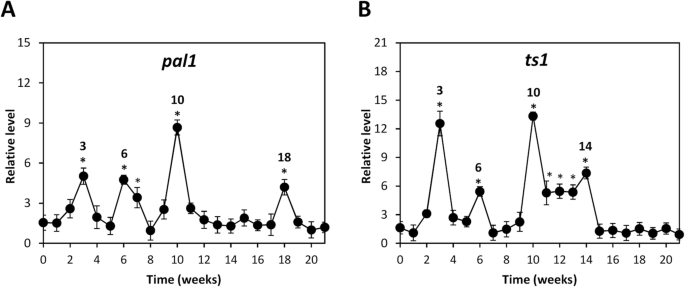
为了分析ocκA诱导的PPC和Terpens增加并在以前的作品中报道的原因,编码PPCS合成的酶苯丙氨酸氨酶(PAL)的转录物水平,朋友,以及涉及萜烯合成的酶萜烯合成酶,TS1,分析了。用OC Kappa治疗的树木表现出增加PAL1数周3,6-7,10和18的转录物(图。6a),还有TS1在第3,6和10-14周的转录物(图。6b)。
讨论
oc kappa诱导葡萄糖,海藻糖和活性Tor-p水平的增加在光合作用和生长的增加之前
在这项工作中,我们展示了治疗桉树与OC Kappa的树木在第1周,第1-2周的第1-3周的海藻糖和Tor-P周期诱导葡萄糖水平初始增加。从这个意义上讲,已经表明葡萄糖和果糖的增加导致G6P和G1P水平的增加[31.]以及植物中的T6P水平[51.].此外,海藻糖的增加反映了水稻中海藻糖合成中间体T6P的增加[32.].此外,显示G1P,G6P和T6P直接抑制SNRK1,抑制TOR的激酶[36.]通过猛烈磷酸化[11].因此,葡萄糖和海藻糖的增加在桉树树木可能导致抑制SnrK1的G1P、G6P和T6P的增加[36.]并导致Tor-P的增加和Tor途径的激活。
此外,OC kappa在第1 - 3周诱导了参与葡萄糖生产的转录酶编码酶(如F16BP和淀粉酶)水平的增加,这解释了第1天观察到的葡萄糖水平的增加。在第9-11周和17-19周观察到葡萄糖水平增加,在第8-9、12、15-16和18-21周海藻糖水平增加,在第7-8周、10-11和13-16周葡萄糖生成酶水平增加。后者表明,在第9-11周和第17-19周观察到的葡萄糖水平升高可能是由于,至少部分地,产生葡萄糖的酶的转录水平升高。另一方面,净光合作用在第3周比第9周增加,这表明光合作用的最初增加可能有助于促进生长E. Globulus.树木。此外,第1-2周内葡萄糖和活性Tor-P的增加在第3周之前的光合作用增加表明,光合作用的转录物的增加可能是由于TOR途径的激活。从这个意义上证明,使用AZD8055使用AZD8055的TOR途径抑制导致编码光学系统亚基的转录物水平和叶绿素合成的酶的转录物水平降低拟南芥[39.表示TOR激酶参与基因表达的激活。从这个意义上讲,它已经在酵母中显示,Tor-p可以进入细胞核并结合RNA聚合酶II,导致基因表达的激活[40].因此。Tor-P也可以进入植物中的细胞核中,允许增加参与光合作用和基础代谢的基因的表达导致刺激生长。
重要的是要提到这一点E.GloBular.植物用50分μ.雷帕霉素或250μ.M AZ8055,它们没有显示出生长抑制(数据未显示),但相反,与对照相比,它们显示出高度。最后,桉树树木可能具有独立无关的控制增长的替代途径。从这个意义上说,它已被展示A. Thaliana.Tor激活抑制自噬。然而,存在替代的独立途径,其通过氧化应激和内质网应力激活,也抑制自噬[52.].因此,桉树树木可以提出一种独立的替代途径,其也可以刺激生长。
OC kappa诱导的光系统和叶绿素合成的转录本编码蛋白水平呈振荡模式增加
之前已经表明了E. Globulus.处理4个月后,净光合作用持续增加[47.].在这里,我们表明,OC Kappa增强了编码光合作用蛋白质的转录物的水平。因此,观察到净光合作用的持续增加E. Globulus.树木至少部分是由于基因表达的增加。此外,在第3-11周观察到的OC Kappa诱导和增加的总叶绿素,并且随着镁切酶的表达,叶绿素合成中的关键酶的较高表达,这增加了叶绿素合成中的重叠,这在第5-15周增加。因此,参与叶绿素合成的基因表达的增加可以部分地负责总叶绿素的增加。重要的是要提到编码PS蛋白的转录物的增加显示出在3-4,5-8,10,14和18周的峰值的振荡图案,因为它被观察到编码产生葡萄糖的酶的转录物。从这个意义上讲,已经显示在动物电池中,即TORC1活性由昼夜时钟控制,并且在植物中可能发生类似的机制[3.].然而,在这项工作中观察到的转录物水平的振荡不是昼夜数周的。因此,可以不同的机制是控制沿着周数观察到的增强的表达,这些表达可以对应于与昼夜钟表不同的“一周时钟”,这涉及刺激光合作用和生长的刺激E. Globulus.树木。
OC Kappa诱导的基础和次级代谢酶的转录物水平的增加,显示振荡图案
以前观察到,用kappa治疗增加涉及C同化,Rubisco的酶活性;在N同化,GLNS和GDH;在S同化,APR和O-ASTL中E. Globulus.[47.].此外,获得的结果大肠gobulus经OC - kappa处理的树木,其PPCs水平增加[46.]以及在挥发性的Terpenes中[50.].在这项工作中,我们确定基础代谢酶的成绩单水平以及参与次级代谢物合成的那些响应于OCκAPA增加。因此,基础和次生代谢的刺激至少部分地归因于基因表达的增加。从这个意义上讲,已经表明,从海洋褐藻的藻酸盐获得的寡核酸馏分与人巨噬细胞的肺状受体4(TLR4)结合,激活途径和促进促炎细胞因子的增殖和表达可能导致刺激免疫反应[53.].因此,有可能E. Globulus.细胞可以具有结合癌症的受体,该受体结合触发TOR途径的激活,导致基础和次级代谢的酶的表达的活化,这可能导致刺激生长和防御反应E. Globulus.树木。
此外,我们表明,OCκAkappa增加了C,N和S同化的基因的表达,其同化呈现振荡模式,在3-4,6-7,10-11,14和17-18周内增加。此外,在第3,5-6,8-11,13-14和17-19周内显示次级代谢,PAL和TP中涉及次生代谢,PAL和TPS的转录物的程度。如前所述,编码基础和次生代谢的酶的转录物水平中的振荡模式可以由不同于植物中的昼夜钟表的“一周时钟”管辖。
结论
oc kappa在第3周开始诱导净光合作用的增加,并在第9周开始随后增加高度E. Globulus.树木。此外,OC Kappa在第1周,第1-3周的第1周,海藻糖诱导葡萄糖水平的初始增加,并在第1-2周的Tor-P.此外,OC Kappa诱导编码光合作用蛋白的转录物的程度,与叶绿素合成的酶,以及参与C,N和S同化的酶,并与PPCS和Terpenes合成相关,从第3周开始-4。有趣的是,后一种蛋白质的转录物的增加表明,主要在第3周,6,10-1,16和18周观察到的振荡模式。因此,OCκA诱导葡萄糖和海藻糖水平的增加,这可能导致G6P增加和T6P可以抑制SNRK1导致TOR通道的激活。因此,对观察到的病原体的生长和防御刺激E. Globulus.树木至少部分地到期,增加了参与光合作用的基因的表达,以及基础和次生代谢,这些增加可能涉及TOR途径的激活。
方法
植物培养,用OC Kappa治疗和高度测量
E. Globulus.这些树是由Semillas Imperial S.A.(洛杉矶,智利)生产的种子获得的。初始高度约为30厘米的植物(N.= 10,每个对照和处理组)用水(对照组)或5毫升含1 mg mL OC kappa的水溶液喷洒在叶子上- 1一旦在每周开始,总共四次,在2015年春季和夏季含有堆肥土壤的塑料袋,植物袋中含有17周的塑料袋。叶(10g)是从控制和经处理的树木的中高部分获得每次治疗后一天,同时在当天(早上11小时),分为三个样本(N. = 3) and frozen in liquid nitrogen for further analyses. The height ofE. Globulus.使用测量胶带确定树木。
定量光合作用
在每个控制和处理的五叶中检测到净光合作用并进行治疗E. Globulus.植物(N. = 10) using a portable infrared gas analyzer Ciras-1 (PP systems, Hitchin, UK), a leaf cuvette of 12. 5 cm2使用红色/白色LED光源,光子辐照度为1000μmolQuanta M.- 2 s- 1光合活性辐射(PAR),CO2浓度为500ppm,相对湿度为70%,24°C保存1分钟。
总叶绿素的定量
量化的叶绿素一种和B.如[54.].将新鲜的叶子(0.1g)在液氮中冷冻并用杵在砂浆中均化。加入一毫升丙酮,将混合物在4℃温育90分钟。使用微离心机将混合物以14.000rpm离心5分钟。回收上清液,使用Hewlett Packard / Agilent分光光度计模型8453(Santa Clara,CA,USA),在665和649nm处测定的吸光度。通过添加叶绿素计算总叶绿素一种和B.使用以下公式计算叶绿素的浓度:
葡萄糖的量化
将新鲜的叶子(0.1g)在液氮中冷冻并在砂浆中均化。加入五百μL蒸馏水,并将混合物以14.000rpm离心5分钟。回收上清液,将等分试样为30μl加入到500μl葡萄糖氧化酶/过氧化物酶试剂酶试剂酶反应混合物(Valtek诊断,Santiago,智利)中。在505nm处测定吸光度,使用使用0.2至2mg mL的浓度的葡萄糖制备的校准曲线计算浓度- 1.
量化海藻糖
如[1中所述)进行海藻糖的定量。55.].将新鲜的叶子(0.1g)在液氮中冷冻并在砂浆中均化。加入两种乙醇;将混合物煮沸1小时,将乙醇在烘箱中在60°蒸发。加入5ml 5mM硫酸,将混合物以3.200rpm离心10分钟。将上清液通过0.2μm孔隙PDVF过滤器过滤,并在水中煮沸1小时以水解蔗糖。冷,用氢氧化钠中和pH,蒸发溶液,将残余物溶于蒸馏水中。通过HPLC(Agilent 1100,Ca,USA)分析20μl的样品,糖包1柱(300mm×6.5mm,水杂志,MA,USA),在75℃下,并在55处耦合到折射率检测器 °C. The isocratic elution program consists of 40 min with a mobile phase 0.1% EDTA-calcium and a flux of 0.35 mL min-1 using a pressure of 38 bars. The calibration curve was prepared using trehalose at concentrations ranging 0 to 5 mg mL- 1.
蛋白质提取物的制备
蛋白质提取物的制备方法见[56.].将新鲜的叶子(1g)用液氮冷冻并在研钵中均化。加入了三毫升萃取缓冲液(0.5M Tris-HCl,0.7M蔗糖,1mM PMSF,50mM EDTA,0.1M KCl和0.2%β-巯基乙醇pH8.0),并在冰上摇动10分钟。加入1mL在pH6-8.0处的苯酚,将混合物在冰上摇动10分钟,并在4℃下以3.200rpm以3.200rpm离心10分钟。回收有机相并将4体积的0.1M乙酸铵混合在甲醇中。使用涡旋摇动混合物,并在-20℃下温育过夜,用于蛋白质沉淀。将混合物在4℃下以3.200rpm离心15分钟,并用乙酸铵在0.1μm的甲醇中用乙酸铵洗涤两次蛋白质沉淀,然后在丙酮中相同的浓度。将沉淀在室温下干燥,并在50mM Tris-HCl pH 8.0中溶解。使用Bradford试剂量化蛋白质,并使用牛血清白蛋白制备校准曲线[57.].
磷酸化的定量(Tor-P)
使用双相变性聚丙烯酰胺凝胶(6%堆叠相和12%分离相)分离蛋白质(5μg),电泳在110V下进行1.5小时。使用瞬发系统(Bio-rad)和400mA在4℃下将蛋白质电转移到硝酸纤维素膜中。通过用Ponceau Red Dye染色膜来验证蛋白质的转移。将膜封闭,用5%脱脂乳溶解在TTBS缓冲液(20mM Tris-HCl pH 7.5,0.1mM NaCl和0.1%吐温20)中,并在室温下用TTB洗涤三次10分钟。将膜与单克隆抗体抗人TOR-P Ser2448一起孵育,其与Ser2424结合在拟南芥TOR (1:1000, Abcam ab109268)或anti-RbcL (1:25 500, Agrisera AS03037) (Schepetelnikov et al., 2013)在室温下1小时。室温下用TTBS洗3次10 min,室温下用HRP标记的二抗抗兔IgG (Agrisera, AS09602)孵育1 h,室温下用TTBS洗3次10 min。将该膜与化学发光底物(SuperSignal West Femto, Thermo Scientific, Rockford, IL, USA)孵育5分钟,然后暴露于x射线胶片(Thermo Scientific, Rockford, IL, USA) 3分钟检测TOR-P ser2448,或30秒检测RbcL。电影中的波段被扫描,然后使用Image Studio软件(Li-Cor, USA)进行量化。
RNA提取
提取总RNA桉树如[58.].将新鲜的叶子(1g)冷冻在液氮中并用杵在砂浆中均化。加入10mL含有100mM Tris-HCl pH 8.0,0.35M山梨糖醇,10%(w / v)聚乙二醇6000和2%(w / v)的β-巯基乙醇的溶液A,并将混合物摇动1分钟。将混合物离心3.500rpm,在4℃下离心15分钟,弃去上清液。将沉淀溶液在含有300mM Tris-HCl pH 8.0,25mM EDTA,2M NaCl,2%(w / v)ctab,0.05%(w / v)固体,2%PVPP和2的溶液B中溶解在10mL溶液B中。%(w / v)β-巯基乙醇;将混合物在65℃加热,并在65℃下孵育10分钟并使用涡旋每2分钟摇动。加入类似体积的氯仿/异戊醇(24:1)的溶液,将混合物在3.200rpm下在4℃下离心10分钟。再萃取水相,用相似体积的氯仿/异戊醇萃取,并在4℃下以3.200rpm离心10分钟。回收水相并通过添加0.1体积为0.3μm乙酸钠,pH5.2和0.6体积的异丙醇沉淀的总RNA;将混合物在-80℃下温育30分钟。 The mixture was centrifuged at 14.000 rpm, at 4 °C, for 20 min, and the supernatant discarded. The pellet was solubilized in 1 mL of nuclease free (DEPC-treated) water and total RNA was precipitated adding 0.3 volumes of 10 M lithium chloride; the mixture was incubated at 4 °C overnight. The mixture was centrifuged at 13.000 rpm, at 4 °C, for 30 min, and the supernatant was discarded. The pellet was solubilized in 0.1 mL of DEPC-treated water and total RNA precipitated adding 0.1 volume of 3 M sodium acetate pH 5.2, and 2 volumes of 70% cold ethanol; the mixture was centrifuged at 13.000 rpm at 4 °C for 20 min, and the supernatant discarded. The pellet was washed with 200 μL of 70% cold ethanol and centrifuged at 13.000 rpm at 4 °C for 10 min, and the supernatant discarded. The pellet was dried at room temperature and solubilized in 50 μL of DEPC-treated water. The concentration and purity of total RNA was determined measuring the absorbance at 260 and 280 nm, and in an agarose gel; RNA was stored at − 80 °C for further gene expression analyses.
通过QRT-PCR定量转录物水平
使用实时热循环仪Rotorgene 6000 (Corbett, Australia)通过qRT-PCR对转录本的相对水平进行定量。参与葡萄糖积累和消耗的转录本:是那些编码果糖-1,6-二磷酸酶1 (fBP1.),葡萄糖合成中的关键酶;A-淀粉酶3(AMY3),是淀粉降解和葡萄糖生产中的重要酶;ADP-葡萄糖PERTOphophorylase 1(APL1),淀粉合成的决定酶。编码光系统蛋白的转录本有:光系统II的亚基A (PSBA.),细胞色素B6F的Rieske亚基(petC),Plastocyanin(皮特),光系统I的亚基A (PSAF.)。编码酶的转录物是镁切酶(CHLH.),叶绿素合成的关键酶;核苷酸-1,5-双磷酸羧酶/氧酶(Rubisco)的大亚基(rbcl.),C同化中的关键酶;谷氨酰胺合成酶(GS1.),一种参与氮同化的酶;谷氨酸脱氢酶(GDH2.),一种参与氮同化的酶;O-乙酰碱硫醇 - 裂解酶(Cysk.),一种涉及S同化的酶;5'-亚甲酰基硫酸盐还原酶(4月),一种涉及S同化的酶;苯丙氨酸氨酶1(PAL1),苯基丙酸途径的关键酶;和萜烯合酶1 (TS1),一种参与萜烯合成的酶。RNA 18S被用作内脏转录物,其水平在对照或治疗植物中的数周内没有变化(数据未显示)。PCR引物列于附加文件中1:表S1。使用Sensimix单步试剂盒(量子,英国),75ng总RNA,200nm底漆溶液和3mM氯化镁进行QRT-PCR反应。来自三个独立重复的相对转录水平表示为2-ΔΔct[59.].为此,减去对照样品的平均值,以确定处理样品的平均值以确定表达的折叠变化。
统计分析
在评估正态性和方差齐性要求之前,对数据进行单因素方差分析(ANOVA)和事后Tukey检验。在95%的置信区间内,通过3个独立的重复估计显著差异。
可用性数据和材料
所有实验数据都在线存储库中提供:https://figshare.com/s/1bd228e7ab5bdbc6427c
缩写
- chlh:
-
镁螯合酶
- Cysk:
-
O-乙酰碱硫醇 - 裂解酶
- GDH2:
-
谷氨酸脱氢酶
- gs1:
-
谷氨酰胺合成酶
- PAL1:
-
苯丙氨酸氨酶1
- 宠物:
-
rieske细胞色素B6F的亚基
- 皮特:
-
Plastocyanin
- PSAF:
-
光系统I的亚基A
- PSBA:
-
Subunit A的照片II
- SNRK1:
-
SNF-1相关激酶1
- TOR:
-
雷帕霉素的目标
- TS1:
-
萜烯合酶1
- apr2:
-
5'-亚丁酰基硫酸盐还原酶
- RBCL:
-
核苷酸 - 1,5-双磷酸羧酶/氧酶(Rubisco)的大亚基
参考
- 1.
Xiong Y,Sheen J.在Tor Plant Kinase信号通信网络中的新颖联系。CurrOp植物BIOL。2015; 28:83-91。
- 2。
Dobrenel T,Caldana C,Hanson J,Robaglia C,Vincent M,VEIT B等。Tor信号和营养传感。Annu Rev植物Biol。2016; 67:21-4。
- 3.
Schepetilnikov M,Ryabova La。最近关于TOR(雷帕霉素)信号传导在植物翻译中的作用的发现。植物理性。2018; 176:1095-105。
- 4.
熊艳艳,陈志强。植物中雷帕霉素(TOR)信号通路的研究进展。J Biol Chem. 2012; 287:2836-42。
- 5。
克努森巴。雷帕霉素靶点结构和结构的深入研究。J Struct Biol. 2010; 170:354-63。
- 6。
Bosotti R,Isacchi A,Sonhammer El。脂肪:PIK相关激酶中的一个新型域。趋势Biochem SCI。2000; 25:225-7。
- 7。
Banaszynski La,Liu CW,Wandless TJ。FKBP.Rapamycin的表征。三元复合体。J am Chem Soc。2005; 127:4715-21。
- 8.
Rodríguez-Camargo DC,Link NM,Dames SA。人体TOR的FKBP12-雷帕霉素结合结构域在具有和没有调节剂磷脂酸的情况下发生膜模拟物存在的强大构象变化。生物化学。2012; 51:4909-21。
- 9.
Moreau M,Azoppardi M,ClémentG,Dobrenel T,Marchive C,Renne C,等。突变在拟南芥同族体LST8 / GβL,雷帕霉素激酶靶标的伴侣,植物生长,开花和代谢适应较长的日子。植物细胞。2012; 24:463-81。
- 10.
Mahfouz MM, Kim S, Delaunay AJ, Verma DP。拟南芥RAPAMYCIN的靶点与RAPTOR相互作用,RAPTOR调节渗透胁迫信号中S6激酶的活性。植物细胞。2006;18:477 - 90。
- 11.
Nukarinen E,HägeleT,Pedrotti L,Wurzinger B,Mair A,Landgraf R等。定量磷蛋白酶揭示了AMPK植物OrthologSnRK1作为能量剥夺下代谢母稳压器的作用。SCI批准。2016; 6:31697。
- 12.
Takahashi T,Hara K,Inoue H,Kawa Y,Tokunawa C,Haydat S,等。与MTOR功能不可缺少的骨碘化物 - 激酶相关激酶中保守的羧基末端区域是必不可少的体内和体外.基因细胞。2000; 5:765-75。
- 13。
萨姆斯sa。雷帕霉素FATC结构域氧化还原诱导靶与膜模拟胶束的结构碱基。J Biol Chem。2010; 285:7766-76。
- 14。
Crespo JL,Díaz-Troya S,Florencio FJ。雷帕霉素在单细胞绿藻中雷帕霉素信号传导的抑制作用Chlamydomonas Reinhardtii..植物理性。2005; 139:1736-49。
- 15.
任敏,邱胜,冯磊,等。雷帕霉素靶蛋白通过激酶结构域调控核糖体RNA的表达和发育拟南芥.植物理性。2011; 155:1367-82。
- 16。
任M,Venglat P,邱S,Feng L,Cao Y,Wang E等人。雷帕霉素信号传导的靶标调节代谢,生长和寿命拟南芥.植物细胞。2012; 24:4850-74。
- 17。
Sormani R,Yao L,Menand B,Ennar N,Lecampion C,Meyer C,等。酿酒酵母酿酒酵母FKBP12绑定拟南芥蒂利亚纳Tor及其在植物中的表达导致雷帕霉素易感性。BMC植物BIOL。2007; 7:26。
- 18。
Xiong Y,Sheen J. ratemcin信号网络在植物生长和新陈代谢中的作用。植物理性。2014; 164:499-512。
- 19.
清亚伯拉罕德·伯拉姆SER-2448在SER-2448的哺乳动物哺乳动物靶标磷酸化由P70S6激酶介导。J Biol Chem。2005; 280:25485-90。
- 20。
Acosta-Jaquez HA,Keller Ja,Foster Kg,Ekim B,Soliman Ga,Feener Bp等。特异性MTOR磷酸化促进MTORC1介导的信号传导和细胞生长。Mol细胞Biol。2009; 29:4308-24。
- 21.
Jewell JL,Kim YC,Russell Rc,Yu FX,Park HW,Plouffe Sw,等。亮氨酸和谷氨酰胺的MTORC1差异调节。科学。2015; 347:194-8。
- 22.
Sarbassov DD,Ali Sm,Kim DH,Guertin Da,Latek Rr,Erdjument-Bromage H等。Rictor是一种新型MTOR的结合伴侣,定义了调节细胞骨架的雷帕霉素不敏感和无关的途径。Curr Biol。2004; 14:1296-302。
- 23.
Sarbassov DD, Guertin DA, Ali SM, Sabatini DM. rictor mTOR复合物磷酸化和调控Akt/PKB。科学。2005;307:1098 - 101。
- 24。
伍尔施莱格S,洛维斯R,霍尔MN。TOR信号在生长和代谢中的作用。细胞。2006;124:471 - 84。
- 25。
Menand T,Desnos T,Nussaume L,Berger F,Bouchez D,Meyer C等人。表达和破坏的拟南芥tor(雷帕霉素的靶标)基因。Proc Natl Acad Sci U S A. 2002; 99:6422-7。
- 26。
Schepetilnikov M,Dimitrova M,Mancera-Martíneze,Geldreich A,Keller M,Ryabova La。Tor和S6K1通过Eief3h的磷酸化促进含有mRNA的U-ORF的翻译重新启动。2013年EMBO J.22:1087-102。
- 27。
Schepetilnikov M,Makararir J,Srour O,Geldreich A,Yang Z,Chicher J等人。GTPase ROP2响应于蟾蜍蛋白结合并促进雷帕霉素,TOR的靶标的激活。2017年EMBO J.26:886-903。
- 28。
Schluepmann H,Van Dijken A,Aghdasi M,Wobbes B,Paul M,Smeekens S.海藻糖调解生长抑制拟南芥幼苗是由于海藻糖-6-磷酸盐积累。植物理性。2004; 135:879-90。
- 29。
Lunn Je,Feil R,Henfriks JHM,Gibon Y,Morcuende R,Osuna D等人。海藻糖6-磷酸盐的糖诱导的增加与氧化还原活化的ADP-葡萄糖焦磷酸化酶和淀粉合成速率较高的速率相关。拟南芥蒂利亚纳.j . 2006; 397:139-48。
- 30.
Xiong Y,McCormack L,Li L,Hall K,Xiang C,Sheen J.Glc-Tor信号导致转录组重新编程和分生激活。自然。2013; 496:181-6。
- 31。
亚达夫UP, Ivakov A, Feil R, Duan GY, Walther D, Giavalisco P,等。蔗糖-海藻糖6-磷酸(Tre6P)联结:Tre6P信号转导蔗糖的特异性和机制。J Exp Bot. 2014; 65:1051-68。
- 32。
李鹤,张女士,邓XW,王XP。海藻糖-6-磷酸合酶基因OSTPS1的过表达增强了水稻中的非生物胁迫耐受性。Planta。2011; 234:1007-18。
- 33.
张勇,Primavesi LF, Jhurrea D, Androlojc PJ, Mitchell RA, Powers SJ。通过海藻糖-6-磷酸抑制snf1相关蛋白激酶1的活性和调节代谢途径。植物杂志。2009;149:1860 - 71。
- 34.
Schluepmannh,贝尔克L,桑切斯佩兹佩斯。新陈代谢控制增长:在植物中的海藻糖-6-苯二甲酸分子。J Exp Bot。2012; 63:3379-90。
- 35.
Piatonni CV, Bustos DM, Guerrero SA, Iglesias A.非磷酸化甘油醛3-磷酸脱氢酶在小麦胚乳ser-404位点被snf -1相关蛋白激酶变构抑制。植物杂志。2011;156:1337-50。
- 36。
Nunes C,Primavesi LF,Patel Mk,Martínez-Barajas E,Powers SJ,Sagar R等人。代谢物抑制SNRK1:组织依赖性效果和葡萄糖1-磷酸盐与海藻糖6-磷酸盐的合作抑制。植物理性生物化学。2013; 63:89-98。
- 37。
徐涛,戴宁,陈建军,曹敏,李华,等。细胞表面ABP1-TMK生长素感知复合物激活ROP GTPases信号。科学。2010;343:1025-8。
- 38。
张丽,李永强,张丽,等。对雷帕霉素诱导靶点的系统分析揭示了控制生长的一般代谢开关拟南芥蒂利亚纳.工厂J. 2013; 73:897-9。
- 39。
MONTANE MH,Menand B. ATP竞争性MTOR激酶通过触发半分化的分解细胞但不是发育模式改变来延迟植物生长。J Exp Bot。2013; 64:4361-74。
- 40。
Dong P,Xiong F,Que Y,Wang K,Yu L,Li Z.表达分析和功能分析表明,Tor是调节光合作用和植物激素信号传导途径的关键球员拟南芥.前植物SCI。2015; 6:677。
- 41。
利用TOR激酶直接结合RNA聚合酶ii转录基因的研究。咕咕叫麝猫》2017。https://doi.org/10.1007/S00294-017-0738Z..
- 42。
Vera J,Castro J,GonzálezA,Moenne A.海藻多糖和衍生的寡糖刺激防御反应和对植物病原体的保护。火药。2011; 9:2514-25。
- 43。
González A, Castro J, Vera J, Moenne A.海藻寡糖通过促进碳氮同化、基础代谢和细胞分裂促进植物生长。植物生长调节剂。2013;32:443-8。
- 44。
Moenne A. Marine藻类Oligo-carrageenans(OCS)刺激陆地植物中的生长和防御反应。在:寡糖中的研究进展。美国:Springer;2016年。
- 45.
Castro J,Vera J,GonzálezA,Moenne A.寡鹿乐蛋白患者通过增强烟草植物中的光合作用,基础代谢和细胞周期来刺激生长(瓦莱。J工厂增长调节。2012; 31:173-85。
- 46.
GonzálezA,Contreras Ra,Moenne A.寡核菜蛋白酶增强纤维素,精油和多酚化合物的生长和含量蓝桉树木。分子。2013; 18:8740-51。
- 47.
González A, Moenne F, Gómez M, Sáez CA, Contreras RA, Moenne A桉树树木。前植物SCI。2014; 5:512。
- 48。
González A, Contreras RA, Zuñiga G, Moenne A.寡聚卡拉胶kappa诱导TRR/TRX体系的还原氧化还原状态和激活增加了吲哚-3-乙酸、赤霉素A3和反式玉米素在蓝桉树木。分子。2014; 19:12690-8。
- 49。
低聚角叉菜胶能提高油菜C、N、S同化、生长素和赤霉素含量,促进油菜生长Pinus Radiata.树木。J Forest Res。2015; 26:635-40。
- 50。
GonzálezA,Gutierrez-CutiñoM,Moenne A. Oligo-carrageenan kappa-诱导还原氧化还原状态和TRR / TRX活动的增加促进了Terpenoid代谢的激活和重新编程桉树树木。分子。2014; 19:7356-67。
- 51。
糖是如何调节植物生长发育的?对海藻糖-6-磷酸作用的新认识。摩尔。2013;6:261 - 74。
- 52。
pu y,罗x,bassham dc。TOR依赖性和依赖性途径调节自噬拟南芥蒂利亚纳.前植物SCI。2017; 8:1204。
- 53。
方武,毕丁,郑河,蔡n,徐H,周r等人。通过藻酸盐衍生的铜酸酯寡糖在Raw264.7巨噬细胞中鉴定和激活TLR4介导的信号通路。SCI批准。2017; 7:1663。
- 54。
总类胡萝卜素和叶绿素的测定一种和B.不同溶剂中的叶子提取物。Biochem Soc Trans。1983; 11:591-2。
- 55。
艾哈迈德,yousef ea,kord ma,quaid ea。小麦植物中的海藻糖累积促进蔗糖和淀粉生物合成。jord j biol sci。2013; 6:143-50。
- 56。
王志强,王志强,王志强,等。植物组织蛋白质组学研究中的苯酚提取方法。见:植物蛋白质组学、方法与协议。美国:胡玛纳出版社;2013.
- 57.
布拉德福德mm。利用蛋白质染料结合原理的微克数量蛋白质量化的快速敏感方法。肛门生物化学。1983; 72:248-54。
- 58.
Morante-Carriel J,Sellés-Marchart S,Martínez-MárquezA,Martínez-estesoMJ,Luque I,Bru-MartínezR.RNArna隔离枇杷和其他顽抗木质植物,具有高质量和产量。肛门生物化学。2014; 452:46-53。
- 59.
Livak KJ,Schmittgen TD。使用实时定量PCR和2的相对基因表达数据分析(-Delta delta c(t))。方法方法。2001; 25:402-8。
资金
这项工作由Sirius Natura S.A.和Vridei-Usach提供资金。Silvia Sauceo由Senecyt-Ecuador,Concocatoria 2011提供资金。
作者信息
隶属关系
贡献
SS分析身高,葡萄糖,叶绿素和转录水平,AG分析光合作用,MG, RAC, GZ分析海藻糖,SS, DL, CA和AM分析数据,AM写手稿。所有作者阅读并批准了最终的手稿。
通讯作者
伦理宣言
伦理批准和同意参与
不适用
同意出版物
不适用
相互竞争的利益
提交人声明他们没有竞争利益。
附加信息
出版商的注意事项
施普林格《自然》杂志对已出版的地图和机构附属机构的管辖权要求保持中立。
附加文件
额外的文件1:
表S1。用于扩增来自参与葡萄糖合成的转录物的转录物的引物,所述蛋白质参与QRT-PCR的光合作用和次生代谢的酶。(DOCX 20 KB)
权利和权限
开放访问本文根据创意公约署署署的条款分发了4.0国际许可证(http://creativecommons.org/licenses/by/4.0/)如果您向原始作者和源给出适当的信用,则允许在任何介质中进行不受限制的使用,分发和再现,提供指向Creative Commons许可证的链接,并指示是否进行了更改。Creative Commons公共领域奉献豁免(http://creativecommons.org/publicdomain/zero/1.0/)除非另有说明,否则适用于本文中提供的数据。
关于这篇文章
引用这篇文章
Sauceo,S.,González,A.,Gómez,M.等等。Oligo-carrageenan Kappa增加葡萄糖,海藻糖和Tor-p,随后刺激参与光合作用的基因的表达,以及基础和次生代谢蓝桉.BMC植物BIOL.19,258(2019)。https://doi.org/10.1186/s12870-019-1858-z
已收到:
接受:
发表:
关键词
- 桉树
- 基因表达
- 葡萄糖
- 生长
- oc kappa.
- 光合作用
- TOR激酶
- 海藻糖