抽象的
背景
干旱胁迫是一种主要的非生物压力,导致农业生产巨大损失。Proso millet(黍miliaceum能有效地适应干旱胁迫,为提高抗旱性提供重要的信息和基因资源。然而,其复杂的干旱响应机制仍不清楚。
结果
在37个核心的中国波尔诺小米中,选择金树6(JS6)作为干旱敏感性试验材料,而Neimi 5(NM5)被选中作为PEG诱导的水胁迫下的耐旱性测试材料。在测序后,在JS6和NM5中观察到1695个差异表达基因(DEG),没有PEG诱导的水分应激(JS6CK和NM5CK)。通过使用20%PEG-6000分别用于6(JS6T6和NM5T6)和24小时(JS6T24和NM5T24),在两种品种下发现了总共833和2166℃。JS6T6和JS6T24处理中的DEG分别比NM5T6和NM5T24高约0.298-和0.754倍。与相应的对照相比,在T6治疗中发现了更多的次数而不是T24治疗。在NM5中观察到ROS清除系统对模拟干旱处理和相对容易恢复光合作用基因表达的转录响应的延迟。与JS6相比,在茉莉酸(JA)的NM5信号转导途径中观察到不同的调节策略。
结论
在peg诱导的水分胁迫下,NM5基因表达保持高度稳定。与干旱敏感品种相比,抗旱品种在JA信号转导途径中的不同调控策略可能是抗旱胁迫的驱动因素之一。
背景
干旱胁迫是一种慢性,随机和不可预测的非生物应激,导致农业作物生产巨大损失[1,2,3.].干旱被认为是严重的粮食短缺和饥荒的主要原因2].目前的统计数据显示,世界农业生产的40%来自灌溉地,而灌溉地占世界蓄水量的70% [4].它仍然是农业生产的主要限制。随着世界人口和全球变暖的增加,由于水资源有限,干旱压力将在未来加剧[5,6,7].因此,为了提高农业生产,必须了解耐旱机制。
小米对干旱、高温和土壤贫瘠的适应能力较好。黍miliaceumL.)是有关抗旱工作的重要[8,9,10].这是一个c4作物和四倍体物种(2 N = 4X = 36) with a short growing season [11].小米是最古老的栽培谷物之一,具有重要的历史意义[12,13]和主要种植作为主食和饲料在中国的半干旱地区[源14,15].它也作为主要作物歉收时的补充作物种植[15].因此,进入干旱耐受机制和ProSo Millet的重要遗传资源的见解将有助于改善其抗旱性和其他作物的遗传资源。
干旱响应机制,包括各种分子,形态和生理反应,帮助植物存活期干旱和保持生产力。植物有形态和生理反应,包括改善根系性状[16],表皮(气孔和角质层)电导降低,蒸发面(叶面积)和辐射吸收减少[3.来应对缺水的情况。激素调节信号转导的复杂网络,以调节和控制植物在无胁迫情况下的生长和在胁迫下生存[3.].当植物经历压力时,第一步是感知环境信号[17].在非生物胁迫,脱落酸(ABA),一种重要的植物激素信号,提供了最快的响应中的一个和触发器随后防御[存在18].它负责调节气孔关闭[19],这是通过植物叶中的气态交换省水的主要方式。响应非生物应激,不同植物激素之间的复杂交叉谈话会导致协同或拮抗作用[20.].ABA和茉莉酸(JA)在调节气孔关闭中发挥了积极作用,而生长素和细胞分裂素则发挥了消极作用[3.,21.].而且,乙烯的作用是由不同的组织在不同的条件下所决定的[3.].
通过调节植物生长和防御反应的平衡,使植物适应变化的条件,JA在压力反应中发挥重要作用22.,23.,24.].水分应激诱导JA积累,以促进抗坏血酸过氧化物酶,单羟基血基酸盐还原酶,谷胱甘肽还原酶,脱氢血液还原酶,抗坏血酸和谷胱甘肽的合成[25.].植物细胞中的抗坏血酸谷胱甘肽循环高度有助于清除活性氧(ROS)[26.].这个循环在需要ROS解毒的所有细胞器中工作[27.,28.].根据Bartoli等人[29.[抗坏血酸的丰度是调节细胞氧化还原缓冲能力的调节,其影响激活激素信号的阈值和不同激素之间的相互作用。此外,Applatic抗坏血酸酯有助于缓解来自应力的增强的氧化负担,并且是对潜在损害外部氧化剂的第一行防御[30.].
在正常情况下,ROS是需氧代谢过程的必然产物[31.,32.,33.],包括光合作用和呼吸作用;活性氧水平通常较低,可以严格控制[26.].然而,水胁迫会破坏细胞稳态并增加ROS生产,从而引发特异性氧化反应[26.].在压力下,ROS是信号级联的次要信使,其传达了重要信息,以调节浓度和/或敏感性的激素变化,以激活下游应力响应和防御过程[29.].然而,活性氧在干旱胁迫下过量生成[31.,32.,33.]并且可以氧化关键细胞组分并引起氧化细胞破坏[28.,34.].此外,ROS的过度处理对蛋白质,膜和DNA致命,并且可以引起细胞死亡[35.,36.,37.]超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、抗坏血酸、谷胱甘肽和过氧化物酶(POD)也参与各种防御反应[2,38.],并在生物和非生物胁迫下的活性氧清除中发挥关键作用[39.].
在干旱条件下,基因调节与渗透保护剂相关的途径,直接保护重要的蛋白质和膜[40].不利条件可诱导膜转运的有关水和离子的摄取[响应和离子通道41.].这些不利条件可诱导相关转录因子调控下游应激相关基因以应对水分胁迫[2].基因组信息的掌握对于了解抗旱性的分子机制和提供重要的基因资源至关重要。近年来,RNA测序(RNA-seq)被广泛应用于各种植物中,被证明是获取转录组数据的一种高效方法[42.,43.,44.].然而,以前关于ProSo Mill的耐旱性的研究主要集中在其形态和生理反应中[45.].近年来,一些研究[13,45.报道了Proso Millet的转录组特征。然而,通过分子水平变化的叶响应和适应性的叶片反应和适应的机制仍不清楚,特别是在不同的耐旱品种中。
在本研究中,进一步阐明黍叶对干旱胁迫和耐旱品种的耐旱性机制反应的分子基础,我们选择了干旱敏感和耐旱品种。基于RNA-seq的数据他们的转录组分析。我们的研究结果提供的信息可以帮助提高我们的分子机制耐旱基本的了解。此外,这项研究提供了重要的基因资源,改善稷等作物的耐受性。
结果
原谷子品种抗旱性评价
37个品种中,对照组的平均发芽率约为92.3%,最高发芽率为99.0,最低发芽率为74.0%。模拟干旱处理组的平均发芽率为72.9%,最高和最低发芽率分别为92.3和43.0%。平均相对发芽率为79.0%,最高和最低的相对发芽率分别为101.6和46.6%1:表S2)。对照组的发芽率超过95%,模拟干旱处理组的最高和最低相对发芽率分别为96.9%和48.6%。在这些品种中,内米5号和金薯6号(分别更名为NM5和JS6)分别作为耐旱性和耐旱性试验材料进行后续分析。
peg诱导水分胁迫下NM5和JS6丙二醛(MDA)含量的差异
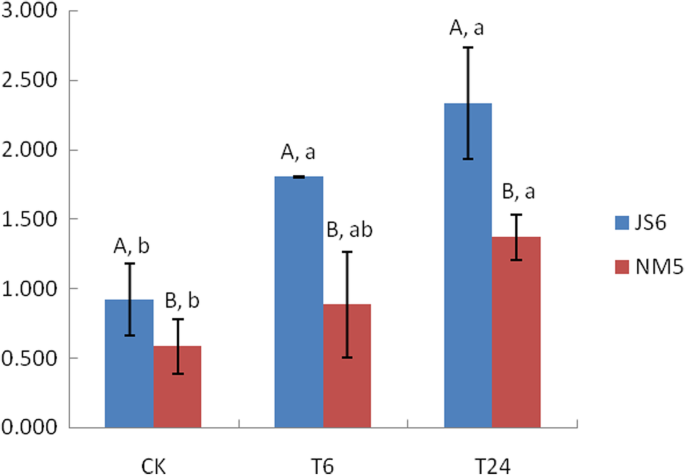
在对照组中,JS6和NM5分别被指定为JS6CK和NM5CK。在20%PEG-6000的组中,6小时,JS6和NM5分别被指定为JS6T6和NM5T6。在20%PEG-6000处理中,24小时,JS6和NM5分别被指定为JS6T24和NM5T24。随着应力时间续时间,MDA含量在两种品种中升高(图。1).JS6始终表现出较高的MDA含量比NM5,不论PEG诱导的水应力的存在或不存在的。具体而言,在JS6 MDA含量约为0.584-,1.042-,并且比那些在NM5正常条件下,T6处理,和T24处理,分别下0.706倍以上。与在正常条件下的MDA含量相比,在JS6品种MDA含量T6和T24的处理下分别增加95.6和152.9%。与对照相比,在NM5品种MDA含量T6和T24的处理下分别增加51.8和134.8%。
RNA测序和DE Novo集装箱
从两个品种的18个文库(包含3个生物重复)中获得rna测序样本。所有RNA测序数据的原始读取数据存储在NCBI Short Read Archive数据库中,登录号为SRP144636 (SAMN08947059-SAMN08947076),与生物项目PRJNA454008相关。从每个样本中获得约4200万个高质量reads(见表)1)共获得115660个转录本和59035个单基因,平均长度为1367 2044年的bp和N50 bp,平均长度为1080 1953年的bp和N50 转录组鸟枪组装数据保存在DDBJ/EMBL/GenBank,登录号为GHHA01000000。
功能注释
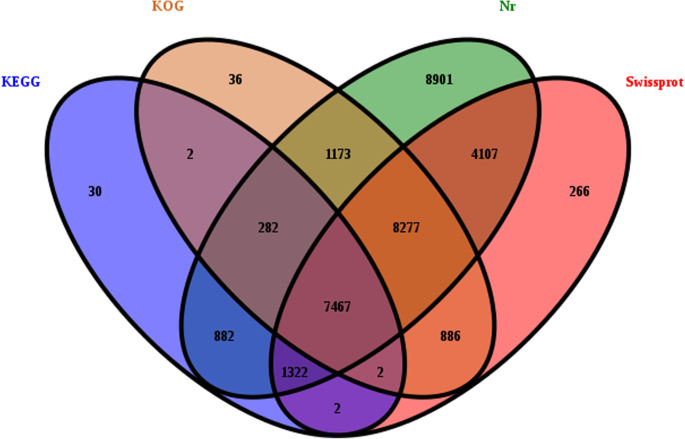
在59035个unigenes数据库中,至少有一个数据库中注释了33634个unigenes,其中nr数据库注释了32410个unigenes, SWISS-PROT数据库注释了22328个unigenes, KEGG数据库注释了9988个unigenes, COG数据库注释了18124个unigenes(图1)。2).
KEGG途径富集分析表明,已知途径中注释了5631个单基因。在细胞过程类中,与内吞作用相关的基因最为丰富,参与植物激素信号转导的基因占环境信息处理类中的最大部分。与核糖体相关的基因在遗传信息处理类中,剪接体、内质网中的蛋白质处理和RNA转运非常丰富。参与碳代谢和氨基酸生物合成的物质在代谢类中占最大比例,与植物-病原相互作用相关的物质在遗传信息处理类中最为丰富组织系统类(附加文件)1:表S3)。
根据基因本体论(gene ontology, GO)术语分析,共注释了10085个unigenes,分别为细胞成分5892个unigenes,分子功能6676个unigenes,生物过程6680个unigenes。在细胞组分类中,与“膜”、“膜部分”、“细胞”和“细胞部分”相关的unigenes非常丰富。在生物过程方面,“代谢过程”和“细胞过程”类的unigenes非常丰富,而“催化活性”和“结合”类的unigenes分别占分子功能类的最大和第二大部分(图)。3.).
JS6和NM5品种差异表达基因(DEGs)的总体分析
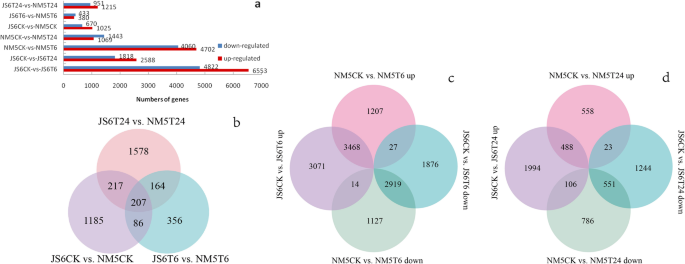
在对照组中,在JS6和NM5中观察到1695次。在模拟干旱处理后收集的样品中,分别在JS6和NM5中鉴定出6和24小时,833和2166℃(图。4a).维恩图显示,两个品种在对照和模拟干旱处理组中有207个基因差异表达(图2)。4b)。
与各自的对照组相比,在JS6T6(包括6553个上调和4822个下调基因)中鉴定11,375次,在NM5T6中发现8762只(包括4702个上调和4060个下调基因),4406次在JS6T24中注意到(包括2588个上调和1818个下调基因),在NM5T24中观察到2512次(包括1069个上调和1443个下调基因;图。4a).在两个品种的T6组中都发现了大量的DEGs。JS6T6和JS6T24处理的deg分别是NM5T6和NM5T24处理的0.298和0.754倍。比较两个品种的GO类别和KEGG通路,发现两个品种的DEGs参与了相似的GO类别和KEGG通路(附加文件)1:表S4和S5)。欧拉图的基础上,比较控制和T6组织透露,1)的2334个基因(1207——1127年下调基因)在NM5专门监管,而4947个基因(3071——1876年下调基因),超过1.12倍,在NM5,特别在JS6监管;2)与各自对照相比,两个品种共表达或共表达下调的基因分别有3468和2919个,而在JS6T6中分别有14个和27个上调或上调基因,在NM5T6中分别有14个和27个上调或上调基因。4c).对照组与T24组比较发现:1)NM5特异调控1344个DEGs(上调558个,下调786个),而JS6特异调控3238个DEGs(上调1994个,下调1244个),是NM5特异调控的1.41倍;2) 488和551个基因在两个品种中分别共表达或共表达下调,而在JS6T24中分别有106和23个基因表达上调或上调,而在NM5T24中分别有106和23个基因表达上调或上调(图2)。4d) 。
deg参与氧化应激反应
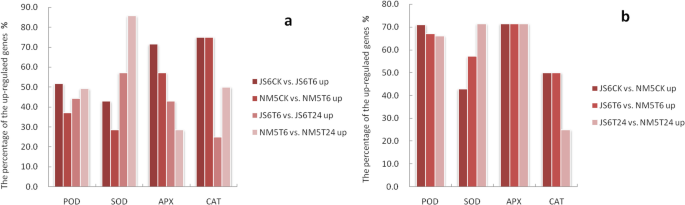
与各自的控制相比,更多的基因属于POD、SOD、APX型家庭和诱导JS6比NM5 T6处理下,而更多的基因属于POD、SOD,和猫家庭诱导NM5比JS6模拟干旱处理后6 h 24 h(无花果。5一个)。具体而言,无论PEG诱导的水应激的存在或不存在,属于POD和APX家族的更多基因在NM5中表现出比JS6更高的表达水平。在模拟干旱治疗后,属于SOD家族的更多基因显示在NM5中的表达水平高于JS6(图。5b).有趣的是,peg诱导水分胁迫6h后,两个品种中APX家族的基因中有57-70%以上表达上调,CAT家族的基因中有75%表达上调,而POD和SOD家族的基因中很少有表达上调。然而,peg诱导水分胁迫6h至24h后,POD和SOD家族上调基因数量增加,APX和CAT家族上调基因数量减少(图)。5一个)。
DEGs参与渗透胁迫反应
无论是否存在peg诱导的水分胁迫,NM5中有更多与脯氨酸生物合成相关的基因保持了高于JS6的表达水平(图6)。6).然而,与它们各自的对照相比,脯氨酸生物合成所涉及的更多基因在JS6中上调而不是模拟干旱处理下的NM5(图。6).
参与光合作用相关反应的DEGs
光合作用相关基因在T6胁迫下大多受到抑制,在peg诱导的水分胁迫6 ~ 24 h后又恢复到上调(图2)。7a).与各自对照相比,这些基因在JS6中以T24下受抑制最多,而在NM5中以T24下诱导最多。与对照相比,在T6处理下,两个品种共下调26个基因,而在JS6T6中下调4个基因,在NM5T6中上调4个基因。模拟干旱处理6 ~ 24 h后,两个品种共表达了25个基因。在JS6T24基因中有25个基因表达下调,而在NM5T24基因表达上调(Additional file)2:图S1a-c)。与叶绿素含量相关的基因也有类似的表达谱。7b).与对照相比,在T6处理下,两个品种共下调20个基因,而在JS6T6中下调4个基因,在NM5T6中上调4个基因。干旱处理6 ~ 24 h后,有23个基因共同上调。在T24处理下,两品种中有14个基因共同上调,而在JS6T24中有11个基因下调,而在NM5T24中有11个基因上调2:图S2a-c)。
在度的视角的表达模式
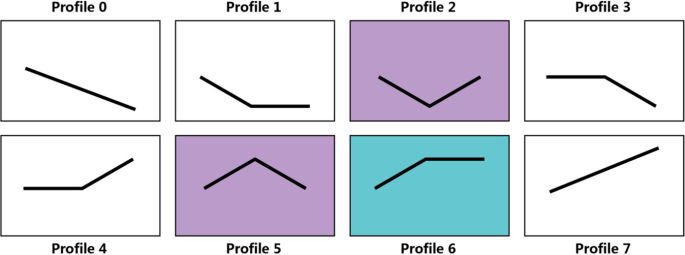
不同处理下各品种的差异基因分别聚类在8个剖面上(图2)。8).结果表明,在peg诱导的水分胁迫下,两品种间基因表达随胁迫时间的变化存在显著差异。在谱2、5和6中,deg显著富集(p< 0.05),但在profiles 2和5中显著富集(p< 0.05)。配置2、配置5和配置6在JS6中分别包含4037、3657和3329个deg,而配置2和配置5在NM5中分别包含4397和4615个deg。
两个品种的氧化石墨烯在生物过程中丰富了“有机物代谢过程”、“细胞代谢过程”和“初级代谢过程”等范畴。在细胞组分中,“膜组分”和“膜固有组分”是最丰富的种类,“有机环化合物结合”和“杂环化合物结合”的基因在分子功能上丰富(附加文件)1:表S6)。
KEGG途径富集分析注释了1943和1738个来自JS6和NM5的DEGs。一些重要的KEGG途径,包括deg含量最高的前10条途径和光合作用途径,在Additional file中显示1:表S7。这些途径包括植物激素信号转导,碳代谢,核糖体,苯丙醇化生物合成,氨基酸的生物合成,淀粉和蔗糖代谢,内质网,植物 - 病原体相互作用和凝血酶组和嘌呤代谢的蛋白质加工,或糖酵解/葡糖生成。
所述DEGS的表达模式参与非生物和生物应激反应相关的生物学过程
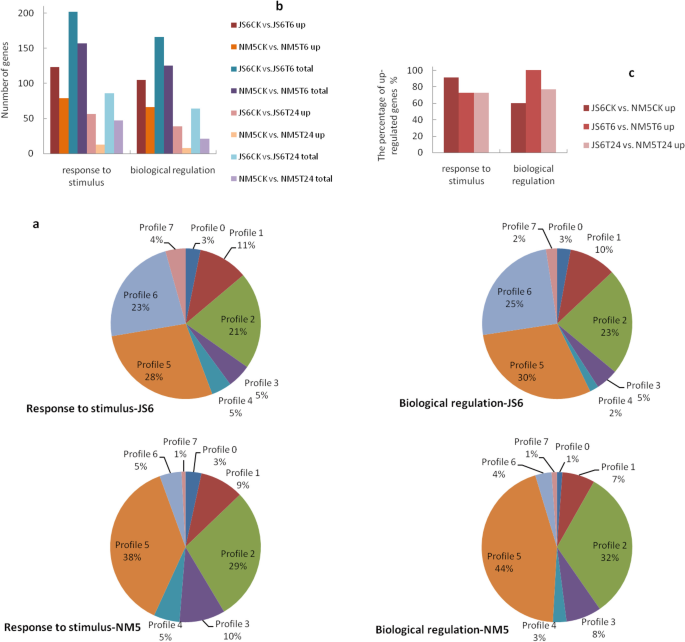
参与“刺激刺激反应”的基因在JS6中的谱5和6中富集,而这些基因在NM5中富含概况5(图。9一个)。在两种品种的“生物调控”的GO类别中观察到类似的结果(图。9a).这些基因的主要表达模式显示,在JS6中,它们在T6位点被促进,在T24位点被抑制(profile 5)或在T24位点保持高表达(profile 6)。相比之下,NM5中观察到这些基因在T6位点的促进和T24位点的抑制(profile 5),这是NM5的主要表达模式。
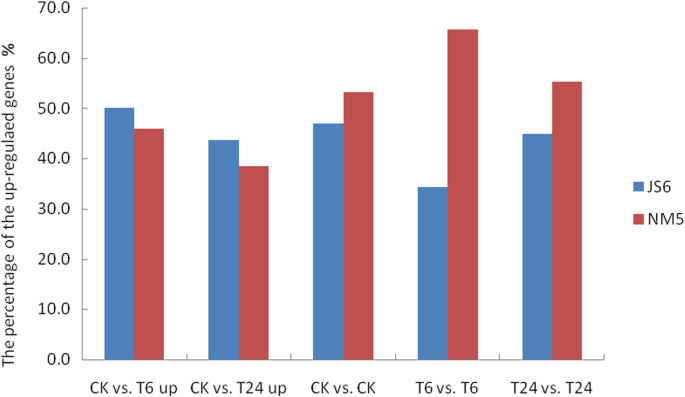
与各自对照相比,JS6T6中与“刺激反应”相关的deg比NM5T6多约28.7%,其中上调基因多55.7%。与NM5T6相比,JS6T6中“生物调控”相关的基因数量增加了32.8%,其中上调基因数量增加了59.1%。与NM5T24相比,JS6T24中鉴定出的与“刺激反应”相关的基因约多83.0%,包括约3.31倍的上调基因。JS6T24中与“生物调控”相关的基因比NM5T24多两倍以上,其中上调基因约为NM5T24的3.88倍(图)。9b).然而,无论是否存在peg诱导的水分胁迫,NM5中参与“刺激响应”和“生物调控”的基因比JS6表达水平更高(图6)。9c) 。
DEGs在植物激素信号转导和光合作用途径中的表达模式
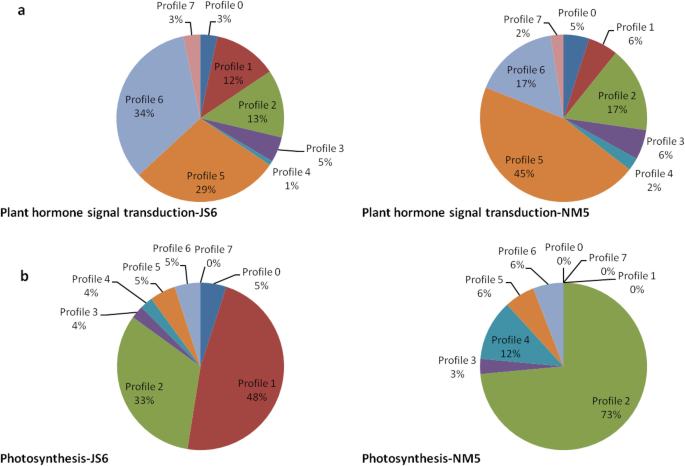
在JS6和NM5中分别注释了122个和121个植物激素信号转导通路的DEGs,这些条目表现出最高的代表性。约45%(55/121)的基因富集在NM5 5型中,占比最大;而在JS6中,34%(41/122)的基因富集在谱6中,29%(35/122)的基因富集在谱5中,分别占JS6中最大和第二大部分(图6)。10),分别。此外,JS6和NM5中分别注释了40和34个光合途径的DEGs。NM5中约73%(25/34)的基因富集在2型基因中,占比最大,而1型基因中没有一个富集。而在JS6中,48%(19/40)的基因富集在基因1中,33%(13/40)的基因富集在基因2中,分别占JS6中最大和第二大部分(图2)。10b)分别。
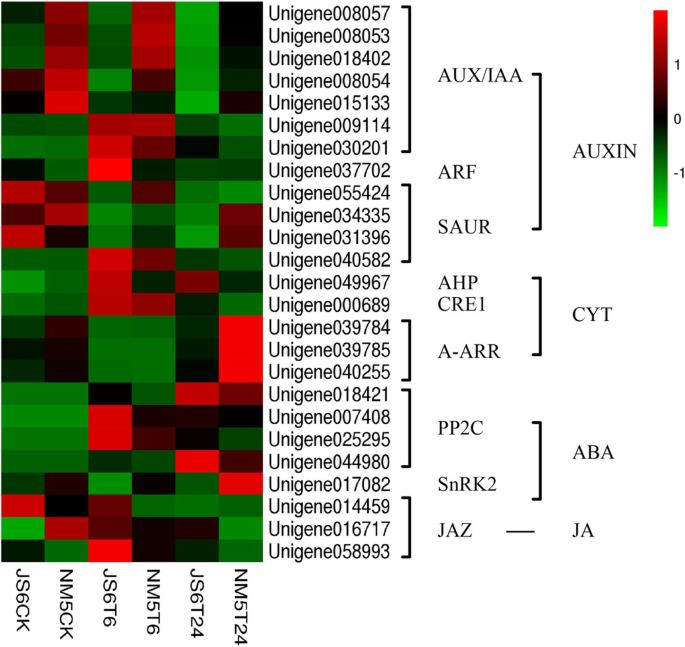
在植物激素信号转导途径的分析中,我们重点对JS6T6与NM5T6、JS6T24与NM5T24进行了两两比较(图5)。11).与JS6相比,在T6下调节编码毒素诱导的蛋白质Aux / IAA的四个unigenes,在T24下调节四个unigenes,在NM5中的T24下调两个unigenes。在NM5T6中发现了一种抑制arf和编码Sur的上调Unigene编码Sur的抑制的Unigene,而在NM5T24中鉴定了两个上调和涉及Saur编码的一个下调和一个下调的未受下调的未经核原。Unigene 049967编码和层次分析法Unigene 000689编码CRE1分别在NM5T6和NM5T24中抑制。Unigene039784.,Unigene039785.,Unigene040255NM5在T24作用下A-ARR编码上调。在NM5中,参与PP2C编码的2个ungene在T6下表达下调,另外2个ungene在T24下表达下调。Unigene 014459和Unigene 058993参与茉莉酸ZIM结构域蛋白(JAZ)编码的NM5在T6下受到抑制。此外,Unigene 016717和Unigene 058993NM5在T24作用下受到抑制。
中存在的验证
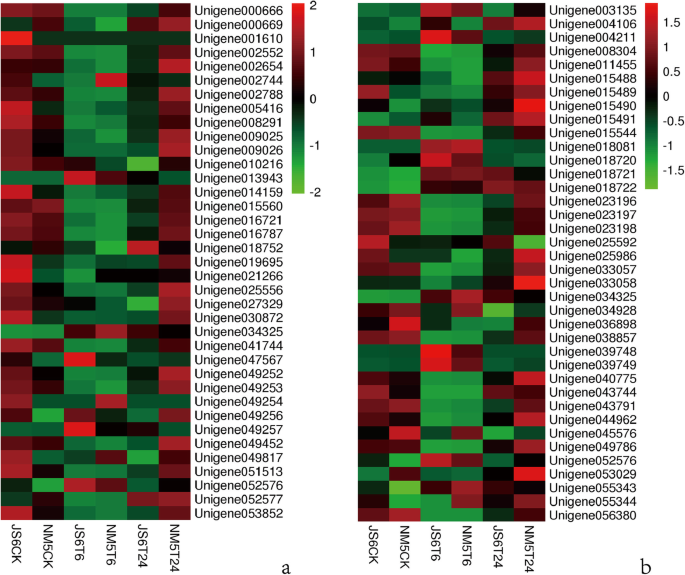
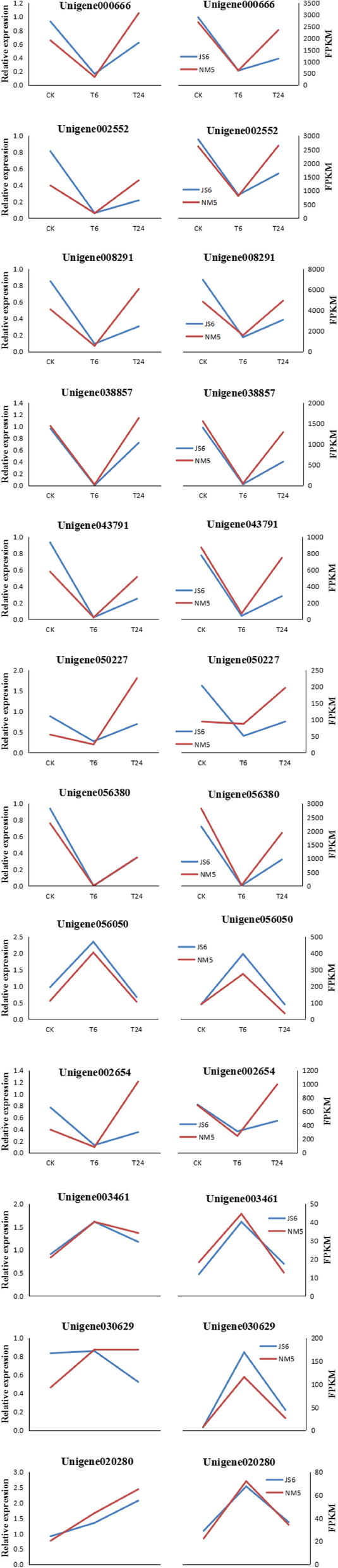
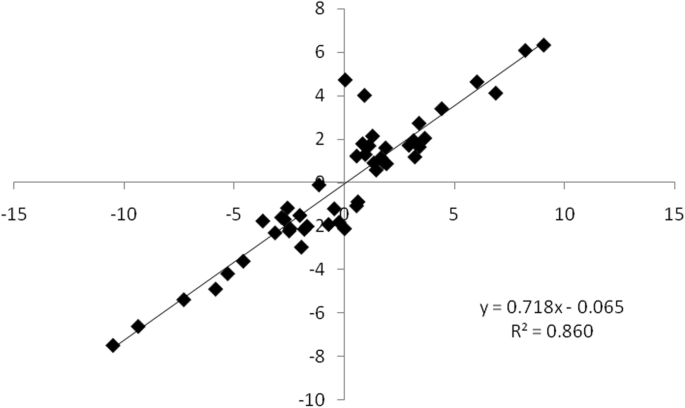
qRT-PCR和RNA-seq数据均表明,8个转录本的表达水平,即Unigene 000666.,Unigene 002552,Unigene 002654,Unigene 008291,Unigene 038857,Unigene 043791.,Unigene 050227,Unigene 056380在T6时被抑制,在T24时被促进(图。12);相比之下,Unigene 003461和Unigene 056050T6表达上调,T24表达下调。通过qRT-PCR获得的转录本表达模式与RNA-seq结果高度一致(图)。12和13).通过线性回归分析,RNA-seq和qRT-PCR数据显著正相关(图)。13),从而确认来自RNA-SEQ的DEGS数据。
讨论
不同的遗传背景不同的品种提供重要的遗传资源,以改善特征的新品种[46.].Proso Millet对干旱的压力非常适应,并研究其对干旱压力的反应可以提供有关其干旱耐受的机制的重要信息,以及改善其干旱适应和其他作物的机制。在这项研究中,分析了两个Proso小米品种,NM5和JS6,并讨论了它们的叶子对干旱的反应。
JS6和NM5品种转录信息综合分析
从RNA-seq数据中获得转录本115 660个,unigenes 59 035个,平均长度分别为1367和1080 bp。其中33634个unigenes使用BLASTX算法在nr、SWISS-PROT、COG、KEGG等4个公共数据库中至少一个数据库中成功注释。这些数据将进一步丰富原小米的转录组信息。
当植物经历干旱胁迫时,它们的基因表达水平通常表现出广泛的变化[47.].在本研究中,响应于PEG诱导的水分应激,在敏感品种中观察到在敏感品种中的T6中发生的剧烈转录变化,而不是耐受性。更DEGS在T6处理被确定不是在T24的处理,以在这两个品种它们各自的对照比较,而被发现和JS6T6之间NM5T6 DEGS的数量是最低(图4一个)。这些结果表明,在两种品种的T6发生的转录变化增加,耐旱培养物在干旱胁迫下可能保持高度稳定的基因表达水平。yates等人。[48.]报道了类似的结果,并将其归因于干旱敏感和耐旱植物的不同反应;这一特性可能是由于两种植物对干旱的敏感性不同造成的。
在peg诱导的水分胁迫下,敏感品种比耐旱品种表现出更多的DEGs,特别是参与调控刺激响应和生物调控过程的上调基因(图2)。9b)。然而,在耐旱品种中,无论是否存在模拟干旱处理,更多的这些基因都保持了较高的转录水平(图2)。9c).在干旱条件下,耐旱品种对强化相关基因调控的要求较敏感品种低。这可能是由于抗旱品种相对于敏感品种条件较轻,相关基因转录水平较高所致。
涉及到植物的光合作用转录变化
在模拟的干旱胁迫存在下,在T6下最抑制了与植物光合作用相关的基因(图。7a) .在与叶绿素含量相关的基因中发现了类似的表达谱(图。7b).这些发现与干旱胁迫下植物的光合作用特征一致。先前的研究已经证明,植物的光合作用在干旱胁迫下会降低[33.,49.,50.],光合作用相关基因在干旱胁迫下优先受到抑制[17,48.].值得注意的是,QRT-PCR数据也呈现了类似的特征。在功能诠释的基础上,Unigene 000666.预测在光系统I中编码亚基O,并预测其与膜的固有成分有关。Unigene 008291和Unigene 002552推测分别编码叶绿体光系统I反应中心的II和III亚基,并预测两者都与细胞代谢过程有关。Unigene002654.被预测为在叶绿体的光系统II反应中心,将其预测为与能量代谢过程编码22 kD的蛋白质。Unigene 038857,Unigene 043791,和Unigene 056380预计分别编码CP26前体,叶绿素A-B结合凋亡和CP24和P4叶绿素A-B结合蛋白,其预测有助于重要的代谢和蛋白质改性过程。Unigene 050227推测编码叶绿体管腔位置2的光合作用NDH亚基。被测的植物光合作用相关基因均在T6位点被抑制,T24位点被促进(图2)。12).
干旱处理6 ~ 24 h后,与植物光合作用相关的基因大部分恢复和上调。然而,与各自的对照相比,JS6在T24下受抑制最多,NM5在T24下诱导最多(附加文件)2:图S1C)。KEGG途径富集分析和qRT-PCR数据的结果也产生类似的特性(图10b和12).在干旱胁迫下抑制的光合相关基因可以更容易地恢复到耐旱培养中的相对正常水平而不是干旱敏感品种。之前的研究还证明,在敏感池中发现与光合仪有关的更多抑制基因在敏感的池中比容忍的池中[48.],可能是因为干旱胁迫降低植物的光合能力。对调节耐旱品种耐旱性,包括与ROS拾荒者和脯氨酸的积累,有利于植物减少ROS损伤的基因的表达水平升高改进策略,生存干旱胁迫,并保持生产力。光合恢复有助于植物恢复后干旱[51.].因此,当一系列防御反应减轻胁迫伤害后,耐旱品种比干旱敏感品种更容易恢复,后者维持了大部分的光合作用。干旱胁迫对耐旱品种生长和产量的不利影响小于敏感品种。
原谷子品种对氧化应激反应的变化
干旱治疗增加MDA积累[52.,53.,54.],干旱敏感品种比耐旱品种积累更多的MDA [54.,55.]本研究表明,随着胁迫时间的延长,两个品种的MDA含量都有所增加,无论是否存在PEG诱导的水分胁迫,JS6中的MDA含量始终高于NM5(图。1).结果表明,在peg诱导的水分胁迫下,干旱敏感品种JS6的ROS水平高于耐旱品种JS6。与这些结果一致的是,在耐旱品种中,预测有更多与ROS清除酶相关的高转录水平基因(图。5B)在这项研究中被确定。无论是否存在peg诱导的水分胁迫,更多与脯氨酸生物合成相关的基因在耐受品种中保持较高的转录水平(图)。6),从而有助于降低抗旱品种的ROS损伤水平。在渗透胁迫下,脯氨酸积累可以通过保护谷胱甘肽-抗坏血酸循环的酶或增强其活性来保护蛋白质和膜[2].因此,在干旱胁迫下,耐受品种比敏感品种更能有效地保护膜系统免受活性氧清除和渗透调节系统的协同作用,调节ROS稳态,减少ROS损伤,提高抗旱性。
在存在模拟的干旱胁迫下,APX和猫显示比豆荚和SOD的更快的转录反应,并且在耐受培养品种中涉及ROS清除系统的干旱响应基因与敏感品种中的那些延迟转录反应显示出延迟的转录反应。在以前的玉米研究中报道了ROS清除系统的协同效应和非同步[56.[米[57.].抗旱品种活性氧清除酶活性高于敏感品种[57.].这些发现有助于进一步阐明谷子脯氨酸对干旱胁迫下不同抗旱品种间脯氨酸含量和活性氧清除剂变化的响应机制。
植物激素对谷子抗旱性和生长的影响
在模拟干旱胁迫下,与干旱敏感品种JS6相比,耐旱品种NM5的JA信号通路中JAZ受到抑制。在干旱胁迫下,抗旱品种的活性JA积累量可能高于敏感品种,从而抑制JAZ,促进JA信号转导。JA在对环境刺激的反应中很重要[22.,23.,24.].它可以促进ROS解毒酶系统和抗坏血回收基因[26.].抗坏血酸的丰度与激素信号的激活阈值和激素交叉对话有关[29.].JAZ可以通过抑制低JA水平的植物细胞中的转录因子来抑制JA应答基因的表达[58.].在环境刺激下,活性JA的积累通过泛素/26S蛋白酶体途径刺激JAZ降解,从抑制中释放转录因子,触发JA信号通路[59.].因此,在干旱条件下,抗旱品种JA信号转导途径的不同响应策略可能是抗旱胁迫的驱动因素之一。在干旱胁迫下,抗旱品种活性JA的高积累可能促进了JA信号转导途径,促进了ROS清除系统,减少了ROS损伤,提高了细胞膜稳定性,缓解了胁迫条件,使光合作用易于恢复。
与JS6相比,NM5信号转导通路中的生长素和细胞分裂素在T6作用下受到抑制。这一反应有助于调节抗旱品种在胁迫下的气孔关闭。此外,NM5信号转导通路中的细胞分裂素在T24作用下被诱导。这一发现与抗旱品种在一系列防御反应后比敏感品种具有更强的恢复能力的假设相一致。此外,NM5在各胁迫处理下都促进了JA和ABA信号转导通路,有助于调控气孔关闭,激活下游防御反应。进一步系统研究不同抗旱品种的激素变化对干旱的响应,将为进一步阐明谷子的响应机制提供重要信息。
结论
在模拟干旱胁迫下,与JS6相比,NM5保持了高度稳定的基因表达水平,并携带了更多预测与ROS清除酶相关的高转录基因。与干旱敏感品种相比,抗旱品种JA信号转导途径的不同调控策略可能是抗旱胁迫的驱动力之一。
方法
植物材料和干旱处理
本研究利用peg诱导的渗透胁迫模拟干旱胁迫。以种子发芽率为基础,从37个谷子核心品种中筛选出抗旱、耐旱材料进行后续分析。上述谷子原种均已在国内发布,试验材料均由西北农林科技大学农学院小粮课题组从田间栽培植物中提供。
从每个普罗索谷子品种中选择600粒大小和外观相似的种子,并随机分为六组进行发芽。所有种子均在30℃通过烘箱干燥进行预处理 摄氏度-35度 摄氏度,适用于48-72 h、 随后,每个品种的100粒种子被分配到一个塑料盒(12)中 厘米 × 12 厘米 × 8. cm)使用滤纸,并用8 mL蒸馏水作为对照,8 最后,种子在一个有盖的塑料箱中生长,光周期为0 h光/24 h 25℃时的黑暗和湿度为70% 3摄氏度 然后测量发芽率。分别选择发芽率高于95%的对照组和相对发芽率最高或最低的处理组中的品种作为耐旱和干旱敏感品种进行后续分析。
这两个品种的种子都在蒸馏水中发芽并在塑料箱中生长了3年 在0的光周期下的天数 h光/24 h 25℃时的黑暗和湿度为70% °C。植物在Hoagland溶液中培养,光周期为16 h灯/8 h 25℃时的黑暗和湿度为70% °C。在三叶期,两个品种的幼苗分别处理0(对照)、6(T6)和24 h(T24)与含有20%PEG-6000的霍格兰溶液混合。处理后,从每组叶片组织中取样进行后续分析,在液氮中快速冷冻,并储存在室温下− 80 摄氏度。
MDA的测定,RNA提取,转录组测序和从头序列组装
如前面所述测量MDA水平[60.].根据制造商的说明,使用TRIzol®试剂(Invitrogen)从收集的叶子组织中提取总RNA。采用Agilent 2100 Bioanalyzer (AgilentTechnologies, Palo Alto, CA, USA)通过琼脂糖凝胶电泳评估提取的rna的完整性。用NanoDrop 8000分光光度计(NanoDrop, Wilmington, DE, USA)测定。所有提取的RNA质量均可用于构建总RNA文库,总RNA RIN值> 6.3,28S:18S比值≥1.1。
使用oligo (dT)磁珠富集总mrna,并通过添加碎片缓冲液将其剪切成短片段。这些RNA片段用随机六聚体合成第一链cDNA,然后用DNA聚合酶I和RNase H (Invitrogen)合成第二链cDNA。用QiaQuick PCR提取试剂盒(QIAGEN)纯化后,将末端修复和a尾测序接头连接到cDNA片段上。用AMPure XP beads对合适的片段进行纯化,通过PCR扩增,构建文库,用于后续测序。在HiSeq™4000平台(SageneBiotech Co. Ltd, Guangzhou, China)上进行转录组测序。通过基调用将测序得到的原始图像数据转换为原始读取数据。通过严格的过滤步骤,包括去除适配器序列、含有10%以上未知碱基的读和低质量读,获得高质量的干净读。使用Trinity程序将获得的高质量的clean reads进行混合和组装。
功能注释和DEG分析
要确定推定功能,我们将组装的未完成数据库搜索,包括NR(http://www.ncbi.nlm.nih.gov/), SWISS-PROT (http://www.expasy.ch/sprot/),KEGG(http://www.genome.jp/kegg/)和KOG (http://www.ncbi.nlm.nih.gov/cog/)通过使用BLASTX算法与数据库e< 1 e的值- 5.通过Blast2GO程序进行NR注释,在GO数据库中对组装的unigenes进行注释,并使用WEGO对unigenes进行GO功能分类。
读取的表达式值用外显子模型每百万映射读取的reads Per Kilobase进行标准化。阈值P在多个假设检测中使用假发现率(FDR)进行调整。在本研究中,将截止设定为FDR≤0.05和| log2 FC | ≥ 1 to determine the DEGs using edgeR package (http://www.r-project.org/).所有的DEG都经过GO功能和KEGG途径的浓缩分析。
实时荧光定量PCR分析
附加文件1表S1为qRT-PCR实验所涉及的引物序列。实验使用SYBR premix Ex Taq试剂盒(TaKaRa,中国大连),以第一链cDNA为模板,在ABI 7500 Real-Time System (Applied Biosystems)上进行qRT-PCR。为验证DEG结果,随机选取12个转录本进行qRT-PCR验证。肌动蛋白作为内部控制。通过相对定量计算靶基因表达水平的fold change (2-△△CT) [13].
数据和材料的可用性
所有RNA测序数据的原始读取数据保存在NCBI Short Read Archive (SRA)数据库中,登录号为SRP144636 (https://www.ncbi.nlm.nih.gov/sra/SRP144636),与BioProject PRJNA454008相关联。转录组鸟枪组件数据在DDBJ / EMBL / GenBank中的登录号GHHA01000000下沉积。
缩写
- 阿巴:
-
脱盐酸
- 爆炸:
-
基本的局部对齐搜索工具
- 猫:
-
催化剂
- cDNA:
-
互补脱氧核糖核酸
- 度:
-
差异表达基因
- 舰队指挥官:
-
折叠变化
- 罗斯福:
-
假发现率
- FPKM:
-
每百万片碎片每千碱基映射的碎片
- 走:
-
基因本体论
- 是:
-
茉莉酸
- 杰兹:
-
jasmonate Zim域蛋白
- MDA:
-
丙二醛
- 荚:
-
过氧化物酶
- 存在:
-
定量实时聚合酶链反应
- RNA-SEQ:
-
RNA测序
- ROS:
-
活性氧
- 草皮:
-
超氧化物歧化酶
参考
- 1.
Boyer JS。植物生产力与环境。科学。1982;218:443-8。
- 2。
汗女士,艾哈迈德D,汗马。渗透保护剂基因在转基因植物中增强非生物胁迫耐受性的研究。电子学报。2015;18:257-66。
- 3.
陈建平,陈志强,陈志强,等。干旱胁迫下植物气孔运动的激素信号调控。植物基因。2017;11:143-53。
- 4.
植物对水分亏缺的恢复机制:节水农业的前景。J Exp Bot. 2004; 55:2365-84。
- 5。
Foley JA, Ramankutty N, Brauman KA, Cassidy ES, Gerber JS, Johnston M, et al.;这是一个被开垦的星球的解决方案。大自然。2011;478:337-42。
- 6。
秦德辉,丁艳华,王斯文,王思明,林东生,等。中国西部生态环境变化及其应对策略。地球科学进展。2002;17:314-9。
- 7。
赵辉,王日日,马宝林,熊永春,强胜胜,王春林,等。全地膜垄沟覆盖提高了半干旱雨养生态系统中马铃薯的水分利用效率和块茎产量。田间作物Res. 2014; 161:137-48。
- 8。
董军,王浩,陈磊,王军,乔忠。96份谷子原种质资源遗传多样性分析。河北农业科学,2014;18:1-4。
- 9.
瞿Y,苏W,张PP,李C,高JF,高XL等。不同集水对所述黍的土壤水分,生长和产量(黍miliaceum在中国西北半干旱区。中国农业科学,2012;4:106-13。
- 10.
苏W,张YP,曲Y,李春苗JY,高XL等。覆盖对土壤水分,黍生长,光合特性和产量的模式在中国黄土高原旱地的影响。Chin J Appl Ecol。2014; 25:3215-22(在中国)。
- 11.
亨特HV,Denyer K,LC帕克曼,琼斯MK,豪CJ。在糜子蜡质胚乳淀粉表型的分子基础(黍miliaceum L。)。mol Biol Evol。2010; 7:1478-94。
- 12.
王里,狩猎hv,qiao zj,王l,韩呀。猴子米兰的多样性和培养(黍miliaceum中国:一篇综述。经济学。机器人。2016;70:332-42。
- 13。
岳辉,王磊,刘辉,岳文军,杜晓华,宋卫宁,等。糜子转录组的从头组装和鉴定(黍miliaceum用于基因发现和标记开发。前面。植物科学。2016;7:1083.
- 14。
胡勇,朱军,刘峰,张智,柴勇,宋卫宁。中国高粱谷子地方品种和品种遗传多样性(黍miliaceum)。Ann Appl Biol. 2008; 153:357-64。
- 15.
张艳艳,韩鸿奎,张德志,李军,龚新伟,冯宝林,等。半干旱区垄作和覆盖组合措施对谷子生长和产量的影响。农田作物Res. 2017; 213:65-74。
- 16。
利用QTL方法将旱稻抗旱机制与旱稻抗旱联系起来:整合气孔和叶肉响应的研究进展和新机遇。中国农业大学学报2002;53:989-1004。
- 17。
陈W,姚Q,帕特林GB,agarwal g,deshmukh rk,lin l等。RNA-SEQ透露型干旱和洪水应力下大豆叶组织差异基因表达的鉴定与对比分析。前植物SCI。2016; 7:1044。
- 18。
在脱水和冷胁迫的细胞反应和耐受性的转录调控网络。植物学报2006;57:781-803。
- 19.
威尔金森S,戴维斯WJ。干旱,臭氧,ABA和乙烯:从细胞新的见解植物社区。植物细胞环境。2010; 33:510-25。
- 20.
王志强,王志强。植物抗逆性和抗逆性的研究进展。植物生态学报。2011;14:290-5。
- 21.
王志强,王志强,王志强。植物气孔功能的激素互作。植物学报。2009;69:451-62。
- 22.
Devoto A,Turner JG。jasMonate-调节的拟南芥应力信号网络。physiol植物。2005; 123:161-72。
- 23.
Giri Ap,wünscheh,mitra s,zavala ja,muck a,svatos a,baldwin它。专家食草动物之间的分子相互作用Manduca sextta(Lepidoptera,Sphingidae)及其天然宿主烟草attenuata则.VII。植物蛋白质组的变化。植物理性。2006; 142:1621-41。
- 24.
杨毅,斯托尔茨,切特拉特A,雷蒙德P,帕格尼M,杜布格农L,法默EE.茉莉酸途径生长抑制分支中的下游介质.植物细胞.2007;19:2470-83。
- 25。
NOCTOR G,Voyer C.抗坏血酸和谷胱甘肽:在控制下保持活性氧气。Annu Rev植物植物植物Mol Biol。1998年; 49:249-79。
- 26。
Nafie E,Hathout T,Mokadem Asa。茉莉酸在Cucumis Melo L.细胞中引发氧化防御和排毒系统。BRAZ J植物理体。2011; 23:161-74。
- 27。
抗坏血酸-谷胱甘肽循环在豌豆叶线粒体和过氧化物酶体中存在的证据。植物杂志。1997;114:275 - 84。
- 28。
亚达K.叶绿体中的水循环:清除活性氧气和过量光子的耗散。Annu Rev植物植物植物Mol Biol。1999年; 50:601-39。
- 29。
Bartoli Cg,CasalonguéCa,Simontacchi M,Marquez-Garcia B,Foyer Ch。激素与氧化还原信号通路之间的相互作用在控制生长和交叉耐受性的压力中。Environ Exp Bot。2013; 94:73-88。
- 30.
Pignocchi C,Fletcher J,Barnes J,Foyer Ch。抗坏血酸氧化酶(AO)在烟草中的功能(烟草《植物生理学》2003;132:1631-41。
- 31.
Davey MW,Stals E,Panis B,Keulemans J,Swennen RL。植物组织中丙二醛的高通量测定。肛门生物化学。2005; 347:201-7。
- 32.
Valliyodan B, Nguyen HT。了解植物抗旱性增强的调控网络和工程。植物学报2006;9:189-95。
- 33.
陈伟,何胜,刘东,翟华,王飞,等。甘薯香叶酰香叶酰焦磷酸合酶基因,IbGGPS提高拟南芥的类胡萝卜素含量和抗渗透胁迫能力。《公共科学图书馆•综合》。2015;16:e0137623。
- 34.
非生物应激信号通路:特异性和串扰。植物科学进展。2001;6:262-7。
- 35.
氧化应激、抗氧化剂与应激耐受性。植物科学进展。2002;7:405-10。
- 36.
Diplock。对抗活性氧的防御。中华人民共和国化学与社会科学杂志1998;29:463-7。
- 37。
Alscher Rg,Donahue JL,Cramer Cl。反应性氧物种和抗氧化剂:绿色细胞中的关系。physiol植物。1997年; 100:224-33。
- 38。
刘艳,潘庆华,杨人瑞,刘艳艳,黄卫东。H之间的关系2O2豌豆叶伤反应中的茉莉酸。Russ J植物理体。2008; 55:851-62。
- 39。
羊肉c,dixon ra。植物疾病抗性的氧化爆发。安努。植物生理原始。植物摩尔。BIOL。1997年; 48:251-75。
- 40.
张志强,王志强。植物逆境适应与代谢运动的关系。植物学报1998;1:267-74。
- 41.
Blumwald E.钠运输和耐盐性植物。CurrOgin Cell Biol。2000; 12:431-4。
- 42.
Clark MB, Mercer TR, Bussotti G, Leonardi T, Haynes KR, Crawford J,等。用靶向RNA测序定量分析长非编码RNA。Nat方法。2015;12:339-42。
- 43.
关键词:柳枝稷,分蘖突变体,De Novo组装,转录组分析黍virgatuml .)。前面。植物科学。2015;6:749。
- 44.
张建军,张志强,张志强,等。激光捕获微解剖的玉米粒室的RNA测序鉴定了与胚乳细胞分化相关的调控模块。植物细胞。2015;27:513-31。
- 45.
王瑞英,王海根,刘学勇,连胜,陈磊,乔志军,McInerney CE,王磊。干旱诱导抗旱性和敏感性普通谷子品种的转录。动物植物学报,2017;27(4):1303-14。
- 46.
雷y,徐y,hettenhausen c,lu ck,shen gj,zhang cp等。苜蓿的比较分析(紫花苜蓿叶片转录组揭示基因型特异性耐盐机制。BMC Plant Biol. 2018;18:35。
- 47.
龙Y,张JW,田XJ,吴SS,张庆,张太平绅士等。从头组装沙漠树梭梭(答:最大经济产量。)基于RNA-SEQ数据,提供对干旱响应的洞察力,基因发现和标记识别。BMC基因组学。2014; 15:1111。
- 48.
Yates SA, Swain MT, Hegarty MJ, Chernukin I, Lowe M, Allison GG,等。基于RNA-Seq数据的红三叶草转录组从头组装为干旱响应、基因发现和标记鉴定提供了深入的了解。BMC基因组学。2014;15:453。
- 49。
Tabaeizadeh Z.植物细胞中的干旱诱导的反应。INT转速cytol。1998年; 182:193-247。
- 50.
干旱、盐和温度胁迫诱导的代谢重组和调控网络。J Exp Bot. 2012; 63:1593-608。
- 51.
干旱和盐胁迫下的光合作用:从全株到细胞的调控机制。安机器人。2009;103:551-60。
- 52.
Fayez Ka,Bazaid Sa。水杨酸和硝酸钾的应用改善大麦的干旱和盐度耐受性。j沙特SoC农业科学。2014; 13:45-55。
- 53.
张鹏,冯宝林,王pk,高新林,塔建明,柴勇,宋华。干旱条件下糜子叶片衰老及保护酶系统的研究。干旱地区农业研究。2010;28:99-8。
- 54.
张女士,谭F,谢b,张Qt,傅yf,杨cx,杨yh。甘薯在水胁迫下膜 - 脂质和膜保护系统在水分胁迫下的影响。科学科学罪。2003; 36:1395-8(中文)。
- 55.
孙峰,刘学森。作物抗旱鉴定指标研究。安徽农业科学,2009;37:12494-5。
- 56.
王志伟,牟世文,严玲,韩庆峰,杨培平。水分胁迫对春玉米幼苗生理生化特性及生长的影响西北植物学报,2013;33:343-51。
- 57.
赵宏伟,王雪萍,于明明,沙慧娟,贾勇,于涛涛,邹德涛。干旱胁迫和复水对分蘖期水稻抗氧化系统和脯氨酸的影响东北农业大学学报;2016;47:1-7。
- 58.
Thines B,Katsir L,Melotto M,Niu Y,Mandaokar A,Liu G,等。Jaz阻遏蛋白是茉莉酸盐信号传导期间SCFCOI1clep的靶标。自然。2007; 448:661-5。
- 59.
Chung HS,Howe Ga。通过拟南芥中斋甲酸Zim-结构域蛋白jaz10的稳定的剪接变体抑制茉莉酮酸盐信号传导中的Tify基序的关键作用。植物细胞。2009; 21:131-45。
- 60
黄志刚,李志刚。叶绿体的光过氧化作用。脂肪酸过氧化反应的动力学和化学计量学。Arch Biochem biophysics . 1968; 125:189-98。
致谢
作者要感谢SageneBiotech Co. (Guangzhou, China)在原始数据处理和生物信息学分析方面的帮助。我们也感谢生物标志物有限公司(北京,中国)在生物信息学分析方面的建议。
资金
研究主要是由资金从国家小米作物研究和开发系统(汽车- 06 - 13.5 a26),中国国家自然科学基金(31371529)、国家科技支撑计划(2014 bad07b03)和项目关键科学技术陕西省(s2018 - yf - tslny - 0005)集合,全文由陕西省小粮作物研究开发系统(2009-2018年)部分资助编撰。
作者信息
从属关系
贡献
ZYY, GXL, WPK和FBL设计了实验。ZYY, LJ, GXW进行了实验。ZYY、GXL和GJF分析了数据。ZYY, GXL, YP撰写论文。所有的作者阅读并批准了最终的手稿。
相应的作者
伦理宣言
伦理批准和同意参与
不适用。
同意出版
不适用。
相互竞争的利益
提交人声明他们没有竞争利益。
额外的信息
出版商的注意
施普林格《自然》杂志对已出版的地图和机构附属机构的管辖权要求保持中立。
附加文件
额外的文件1:
表S1。qRT-PCR实验所涉及的引物信息。表S2。37核心中国稷品种的发芽率。表S3。不同KEGG类中deg含量最高的途径的信息。表S4。两个品种中三个主要氧化石墨烯类中deg含量最高的前30个氧化石墨烯类的信息。表S5。两个品种KEGG通路中所涉及的DEGs信息。表S6。3级别在两个品种中的三个主要去课程中的DEGS注释。表S7。基于KEGG途径富集分析,deg和光合作用最多的10个途径概况。(XLSX 36 kb)
额外的文件2:
JS6和NM5分别用20%PEG-6000溶液治疗6(JS6T6和NM5T6)和24小时(分别为24小时)或水分(对照组; JS6CK和NM5CK)。图S1。在干旱处理和不干旱处理下,JS6和NM5中的DEGs参与了光合作用。一个通过对比对照和T6处理组,包括JS6T6和NM5T6中上调和下调的基因,得到了参与光合作用的DEGs的Euler图。b从T6和T24治疗组之间的比较中涉及光合作用的DEG的欧拉图,包括上调和下调基因。c通过对比对照和T24处理组,包括JS6T24和NM5T24中上调和下调的基因,得到了参与光合作用的DEGs的Euler图。图S2。JS6中的叶绿素含量相关基因和NM5在存在和不存在干旱处理的情况下差异表达。一个对照与T6处理组比较叶绿素相关基因的欧拉图,包括JS6T6和NM5T6中上调和下调的基因。b通过比较T6和T24处理组,包括上调和下调基因,得到叶绿素相关DEGs的Euler图。c对照与T24处理组比较叶绿素相关基因的欧拉图,包括JS6T24和NM5T24中上调和下调的基因。(邮政编码544 kb)
权利和权限
开放获取本文根据知识共享署名4.0国际许可的条款分发(http://creativecommons.org/licenses/by/4.0/)如果您向原始作者和源给出适当的信用,则允许在任何介质中进行不受限制的使用,分发和再现,提供指向Creative Commons许可证的链接,并指示是否进行了更改。Creative Commons公共领域奉献豁免(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条提供的数据,除非另有说明。
关于这篇文章
引用这篇文章
张勇,高,X,李,J。等原谷子(黍miliaceum叶片转录组对抗旱机制的研究。BMC植物BIOL.19,397 (2019). https://doi.org/10.1186/s12870-019-2001-x
收到了:
接受:
发表:
关键词
- 干旱
- Proso millet.
- RNA-SEQ.
- 基因表达
- 茉莉酸