抽象的
背景
C2H2-锌指蛋白质家族通常在植物中发现,称为染色质结构转录和重要组成部分中的关键参与者。基于它们的棉花的功能和结构,大量的C 2 H 2-锌指基因构件没有很好地表征。然而,在其他植物中,已经研究了几种C2H2-锌手指基因。
结果
在这项工作中,我们进行了综合分析和确定了386,196和195 C2H2-锌手指基因陆地棉(陆地棉),木本棉和Gossypium raimondii就, 分别。将编码C2H2-锌指基因的C2H2-锌指蛋白的系统发育树分析分为七(7)个亚组。此外,C 2 H 2-锌指基因成员在所有棉染色体中分布,虽然具有不对称的分布模式。在四倍体和二倍体棉之间检测到所有正交基因,在Upland棉和棉花之间检测到154个外科基因对木本棉虽然隆起和棉花之间发现了165个直字基因Gossypium raimondii就.同义(KS)和非同义(KA)核苷酸取代率(KA / KS)分析表明,棉C2H2-锌手指基因的主要影响主要受阴性选择,在重复事件后保持其蛋白质水平。RNA-SEQ数据和RTNA SEQ的RT-QPCR验证结果显示了在棉纤维发育的不同阶段的一些C2H2-锌手指基因的差异表达模式,表明C2H2-锌指基因在启动中发挥着重要作用调节棉花纤维开发。
结论
本研究为未来的实际基因组研究对Upland棉花的C2H2-锌手指基因进行了强大的基础。C 2 H 2-锌指基因家族的表达水平是其参与各种生物化学和生理功能的指针,其在起始和伸长级期间与棉纤维发育直接相关。这项工作不仅为确定C2H2-锌手指基因在纤维开发中的标称作用提供了基础,还提供了有价值的信息,以表征参与棉纤维发育的调节的潜在候选基因。
背景
锌指蛋白家族是高等植物中发现的最丰富的转录因子之一[1].此外,锌指蛋白是一种独特的蛋白质结构域,其中锌离子由半胱氨酸和组氨酸残基有界[2,主要分为不同的类型,即C2H2C2HC, C2HC.5.C2C2,ccch,c3.HC.4.C4.C4.HC.3.C6.C8.根据组氨酸和半胱氨酸残基的位置和数量[3.].C2H2- 凝胶手指蛋白,也称为TFIIA型手指蛋白,具有X的通式2CX.2-4CX.12HX.2-8h,其中X代表氨基酸,C代表半胱氨酸,而H代表组氨酸,其形成锌指蛋白家族的一种,其在各种植物种类中具有很好的特征[4.],在植物界广泛分布[3.那5.].该C2H2锌指蛋白首先在矮牵牛[发现6.].到目前为止,在拟南芥、水稻和谷子中分别鉴定出了176、189和124个c2h2 -锌指基因[3.],109 in杨树trichocarpa[7.]和211在玉米[8.].在之前对c2h2 -锌手指转录因子蛋白的研究中,发现它们在促进植物生长发育中具有重要作用[9.].c2h2 -锌指状蛋白构成高等生物基因组中蛋白质的主要部分[10].它们发挥不同的功能,包括DNA的识别、RNA的包装、转录的激活、凋亡的调节、蛋白质的组装和折叠以及脂质的结合[11].此外,c2h2 -锌指转录因子蛋白广泛参与生物和非生物胁迫等各种过程[12,叶毛状体发育[13,花细胞器[14[拟南芥中的种子萌发和原发性microRNA生物发生[15].在水稻、大豆和杨树中,c2h2 -锌指蛋白确实增强了对寒冷和干旱胁迫的适应[16那17那18].据报道,C2H2-锌手指基因确实促进了病原体防御甜椒[19].此外,一种新的基因,AtGIS,被发现能促进转基因烟草毛状体的发育[20.].在棉花中,C 2 H 2-锌指蛋白质家族在纤维起始阶段下调在模糊和较少(fl)突变体21],发现几个c2h2 -锌指基因在Ligon-lintless-1中下调,而在野生型中上调[22].最近,与野生型相比,c2h2 -锌指基因被认为是控制Ligon-lintless-2突变体棉纤维发育的候选基因[23].种植棉花主要是为了生产天然纤维和籽油[24]在全世界80多个国家[25].纺纱技术的进步在长度和细度方面创造了对高纤维质量的需求,此外,棉纤维发育过程通过四个重叠阶段,即引发,伸长,二次电池壁形成和成熟[25]纤维引发,伸长率和次级细胞壁对纤维的数量,长度和细度产生很大影响,这是确定棉绒质量和产量数量的主要因素[25].棉纤维的伸长阶段在起始阶段后立即开始,持续3周,此后纤维细胞转向二次细胞壁的密集沉积[26棉纤维不仅是世界纺织工业的天然资源,而且是检测棉纤维发展中基因表达的优良系统[26].因此,深入了解棉花纤维开发的分子基础将提供所需的信息如何提高棉纤维长度,这是确定纺织工业中纤维质量的主要因素。棉C2H2-锌手指蛋白的综合分析及表征及其在全多大倍棉中的进化时间,可能有利于揭示棉纤维发育中的关键基因或分子机制。
此外,目前发表了g .分子(Upland棉)基因组序列[27],g . arboreum[28),G.raimondii[29,为棉花c2h2 -锌指蛋白的整体鉴定和表征提供了有价值的信息。系统发育分析表明,陆地棉与玉米、可可、V. Vinifera.、拟南芥和p . trichocarpa.raimondii和arboreum经过大约166万年前(Mya)的全基因组重复事件,以及从近1.5 mya的杂交中出现的Upland棉花(同种异体四倍体),其产生高品质的纤维,与其二倍体亲属相比。为了了解锌比较基因的所有增加或减少,可能导致棉纤维发育动态的任何变化。此外,Upland棉是一种多倍体物种,其基因组含有母体基因组(g . arboreum像一个 - 基因组)和父亲基因组(G. Raimondii.比如D基因组)[30.].与其他植物物种相比,关于棉花c2h2 -锌指状蛋白的信息很少[23].在高等植物中,c2h2 -锌指蛋白是主要的转录因子家族之一,在调控棉花纤维发育的不同途径中可能发挥重要作用[2].本文对棉花c2h2 -锌指蛋白家族及其在棉纤维发育中的表达进行了综合分析。结果共鉴定出386、196和195个c2h2 -锌指状蛋白g .分子那g . arboreum和G. Raimondii,分析了它们的染色体位置、重复基因事件、系统发育关系、基因结构、保守基序和不同发育阶段的表达谱。
结果
棉花c2h2 -锌指蛋白家族的鉴定
在对所有C2H2-锌指基因成员的鉴定中,在全棉基因组中,从Pfam数据库(http://pfam.sanger.ac.uk/)并用来针对整个棉蛋白质组序列进行查询。我们鉴定了Upland棉花的420,236和230c2H2-锌手指候选基因,g . arboreum和G. Raimondii,分别。此外,SMART对检索到的序列进行物理检查(http://smart.emblheidelberg.de /)检查C2H2-锌指蛋白结构域的存在或不存在。最后,在Upland Cotton中鉴定了386,196和195 C 2 H 2-锌手指基因,g . arboreum和G. Raimondii,分别含有一个或多个C2H2-锌指蛋白域(附加文件5.:表S1)。结果与植物转录因子数据库(http://planttfdb.cbi.edu.cn/) [31]其中仅发现318名C2H2-锌手指家族基因的成员g .分子.这种差异可能是由于改进了基因注释。陆地棉c2h2 -锌指蛋白的长度范围为101 ~ 1614个氨基酸,平均374个氨基酸。为了了解被研究基因编码的蛋白质可能的功能,了解它们的理化性质是不可避免的,例如蛋白质可以根据它们的分子质量(大小)和等电点(电荷)性质进行分离,然后再决定它们的丰度[32].酶的等电点性质是有意义的。通过酶在载体上的运动,缓冲器应具有支持与载体表面静电相互作用的pH值[32].此外,在估计植物中任何给定的蛋白家族时,都要考察不同的生理特性,例如棉花中的蔗糖合酶蛋白家族,等电点、分子量等因素都被考虑在内[33].通过ExPaSy分析鉴定其分子量,分子量在11059.09 ~ 182448.43 Da(道尔顿)之间变化较大,平均为41473.5 Da。利用WoLF PSORT分析对386个c2h2 -锌指蛋白的亚细胞定位进行了预测,结果显示351个c2h2 -锌指蛋白定位于细胞核内,这与它们与DNA相互作用的功能相符[1].然而,仅35 C2H2锌指蛋白分别位于不同的亚细胞膜,例如叶绿体,液泡,质体胞质溶胶和线粒体中。C2H2锌指蛋白的详细信息在(附加文件中列出6.:表S2),包括蛋白质结构域,蛋白质长度,分子量和亚细胞位置。另外,在高地棉花中鉴定了大部分C 2 H 2-锌手指基因,而不是二倍体棉基因组g .分子是一种多倍体,通过全基因组重复(WGD)出现[34].
棉花c2h2 -锌指基因的染色体分布
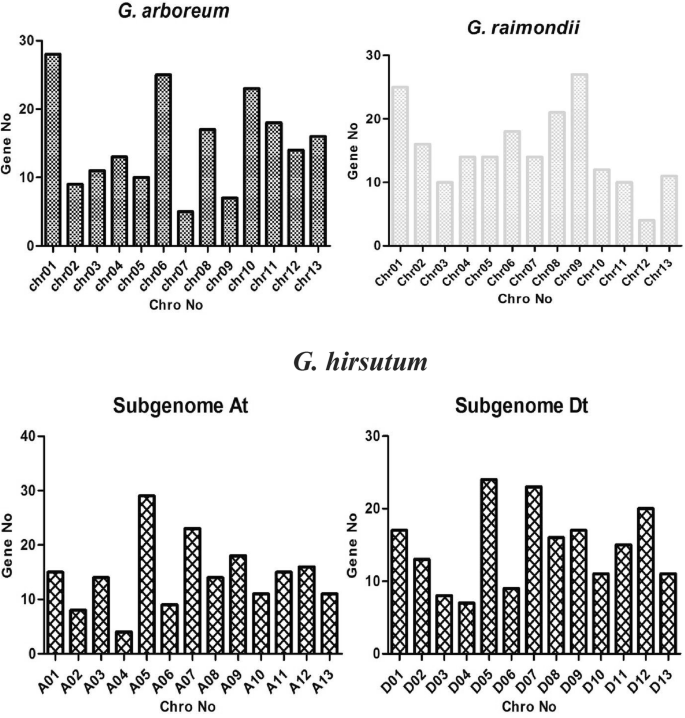
利用全棉基因组序列检索的数据集,分析c2h2 -锌指基因的染色体位置。378个陆地棉c2h2 -锌指基因在所有染色体上被定位,并根据其染色体位置进行命名GHZF.1到GHZF.378,虽然只有8GHZF.基因未被映射到任何引用支架的染色体并指定为GHZF.379年到GHZF.386.一百九十六(196)g . arboreum(一个2)和195G. Raimondii.(D5.)C 2 H 2-锌指基因全部映射到染色体并根据其染色体位置命名。在不同染色体上的C 2 H 2-锌指基因的分布不均匀(图。1);例如;一些染色体和基因座,具有高密度的C2H2-锌指基因,而其他染色体没有(图。1和附加文件5.:表S1)。在染色体A05(AT)及其同源物染色体D05(DT)上检测到最高密度,其中同源物染色体D05(DT),而在染色体A04及其同源物染色体D04上检测到最低密度,具有11个基因(附加文件1:图S1)。此外,相对大量的C 2 H 2-锌指基因位于一些染色体的特定区域,例如上部和下厘米区域。在g . arboreumc2h2 -锌指基因在1号染色体上最多,有28个,在9号染色体上最少,有7个。而在G. Raimondii,9号染色体c2h2 -锌指基因最多,为27个,12号染色体最少,为4个。1).
陆地棉c2h2 -锌指基因复制事件
基因复制,串联和节段性重复事件已被证明是在植物中引发基因家族表达的两个主要机制[35].研究了重复事件,目的是解释隆起棉C2H2-锌指转录因子家族的多样化机制,这在整个基因组进化过程中出现了[36].基于对准序列长度和对准区域的相似性,确定了37基因对参与两个串联和节段性重复事件,36基因对,在和DT,表现节段性重复且仅一对,在染色体甲5.,串联复制(表1).为了探讨多倍化复制后C2H2-锌指基因发散的机制,估计在Upland棉中的同源基因对的非同义(KA),同义(KS)和KA / Ksg .分子.如果,则Ka / Ks的值超过1表示阳性选择或有利选择下的演变,并且一些突变事件最有利可图。如果,ka / ks比率= 1表示中性选择。Ka / ks比例小于1表示阴性选择或突变限制具有缺点效果,在其他文献中,它被称为纯化选择。在37个重复的基因对中,29具有低于1的KA / Ks比,表明C2H2-锌指基因主要在阴性选择的影响下进化,或者它们的突变具有不利影响。Ka / ks比例小于1给出了在重复事件后蛋白质水平的慢速演化的C2H2-锌指基因的强烈指示。然而,只有8个C 2 H 2-锌指基因的KA / Ks比率超过1,表明这些基因已经通过阳性选择演变。这是一个显着的证据,注意在阴性选择下演化的大多数普满棉C2H2-锌手指基因。此外,我们使用KS计算高于棉花基因组的进化时间期间的复制事件的时间。旱地棉中的串联和节段性重复事件发生在0.25和3.56 mya(百万年前)之间,平均为1.05 mya,这与全那时性棉花的全基因组重复一致[27那37].结果表明,旱地棉中的C2H2-锌手指基因的扩展,源于a2和D5.基因组,大多是从全基因组复制事件的进化过程中产生的。
C2H2-锌手指蛋白质棉与其他植物的关系
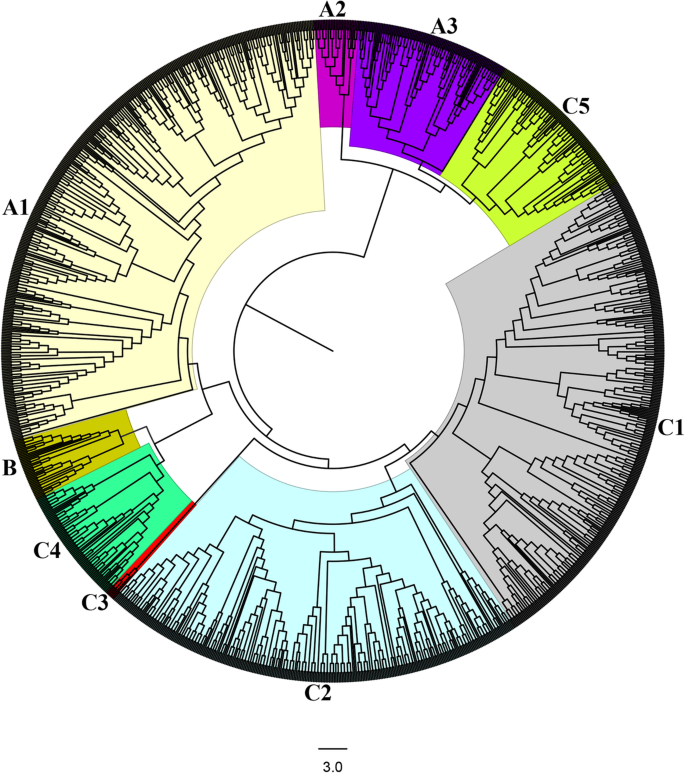
进一步分析了C2H2-锌手指蛋白家庭在棉花等植物中的进化关系386万亿棉,196 g . arboreum195年G. Raimondii,97年t .可可, 179年Z. Mays.,64. V. Vinifera., 118年p . trichocarpa和60答:芥采用mega6软件的neighbor-joining (NJ)方法构建系统发育树。根据序列相似性和树状结构,将c2h2 -锌指蛋白分为A、B、C三个主要类群(见表1)2).三组C2H2-锌手指蛋白的数量不同,C组含有最大数量,其次是A组,而B组具有C2H2-锌指蛋白的数量最少。结果与其他植物中的早期发现有关这些基因在各种分组中的定量[2].最后,三个主要组(A, B和C)进一步细分为不同的子组A1, A2, A3, B和C1到C5(图5)。2和表2).在这个细分中,我们认为这个家庭被深刻表征的其他工厂中的群体的先前注释拟南芥[2],Z. Mays.[8.),p . trichocarpa[7.].总的来说,A1亚群中检测到的基因数量最多,有366个,C1亚群次之,有312个,而C3亚群中c2h2 -锌指基因最少,只有6个。结果表明,8种植物包含7个c2h2 -锌指基因亚群,这为这些植物在c2h2 -锌指转录因子家族扩展后发生分化提供了有力的证据。棉花基因组中c2h2 -锌指基因的分布远高于其他植物,在棉花基因组中,除B亚群和C3亚群外,陆地棉所有亚群中c2h2 -锌指基因的数量均最高(表2)2).此外,还进行了一项独特的观察,发现有些进化支完全由来自某一特定植物物种的基因组成,这些基因被称为同源基因对,因为在一个物种内同源基因彼此之间存在差异[38].为鉴定陆地棉、棉、棉之间的同源c2h2 -锌指基因,arboreum, G. raimondii, Z. mays, T . coco那V. Vinifera.那一个.thaliana和p . trichocarpa.在陆地棉与其他植物之间未检测到同源基因,但在陆地棉与其他植物之间共检测到154对同源基因g . arboreum和165之间的陆地棉花G. Raimondii。所有正交基因主要存在于高地棉花和二倍体棉之间那陆地棉花的起源是什么G. Raimondii.和g . arboreum.该发现意味着C2H2-锌手指基因主要来自整个进化期间的全基因组重复事件。结果表明,棉C2H2-锌手指蛋白与来自可可的CACAO蛋白比任何其他植物物种更密切相关,因此与早期的报告一致,表明棉花和可可从同一祖先中出现[28].
为了探讨多倍体复制后c2h2 -锌指基因分化的机制,我们估算了同源基因对之间的Ka、Ks和Ka/Ks值G. Arboreum(一种2),g .分子(亚基因组),以及介于两者之间的基因G. Raimondii.(D5.),g .分子(Dt子基因组)。Ka/Ks比值的值是在进化过程中作用于蛋白质编码基因的选择压力的指标(附加文件7.:表S3)。基于该结果,我们发现,152 C2H2锌指基因对A2 /在,147有嘉/ Ks率小于1,这表明C2H2锌指基因已稳定化选择的作用下在三个棉花物种主要演进.然而,只有5 C2H2锌指基因有嘉/ Ks率超过1,从而通过正选择演变。此外,165 C2H2锌指基因对D5 / DT,151有嘉/ Ks的小于1表示阴性选择的。While only, 13 gene pairs had a Ka/Ks ratio more than 1 suggested positive selection and 1 gene pair had a Ka/Ks ratio = 1 suggested neutral section (Additional file7.:表S3)。值得注意的是,较大百分比的正交棉C2H2-锌手指基因g . arboreum或G. Raimondii.在稳定选择的影响下进化,因此这些基因在重复事件后蛋白质水平缓慢进化并具有保守的特征。
陆地棉c2h2 -锌指基因家族的系统发育树、基因结构及保守基序分析
通过进行邻近的系统发育树分析,通过建立一个邻近的邻近的系统,通过邻近接合方法建立一个综合的系统发育树,通过建立一个综合的系统发育树,通过邻近加入方法进行了综合的系统发育树分析。基于蛋白质序列相似性,将Upland棉C2H2-锌手指蛋白质分为七个亚组(I至VII),其数在4至105个基因中变化(附加文件2:图S2A)。用最小进化法检验系统发生树的可靠性。上面提到的两个方法创建的树是相同的,这意味着两个方法彼此是一致的(附加文件)3.:图S3)。
进一步研究陆地棉c2h2 -锌指基因的外显子-内含子结构,发现51.6%(199)的c2h2 -锌指基因无内含子,48.4%(187)的c2h2 -锌指基因有1 ~ 10个内含子。此外,大多数含有内含子的c2h2 -锌指基因,101个含有1或2个内含子,其余的则被2个以上的内含子干扰(附加文件)2:图开通)。然而,大多数无内含子基因(199个)聚类为亚群I和亚群II。此外,通过系统发育胁迫分析进一步评估了c2h2 -锌指基因亚群的内含子-外显子相似性。此外,大多数聚类的c2h2 -锌指基因在外显子长度和外显子数目上表现出高度的相似性。例如,95个基因聚集在亚群I中,除了只有6个基因有一个内含子外,更多的基因是无内含子的。在V亚群和VI亚群中,c2h2 -锌指基因的外显子长度和内含子数量差异很大,从0到10个不等2:图开通)。Upland棉C2H2-锌指基因的外显子内部结构与系统发育树分析几乎一致。
为了进一步分析I ~ VII亚群386个c2h2 -锌指蛋白的保守基序多样性,使用MEME工具进行分析。在c2h2 -锌指蛋白中鉴定了20个保守的motif,分别为motif 1到motif 20(附加文件)2:图S2D)。同一亚群中的大部分c2h2 -锌指蛋白在基序组成和分布上都有一个共同的基序,表明同一亚群中的c2h2 -锌指蛋白成员可能具有相似的功能。然而,在不同的亚组之间也表现出很大的差异。例如,亚群I的所有蛋白序列都有motif 1和7,包含QALGGH和WSKRKRSKRPR motif,而亚群II的motif 1、2和4包含两个QALGGH motif结构域和一个LDLDL motif (Additional file)4.:图S4),之前在高等植物中描述了[3.].在亚组中,IV和V的motif 5描述为ALGGH(附加文件2:图S2D)。保守基序1和2包含QALGGH和ALGGH基序,这两个基序此前被报道参与植物生长发育过程中的非生物胁迫响应[3.].此外,在特定亚组中观察到一些独特的基序,其提供了较强的植物在植物内特定功能中这些基板的参与的指示。
为了确定高地棉C2H2-锌手指蛋白的相似性,我们将386个Upland棉C2H2-锌手指蛋白序列对齐,每个子组I到VII(附加文件8.:表S4)。基于多序列比对结果,我们发现整个陆地棉c2h2 -锌指蛋白含有3个主要motif域q型(QALGGH motif)、z型和c型,其中陆地棉c2h2 -锌指蛋白分别有196、105和85个。q型结构域包含两个主要的基序QALGGH和ALGGH,除这两个基序外,一些蛋白序列还包含LDLDL、FDLDL和IDLDL基序,此前有报道称这些基序在植物的防御系统中起着至关重要的作用[3.].此外,含有锌手指的Q型,但在第二位置的半胱氨酸残留物由酪氨酸改变并在亚组I,II,IV和v中聚集,如黄色所示(附加文件8.:表S4)。锌指z型在手指和侧翼区域的基模极为保守,之前被注释为c型[39].所有陆地棉c2h2 -锌指基因均属于z型,聚在第VII亚群中,如绿色所示(附加文件)8.:表S4)。c型锌指与q型、z型锌指相比,在锌指区域没有保守基序,主要聚集在III、VI亚群中。为进化关系和系统发育树分析的可靠性提供了有力的支持。
旱地棉C2H2-锌手指基因在不同发育阶段的表达谱
基因表达水平和功能是高度相关的,并提供关于C2H2-锌指基因是否实际参与调查过程中的过程的重要信息。C2H2-锌指基因主要涉及各种植物细胞分化和发育机制,例如培养体引发[40,花细胞器[14]和根发发育[41].所有Upland棉C2H2-锌指基因的表达水平在0,3,5,10,20和25dPA的各种植物组织上,使用公共可用的RNA-SEQ数据(prjna248163)[27].结果表明,378个c2h2 -锌指基因在棉纤维发育的至少一个组织或阶段表达,而只有8个陆地棉c2h2 -锌指基因的表达无法通过RNA-seq分析检测到2:图S2C和附加文件9.:表S5)。此外,c2h2 -锌指基因在棉纤维不同发育阶段表达水平差异较大,少数表达水平相同。基于系统发育树分析,将c2h2 -锌指基因家族的表达水平划分为7个亚群。在只包含一个QALGGH基序的亚群I中,除了4个基因外,这些基因中的大量基因在几乎所有检测的组织中都以较低水平表达,GH_A05G2741那Gh_D05G3769那gh_a04g0449.和Gh_Sca045498G01,这是同源的AT2G41940基因编码拟南芥锌指蛋白8,在野生型棉纤维发育起始阶段0和3 DPA高度表达。子群1的两个成员,Gh_D13G0287和gh_a13g0268在棉纤维发育伸长后期25 DPA高度表达。在茎组织中,表达量最高的是在Gh_D02G1695和Gh_A03G1255,这是同源的AT1G10480该锌指蛋白在ZFP6下游通过整合赤霉素(GA)和细胞分裂素信号调节毛状体发育。[13].在纤维发育阶段,这两个基因在0dPa下表达更高的表达水平,但在其他纤维开发阶段的表达显着降低(附加文件2:图S2C和附加文件9.:表S5)。该结果表明这些基因可以直接或间接地涉及棉纤维发育,主要是引发阶段的强烈。在亚组II中,与亚组I的亚组II基因相比,包括GH_D05G2011(包括GH_D05G2011),其中包括GH_D05G2011的亚组II基因,许多基因和具有LDLGL,FDLDL和IDLD基序的那些基因显着较高,Gh_A05G1815那Gh_D06G2303那Gh_A01G0984那gh_d01g1033那Gh_A02G0836那gh_d13g0451那Gh_A13G2112等等。其中部分基因在棉花纤维发育过程中存在差异表达,可能参与了棉花纤维发育不同阶段的调控机制。大量含有ALGGH基序的基因被发现是IV亚群的成员,其中包括:Gh_A09G0743那gh_d09g0744那Gh_D10G0401和Gh_Sca004883G01(附加文件2:图S2C)。亚组IV的成员在测试的所有组织中显示出类似的表达,但具有较低的表达水平。在亚组v中,含有藻类基序的8个基因,表达水平非常低,所有棉纸组织的零标记除外,gh_d01g1111.和gh_a01g1056在测试的不同组织中略高但相似的表达模式(附加文件2:图S2C)。这一结果给出指示,这些基因与QALGGH和ALGGH图案可能的棉株生长发育的特殊条件下参与了具体的发展阶段。大多数在亚组III的基因的表现出差异表达在不同棉花组织中,但相比于根,叶和茎组织在棉花纤维发育的起始和延长阶段高度表达。在子组VI,许多基因具有比组,基因的其余部分更高的表达水平gh_d05g0849.那Gh_D02G2408那Gh_A03G0820那Gh_A05G0702那gh_d01g2032那Gh_D05G0663那Gh_A09G0878在根、茎、叶和纤维发育的不同阶段表达水平存在差异,说明VI亚群成员可能在棉花纤维发育的调控中发挥重要作用。在亚群VII中,少数基因在各组织中表达量较低,而大量基因在茎秆和棉纤维发育中表达量较高,包括:Gh_A02G0617那Gh_D02G0671和其他人。一般来说,一些同源陆地棉c2h2 -锌指基因对在dt -亚基因组和at -亚基因组中均有表达,例如:Gh_D02G1695和Gh_A03G1255在5和20dPA时显示出茎和棉纤维发育中类似的表达水平。Gh_A10G1921及其同源gh_d10g2215在20 dPA的根本,叶和纤维发育中同样表达。具有相似表达图案的副骨基因对具有比具有不同表达水平的副骨基因对更高的序列相似性[42].该结果暗示一种基因对的重复表达水平足以保持棉纤维发育,而另一个基因对的表达水平足以涉及其他调节过程。
c2h2 -锌指基因及其与棉纤维突变的关系
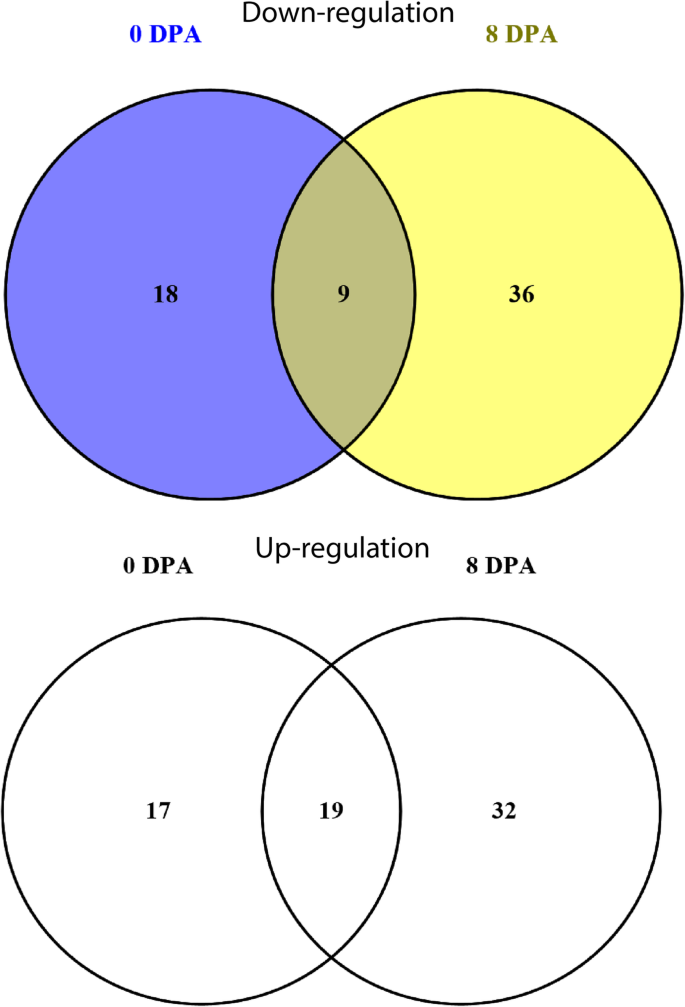
为深入了解c2h2 -锌指基因在棉纤维发育中的作用,利用0 DPA和8 DPA时Ligon-lintless-1突变体和野生型的RNA-seq转录组数据分析了c2h2 -锌指基因的表达模式。研究了c2h2 -锌指基因在棉纤维发育起始和伸长阶段的表达分析。多个c2h2 -锌指基因表达水平差异显著(fold change≥2和P.-值≤0.05)。结果表明,Li1突变体和野生型在0 DPA和8 DPA处分别有63和96个c2h2 -锌指基因的差异表达10:表S6)。总共27和45个基因表现出显着的下调,而36和51个基因分别在0和8dPa分别表现出棉纤维发育的显着上调(图。3.和附加文件10:表S6)提供了在Ligon-inlless-1的起始和伸长阶段和其野生型期间正面或负面控制纤维显影的线索。与野生型相比,在Li1突变体中具有更高调节的C 2 H 2-锌指基因,这可能意味着这些基因可参与调节突变棉中的棉纤维发育。此外,本研究的结果显示大多数差异表达基因在纤维发育(8dPA)的特定阶段特异性表达,这表明这些C2H2-锌指基因在调节棉纤维的各个阶段发挥关键作用发展。
RT-qPCR验证c2h2 -锌指基因表达
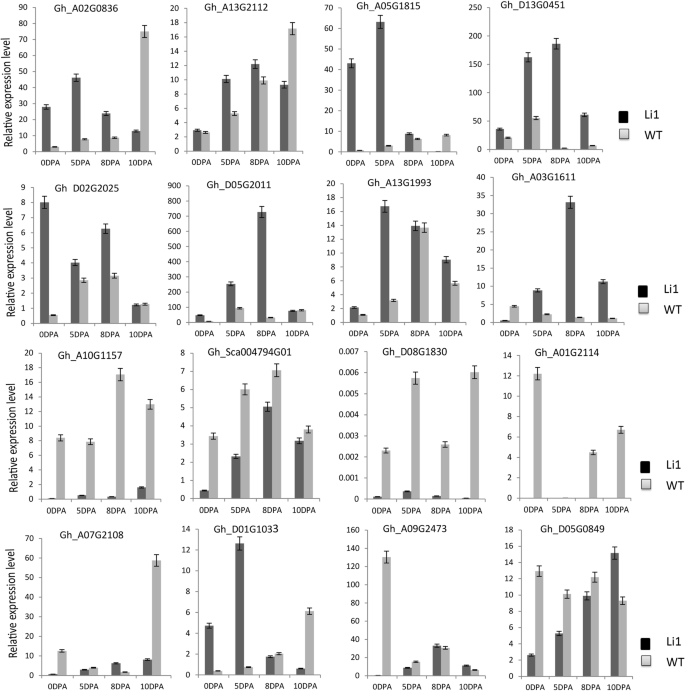
为了检查这些差异表达的C 2 H 2-锌指基因在引发和伸长级的棉纤维发育中具有作用,基于棉纤维发育的启动和伸长级的表达模式选择16个C 2 H 2-锌指基因,8受调节基因(Gh_A02G0836那Gh_A13G2112那Gh_A13G1993那gh_d13g0451那Gh_D05G2011那gh_a03g1611那Gh_D02G2025和Gh_A05G1815)8个下调基因(Gh_A07G2108那gh_a10g1157那GH_SCA004794G01那gh_d05g0849.那gh_a09g2473那gh_d01g1033那gh_a01g2114和Gh_D08G1830),其在纤维发育的开始和伸长阶段进行差异表达。RT-QPCR用于在棉纤维,0,5,8和10dPa的不同阶段验证Li1突变体和野生型中C2H2-锌手指基因家族的表达水平(图。4.).在棉纤维发育过程中,所有的c2h2 -锌指基因在Li1突变体和野生型之间都表现出不同的表达谱。Gh_D02G0836那Gh_A13G2112那Gh_A05G1815那Gh_D02G2025和Gh_D02G2011基因在Li1突变体中高于野生型在0,5和8,但不在10dPa。结果表明,该组基因在工艺纤维发育中具有抑制作用。此外,Gh_A13G1993和gh_d13g0451基因在Ligon-lintless-1中完全表达,在所有纤维发育中都有高表达水平(不同的测试时间),但在野生型中没有。gh_a03g1611与野生型相比,Li1突变体在5、8和10 DPA处表达量高,而在0 DPA处表达量低。这一结果与RNA-seq分析结果一致,Li1突变体中这些基因均较野生型上调,表明这些基因可能在纤维起始和发育的正常过程中起到抑制作用。相反,8个下调c2h2 -锌指基因,如gh_a10g1157那GH_SCA004794G01那Gh_D08G1830和gh_a01g2114Ligon-lintless-1突变体在棉纤维发育的各个阶段表达量较低,表明这些对突变体棉纤维的正常发育很重要。其他一些c2h2 -锌指状基因,如Gh_A07G2108那gh_d01g1033那gh_a09g2473和gh_d05g0849.在野生型和Ligon-lintless-1突变体中均有不同水平的表达,表明c2h2 -锌指基因在棉纤维发育的起始和伸长阶段存在功能分化。
讨论
C2H2-锌手指蛋白家族已被识别拟南芥,大米和杨树[2那7.那8.].有趣的是,没有以前的报告已经在棉花上展示。在这项工作中,我们对棉花C2H2-锌手指基因家族进行了全面分析及其参与棉纤维开发。我们鉴定了Upland棉的386,196和195个非冗余C2H2-锌手指基因,g . arboreum和G. Raimondii.,分别(附加文件5.:表S1)。陆地棉是由天然杂交得来的g . arboreum和G. Raimondii.因此,自然会找到196个后代的两个副本g . arboreum和195年G. Raimondii.高地棉花中的C2H2-锌指基因。然而,它在隆起棉C2H2-锌指蛋白的总数中检测到,其中Upland棉中的386中仅为317ghC2H2-锌指蛋白具有相应的蛋白质序列g . arboreum和G. Raimondii.哪个是二倍体父母线。旱地棉花和二倍体棉之间发现了大多数原基因基因那这是由于普满棉花出现的起源G. Raimondii.和g . arboreum,通过整个基因组的多倍体化在它们的过程进化[43].我们的结果表明,杂交后可能有某些方面的基因丢失。棉中c2h2 -锌指蛋白与棉中c2h2 -锌指蛋白亲缘关系更密切t .可可与其他任何植物相比,棉花和可可有一个共同的祖先[28].
24对同源基因的Ka/Ks比值均小于1,说明这些基因主要是在负选择条件下进化的。这一发现与最近的报道一致,该报道发现大多数MYB转录因子基因是在负选择下进化的[44].基因复制,串联和节段性,对扩展基因家族的数量非常重要[35].在高地棉花基因组重复的C2H2-锌手指基因家族的演化和多样化中,节段性类型的基因重复发挥了重要作用,这也与先前的研究结果一致[8.].通过计算基因对复制日期,陆地棉c2h2 -锌指家族的基因复制事件与全陆地棉基因组复制时间尺度(1-2 MYA)一致[27那37].
陆地棉c2h2 -锌指蛋白序列在蛋白质长度、分子量和亚细胞位置等方面存在较大差异,具有高度的复杂性。这些结果表明,这些基因可能根据其在植物细胞中的确切位置,在植物生长发育中发挥不同的功能,从而与早期的研究结果一致,即c2h2 -锌指家族参与植物生长发育的各个方面[3.那16那19那22].系统发育树分析表明,同一亚群中的大部分c2h2 -锌指基因具有相似的外显子-内含子结构和保守的基序,但不同亚群之间存在较大的差异。提示蛋白排列相似的c2h2 -锌指状家族成员可分为相同的亚群。此外,某些外显子-内含子结构和基序组成主要存在于某一特定亚群中,这可能与该亚群的功能多样性有关。本研究发现,c2h2 -锌指家族的内含子-外显子结构、保守基序与系统发育树分析之间存在较强的联系g .分子。通过对c2h2 -锌指蛋白的多重比对,我们确定了c2h2 -锌指的3个主要亚类,包括q型、z型和c型。q型锌指包含一个保守基序QALGGH,该基序主要是植物特有的,而c型锌指和z型锌指同时存在于植物和其他生物中[39那45那46].结果表明三种不同亚类具有各种氨基酸序列基质,其可参与植物生长和发育的不同特征。例如,C2H2-锌手指家族的Q型已经在子组I,II,IV和V中聚集,并且仅亚组II包含先前报告的LDLDL,FDLDL和IDLDL主题的QALGGH图案(Q型)在植物生长和发展过程中发挥不同的功能[3.].
386个陆地棉c2h2 -锌指分子的表达谱,总共378个在陆地棉中被检测到,只有8个c2h2 -锌指分子的RNA-Seq数据无法检测到。这些c2h2 -锌指基因在不同发育阶段表现出广泛的表达水平。有趣的是,大多数属于I、IV和V亚群的c2h2 -锌指成员在不同组织中表达水平相对较低,这提供了更有力的证据,表明这些亚群中的许多c2h2 -锌指基因并不直接参与棉纤维发育(Additional file)2:图S2C)。在子组的某些成员II在棉花纤维的发育阶段中呈高表达。这个结果与先前的报告一致这表明,C2H2锌指蛋白基因与QALGGH图案和LDLDL,FDLDL和IDLDL图案是为了响应生物和非生物胁迫作用[3.那17那19].此外,AT1G10480 (ZFP5)与Gh_D02G1695和Gh_A03G1255,通过GA信令调节毛状体细胞开发的功能拟南芥, (13那47].这种基因的过度表达拟南芥蒂利亚纳,加速高水平的培养型启动[40].AT1G67030(ZFP6)与Gh_D09G0619通过整合细胞分裂素和赤霉素信号通路调控毛状体发育(起始)拟南芥.这两个拟南芥来自Upland棉的基因及其同源基因在纤维发育的不同阶段显示出低的表达水平,表明这些基因可以通过整合植物激素或植物途径来控制纤维开发中的负面作用。AT2G41940(ZFP8)和ZFP5相互作用,有助于对表皮细胞分化的调节[47].陆地棉c2h2 -锌指基因,GH_A05G2741那Gh_D05G3769那gh_a04g0449.和Gh_Sca045498G01(AT2G41940的同源物)在棉纤维的起始阶段(0和3 DPA)显著表达,而在伸长阶段不表达。c2h2 -锌指基因在Li1突变体和野生型纤维发育过程中存在差异表达。在0和8 DPA处理时,c2h2 -锌指基因分别有27和45个表达下调,而在同时期表达上调的c2h2 -锌指基因分别有36和51个表达上调。这为这些基因在Li1突变体和野生型棉纤维发育的起始和伸长阶段的参与提供了更有力的证据(图1)。3.).以前,据称,在起始和伸长阶段的棉花模糊纤维突变体中,C2H2-锌手指基因在棉花模糊纤维突变体中差异表达[48].在Ligon-lintless-2突变体中,c2h2 -锌指基因被认为是调控棉纤维发育的候选基因[23[相比之下,与Q型相比,属于亚组III,VI和VII(Z型和C型)的C2H2-锌指基因在棉纤维和组织中显着表达,这指出,它们可能参与调节棉纤维开发。之前的报道显示,在棉纤维发育的5和7dPa的Ligon-无抗-1突变体中,将一些C2H2-锌手指基因上调,下调在Ligon-无凝-1突变体中[22].Ligon-lintless-2中未检测到c2h2 -锌指基因的表达水平,但在野生型16 DPA中有显著表达[23].在Ligon-lintless-2突变体中,c2h2 -锌指基因被认为是调控棉纤维发育的候选基因[23]。此外,一些c2h2 -锌指基因可能与ligon - linless -1短纤维发育有关。本研究结果有助于阐明c2h2 -锌指基因在棉花纤维发育中的可能作用,并为进一步研究棉花c2h2 -锌指基因的分子和功能奠定基础。
结论
c2h2 -锌指基因家族是高等植物中最丰富的转录因子家族之一,在植物的生长发育中起着关键作用。本研究是首次全面分析c2h2 -锌指基因及其在棉纤维发育中的表达分析。陆地棉共有386、196和195个c2h2 -锌指基因,g . arboreum和G. Raimondii,分别。结果表明,C2H2锌指蛋白基因成员在整个棉花基因组分布。基于系统发生树分析,这些C2H2锌指基因成员分成7个亚组。同一子组内的C2H2锌指蛋白包含相似的外显子 - 内含子结构和蛋白质基序的组合物。此外,RNA测序数据表明,至少一些的C2H2锌指基因棉花纤维发育期间参与多种功能,而最陆地棉C2H2锌指基因的功能仍然不清楚。因此,需要进一步的研究,以确定一个这组植物王国中最丰富的转录因子的特定功能。棉纤维发育过程中的16个基因的表达谱,通过RT-qPCR的,表明不同C2H2锌指基因无论是在棉花纤维发育的调节正或负参与。根据我们的发现,C2H2锌指基因家族的表达水平是它们在各种生化和生理功能参与其起始和延伸阶段期间直接相关的棉纤维发育的一个指针。在这个家庭C2H2锌指蛋白的功能研究进一步的研究是必要的,以便了解在刺激棉花纤维发育及其相互作用和各种途径的规定。这项研究的结果提供了有关的C2H2锌指蛋白基因在棉花纤维发育中的作用进一步调查的基本信息,将成为对C2H2锌指蛋白基因在其他植物物种的进化时间进一步研究非常有用。
方法
纯棉中C2H2-锌指基因家族的鉴定
陆地棉花和G. Raimondii.(D5.)基因组序列从棉花族数据库中提取(http://www.ctongen.org.);g . arboreum(一个2)基因组序列下载自棉花基因组计划(http://cgp.genomics.org.cn/page/species/download).从Pfam数据库(http://pfam.sanger.ac.uk/)使用Hmmer 3.0软件用于鉴定棉基因组(蛋白质组序列)中的C 2 H 2-锌指基因[49, E值< 10−10.此外,从Arabidopsis数据库(Tair;)下载了C2H2-锌指蛋白的相应蛋白质序列http://www.Arabidopsis.org/),t .可可那Z. Mays.那V. Vinifera.和p . trichocarpa从植物转录因子数据库获得蛋白质序列(http://planttfdb.cbi.edu.cn/).因此,它们被用作查询序列,以识别通过对棉蛋白质组序列进行搜索而编码的所有棉C2H2-锌手指蛋白,然后通过所有搜索结果去除相同的序列。此外,为了确认衍生自选选棉C2H2-锌手指的蛋白质序列,使用域分析智能检查候选基因(http://smart.emblheidelberg.de/).仅取用于进一步分析与C2H2锌指结构域蛋白序列。所有冗余序列手工去除,导致在386个蛋白质序列g .分子含有C2H2-锌指域。此外,通过扩展服务器工具估计了Upland棉C2H2-锌指蛋白的等电点(PI)和分子量(http://web.expasy.org/compute_pi/).此外,WoLFPSORT (http://wolfpsort.org/)预测陆地棉c2h2 -锌指蛋白的亚细胞定位。
高地C2H2锌指蛋白的系统进化分析
高地棉花的多个序列对齐,G. arboreum, G. raimondii, T. coco那Z. Mays.那V. Vinifera.那p . trichocarpa和答:芥使用CLUSTALW进行C2H2-锌手指蛋白(http://www.clustal.org/clustal2/).用mega6.0软件构建系统进化树(http://www.mega软件网络/)使用邻居连接(NJ)算法和1000次bootstrap重复。用以下参数构造树:代换、泊松模型;数据子集使用,p-距离,两两删除;复制,引导分析与1000个重复。此外,利用最小演化法对NJ方法的结果进行了验证。利用陆地棉c2h2 -锌指蛋白构建了单独的系统进化树,以进行进一步分析。
外显子内部结构分析和保守的主题识别
基因结构显示服务器(GSDS 2.0,http://gsds.cbi.pku.edu.cn/index.php) [50]被用来执行外显子/内含子结构。模序阐明(MEME)系统的多重期望最大化(版本4.9.1,http://meme.nbcr.net/meme/) [51用于找到每个隆起棉C2H2-锌手指蛋白的保守基序。使用以下参数:“任意重复数量,最大矩阵-20,以及6到250的最佳宽度”。
染色体定位与基因复制
基于从棉花基因组序列检索的位置数据,C2H2-锌指基因位于棉染色体上。通过地图图表软件映射棉染色体上基因的分布。基于前一项研究中定义的标准鉴定了重复的基因事件,该标准鉴定了两个序列的对齐区域覆盖较长序列的> 80%,并且对准区域的相似性> 70%[52].DnaSP软件(版本5.10)[53]估计了非同义替换率(Ka)和同义替换率(Ks),并以类时钟率(λ)为1.5× 10,用eq. T = Ks/2λ计算复制事件的日期−6(妙)同义替代每10速率−8棉花年[54].
植物材料,RNA提取和RT-qPCR分析
两种陆地棉(g .分子Ligon-lintless-1 (Li1将突变体TM-1及其野生型(TM-1)种在中国农业科学院棉花研究所试验田,田间条件正常。Ligon-lintless-1 (Li1)是一种陆地棉花的突变体,具有异常的形态特征,如叶片、茎部扭曲,成熟种子上的皮棉纤维长度明显减少或短约4 - 6毫米[55].在开花阶段,在试验点进行开花前自花授粉标记。分别在花后0、5、8和10 d (DPA)采集Li1和野生型(TM-1)的C2H2-锌指基因表达情况。棉纤维是单细胞的、分枝的、简单的毛状体(或种子毛),它确实是从正在发育的种子外表皮中约25%的表皮细胞分化出来的[26].棉纤维发育的第一个明显迹象是在花期(开花期)那天[56].利用RNA Aprep Pure Plant Kit(天根生物技术,北京,中国)从胚珠和纤维中分离RNA。采用凝胶电泳和美国Thermo Fisher, Waltham, MA, USA开发的NanoDrop 2000分光光度计测定RNA样品的质量和浓度。采用Applied Biosystems公司7500 Real-Time PCR系统和SYBER premix ExTaq试剂盒(TaKaRa Bio Inc., Nojihigashi 7-4-38, Kisatsu, Shiga 525-0058, Japan)进行RT-qPCR分析。用SYBR Green荧光信号检测目的基因的扩增情况。g .分子β-肌动蛋白基因(GenBank登录No:AY305733)用作参考基因,并且基于棉纤维发育的引发和伸长级的表达水平,使用特异于16C 2 -2-锌指基因的引物。如Salih等人所述进行RT-QPCR程序和基因表达分析的详细信息。2016 [44].
使用公开的RNA-seq数据进行基因表达分析
野生型(TM-1)不同组织的rna测序(RNA-seq)数据(g .分子)从国家生物技术信息中心的数据库下载(http://www.ncbi.nlm.nih.gov/)在加入号码下(prjna248163)[27].为了估计不同发育阶段的基因表达水平,包括在0,3,5,10,20和25dPa的根,茎,叶和纤维,我们计算每种基因的表达使用FPKM(每千碱基每千碱基百万映射的读数)用袖扣(2.1.1版)[57](http://cufflinks.cbcb.umd.edu/).使用MeV_4_9_0软件生成热图并进行分层聚类[58].此外,利用Illumina测序技术对ligon - lintless1突变型陆地棉(TM−1)的棉纤维发育两个阶段(0 DPA和8 DPA)进行RNA-seq实验。RNA-seq数据被映射到整个基因组g .分子(tm-1)[27]使用TOPHAT2(v2.0.9)软件[59].袖扣(v2.1.1)软件[57]构建棉花转录组,然后进行转录丰富度组装和差异亚型分析。计算0 DPA和8 DPA时棉纤维发育不同发育阶段的基因表达水平。通过汇总各基因组转录本的FPKMs计算基因FPKMs。使用DESeq R软件包(1.10.1)对两种试验条件进行不同基因表达的Fold change分析及相关统计计算[60].由此产生的P.- 使用Benjamini's和Hochberg的方法调整值,以控制虚假率[61].只有基因与调整P.-value≤0.05为差异表达。
数据和材料的可用性
支持本研究结果的所有相关数据集均可在手稿及其补充文件中找到。
缩写
- DPA:
-
黄花木后天数
- DT:
-
四倍体的一个
- DT:
-
四倍体的维
- K a:
-
非同义替换率
- ks:
-
同义替换率
- Li1:
-
Ligon-inlless-1
- 米娅:
-
百万par岁
- TFS:
-
转录因素
参考
- 1.
Takatsuji H.锌手指蛋白:古典锌手指在现代植物科学中出现。植物mol biol。1999年; 39:1073-8。
- 2.
关键词:锌指蛋白,基因工程,基因工程abstract拟南芥蒂利亚纳基因组。BMC基因组学。2004;第五章39节。
- 3.
Kiełbowicz-Matuk A.植物c2h2型锌指转录因子在胁迫响应中的参与。植物科学。2012;185 - 186:78 - 85。
- 4.
Cys2His2锌指蛋白的DNA识别。生物物理学报2000;29:183-212。https://doi.org/10.1146/annurev.biophys.29.1.183.
- 5.
植物锌指转录因子的研究。细胞生物学杂志。1998;54:582-96。
- 6.
高胜二,森敏,Benfey PN, Ren L, Chua NH。在矮牵牛花花瓣和幼苗中特异表达的锌指dna结合蛋白的特性。EMBO j . 1992; 11:241-9。
- 7.
刘q,王z,徐x,张h,李立肝素锌 - 手指系列转录因子的基因组宽分析及其对杨树中非生物胁迫的反应(杨树trichocarpa)Plos一个。2015; 10:e0134753
- 8.
关键词:玉米,锌指基因,C2H2,功能特性Plant Mol Biol rep 2015:1-16。https://doi.org/10.1007/s11105-015-0958-7.
- 9.
王勇,窦东,王旭,李安生,华晨,等。编码C2H2锌指蛋白的PsCZF1基因在大豆疫霉菌的生长发育和发病过程中是必需的。活细胞Pathog。2009;47:78 - 86。
- 10.
Weirauch Mt,Hughes Tr。真核转录因子类型的目录,它们的进化原因和物种分布;2011年。https://doi.org/10.1007/978-90-481-9069-0.
- 11.
Laity JH, Lee BM, Wright PE。锌指蛋白:结构和功能多样性的新见解。《观点结构生物学》2001;11:39-46。
- 12.
作者单位:国家自然科学基金青年基金,国家自然科学基金青年基金,国家自然科学基金青年基金。拟南芥锌指蛋白3在种子萌发和植物发育过程中干扰ABA和光信号传导。植物杂志。2014;165:1203-20。https://doi.org/10.1104/pp.113.234294.
- 13.
周志强,孙丽,赵玉兰,安玲,严安,等。锌指蛋白6 (Zinc Finger protein 6, ZFP6)通过整合赤霉素和细胞分裂素信号来调控毛状体的起始拟南芥蒂利亚纳.新植醇。2013;198:699 - 708。
- 14.
dineny JR, Weigel D, Yanofsky MF。在拟南芥中,花蕊和心皮的形状主要表现为突起和锯齿状。发展。2006;133:1645-55。
- 15.
杨磊,刘志强,陆芳,董安,黄海涛。拟南芥microRNA转录过程中SERRATE的调控机制。植物j . 2006; 47:841-50。
- 16.
孙树军,郭树强,杨旭,鲍艳梅,唐慧娟,孙辉,等。水稻耐盐新基因Cys2/ his2型锌指蛋白的功能分析J Exp Bot. 2010; 61:2807-18。https://doi.org/10.1093/jxb/erq120.
- 17.
Zhang D, Tong J, Xu Z ., Wei P ., Xu L ., Wan qiang . Soybean C2H2-Type zinc finger protein GmZFP3 with conalggh Motif负调控拟南芥干旱响应,vol. 7;2016.1 - 9页。
- 18.
Gourcilleau D, Lenne C, Armenise C, Moulia B, Julien JL, Bronner G, et al.;植物q型C2H2锌指蛋白的系统发育及杨树响应渗透、冷和机械胁迫的基因表达分析DNA研究》2011;18:77 - 92。
- 19.
关键词:锌指转录因子,CAZFP1, Cys2/ his2,早期防御基因甜椒.植物mol biol。2004; 55:883-904。https://doi.org/10.1007/s11103-004-2151-5.
- 20.
刘毅,刘d,胡R,华C,阿里我,张A等人。AtGIS,从拟南芥C2H2锌指转录因子通过GA烟草信号调节腺毛发展。Biochem Biophys Res Communce。2017; 483:209-15。
- 21.
Padmalatha KV, Patil DP, Kumar K, Dhandapani G, Kanakachari M, Phanindra MLV等。无绒毛突变体的功能基因组学陆地棉l .简历。MCU5揭示了棉纤维起始和伸长的关键基因和途径。BMC基因组学。2012;13:624。https://doi.org/10.1186/1471-2164-13-624.
- 22.
Salih H,Leng x,他s-p,jia y,gong w,du x-m。使用微阵列的早期纤维发育基因的表征,Ligon-151(Li1)。植物基因。2016; 6:59-66。https://doi.org/10.1016/j.plgene.2016.03.006.
- 23.
Thyssen GN ., Fang DD ., Turley RB ., Florane C ., Li P ., Naoumkina M.下一代Ligon-lintless-2的遗传定位2)在陆地棉(陆地棉L.)。Al Appl Genet。2014; 127:2183-92。https://doi.org/10.1007/S00122-014-2372-1..
- 24.
张亮,李远达,陈彩平,田向超,陈向东,张伟,等。朝向异源四倍体棉花基因组组装:高密度分子遗传连锁图与DNA序列信息的整合。BMC基因组学。2012;13:539。https://doi.org/10.1186/1471-2164-13-539.
- 25.
Lee JJ,Woodward AW,Chen ZJ。基因表达变化和棉纤维发展中的早期事件。Ann Bot。2007; 100:1391-401。https://doi.org/10.1093/aob/mcm232.
- 26.
张志强。棉纤维的研究进展。见于:国际细胞学评论;1984.p . 65 - 113。https://doi.org/10.1016/s0074 - 7696 (08) 61300 - 5.
- 27.
张涛,胡勇,姜伟,方磊,关旭,陈建军,等。异源四倍体棉花的测序(陆地棉l . acc。TM-1)为纤维改良提供资源。生物科技Nat》。2015;33:531-7。
- 28.
李飞,范光国,王凯,孙飞,袁勇,宋光国,等。栽培棉花的基因组序列木本棉.Nat麝猫。2014;46:567 - 72。https://doi.org/10.1038/ng.2987.
- 29.
郭华,金东东,郭洪波,等。棉基因组的重复多倍体化与可纺棉纤维的进化。大自然。2012;492:423-7。https://doi.org/10.1038/nature11798.
- 30。
Xu Z, Yu JZ, Cho J, Yu J, Kohel RJ, Percy RG。多倍体化改变棉花基因功能(Gossypium spp。)plos一个。2010; 5:E14351
- 31。
金建军,张洪,孔林,高光,罗建军。植物转录因子功能和进化研究的门户。核酸学报2014;42:1182-7。
- 32。
Tartaglione A, Mazzeo C, Dell’Aversano M, Forino V, Giussani S, Capellacci A, Penna V, Asnaghi M, Faimali M, Chiantore T, Yasumoto P, Ciminiello P. Chemical, molecular, and eco-toxicological investigation of Ostreopsis sp. from Cyprus Isla. ABC. 2016;408:915–32.
- 33.
关键词:棉花,蔗糖合酶,基因家族,结构,系统发育,表达模式植物学报。2012;12(1):85。
- 34.
帕特森AH,文德尔JF。解开多倍体的织物。NAT BIOTECHNOL。2015; 33:491-3。
- 35.
引用本文:王志刚,王志刚,王志刚。基因复制在大基因家族进化中的作用[j]拟南芥蒂利亚纳.BMC植物BIOL。2004; 4:10。
- 36.
高W,Long L,Tian X,Jin J,Liu H,Zhang H等人。棉花中含有A20 / An1锌手指的应激相关蛋白(SAP)的基因组鉴定及表达分析。Mol Gen Genomics。2016; 291:2199-213。
- 37.
李F,风扇G,Lu C,Xiao G,Zou C,Kohel RJ等。培养旱地棉(Gossypium hirsutum TM-1)的基因组序列提供了对基因组进化的见解。NAT BIOTECHNOL。2015; 33:524-30。https://doi.org/10.1038/nbt.3208.
- 38.
植物的基因组编辑工具。基因。2017;8(12):399。
- 39.
Agarwal P, Arora R, Ray S, Singh AK, Singh VP, Takatsuji H,等。水稻C2H2锌指基因家族的全基因组鉴定及其系统发育和表达分析。植物学报。2007;65:467-85。
- 40。
周志,安霖,孙霖,甘云。©2012 Landes Bioscience。不要分发。2012; 7:28-30。
- 41.
安霖,周志,孙丽,严安,席伟,于宁,等。在拟南芥中,锌指蛋白基因ZFP5整合植物激素信号调控根毛发育。植物j . 2012; 72:474 - 90。
- 42.
杨志强,王志强,王志强,等。杨柳副亲本基因的基因表达及其序列分析。Nat Publ Gr. 2015:1-10。https://doi.org/10.1038/srep18662.
- 43.
Schnable JC,Wang X,Pires JC,Freeling M.逃离植物中重复全基因组重复后的优先保留。前植物SCI。2012; 3:1-8。
- 44.
SALIH H,GONG W,HE S,SUN G,SUN J,DU X.基因组的表征和MYB转录因子的表达分析陆地棉.BMC Genet。2016:1-12。https://doi.org/10.1186/s12863-016-0436-8.
- 45.
Isernia C,Bucci E,Leone M,Zaccaro L,Di Lello P,Digilio G,等。来自拟南芥超人蛋白的单个Qalggh锌指域的NMR结构。Chembiochem。2003; 4:171-80。
- 46.
拟南芥冷激结构域蛋白c -末端锌指结构域在冷适应过程中具有重要的RNA伴侣活性。植物化学。2010;71:543-7。
- 47.
周ZJ,LJ,Sun LL,朱SJ,XI WY,Broun P,Yu H,GaN Y.通过在拟南芥中的锌指蛋白8上游来控制培训蛋白的启动所必需的。植物生理学。2011; 111:180281
- 48.
万Q,张H,叶W,吴H,张T.基因组宽转录组分析揭示了具有与拟南芥类似分子模型的棉花模糊纤维发育。Plos一个。2014; 9:1-12。
- 49.
HMMER网络服务器:交互式序列相似性搜索。核酸学报2011;39(增刊):W29-W37。
- 50.
胡b,金吉,郭艾,张h,罗j,高g. gsds 2.0:升级基因特征可视化服务器。生物信息学。2015; 31:1296-7。
- 51.
Bailey TL,Boden M,Buske Fa,Frith M,Grant Ce,Clementi L,Ren J,Li WW,Noble WS。MEME SUITE:主题发现和搜索的工具。核酸RES。2009; 37(Web服务器问题):W202-W208。
- 52.
杨松,张旭,岳建新,田东,陈建强。在两种木本植物中,nbs编码基因的扩展主要是最近的重复。基因组学。2008;280:187-98。
- 53。
Librado P,Rozas J.DNASP V5:一种用于综合分析DNA多态性数据的软件。生物信息学。2009; 25:1451-2。
- 54。
王k,王z,李f,ye w,王j,歌g等。二倍体棉花棉质raimondii的基因组草案。NAT Genet。2012; 44:1098-103。
- 55。
李鹏,唐勇,李鹏,等。利用微阵列和标记分析短棉的转录谱(陆地棉L.)纤维突变体Ligon无无线-1(Li1)。BMC基因组学。2013; 14:403。
- 56。
Singh B,Avci U,Eichler Inwood Se,Grimson MJ,Landgraf J,Mohnen D等人。主电池壁的专用外层连接到伸长棉纤维的组织状束中。植物理性。2009; 150:684-99。
- 57.
Trapnell C,Williams Ba,Pertea G,Mortazavi A,Kwan G,Van Baren MJ,等。通过RNA-SEQ的转录程序组件和定量揭示了细胞分化期间未经发布的转录物和同种型切换。NAT BIOTECHNOL。2010; 28:511-5。https://doi.org/10.1038/nbt.1621.
- 58.
Howe E,Holton K,Nair S,Schlauch D,Sinha R,Quackenbush J. Mev:MultiExperiment Viewer。在:癌症研究的生物医学信息学;2010. p。267-77。
- 59.
Kim D,Pertea G,Trapnell C,Pimentel H,Kelley R,Salzberg SL。TOPHAT2:在存在插入,缺失和基因融合情况下转录om的精确对准;2013年。
- 60。
序列计数数据的差异表达分析。基因组医学杂志。2010;11:R106。https://doi.org/10.1186/gb-2010-11-10-r106.
- 61。
控制错误发现率:一种实用而强大的多重检测方法。J R Stat Soc. 1995; 57:289-300。
致谢
作者感谢中国奖学金委员会(CSC)本研究计划的支持者。
资金
本研究由国家科技支撑计划项目(No. 2013BAD01B03)和国家重点研发计划项目(No. 2016YFD0100203)资助。资助数字为研究项目提供了资金支持,但没有参与工作设计、数据收集、分析和手稿准备。
作者信息
从属关系
贡献
HS和WG进行了实验。HS起草了稿件。HS和SH进行了生物信息学分析。XMD监督了该项目。HS,MRO和XMD解释了数据并修改了稿件。所有作者都已经阅读并赞成最终的手稿。
相应的作者
道德声明
伦理批准和同意参与
不适用。
同意出版物
不适用。
利益争夺
两位作者宣称他们没有相互竞争的利益。
附加信息
出版商的注意事项
Springer Nature在发表地图和机构附属机构中的司法管辖权索赔方面仍然是中立的。
附加文件
额外的文件1:
图S1。棉花染色体上c2h2 -锌指基因的分布。每个c2h2 -锌指基因的染色体位置均定位于g .分子基因组。(PDF 96 KB)
附加文件2:
图S2。进行了旱地棉C2H2-锌指基因的系统发育树分析,基因结构和保守基序。(一种)由MEGA6.0软件通过邻近连接方法使用386 upland棉C2H2-锌手指蛋白的全长氨基酸序列来构建大型树木。基于系统发育树,Upland棉C2H2-锌手指分为七个主要亚组(I至VII组)和每个子组,用不同的颜色和(B.“旱地棉C2H2-锌指基因的外显子结构。黄色框代表外显子,黑线代表内含子和蓝色框代表上游/下游(UTRS)。可以使用底部的刻度来估计外显子和内含子的尺寸。(C)普通棉C2H2-锌指构件在不同组织(根,茎和叶)中的表达模式和纤维发育阶段的不同(0,3,5,10,20和25dPa)。表达水平由彩色棒表示。(D.)陆地棉c2h2 -锌指型成员和不同图案盒中保存图案的分布(图案1 ~ 20)。(TIFF 6685 kb)
附加文件3:
图S3。C2H2-锌手指蛋白家族的邻居加入(NJ)和最小演化方法g .分子.(TIFF 3125 KB)
额外的文件4:
图S4。高地棉花C2H2-锌手指基因家族的基序分析。使用MEME在线计划鉴定了普满棉TPS蛋白的20个推定的20个推定的保守基序。(PDF 300 KB)
额外的文件5:
表S1。棉花基因组中C2H2-锌指基因的位置,注释和蛋白质结构域。(XLSX 54 KB)
额外的文件6:
表S2。在陆地棉386 C2HC2锌指基因及其蛋白质序列的功能,包括,蛋白质的长度,分子量和亚细胞位置列表。(XLSX 23 KB)
额外的文件7:
表S3。同义替代率(KS)和非同义替代率(KA)在陆地棉及其祖先二倍体棉之间的每个正交基因对中表示,G. Arboreum(一种2),G. Raimondii.(D5.).(35 XLSX kb)
附加文件8:
表S4。陆地棉c2h2 -锌指蛋白的多序列比对。(PDF 494 kb)
额外的文件9:
表S5。各种发育阶段C2H2-锌手指基因的表达模式g .分子(TM-1)采用RNA-seq测定。(XLSX 49 kb)
额外的文件10:
表S6。通过RNA-SEQ测量Ligon-151-1和野生型(WT)中棉纤维发育的两个阶段C2H2-锌指基因的表达模式。(XLSX 38 KB)
权利和权限
开放获取本文根据创意公约署署署的条款分发了4.0国际许可证(http://creativecommons.org/licenses/by/4.0/)如果您向原始作者和源给出适当的信用,则允许在任何介质中进行不受限制的使用,分发和再现,提供指向Creative Commons许可证的链接,并指示是否进行了更改。Creative Commons公共领域奉献豁免(http://creativecommons.org/publicdomain/zero/1.0/)除非另有说明,否则适用于本文中提供的数据。
关于这篇文章
引用这篇文章
Salih H, Odongo M.R., Gong W.。等等。棉花c2h2 -锌指转录因子家族的全基因组分析及其在纤维发育中的表达分析BMC植物杂志19,400(2019)。https://doi.org/10.1186/s12870-019-2003-8
已收到:
公认:
发表:
关键词
- 比较基因组学分析
- C2H2-zinc手指家庭
- 棉花
- 纤维开发
- 系统发育