摘要
背景
在植物中,铵代谢对于将吸收的氮转化为氨基酸特别重要。然而,这种转化背后的分子机制在很大程度上仍然未知。
结果
使用野生型拟南芥(Col-0)和AtPDF2.1突变体(pdf2.1-1而且pdf2.1-2),我们发现富含半胱氨酸的小肽AtPDF2.1,一种植物防御素,参与调节茎部的铵代谢。铵显著诱导AtPDF2.1在茎部和根中,特别是在根木质部维管束中,如组织化学分析所示。亚细胞定位分析显示AtPDF2.1定位于细胞壁。突变体茎部铵浓度高于Col-0处理,但总氮含量、根铵浓度和铵转运体基因表达无显著差异AtAMT2.1.突变体中谷氨酰胺合成酶活性显著降低,谷氨酰胺合成酶家族基因活性显著降低GLN1.3而且GLN1.5与Col-0相比,突变体中显著下调。硝酸还原酶活性与Col-0无明显差异。
结论
总的来说,这些数据表明AtPDF2.1通过调控酶的表达影响铵代谢GLN1.3而且GLN1.5通过一种未知的机制。
背景
植物防御素(Plant defensins, PDFs)是富含半胱氨酸的小肽,通常由n端信号肽、c端可变区和富半胱氨酸结构域组成[1,2].对萝卜RsAFP1结构和同源性的核磁共振分析显示,该防御素具有一个共同的半胱氨酸稳定的α - β构象,在α螺旋上有四个二硫键,与三个β角反向平行[3.].植物防御素在动植物中普遍存在,并介导先天的非特异性免疫反应[4].在植物中发现的防御素大多具有广谱抗菌活性,可抑制淀粉酶和阻断离子通道[2,5].中已经报道了两个pdf家族拟南芥.第一个家族包含7个高同源性的成员(PDF1.1, PDF1.2a, PDF1.2b, PDF1.2c, PDF1.3, PDF1.4和PDF1.5),其中5个非常相似(PDF1.1到1.3)。此外,预测的PDF1.2a、b和c的成熟结构相似。第二家族的成员(pdf 2.1至2.6)也非常亲密。pdf2.1、2.3和2.6是串联序列,而pdf2.2和其他基因不在同一分支[2].以往对不同PDF基因的研究(PDF1.1,1.2,2.1,2.2,2.3)显示出它们的器官特异性表达模式[2,6].最近的研究证明PDFs也参与了非生物胁迫反应,它们的表达水平受到寒冷、干旱和重金属胁迫的诱导[7,8,9],而PDF2.3可能与钾离子稳态有关[10].最新研究表明,pdf介导水稻耐镉性和镉积累答:芥[11,12].
小肽可作为调控氮(N)反应和胁迫适应的信号分子[13,14].小c端编码肽(CEPs) [15],例如,由缺氮的根产生,并转移到芽中,在那里它们与富含亮氨酸重复受体激酶CEP受体1/2 (CEPR1/2)相互作用[13].根瘤菌诱导的木质部移动CLAVATA3/胚胎周围区域相关(CLE)肽已被证明可以抑制豆科植物的结瘤[16].虽然目前还不清楚pdf是否与N in相互作用答:芥,我们假设小PDFs也可能作为信号分子调节N代谢。
氮是植物必需的矿质元素,在植物生长发育中起着重要作用。它不仅是核酸、氨基酸和蛋白质的组成部分;它还作为叶绿素的组成部分参与光合作用期间的碳同化,并且在水稻中报道了N和磷之间的相互作用[17].硝酸盐和铵是植物吸收氮的主要形式。硝酸盐被植物吸收后,一部分直接运输到地上部分或储存在根细胞的液泡中,另一部分转化为铵或整合成氨基酸,代谢或运输到地上部分[18].
在农业生产中,施N肥一般有显著的增产效果[19,20.].然而,氮肥利用率低,不仅造成资源浪费和环境污染,还严重威胁人类健康。因此,提高植物氮素利用效率、减少环境污染具有十分重要的意义。从土壤到根系、从根系到茎部和其他植物器官的转运涉及到氮的吸收、同化、转运和再利用等多个过程。氮同化不仅是这些过程中最关键的一步,也是植物生长的重要限制因素之一。因此,提高氮素同化效率是提高植物氮素利用效率的重要方面。
在几种植物中,根部吸收的硝酸盐有一部分在根部被吸收,但大部分被运输到茎部,然后被吸收。硝酸还原酶(Nitrate reductase, NR)在细胞质中首先将硝酸盐还原为亚硝酸盐,前期研究表明NR的活性受14-3-3蛋白、蛋白激酶、蛋白酶和蛋白磷酸酶的调控[21].这种酶是由NR [NADH]蛋白(NIAs)调节的,而NIA2,而不是NIA1,调节NR活性答:芥[18,22].亚硝酸盐还原酶将亚硝酸盐还原为铵需要NAD(P)H。此外,通过谷氨酰胺合成酶(GS)/NADH-谷氨酰胺氧谷氨酸转氨酶(NADH- gogat)循环将铵同化为氨基酸也需要ATP和NADH或还原铁还蛋白[18].近年来的研究表明,nin样蛋白转录因子是硝酸盐诱导的关键调控因子NR基因的表达和nin样蛋白转录因子可能与硝酸盐诱导的其他硝酸盐同化相关基因的表达一致[23,24].
从硝酸盐中恢复或通过铵转运体(AMTs)作用直接吸收的铵被质体中的亚硝酸盐还原酶和质体和细胞质中的GS进一步还原[25]或通过GS和GOGAT循环同化为氨基酸。参与这些过程的主要GS/GOGAT同工酶是叶绿体中的GS2和铁氧还原蛋白依赖的GOGAT (Fe-GOGAT),以及细胞质中的GS1和NADH-GOGAT [26,27].部分GS1同工酶的生理功能答:芥据报道[28,29,30.].其中GLN1.1和GLN1.4对铵的亲和力较高,GLN1.2和GLN1.3亲和力较低[31].在低浓度时,铵被GLN1.1、GLN1.2和GLN1.3同化,它们具有功能冗余[32].在玉米上也有研究指出GLN1.4对释放铵的再同化有作用[33,34].在答:芥,在转录水平上未检测到GLN1.5 [35]而gln2编码的GS具有叶线粒体和叶绿体的双重靶向性[36].除了主要的氮同化外,氮再同化还通过光合组织的光呼吸和衰老或种子萌发过程中的蛋白质转化捕获大量的氨[37].
谷氨酸代谢与谷氨酸脱氢酶(Glutamate dehydrogenase, GDH)活性有关,它催化谷氨酸和2-氧谷氨酸的相互转化。最近的研究答:芥明确表明GDH在缺碳条件下的氨基酸分解中起核心作用,NADH-GDH的主要生理功能是为三羧酸循环提供2-羟戊二酸[38,39].
氮同化是对氨基酸、铵和硝酸盐等氮代谢物的内部和外部线索的反应。同工酶在转录、翻译和翻译后修饰水平上受到调控[40].氮素吸收和同化的调控也与根系发育有关。吸收尤其依赖于与根相关的特征,因为植物不仅通过根来调节自身的代谢和基因表达,而且还通过根的结构来优化资源的获取[41,42].
在不断变化的环境中,更全面地了解氮同化及其调控对提高植物生产力具有重要意义。因此,有必要加强对参考种和其他植物种的基础研究。在本研究中,通过研究氮同化的分子和遗传机制答:芥,我们探讨了的作用AtPDF2.1氨代谢调节。
结果
AtPDF2.1对铵的反应
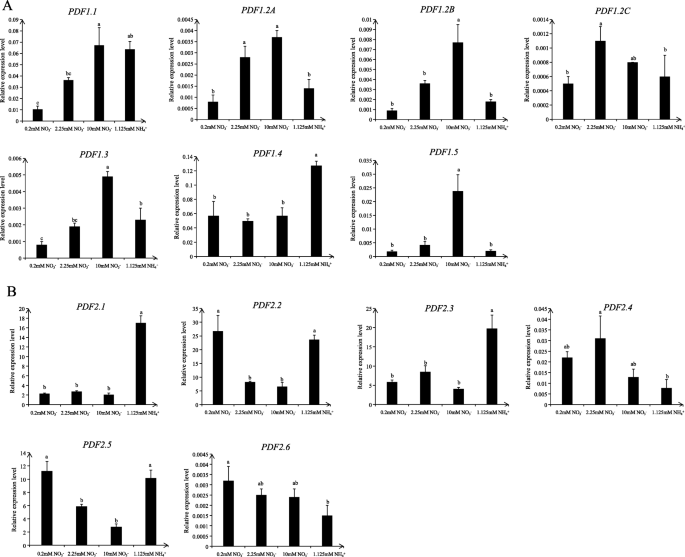
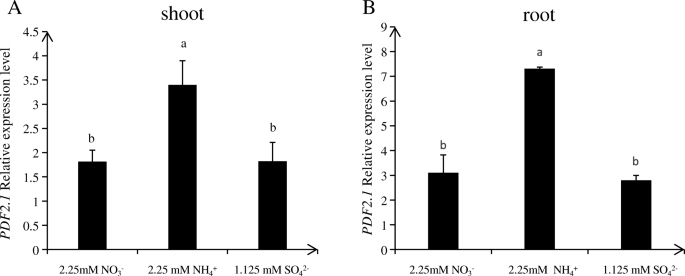
首先,我们对所有成员进行了诱导实验PDF家族基因来评估他们对高硝酸盐,低硝酸盐和铵的反应。Col-0在培养条件下水培18 d,缺氮3 d,然后用0.2 mM KNO处理3., 2.25毫米知3., 10毫米知道3.,或1.125 mM NH4没有3.根系取样前6 h显示PDF2.1而且PDF2.3是由铵引起的,特别是PDF2.1(无花果。1).为了进一步验证PDF2.1在纯铵生长条件下诱导,采用野生型Col-0在培养条件下水培18 d,缺氮3 d,然后用2.25 mM KNO3., 1.125 mM(NH4)2所以4,或1.125 mM K2所以46小时后再进行茎部和根部取样。这个实验揭示了AtPDF2.1铵处理对茎部和根部均有显著的诱导作用(图;2).
AtPDF2.1主要在根维管束和子叶中表达,其蛋白定位于细胞壁
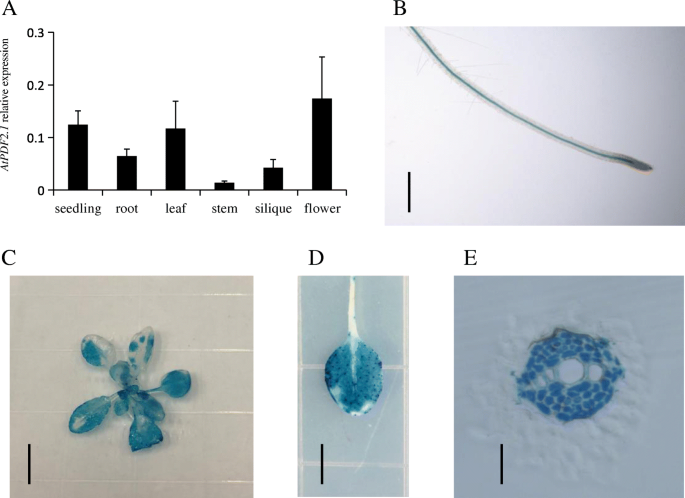
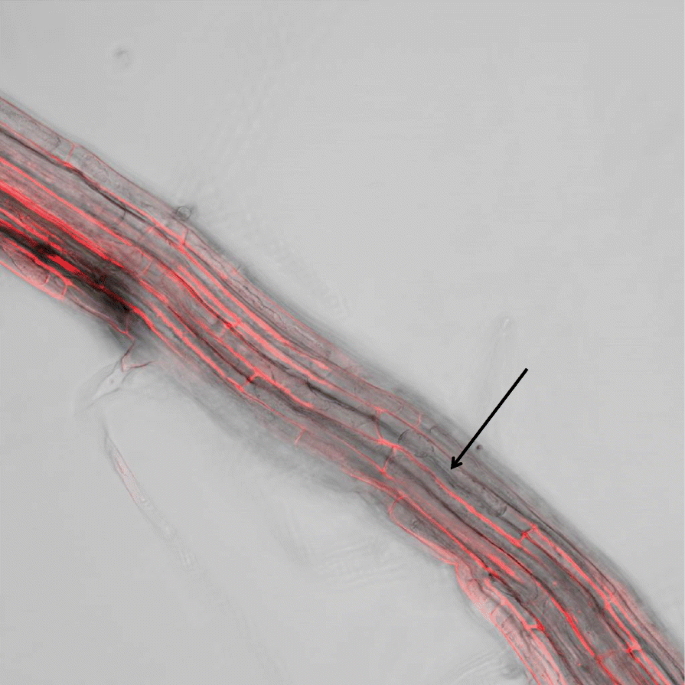
的表达模式AtPDF2.1,我们生成AtPDF2.1启动子驱动的β-葡萄糖醛酸酶(GUS)转基因植物。PDF2.1经定量PCR分析,在根、苗、叶、茎、角果和花中均有表达(图2)。3.a).我们在叶片、子叶和根维管束中检测到强烈的GUS信号(图。3.罪犯)。横截面GUS分析显示,根中维管木质部薄壁细胞表达较强(图2)。3.e).确定的亚细胞定位AtPDF2.1,我们进行了变换答:芥植物与AtPDF2.1-mRFP使用35S启动子。亚细胞定位分析表明,转化植株细胞壁以荧光信号为主(图2)。4).这些结果表明,AtPDF2.1定位于细胞壁。
AtPDF2.1影响笋中铵的浓度
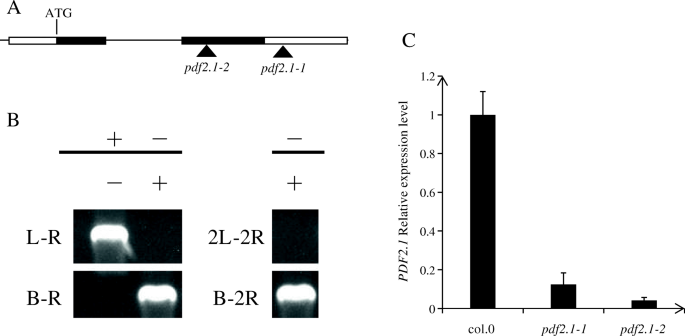
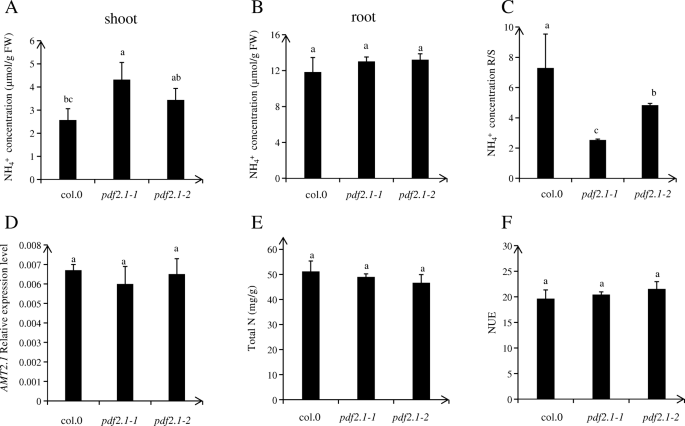
我们首先筛选和识别AtPDF2.1突变体。虽然表达水平AtPDF2.1在突变体中明显低于野生型,但仍检测到该基因的表达。因此,我们获得了两个功能性敲除突变体,pdf2.1-1而且pdf2.1-2(无花果。5).移植后,col0,pdf2.1-1,pdf2.1-2将幼苗在正常条件下(1/4植物营养液)培养18 d,取样分析总N含量、NUE、铵态氮浓度和基因表达的差异AMT2.1在被选中的AtPDF2.1突变体和col0。在正常条件下,铵的浓度较高pdf2.1-1而且pdf2.1-2与Col-0处理相比,根系间无显著差异(图2)。6a, b). Col-0处理的嫩枝和根中硝酸盐含量也无显著差异,pdf2.1-1,pdf2.1-2植物(附加文件1:图S1)。蛋白质AMT2.1将铵从根运输到芽[43,44].在正常情况下,没有差异AtAMT2.1col0的根表达式,pdf2.1-1,pdf2.1-2(无花果。6D),表明AtPDF2.1不参与铵从根到芽的运输。Col-0的总N含量和NUE,pdf2.1-1,pdf2.1-2植物也没有表现出差异(图;6e, f).这些结果表明AtPDF2.1可能影响嫩枝中铵的代谢。
的识别pdf2.1突变体。一个等位基因转移DNA插入线的示意图pdf2.1-1(SALK_110286)和pdf2.1-2(SALK_206700C)。的white blocks represent 5′-3′ UTR and the line connected the two black blocks represents intron.b通过PCR筛选和测序鉴定纯合子突变体。第一柱为野生型,第二、三柱为筛选纯合子。L和2l代表两个突变体的左边引物,R和2R代表两个突变体的右边引物,B代表插入的序列。c实时荧光定量PCR未检测到完整的AtPDF2.1 mRNApdf2.1突变体植物。Actin2被用作内部控制
AtPDF2.1通过调节蛋白的表达来影响GS活性GLN1.3而且GLN1.5在拍摄
虽然AtPDF2.1对全氮含量、根铵浓度和AtAMT2.1,突变体芽中铵离子浓度显著升高答:芥比Col-0芽的含量高。因此,我们假设AtPDF2.1可能参与茎部铵代谢的调节。
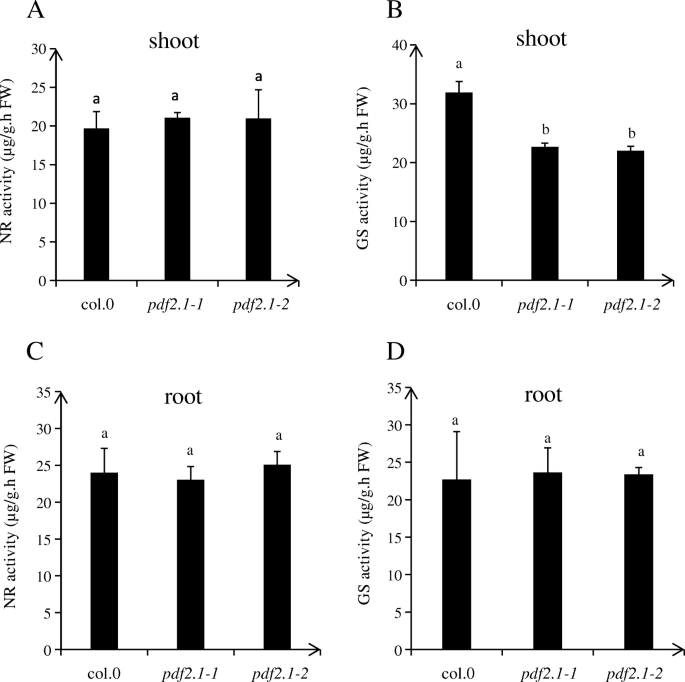
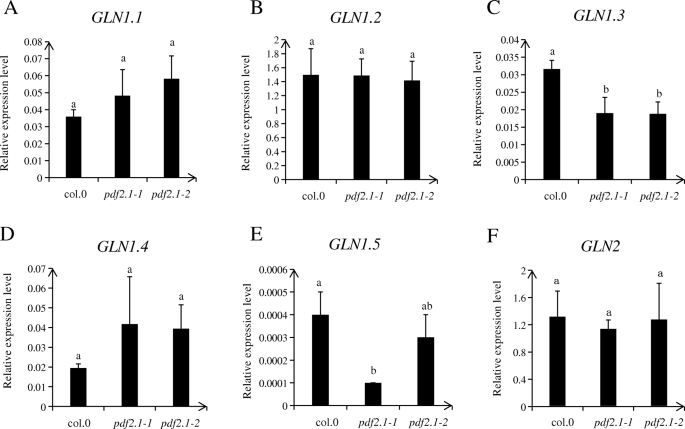
在正常条件下,Col-0的嫩枝间NR活性没有差异,pdf2.1-1,pdf2.1-2,而GS活动在嫩芽pdf2.1-1而且pdf2.1-2显著低于Col-0苗。此外,笋中铵的浓度pdf2.1-1而且pdf2.1-2均高于Col-0苗(图;7).在pdf2.1突变体,GLN1.3而且GLN1.5下调,但没有检测到对其他GLN家族的基因。因此,AtPDF2.1可能通过调节?的表达影响氨同化为谷氨酰胺GLN1.3而且GLN1.5(无花果。8).
AtPDF2.1影响嫩枝铵代谢
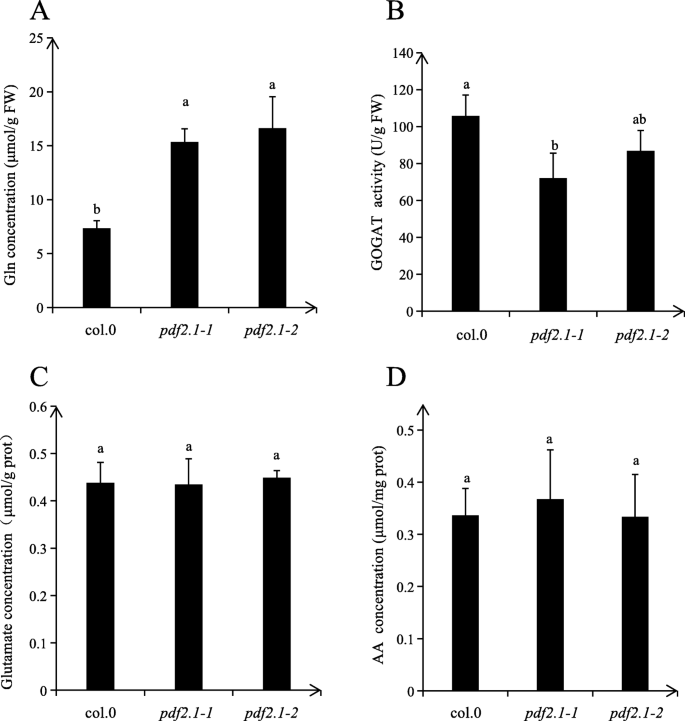
来研究铵代谢的哪些步骤会受到影响AtPDF2.1,测定了谷氨酰胺和谷氨酸的浓度,NADH-GOGAT的活性,以及游离氨基酸的浓度。谷氨酰胺浓度pdf2.1-1而且pdf2.1-2突变体的NADH-GOGAT活性也低于Col-0(图2)。9a, b).因此,突变体GS活性的降低可能影响了后续的代谢途径。Col-0对谷氨酸和游离氨基酸浓度无显著差异,pdf2.1-1,pdf2.1-2(无花果。9C, d),可能是由于功能冗余GLN1.3而且GLN1.1极低的表达GLN1.5的主导作用GLN1.2[32,34].
总的来说,结果表明AtPDF2.1通过改变蛋白的表达来调节GS的活性GLN1.3而且GLN1.5,导致笋中铵同化的变化。这改变了谷氨酰胺浓度和NADH-GOGAT活性,从而影响了铵的同化。
讨论
pdf是最早在小麦和大麦种子中发现的富含半胱氨酸的小肽[45].在答:芥,防御素分为PDF1s和PDF2s两个家族。之前的一项研究表明,AtPDF1.1参与植物对生物胁迫的反应[46].其他研究发现PDF1s可以提高植物和酵母的锌耐受性[9,47,48].然而,据我们所知,PDFs的分子机制尚未明确。
一些报道发现小肽与N. In有关一个芥在硝酸盐缺乏的情况下,表达CEP3在根部增加了10倍CEP1幼苗表达量增加;在铵限制下,CEP9表达被抑制[15].近年来的研究表明,CEP家族肽是根系系统性n -需求信号转导的一部分。它们通过受体cepr感知信号,从而介导根中硝酸盐转运蛋白基因的系统性上调[13].然而,pdf是否在营养吸收、运输或同化中发挥调节作用还没有报道。在本研究中,对野生型Col-0进行了低硝酸盐、高硝酸盐和铵处理,结果表明AtPDF在此条件下对家族基因进行分析。我们发现大多数PDF1S对硝酸盐有反应,而PDF2.1而且PDF2.3是由铵引起的,特别是PDF2.1(无花果。1).有报道称PDF2.1和PDF2.3具有很高的同源性[2],我们发现PDF2.1和PDF2.3受到铵的诱导相似,这表明它们可能具有一定的功能冗余,这可以解释为什么野生型和PDF2.1突变体之间的表型差异不明显。近期,我们通过聚类规则间隔短回文重复序列(CRISPR)/CRISPR-associated protein 9技术获得PDF2.3纯合突变体,并拟对其进行一系列测试pdf2.3单个或pdf2.1/pdf2.3双突变体,并将这些结果与之前的结果结合起来,以深入了解PDF2.1和PDF2.3的功能。在本研究中,PDF2.1在纯铵培养条件下诱导(图;2).PDFs在木质部、气孔和气孔细胞、薄壁细胞和其他外周区域表达[1,49].我们的结果也证实了AtPDF2.1是一种细胞壁蛋白答:芥在所有组织中都有表达。然而,因为我们不知道如何AtPDF2.1调节氮和/或铵代谢答:芥,我们检查了Col-0和PDF2.1突变反应AtPDF2.1在正常培养条件下。
首先,我们测定了Col-0中铵的浓度,pdf2.1-1,pdf2.1-2.结果表明,突变体与Col-0处理根系中铵离子浓度无显著差异,但突变体的铵离子浓度显著高于Col-0处理。然而,在表达中未检测到显著差异AtAMT2.1Col-0与突变体之间的差异(图;6),表示AtPDF2.1不影响铵从根向芽的运输。然而,不同浓度的Col-0对地上部和根部硝酸盐含量无显著影响pdf2.1变种人(附加文件1:图S1),总N含量和氮素利用率无差异(图1)。6).因此,AtPDF2.1可能影响嫩枝的铵代谢。位于叶绿体和细胞质中的GS酶负责同化通过硝酸盐还原产生的铵[9,47,48].
我们测定了嫩枝中与N代谢相关的酶的活性,发现嫩枝中NR活性无显著差异,而GS活性显著降低pdf2.1-1而且pdf2.1-2而不是Col-0。这表明AtPDF2.1可能通过调节GS活性来调节铵的进一步代谢。的pdf2.1突变体对大多数没有影响GLN但对家族基因有调节作用GLN1.3而且GLN1.5.的相对表达式GLN1.5很低。这可能解释了为什么表型不明显。最近的一项研究表明GLN1.1,GLN1.2,GLN1.3,GLN1.4的功能成员是GLN1基因家族答:芥它们在初级氮同化、植物生长、种子萌发和产生以及花粉发育中发挥协同或补充作用[50].此外,的主要异构体答:芥苗期表达的GLN1.1、GLN1.2和GLN1.3 [43].另有研究报道GLN1.2在莲藕种子产量、莲座丛生物量和萌发中起着重要作用[28,30.], GLN1.1和GLN1.3功能的缺失降低了植物的发芽率[50].这可能就是为什么PDF2.1突变体只部分影响铵代谢的原因。
在本实验中,突变体中谷氨酰胺的浓度高于野生型,可能是由于突变体中NADH-GOGAT活性的降低。然而,谷氨酸转运体1 (GLT1),调控NADH-GOGAT的基因在野生型和突变体之间没有差异(附加文件)1:图S2)。因此,这种调控可能不会发生在转录水平。GS活性的降低影响了后续代谢过程。然而,谷氨酸和游离氨基酸浓度在Col-0和突变体之间没有显著差异。这可能是由于功能冗余之间GLN1.3而且GLN1.1[50,低表达的GLN1.5,或GLN1.2在…中起主导作用的GLN1.1,GLN1.2,GLN1.3[51].
总的来说,PDF2.1是一种细胞壁蛋白,通过调节核基因来影响铵代谢GLN1.3.多项研究表明,小肽可以作为蛋白激酶通路的信号分子,间接调控其他基因的表达[13,14,52].例如,小肽CLE25可以通过受体激酶BAM调节NCED3在叶片中的表达,从而传递缺水信号,影响脱落酸的生物合成和蒸腾作用,调节气孔[14].也有研究表明,CEP家族肽是根系统中n信号的一部分。它们通过两个LRR标记,即CEPR1和CEPR2感知信号,以调节根中硝酸盐转运蛋白基因的系统性上调[13].研究表明,根源性CEP诱导叶片中韧皮部特异性多肽CEPD1和CEPD2,并激活NRT2.1的表达,特别是在根吸收硝酸盐的过程中[52].因此,我们假设PDF2.1也可以通过蛋白激酶或下游转录因子调控GLN1.3和AMT2.1,从而影响铵代谢,但具体过程尚未确定。
基于这些结果,我们认为AtPDF2.1通过调节茎部GS活性来调节铵的代谢,从而影响谷氨酰胺浓度和NADH-GOGAT活性。
结论
我们的研究结果表明,PDF2.1是多种器官的细胞壁蛋白,它通过调控蛋白的表达来影响铵的代谢GLN1.3在植物的嫩枝中。
方法
实验材料和生长条件
的答:芥对照组均为野生型(Col-0),由上海植物生理生态研究所龚继明提供。的AtPDF2.1基因敲除突变体(pdf2.1-1而且pdf2.1-2)是从拟南芥信息资源(TAIR;http://www.arabidopsis.org/).Col-0和AtPDF2.1敲除突变体在温室(300 μmol光子m−2年代−1将一对真叶苗移栽到4.5 l的花盆中,在含有1.25 mM KNO的1/4植物营养液中培养21天3., KH为0.625 mM2阿宝4, 1.25 μM Fe-EDTA, 0.5 mM MgSO4, 0.5 mM Ca(NO3.)2, 0.05 μM NaMoO4, 0.125 μM CuSO40.25 μM ZnSO4, 3.5 μM MnCl2、17.5 μM H3.薄3..将培养基的pH调至5.8,并在缓冲液中加入MES (2.5 mm)以调节pH可能发生的变化。每4 d更换一次培养基。每个盆地种植48株植物,所有盆地的生长条件相同。
在铵态诱导实验中,设置相对表达量分析AtPDF2.1在不同处理下,用1/4植物营养液处理Col-0幼苗18 d,然后进行N饥饿处理3 d,之后用2.25 mM KNO处理幼苗3., 1.125 mM (NH4)2所以4,或1.125 mM K2所以46 h,然后分别收获根和芽进行RNA提取和AtPDF2.1表达分析。
在其他实验中,col0,pdf2.1-1,pdf2.1-2用1/4植物营养液处理幼苗21 d后取样分析。
组织化学分析
AtPDF2.1初始密码子上游的1805 bp基因组片段使用引物ProAtPDF2.1进行PCR扩增1:表S1)。然后,亚克隆生成的ProAtPDF2.1启动子,分裂成二进制载体pCAMBIA1300 [53].的答:芥根据“实验材料和生长条件”部分的报道,在水中培养21 d的幼苗取样。从根中切下半薄片(4 μm)固定在载玻片上,在徕卡- dm6000显微镜下观察。使用GUS组织化学分析试剂盒(Real-Times)进行ProAtPDF2.1启动子驱动的组织化学染色。在Olympus BX51显微镜下观察GUS在根部的染色模式,使用Fujifilm X-A3相机拍摄。
DNA构建并转化为植物
的编码序列AtPDF2.1使用引物AtPDF2.1F和AtPDF2.1R进行PCR扩增(附加文件1:表S1),然后分析AtPDF2.1的亚细胞位置拟南芥是确定。子克隆生成结构35S::mRFP/1300。由此产生的片段与单个红色荧光蛋白(mRFP)基因的5 '端框在一起,产生35S::AtPDF2.1-mRFP/ pCAMBIA1300结构。通过将35S启动子替换为原生启动子proAtPDF2.1,对这些结构进行了修改,得到proAtPDF2.1::AtPDF2.1-mRFP/pCAMBIA1300构造,这些构造被转换为答:芥使用花浸法[54].然后用共聚焦显微镜(LSM880;蔡司)。
N浓度的定量
水培法培养21 d后,Col-0和突变体的茎和根均得到培养答:芥植物单独采样,在N液中冷冻,并在- 80°C保存,直到进一步分析。靛酚蓝比色法,在630 nm处[55,56,57和使用(NH4)2所以4,测定铵浓度。在410 nm处测定根和叶中的硝酸盐浓度[57,58,59spectrophotometrically。总氮浓度的测定如Wang等所述[60].在本研究中,NUE被确定为总生物量/总N积累量[61].
氮和铵代谢相关酶活性
植物氮代谢与几种关键酶的活性密切相关,如NR和GS [62].为了测定NR活性,将收获的根和叶立即冷冻在N液中,然后在- 80°C保存,直到进一步分析。样品研磨成细粉(~ 100 mg),提取,分光光度法分析[57,63,64].GS活性测定如Wang等报道[65].使用NADH-GOGAT测量试剂盒(Solarbio生物工程研究所)对NADH-GOGAT的活性进行量化。谷氨酸和谷氨酰胺分别使用谷氨酸测量试剂盒和谷氨酰胺测量试剂盒进行定量(均来自南京建成生物工程研究所)。酶活性以单位时间内每毫克新鲜体重或蛋白质产生/消耗的代谢物摩尔数表示。蛋白浓度采用考马斯亮蓝法测定,采用改良BCA蛋白测定试剂盒,C503051,生工生物科技。
氨基酸定量
根据Del Campo等人的报道,使用高效液相色谱法(HPLC)定量芽中的氨基酸。[66].冷冻叶片样品(200 mg)用N液粉碎,并在1.5 mL 0.1%苯酚和6 M HCl中均质。匀浆在100°C下水解22 h,然后冷却。使用NDK200-2组织(杭州MIU仪器有限公司)干燥1毫升水解物,并在1 mL 0.1 M HCl中重新溶解。将200 μL再溶水解液与20 μL去亮氨酸内标液、200 μL三乙胺乙腈(pH > 7)、100 μL异硫氰酸乙腈混合,25℃孵育1 h,定量氨基酸。加入400 μL正己烷后,摇匀再孵育10 min。衬底中的溶液通过0.45 μm注射器过滤器。所有HPLC分析均在RIGOL L3000系统(北京RIGOL科技有限公司)上进行。采用RP-HPLC ACE柱(5C18-HL),粒径为5 μm (250 mm × 4.6 mm),在100℃下,通过二元梯度进行色谱分离。流动相A为25 mM醋酸缓冲液(pH 6.5)和70 mL乙腈。 Mobile phase B was 80% acetonitrile aqueous solution. The flow rate was 1.0 mL min−1柱温为40℃。
基因分型,RNA提取,定量PCR
为了鉴定突变体,从生长在1/2植物营养液(叶子)中的21 d老植物中提取总DNA,用附加文件中提供的引物作为PCR模板1:表S1。
在铵诱导实验中,分别采集Col-0幼苗的根和芽,用1/4植物营养液处理18 d,处理前进行N饥饿处理3 d,在N液中冷冻,在- 80℃保存至RNA分析。的表达模式分析PDF2.1,从水培法生长的45 d老植物(叶、茎、角果和花)或在1/2植物营养液中生长的7 d老植物(幼苗)中收获组织。按照制造商的说明,用TRIzol (Invitrogen)提取总RNA,用等体积的异丙醇沉淀,用75%乙醇洗涤,并溶解在不含rnase的水中。互补DNA合成使用PrimeScript™RT Kit与gDNA Eraser (Perfect Real Time;TAKARA)遵循制造商的协议。目标基因的相对表达是通过实时定量PCR在应用生物系统StepOne™实时PCR系统和SYBR Premix Ex-Taq (TAKARA)上进行的,根据制造商的说明。将靶基因的相对表达量归一化至内参基因的相对表达量——ΔΔCT方法(67].分析中使用的引物列在附加文件中1:表S1,表达式数据归一化为Actin2,作为内部标准。
统计分析
在本研究中,所有实验均采用完全随机设计进行。每个处理设4个生物重复和2个技术重复。采用最小显著性差异多极差检验进行多重比较。野生型和突变型之间的差异用Student 's进行评估t-使用统计产品和服务解决方案17.0 (SPSS,芝加哥,伊利诺伊州,美国)进行测试。这些差异被认为有统计学意义P< 0.05。
数据和材料的可用性
本研究中使用和/或分析的数据集可根据合理要求从通讯作者处获得。
缩写
- AMT:
-
铵转运蛋白
- 国民幸福指数:
-
谷氨酸脱氢酶
- GOGAT:
-
谷氨酰胺转氨酶
- g:
-
谷氨酰胺合成酶
- 护士:
-
氮
- NR:
-
硝酸还原酶
- 自虐:
-
氮利用效率
- PDF格式:
-
植物defensins
参考文献
García-Olmedo F, Molina A, Alamillo JM, Rodríguez-Palenzuéla P.植物防御肽。生物聚合物。1998;47:479 - 91。
王志刚,王志刚,王志刚。植物防御素的研究进展。足底。2002;216:193 - 202。
Fant F, Vranken W, Broekaert W, Borremans F. Raphanus sativus抗真菌蛋白1三维溶液结构的1H NMR测定。中华药理学杂志,1998;29(2):349 - 349。
甘茨T.防御素:先天免疫的抗菌肽。中华免疫杂志2003;3:710-20。
Thevissen K, Warnecke DC, François IEJA, Leipelt M, Heiz E, Ott C, Zähringer U, Thomma BP, Ferket KK, Cammue BP。来自昆虫和植物的防御素与真菌的葡萄糖神经酰胺相互作用。生物化学学报。2004;39:3900 - 5。
Penninckx IA, Eggermont K, Terras FR, Thomma BP, De Samblanx GW, Buchala a .拟南芥病原菌诱导的植物防御素基因系统激活遵循水杨酸独立途径。《植物细胞》1996;8:2309-23。
小池M,冈本T,津田S,今井R.冬小麦在冷驯化过程中特异诱导了一种新的植物防御素样基因。Biochem Bioph Res Co. 2002; 298:46-53。
杜敏,李世峰,郑华伟,孙克辉,黄伯凯。辣椒防御素(CADEF1)基因的差异表达和原位定位及其对病原菌侵染、非生物诱导子和环境胁迫的响应。植物科学学报,2004;26(3):344 - 344。
Mirouze M, Sels J, Richard O, Czrnic P, Loubet S, Jacqyuier A, François IE, Cammue BP, Lebrun M, Berthomieu P, Marquès L.植物防御素的新作用:一种来自高锌积累植物拟南芥的防御素具有锌耐受性。植物J. 2006; 47:329-42。
冯丽娟,李丽娟,李丽娟,李丽娟。植物抗真菌植物防御蛋白AtPDF2的研究进展。3答:芥阻断钾离子通道。科学通报2016;6:32121。
罗建军,黄军,曾德龙,彭建军,张国宝,马海林,关勇,易海燕,付玉林,韩波,林海霞,钱倩,龚建民。一种防御素样蛋白驱动镉在水稻中的流出和分配。Nat Commun. 2018;9:645。
罗建军,杨勇,顾泰,吴志明,张志辉。拟南芥防御素基因AtPDF2。5介导镉耐受性和积累。植物细胞环境。2019:1-15。https://doi.org/10.1111/pce.13592.
Tabata R, Sumida K, Yoshii T, Ohyama K, Shinohara H, Matsubayashi Y.根源多肽通过芽LRR-RKs介导系统性n -需求信号。科学。2014;346:343-6。
Takahashi F, Suzuki T, Osakabe Y, Betsuyaku S, Kondo Y, Dohmae N, Fukuda H, Yamaguchi-Shinozaki K, Shinozaki K.长距离信号通路中通过脱落酸调节气孔控制的小肽。大自然。2018;556:235-8。
Delay C, Imin N, Djordjevic MA。CEP基因根据环境信号调节根和芽的发育,是种子植物特有的。中国科学(d辑),2013;
Soyano T, Hirakawa H, Sato S, Hayashi M, Kawaguchi M.结节INCEPTION创建了一个参与结节器官生成稳态调节的长距离负反馈环路。美国国家科学院。2014; 111:14607-12。
胡斌,姜志明,王伟,邱永华,张志辉,刘永强,李芳芳,高晓康,刘丽坤,钱永伟,黄晓华,余FF,康森,王永强,谢建平,曹玉生,张丽华,王玉春,谢青,Kopriva S,褚成昌。硝酸盐- nrt1.1 B - spx4级联在植物中整合氮磷信号网络。植物学报。2019;5:401-13。
克劳福德NM。硝酸盐:植物生长的养分和信号。《植物科学》1995;7:859-68。
Barlóg P, Grzebisz W.氮肥施用时机对甘蓝型油菜(Brassica napus L.)的影响。2氮素吸收动态与肥料效率。中国农业科学(英文版),2004;
Grant CA, Wu R, Selles F, Harker KN, Clayton GW, Bittman S, Zebarth BJ, Lupwayi NZ。与播种时施用无包衣尿素相比,控释尿素和分施氮肥的作物产量和氮浓度。农田作物决议2012;127:170-80。
MacKintosh C, Meek SEM。可逆磷酸化、14-3-3蛋白和蛋白水解对植物NR活性的调控细胞生物学与生命科学,2001;
Hoff T, Truong HN, Caboche M.利用突变体和转基因植物研究硝酸盐同化。植物细胞环境。1994;17:489-506。
拟南芥n -like转录因子在硝酸盐信号传导中的核心作用。Nat Commun. 2013; 4:1617-25。
Konishi M, Yanagisawa S.在理解硝酸盐调控基因表达的分子机制方面迈出了新的一步。中国机械工程学报(自然科学版),2014;
林敏,李志强,李志强,李志强。植物氮同化过程的分子遗传学研究。植物学报1996;47:569-93。
Khademi S, O'Connell J 3rd, Remis J, Robles-Colmenares Y, Miercke LJ, Stroud RM。Amt/MEP/Rh输氨机理:AmtB在1.35 Å的结构。科学。2004;305:1587 - 94。
ortizz - ramirez C, Mora SI, Trejo J, Pantoja O. PvAMT1;1,一种高选择性铵转运体,功能为H+/ NH4+同向转运。生物化学学报。2011;286:31113-22。
Lothier J, Gaufichon L, Sormani R, Lemaître T, Azzopardi M, Morin H, Chardon F, Reisdorf-Cren M, Avice J, Masclaux-Daubresse C.当硝酸盐供应不受限制时,细胞质谷氨酰胺合成酶GLN1;2在拟南芥蔷薇丛中发挥控制植物生长和铵稳态的作用。中国科学(d辑),2011;
关M, Møller IS, Schjørring JK。两种细胞质谷氨酰胺合成酶异构体在拟南芥种子萌发和种子产量结构中起着特定的作用。中国科学(d辑),2014;
管明,德邦TC, Pedersen C, Schjoerring JK。胞质谷氨酰胺合成酶Gln1;2是参与GS1活性的主要同工酶,可上调以缓解铵毒性。植物物理学报。2016;171:1921-33。
石山K, Inoue, Watanabe-Takahashi A, Obara M, Yamaya T, Takahashi H.拟南芥谷氨酰胺合成酶胞质同工酶的动力学性质和氨依赖性调控。中国生物医学工程学报。2004;
Konishi N, Saito M, Imagawa F, Kanno K, Yamaya T, Kojima S.胞质谷氨酰胺合成酶同工酶在低铵条件下根系铵同化中发挥冗余作用拟南芥.中国生物医学工程学报,2018;
Martin A, Belastegui-Macadam X, Quilleré I, Floriot M, Valadier MH, Pommel B, Andrieu B, Donnison I, Hirel B.两个不同叶片绿色持久性的玉米杂交种的氮管理和衰老:农艺、生理和分子方面。新植物,2005;167:483-92。
Martin A, Lee J, kiichey T, Gerentes D, Zivy M, Tatout C, Dubois F, Balliau T, Valot B, Davanture M, Tercé-Laforgue T, Quilleré I, Coque M, Gallais A, Gonzalez-Moro M, bethcourt L, Habash D, Lea P, Charcosset A, Perez P, Murigneux A, Sakakibara H, Edwards K, Hirel B.玉米的两种细胞质谷氨酰胺合成酶异构体专门参与谷物生产的控制。《植物细胞》2006;18:3252-74。
dragievviic M, simonoviic A, bogdanoviic M, subotiic A, Ghalawenji N, dragievviic I, todoroviic S.植物生长调节剂对拟南芥幼苗GS-GOGAT基因表达的差异调控。中国生物医学工程学报(英文版);
李志强,李志强,李志强。拟南芥gln2编码的谷氨酰胺合成酶对叶片线粒体和叶绿体具有双重靶向作用。植物学报。2004;16:2048-58。
徐刚,范X,米勒AJ。植物氮同化与利用效率。植物学报2012;63:153-82。
Fontaine JX, Tercé-Laforgue T, Armengaud P, Clément G, Renou JP, Pelletier S, Catterou M, Azzopardi M, Gibon Y, Lea PJ, Hirel B, Dubois F.拟南芥nadh依赖谷氨酸脱氢酶突变体的鉴定表明该酶在根系碳氮代谢中的关键作用。《植物科学》2012;24:4044-65。
Tercé-Laforgue T, Bedu M, Dargel-Grafin C, Dubois F, Gibon Y, Restivo FM, Hirel B.植物谷氨酸脱氢酶作用的解析:II。植物单独或同时过表达两种酶亚基的生理特性。中国生物医学工程学报,2013;
梅耶C,斯蒂特M.硝酸盐还原和信号。植物氮。柏林:施普林格;2001.37-59页。
福德BG。氮信号通路塑造根系结构:更新。植物学报。2014;21:30-6。
李志强,李志强,李志强,等。植物根系吸收氮素的生理发育机制研究。植物学报,2013;
王晓明,王晓明,王晓明,等。拟南芥中氨转运蛋白AtAMT2的研究进展。FEBS Lett. 2000; 467:273-8。
Giehl RFH, Laginha AM, Duan F, Rentsch D, Yuan L, von Wirén N. AMT2的关键作用;1在拟南芥铵根-茎转运中的作用。植物学报。2017;10:1449-60。
Mendez E, Moreno A, Colilla F, Pelaez F, Limas GG, Mendez R, Soriano F, Salinas M, de HARO C.大麦中一种新型硫蛋白γ -hordothionin真核无细胞系统的初级结构和蛋白质合成抑制。生物化学。1990;194:533-9。
De Coninck BM, Sels J, Venmans E, Thys W, Goderis IJ, Carron D, Delauré SL, Cammue BP, De Bolle MF, Mathys J。拟南芥植物防御素AtPDF1。1参与植物对生物胁迫的反应。新植物学报,2010;187:1075-88。
Shahzad Z, Ranwez V, Fizames C, Marquès L, Le Martret B, Alassimone J, Godé C, Lacombe E, Castillo T, Saumitou-Laprade P, Berthomieu P, Gosti F.植物防御素1型(Plant defense in type 1, PDF1):拟南芥属内蛋白质混杂和表达变异对锌耐受性获取的影响。新植物学报。2013;200:820-33。
Nguyen NN, Ranwez V, Vile D, SOULIE MC, Dellagi A, Expert D, Gosti F. PDF1s表达的进化修补表明它们在锌耐受性和对病原体攻击的反应中具有联合作用。植物科学进展(英文版);
Kragh KM, Nielsen JE, Nielsen KK, Dreboldt S, Mikkelsen JD。新富半胱氨酸抗真菌蛋白的鉴定与定位。植物与微生物相互作用,1995;8:424-34。
姬艳,李强,刘刚,Selvaraj G,郑铮,邹娟,魏勇。细胞质谷氨酰胺合成酶在拟南芥发育及胁迫响应中的作用。植物细胞物理学报2019;60:657-71。
Konishi N, Ishiyama K, Beier MP, Inoue, Kanno K, Yamaya T, Takahashi H, Kojima S.两种胞质谷氨酰胺合成酶同工酶对拟南芥根系铵同化的贡献。中国科学(d辑),2016;
Ohkubo Y, Tanaka M, Tabata R, Ogawa-Ohnishi M, Matsubayashi Y.茎根移动多肽参与氮获取的系统调节。植物学报。2017;3:17029。
张国国,易海海,龚建民。拟南芥乙烯/茉莉酸- nrt信号模块协调硝酸盐的重新分配和生长与环境适应之间的权衡。《植物科学》2014;26:3984-98。
农杆菌介导的花浸渍转化的简化方法拟南芥.植物学报(英文版);1998;
Cataldo DA, Maroon M, Schrader LE, young VL。水杨酸硝化法快速比色法测定植物组织中硝酸盐。公共土壤科学计划,1975;6:71-80。
Santoni S, Bonifacio E, Zanini E.靛酚蓝比色法测量砂质土壤阳离子交换能力。中国土壤科学。2001;32:2519-30。
辛格R,帕里哈尔P,普拉萨德SM。硫和钙同时调控芥菜幼苗的光合性能和氮代谢状态。植物科学,2018;9:772。
Molins-Legua C, Meseguer-Lloret S, Moliner-Martinez Y, Campíns-Falcó P.水分析中铵的测定方法选择指南。track - trend Anal chemistry, 2006; 25:82 - 90。
Patterson K, Cakmak T, Cooper A, Lager I, Rasmusson AG, Escober MA。不同的信号通路和转录组反应特征区分了提供铵和硝酸盐的植物。植物生态学报,2010;
王荣荣,邢晓军,王勇,陈安,郭伟强,刘国强。硝酸盐调控突变体的基因筛选捕获了硝酸盐转运蛋白基因NRT1.1。植物科学进展。2009;
李辉,李春春,罗娟,曹霞,曲林,盖勇,姜晓宁,刘天宁,白华,杨子德,Polle A,彭超,罗志斌。施氮对速生杨树和慢生杨树的生长、碳氮生理和木材特性均有不同程度的影响。中国科学(d辑),2012;
杨树氮营养的研究进展。植物学报。2010;12:275-91。
罗宾P.硝酸盐还原酶的提取条件研究拉辛和植物的肥料maïs。植物学报,1979;17:45-54。
Ehlting B, Dluzniewska P, Dietrich H, Selle A, Teuber M, Hänsch R, Nehls U, Polle A, Schnitzler JP, Rennenberg H, Gessler A.灰杨氮营养与盐度的相互作用。植物生态学报。2007;30:796-811。
王玲,周强,丁玲,孙勇。镉毒性对新发现的镉超蓄积植物龙葵叶片氮代谢的影响。J危险材料,2008;154:818-25。
Del Campo CP, Garde-Cerdán T, Sánchez AM, Maggi L, Carmona M, Alonso GL.不同产地藏红花中游离氨基酸和铵离子的测定。食品化学。2009;114:1542-8
李纪勇,付玉林,Pike SM,鲍杰,田文智,陈长忠,张勇,李红梅,黄娟,李乐根,Schroeder JI, Gassmann W,龚纪明。拟南芥硝酸盐转运蛋白NRT1.8在木质部液中硝酸盐的去除和镉耐受性的调节中起作用。《植物科学》2010;22:1633-46。
致谢
感谢彭灿(中国科学院亚热带农业研究所核心设施)对共聚焦显微技术的帮助。
资金
国家重点研发计划项目(2017YFD0200100;2017 yfd0200103);国家自然科学基金(31800202);湖南省重点研发计划项目(2018NK1010);中国博士后科学基金(2018 M630900);湖南省外国专家招聘计划;国家油菜生产技术体系;教育部“2011计划”;湖南农业大学双一流建设项目(kxk201801005)、湖南省自然科学基金创新课题组(2019JJ10003)。资助机构没有参与研究的设计、数据的收集、分析和解释,也没有参与撰写手稿。
作者信息
从属关系
贡献
J-YY、J-SL和Z-HZ设计实验;J-YY完成了大部分实验;YX负责部分实验;J-YY和Z-HZ对数据进行分析;J-YY、Z-HZ撰写稿件。所有作者均同意稿件内容及投稿。所有作者都阅读并批准了最终的手稿
相应的作者
道德声明
伦理批准并同意参与
不适用。
发表同意书
不适用。
相互竞争的利益
作者宣称他们之间没有利益冲突。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
附加文件1:
图S1。硝酸盐浓度答:芥,图S2。相对表达量AtGLT1在Col-0的芽中pdf2.1-1,A. thaliana . pdf2.1 . 2在1/4植物营养液中培养21 d,表S1。本研究中使用的引物
权利和权限
开放获取本文根据创作共用属性4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),允许在任何媒介上不受限制地使用、分发和复制,前提是您对原作者和来源给予适当的赞扬,提供到创作共用许可证的链接,并注明是否进行了更改。创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)除另有说明外,适用于本条所提供的资料。
关于本文
引用本文
姚俊,罗俊。,小,Y。et al。植物防御素基因AtPDF2.1通过调节谷氨酰胺合成酶活性介导氨代谢拟南芥.BMC植物生物学19日,557(2019)。https://doi.org/10.1186/s12870-019-2183-2
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12870-019-2183-2
关键字
- 铵新陈代谢
- 拟南芥
- GLN1.3
- GLN1.5
- PDF2.1
- 植物defensins