抽象的
背景
以往的研究主要集中在柑橘果实中,对柑橘叶和花中挥发物的研究较少。然而,柑橘的叶子和花也富含挥发性化合物,具有独特的香味。本文对62份柑橘种质资源的叶片和25份柑橘种质资源的花进行了挥发性分析,研究了柑橘叶和花中的挥发性成分。
结果
总共,从62个柑橘种质和25种柑橘种质的叶片中鉴定了196和82个挥发性化合物。主要挥发性萜类化合物在柑橘饲料中比果皮更多样化。在至少20种种质的叶片中通常检测到总共34种挥发性萜类化合物,其中在野生或半瓦米尔种质的叶子中过度累积了31种。该结果分别与甲氧基和2-C-甲基-D-赤藓糖醇-4-磷酸盐(MEP)生物合成途径的高表达水平一致,以及甲酸二甲酸二甲酸酯-4-磷酸盐(MEP)的低表达水平,以及Geranylgeranyl的低表达水平相对于品种水平的MEP途径二磷酸二磷酸二磷酸二磷酸合成酶。完全开花显示出四个萜烯醇的水平增加,与球囊阶段花相比,三萜烯含量的降低,特别是在甜橙色。鉴定单萜酶基因并在功能形式中以体外作为三丁烯合酶的特征。
结论
我们的结果表明,31种重要的三萜类化合物在野生或半孢子种质中丰富,可能是因为驯化在柑橘叶中挥发物的负面影响。完全开放的花的香味可能是由于四种萜烯醇含量的增加。此外,通过组合转录组和代谢物分析鉴定了三丁烯合酶基因。
背景
植物中的数千种代谢物,如类黄酮[1类胡萝卜素,唇脂蛋白,Nomilins [2],Furanocoumarins [3.[挥发性Terpenoids [4.],具有多种对人类有益的生物作用[5.].分别是植物血浆和细胞质中的2-C-甲基-D-赤藓糖醇-4-磷酸(MEP)和甲羟戊酯(MVA)途径,合成C5异戊烯基焦磷酸(IPP)[5.那6.].IPP及其异构体二甲基烯丙基二磷酸盐(DMAPP)是分别在质体和细胞质中生物合成香叶基焦磷酸盐(GPP)和法尼基焦磷酸盐(FPP)的底物[6.那7.].单调萜(C.10.)和倍半萜(C15.)通过各种萜烯合成从FPP合成(TPS.)基因[8.].然后,单萜和倍半萜可被细胞色素P450 (CYP450)酶、脱氢酶和还原酶用于合成各种萜衍生物[7.那9.].例如,CYP76C1和CYP76C3将LINALOOL代谢到8-羟基氨基拟南芥[9.那10.].
作为最重要的植物挥发物群之一,萜类化合物广泛存在于高等植物中并参与广泛的生物活动[5.].萜类化合物是初级代谢物或次级代谢物,在植物-微生物、植物-昆虫、植物-动物和植物-植物相互作用中发挥重要作用[11.那12.].植物中积累的萜烯不仅参与对抗昆虫或细菌的直接或间接防御[11.那12.那13.]但还有助于有益于植物的特定香气。此外,挥发性萜件被广泛用作精油中的重要组分或用于合成风味产品的前体。例如,Sabinene具有抗炎活动[14.];β-芳樟醇具有抗炎作用,是一种广泛应用的食品和香水添加剂[15.];β-月桂烯常作为原料进行合成β-linalool和geraniol [16.];据报道,乙酸乙酸酯具有抗炎活动[15.];和β-榄香烯具有抗肿瘤活性[17.].
Terpenoids主要由各种各样的TPS.植物中的基因。以前的研究表明有95个TPS.瓦伦西亚甜橙基因组中的基因座[18.],其中很少有功能表征。CSTPS1.已被证明在甜橙色的生产中的生产(+) - valencene [19.].Citmtse1,Citmts3,Citmts61和CitMTS62与生产有关D.- 二烷烃,γ-萜烯,γ-萜烯和β- 分别在C. unshiu.[20.];CS3G04360.1.被发现影响生产D.- 新霍尔·脐橙的二烯酮[21.].此外,七个倍二萜合酶基因的特征在于甜橙[18.].由于高序列相似之处TPS.基因,很难通过序列同源性和基因组注释来寻找候选基因。因此,结合转录组学和代谢组学分析可能是缩小候选基因范围的好方法。
作为全球范围内的一些最重要的水果作物,柑橘植物富含挥发性Terpenoids [22.].值得注意的是,对柑橘类植物挥发性化合物的研究可以追溯到1925年[23.].目前,柑橘味是必需石油工业中最重要的香料之一,用于25%的精油[24.].各种柑橘精油,如甜橙色油,柠檬油和葡萄柚油,从柑橘类水果,花和叶中提取[24.].总的来说,有大量的证据表明人类对柑橘挥发物的热情追求。
柑橘植物包括几百种种质,带有摆动[25.]和tanaka [26.]系统是种质分类最广泛接受的系统[22.那27.那28.].最近,代谢组分,特别是挥发性曲线的测定,已用于柑橘植物的分类,从趋化式的视角下使用[22.那27.那28.].以往的研究表明,植物的化学分类学柑橘那Poncirus.和Fortunella基于果皮和叶挥发物的主成分分析(PCA)和层次聚类分析(HCA),探讨了芒山叶干(柑橘Nobilis.Lauriro)[28.].使用HCA和局部最小二乘判别分析(PLS-DA)基于其果皮挥发物进行20柑橘种质的分类(PLS-DA)[27.].Zhang等[22.基于108柑橘种质剥离的挥发物,通过HCA分析了不同柑橘类物种之间的关系。受约束的主坐标分析(CPCOA)始终用于确定不同物种之间挥发性化合物的差异。上述分类类似于现有摆动系统的分类,证明了基于各种柑橘基因型的挥发性型材的趋化工的可靠性。
最近的研究和我们之前的报告主要集中在柑橘类水果中的挥发物[4.那22.那24.那29.那30.],而叶子和鲜花的挥发物则不太常见。然而,柑橘叶和花也富含挥发性化合物,并且可以在昆虫发作时发出特异性挥发物,以吸引昆虫捕食的自然敌人[11.]或防御真菌病原体[12.].柑橘叶,具有生长周期短、生物量高,可用性,和柑橘花,发出特定挥发物在不同的阶段,都是极具价值的柑橘类精油产业的研究基因型和spatiotemporal-specific基因表达和调控,阐明植物、动物、微生物和昆虫之间的相互作用机制。
本研究旨在识别和更好地了解挥发物的代谢,然后探讨各种挥发性化合物的生物合成的候选基因,具有植物和柑橘叶和花的特殊生物益处。确定叶子和花的挥发性概况。此外,转录组分析和RT-QPCR用于检查柑橘叶中挥发物的驯化。来自Cara Cara Navel橙的两个不同开口阶段的转录组数据和挥发性分析数据进行了相关分析以识别候选人TPS.沙CYP450此外,本文还分析了柑橘栽培与野生或半野生植物挥发性成分分化的机理以及叶片和花挥发物的生理特性,为柑橘种质资源在育种和精油工业上的优化利用提供了依据。
结果
在柑橘叶中检测到的挥发性化合物
共有196种挥发性化合物(附加文件1:在62个柑橘种质的叶子中检测到表S1)(表1)基于NIST质谱库,其中57种化合物用真实标准鉴定(附加文件2:表S2)。196种化合物可以分为16组,其中包括19个单选醇,15个单萜醛,五种单萜醛,五种单萜酮,五种单萜氧化物,六个单萜酯,72个酪蛋白萜烯,16倍萜醇,氧化三萜醛,两种酪酮萜烯,五个醇,15醛,五酸,五酯,四个酮和16其他化合物(附加档案1:表S1)。
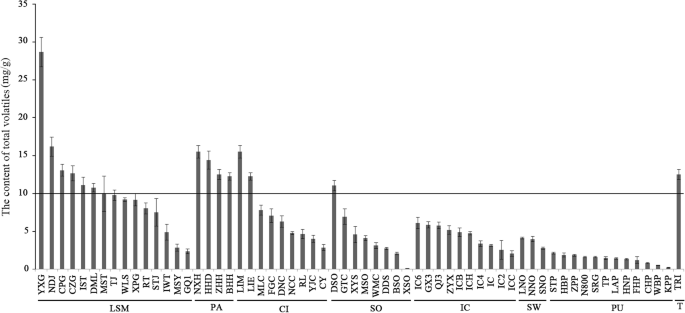
不同柑橘种质资源挥发性成分含量(TVC)范围为0.13±0.01 mg/g(杏山酸橙)~ 28.69±1.94 mg/g(瑶香柑、杨香柑、松皮柑桔),化合物数量范围为13个(HB柚)~ 69个(杨香柑)1).
叶子中不同物种的含量比皮肤更高多样化。例如,最丰富的化合物是香桶,乙酸甲苯甲酯和Trans-β.- 帕帕皮亚胺;Trans-β.- 外亚烷,乙酸乙酸酯,α-折烯,(E.)-β金合欢烯和γ.-elemene in.Citrus ichangensis.;人民币,γ.萜品烯,D.-柠檬烯和锗烯D香橙;D.- 二烷烯,α-柠檬,β-柠檬醛和香茅醛;β---丁烯,(+) - 丙二酰胺丙烯,Trans-β.- 聚亚胺和亚芳芬啉在Pummelo;莱纳洛,Trans-β.- 外君和β- 松弛皮肤普通话中的内容;人民币,Trans-β.-ocimene和3- carene在甜橙;和linalyl,linalool,caryophylne和β-蒎烯酸橙(附加文件3.:表S3)。
在至少20份种质中共检出43种化合物,其中萜类化合物34种。值得注意的是,在野生或半野生种质中发现了31种含量最高的萜类化合物。例如,八种萜类化合物(沙宾烯,β- 金英,D.- 司,allo-ocimene,α-榄烯,β-ELEMENE,( - ) - 海拔和生殖器酮D)是最丰富的YXG;七萜件(樟烯,β---丁烯,异戊烯醇,Germacrene D-4-OL,Trans-β.- 离亚胺,α-豆类和萜烯)是Niedu野生橘子(NDT,松弛的普通话)的最高水平;γ.-ELEMENE和GERMACRENE B是印度酸橘(松弛皮肤普通话)中最丰富的人;(+) -δ.-cadinene和(+) - 沃隆酸普通话中最丰富的甘蓝丙烯(松动普通话);α-磷锡和3- carene是Muli Citron(Citron)和Newhall Navel橙(甜橙)中最丰富的(表2).
62份调查材料可分为7种。大部分木瓜和松皮柑橘种质的TVC水平为> 10 mg/g;大多数为3-10毫克/克C. ichangensis.种质,香橼,甜橙和酸橙种质;对于大多数pummelo种质,<2.5 mg / g(图。1).在所有七种柑橘种类中,松弛皮肤普通话和甜橙分别具有最大,最小的挥发性化合物。
在15个松弛型普通话种质的叶片中检测到总共140种挥发性化合物。总含量从2.39±0.33mg / g中的Guoqing No.1(GQ.1)中的2.39±0.33mg / g变化至28.69±1.94mg / g,在大多数松弛皮肤普通话种质中鉴定了超过50种化合物(表1).蒙特金人占松有皮肤普通话的42-78%,除Chachi和Red-Tangerine之外(附加档案)4.:图S1);Chachi和red- tangerve叶片特异积累了邻氨基苯甲酸甲酯,分别占TVC的69.88和43%D.- 二烯酮,烯丙和三丁烯是其他松弛皮肤普通话种质中的主要挥发性化合物。Sesquiterpenoids仅占Chachi中的5%的TVC,其明显低于其他普通话种质(附加档案)1:表S1和附加文件5.:图S2)。
在10C. ichangensis.检测到128种挥发性化合物,其中包括76个酪蛋白萜类化合物,其占TVC的30-50%(表1;附加文件4.:图S1)。在C. Junos.,共鉴定出55个化合物,其中萜类化合物47个。这些挥发性化合物中有73种和13种为特征性C. ichangensis.和C. Junos.,分别(附加文件1:表S1)。虽然检测到的化合物数量C. Junos.比在C. ichangensis.那C. Junos.展出了更高的TVC水平。值得注意的是,人世尼烯,水平β-Cubebene,Germacrene D和β-elemene in.C. Junos.显着高于最多C. ichangensis.种质(> 10倍),而Trans-β.-ocimene和(+) -δ.-cadinene在显着更高的水平下存在C. ichangensis.而不是C. Junos.(> 10倍)(附加文件1:表S1)。
9份香橼种质共鉴定出119个挥发性化合物,挥发性成分的TVC范围为4.03±0.44 mg/g(元江香橼)~ 15.52±0.84 mg/g(红柠檬),挥发性成分的数量范围为41个(丹纳香橼)~ 65个(酸橙)1).单波培是Citron Gromplasms中的主要化合物(附加文件4.:图S1)。RL叶含有60个挥发性化合物,具有最高的TVC,有D.-柠檬烯含量最高,其次是β蒎烯(Z Z) - α-法呢粮,和亚曲线(附加文件1:表S1)。
在12个pummelo种质中,检测到73种挥发性化合物。TVC范围为0.22±0.03 mg / g(kaopan pummelo)至2.15±0.12 mg / g(Shatian Pummelo)(表1),单调位是大多数Pummelo种系中最丰富的,占TVC的50%以上(附加文件4.:图S1)。Hb Pumlo叶子的TVC低(1.90±0.26 mg / g),几乎不可检测的倍半萜(额外文件1:表S1)。
在八个酸橙和三种酸橙和三种甜橙色种质中,分别检测88和64种挥发性化合物。单调萜是橙色物种中最丰富的(附加文件4.:图S1)。从钩头成的叶片中检测到52种化合物(见表)1),β- 丁烯是最丰富的,其次是LINALOOL,亚氰基烯酮,人屈苯胺和反式-β-ocimene。最丰富的化合物是小妃酸橙的乙酸盐;Linalool和(+) - Defuniya酸橙的双环伯烯;和反式-β-甜橙中胭脂烯和沙宾烯(附加文件1:表S1和附加文件3.:表S3)。
基于叶波挥发性概况的柑橘类别CPCOA
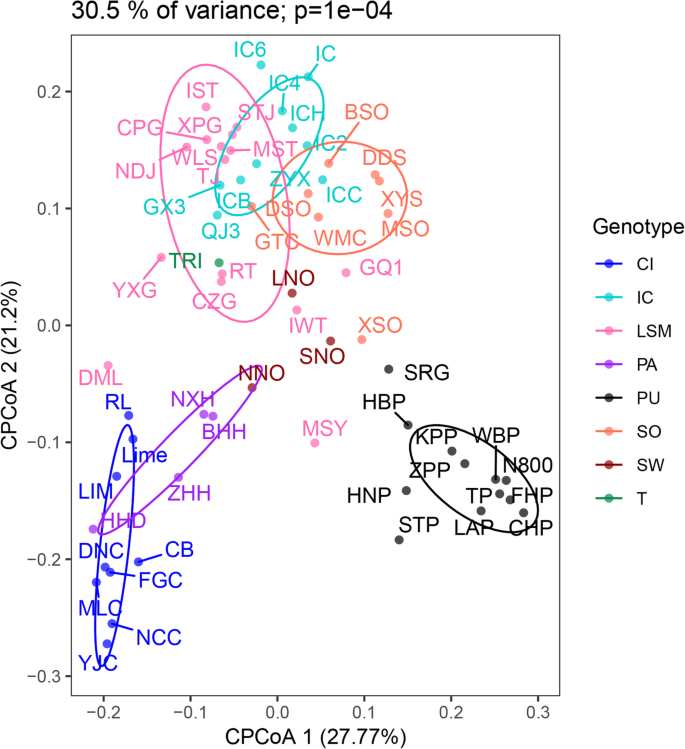
CPCOA基于叶挥发物将62种柑橘种质分为六簇:簇1,松弛皮肤普通话;集群2,C. ichangensis.;簇3,酸橙;群集4,Pumlo;第5群,Papeda;和群集6,citron。通常,将相同物种的不同含义聚集在一起。三C. Junos.Germplass(冠县湘城3号,千江祥城3号和Ziyang Xiangcheng)与松弛皮肤普通话聚集(图。2).
柑橘种质资源中单萜类和倍半萜类的生物合成
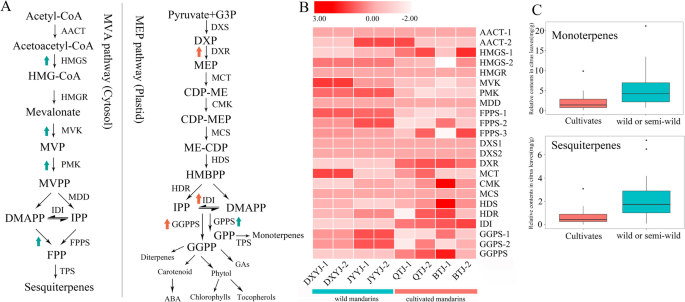
在大多数野生或半周半种质中的叶片中,含有更高的水平和更多种类的挥发性化合物,特别是单萜和酪蛋白萜烯比在品种的叶子中(图。3.c),与Flavedo和果汁囊的挥发性曲线一致(附加文件6.:图S3)。在两个野生种(JYYJ和DXYJ)和两个品种(BTJ和QTJ)中进行表达水平的比较。在野生种子中,表达3-羟基-3-甲基戊齐芳基 - 辛酸酶-2(HMGS-2),甲戊二醇酯激酶(MVK.),磷酮激酶(PMK.) 和法呢基焦磷酸合成酶(FPPS.)在MVA途径和Geranyl焦磷酸合酶(gpp)在MEP途径中显着高于品种。此外,天竺葵二磷酸二磷酸合成酶(GGPPS.在参与类胡萝卜素、脱落酸(ABA)和二萜代谢的MEP通路中,野生品种的表达量显著低于栽培品种(图。3.)ab。
柑橘栽培种与野生或半野生种质叶片中萜类生物合成途径的差异基因表达模式一种:植物中萜类化合物的生物合成途径。AACT:乙酰乙酰-CoA硫醇酶;HMGS:3-羟基-3-甲基戊芳基合成酶;HMGR:HMG-COA还原酶;MVK:Mevalonate激酶;PMK:磷酮酸酯激酶;IDI:异戊烯基二磷酸异构酶;DXS:1-脱氧-D-木糖5-磷酸合成酶;DXR:1-脱氧-D-木糖5-磷酸氧化酯酶;IPP:异戊烯基二磷酸; FPPS: farnesyl pyrophosphate synthase; GPPS: geranyl pyrophosphate synthase; GGPPS: geranylgeranyl diphosphate synthase.B.: MVA和MEP途径的差异表达基因;C:在野生或半瓦米种和品种的叶片中聚会和Sesquiterpenes积累的差异
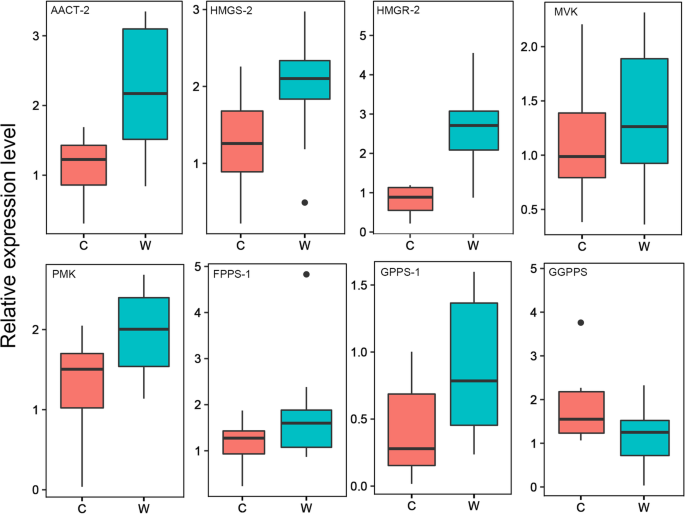
为了进一步阐明MVA和MEP途径在野生和品种种质中的萜类化合物的表达水平,10种野生和10种柑橘种质的叶样品用于RT-QPCR分析。(附加文件7.:表S4)。大多数基因的表达水平在RT-QPCR和转录组数据分析中显示出野生和品种柑橘种质之间的趋势。RT-QPCR结果表明,野生柑橘种质中MVA途径中大多数基因的表达水平高于品种中的基因,而MEP途径中的大多数基因在野生和品种种质之间没有显着差异。在野生种子中,表达gpp(GPPS-1和GPPS-2)高于栽培品种GGPPS.在野生种质中表达较低的表达,而不是在栽培种中(图。4.和附加文件8.:图S4)。
鲜花中的挥发性概况
25份柑橘种质资源在两个开放阶段(球囊期、F1;完全开放阶段,F2),包括60个萜类化合物和22个其他化合物(附加文件9.:表S5)。TVC范围从1414.33±51.39μg/ g(GQ1,F1)到6235.60±142.94μg/ g(星形Ruby葡萄柚,SRG,F1),以及从19(Fenghuang Pummelo,FHP,F1&F2)到45的化合物的数量(SRG,F2)(附加文件9.:表S5)。Terpenoids是柑橘花中最丰富的挥发物,在大多数柑橘种质中占TVC的80%以上,除了红橘(约39%)(约39%)(附加档案10.:表S6)。不同种属花的主要化学成分不同,甜橙花的主要化学成分为沙宾烯,其次为沙宾烯D.- 二烯酮和李纳洛;γ-萜烯是最丰富的大多数松弛皮肤普通话种质,除了红橘(二甲基炭疽酸);D.- 司和β- 离亚胺在Pummelo中占主导地位;和D.- 司,β- 新尼和β-ocimene是柠檬中最丰富的柠檬(附加文件9.:表S5和附加文件10.:表S6)。与叶片中的挥发物相比,8-羟基氨基是花的,花朵,花朵,花朵的水平高于叶片中的那些水平,而Linalool含量与叶片相似。然而,对于大多数挥发物,例如亚氰基和生殖器乙烯D,在花中检测到较低的水平(附加文件11.:图S5)。
在同一种质中,两次调查阶段之间的花挥发性概况通常相似(附加文件12.:表S7)。而在完全开放期,甜橙中芳樟醇、8-羟基芳樟醇、橙花醇和法尼醇含量显著升高,而沙滨烯含量显著降低13.:图S6)。柚子的芳樟醇、橙花醇和法尼醇水平显著升高,而在β- 金英,β- 观察到丁烯和单屈苯尼水平。松弛皮肤普通话和柠檬在法鼻机级别的增加(附加档案9.:表S5)。
在卡拉卡拉肚脐橙色花朵和表征的Deg曲线stps.
在Cara Cara Navel橙色的花朵中检测到总共36种挥发性化合物,包括27萜件(附加文件9.:表S5),其中沙宾烯含量最高。对两个开花期的花进行转录组分析,共获得35.8 G高质量碱基对(每个样品至少5.2 G)。大约96.16-98.19%的测序结果与甜橙基因组一致。在已对齐的读中,89.67-92.41%是唯一对齐的,5.64-6.59%被映射到多个loci(附加文件14.:表S8)。总的来说,F1和F2中的18,654和18,267个表达基因的表达模式具有高于0.5的FPKM值。平均FPKM值为33.17和44.53,分别为1至100的FPKM值的表达基因分别为F1和F2中所有未成熟的86.71%和85.24%。有1013和626个基因分别在F1和F2中表达(附加文件15.:图S7)。
通过RNA-Seq分析(| Log)共鉴定出2528个差异表达基因(DEGs)2FC | > 1.5 andP.-value < 0.05)(附加文件16.:表S9)。GO注释和富集结果主要与植物代谢物相关,例如木质素,苯丙醇,第二代谢物和芳烃(附加文件17.:图S8)。与气球阶段花卉相比,1281和1247个基因分别在完全开花中显着上调 - 下调。其中,47TPS.和65年CYP450找到基因(附加文件18.:表S10)。萜烯谱与基因表达水平之间的相关性分析显示,三丁烯含量及表达水平CS3G04360有最高的Pearson相关系数(0.95)。Pearson相关系数高于Linalool含量和10之间的0.9TPS.基因(CS5G23540,CS5G22980,CS2G03570,CS3G21560,CS2G22180,CS2G07250,CS2G07240,CS2G06470,CS2G07230和CS7G17670)(附加文件17.:图S8和“附加”文件18.:表S10)。Pearson相关系数高于8-羟基氨基和36之间的0.9CYP450基因,包括七种CYP76C亚家族基因。这些候选基因可能有助于产生相应的挥发性Terpenes。
根据高Pearson相关系数,aTPS.候选基因命名stps.在这项研究中,从卡拉卡拉脐橙花克隆,具有1824年的开放阅读框架,并编码607个氨基酸的蛋白质(附加文件19.:表S11),它类似于CS3G04360但有10个不同的残留物(附加文件20.:图S9a)。该蛋白质含有TPS活性和RRX所需的预期二价金属结合区域(DDXXD)8.W常见的基质常见于循环单萜烯酶(附加文件21.:表S12)。表达stps.在完全开放的花中显著减少(附加文件20.:图S9
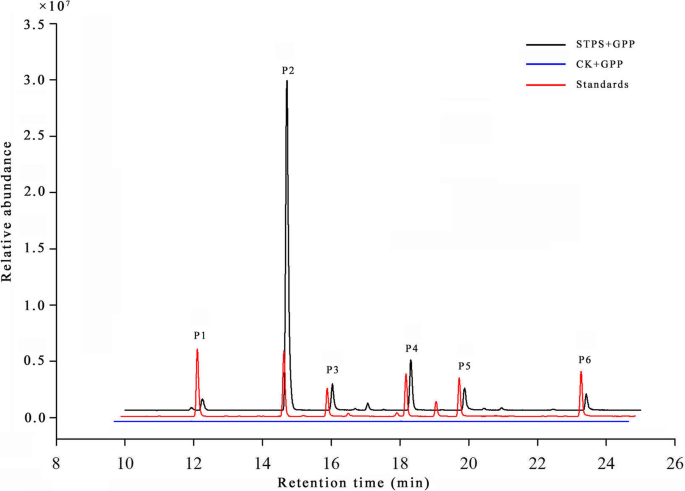
重组蛋白表达大肠杆菌并使用Ni的组合纯化2+亲和力和尺寸排阻色谱。Western印迹分析表明,成功构建了产生大量蛋白质的原核表达载体(附加文件17.:图S8 CD)。体外加入GPP或FPP,溶剂萃取后GC-MS检测表明,STPS催化GPP转化为单萜,其中sabine占18.68%,占61.26%D.- 二烯酮,7.89%LILLOOL,5.65%Trans-β.- 离亚胺,4.32%β- -Myrcene和2.20%α-拼烯(图。5.).当FPP用作基材时,检测到萜烯化合物。
讨论
叶子中的不同叶挥发物可以促进柑橘类分类的研究
以前的研究表明,柑橘植物,特别是皮肤,富含挥发物[4.那22.].柑橘植物皮下的TVC高于10毫克/克,但在果汁囊中大部分低于0.05mg / g,叶子3-10mg / g,花中2.5-5毫克/ g(附加文件22.:图S10)。我们以前的工作报道,果皮中挥发性化合物的数量为40-60,汁囊中的20以下[22.].然而,本研究在叶中鉴定出30-50种挥发性化合物,在花中鉴定出30-40种挥发性化合物1;附加文件22.:图S10和附加文件9.:表S5)。虽然在叶片和花中检测到的化合物的总水平和数量小于果皮,但发现一些化合物是特异于叶和花的,并且叶片中的主要化合物比剥离中的那些更多样化。
在大部分柑橘种质中,黄酮和果汁囊中挥发性成分以单萜为主,尤以单萜为主D.-柠檬烯(大部分超过60%)[22.那24.].但是,与之前的研究一致[31.],D.- 二烷烃不是大多数柑橘种质叶子中最丰富的挥发性。值得注意的是,乙酸烯丙酯,李纳洛团和β-elemene主要累积在酸橙和yxg中(附加文件3.:表S3),其据报道患有抗炎和抗肿瘤生物活跃[15.那17.].
此外,我们之前的工作揭示了C. ichangensis.富含倍半萜。据此,在10种植物的叶片中检出76种倍半萜类化合物C. ichangensis.种质,其中七个是特定的C. ichangensis.(附加文件1:表S1)。叶片中的挥发性曲线可用于研究柑橘类分类物。基于柑橘叶中挥发性化合物的CPCOA分类的结果与基于柑橘剥离挥发物的HCA结果相似[22.].以前的研究表明,酸橙是松弛皮肤普通话和Pummelo的杂交[32.].在这项研究中,酸橙被聚集在松弛的皮肤普通话附近,暗示松弛皮肤普通话对酸橙挥发性代谢的强烈影响,这也与剥离的聚类结果一致[22.].C. Junos.是一种混合C. ichangensis.和松弛皮肤普通话[33.].CPCOA分析显示C. Junos.被聚集在一起C. ichangensis.和松弛皮肤普通话(图。2).的分类柑橘曼加山在以前的报告中有争议[28.那32.].该研究邻近Pumelo的聚类该物种(图。2),类似于Liu等人的报告。[28.].已经证明挥发物可以应用于柑橘植物的趋化性研究[34.]最近通过其他研究人员验证了哪些可靠性[22.那27.那28.].我们的CPCOA分析提供了提供可靠性的进一步证据。
在精华油工业中,甜橙叶和鲜花丰富的人楸是胡萝卜籽油的主要组成部分。Linalool大多数松弛皮肤普通话种质种质的李纳洛有多种商业应用,其中大多数是基于其令人愉快的气味。乙酸盐含有丰富的叶片,最酸橙种质的叶子,C. ichangensis.是佛手柑精油的主要成分之一。D.- 二烷烃,食品制造中的调味剂,是大多数柑橘皮中最重要的化合物,也是Citron叶子的丰富(附加文件3.:表S3)。在柑橘叶中发现了许多风味化合物,其中一些可用于食品添加剂,化妆品和香水中。
此外,随着叶子是主要的光合器官,叶挥发物可能在排斥害虫和有害微生物中发挥作用[11.那12.].考虑到柑橘叶的快速增长,高生物量和四季收获时间跨度,柑橘叶片挥发物的组成和生物合成机制令要求进一步深入研究工业应用。
柑橘品种中的叶片挥发物的降低是由于柑橘驯化的负面影响
野生和半野生种质各组织中单萜类和倍半萜类总含量均高于品种,尤其是叶片。因此,单萜和倍半萜的含量可能在驯化过程中有所下降。对野生和栽培柑橘叶片关键基因表达量的转录组和RT-qPCR分析表明,大部分基因(HMGS-2那MVK.那PMK.和FPPS.)在MVA途径和gpp在MEP途径中,野生橘子的表达水平明显高于品种。然而,GGPPS.在MEP途径在野生橘子中的表达水平较低,而不是品种(图。3.;无花果。4.).MVA和MEP途径中这些基因的不同表达水平可能影响野生和品种橘子中单口和筛氏萜烯的积累。据报道了这一点GGPPS.负责一些化合物的代谢,如与成熟相关的ABA和与颜色相关的类胡萝卜素[35.].在柑橘育种/选择的长期过程中,果实尺寸,颜色,产量,糖酸比和成熟季节非常重要。结果,在人工选择和驯化过程中,柑橘的有机酸水平显着减少了[36.].水果的颜色一直是人工育种的目标,类胡萝卜素水平的提高可能导致了柑橘植物中挥发性化合物水平的下降。
在柑橘花中发现的候选基因解释了它们独特的香味
与柑橘皮和叶挥发物相比,柑橘类植物虫性花挥发物含量低,数量少。芳樟醇、8-羟基芳樟醇、橙花醇和法尼醇水平升高和某些单萜水平降低(附加文件13.:图S6)在完全开花阶段与甜花香密切相关(http://www.thegoodscentscomp-yany.com/index.html.)和授粉的特定昆虫的吸引力,在理论和实践研究方面都是至关重要的。
有95名候选人TPS.在甜橙色发现的基因座,但很少有这些基因座已经过验证[18.那19.那21.].在鲜花的两个开口阶段有一些三萜类化合物显着差异,具有一些高保性的相关系数观察到TPS.沙CYP450S通过转录组和相关系数分析,例如两个TPS.基因(CS3G04360和Orange1.1 T00017),其可以在生产的生产中起作用(附加文件17.:图S8)。STPS体外功能分析表明,该酶是一种单萜合成酶,可产生6种单萜,其中以GPP为底物时主要产物为沙宾烯(图)。5.),这表明stps.是三丁烯合成的重要基因。
结论
本研究从柑橘叶和花中鉴定了挥发性化合物。结果表明,野生和半野生植物中有31种重要的萜类化合物。转录组学和RT-qPCR分析表明,大部分基因在野生和半野生种质中的表达量高于品种,可能是驯化对柑橘叶片中挥发性萜类生物合酶的负面影响。完全开放的花的香味可能是由于四种萜烯醇含量的增加。结果表明,柑桔叶可作为植物精油生产、萜类生物合成及萜类代谢调控研究的重要原料。
方法
材料和样品收集
2016年,从中国4个柑橘产区采集62份柑橘种质资源,其中16份来自国家柑橘育种中心(武汉,湖北),40份来自中国农业科学院柑橘研究所(重庆,北碚),3份来自瑞丽市柑橘研究所(瑞丽市,3个来自广东省农业科学院(广东广州)。有15个皮肤松弛的官员(柑橘类reticulata.),三个甜橙(c . sinensis),12 pummelos(C. Maxim.),10C. ichangensis.,九个香吨(c .柠檬),四个papedas(C. hystrix.),八个酸橙(c .橙)和一个poncirus trifoliata(桌子1).新春拍摄的完全扩张的叶子在果园在果园在果园在果树在7月份。每种种质共30-40个平均大小的成人叶子用自来水洗涤,用清洁纸擦干,然后随机分为三个生物重复。将叶子置于液氮中并储存在-80℃以进一步分析。
花的25个种质(附加文件9.在2017年NCBC的两个开放阶段(球囊期第4天和完全开放期第2天),从成年健康树木的冠层外部采集。将12-15朵花随机分为3个重复,放置于液氮中,在−80℃下保存以备进一步分析。
标准和试剂
为了测定GC-MS上的挥发性化合物,从Sigma(St.Louis,Mo,USA)和Alfa(Alfa Aesar Co.Lten UK)购买了57个真实标准,如额外文件所示2表S2,在甲基叔丁基醚(MTBE, HPLC级)中溶解。MTBE购自美国Tedia (Fairfield, OH, USA),用作溶剂提取挥发物。
挥发性提取和GC-MS分析
根据Zhang等人进行挥发性提取。[22.]微小修改。将叶子或全鲜花磨碎为粉末。然后,将0.3g样品用于促进挥发物。通过痕量GC超GC与DSQ 8000质谱仪(Thermo Fisher Scientific,Waltham,MA)通过痕量TR-5 MS柱(30m×0.25mm×0.25μm; Thermo Scientific,Bellefonte,PA)分裂比例为20:1。挥发物GC-MS的其他参数基于Liu等人的研究。[24.].
RNA提取和转录组测序
遵循Cao等人的方法。[37.],从气球(F1-1,F1-2和F1-3)的Cara Cara Navel橙色的花中提取总RNA,并完全打开(F2-1,F2-2和F2-3)阶段,具有三个生物学重复。对于每个样品,将2μg总RNA发送到千年Co.(韩国),用于RNA-SEQ图书馆构建和测序。使用Illumina Truseq RNA样品制备试剂盒V2从总RNA纯化mRNA,并使用安捷伦技术2100生物分析仪(Agilent,美国)评估。遵循Truseq RNA样品制备v2指南(15026495)(Illumina,美国),合成第一和第二链互补DNA,然后纯化双链cDNA,并加入适配器。将mRNA切割成约300bp的短片段,并且在终端模式下对Illumina Hiseq 4000平台进行测序。
RNA-SEQ数据分析
在本研究中新测序F1和F2的RNA-SEQ数据。RNA-SEQ用于两种野生柑橘种质的叶子的原始数据(DXYJ,SRR5807703; JYYJ,SRR5807742)和两种品种(BTJ,SRR580774; QTJ,SRR5807788)[36.]下载自NCBI (https://www.ncbi.nlm.nih.gov/).参考柑橘基因组V2.1和注释文件从中下载柑橘sinensis.注释项目(http://citrus.hzau.edu.cn/orange/index.php.).参考基因组的指标由Star_2.6.0a产生[38.].使用Trimmomatic-0.36过滤所有RNA-Seq原始数据以去除低质量reads [39.].使用Star_2.6.0a将清洁的读数映射到参考柑橘基因组[38.].基于比对,使用HTSeq估计转录本丰度[40].使用R包edgeR对DEGs进行分析[41.].F1和F2用于鉴定萜烯合酶的候选基因。DXYJ,JYYJ,BTJ和QTJ用于分析MVA和MEP途径中基因的表达模式。
RNA提取和RT-QPCR
从20个柑橘叶样品中提取总RNA(附加文件7.:表S4)使用EasySpin Plus植物RNA套件(RN38,AIDLAB)。使用Hiscrip®IIQTTRT超混合物合成第一链cDNA,用于QPCR(+ GDNA刮水器,Vazyme)。用于RT-QPCR的基因特异性引物在附加文件中列出21.:表S12。使用Hieff™QPCR Sybr Green Master Mix使用带384孔板的Roche LightCycler 480系统进行RT-QPCR(NO ROX,Yeasen Biotech Co.,Ltd.,Shanghai,China),根据此处进行manufacturer’s protocol.施作为内源对照。RT-qPCR数据分析按照Lu等人的方法进行[42.].
stps.基因鉴定和功能分析
stps.是用附加文件中描述的引物和载体克隆的21.:表S12。使用ORF Finder预测开放阅读框和过境肽(http://www.ncbi.nlm.nih.gov.)和目标(http://www.cbs.dut.dk/service/Targetp)分别。如Cao等人所述进行STP的蛋白质印迹分析。[37.].
对于功能分析,stps.扩增去除叶绿体靶向肽,克隆到pET-28a(+)载体中,引物列于Additional file21.:表S12。重组N-末端他标记的蛋白质被表达大肠杆菌BL21(DE3)。细菌菌株种植到a600 = 0.6 at 37 °C in 100 ml of LB medium with 50 μg/ml kanamycin. Cultures were induced with 1 mM isopropyl 1-thio-β-D-galactopyranoside (IPTG) and incubated with shaking for 16 h at 180 rpm and 16 °C. The proteins were purified by Ni2+如前所述的亲和力和尺寸排阻色谱。如Brillada等人所述的体外表征STP。[43.]微小修改。将STP加入到500μL的测定缓冲液(25mM HEPES(pH7.3),10mM MgCl中2,0.1 mm mncl2,0.2 mm Nawo4.,0.1mm NAF,5mM DTT和10%甘油),与50μmGPP或FPP混合,覆盖着戊烷,并在30℃下孵育30分钟。将戊烷层转移到玻璃瓶中并如Liu等人所述对GC-MS分析进行。[24.].
数据分析
共使用57种标准挥发性化合物进行鉴定。对于那些没有真实标准的,鉴定是基于Xcalibur软件和NIST质谱库(NIST 2015)。通过与内标比较,定量测定各挥发性化合物的浓度。正如Zhang等人报道的那样,柑桔皮和果汁囊中的挥发性化合物含量是由我们之前的研究结果获得的[22.].
使用Excel(Microsoft,Seattle,WA)产生散点图。使用r中的ggplot2包构建直方图和boxplots [44.]和Sigmaplot 12.0,并且使用TBTOOLS构建热图[45.].使用素食包装进行CPCoA分析46.].使用r中的混合物(PLS-DA)和GGPLOT2封装分析甜橙色F1和F2中挥发性化合物的差异积分。47.].使用r中的性能Areanalytics包进行萜烯谱和基因表达水平的相关系数分析[48.].
数据和材料的可用性
本研究中产生或分析的所有数据均包含在本文和附加文件中。RNA-seq数据可从NCBI获得,登录号为PRJNA579049。
缩写
- cpcoa:
-
受限主坐标分析
- CYP450:
-
细胞色素P450
- 可见:
-
不同的基因表达
- DMAPP:
-
异构体二甲基丙烯酸二磷酸
- FPP:
-
法呢基焦磷酸盐
- FPPS:
-
FPP合酶
- GC-MS:
-
气相色谱分析-质谱法
- GGPPS:
-
天竺葵二磷酸二磷酸合成酶
- GPP:
-
大烷基焦磷酸盐
- gpp:
-
GPP合成酶
- HCA:
-
分层集群分析
- HMGS:
-
3-羟基-3-甲基戊芳基 - COA合成酶
- IPP:
-
异戊烯基焦磷酸盐;
- MEP:
-
2-C-甲基-D-赤藓糖醇-4-磷酸盐
- MTBE:
-
甲基叔丁基醚
- MVA:
-
米瓦洛酸盐
- MVK:
-
甲戊二醇酯激酶
- PCA:
-
主要成分分析
- PLS-DA:
-
偏最小二乘-判别分析
- PMK:
-
Phosphomevalonate激酶
- STPS:
-
Sabinene合成基因
- TPS:
-
萜烯合成基因
- TVC:
-
总挥发性内容
参考文献
- 1。
陈俊,张H,庞y,程y,邓x,徐J.番茄红素累积和金发肉甜橙黄素生产的比较研究(柑橘sinensis.)在水果开发期间。食品化学。2015; 184:238-46。
- 2。
李W,刘C,李c,李杰,蔡Y,Ma y,Xu J.在大量不同含量的牛肉红肉橘子及其野生型。BMC植物BIOL。2017; 17(1):36。
- 3.
徐杰,马尔,江德,朱思,闫硕,谢y,谢z,郭伟,邓小平4例柑橘种质中4例呋喃加仑单体的含量评价。食品化学。2015; 187:75-81。
- 4.
González-Mas MC,Rambla JL,López-Gresa MP,BlázquezMa,Granell A.柑橘精油的挥发性化合物:全面审查。前植物SCI。2019; 10:12。
- 5。
鲍德温。植物挥发物。咕咕叫医学杂志,2010;20 (9):R392-7。
- 6。
Bohlmann J,Meyer-Gauen G,Croteau R. Plant Terpenoid合成酶:分子生物学和系统发育分析。P Natl Acad Sci USA。1998; 95(8):4126-33。
- 7。
Chappell J.异戊二烯代谢的生物化学和分子生物学。植物理性。1995; 107(1):1-6。
- 8。
程爱森,娄永刚,毛彦波,卢松,王丽娟,陈小勇。植物萜类化合物的生物合成与生态功能。植物学报,2007;49(2):179-86。
- 9。
Boachon B,Junker Rr,Miesch L,Bassard J-E,HöferR,CaillieAudeaux R,Seidel de,Lesot A,Heinrich C,Ginglinger J-F。CYP76C1(细胞色素P450)介导的LINALOOL代谢和拟南芥挥发性和可溶性LINALOOL氧化物的形成:一种防御花卉拮抗剂的策略。植物细胞。2015; 27(10):2972-90。
- 10。
Weitzel C,Simonsen HT。细胞色素P450-酶参与单萜和筛氏萜烯的生物合成。Phytochem Rev. 2013; 14(1):7-24。
- 11.
Schnee C,Kollner TG,举行M,卧耳TC,Gershenzon J,Degenhardt J.单一玉米倍二萜合酶的产品形成了一种挥发性防御信号,吸引了玉米食草动物的自然敌人。P Natl Acad Sci USA。2006; 103(4):1129-34。
- 12.
丁颖,huhuffaker A, Köllner TG, Weckwerth P, Robert CAM, Spencer JL, Lipka AE, Schmelz EA. Selinene挥发物是促进玉米抗病的重要前体。植物杂志。2017;175(3):1455 - 68。
- 13。
KöllnerTG,Matthias H,Claudia L,Ivan H,Turlings TCJ,Jonathan G,Jörgd.A玉米(E.) - 在大多数美国玉米品种中没有表达患有针对草食物的间接防御反应的β-亚芳啉基合成酶。植物细胞。2008; 20(2):482-94。
- 14。
andrade ln,de sousa dp。单调位抗炎活动综述。分子。2013; 18(1):1227-54。
- 15.
PEANA AT,D'AQUILA PS,PANIN F,SERRA G,PIPPIA P,MORETTI MD。烯加索机的抗炎活性和精油的LINALOOL和LINALYLATE组分。phyt int phyto phytoph。2002; 9(8):721-6。
- 16。
可再生化学中天然基础化学成分的研究进展。Chemsuschem。2010;2(12):1072 - 95。
- 17。
姚益,丁X,佳益,黄cx,王yz,徐耶。胶质母细胞瘤细胞中β-榄烯的抗肿瘤作用取决于P38 MAPK激活。癌症吧。2008; 264(1):127-34。
- 18。
Alquézarb,rodrígueza,peñamdl,peña1.萜烯合成酶系列的基因组分析和七个倍二萜合酶的功能性表征柑橘sinensis..前植物SCI。2017; 8:1481。
- 19。
陈志刚,李志刚,李志刚,等。柑橘果实风味和香气的生物合成:分离、功能鉴定和发育调控CSTPS1.,筛选酪蛋白酶芳香化合物巴伦烯的主要基因。工厂J. 2003; 36(5):664。
- 20。
岛田,藤井,原原,上田,喜多,大村等柑橘unshiu.马克。植物SCI。2004; 166(1):49-58。
- 21。
Li X, Xu Y, Shen S, Yin X, Klee H, Zhang B, Chen K.转录因子CitERF71激活萜烯合成酶基因CITTPS16参与甜橙果实中E-Geraniol的合成。J Exp Bot。2017; 68(17):4929-38。
- 22。
张H,谢y,刘C,陈S,hu s,xie z,deng x,xu J.含有不同物种柑橘果实挥发性化合物的综合对比分析。食品化学。2017; 230:316-26。
- 23。
大厅Ja,Wilson CP。瓦伦西亚橙汁的挥发性成分。Jamchemsoc。1925; 10:2575-84。
- 24.
刘超,程勇,张辉,邓欣,陈飞,徐军。野生柑橘挥发性成分的研究进展柑橘Nobilis.Lauriro)剥油。j农业食品化学。2012; 60(10):2617-28。
- 25.
摆动wt。柑橘的植物学和橙色亚家族的野生亲属。柑橘行业。1943; 1:128-474。
- 26.
田中平,田中平。柑橘的物种问题:基于野生和栽培单元的柑橘的研究。中国柑橘科学。1954;9:139。
- 27.
景L,Lei Z,张G,赃物AC,Huhman Dv,谢R,Xi W,周Z,Sumner LW。柑橘皮中精油的代谢物谱及其分类症状。代谢组学。2015; 11(4):952-63。
- 28.
刘C,江D,程义,邓X,陈福,方升,马Z,徐J。趋化学研究柑橘那Poncirus.和Fortunella基于剥离油挥发性化合物的基因型 - 解密Mangshanyegan的遗传来源(柑橘Nobilis.Lauriro)。Plos一个。2013; 8(3):E58411。
- 29。
Gonzalez-Mas MC,Rambla JL,Alamar MC,Gutierrez A,Granell A.来自不同柑橘种类果汁的挥发性分数的比较分析。Plos一个。2011; 6(7):E22016。
- 30。
张H,刘C,姚吉,邓Ch,陈某,陈继,王z,yu q,cheng y,xu J.柑橘曼加山花粉通过增强细胞色素P450 78A7基因冠军1的表达,赋予Xenia对裂解氧化物氧化物积累的血清氧化物积累。j农业食品化学。2019; 67(34):9468-76。
- 31。
AZAM M,江Q,张B,徐C,陈克。柑橘叶挥发物受发育阶段和遗传型的影响。int j mol sci。2013; 14(9):17744-66。
- 32。
Wu Ga,Prochnik S,Jenkins J,Salse J,Hellsten U,Hellsten U,Murat F,Perrier X,Ruiz M,Scalabrin S,Terol J.序列的不同普通话,Pummelo和Orange Genomes揭示了柑橘驯化期间的复杂混合物历史。NAT BIOTECHNOL。2014; 32(7):656。
- 33。
Merle H,MorónM,BlázquezMa,Boira H.普通话品种精油的分类贡献。生物学习系统系统。2004; 32(5):491-7。
- 34。
Scora RW, Malik MN。柑橘的化学特征作为系统发育的工具。分类单元。1970;19(2):215 - 28。
- 35。
Aharoni A,Jongsma Ma,Bouwmeester HJ。挥发性科学?植物萜类化合物的代谢工程。趋势植物SCI。2005; 10(12):594-602。
- 36。
王丽,何芳,黄勇,何杰,杨胜,曾杰,邓超,姜旭,方勇,温胜。野生柑桔基因组与驯化历史。摩尔。2018;11(8):1024 - 37。
- 37。
Cao H,Wang J,Dong X,Han Y,MA Q,Ding Y,Zhao F,张J,陈H,徐Q.类胡萝卜素积累影响氧化还原状态,淀粉代谢和黄酮类药物在柑橘中的积累。BMC植物BIOL。2015; 15(1):27。
- 38。
Dobin A,Davis Ca,Schlesinger F,Drenkow J,Zaleski C,JHA S,Batut P,Chaisson M,Gingeras TR。星:超快通用RNA-SEQ对齐器。生物信息学。2013; 29(1):15-21。
- 39。
Bolger Am,Lohse M,Usadel B. Trimmomatic:用于Illumina序列数据的灵活修剪器。生物信息学。2014; 30(15):2114-20。
- 40。
Anders S,Pyl Pt,Huber W. Htseq-A Python框架,用于使用高吞吐量排序数据。生物信息学。2015; 31(2):166-9。
- 41。
DM MDR,SMYTH GK。编辑:用于数字基因表达数据的差异表达分析的生物导体包。生物信息学。2010; 26(1):139-40。
- 42。
吕某,张y,朱克,杨,叶茹,柴l,徐q,邓x。柑橘转录因子Csmads6通过直接调节致癌基因来调节类胡萝卜素代谢。植物理性。2018; 176(4):2657-76。
- 43。
Carla B,Masahiro N,Takeshi S,Stefan G,Wilhelm B,Maffei Me,Gen-Ichiro A. C16-Homoterpene TMTT的代谢工程莲花japonicus.通过过度表达(e,E.香叶醇合酶以不同的方式吸引通才捕食者和专才捕食者。新植醇。2013;200(4):1200 - 11所示。
- 44。
Wickham H: ggplot2:优雅的数据分析图形:施普林格;2016.
- 45。
Chen C,夏R,陈H,何Y.TBTools,生物学家的工具包与用户友好的界面集成了各种HTS数据处理工具;2018年。
- 46。
Oksanen J, Blanchet F, Kindt R, Legendre P, Minchin P, O’hara R, Simpson G, Solymos P, Henry M, Stevens H.排序方法、多样性分析和其他功能的群落和植被生态学家。素食:社区生态包。2017:05-26。
- 47。
Rohart F,Gautier B,Singh A,LêCaoK-A。混合组:“OMICS”功能选择和多个数据集成的R包。PLOS计算BIOL。2017; 13(11):E1005752。
- 48.
Peterson BG,Carl P,Boudt K,Bennett R,Ulrich J,Zivot E,Cornilly D,Hung E,Lestel M,Balphissoon K,Wuertz D. R包装'PerformanceAnalytics'。2018年。https://cran.r-project.org/web/packages/performanceanancytics/.
确认
我们感谢Shouping Shouping Zhu博士西南大学柑橘研究所,为她在样品收藏中的帮助下。我们还感谢Zuoxiong Liu教授,从外国语学院of Huazhong农业大学进行修改和改进稿件的英语。
资金
该工作得到了国家重点研究和发展计划(2018YFD1000200)和中国国家自然科学基金(NSFC 31272122)的支持。该资助者支付了与实验成本和出版费用相关的成本,但在研究和收集,分析和数据的诠释方面没有作用以及写作稿件。
作者信息
隶属关系
贡献
JX和YC设计了实验;赫兹表演了大部分实验;MC,HW和LF执行了一部分实验;Hz和Hyz分析了挥发性化合物数据;ZW和JC提取叶RNA;ZX和DJ收集的材料,提供了分析方法并改进了稿件。Hz和JX写了稿件。JX和YC审查并编辑了手稿。所有作者都同意稿件内容并提交。所有作者阅读并认可的终稿。
通讯作者
伦理宣言
伦理批准和同意参与
我们在本研究中遵守国家法律和伦理批准。
同意出版
不适用。
相互竞争的利益
提交人声明他们没有竞争利益。
附加信息
出版商的注意事项
Springer Nature在发表地图和机构附属机构中的司法管辖权索赔方面仍然是中立的。
补充信息
附加文件1:表S1。
柑桔叶挥发物(μg/g)。U:察觉。
附加文件2:表S2
.挥发性复合测定中使用的五十七项标准。一种Sigma,Sigma-Aldrich(圣路易斯,MO);Alfa,Alfa Aesar Co. Ltd.(英国Heysham)。
附加文件3:表S3
.柑桔种质叶片高含量挥发物前5名,包括柑橘hystrix.那C. ichangensis.,citron,pummelo,松弛的橘子,甜橙,酸橙和poncirus trifoliata.
附加文件4:图S1
.各种种质叶片中总挥发物中的单口和塞萜的比例。LSM:松弛皮肤普通话;PA:Papeda;CI:Citron;所以:酸橙;我知道了:C. ichangensis.;西南:甜橙;菩:柚子;T:poncirus trifoliata.
附加文件5:图S2
.松弛皮肤野生叶子的总挥发物(mg / g)。
附加文件6:图S3
.野生或半瓦米种类和品种果皮和果汁和品种的果皮和果汁中的总挥发性水平和化合物数量(mg / g)。
附加文件7:表S4
.柑橘种质的叶子用于RT-QPCR分析。
附加文件8:图S4
.RT-qPCR分析了柑橘品种和野生或半野生种质MVA途径中的8个基因和MEP途径中的10个基因的转录水平。转录物水平相对于编码的基因的表达水平表达施延伸蛋白。C:品种柑橘种质;W:野生或半孢子种质。
附加文件9:表S5
.柑橘类花(μg/ g)的挥发物。F1:气球舞台,F2:完全开放的舞台。U:察觉。
附加文件10:表S6
.鲜花中重要挥发物和三萜类化综述。(1):鲜花中最丰富的挥发物;(2):总挥发物中单口的比例;(3):总挥发物中的倍半萜烯比例;(4):总挥发物中其他化合物的比例。
附加文件11:图S5
.叶子和花的挥发物水平(μg/ g)。
附加文件12:表S7
.在花的两个开放阶段检测到的总挥发性水平和化合物。外国游客1:气球阶段;F2:完全开放阶段。
附加文件13:图S6
.花中挥发物的PLS-DA分析。答:PLS-DA评分花块。利用挥发性分布图,PLS-DA的结果清楚地区分了两个开放阶段的花。B: PLS-DA模型中挥发物的VIP分数进行判别。C:花在两个开放阶段的生物标志物水平。化合物的水平被归一化为Log2.F1:气球舞台,F2:完全开放的舞台。
附加文件14:表S8
.RNA-Seq原始数据的基本统计。
附加文件15:图S7
.有关鲜花转录组数据的基本信息。A:基于来自花的RNA-SEQ数据的基因表达水平。B:在两个开口阶段的花中基因的组织特异性表达。C:Boxplot显示鲜花的表达水平。原始FPKM数据被标准化为日志10..F1:气球舞台,F2:完全开放的舞台。
附加文件16:表S9
.球囊(F1)之间的差异表达基因和完全打开(F2)花级。
附加文件17:图S8
.在两个开放阶段的鲜花中的差异表达基因。答:差异表达基因的注释。B:萜烯含量的相关系数分析及表达水平TPS.基因。C: Cytoscape_3.7.2与TPS基因表达水平的关系。挥发性化合物TPS.基因列于附加文件18.:表S10。
附加文件18:表S10
.表达水平的TPS.的基因,CYP450花中的基因和挥发性化合物含量。
附加文件19:表S11
.cDNA和蛋白质序列stps..叶绿体靶向肽的cDNA序列用灰色遮荫标记;蛋白质序列中的保守结构域用绿松石着色标记。
附加文件20:图S9
.A:STP和四之间推导的氨基酸序列的对准D.- 二烷基合酶基因。Ku746814,AB110637,AB266584和CS3G04360的氨基酸序列是从NCBI网站和瓦伦西亚甜橙的基因组序列获得的。B:人世替烯含量和相对表达水平stps。C: his标记的STPS蛋白的纯化,SDS-PAGE分析大肠杆菌Western blot分析。M: Protein Ladder (#SM0671);1: Ni-NTA His-Bind Resin色谱柱裂解液的STPS-tr流程;2、3:STPS洗脱物;4: Ni-NTA His-Bind Resin柱裂解液的STPS-fl流动;5,6: STPS-fl洗脱液。D: Western blot法鉴定重组蛋白STPS-tr和STPS-fl。
附加文件21:表S12
.用于克隆的引物stps.和表达载体的构建。
附加文件22:图S10
.不同柑橘组织中的总挥发性含量(mg / g)。
权利和权限
开放访问本文根据创意公约署署署的条款分发了4.0国际许可证(http://creativecommons.org/licenses/by/4.0/)如果您向原始作者和源给出适当的信用,则允许在任何介质中进行不受限制的使用,分发和再现,提供指向Creative Commons许可证的链接,并指示是否进行了更改。Creative Commons公共领域奉献豁免(http://creativecommons.org/publicdomain/zero/1.0/)除非另有说明,否则适用于本文中提供的数据。
关于这篇文章
引用这篇文章
张,H.,Chen,M.,Wen,H.等等。转录组和代谢物分析提供了含有柑橘叶和花的挥发性化合物的洞察力。BMC植物BIOL.20,7(2020)。https://doi.org/10.1186/s12870-019-2222-z.
已收到:
公认:
发表:
关键词
- 柑橘
- 挥发性剖面
- terpenoid生物合成
- 野生或半瓦米德
- stps.