- 研究文章GydF4y2Ba
- 开放访问GydF4y2Ba
- 发布:GydF4y2Ba
探索植物在空间(叶和茎)成分和系统发育组间的代谢组学多样性GydF4y2Ba
BMC植物生物学GydF4y2Ba体积GydF4y2Ba20.GydF4y2Ba文章编号:GydF4y2Ba39GydF4y2Ba(GydF4y2Ba2020.GydF4y2Ba)GydF4y2Ba
摘要GydF4y2Ba
背景GydF4y2Ba
植物是各种化妆品、食品和药品中不可缺少的生物活性化合物的重要来源。然而,这些化合物的后续功能注释似乎是艰巨的,因为大部分未被描述,庞大的代谢库植物物种与已知的生物学表型。因此,需要一种快速的多平行筛选和表征植物功能代谢物的方法。GydF4y2Ba
结果GydF4y2Ba
51种植物代表三科,即菊科、豆科和蔷薇科,采用气相色谱飞行时间质谱(GC-TOF-MS)和超高效液相色谱四极杆轨道阱离子阱串联质谱(UHPLC-Q-orbitrap-MS/MS)对代谢产物进行分析,并进行多因素分析。偏最小二乘判别分析(PLS-DA)显示,51种植物在不同部位(叶和茎)和相对系统发育程度上存在明显的聚类模式。相对代谢物含量的测定表明,豆科植物提取物中含有丰富的氨基酸、脂肪酸和染料木素类化合物。蔷薇科提取物中儿茶素和鞣花酸衍生物含量较高,而菊科提取物中山奈酚衍生物和有机酸含量较高。除不同科外,叶中含有大量与莽草酸途径相关的芳香氨基酸、支链氨基酸、绿原酸、黄酮类化合物和苯丙素。另外,茎提取物中某些氨基酸(脯氨酸、赖氨酸和精氨酸)和脂肪酸水平较高。进一步,我们研究了植物提取物受空间(叶和茎)和家族内代谢组差异影响的相关表型,即抗氧化活性。Pearson相关性分析显示鞣花酸、甘露醇、儿茶素、表儿茶素、槲皮素衍生物与抗氧化表型呈正相关,而穗双酚与酪氨酸酶抑制活性呈正相关。GydF4y2Ba
结论GydF4y2Ba
这些工作表明,代谢谱,包括多平行方法和综合生物分析,可能有助于快速表征植物衍生代谢物,同时阐明其化学多样性。GydF4y2Ba
背景GydF4y2Ba
传统上,植物被用作维持人类健康的药理学活性化合物的重要来源。值得注意的是,植物是药物,化妆品和食品工业中众多抗氧化剂化合物的主要来源[GydF4y2Ba1GydF4y2Ba].特别地,水果和植物提取物中的抗氧化代谢物具有一系列健康益处,例如维持心血管健康和癌症预防,其中许多其他人[GydF4y2Ba2GydF4y2Ba,GydF4y2Ba3.GydF4y2Ba].在草药化妆品中,来自植物的酪氨酸酶抑制化合物用作抗澄清剂[GydF4y2Ba4GydF4y2Ba].酪氨酸酶是一种含铜的单加氧酶,广泛存在于自然界,包括植物、真菌和动物。它催化酪氨酸羟基化生成L-DOPA (l -3,4-二羟基苯丙氨酸),后者随后被氧化生成l -dopaquino。然后它们自动聚合形成黑色素[GydF4y2Ba5GydF4y2Ba].因此,酪氨酸酶的天然抑制剂被认为是治疗黑色素生成过剩引起的皮肤色素沉着的关键[GydF4y2Ba6GydF4y2Ba,GydF4y2Ba7GydF4y2Ba].GydF4y2Ba
随着代谢组学时代的到来,以质谱(MS)为基础的代谢物特征已经演变为一种熟练的方法来识别化学分类学、代谢途径和植物化学特征,补充基因组学和蛋白质组学的级联[GydF4y2Ba8GydF4y2Ba].代谢组学能够通过色谱分离、高分辨率MS和提高检测灵敏度,无偏、高通量筛选和表征生物样品提取物中的代谢物域[GydF4y2Ba9GydF4y2Ba,GydF4y2Ba10.GydF4y2Ba,GydF4y2Ba11.GydF4y2Ba].然而,由于影响生物表型的代谢谱的不同滴度,对所鉴定的代谢物的后续功能注释往往显得困难。因此,需要探索新的多平行方法来快速筛选和表征不同植物样品中的功能性代谢物[GydF4y2Ba12.GydF4y2Ba,GydF4y2Ba13.GydF4y2Ba].GydF4y2Ba
已经观察到,由于存在类似的生物合成途径和调节酶,同一科的植物通常合成类似类的化合物[GydF4y2Ba14.GydF4y2Ba].以前,鉴别代谢物,包括植物提取物中黄酮类化合物的含量,已被报道为不同的分类顺序。然而,植物不同部分(叶和茎)之间的空间代谢差异尚未被全面解构[GydF4y2Ba8GydF4y2Ba,GydF4y2Ba15.GydF4y2Ba].一般来说,植物不同部位的化学成分在很大程度上受遗传因素、营养状况和地理气候条件的影响[GydF4y2Ba16.GydF4y2Ba].此外,功能性代谢物的不同分布包括叶,茎和鲜花,需要在空间部件中除系统中描绘植物化学多样性[GydF4y2Ba17.GydF4y2Ba,GydF4y2Ba18.GydF4y2Ba,GydF4y2Ba19.GydF4y2Ba].GydF4y2Ba
本文以菊科、豆科和蔷薇科3个不同植物科的叶和茎为研究对象,提出了一种基于代谢组学和生物分析的多平行代谢组学分析方法。我们采用基于非目标质谱(MS)的代谢组学结合生化表型分析,对有助于不同植物物种间空间和系统发育化学多样性的具有显著区别的代谢物进行综合表征。GydF4y2Ba
结果GydF4y2Ba
跨空间组分(叶子和茎)和家族(Asteraceae,Fabaceae和Rosaceae)的代谢物分析GydF4y2Ba
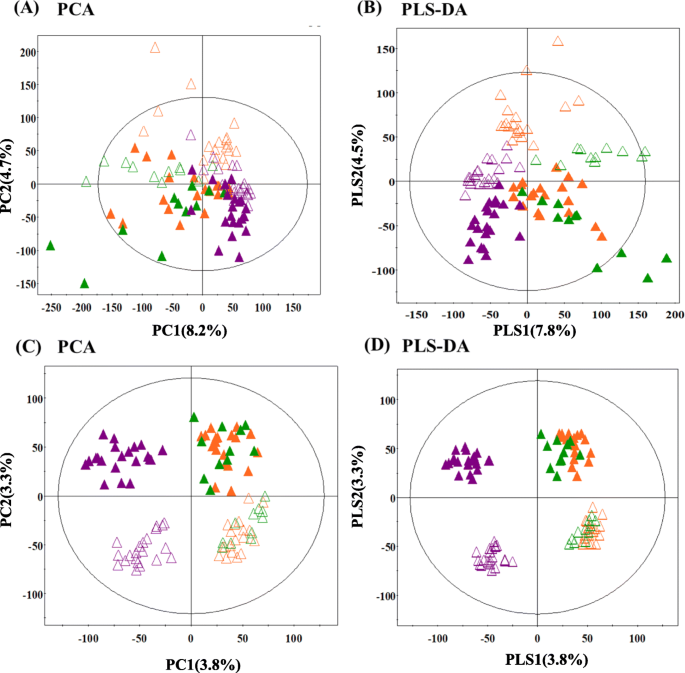
在此,我们研究了属于朝鲜半岛的三种不同家族(Asteraceae,Fabaceae和Rosaceae)的51种植物物种的空间组分上的2-D代谢物谱。使用GC-TOF-MS和UHPLC-Q-ORBITRAP-MS进行植物样品之间的微妙代谢视差,然后对相应数据集进行多变量统计分析。基于GC-TOF-MS数据的主成分分析(PCA)得分曲线显示为51个样本的聚类图案,根据PC 1(8.2%)和PC 2的相应植物家族分离成三个不同的组(4.7%),而它们的空间代谢差距沿PC 2是明显的(图。GydF4y2Ba1GydF4y2Baa).此外,基于UHPLC-Q-Orbitrap-MS数据集的主成分分析表明,在相应的植物科和植物部分,pc1(3.8%)和pc2 (3.3%;无花果。GydF4y2Ba1GydF4y2Ba分别c)。在预测(VIP) > 0.7或变量重要性上,统计选择了可能导致观测到的不同植物间化学分类差异的空间组分之间具有显著鉴别性的代谢物GydF4y2BaP.GydF4y2Ba< 0.05,基于PLS-DA模型(图。GydF4y2Ba1GydF4y2Ba共鉴定出64个代谢物,包括41个初级代谢物和23个次级代谢物,具有显著鉴别性。主要代谢物使用标准化合物进行鉴定,其光谱详细信息作为附加文件提供GydF4y2Ba1GydF4y2Ba:表S1。此外,基于其UV吸收,质量(M / Z),质量碎片模式和元素组成(附加文件,表征次级代谢物GydF4y2Ba2GydF4y2Ba:表S2)。我们通过公布的方法全面建立了这些化合物的推定标识[GydF4y2Ba20.GydF4y2Ba].使用上述参数表征的代谢物与在线数据库,标准和标准和标准相匹配GydF4y2Ba内部GydF4y2Ba最后利用已发表文献进行交叉验证。有趣的是,植物的初级代谢物在空间(叶和茎)组分中表现出明显的异质性,而次级代谢物在空间和跨科中表现出更大的多样性。GydF4y2Ba
在空间部件和家庭的植物样本中相对代谢物丰富GydF4y2Ba
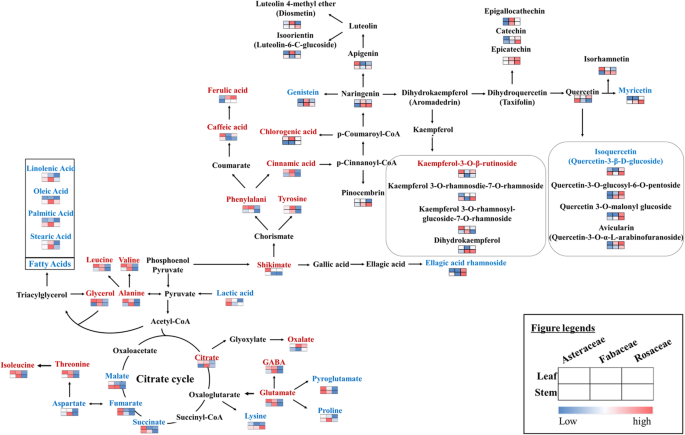
参与显着判别初级和次级代谢物的生物合成的代谢途径被映射,并指示了它们相应的植物样品中的相对丰度(图。GydF4y2Ba2GydF4y2Ba).考虑到菊科3个科的主要代谢物差异,菊科提取物中有机酸(咖啡酸、乳酸、琥珀酸、莽草酸和延胡索酸)含量较高。豆科植物提取物中含有丰富的氨基酸(苯丙氨酸、酪氨酸、GABA、丝氨酸、精氨酸、天冬氨酸)和脂肪酸(硬脂酸、油酸、棕榈酸、油酰胺),而蔷薇科植物提取物中含有较高水平的糖醇、山梨醇、阿鲁酸等代谢物。在次生代谢产物方面,三科菊科提取物中山奈酚葡萄糖苷和山奈酚-3- o -β-芦丁苷的相对丰度最高。豆科植物中染料木素、柚皮素和异荭草苷含量最高,蔷薇科植物中针叶苷VIII、异槲皮素、槲皮素-3- o -葡萄糖-6- o -戊糖苷、鞣花酸鼠李糖苷、皮诺乔苷、表儿茶素和儿茶素的相对含量最高。GydF4y2Ba
表示其相应的生物合成途径中具有明显判别代谢物的相对含量的示意图,跨越51种植物物种和植物空间部件。修改的途径由Kegg数据库(GydF4y2Bahttp://www.genome.jp/kegg/GydF4y2Ba).热线图表示用于三种植物家族(Asteraceae,Fabaceae和Rosaceae)的空间零件(叶子和茎)检测到判别代谢物的峰面积的平均值。叶子和干萃取物之间的判别代谢物分别以红色和蓝色字体表示。用于代谢物水平的热图的颜色代表了它们的平均折叠变化值GydF4y2Ba
显著鉴别代谢物的生物活性相关性GydF4y2Ba
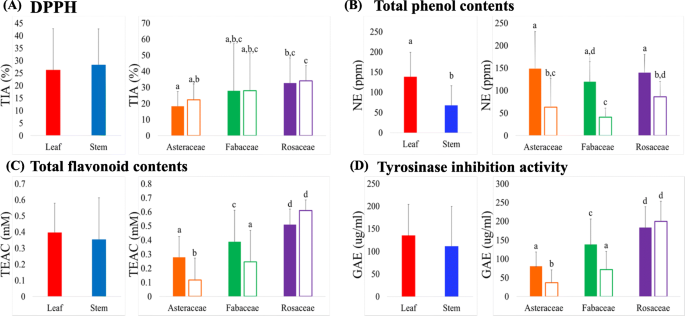
植物化学提取物的生物活性主要是由于次生代谢产物的不同组成,在植物物种中发挥着多种生态作用。这些化合物在不同系统发育类群和植物组分间的空间分布具有明显的判别性。本研究采用DPPH自由基清除、总酚含量、总黄酮含量和酪氨酸酶抑制等方法对51种植物的102份(叶和茎)样品进行了相关生物活性研究。GydF4y2Ba3.GydF4y2Ba).在植物家庭以及它们的空间组分(叶子和茎)上估计了51种(家族:Asteraceae,Fabaceae和Rosaceae)的生物活性测定结果。从最高到最低的顺序观察到平均DPPH抗氧化活性;蔷薇科茎> Rosaceae叶子> Fabaceae叶子> Asteraceae叶子> Fabaceae茎>菊科茎(图。GydF4y2Ba3.GydF4y2Ba一种)。类似地,按以下顺序观察平均酚含量;蔷薇科茎> Rosaceae叶子> Fabaceae叶子> Asteraceae叶子> Fabaceae茎>菊科茎(图。GydF4y2Ba3.GydF4y2Bab).总黄酮含量平均值的变化顺序为:菊科叶片>蔷薇科叶片>豆科叶片>蔷薇科茎>菊科茎>豆科茎(图2)。GydF4y2Ba3.GydF4y2Bad).总的来说,除蔷薇科植物外,叶提取物的抗氧化活性高于茎提取物。相反,茎样的平均酪氨酸酶抑制活性显著高于叶样,无论植物家族如何。GydF4y2Ba
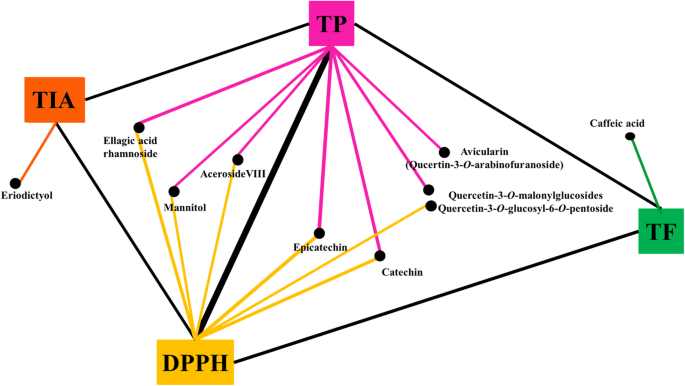
皮尔森的相关性分析初步确定了对观察到的植物提取物的生物活性有最大贡献的化合物。对Pearson相关值为> 0.3的变量进行相关网络评估(图。GydF4y2Ba4GydF4y2Ba).有趣的,Aceroside VIII,鞣果果酱,儿茶素,表人苷蛋白,甘氨酸,槲皮素-3-O-丙糖苷和槲皮素-3-O-葡糖基-6-O-戊苷与总酚含量(TPC)和槲皮素 - 3-O-葡糖基-6-O-五核苷酸酯DPPH抗氧化活性。GydF4y2Ba
讨论GydF4y2Ba
我们施加了未标准的代谢组合,与生物活性测定相结合,以评估属于三个主要植物家族的51种和其空间植物部件(叶子和茎)的51种物种中的二维(2D)代谢物多样性。不同植物部件的化学成分受多种因素的影响,包括遗传,代谢因素和地质气候条件[GydF4y2Ba14.GydF4y2Ba].以前,我们突出了质谱(MS)的代谢物的重要性,以识别各种属和家庭的不同植物样品的趋化性曲线[GydF4y2Ba8GydF4y2Ba].无目标代谢组学和多变量分析表明,不同系统发育和空间部分的植物样品的代谢物谱存在显著差异,而不考虑地理位置或样品采集时期的差异(2011-2015)。GydF4y2Ba
与Cornaceae和Rosaceae相比,Fabaceae物种中氨基酸的水平相对较高[GydF4y2Ba15.GydF4y2Ba].此外,Genistein,一种重要的异黄酮,从大豆和其他可食用的Fabaceae物种以及Naringenin和Isoorientin一起报道了很好的异黄酮[GydF4y2Ba21GydF4y2Ba].在一致中,我们观察到氨基酸和异黄酮在Fabaceae中丰富,而Kaempferol和槲皮素的衍生物分别在Asteraceae和Rosaceae家庭提取物中相对较高。据报道,Kaempferol糖苷是奥斯特科伊家族植物中的主要多酚化合物[GydF4y2Ba22GydF4y2Ba].而槲皮素苷是蔷薇科中典型的黄酮醇苷,与黄酮-3-醇(儿茶素和表儿茶素)和多酚化合物,包括鞣花酸[GydF4y2Ba23GydF4y2Ba].GydF4y2Ba
考虑到叶子和干燥组分之间代谢物的空间差异,分支链氨基酸(BCAA)(异亮氨酸)(异亮氨酸,亮氨酸,缬氨酸),芳族氨基酸(AAA)(苯丙氨酸,酪氨酸),苯丙醇(肉桂酸,甘露糖,在叶子中的叶子中相对较高,糖醇(木糖醇,肌醇,中赤藓糖醇)和甘油衍生物(甘油,甘油,甘油,甘油,甘油 - 甘油)相对较高。分支链氨基酸不能被动物合成;然而,植物可以合成这些氨基酸de novo,因此用作这些化合物的人饮食中的重要来源[GydF4y2Ba24GydF4y2Ba].在植物中,异亮氨酸,亮氨酸和缬氨酸在其生物合成途径中享受常见的BCAA水解酶。游离氨基酸的积累在植物应激耐受性中起重要作用,这些作用可以在某些非生物胁迫条件下充当渗透物[GydF4y2Ba25GydF4y2Ba].类似地,苯丙素是具有抗氧化功能的关键成分,可以改善高强度光胁迫对叶子造成的损伤[GydF4y2Ba26GydF4y2Ba].相反,与茎萃取液相比,叶片(油酸,硬脂酸,棕榈酸,棕榈酸和亚麻酸)和氨基酸(脯氨酸,赖氨酸和精氨酸)的水平相对较高。油酸和亚麻酸衍生物通过各种机制部分调节植物发育,种子定植和防御反应对病原体[GydF4y2Ba27GydF4y2Ba,GydF4y2Ba28GydF4y2Ba].值得注意的是,叶片中绿原酸和大部分黄酮(二氢戊戊醇,槲皮素,槲皮素衍生物和霉菌素衍生物)的相对丰富的叶片较高,而Kaempferol葡萄糖蛋白酶和吡塞蛋白酶在茎中更丰富。叶片中的黄酮类化合物较高可能归因于它们的局部生物合作以及它们在不同发展阶段的其他植物器官的活跃易位[GydF4y2Ba29GydF4y2Ba].GydF4y2Ba
一般而言,同一属群的抗氧化活性水平相近,但属内的种不同GydF4y2Ba阿尔纳斯GydF4y2Ba显示出显着不同的抗氧化水平。这些结果表明,属于同一属属的物种之间的化学组成的差异可以在不同的趋化学和相关的生物活化方面表达。在本研究中,多变量分析表明根据不同植物家族和空间部件的植物提取物的不同代谢物谱。因此,植物的趋化层级取决于它们的生物合成相关性,以合成相应的代谢物池[GydF4y2Ba30.GydF4y2Ba].GydF4y2Ba
我们观察到硫代钠VIII,儿茶素和槲皮素衍生物与DPPH抗氧化表型正相关,而ERIODICTYOL与酪氨酸酶抑制作用有关。根据最近的研究,Aceroside VIII是一种具有显着抗氧化活性的Acerogenin衍生物[GydF4y2Ba31GydF4y2Ba].鞣花酸在结构上是酚类抗氧化剂,其具有显着的自由基清除活性。它还促进了三种抗氧化酶的活性,即超氧化物歧化酶(SOD),过氧化氢酶(猫)和谷胱甘肽过氧化物酶(GPX),其在涉及自由基攻击的各种生理状态下改变了[GydF4y2Ba32GydF4y2Ba].甘露醇作为一种渗透保护剂和自由基清除剂的作用,影响抗氧化酶的活性,包括SOD、CAT、谷胱甘肽还原酶(GR)、过氧化物酶(POX)和抗坏血酸过氧化物酶(APX) [GydF4y2Ba33GydF4y2Ba].此前,Iacopini等人将儿茶素、表儿茶素和槲皮素描述为酚类化合物,可独立或协同表现出DPPH自由基活性[GydF4y2Ba34GydF4y2Ba].然而,在本研究中,花生二酚和咖啡酸分别与酪氨酸酶抑制和总黄酮含量测定有关。值得一提的是,穗二酚是一种可以抑制黑色素生成的类黄酮[GydF4y2Ba35GydF4y2Ba].GydF4y2Ba
结论GydF4y2Ba
本研究分析了51个植物样品的系统发育组和空间部分的化学计量特征,并将其非靶向代谢特征与相应的生物活性表型进行了关联。尽管不同的收获时间和地区有不同的影响,我们观察到不同家族的叶和茎提取物具有不同的代谢组学特征,分别具有更高的抗氧化活性和酪氨酸酶抑制活性。相关分析表明,植物提取物中多种代谢物或独立或协同影响抗氧化表型。考虑到这些微妙的机制,观察到的不同植物样品的化学多样性为了解可能影响表型变异的特殊代谢途径提供了线索。此外,研究报告的整体代谢产物库和相关的生物活性可以补充现有的植物代谢组学数据。GydF4y2Ba
方法GydF4y2Ba
化学药品和试剂GydF4y2Ba
hplc级的水、乙醇、甲醇和乙腈购自Fisher Scientific (Pittsburgh, PA, USA)。甲酸、n-甲基- n-(三甲基硅基)三氟乙酰胺(MSTFA)、盐酸甲氧胺、吡啶、2,2-二苯基-1-pricrylhydrazyl (DPPH)、氢氧化钠、二甘醇、福林- ciocalteu的酚试剂和碳酸钠均购自Sigma Aldrich (St. Louis, MO, USA)。GydF4y2Ba
植物材料GydF4y2Ba
我们为属于国家生物资源研究所(NIBR,仁川,韩国)的三种不同植物家族的51种不同的51种不同植物样本。使用混合器磨机将植物样品在阴影,合并并研磨成精细均相粉末中。关于本研究中使用的植物的信息列于表中GydF4y2Ba1GydF4y2Ba.GydF4y2Ba
样品提取制备GydF4y2Ba
用10 mL 80%甲醇在200 rpm下连续摇匀24小时后提取约1g样品粉。所得混合物在2800× ×温度下冷离心(4°C)GydF4y2BaGGydF4y2Ba(Hettich Zentrifugen, Universal 320),用0.2 μm注射器过滤上清。上清液在快速真空浓缩器(Modulspin 31, Biotron, Korea)下干燥,并在80%甲醇中以适当浓度重悬。该悬浊液通过UHPLC-Q-Orbitrap-MS检测次级代谢物。气相色谱-质谱联用(GC-TOF-MS)分析,提取液用盐酸甲氧胺(20 mg mL)肟化GydF4y2Ba−1GydF4y2Ba)在30°C吡啶处理90分钟。然后,用MSTFA在37°C下硅烷化30分钟。所有的质谱分析都进行了三个分析重复。GydF4y2Ba
生物活性测定GydF4y2Ba
DPPH实验GydF4y2Ba
抗氧化活性的测定采用DPPH法,采用维拉诺等人最初提出的方法[GydF4y2Ba36GydF4y2Ba],有一些修改。简而言之,将DPPH(200μmol)试剂溶解在乙醇中并在60-70℃下保持20分钟,直到通过分光光度计(Thermo电子,光谱遗传学6,所述溶液吸光度在515nm处达到1.0±0.02),麦迪逊,威廉,美国)。将所得溶液保持稳定于接下来的16小时并在4℃下储存。通过向植物样品提取物(20μL,1mg mL中,通过向植物样品提取物中加入180μl的DPPH溶液来进行测定GydF4y2Ba−1GydF4y2Ba), 37℃避光孵育20 min。在515 nm处测定反应吸光度。结果以Trolox等效活性浓度(mM)表示,并作为三个分析重复的平均值。GydF4y2Ba
总酚含量GydF4y2Ba
总酚含量测定分两步进行。首先,在80%甲醇中含有20μl植物样品提取物(1mg mlGydF4y2Ba−1GydF4y2Ba)和100 μL 0.2 N福林酚试剂在黑暗中孵育5min。然后加入80 μL 7.5%钠GydF4y2Ba2GydF4y2BaCO.GydF4y2Ba3.GydF4y2Ba加入反应混合物,孵育60 min。最后,在750 nm处测定吸光度。检测结果以活性的没食子酸当量(μg mL)表示GydF4y2Ba−1GydF4y2Ba),并作为三个分析重复的平均值。GydF4y2Ba
总黄酮含量(原浆1000ppm)GydF4y2Ba
对于总黄酮含量测定,反应混合物在80%甲醇中含有20μl植物样品提取物(1mg mlGydF4y2Ba−1GydF4y2Ba),20μl01nNaOH,160μl90%二乙二醇。将反应混合物温育60分钟,并将得到的吸光度记录在405nm。结果表达为Naringin当量活性浓度(μgmLGydF4y2Ba−1GydF4y2Ba).数据被呈现为三种分析重复的平均值。GydF4y2Ba
酪氨酸酶抑制活性GydF4y2Ba
使用以下方法测定蘑菇酪氨酸酶抑制活性。用125μl0.1M磷酸钠缓冲液(pH6.5)制备反应混合物,在80%甲醇中(10mg mL),5μl植物样品提取物(10mgGydF4y2Ba−1GydF4y2Ba)、30 μL蘑菇酪氨酸酶(1000单位mLGydF4y2Ba−1GydF4y2Ba)、40 μL 1.5 mM l -酪氨酸,加入96孔板。反应混合物在37°C孵育20分钟,在490 nm处测量吸光度。数据以三个分析重复的平均值表示。GydF4y2Ba
质谱分析GydF4y2Ba
GC-TOF-MS分析GydF4y2Ba
如Lee等人所述,使用Agilent 7890A气相色谱(GC)系统进行GC-TOF-MS分析,该系统配备Agilent 7693自动进样器,并与Pegasus飞行时间质谱(TOF-MS)检测器(Leco Corporation, St. Joseph, MI, USA)耦合。[GydF4y2Ba13.GydF4y2Ba].GydF4y2Ba
UHPLC-Q-Orbitrap-MS分析GydF4y2Ba
样品使用Q-Exactive Orbitrap MS分析,该MS配有加热电喷雾电离源(Thermo Fischer Scientific, CA, USA),由DIONEX UltiMate 3000 UHPLC系统(UltiMate 3000 RS泵,UltiMate 3000 RS柱室,UltiMate 3000 RS自动进样器;Dionex公司,CA, USA)。样品采用hypersil gold C18选择性色谱柱(内径1.9 μm, 50 × 2.1 mm;在25°C的柱箱温度下。流动相为0.1%甲酸水溶液(B)和乙腈(C),梯度流动的组成相同。20 min后,梯度由0%溶剂C逐渐增加到100%溶剂C,再维持2 min。流速为0.3 mL minGydF4y2Ba−1GydF4y2Ba进样量为10 μL。质谱采用电喷雾电离在m/z 100-1000范围内的负扫描和全扫描模式获得。工作参数为:喷针电压±3.3 kV;毛细管温度,320°C;探头加热器温度,300°C;叠环离子波导(s透镜)射频(RF)水平,60%;分辨率(半最大值全宽度;应用,35000年。GydF4y2Ba
超级性能液相色谱 - 四极轴 - 飞行时间质谱(UPLC-Q-TOF-MS)分析GydF4y2Ba
如Son等人所述,使用Waters Micromass Q-Tof Premier进行UPLC-Q-TOF-MS分析。[GydF4y2Ba15.GydF4y2Ba].流动相为0.1% v/v甲酸水溶液(A)和乙腈(B)。溶剂梯度体系为:B从5 v/v增加到100% (11 min),并保持在100% (12 min)。B在0.01 min内降至5%,并维持至13 min。进样量为5 μL,流速维持在0.3 mL minGydF4y2Ba−1GydF4y2Ba.GydF4y2Ba
数据处理和多变量分析GydF4y2Ba
使用Chromatof软件V4.44(LeCo Co.,CA,USA)将GC-TOF-MS数据文件转换为CDF格式。使用XCALIBUR(版本2.2版本2.2; Thermo Fischer Scientific,CA,USA)将LC-MS数据(* .RAW)转换为NetCDF(* .cdf)格式。转换后,使用Metalign软件包和SIMCA-P + 12.0(UMetrics,UMEA,瑞典)处理CDF格式数据,如所描述所述的主要成分分析(PCA)和偏最小二乘判别分析(PLS-DA)建模李等人。[GydF4y2Ba13.GydF4y2Ba].显著不同(GydF4y2BaP.GydF4y2Ba使用单向ANOVA对植物物的单向ANOVA进行植物物种统计方差的价值<0.05)代谢物在Statisca(版本7.0,Stasoft Inc.,Tulsa,OK,USA)上进行了测试。GydF4y2Ba
在抗氧化和酪氨酸酶抑制活性试验中,使用PASW Statistics 18 (SPSS Inc., Chicago, IL, USA)进行t检验来识别差异。通过Pearson相关系数计算代谢产物与生物活性(抗氧化活性和酪氨酸酶抑制活性)之间的两两相关关系。代谢产物和抗氧化生物活性之间的相关性通过MEV 4.8软件绘制的热图(多阵列查看器,GydF4y2Bahttp://www.tm4.org/GydF4y2Ba).GydF4y2Ba
可用性数据和材料GydF4y2Ba
支持本文结果的数据集包含在文章及其附加文件中。GydF4y2Ba
缩写GydF4y2Ba
- AAA级:GydF4y2Ba
-
芳香族氨基酸GydF4y2Ba
- APX型:GydF4y2Ba
-
抗坏血酸过氧化物酶GydF4y2Ba
- BCAA:GydF4y2Ba
-
支链氨基酸GydF4y2Ba
- 猫:GydF4y2Ba
-
过氧化氢酶GydF4y2Ba
- DPPH:GydF4y2Ba
-
2, 2-diphenyl-1-pricrylhydrazylGydF4y2Ba
- GC-TOF-MS:GydF4y2Ba
-
气相色谱飞行时间质谱法GydF4y2Ba
- GPX:GydF4y2Ba
-
谷胱甘肽过氧化物酶GydF4y2Ba
- gr:GydF4y2Ba
-
谷胱甘肽还原酶GydF4y2Ba
- 高效液相色谱法:GydF4y2Ba
-
高效液相色谱GydF4y2Ba
- 女士:GydF4y2Ba
-
质谱分析GydF4y2Ba
- MSTFA:GydF4y2Ba
-
盐酸甲氧基胺,N-甲基-N-(三甲基甲硅烷基)三氟乙酰胺GydF4y2Ba
- PCA:GydF4y2Ba
-
主要成分分析GydF4y2Ba
- PLS-DA:GydF4y2Ba
-
偏最小二乘判别分析GydF4y2Ba
- POX:GydF4y2Ba
-
过氧化物酶GydF4y2Ba
- 草皮:GydF4y2Ba
-
超氧化物歧化酶GydF4y2Ba
- UHPLC-Q-orbitrap-MS /女士:GydF4y2Ba
-
超高效液相色谱四极杆轨道阱离子阱串联质谱GydF4y2Ba
- VIP:GydF4y2Ba
-
投影中的可变重要性GydF4y2Ba
参考GydF4y2Ba
- 1。GydF4y2Ba
Ribeiro As,Estanqueiro M,Oliveira MB,Sousa Lobo JM。植物提取物在皮肤护理产品中的主要益处和适用性。化妆品。2015; 2:48-65。GydF4y2Ba
- 2.GydF4y2Ba
Javanmardi J, Stushnoff C, Locke E, Vivanco JM。伊朗乌桕抗氧化活性及总酚含量研究。食品化学。2003;83:547-50。GydF4y2Ba
- 3.GydF4y2Ba
用改良的铁还原/抗氧化能力测定法测定饲料中多酚的抗氧化活性农业食品化学。2000;48:3396-402。GydF4y2Ba
- 4.GydF4y2Ba
Kumar Ks,Yang Jc,Chu Fh,Chang ST,王Sy。Lucidone是一种新的黑色素抑制剂,来自Lindera Erythrocarpa Makino的果实。植物素描妇。2010; 24:1158-65。GydF4y2Ba
- 5.GydF4y2Ba
黄jh,李BM。植物提取物对酪氨酸酶、L-DOPA氧化和黑色素合成的抑制作用。中国环境卫生杂志a辑,2007;70:393-407。GydF4y2Ba
- 6.GydF4y2Ba
Chen Cy,Kuo Pl,Chen Yh,Huang Jc,Ho ML,Lin RJ等。酪氨酸酶的抑制,自由基清除,酸胞嘧梭提取物的抗杀菌剂和抗癌活性。J台宇宙科学工程。2010; 41:129-35。GydF4y2Ba
- 7.GydF4y2Ba
关键词:酪氨酸酶,n -亚硝基羟胺,合成生物组织医学化学2001;9:1233-40。GydF4y2Ba
- 8.GydF4y2Ba
李S,吴DG,李S, Kim GR, Lee JS, Son YK,等。62种乡土植物的化学分类学代谢物图谱及其与生物活性的相关性。分子。2015;20:19719-34。GydF4y2Ba
- 9.GydF4y2Ba
康D,儿子GH,Park HM,Kim J,Choi Jn,Kim Hy等。含有抗真菌活性的培养条件依赖性代谢物分析。真菌Biol。2013; 117:211-9。GydF4y2Ba
- 10。GydF4y2Ba
金俊,崔金珍,崔jh,查勇,Muthaiya MJ,李昌华。高脂饮食对发酵豆制品(清国酱)摄入对小鼠代谢参数的影响。营养食品学报2013;57:1886-91。GydF4y2Ba
- 11.GydF4y2Ba
基于质谱技术的芦荟(Aloe barbadensis Miller)代谢产物分析和抗氧化活性研究。中国农业科学。2012;60:11222-8。GydF4y2Ba
- 12.GydF4y2Ba
陈伟,龚玲,郭震,王伟,张辉,刘旭,余胜,熊磊,罗建军。一种新型的代谢产物大规模检测、鉴定和定量的集成方法:在水稻代谢组学研究中的应用。摩尔。2013;6:1769 - 80。GydF4y2Ba
- 13.GydF4y2Ba
李志刚,李志刚,李志刚。桦木科植物提取物中抗氧化成分的非靶向代谢组学研究。代谢物。2019;9:186。GydF4y2Ba
- 14.GydF4y2Ba
ntie kang F, Lifongo LL, Mbaze LMA, Ekwelle N, Owono LCO。喀麦隆药用植物:生物活性与民族植物学调查和化学分类。BMC Complement Altern Med. 2013;13:147。GydF4y2Ba
- 15.GydF4y2Ba
儿子Sy,Kim NK,Lee S,Singh D,Kim Gr,Lee Js等。代谢物指纹,途径分析以及属于康西科,Fabaceae和Rosaceae家族的植物物种的生物活性相关性。植物细胞代表2016; 35:917-31。GydF4y2Ba
- 16.GydF4y2Ba
Diasmi,Sousa MJ,Alves Rc,Ferreira Ic。探索植物组织培养,提高酚类化合物的生产:综述。ind crop prod。2016; 82:9-22。GydF4y2Ba
- 17.GydF4y2Ba
DelBañoMJ,Lorente J,Castillo J,Benavente-GarcíaO,DelRíoJA,OrtuñoA等。酚类脱萜,黄酮和玫瑰花酸分布在Rosmarinus Officinalis的叶片,花,茎和根部的发育过程中。抗氧化活性。JAgric Food Chem。2003; 51:4247-53。GydF4y2Ba
- 18.GydF4y2Ba
小茴香(Cuminum cyminum L.)不同部位精油、酚类成分及抗氧化活性研究。农业食品化学学报,2010;58:10410-8。GydF4y2Ba
- 19.GydF4y2Ba
Shahhoseini R,Hosseinin N,Ghorbanpour M.在伊朗种植的柠檬马鞭草(Lippia Citriodora的不同部分的基本油含量和组成。j ensent油熊植物。2014; 17:120-5。GydF4y2Ba
- 20。GydF4y2Ba
陈玉玲,陈爱玲,陈爱玲,等。基于质谱的代谢组学代谢产物鉴定使用多种类型的相关离子信息。肛门化学2015;87:2143-51。GydF4y2Ba
- 21。GydF4y2Ba
Spinola V, Llorent-Martinez EJ, Gouveia-Figueira S, Castilho PC。乌来草:从有害杂草到有价值的异黄酮和黄酮的来源。作物学报2016;90:9-27。GydF4y2Ba
- 22。GydF4y2Ba
Mejía-Giraldo JC, Winkler R, Gallardo C, Sánchez-Zapata AM, Puertas-Mejía MA。紫菀科天然遮光剂的光保护作用。Photochem Photobiol。2016;92:742-52。GydF4y2Ba
- 23。GydF4y2Ba
Määttä-Riihinen KR,Kamal-Eldin A,TörrönenAR。钙葡萄植物浆果酚类化合物及荷兰物种(家庭蔷薇科)鉴定及定量。JAgric Food Chem。2004; 52:6178-87。GydF4y2Ba
- 24。GydF4y2Ba
高等植物中支链氨基酸的代谢。杂志。2007;129:68 - 78。GydF4y2Ba
- 25.GydF4y2Ba
王志强,王志强,王志强,等。植物体内苏氨酸、蛋氨酸和异亮氨酸代谢的相互依赖关系:非生物胁迫下的积累和转录调控。氨基酸。2010;39:933-47。GydF4y2Ba
- 26.GydF4y2Ba
异戊二烯和苯丙素是植物抗氧化防御系统的重要组成部分。Environ Exp Bot. 2015; 119:54-62。GydF4y2Ba
- 27.GydF4y2Ba
升起rg。脂肪酸不饱和,动员和调节植物对应力的反应。Biotechnol Lett。2008; 30:967-77。GydF4y2Ba
- 28.GydF4y2Ba
Walters D,Raynor L,Mitchell A,Walker R,Walker K.四种脂肪酸对抗植物病原真菌的抗真菌。肌病理学。2004; 157:87-90。GydF4y2Ba
- 29.GydF4y2Ba
del Baño MJ, Lorente J, Castillo J, Benavente-García O, Marín MP, del Río JA,等。迷迭香叶、花、茎、根发育过程中类黄酮的分布。生物合成途径的假设。中国农业科学(英文版)。GydF4y2Ba
- 30。GydF4y2Ba
HATACEK F.次生代谢产物作为植物特征:当前的评估和未来的观点。CRIT Rev Plant Sci。2002; 21:273-322。GydF4y2Ba
- 31.GydF4y2Ba
李志刚,李志刚,李志刚。槭树科植物生物转化的系统代谢谱和生物活性分析。《公共科学图书馆•综合》。2018;13:e0198739。GydF4y2Ba
- 32。GydF4y2Ba
韩德,李米,金杰。鞣酸抗氧化和凋亡诱导活性。抗癌es。2006; 26:3601-6。GydF4y2Ba
- 33。GydF4y2Ba
Seckin B,Sekmen Ah,Türkani。外源甘露醇在盐胁迫下小麦根抗氧化酶活性上的增强作用。J工厂增长调节。2009; 28:12。GydF4y2Ba
- 34。GydF4y2Ba
IACOPINI P,Baldi M,Storchi P,Sebastiani L.儿茶素,EpicaTechin,槲皮素,芦丁和白藜芦醇在红葡萄中:含量,体外抗氧化活性和相互作用。J Food Compos Anal。2008; 21:589-98。GydF4y2Ba
- 35。GydF4y2Ba
徐峰,田志强,田志强,等。黑素瘤B16细胞中黑色素生成抑制剂的研究进展。生物器官医学化学2010;18:2337-45。GydF4y2Ba
- 36。GydF4y2Ba
Villano D, Fernández-Pachón MS, Moyá ML, Troncoso AM。多酚类化合物对DPPH自由基的清除能力。Talanta。2007;71:230-5。GydF4y2Ba
确认GydF4y2Ba
不适用。GydF4y2Ba
资金GydF4y2Ba
通过由农业部,粮食和农村事务部(MAFRA)资助的高附加值的食品技术发展计划,韩国规划和评估技术支持韩国规划和评估研究所支持。318027-04-3-HD030),由朝鲜共和国环境部(MOE)资助的国家生物资源(NIBR)的授予,并由Konkuk大学的WTU联合研究授予2017年。资助者在研究和收集,分析和解释的设计中没有作用,以及编写手稿。GydF4y2Ba
作者信息GydF4y2Ba
隶属关系GydF4y2Ba
贡献GydF4y2Ba
CHL和SaL为本研究提供了概念和设计。JSL和SaL提供了样本。SuL进行了大部分的实验工作和数据分析。SuL、D-GO、DS、JSL、SaL和CHL进行了数据解释。沙尔写了手稿。所有作者阅读并批准了最终的手稿。GydF4y2Ba
相应的作者GydF4y2Ba
道德声明GydF4y2Ba
伦理批准和同意参与GydF4y2Ba
不适用。GydF4y2Ba
同意出版物GydF4y2Ba
不适用。GydF4y2Ba
相互竞争的利益GydF4y2Ba
两位作者宣称他们没有相互竞争的利益。GydF4y2Ba
附加信息GydF4y2Ba
出版商的注意事项GydF4y2Ba
施普林格《自然》杂志对已出版的地图和机构附属机构的管辖权要求保持中立。GydF4y2Ba
补充信息GydF4y2Ba
额外的文件1。GydF4y2Ba
基于多因素分析的代谢物图谱初步鉴定了植物的主要代谢物。GydF4y2Ba
附加文件2。GydF4y2Ba
基于多变量代谢谱分析初步鉴定了植物次生代谢产物。GydF4y2Ba
权利和权限GydF4y2Ba
开放访问GydF4y2Ba本文根据创意公约署署署的条款分发了4.0国际许可证(GydF4y2Bahttp://creativecommons.org/licenses/by/4.0/GydF4y2Ba),它允许在任何媒体上无限制地使用、分发和复制,前提是你给予原作者和来源适当的荣誉,提供一个到知识共享许可协议的链接,并指出是否作出了更改。创作共用及公共领域专用豁免书(GydF4y2Bahttp://creativecommons.org/publicdomain/zero/1.0/GydF4y2Ba)适用于本条提供的数据,除非另有说明。GydF4y2Ba
关于这篇文章GydF4y2Ba
引用这篇文章GydF4y2Ba
Lee,S.,哦,DG。,Singh,D。GydF4y2Ba等等。GydF4y2Ba探索植物在空间(叶和茎)成分和系统发育组间的代谢组学多样性。GydF4y2BaBMC植物杂志GydF4y2Ba20.GydF4y2Ba39(2020)。https://doi.org/10.1186/s12870-019-2231-yGydF4y2Ba
收到了GydF4y2Ba:GydF4y2Ba
接受GydF4y2Ba:GydF4y2Ba
发表GydF4y2Ba:GydF4y2Ba
迪伊GydF4y2Ba:GydF4y2Bahttps://doi.org/10.1186/s12870-019-2231-yGydF4y2Ba
关键词GydF4y2Ba
- 植物零件GydF4y2Ba
- ChemodiversityGydF4y2Ba
- 抗氧化活性GydF4y2Ba
- 酪氨酸酶抑制活性GydF4y2Ba
- 代谢产物分析GydF4y2Ba