摘要
背景
叶霉病引起的枝孢属fulvum是影响全球生产番茄的严重威胁。CF基因与叶霉病抗性相关联,包括CF-16,能有效抵抗番茄叶霉。然而,Cf的分子机制-16-介导的耐药反应在很大程度上是未知的。
结果
我们进行了比较转录组分析c . fulvum防(简历。Ontario7816)和c . fulvum敏感(简历。结果表明,不同番茄品种的差异表达基因(DEGs)在接种后4 d和8 d进行了鉴定c . fulvum.Cf中多检出1588和939个DEGs-16与Moneymaker相比,番茄的dpi分别为4和8。此外,4-和8-dpi Cf共有1350个DEGs-16,表明存在共同的核心发展目标c . fulvum感染。Cf中上调的DEGs-16番茄主要与防御过程和植物激素信号转导有关,包括水杨酸(SA)和茉莉酸(JA)。此外,Cf中SA和JA水平显著升高-16番茄初期c . fulvum感染。与之前的研究相反,Cf中上调基因的数量-16Cf相比-10和Cf-12年番茄在早期显著升高c . fulvum感染。
结论
我们的研究结果为cf介导的耐药机制提供了新的见解c . fulvum,特别是Cf的独特特性-16番茄对这种真菌的反应。
背景
番茄(茄属植物lycopersicum)是世界上第二大最重要的园艺作物[1,2],是肉质果实发育和植物与病原互作的重要模式植物。叶霉病引起的枝孢属fulvum被认为是番茄中最具毁灭性的疾病之一.c . fulvum是一种非专性、非营养的致病真菌,侵染叶,有时侵染叶柄和茎[3.,4,5].叶霉在许多国家长期流行,造成严重的经济损失,特别是在高温高湿条件下[6].目前,最有效的方法是培养c . fulvum具有抗-抗性基因的番茄品种。
从共同进化的角度来看,植物识别病原体和对病原体作出反应的过程有几个阶段。在第一阶段,病原体相关分子模式(pathogen associated molecular patterns, PAMPs)被植物中的模式识别受体(pattern recognition receptor, PRRs)识别,诱导pamp触发免疫(PTI),防止病原体定植[7,8].在第二阶段,病原菌成功绕过PTI,分泌效应体进入植物细胞,随后发生效应体触发的敏感反应(ETS)。在第三阶段,植物逐渐进化产生NB-LRR(核苷酸结合位点和富亮氨酸重复序列)蛋白,直接或间接识别特定的病原体效应物,并诱导效应物触发免疫(ETI)。最后,病原体通过抑制或改变植物可能识别的效应子,产生植物nb - lrr无法识别的新效应子,成功感染植物并诱导ETS。同时,植物通过产生新的R基因来诱导ETI,这些R基因编码的蛋白质能够识别新的效应器[9,10,11].
在植物与病原体的相互作用方面,不同病原体具有无毒性(AVR的)相应于植物R基因的基因,并编码被效应蛋白识别的蛋白质[12].这些蛋白质在感染期间分泌到质外体空间,并诱导真菌和侵染的植物[之间的任一方或兼容不相容的相互作用13].不亲和互作(褪绿)导致植物抗病原菌时的超敏反应(HR);当病原体可以生长和分枝,导致受感染细胞坏死时,就会发生兼容相互作用[14,15,16,17].番茄,c . fulvum相互作用遵循一种典型的基因对基因的关系,并且产物c . fulvum抗性基因(Cf基因)特异地识别由番茄抗病基因编码的产物AVR的基因在c . fulvum,导致人力资源[18,19].自Cf发现以来,至少有24个Cf基因被报道-120世纪30年代的基因[20.,21],和这些基因已被引入到栽培番茄[22,23,24,25,26,27,28,29,30.].
转录组测序(RNA-Seq)强烈加快了对水稻等植物中宿主-病原体相互作用的研究[31)、玉米(32),黄瓜33,西瓜34]和草莓[35].Avr4 /Cf4 -和Avr9 /Cf9 -依赖防御基因表达已被cDNA-AFLP (cdna扩增片段长度多态性)分析证实[36].的Avr5基因已经通过结合生物信息学和基于rna - seq的转录组测序方法克隆[18].Cf-19 -, Cf-12 -和Cf-10 -介导的抗c . fulvum已通过cDNA-AFLP和RNA-Seq分析对番茄的特征进行了表征[37,38,39].然而,很少有转录组学研究检测Cf-16介导的耐药性。
在本研究中,除了进行转录组分析外,我们还测定了抗病和感病番茄品种对番茄红素的内源激素水平c . fulvum感染。我们的研究结果不仅有助于理解cf介导的耐药机制c . fulvum同时也为Cf的克隆提供了基础-16基因。
结果
微观的分析c . fulvum两个番茄品种的入侵
的c . fulvum在比照感染过程-16用光镜观察番茄或摇钱树叶片的变化。1).如图所示。1a和g, Cf之间无差异-16番茄和Moneymaker, dpi为0。我们的结果表明,分生孢子在2-3 dpi时萌发(图。1b),在Moneymaker和Cf中菌丝生长进入气孔-164 dpi的番茄叶片(图。1c).菌丝随后在8 dpi时通过Moneymaker叶片的气孔出现(图。1d),随着菌丝的生长和数量在10 dpi时持续增加,最后几个感染细胞在10 - 21 dpi时开始坏死(图2)。1e, f)。相比之下,Cf在8 dpi时出现少量HR区域-16番茄(图。1h),在10dpi时逐渐生长(图。1此外,菌丝生长仅限于坏死区域(图。1j)直到12至21 dpi之间,叶肉细胞和叶脉出现更多坏死病变(图。1k).显然,携带Cf的植物-16抗性基因在感染后表现出较强的HRc . fulvum,而敏感植物(即摇钱树)菌丝持续生长。基于这些观察结果,我们分别在4 dpi和8 dpi处理下收集样本,进行RNA-Seq和qRT-PCR(实时定量PCR)分析。
荷尔蒙反应分析c . fulvum感染
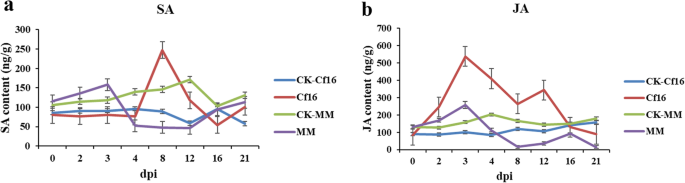
研究激素对c . fulvum采用高效液相色谱-串联质谱法(HPLC-MS/MS)测定SA和JA水平。如图所示。2a, Cf中SA含量迅速增加-16番茄接种后在4 ~ 8 dpi处达到高峰,在8 ~ 16 dpi处降至原来水平。摇钱树的SA含量在接种后逐渐升高,在0 ~ 3 dpi时高于对照组,在12 dpi时下降到最低水平。在Cf-16番茄接种后JA含量迅速增加,在0 ~ 3 dpi时达到峰值,在4 ~ 21 dpi时迅速下降;然而,JA水平普遍高于Cf对照组-16番茄和Moneymaker的感染后(从2到16 DPI)。在的Moneymaker中,JA含量感染后增加到最大值在3 dpi和然后逐渐下降(图2b).总体而言,在0 - 3dpi时,Moneymaker的SA和JA水平在感染后高于对照组。这些结果表明,SA和JA在侵染早期水平迅速上升,这些激素在调控植物对病原菌的反应和增强Cf的防御能力方面发挥着重要作用-16番茄感染c . fulvum.
RNA测序和转录本鉴定
为了获得Cf的转录谱-16番茄和Moneymaker紧随其后c . fulvum在感染后,我们在4和8 dpi处进行RNA-Seq分析,每个处理的每个时间点进行三个生物重复。在本研究中,使用bgiiseq -500平台为每个样本生成了平均约6.87 Gb的干净数据(附加文件9:图S1,附加文件1:表S1)。如附加文件所示1表S1中,98%以上的reads质量分数≥20%,91%以上的clean reads质量分数≥30%。筛选后得到64.15 ~ 7264万条clean reads,其中至少93.29%的reads被定位到番茄参考基因组,其中78.26%以上的reads被定位到唯一位置。最终获得18514个新转录本,其中已知基因的未知剪接事件12,790个,无任何已知特征的新编码转录本2047个,长链非编码rna的转录本3677个。
deg的响应c . fulvum
度从Cf-16番茄和Moneymaker的反应c . fulvum在4和8 dpi的基础上进行校正P-value≤0.001,记录日志2≥2倍变化。FPKM(每千碱基的外显子片段每百万片段的图谱)值为所有基因和fold的变化和调整Pdeg的-values显示在附加文件中2:表S2和附加文件3.:表S3。
对照组Cf间差异有3298和2464个差异-16番茄和Moneymaker的dpi分别为4和8。在感染后采集的样本中c . fulvum在4和8 dpi时,Cf之间分别鉴定出2242和3095个DEGs-16分别是番茄和Moneymaker1).与各自的对照组相比,Cf中鉴定出8526个DEGs-16在4dpi, Cf中为3711,Moneymaker中为6938,Moneymaker中为4213,下调2725-16番茄(包括1609个上调基因和2102个下调基因)在8 dpi, Moneymaker(包括757个上调基因和2015年下调基因)在8 dpi有2772个。
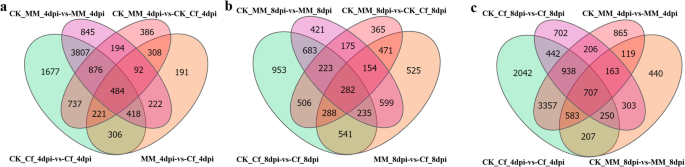
在两个品种中均检测到4 dpi的大量DEGs(见表)1);然而,我们也注意到两个品种(CK_MM_4dpi-vs-CK_Cf_4dpi和CK_MM_8dpi-vs-CK_Cf_8dpi)的对照组之间存在一些差异。另外,Moneymaker组和Cf组的对照和接种组共有707个DEGs-16番茄(图。3.c).因此,在每次比较中,有些deg可能与叶霉抗性无关。值得注意的是,306个deg之间存在重叠Cf-16番茄和Moneymaker仅在4dpi (CK_Cf_4dpi-vs-Cf_4dpi和MM_4dpi-vs-Cf_4dpi)(图。3.而541个DEGs只在8dpi (CK_Cf_8dpi-vs-Cf_8dpi和MM_8dpi-vs-Cf_8dpi)处重叠(图。3.b).基于这些更严格的标准,这些deg可能是抗叶霉最有希望的候选基因;因此,对这些DEGs进行了进一步的研究。
维恩图显示了不同接种后的差异c . fulvum。一个CK_Cf_4dpi-vs-Cf_4dpi、CK_MM_4dpi-vs-MM_4dpi、CK_MM_4dpi-vs-CK_Cf_4dpi和MM_4dpi-vs-Cf_4dpi之间的差异维恩图bCK_Cf_8dpi-vs-Cf_8dpi、CK_MM_8dpi-vs-MM_8dpi、CK_MM_8dpi-vs-CK_Cf_8dpi和mm_8dpi之间的差异维恩图。c间的CK_Cf_4dpi-VS-Cf_4dpi DEGS的维恩图,CK_MM_4dpi-VS-MM_4dpi,CK_Cf_8dpi-VS-Cf_8dpi和CK_MM_8dpi-VS-MM_8dpi比较。这些数字表明了不同的比较独特,共同度的视角。CK_Cf_4dpi,CK_Cf_8dpi,CK_MM_4dpi和CK_MM_8dpi:Cf-16番茄和Moneymaker的用水接种,并在4和8 dpi的收集。Cf_4dpi,Cf_8dpi,MM_4dpi和MM_8dpi:Cf-16番茄和摇钱树被接种c . fulvum分别在4和8 dpi处采集
GO和KEGG富集分析
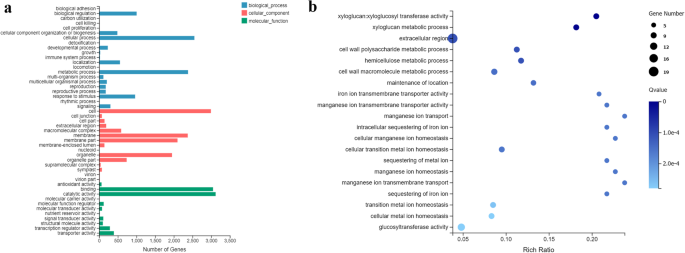
确定响应过程中所涉及的deg的功能c . fulvum,利用R软件中的Phyper函数进行GO (Gene Ontology)分类和KEGG (Kyoto Encyclopedia of Gene and Genomes)功能富集分析[40].Cf中检测到的DEGs-16在番茄中,重要的氧化石墨烯术语主要富集在生物过程类别中的“生物调节”、“细胞过程”、“代谢过程”和“对刺激的反应”,这些术语与抗病有关。在细胞成分本体论中,“细胞”、“膜”、“膜部”和“细胞器”是抗病番茄品种所特有的最丰富的类别。参与“结合”、“催化活性”、“转录调节活性”和“转运体活性”的基因在分子功能范畴中富集。值得注意的是,术语“结合”和“催化活性”在植物激素信号转导中起着重要作用。4一个)。
随后,前200名之间的温度Cf-16选择4dpi番茄及其对照组(CK_Cf_4dpi-vs-Cf_4dpi)进行氧化石墨烯富集分析,以更好地了解Cf-16-介导抗性反应c . fulvum.如图所示。4b,富集程度最高的氧化石墨烯术语是与细胞壁组织或其组分代谢有关的,包括“木葡聚糖:木葡聚糖转移酶活性”、“木葡聚糖代谢过程”、“细胞壁多糖代谢过程”和“半纤维素代谢过程”。细胞壁作为入侵的第一道屏障,是大多数病原体的第一道屏障[41,42].因此,与这些显著条款相关度的视角可以对战重要作用c . fulvum感染的CF-16番茄。
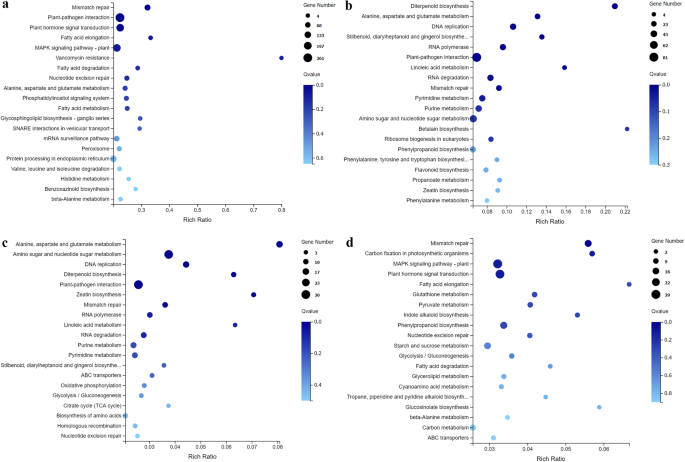
通过KEGG途径富集分析,探讨不相容相互作用的生物学途径。如图所示。5a,“植物激素信号转导”和“植物与病原互作”途径显著富集(图中每个点的颜色表示q值,显著富集的标准为q值≤0.01)。此外,“脂肪酸代谢”和“磷脂酰肌醇信号系统”也与Cf有关-16番茄的反应c . fulvum感染。此外,34个抗病基因(附加文件6:表S6)和32个deg(附加文件7表S7)在显著富集的KEGG通路“植物-病原互作”和“植物激素信号转导”中分别被鉴定。综上所述,“植物激素信号转导”和“植物与病原菌相互作用”可能是参与Cf的主要代谢途径-16-介导的抗性反应c . fulvum.
KEGG通路富集DEGs的散点图。富度比值是指特定途径中DEG数与背景数的比值。点的大小表示基因的数量,点的颜色表示q值的范围。一个在ck_cf_4dpi与cf_4dpi比较中,基于上调的deg的KEGG通路。b在MM_4dpi-vs-Cf_4dpi比较中,基于DEGs上调的KEGG通路。c基于306个deg的KEGG通路,这些deg只在CK_Cf_4dpi-vs-Cf_4dpi和MM_4dpi-vs-Cf_4dpi之间重叠,根据图中的维恩图。3.一个。dKEGG通路基于541个仅在CK_Cf_8dpi-vs-Cf_8dpi和MM_8dpi-vs-Cf_8dpi比较之间重叠的DEGs,根据图中的维恩图。3.b
Moneymaker和Cf之间也显著富集了参与“植物-病原体相互作用”途径的上调基因-16番茄(图。5b,额外的文件8:表S8)。因此,我们对Cf之间重叠的306和541个DEGs进行了KEGG通路分析-16番茄和Moneymaker分别只有4和8 dpi(图。3.有趣的是,“植物-病原体相互作用”和“植物激素信号转导”的通路显著富集(图2)。5c、d).表中列出了参与“植物-病原互作”的部分抗病基因和参与“植物激素信号转导”的6个激素相关基因2和表3.,分别。这些DEGs可能是抗叶霉最有希望的候选基因。这些结果再次表明,植物激素在细胞发育中起着关键作用Cf-16番茄的反应c . fulvum感染。
代谢和监管的途径分析
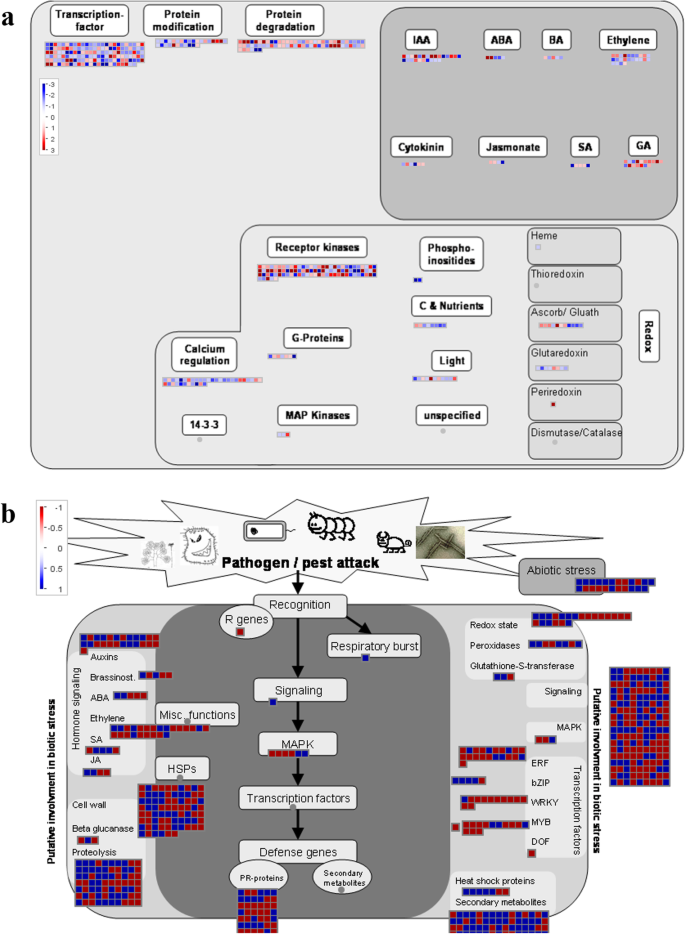
要获取引起的调控途径的概述c . fulvum,通过MapMan分析可视化。根据结果(图。6a),大多数deg在转录因子(包括受体激酶)中上调和功能富集。其他途径,包括“钙调节”和“光”,也会随之上调或下调c . fulvum感染。大多数deg与IAA(吲哚-3-乙酸)、ABA(脱落酸)和乙烯的上调相关激素有关。事实上,上调的基因分为R基因、MAPKs、PR蛋白、TFs和乙烯、ABA、SA、JA相关基因,进一步证明了这些途径在Cf中的重要性-16介导的抗性反应c . fulvum感染(图。6b,额外的文件4:表S4)。
基因共表达网络分析
加权基因共表达网络分析(WGCNA)是转录组学研究中常用的算法[43].根据基因表达水平之间的相关性,使用染色的基因树状图获得13个不同的模块(图2)。7a).其中,MEred和MEgreenyellow基因在Cf中高表达-16而MEpurple基因在两种Cf中均有较高的表达-16番茄和Moneymaker的4 dpi(图。7b).我们对这三个模块进行了KEGG分析。MEred模块富集了“植物-病原体相互作用”、“氧化磷酸化”和“苯丙氨酸、酪氨酸和色氨酸生物合成”相关通路;MEgreenyellow富集了“戊糖磷酸途径”、“类黄酮生物合成”、“苯丙素生物合成”和“植物激素信号转导”相关通路(补充文件)10:图S2)。值得注意的是,MEred模块中“植物-病原体相互作用”途径的一些DEGs也出现在了Additional file中8表S8 (MM_4dpi-vs-Cf_4dpi和CK_Cf_4dpi-vs-Cf_4dpi之间显著富集的KEGG通路“植物-病原体相互作用”中的DEGs)。因此,未来需要对这些抗病基因进行更深入的研究,以阐明它们在Cf中的作用-16-介导的抗性反应c . fulvum感染番茄。
qRT-PCR验证RNA-Seq数据
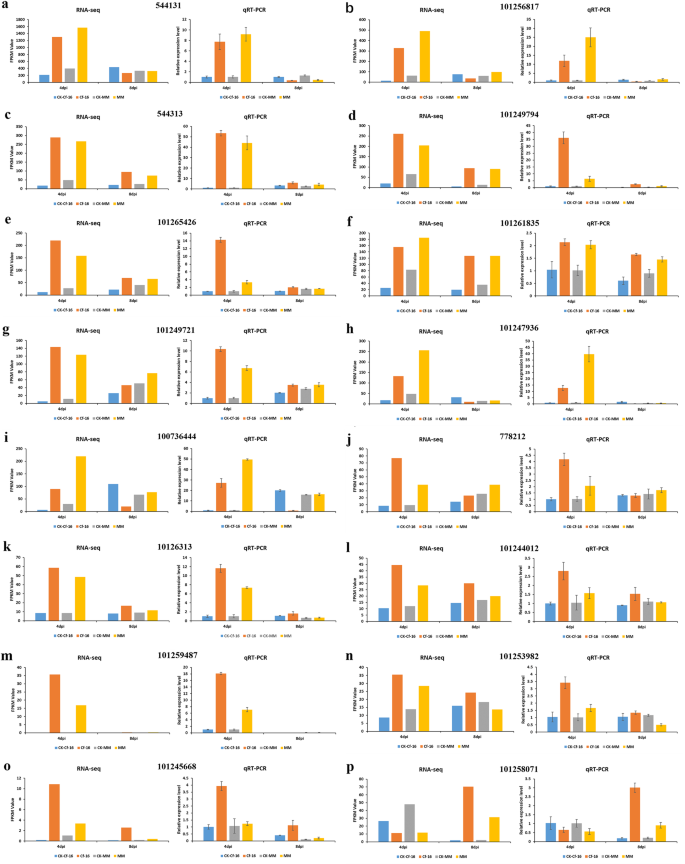
为了验证RNA-Seq数据,选择16个deg进行qRT-PCR;进行了3次生物重复。这16个基因是从显著富集的KEGG通路(如“植物激素信号转导”、“植物-病原互作”和“代谢通路”)中选择的。通过qRT-PCR得到的表达数据与RNA-Seq结果一致,说明转录组和qRT-PCR数据集的趋势相似(图)。8).之间的16度的视角,一个显著上调的基因与ID 101247936(图8h)预测在“植物激素信号转导”途径中编码一个茉莉酸- zim结构域蛋白,与茉莉酸对植物激素的响应平行c . fulvum感染(图。2b).同样,基因100,736,444的表达量(图。8ⅰ),其编码疾病抗性蛋白RPM1,增加的CF至少27倍-16番茄。此外,基因101,259,487的表达量(图。8m),编码过氧化物酶,基因101,256,817(图。8b),编码钙结合蛋白CML的,至少增加了11倍。
讨论
在这项研究中,我们描述了c . fulvum和Cf-16通过显微镜观察番茄或摇钱树。Cf组出现HR-16而在Moneymaker中,菌丝通过气孔出现,在8 dpi时菌丝数量继续增加并生长。1).抗性基因介导的系统防御反应在早期被激活c . fulvum感染。这一发现与之前对其他Cf基因的研究一致[37,38,39].通过比较转录组分析,我们证实了耐药反应c . fulvum在Cf-16番茄。为了应对c . fulvum在4 dpi时,两个番茄品种都发生了激烈的转录变化,尽管在各自的对照组之间也检测到一些DEGs(表1).由于这些结果表明,在每次比较中,许多deg可能与抗性无关,因此我们筛选了Cf中的抗性基因-16番茄更严格通过比较对照组的转录。显著GO术语主要包括在生物处理类别“生物调节”,“细胞过程”,“代谢过程”和“响应于刺激”,并且这些术语与疾病抗性相关。此外,KEGG富集分析表明,大多数度的视角被分为“植物激素信号转导”和“植物病原体相互作用”。在这个初步比较,CF中检测到多种上调的DEGS-16Cf相比-10和Cf-12年番茄生长初期c . fulvum感染(38,39].Cf的综合比较分析-19年,Cf-12年, Cf-10和Cf-16将为进一步探讨cf基因介导的抗c . fulvum感染。
植物有一系列的防御机制来应对病原体的攻击。PRRs是第一道防线[44,45];这些受体识别c . fulvum并激活抵抗反应[46].在我们的研究中,几丁质激发子受体激酶1 (CERK1;模式识别蛋白BGI_novel_G000519)的表达显著上调Cf-16番茄在4 dpi(附加文件6:表S6)。这一结果与Xue et al.(2017)对Cf的研究一致-12年.我们将研究CERK1表达的增加是否与几丁质信号的激活有关,并确定这种增加是否影响番茄-c . fulvum交互的过程。
识别感染后,Cf-16番茄迅速激活了一系列复杂的防御相关信号通路。Ca2+内流被认为在许多PAMP传感过程的早期下游反应中起着关键作用,导致局部和全身获得性耐药性[47,48].Ca2+钙依赖蛋白激酶(CDPKs)在植物对非生物胁迫和病原体的响应中发挥重要作用[49,50].在我们的研究中,CDPKs(101,249,495、101,055,527和101,255,379)在Cf中高水平表达-16番茄在感染的早期阶段(附加文件2:表S2)。这一结果与之前的研究结果一致,说明这些基因在Cf中起着至关重要的作用-16-介导抗性反应c . fulvum感染(51].此外,Ca2+导致一氧化氮(NO)的产生,进一步促进植物HR或自身免疫反应[52].有趣的是,我们的研究结果显示,在Cf中有11个CML基因在4dpi显著表达-16番茄与Moneymaker(图。9a).特别是在Cf中,id为543,942和101,245,711的基因表达上调约8倍-16番茄和摇钱树。基于这些结果,我们提出这些CML基因参与了Cf-16番茄防御反应c . fulvum.同样,Ranty(2016)证实,CML基因在植物响应至关重要的作用这两个非生物胁迫和病原体[53].FLS2识别flg22,随后激活下游信号通路,包括WRKY转录因子,以促进对细菌和真菌病原体和线虫的防御反应[54,55].在我们的研究中,12个WRKY基因在4 dpi特异上调,这在两个番茄品种中由DEGs的层次聚类显示(图2)。9b).其中,id为101,268,780、101,258,361、101,248,996和101,246,812的基因在Cf中上调了6倍以上-16番茄和摇钱树。这些结果表明,这些WRKY基因可能激活了一系列下游PR基因,从而在Cf的抗性反应中发挥了关键作用-16西红柿c . fulvum.我们的研究结果还表明,在Cf中PR-1基因(id分别为544,123和100,191,111)显著上调-16接种后的番茄(附加文件6:表S6)。总之,我们的结果表明,PRRs激活并促进下游CDPKs、cml和WRKY转录因子的表达;诱导活性氧的积累;并引起cystatin在细胞壁沉积,从而诱导Cf中的PTI-16番茄。
在与植物的长期进化相互作用中,一些病原体通过产生一些效应体成功地引起了ETS。同时,植物已经进化出R基因,能够识别这些效应子,并通过效应子与其相应的NB-LRR类受体之间高度特异性的相互作用发挥作用。水稻cc - pb -LRR蛋白Pi-to可以直接与Avr因子互作,其LRR结构域可以直接识别Avrpita的效应体Magnaporthe oryzae并诱导ETI [56].也有研究表明,NBS-LRR蛋白来源于拟南芥RPM1提供抵抗两.RPM1也参与HR的发病[16,57].与既往研究一致,我们的研究结果显示,Cf中编码RPM1的基因(101,261,141、100,736,444、109,120,689、101,253,178和BGI_novel_G001591)显著上调-16番茄在4 dpi(附加文件3.:表S3a)。这些基因可能在Cf的反应中起关键作用-16西红柿c . fulvum感染。更重要的是,id为109,120,689,101,253,178和BGI_novel_G001591的基因被鉴定为在Cf之间重叠的DEGs-16番茄和Moneymaker仅在4 dpi(表2).这些基因可能是抗叶霉最有希望的候选基因。
众所周知,植物激素在调节植物的防御反应中起重要作用[58,59,60].SA是植物与病原体相互作用的关键调控因子,可诱导HR和系统获得性抗性[61].在我们的研究中,在显著富集的KEGG通路“植物激素信号转导”中鉴定了32个DEGs(补充文件)7:表S7)。有趣的是,Cf中参与SA信号通路的TGA(104645,854, 101,250,172, 101,253,982)和PR-1(544123)显著上调-16番茄后c . fulvum接种。重要的是,在Cf中PR-1(544123)的表达显著升高-16在4和8 dpi时,番茄中PR-1对Cf的响应明显高于Moneymaker,提示PR-1可能在Cf的响应中起重要作用-16西红柿c . fulvum感染。这一结果与之前的研究一致[62].在Cf中,编码JA信号主要蛋白的JAZ基因(101、247、936和100、134,911)表达上调-16番茄4 dpi。这一发现与之前测定的感染后JA含量变化相一致。此外,在KEGG通路“植物激素信号转导”中,SAUR家族蛋白(BGI_novel_G000650, BGI_novel_G001679, 101,255,313, 101,257,321, 104,648,957和101,264,326)和PP2Cs(101,249,794和101,261,835)7:表S7)在本研究中进行了鉴定,这表明SAUR家族蛋白和PP2Cs也Cf的阻力发挥作用-16西红柿c . fulvum.特别是在Cf之间重叠的DEGs中发现了ID为101264326的SAUR家族蛋白-16番茄和Moneymaker的仅在8 dpi的(表3.).阐明该蛋白在Cf反应中的作用-16西红柿c . fulvum是必要的。总的来说,不同研究之间的差异表明所涉及的特定激素可能在不同的番茄中有不同的表现c . fulvum不同的条件下和在不同时间点的相互作用。因此,探索在Cf的激活SA和JA信令之间的串扰是很重要-16-介导的防御系统c . fulvum攻击并与其他Cf基因密切相互作用。
结论
本研究分析了首个Cf的全面转录组-16抗番茄的简历。和敏感番茄cv。并探讨了Cf与Cf之间的互动-16番茄和c . fulvum.发现了一些与抗病相关的DEGs,并预测它们与植物固有免疫应答(Ca)有关2+途径和植物激素信号转导途径。这些结果有助于我们理解Cf的潜在机制-16番茄打击c . fulvum并有助于Cf的精细定位和克隆-16基因的未来。
方法
植物材料和c . fulvum接种
两个番茄品种,抗性品种安大略7816,包括Cf-16基因(由中国农业科学院蔬菜花卉研究所提供)[23和易受影响的Moneymaker品种,这是缺乏的c . fulvum-resistance基因(由番茄遗传资源中心,LA2706友情提供),在本研究中使用。Tomato seeds were sown in pots filled with soil and grown under controlled conditions (16 h light, 25 °C and 95% ambient humidity) in a greenhouse at the Horticultural Station of Northeast Agricultural University (Harbin, China). At the four- to six-leaf stage, the abaxial leaf surfaces of 40 plants per line were sprayed with a suspension ofc . fulvum(比赛1.2.3.4)1 × 107每毫升孢子囊[63].各株系模拟处理后,在相同条件下喷洒灭菌水。所有植物保持在25°C, 95%的相对湿度。
显微观察的c . fulvum在Cf-16番茄
评估Cf的形成过程-16-介导的HR和耐药机制的关键时间点,参照Franco的方法进行乳酚台台蓝染色[64].抗性和敏感品系的叶片样品在0-21 dpi下收获,立即染色,在水合氯醛溶液(2.5 mg/ml)中澄清过夜[65],并使用奥林巴斯SZX10解剖显微镜(奥林巴斯,日本)进行检查。
内源JA和SA水平
分别采0、2、3、4、8、12、16和21 dpi接种组和对照组的叶片样品。采用Llugany et al.(2013)的改良方法从叶片中提取内源性SA和JA [66];使用AB SCIEX Triple TOF5600通过HPLC-MS/MS测量+质谱仪(SCIEX,USA)[67].
RNA提取、cDNA文库构建及测序
每组4和8 dpi提取总RNA,共24个样本,进行RNA- seq和qRT-PCR分析。使用RNAprep Pure Plant Kit (ThermoFisher, USA)从3株植物每组3个生物重复中提取总RNA,然后用于qRT-PCR [68,69];定量RNA样本用于cDNA文库的构建。由华大基因科技(中国深圳)进行文库准备和测序。使用NEBNext®Ultra™RNA Library Prep Kit for Illumina R (NEB, USA)生成文库,并使用bgiiseq -500测序,生成150 bp配对端reads。测序原始数据保存在NCBI Sequence Read Archive中,登录号为GSE133678 (https://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE133678).
测序、读图和识别
FASTQ格式的原始读取由基本调用生成,使用SOAPnuke v1.4.0进行统计分析,使用Trimmomatic v0.36进行过滤[70].通过删除带有适配器的读、包含超过5% poly-N(其中N表示未知碱基)的读和低质量读(质量值小于10,读中碱基总数的比例大于20%),可以获得干净的读。
干净的读数对齐到美国lycopersicum参考基因组序列(NCBI_GCF_000188115.3_SL2.50)使用HISATv2.1.0 [71].基因表达水平利用RSEMv1.2.8的FPKM方法[定量40].DEGs检测采用基于泊松分布的DEGseq方法[72].基因的调整P-value≤0.001,记录日志2≥2的Fold change定义为差异表达[73].
DEGs的功能注释和富集途径分析
利用R软件的Phyper函数对DEGs进行GO和KEGG通路富集分析;调整后p值≤0.01的GO项和KEGG通路被认为显著富集。使用MapMan工具将deg映射到各种代谢和调节途径(bins),以获得图形概述。每个箱子里的彩色盒子代表日志2转换后的折叠会改变deg的值。
基因共表达网络分析
使用WGCNA软件包v1.48进行基因共表达网络分析。根据基因表达水平之间的相关性,用颜色构建基因树状图,用于构建聚类树和划分模块。此外,利用WGCNA分析模块与样本之间的相关性。
存在分析
使用qRT-PCR验证16个deg,验证RNA-Seq获得的表达谱。qRT-PCR使用AceQ®qPCR SYBR®Green Master Mix (Vazyme, USA)和qTOWER进行3.G检测系统(德国耶拿分析公司)。每个样本重复3次,使用2-△△CT方法(74].的基因EFα1(R: 5 ' -CCACCAATCTTGTACACATCC-3 ', S: 5 ' - agaccaccaagtactactgcc -3 ')(附加文件5:表S5)。
数据和材料的可用性
与本研究有关的所有数据都包含在手稿的表格和图表中。测序原始数据保存在NCBI Sequence Read Archive中,登录号为GSE133678 (https://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE133678).
缩写
- 阿坝:
-
脱落酸
- cDNA-AFLP:
-
cdna扩增片段长度多态性
- CDPK:
-
Calcium-dependent蛋白激酶
- CERK1:
-
几丁质诱导受体激酶1
- CML:
-
钙结合蛋白
- CNCG:
-
植物环核苷酸门控离子通道
- 度:
-
差异表达基因
- dpi:
-
一天后接种
- 指数:
-
Effector-triggered免疫力
- ETS:
-
Effector-triggered敏感性反应
- FPKM:
-
每千碱基外显子的片段,每百万片段的图谱
- 走:
-
基因本体论
- HPLC-MS /女士:
-
高效液相色谱-串联质谱
- 人力资源:
-
过敏的反应
- IAA:
-
Indole-3-acetic酸
- 是:
-
茉莉酸
- JAZ:
-
Jasmonate-zim-domain基因
- KEGG:
-
京都基因和基因组百科全书
- NB-LRR:
-
核苷酸结合位点和富亮氨酸重复序列
- PAMP时:
-
其分子模式
- PRR:
-
模式识别受体
- PTI:
-
PAMP-triggered免疫力
- 存在:
-
实时定量聚合酶链反应
- 山:
-
水杨酸
- TF:
-
转录因子
- WGCNA:
-
加权基因共表达网络分析
参考文献
- 1.
等。基于形态性状的番茄基因型多样性分析对美国东部新鲜市场生产具有商业育种意义。作物科学,2016;10(8):1098。https://doi.org/10.21475/ajcs.2016.10.08.p7391.
- 2.
陈志强,陈志强,陈志强,等。番茄中Cf-4和Cf-19的生物信息学分析。中国农业科学。2017;87(10):1365-70。
- 3.
美国新真菌。Grevillea。1883;32。
- 4.
巴特勒。[J]。植物病理学研究。1949:672-8。
- 5.
等。番茄病害概要[M]。植物病理学杂志1991。https://doi.org/10.2307/3760420.
- 6.
托马BPHJ,范爱喜HP,CROUS PW等。叶霉病菌(同义词褐孢霉),高度专业化的植物病原体为我国植物病原真菌球腔菌科的功能研究的典范。分子植物病理学。2005; 6(4):379-93。https://doi.org/10.1111/j.1364-3703.2005.00292.x.
- 7.
奥苏贝尔调频。植物和动物的先天免疫信号通路是保守的吗?Nat Immunol。2005;6(10):973 - 9。https://doi.org/10.1038/ni1253.
- 8.
模式触发免疫(PTI)的信号传导机制。摩尔。2015;8(4):521 - 39。https://doi.org/10.1016/j.molp.2014.12.022.
- 9.
Dodds PN, Rathjen JP。植物免疫:植物-病原体相互作用的综合观点。[j] .地理科学进展,2010;https://doi.org/10.1038/nrg2812.
- 10.
Thomma BPHJ, Nurnberger T, Joosten MHAJ。基于模糊PTI-ETI二分法的聚类分析[J]。植物细胞。2011;23(1):4-15。https://doi.org/10.1105/tpc.110.082602.
- 11.
Jones JD, Dangl JL。植物的免疫系统。自然,2006;444(7117):323 - 9。https://doi.org/10.1038/nature05286.
- 12.
高湿度抑制Cf-4/ avr4和Cf-9/ avr9依赖性超敏细胞死亡和防御基因表达。足底。2005;222(6):947 - 56。https://doi.org/10.1007/s00425-005-0036-8.
- 13.
Nekrasov V, Ludwig AA, Jones JDG。CITRX硫氧还蛋白是在Cf-9/ avr9诱导的防御反应中连接Cf-9和ACIK1蛋白激酶的一种可能的接合蛋白。2月。2006;580(17):4236 - 41。https://doi.org/10.1016/j.febslet.2006.06.077.
- 14.
哈蒙德-科萨克KE,琼斯JD抗性基因依赖的植物防御反应。植物细胞。1996;8(10):1773。https://doi.org/10.1105/tpc.8.10.1773.
- 15.
Soylu EM, Soylu S, Mansfield JW。拟南芥与寄生蜂亲和不亲和互作过程中病原菌发育和寄主反应的超微结构特征植物病理学杂志。2004;65(2):67-78。https://doi.org/10.1016/j.pmpp.2004.12.002.
- 16.
Soylu S, Brown I, Mansfield JW。拟南芥受丁香假单胞菌菌株挑战后的细胞反应:从基础抗性到相容性。植物病理学杂志。2005;66(6):232-43。https://doi.org/10.1016/j.pmpp.2005.08.005.
- 17.
裴超,王洪,张建军,等。番茄遗传标记PI128216对细菌斑点小种T3超敏抗性候选基因的精细定位与分析acta photonica sinica, 2012; 40(3): 533-42。https://doi.org/10.1007/s00122-011-1726-1.
- 18.
陈志强,陈志强,陈志强,等。转录组测序揭示了番茄叶霉病原菌黄分枝杆菌Avr5的毒力基因。植物与微生物学报。2014;27(8):846-57。https://doi.org/10.1094/MPMI-02-14-0050-R.
- 19.
引用本文:王志强,王志强,王志强,等。野生番茄叶顶孢霉新质外体效应的特异性超敏反应相关识别。植物与微生物学报,2017;31(1):145-62。https://doi.org/10.1094/MPMI-05-17-0114-FI.
- 20.
朗格弗德。黄茎分枝杆菌的寄生及其抗性遗传。中国科学(d辑:地球科学)1937;15(3):108-28。https://doi.org/10.1139/cjr37c-008.
- 21.
Kanwar JS, Kerr EA, Harney PM。抗叶霉菌分枝杆菌Cf-1与Cf-11基因的连锁番茄热内鸡舍1980;30:20-1。
- 22.
Kerr EA, Bailey DL。黄分枝杆菌的抗性。从野生番茄种中获得。[J] .植物学报,1964;42(11):1541-54 .]https://doi.org/10.1139/b64-153.
- 23.
Kanwar JS, Kerr EA, Harney PM。抗番茄叶霉菌分枝杆菌(Cladosporium fulvum Cke)的Cf-12与Cf-24基因连锁。代表番茄,1980;30:22-3。
- 24.
MA Stevens, CM Rick。[M]。多德雷赫特:施普林格;1986.35 - 109页。https://doi.org/10.1007/978-94-009-3137-4_2.
- 25.
迪金森MJ,琼斯DA,琼斯JD。Cf-2/Cf-5与番茄抗Mi基因座密切相关。植物微生物学报。1993;6(3):341-7。https://doi.org/10.1094/MPMI-6-341.
- 26.
琼斯DA,迪金森MJ,巴林特-Kurti PJ等。两个复抗性基因座在番茄揭示的CF-2,CF-4,CF-5的经典和RFLP映射,和CF-9基因以叶霉病菌的阻力。Mol植物微生物相互作用。1993; 6:348。https://doi.org/10.1094/MPMI-6-348.
- 27.
Joosten MHAJ, De Wit PJGM。番茄-枝孢菌互作:研究植物-病原互作的通用实验系统。植物病理学杂志。1999;37(1):335-67。https://doi.org/10.1146/annurev.phyto.37.1.335.
- 28.
韩斯特拉JPW,托马斯CM,琼斯JDG等。Cf-4抗病基因在番茄种质资源中的分布。遗传。2000;85(3):266。https://doi.org/10.1046/j.1365-2540.2000.00754.x.
- 29.
赵涛,姜军,刘刚,等。基于高通量测序技术的番茄分枝杆菌抗黄腐基因Cf-19定位及候选基因筛选植物学报。2016;16(1):51。https://doi.org/10.1186/s12870-016-0737-0.
- 30.
刘刚,赵涛,尤旭,等。结合SNP/InDel-index和连锁分析对番茄Cf-10基因进行分子定位。植物学报。2019;19(1):15。https://doi.org/10.1186/s12870-018-1616-7.
- 31.
张志强,张志强,张志强,等。RNA-seq揭示了水稻有氧适应关键基因的参与。Sci众议员2019;9(1):5235。https://doi.org/10.1038/s41598-019-41703-2.
- 32.
刘胜,王旭,等。通过对比自交系的比较转录组和生理分析揭示玉米干旱响应的关键基因和途径。中华医学杂志。2019;20(6):1268。https://doi.org/10.3390/ijms20061268.
- 33.
隋旭,聂军,李旭,等。黄瓜的转录组和功能分析(Cucumis巨大成功(l)果实发育早期的韧皮部。工厂j . 2018, 96(5): 982 - 96。https://doi.org/10.1111/tpj.14084.
- 34.
等。bZIP基因家族成员在西瓜和甜瓜基因组中的比较鉴定、鉴定和表达分析。植物生长规律。2019;87(2):227-43。https://doi.org/10.1007/s10725-018-0465-6.
- 35.
胡鹏,李光国,赵旭,等。通过RNA-Seq转录组分析揭示了草莓果实发育和成熟特性相关的差异表达基因。同行j . 2018; 6: e4976。https://doi.org/10.7717/peerj.4976.
- 36.
朱建伟,徐亚平,张志新,等。Avr4/ cf -4和Avr9/ cf -9依赖的防御基因表达的转录谱分析。acta botanica sinica(云南植物学报). 2008;22(2):207 - 214。https://doi.org/10.1007/s10658-008-9294-1.
- 37.
赵涛,刘刚,李胜,等。cf -19介导的番茄对黄分枝杆菌感染抗性相关基因的差异表达植物病理学杂志。2015;89:8-15。https://doi.org/10.1016/j.pmpp.2014.11.003.
- 38.
薛道强,陈小龙,张辉,等。cf -12介导的番茄枝孢霉抗性反应的转录组分析。植物学报2017;7:2012。https://doi.org/10.3389/fpls.2016.02012.
- 39.
刘国栋,刘建军,张超,等。生理分析和RNA-seq分析揭示了cf -10介导的番茄叶枯病菌抗性的响应机制。acta botanica sinica(云南植物学报),2018;https://doi.org/10.1007/s11103-018-0706-0.
- 40.
李斌,杜威出版社。RSEM:从有或没有参考基因组的RNA-Seq数据中准确的转录本定量。BMC生物信息学。2011; 12(1): 323。https://doi.org/10.1186/1471-2105-12-323.
- 41.
陈志强,陈志强,陈志强,等。基质中的陌生人:植物细胞壁和病原易感性。植物科学进展,2008;13(11):610-7。https://doi.org/10.1016/j.tplants.2008.09.002.
- 42.
王志强,王志强,王志强,等。细胞壁来源的木葡聚糖是一种新的wet触发植物免疫葡萄和拟南芥。植物学报。2018;9:1725。https://doi.org/10.3389/fpls.2018.01725.
- 43.
张志强,张志强。基于遗传算法的基因共表达网络分析。中华医学杂志。2005;4(1)。https://doi.org/10.2202/1544-6115.1128.
- 44.
贝克男,赫德W,姆本格M等人。在细胞表面的插件和模式识别受体的超时。目前的意见植物生物学。2012; 15(4):367-74。https://doi.org/10.1016/j.pbi.2012.05.004.
- 45.
拟南芥类受体激酶形成一个与动物受体激酶相关的单系基因家族。中国科学院院刊。2001;98(19):10763-8。https://doi.org/10.1073/pnas.181141598.
- 46.
Gimenez的-Ibanez的S,汉恩DR,Ntoukakis V,等人。AvrPtoB针对LysM结构受体激酶CERK1促进对植物细菌的毒力。Curr Biol。2009; 19(5):423-9。https://doi.org/10.1016/j.cub.2009.01.054.
- 47.
刘志强,刘志强,刘志强,等。蛋白质和寡糖诱导子在烟草细胞核中诱导不同的钙信号。38细胞钙。2005;(6):527 - 38。https://doi.org/10.1016/j.ceca.2005.06.036.
- 48.
等。通过钙离子传感器蛋白激酶的差异先天免疫信号。大自然。2010;464(7287):-418。https://doi.org/10.1038/nature08794.
- 49.
小林等。钙依赖蛋白激酶通过马铃薯NADPH氧化酶调节活性氧的产生。植物细胞。2007;19(3):1065 - 80。https://doi.org/10.1105/tpc.106.048884.
- 50.
王志强,王志强,王志强,等。钙依赖型蛋白激酶/NADPH氧化酶激活通路的研究进展[J]。中国科学院院刊。2013;110(21):8744-9。https://doi.org/10.1073/pnas.122.1294110.
- 51.
胡Z,吕X,夏X等。在番茄钙依赖性蛋白激酶的基因组范围的鉴定和表达分析。前植物科学,469. 2016; 7。https://doi.org/10.3389/fpls.2016.00469.
- 52.
马伟,蔡永春,等。先天免疫信号:胞浆Ca2+升高与下游一氧化氮生成有关,通过钙调素或钙调素样蛋白的作用。植物杂志。2008;148(2):818 - 28。https://doi.org/10.1104/pp.108.125104.
- 53.
引用本文:王志强,王志强,王志强,等。钙传感器作为植物对生物和非生物胁迫反应的关键枢纽。植物学报2016;7:327。https://doi.org/10.3389/fpls.2016.00327.
- 54.
张志强,张志强,张志强,等。拟南芥先天免疫中的MAP激酶信号级联反应。大自然。2002;415(6875):977。https://doi.org/10.1038/415977a.
- 55.
赵伟林,王志强,王志强,等。植物丝裂原活化蛋白激酶信号级联。植物学报。2001;4(5):392-400。https://doi.org/10.1016/s1369 - 5266 (00) 00191 - 6.
- 56.
贾勇,杨志强,杨志强,等。抗性基因与无毒基因产物的直接互作是水稻抗稻瘟病的关键。EMBO j . 2000; 19(1): 4004 - 14所示。https://doi.org/10.1093/emboj/19.15.4004.
- 57.
马凯,霍尔特BF III,韦格,等。RIN4与丁香假单胞菌III型效应分子相互作用,是rpm1介导的拟南芥抗性所必需的。细胞。2002;108(6):743 - 54。https://doi.org/10.1016/s0092 - 8674 (02) 00661 - x.
- 58.
毛彦波,刘宇强,陈大勇,等。茉莉酸反应的衰减和防御代谢物的积累是植物抗虫性随年龄变化而变化的重要因素。Nat Commun。2017;8:13925。https://doi.org/10.1038/ncomms13925.
- 59.
等。水杨酸和茉莉酸途径被激活的空间不同的区域周围的感染部位在效应触发免疫拟南芥.植物学报。2017;59(1):8-16。https://doi.org/10.1093/pcp/pcx181.
- 60.
等。植物防御中激素信号网络的进化。Ann Rev Phytopathol. 2017; 55:401-25。https://doi.org/10.1146/annurev-phyto-080516-035544.
- 61.
Klessig DF, Choi HW, Dempsey DMA。系统性获得性抗性和水杨酸:过去、现在和未来。植物微生物学报,2018;31(9):871-88。https://doi.org/10.1094/MPMI-03-18-0067-CR.
- 62.
杨志强,杨志强,杨志强,等。对茄科基因组学参考系统——茄科小番茄(Solanum lycopersicum)的全长cdna进行了大规模分析。BMC基因组学。2010;11(1):210。https://doi.org/10.1186/1471-2164-11-210.
- 63.
王安华,徐旭,等。利用RAPD和SSR技术开发番茄抗黄分枝杆菌基因Cf-6的分子标记。HortScience。2007年,42(1):把。https://doi.org/10.21273/HORTSCI.42.1.11.
- 64.
张志强,张志强,张志强,等。壳聚糖和苯并噻二唑对大麦白粉病的化学诱导抗性。生物防除。2008;53(2):387 - 401。https://doi.org/10.1007/s10526-007-9091-3.
- 65.
黄志强,王志强,王志强,等。大豆赤霉病抗性和敏感大豆对赤霉病的生理和组织学响应。acta physica sinica (physica sinica), 2000;https://doi.org/10.1016/s0007 - 1536 (80) 80163 - x.
- 66.
王志强,王志强,王志强,等。真菌感染和/或机械胁迫下,镉超富集植物早熟禾的内源茉莉酸和水杨酸水平。植物学报2013;32(8):1243-9。https://doi.org/10.1007/s00299-013-1427-0.
- 67.
关键词:植物粗提物,高效液相色谱-质谱法,植物激素Nat Protoc。2010;5(6):986。https://doi.org/10.1038/nprot.2010.37.
- 68.
引用本文:施瑞德,缪立波,施瑞德等。RIN:一个RNA完整性号,用于为RNA测量值分配完整性值。中国生物医学工程学报。2006;7(1):3。https://doi.org/10.1186/1471-2199-7-3.
- 69.
方SM,胡BL,周QZ等。丝绸的对比分析腺国内和野生蚕之间的转录。BMC基因组学。2015; 16(1):60。https://doi.org/10.1186/s12864-015-1287-9.
- 70.
Cock PJA, Fields CJ, Goto N,等。sanger FASTQ文件格式的序列与质量分数,和Solexa/Illumina FASTQ变体。核酸学报2009;38(6):1767-71。https://doi.org/10.1093/nar/gkp1137.
- 71.
HISAT:低内存要求的快速拼接对准器。Nat方法。2015;12(4):357。https://doi.org/10.1038/nmeth.3317.
- 72.
王磊,冯震,王旭,等。DEGseq:一个用于从RNA-seq数据中识别差异表达基因的R包。生物信息学,2009,26(1):136 - 8。https://doi.org/10.1093/bioinformatics/btp612.
- 73.
控制错误发现率:一种实用而强大的多重检测方法。[J] .心理学报,1995;57(1):289-300 .]https://doi.org/10.1111/j.2517-6161.1995.tb02031.x.
- 74.
Livak KJ, Schmittgen TD。使用实时定量PCR和2−ΔΔCT方法分析相关基因表达数据。方法。2001;25(4):402 - 8。https://doi.org/10.1006/meth.2001.1262.
致谢
感谢黑龙江省大学低温生物学重点实验室、黑龙江省北部园艺作物遗传改良与栽培重点实验室。
资金
文章发表费用由中国农业研究系统(CARS-23-A-16)资助。本研究由国家重点研发计划项目(2017YFD0101900和2016YFD0101703)资助。本研究由黑龙江省自然科学基金项目(C2017024和LH2019C037)资助。农业部东北地区园艺作物生物学与遗传改良重点实验室开放项目。
作者信息
从属关系
贡献
XX构思并设计了该项目。DZ进行实验,分析RNA-Seq数据,撰写手稿。HY修改了原稿。YB和YS参与了实验的前期准备工作。YB, YS, TZ, HL, CD, JJ, JL, LX参与了数据讨论。所有作者都已阅读并批准了最终稿。
相应的作者
道德声明
伦理批准和同意参与
不适用。
同意出版
不适用。
相互竞争的利益
两位作者宣称他们没有相互竞争的利益。
额外的信息
出版商的注意
施普林格《自然》杂志对已出版的地图和机构附属机构的管辖权要求保持中立。
补充信息
附加文件1:表S1。
RNA-Seq数据总结。
附加文件2:表S2。
所有FPKM值的每个基因。
附加文件3:表S3。
所有的折叠变化P-值用于不同组之间的deg。
附加文件4:表S4。
摇钱树和CF之间度的视角-16番茄在4dpi,基于MapMan分析。
附加文件5:表S5。
qPCR的引物。
附加文件6:表S6。
在Cf中显著富集的KEGG通路“植物-病原体相互作用”中,上调了DEGs-16番茄和摇钱树4点。
附加文件7:表S7。
Cf中显著富集的KEGG通路“植物激素信号转导”中的DEGs上调-16番茄和摇钱树4点。
附加文件8:表S8。
MM_4dpi-vs-Cf_4dpi与CK_Cf_4dpi-vs-Cf_4dpi比较显著富集KEGG通路“植物-病原体相互作用”中常见的DEGs。
附加文件9:图S1。
对不同样本的原始读取进行分类。
附加文件10:图S2。
WGCNA中三个模块KEGG通路富集的散点图。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),它允许在任何媒体上无限制地使用、分发和复制,前提是你给予原作者和来源适当的荣誉,提供一个到知识共享许可协议的链接,并指出是否作出了更改。创作共用及公共领域专用豁免书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条提供的数据,除非另有说明。
关于这篇文章
引用这篇文章
张东,鲍勇,孙勇。et al。比较转录组分析揭示了Cf的反应机制-16介导的抗枝孢属fulvum感染番茄。BMC植物杂志20.33(2020)。https://doi.org/10.1186/s12870-020-2245-5
收到了:
接受:
发表:
关键字
- 比较转录组
- 枝孢属fulvum
- Cf-16番茄
- 分子机制