摘要
背景
土壤盐碱化和重金属毒性等非生物胁迫已对全球作物的可持续生产构成重大威胁。先前的研究表明,盐生植物应该能够忍受其他压力,包括重金属毒性。虽然HMAD(重金属相关结构域)被报道在拟南芥,很少有人知道Gossypium.
结果
共169个g .分子基因被鉴定属于HMAD基因家族的氨基酸数量在56 ~ 1011之间。另外,84、76和159HMAD每个基因都被鉴定出来G. arboreum, G. raimondii而且g .取得,分别。系统发育树分析结果表明HMAD基因家族分为5类,87个同源基因HMAD其中4个基因被鉴定出来Gossypium物种,比如基因Gh_D08G1950而且Gh_A08G2387的g .分子是Gorai.004G210800.1而且Cotton_A_25987基因g . raimondii就而且g . arboreum,分别。此外,在进化过程中丢失了15个基因。此外,保守序列分析发现,保守的催化中心含有一个阴离子结合盒(CXXC)。的HMAD基因家族在不同组织和发育阶段表达量不同g .分子不同的顺式元件用于非生物胁迫。
结论
目前的研究提供了重要的信息HMAD盐胁迫下的家族基因Gossypium基因组,这将有助于了解其在不同棉花品种中的假定功能。
背景
盐生植物是重金属污染土壤复垦的理想候选作物[1].一方面,重金属作为微量元素(如Fe、Cu、Zn、Co、Mn、Mo、Ni)是植物生长所必需的,过量则具有毒性;另一方面,其他重金属(Ag+、Cd2 +、铅2 +、汞2 +)即使是低剂量,也具有剧毒,因为它们不需要生命和生物作用[2].HMs污染不仅对植物本身有显著影响,而且对土壤微生物群落结构和功能也有显著影响[3.,4,5].重金属胁迫主要集中在钙信号、激素信号、MAPK(丝裂原活化蛋白激酶)信号和过氧化物信号网络中,侧重于离子解毒和转运[6,7].金属螯合剂主要是Phytochelatins (PCs)和Metallothioneins (MTs),尽管MTs通过清除ROS和隔离来保护植物免受重金属的侵害,即使在冷、热、盐、干旱等非生物胁迫下也具有多重抗性[8,9].与金属螯合剂相比,重金属离子转运家族的突出类群是p型atp酶和阳离子反转运物,如协会(重金属atp酶),美国广播公司(atp结合盒),NRAMP(天然抗性和巨噬细胞蛋白),提供(阳离子扩散促进剂),黄条纹(YSL)转运体,邮政编码(Zrt, irt样蛋白),CAX(阳离子交换器),CTR(铜转运体)、多效耐药转运体(PDR)、金属反应转录因子1 (MTF-1)等,分布于细胞的质膜或膜上[10,11,12,13,14].为协会依赖于p型atp酶和一组液泡体转运蛋白的超蓄能器、液泡区隔化和HMs离子长距离转运在重金属稳态中发挥重要作用[15,16,17].
p型ATPases分为5个亚家族,P1B ATPases(重金属泵),P2A和P2B ATPases (Ca2 +P3A atp酶(质膜H+泵)、P4 atp酶(磷脂转运atp酶)和P5(未指定特异性)亚家族[18,19,20.].至少有四个具有明显金属选择性的p1b - atp酶亚群:P1B-1(包括AtHMA5-8, OsHMA4-9), Cu2 +、P1B-2(包括AtHMA2-4)、Zn .2 +, P1B-3, Cu2 +, P1B-4(含AtHMA1), Co .2 +,它们有四个重要的催化结构域,分别是酶磷酸化(p -结构域)、核苷酸结合(n -结构域)和能量转导(a -结构域)和跨膜结构域[21,22,23].pib型atp酶lpg1024 (LpCopA)退伍军人表明Cu2 +离子进入路径包括两个离子结合位点:一个是短暂的Met148-Cys382位点,另一个是与Cys384、Asn689和Met717三角配位形成的膜内位点[24].选用一种纳米体(Nbs)对抗锌转运PIB-2-ATPases ZntA志贺氏杆菌sonnei(SsZntA),显著降低atp酶活性[25].多功能p1b -4- atp酶CzcP是耐金属模式生物抗钴、锌和镉系统的一部分会茁壮地生长,因为TM区域进化适应的灵活性可能为CzcP提供了运输Cd的能力2 +和锌2 +除Co外2 +[26].在结核分枝杆菌, P1B-4-ATPases在金属结合袋处的保守Cys的替换导致Fe的大量减少2 +而不是Co2 +绑定亲和性[27].在Sphaerobacter酸奶, P1B-1和p1b -3- atp酶亚家族均由Cu组成2 +转运蛋白(28].
协会(Heavy Metal ATPase)属于p1b型ATPases(也称为CPx-ATPases),负责离子解毒/转运[29,30.,31]和液泡区隔[32].在双突变体中很有趣协会不仅影响重金属的运输[33],还会影响植物的生长发育[33].而在水稻中,DNA甲基化状态因重金属胁迫而改变,并表现出跨代遗传[34].在高粱二色的,砷通过脱落酸信号通路刺激p1b - atp酶转运体的表达。此外,抗氧化蛋白1 (OsATX1)在水稻中作为Cu伴侣,与P1B-ATPases相互作用HMA4,HMA5,HMA6,HMA9,从而导致Cu在不同水稻组织中的转运和分布,以维持Cu在不同水稻组织中的稳态[35].在半盐生植物模型中m . crystallinum,HMA4(重金属atp酶4)和IRT2(铁调节蛋白2)在cd处理和nacl处理下的表达量显著高于对照,且影响IRT2表达累积[36].此外,盐度胁迫与HMs毒性在一定程度上有重叠,因为几个综合的机械和化学信号负责与胁迫相关的响应[37].例如,叶绿体和叶绿素含量可以测量盐胁迫[38],亦会影响重金属的转运[39,40].甚至黄酮醇也表现出缓解铅毒害作用和提高植物抵抗力的能力,因为它激活了抗氧化过程[41].
重金属胁迫与盐胁迫作为植物指标有许多相似之处,如光合性能和气孔行为[42],光合色素[43],脯氨酸[44,45]和过氧化物酶[43].ROS(活性氧)信号与抗氧化系统是非生物胁迫之间的串扰,盐胁迫和重金属胁迫也是如此[46,47,48,49,50],其中有关过氧化物酶和GSH-AsA系统的基因不仅能提高耐盐性,还能提高重金属耐受性[51,52,53,54].甚至在硫代谢中与谷胱甘肽相关的基因也能增强耐盐性和耐重金属性[55,56,57,58].此外,激素还能缓解盐胁迫和重金属胁迫,如IAA(吲哚-3-乙酸)[59,60],表油菜素内酯[61,62]、褪黑素[63,64],乙烯相关基因[65,66].而水杨酸[67,68,69],不[70,71,72],硅[73,74]和生物炭[75,76也能增加对盐和重金属压力的抵抗力。
除了与抗氧化系统相关的基因外,一些与耐盐性有关的基因提高了对重金属胁迫的抵抗力。例如,一种新的盐过敏2 (SOS2)相互作用蛋白SIP1 (SOS2相互作用蛋白1)[77],泛素特异性蛋白酶(ZmUBP15, ZmUBP16和ZmUBP19) [78],一种ABA生物发生抑制剂氟脲酮(FLUN) [79,80],胚胎发生后期丰富(LEA)或相关蛋白[81,82]、水通道蛋白(AQP) [83,84],质膜+atp酶(85,86]、热休克蛋白[87,88],苎麻bZIP转录因子BnbZIP2 [89].一些对重金属耐受性有反应的基因也增强了对盐胁迫的抗性,如植物螯合酶AtPCS2 [90], OsMT-3a(类金属硫蛋白3型)[91].此外,一些未报道的盐和重金属胁迫基因也可以提高盐和重金属耐受性,例如致病相关蛋白[92,93,94], atp结合盒(ABC)转运体AtABCG36/AtPDR8 [95,96,97], CBS结构域含蛋白OsCBSX4 [98], OsMIZ1 (MIZU-KUSSEI1) [99], OsSMP1(应激膜蛋白)[One hundred.].
盐与重金属的关系需要进一步的研究来证明NaCl和CuSO的联合应用4对小麦品种有显著不利影响[101].,while in cucumber (Cucumis巨大成功L.),盐度降低了Zn的吸收,增加了其他重金属(Cd、Cu、Ni、Pb)的吸收[102].此外,氯化钠对重金属毒性有拮抗作用,特别是对镉的拮抗作用2 +[103].在Spirodela polyrrhiza(柠檬科),高盐度会抑制镉(Cd)和镍(Ni)的积累[104].20 mg kg-1的Ni可缓解盐胁迫,促进小麦生长[105].此外,Cd抑制了根系对Cu的吸收[106],而镉对植物的毒性比铜更大[107].迄今为止,关于微生物耐盐和耐重金属的研究最多,其中一些微生物可以缓解植物的重金属和盐胁迫[108,109,110,111].此外,盐生植物[112]和半盐生植物[36]已知与盐和重金属有关。此外,茄子耐盐、耐旱品种对铅的耐受性较高[113].在柳树种类中,美国linearistipularis耐盐性比美国matsudana,在重金属植物提取中起重要作用[106,114].
棉(Gossypiuml.),是一种中等耐盐经济作物,是盐碱地土壤复垦的先驱作物[115,116].棉花是一种重要的纤维作物,为纺织业提供天然纤维[117].在此之前,在鉴别方面已经取得了很大的进展HMAD(重金属相关结构域)基因[118,119,120].然而,在其鉴定、功能表征、保守结构域分析和表达谱等方面尚未见详细的研究报道HMAD棉花盐胁迫下的基因。已公开的棉花基因组序列数据及CottonGen (https://www.cottongen.org/)使我们能够全面地识别和分析HMAD棉花的基因家族[117].在本研究中,我们对HMAD基因在g .分子,g .取得,g . raimondii就而且g . arboreum的染色体分布、共向分析、基因结构和保守基序分析,以及Ka/Ks值和表达谱。此外,预测的调控机制为111个HMAD基因可能受到盐胁迫的调控。本研究将为探索其具体功能提供基本信息HMAD盐胁迫下棉花的基因家族。
结果
全基因组鉴定和系统发育分析
我们使用隐马尔可夫模型(HMM)的配置文件HMAD域(PF00403)http://www.pfam.sanger.ac.uk/)数据库作为查询来搜索HMAD成员g .分子,g . arboreum,g . raimondii就而且g .取得由Hmmer软件默认参数。共有169个蛋白质被鉴定属于HMAD基因家族g .分子氨基酸的数量在56 - 1011之间1).此外,我们确定了84、76和159HMAD每种蛋白质g . raimondii就,g . arboreum而且g .取得,(表S .1).
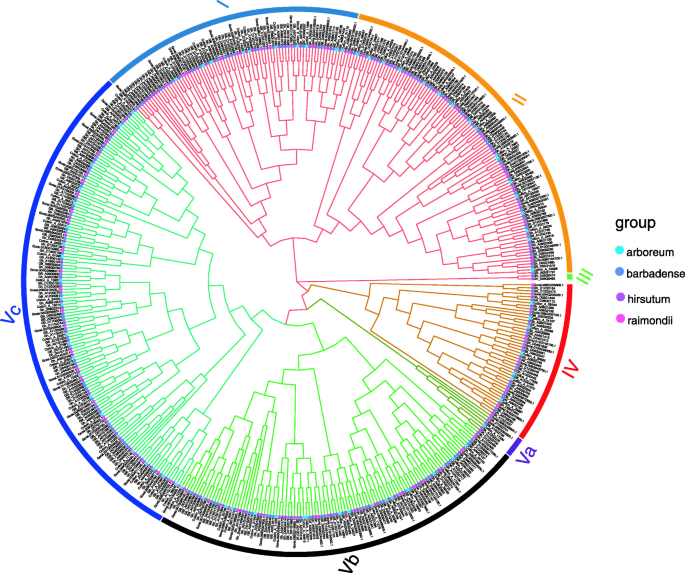
为了探索进化的关系HMAD基因家族,利用全长构建无根系统发育树HMAD蛋白质序列g . arboreum,G. barbadense, G. raimondii,g .分子(无花果。1).的HMAD四种蛋白质GossypiumP1B-ATPases被分为5个类群(I、II、III、IV、Va、Vb、Vc)HMA5-8IV组(表S3.).此外,87位骨科医生HMAD基因(表2)在4个Gossypium种(I占18.39%,II占18.39%,III占1.15%,IV占10.34%,Va占1.15%,Vb占20.69%,Vc占29.89%)(图;1),例如基因Gh_D08G1950而且Gh_A08G2387的g .分子是Gorai.004G210800.1而且Cotton_A_25987基因g . raimondii就而且g . arboreum,分别。
染色体分布及共线分析
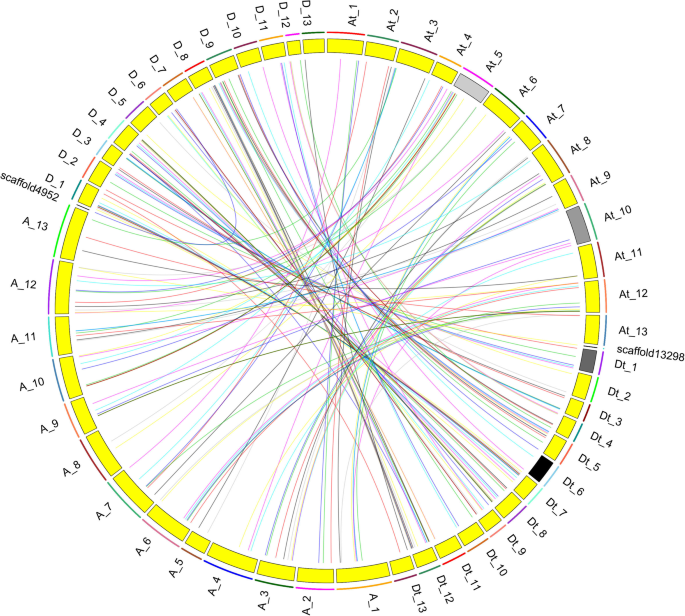
物理映射169G. hirsutum HMAD基因显示79和77HMAD基因分别分布在A和D亚基因组的26条染色体上(图2)。2),其中13个基因定位于支架。此外,在a亚基因组和D亚基因组的第12号副同源染色体上最多有17个和16个基因。此外,根据介入基因少于5个的标准,有9对和2个基因簇被标记为串联复制。在这些串联复制基因中,有5对和2簇属于Vb类群Gh_D05G1684-Gh_D05G1685而且Gh_A05G1510-Gh_A05G1511对,属于第三组。为了研究A亚基因组和D亚基因组的直系同源位点之间的关系,我们还进行了同向性分析。72和73HMAD基因不均匀地分布在13条染色体上g . arboreum而且g . raimondii就,分别。在g . arboreum,每条染色体包含2-11个HMAD成员。12号染色体包含11个HMAD基因方面,5号染色体和8号染色体有两个HMAD基因,分别。一个基因g . arboreum在染色体12上对应Gh_Sca013298G01在scaffold13298中(图;3.).在g . raimondii就,每条染色体的基因数在1 ~ 15之间HMAD成员。8号染色体最多含有15个HMAD基因,而染色体13只有一个HMAD基因。否则,一个基因的g . raimondii就在染色体6上对应Gh_Sca004952G01在scaffold4952中(图;3.).同步性分析结果表明,大部分的HMADA亚基因组和D亚基因组的基因位点分别高度保守。3.), 15个基因在进化过程中丢失,其中4个在A基因组(Cotton_A_04626,Cotton_A_25931,Cotton_A_00150,Cotton_A_35231), 11个位于D基因组(Gorai.001G250300.1,Gorai.005G218500.1,Gorai.005G220100.1,Gorai.007G134300.1,Gorai.007G295300.1,Gorai.008G005700.1,Gorai.009G162900.1,Gorai.009G199900.1,Gorai.009G414800.1,Gorai.012G027800.1,Gorai.008G245900.1).我们考察了正交的共线关系HMAD基因之间的g .取得而且g .分子(无花果。2).共有161对基因g .取得而且g .分子.在g .取得, 154个基因(除了GB_A01G1916,GB_A03G2039,GB_A04G0061,GB_A12G2848,GB_D05G3226,GB_D07G1125,GB_D12G2855之间的对应关系HMAD基因家族分别来自a亚基因组、d亚基因组之间g .取得而且G分子(无花果。2),以及5个基因(GB_A09G0824,GB_D05G1602,GB_D05G1968,GB_D07G0037,GB_D12G0056的对应关系HMAD基因家族g .分子.来g .分子, 153个基因(除了Gh_A03G1525,Gh_A03G2159,Gh_A05G1511,Gh_A10G2291,Gh_D08G2126,Gh_D12G2433,Gh_A08G0952与三个对应关系)之间显示了对应关系HMAD基因家族分别来自a亚基因组、d亚基因组之间g .分子而且g .取得(无花果。2),以及16个基因(Gh_A04G0031,Gh_A05G1510,Gh_A06G1378,Gh_A07G1489,Gh_A07G2000,Gh_A09G0465,Gh_A11G1104,Gh_A12G1537,Gh_D05G1684,Gh_D07G0041,Gh_D07G1640,Gh_D08G0132,Gh_D09G0474,Gh_D10G0078,Gh_D12G0431,Gh_D12G2254的对应关系HMAD基因家族g .取得.我们还发现HMAD基因位于A02和A03染色体上,其对应的同源体位于D03和D02染色体上2),分别。这些结果与之前的研究一致[121],这可能是由于棉花多倍体形成异体四倍体之前,染色体在Chr02和Chr03之间发生了易位[121].
基因结构及保守基序分析
基因结构是重要的,以确定其作用,显示之间的系统发育关系HMAD基因。用MEGA生成了一个NJ树HMAD蛋白质序列g .分子基因结构测定(图;4).如图所示。4,HMAD基因g .分子分为5个亚分支(组I、组II、组III、组IV、组Va和组Vb),其中组I包含13个基因,组II到组Va和组Vb分别包含66个、29个、14个、22个和25个基因。此外,对基因结构的分析表明,基因结构中的内含子在不同的基因中变化特别大HMAD基因家族,包括5个基因(Gh_D01G1640,Gh_Sca011408G01,Gh_A05G3385第一组,Gh_D08G1263而且Gh_A08G0990(Vb组),1内含子基因35个,2内含子基因79个,3内含子基因23个,4内含子基因17个,1个基因(Gh_A05G0564属于p1b - atp酶HMA5)含有7个内含子,3个基因(Gh_D05G0693属于p1b - atp酶HMA5,Gh_A12G0443属于p1b - atp酶HMA7,Gh_D12G0446属于p1b - atp酶HMA7)含有8个内含子,1个基因(Gh_D07G0041)含有15个内含子,3个基因(Gh_D06G0881属于p1b - atp酶HMA8,Gh_A06G0745属于p1b - atp酶HMA8而且Gh_A03G1525属于p1b - atp酶HMA6),有16个内含子。Gh_D06G0881而且Gh_A06G0745被划分为群集I,在四个之间Gossypium物种(图。1),并在g .分子(无花果。4).Gh_A03G1525被分成了第1组在4个人之间Gossypium物种(图。1),而在g .分子(无花果。4).Gh_A12G0443,Gh_D12G0446,Gh_D05G0693,Gh_A05G0564被划分为群集I,在四个之间Gossypium物种(图。1),而在g .分子(无花果。4).虽然用于生成该系统发生树的基因数量与图中所示的系统发生树不同。1,亚支内的基因成员基本相同。
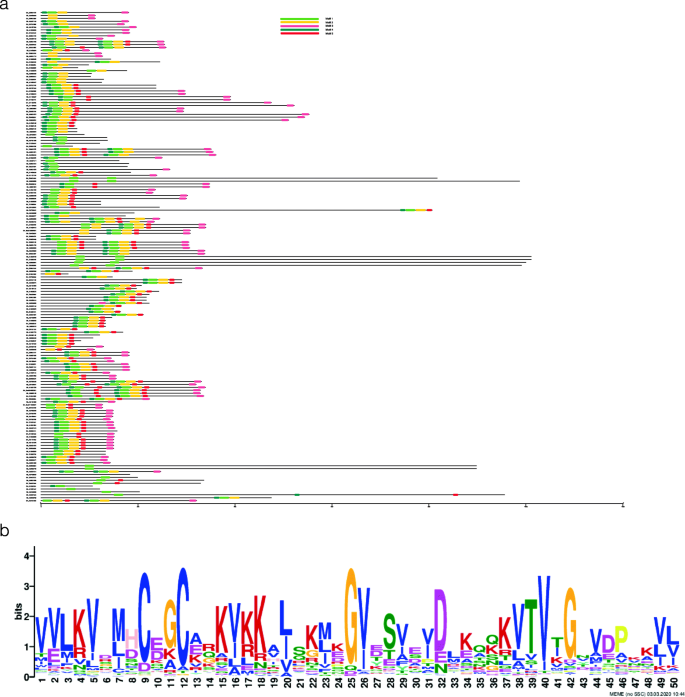
研究结构域序列的存在性和结构域的守恒程度HMAD域的g .分子的全长序列进行多序列比对HMAD家庭的蛋白质。不同的结果HMAD蛋白组表明,在序列中鉴定出5个保守基序HMAD每个家族蛋白上的基序顺序并不完全相同(图2)。5a).此外,我们还分析了守恒HMAD通过多序列比对,发现该结构域存在高度保守的motif(图2)。5b),其中催化中心有阴离子结合盒(CXXC)。与以往的研究一致[122,123],该阴离子结合盒以两个保守的半胱氨酸作为金属结合。
在HMAD领域保守图案的标志g .分子.a:从MEME预测保守基序(http://meme-suite.org/tools/meme).蛋白质的长度是用下面的刻度来估计的。基序显示在不同颜色的盒子中,用不同的数字表示,黑线表示非保守氨基酸。b:保守图案Logo由MEME预测(http://meme-suite.org/tools/meme)
根据Ka/Ks比值,可以假设达尔文的积极选择与HMAD复制后的基因分化[124,125].在我们的研究中,我们发现79对基因的Ka/Ks比较低(小于0.5),24对基因的Ka/Ks比在0.5 - 1.0之间。其中13对基因Ka/Ks大于1,可能是由于重复后进化较快(表2)2).由于大多数Ka/Ks比值小于1.0,我们推测棉花HMAD基因家族经历了强大的纯化选择压力,在部分复制和全基因组复制(WGDs)后出现有限的功能分化。
表达谱HMADTM-1在不同组织和不同应激条件下的基因
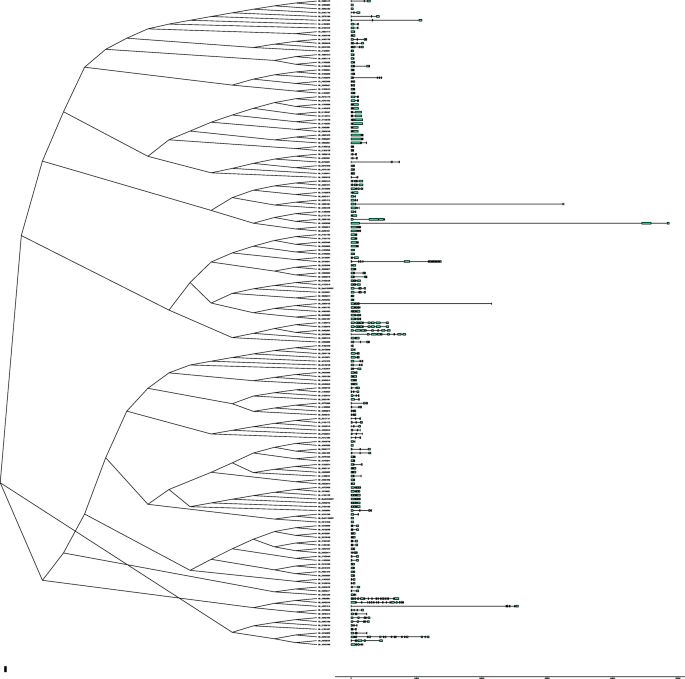
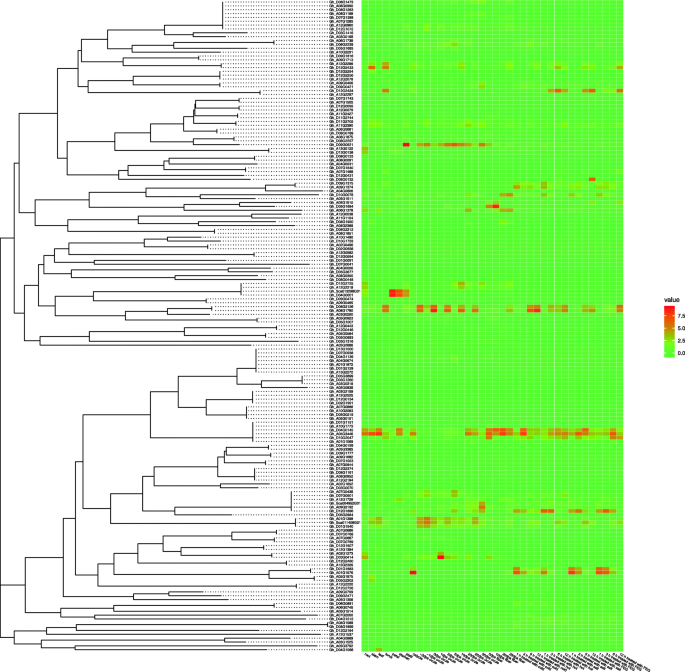
了解不同的时空表达模式HMAD利用公开保存的RNA-seq数据,评估不同组织(根、茎、叶、环面、花瓣、雄蕊、雌蕊、萼轮)、发育阶段(−3dpa胚珠、−1dpa胚珠、0dpa胚珠、1dpa胚珠、3dpa胚珠、5dpa胚珠、10dpa胚珠、20dpa胚珠、25dpa胚珠、5dpa纤维、10dpa纤维、20dpa纤维、25dpa纤维)和胁迫处理(冷处理1 h、冷处理3 h、冷处理6 h、冷处理12 h、1 h热处理,3 h热处理,6 h热处理,12 h热处理,1 h盐处理,3 h盐处理,6 h盐处理,12 h盐处理,1 h PEG处理,3 h PEG处理,6 h PEG处理,12 h PEG处理)。结果表明,169个基因可分为10个组,其中第1簇有2个基因(Gh_A08G1780,Gh_D08G2126),第2簇有两个基因(Gh_A05G3446,Gh_D04G0145),第三簇只有一个基因(Gh_A01G1576),第4簇有两个基因(Gh_D01G1883,Gh_D12G1886),第5簇只有一个基因(Gh_D03G0414),第6簇只有一个基因(Gh_D09G0521),第7簇有3个基因(Gh_A01G1399,Gh_D01G1640而且Gh_Sca011408G01),第8簇有两个基因(Gh_D04G0001,Gh_Sca013298G01),第9簇有4个基因(Gh_A12G2296,Gh_D10G2047,Gh_D12G2433而且Gh_D12G2434),簇10有151个基因(图S3.).
在聚类1中,环面、胚珠发育1次、25dpa纤维和胁迫处理6 h表达量较高。聚类2中,除花瓣、- 3dpa胚珠、- 1dpa胚珠、0dpa胚珠、1dpa胚珠、3dpa胚珠、5dpa胚珠、10dpa胚珠外,表达量均较高。在聚类3中,胁迫处理1 h后,其在花萼组织和胁迫处理1 h后表达量较高,并逐渐降低。聚类4中,冷处理1 h,热处理1 h,盐处理1 h,盐处理3 h, PEG处理1 h, PEG处理3 h,萼轮组织表达量较高。在聚类5中,根组织和1dpa胚珠中表达量较高。聚类6在雌蕊组织和胚珠发育中表达量较高,尤其是3dpa、5dpa和35dpa。聚类7在叶片组织和胚珠发育中表达量较高,尤其是在-1dpa胚珠。在聚8中,根、花瓣、雄蕊和雌蕊的表达量较高。聚类9中,环面组织、花萼、热处理6 h、盐处理6 h和聚乙二醇处理12 h表达量较高。在聚类10中,数量最多的基因有151个,但大多数表达量较低,甚至没有表达。 While some genes expression level is different, for example,Gh_D05G1684在纤维中高表达于10dpa。有趣的是,我们发现一些HMAD在胁迫条件下高表达的基因(图;6).例如,Gh_D08G0132而且Gh_A05G1510在盐胁迫条件下12 h高表达,而Gh_A01G1576胁迫条件(冷、盐、PEG) 1 h后高表达。Gh_A09G1374,Gh_D09G1375,Gh_D10G0078胁迫条件(冷、盐、PEG)下表达水平升高。
表达水平HMAD不同组织中的基因和不同的压力。用MEGA X近邻连接法构建HMAD蛋白序列的系统发育树(图左)。右边的热图是根据网站的RNA-seq数据(http://structuralbiology.cau.edu.cn/gossypium/).颜色条表示表达式值。颜色刻度显示在图的右边。红色表示表达水平较高,绿色表示表达水平较低
核心启动子元素分析
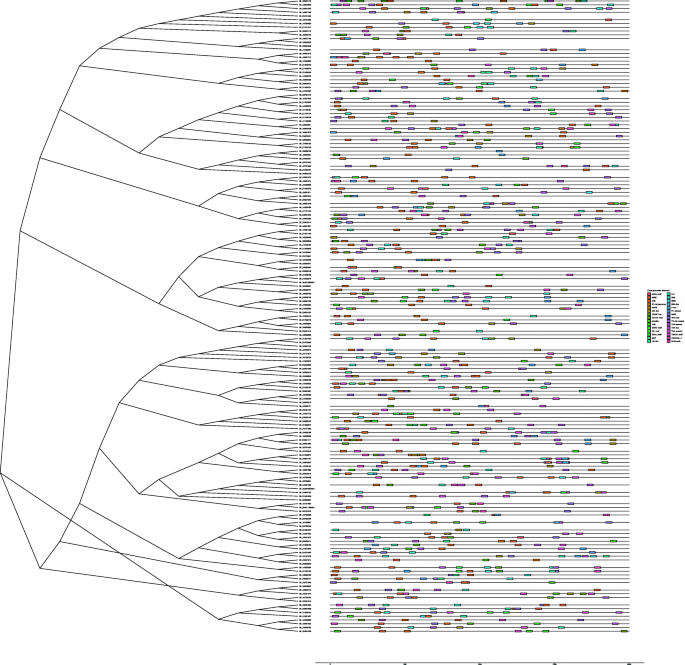
为了进一步探究原因HMAD基因家族在生物胁迫条件下高表达,除了重金属,核心启动子元素HMAD基因g .分子分为四种类型(激素,压力,组织和其他)(图。7),其中参与激素反应性的元素主要有ABA(脱落酸)、GA(赤霉素)、IAA/生长素、SA(水杨酸)、MeJA(茉莉酸甲酯)。涉及防御和应激反应的元件主要有干旱、低温、脱水、盐胁迫、厌氧,其中涉及干旱的基因72个,涉及低温反应的基因51个,涉及防御和应激反应的基因55个,含有富tc重复序列元件,1个基因(Gh_D04G1066)均与盐和低温反应有关。总共有169种基因的111种HMAD具有核心启动子元件的基因对胁迫有反应。如上在TM-1 RNA-seq数据中所述,18个基因中有12个至少有一个非生物胁迫相关启动子元件高表达(表S2).参与组织包括栅栏叶肉细胞、分生组织、胚乳、种子特异性的成分。而其他元素则参与了其他功能,如昼夜节律控制、细胞周期、类黄酮生物合成。有趣的是,黄酮类化合物生物合成元素的12个基因中有9个与其他胁迫元素同时存在。在以往的研究中,花青素作为次生代谢产物,可能通过渗透平衡来响应抗逆性[126,127,128].例如,Gh_A01G1576胁迫条件(冷、盐、PEG) 1 h后高表达,其核心启动子元件包含干旱诱导性、低温响应性和参与类黄酮生物合成基因调控的MBSI启动子元件(表S2).
核心启动子元素。用MEGA X近邻连接法构建HMAD蛋白序列的系统发育树(图左)。右边的核心启动子元件是根据Plant CARE数据库(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/).AACA_motif:参与胚乳特异性阴性表达。 ABRE:参与脱落酸反应的顺式作用元件。
ABRE:参与脱落酸反应的顺式作用元件。 ARE:对厌氧诱导必不可少的顺式作用调节元件。
ARE:对厌氧诱导必不可少的顺式作用调节元件。 AT -富序列:最大诱导介导激活的元素(2个副本)。
AT -富序列:最大诱导介导激活的元素(2个副本)。 AuxRE:生长素响应元件的一部分。
AuxRE:生长素响应元件的一部分。 CAT - box:与分生组织表达相关的顺式作用调控元件。
CAT - box:与分生组织表达相关的顺式作用调控元件。 CCAAT−box: MYBHv1绑定位点。
CCAAT−box: MYBHv1绑定位点。 CGTCA - motif:参与MeJA-responsiveness的顺式作用调控元件。
CGTCA - motif:参与MeJA-responsiveness的顺式作用调控元件。 昼夜节律:参与昼夜节律控制的顺式调节元件。
昼夜节律:参与昼夜节律控制的顺式调节元件。 DRE:参与脱水、低温、盐胁迫的顺式作用元件。
DRE:参与脱水、低温、盐胁迫的顺式作用元件。 GARE−motif:赤霉素响应元件。
GARE−motif:赤霉素响应元件。 GC - motif:参与缺氧特异性诱导的增强子样元件。
GC - motif:参与缺氧特异性诱导的增强子样元件。 GCN4 - motif:参与胚乳表达的顺式调控元件。
GCN4 - motif:参与胚乳表达的顺式调控元件。 HD−Zip 1:参与栅栏状叶肉细胞分化的因子。
HD−Zip 1:参与栅栏状叶肉细胞分化的因子。 LTR:参与低温响应的顺式元件。
LTR:参与低温响应的顺式元件。 MBS: MYB结合位点参与干旱诱导。
MBS: MYB结合位点参与干旱诱导。 MBSI: MYB结合位点参与类黄酮生物合成基因调控。
MBSI: MYB结合位点参与类黄酮生物合成基因调控。 类MSA:参与细胞周期调节的顺式作用元件
类MSA:参与细胞周期调节的顺式作用元件 P−box:赤霉素响应元件。
P−box:赤霉素响应元件。 RY -元件:参与种子特异性调控的顺式作用调控元件。
RY -元件:参与种子特异性调控的顺式作用调控元件。 参与水杨酸反应的顺式作用元件。
参与水杨酸反应的顺式作用元件。 TATC−box:参与赤霉素反应的顺式作用元件。
TATC−box:参与赤霉素反应的顺式作用元件。 TC -富重复:参与防御和应激反应的顺式作用元件。
TC -富重复:参与防御和应激反应的顺式作用元件。 TCA元素:参与水杨酸反应的顺式作用元素。
TCA元素:参与水杨酸反应的顺式作用元素。 TGA - box:生长素响应元件的一部分。
TGA - box:生长素响应元件的一部分。 TGA - element:生长素响应元件。
TGA - element:生长素响应元件。 TGACG - motif:参与meja响应的顺式作用调控元件。
TGACG - motif:参与meja响应的顺式作用调控元件。 Unnamed_1: 60k蛋白结合位点。
Unnamed_1: 60k蛋白结合位点。 WUN - motif:创伤响应元件
WUN - motif:创伤响应元件
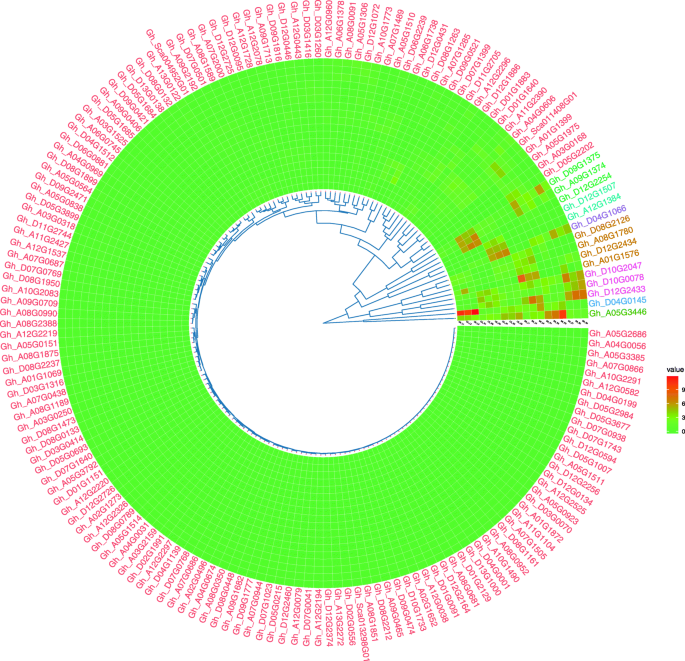
表达水平HMAD基因在不同组织中表达2所以4压力
确定…的功能HMAD在其他非生物胁迫下,我们使用Zhong 9835 [129].基于HMADRNA-seq数据的基因家族(图;8)(表S .5),有14个基因在根、茎、叶中表达量在300 mM Na处理和对照之间存在显著差异2所以4(表4,图S1),其中10个基因至少含有一个有关应激的核心启动子元件(表S2).有趣的是,4个类黄酮生物合成元素中有3个与应激元素同时存在。更重要的是,一些基因在胁迫条件下TM-1和Zhong 9835均高表达,如Gh_D04G0145,Gh_D10G0078,Gh_Sca011408G01,Gh_A01G1576等等。
讨论
在这项研究中,HMAD家族基因来自G.arboreum(84个基因),g . raimondii就(76个基因),g .分子(169个基因),和g .取得(159个基因),分别被鉴定,其中包含的总数量HMAD两个二倍体棉花(g . arboreum而且g . raimondii就),作为A和D基因组供体种,均低于同种四倍体(g .分子而且g .取得)棉花。的共时分析HMAD4个棉花品种的基因家族中,有4个基因在棉花品种中g . arboreum11个基因g . raimondii就在进化过程中丢失了24个基因,而在g .分子表明这些基因在棉花进化中发挥了关键作用。由于大多数Ka/Ks比值小于1.0,我们推测棉花HMAD基因家族经历了强大的纯化选择压力,功能分化有限。这些结果表明,在进化过程中可能存在基因丢失和/或染色体重排的结果[121].
169年g .分子基因被鉴定属于HMAD基因家族。分子量(kDa)为169HMAD蛋白质含量从5.8到108.5 kDa不等1).等电点(pI)的大多数169HMAD除55个小于7.6的基因外,其余蛋白质均呈碱性1).不同的分子质量和基因序列长度表明了其物理化学性质HMAD家族基因差异不大。基于WoLF PSORT分析,得到HMAD科基因主要分布在叶绿体(62个基因)、细胞质(54个基因)、细胞核(39个基因)和质膜(11个基因)1).169HMAD基因分为I、II、III、IV、Va、Vb五个亚类,其中II亚类含有最多的基因(66个成员),III亚类含有29个成员。结构分析169HMAD基因家族显示只有5个基因(Gh_D01G1640,Gh_Sca011408G01,Gh_A05G3385第一组,Gh_D08G1263而且Gh_A08G0990(Vb组)不含内含子。而剩下的HMAD基因含有多个内含子,尤其是p1b - atp酶HMA5-8内含子比其他基因多。其中基因功能注释169条HMAD基因中,重金属转运/解毒超家族蛋白数量为116个(表S5),按系统发生树和基因结构分为四类。Ka/Ks大于1的基因对有13对,其中包括13个重金属转运/解毒超家族蛋白(Gh_A05G2686,Gh_A08G1875,Gh_A10G1490,Gh_A10G2083,Gh_A11G1104,Gh_A12G0038,Gh_A12G0079,Gh_A13G2272,Gh_D05G0215,Gh_D05G2984,Gh_D07G0938,Gh_D08G2237,Gh_D10G1733).此外,通过序列比对发现了四种用于结合金属离子的保守氨基酸CXXC的特征[54,55].结合金属离子的保守氨基酸CXXC的分类基因和保守基序表明169HMAD不同细胞器中基因对重金属的反应可能不同,尤其是某些在相对快速进化下的重金属转运/解毒超家族蛋白。
启动子区分化的基因表达模式可以为基因功能的研究提供重要的见解[130].经TM-1分析RNA-seq数据,表达水平聚10的151个基因中大部分表达水平较低或无表达。对激素、应激、组织和其他四种类型的启动子元件进行分析,共检测到169个基因中的111个HMAD具有核心启动子元件的基因对胁迫有反应。结果表明,169HMAD基因在胁迫条件下(冷、盐、PEG)在组织中表达不广泛(图2)。6),表明不同启动子在不同组织和应激条件下的重要作用。
棉花是半盐生植物,中9835耐盐[131],包括Na2所以4.根据TM-1的转录组数据,我们发现在逆境非生物胁迫条件下重金属转运蛋白高度表达。进一步,通过基因序列和启动子元件分析,我们发现HMAD进化速度快,分为五种类型HMAD在逆境非生物胁迫条件下,一些具有应激因子反应的基因有较高的表达。根据分析根、茎、叶之间的钠含量2所以4在处理组和对照组中,14个含有应激元件的基因表达差异显著(图S1).HMAD在盐条件下高表达,可能是由于离子平衡引起的ROS [6].例如,一方面,ROS方式的基因表达和离子平衡的维持,如Ca2 +MAPK、MYB转录因子[132,133],程序性细胞死亡[134,135].而GSH作为高浓度条件下去除ROS的主要途径,不仅对重金属离子有反应[136],也对盐胁迫离子有反应[137].最后,花青素等离子的平衡与盐胁迫有关。6].HMAD花青素相关启动子元素在Na下高度表达2所以4条件,类似于以往的研究,花青素参与耐盐,同时参与重金属运输[137].另一方面,重金属的转移和盐胁迫是液泡偏析[138,139],如p型ATP作为重要的作用,不仅可以平衡盐离子,还可以平衡重金属离子[140,141].
在另外,协会基因可选择性地吸收和运输金属离子[142].CtpB作为质膜铜(I)转运的p型atp酶结核分枝杆菌,与铜解毒不同[143].在结核分枝杆菌、铜2 +、有限公司2 +、镍2 +、锌2 +、Cd2 +和铅2 +刺激质膜中推定的p1b型atp酶CtpG的atp酶活性,而Cd2 +比其他重金属阳离子更有效地穿过分枝杆菌质膜[144].伴侣蛋白是将Cu传递给重金属p1b - atp酶的重要途径[143].一般来说,协会包含约6-8个跨膜螺旋,一个可溶性核苷酸结合结构域,磷酸化结构域和一个可溶性致动器结构域,其中HMA1-4属于Zn2 +/公司2 +/ Cd2 +/ Pb2 +运输,虽然HMA1保守氨基酸不同于HMA2,HMA3而且HMA4[143),而HMA5-8属于Cu+/ Ag)+子类(144].
的序列协会(重金属atp酶)从P1B-ATPg .分子的序列协会在答:芥,也含有P-ATPases (E1-E2 ATPases)和有(晕轮酸脱氢酶)结构域和HMAD(重金属相关域)域(表S3.).在这项研究中,HMAD包含基因家族HMA5-HMA8(除了Gh_A08G2387)(表S3.).HMA5局限于质膜Gh_A05G0564,Gh_A08G2388,Gh_D05G0693有8个ths,而Gh_D08G19506个ths。在HMA6,Gh_A03G1525有7个ths定位于质膜,而Gh_A04G0969而且Gh_D04G1512没有TMHs定位在叶绿体中。HMA7而且HMA8定位于质膜,分别有8个和5个TMHs。很明显,在棉花中协会基因序列、基因结构、Ka/Ks比值及系统进化树分析[144].
结论
综上所述,我们确定了169、159、76和84个全长推定HMAD基因在g .分子,g .取得,g . arboreum而且g . raimondii就这些基因比其他基因家族的要大得多。我们还发现HMAD具有启动子元件的胁迫应答基因家族可能在不同的非生物胁迫中发挥重要作用。本研究结果为进一步探索分子串扰机制提供了基础HMAD非生物胁迫和重金属条件下的基因。
方法
棉花基因组和RNA-seq资源
四种基因组测序数据和注释信息Gossypium物种包括g . raimondii就(JGI_v2)g . arboreum(CRI_v1.1)g .分子(NAU-NBI_v1.1)和g .取得(ZJU_v1.1)已从Cottongen (https://www.cottongen.org/).用于基因表达分析的RNA-seq数据g .分子已从ccNET数据库下载(http://structuralbiology.cau.edu.cn/gossypium/),主要包括部分胁迫条件下的基因表达数据。PRJNA248163,如根(SRR1695173)、茎(SRR1695174)、叶(SRR1695175)、环面(SRR1695176)、花瓣(SRR1695177)、雄蕊(SRR1695178)、雌蕊(SRR1695179)、花萼(SRR1695180)、−3dpa胚珠(SRR1695181)、−1dpa胚珠(SRR1695182)、0dpa胚珠(SRR1695183)、1dpa胚珠(SRR1695184)、3dpa胚珠(SRR1695185)、5dpa胚珠(SRR1695186)、10dpa胚珠(SRR1695187)、20dpa胚珠(SRR1695188)、25dpa胚珠(SRR1695189)、35dpa胚珠(SRR1695190)、5dpa胚珠(SRR1695191)、10dpa胚珠(SRR1695192)、20dpa纤维(SRR1695193), 25dpa纤维(SRR1695194), 1小时冷处理(SRR1768504), 3小时冷处理(SRR1768505), 6小时冷处理(SRR1768507), 1小时热处理(SRR1768508), 3小时热处理(SRR1768509), 6小时热处理(SRR1768510), 12小时热处理(SRR1768511), 1小时盐处理(SRR1768512), 3小时盐处理(SRR1768513), 6小时盐处理(SRR1768514), 12小时盐处理(SRR1768515),用PEG处理1小时(SRR1768516),用PEG处理3小时(SRR1768517),用PEG处理6小时(SRR1768518),用PEG处理12小时(SRR1768519)。高粱品种自交系中9835的原始RNA-Seq数据g .分子,关于Na2所以4本研究中产生的耐受性可在生物计划数据库中获得,登录号为。PRJNA703009。
含HMAD结构域基因的鉴定
为了鉴定含HMAD结构域的基因,从Pfam 29.0数据库(http://pfam.xfam.org/),利用HMMER 3.0软件检索4个棉花品种的全基因组数据库[145],并通过pfamscan网站(https://www.ebi.ac.uk/Tools/pfa/pfamscan/)及(http://smart.emblheidelberg.de/SMART(简单模块化体系结构研究工具),用于确认结果。对无HMAD结构域的冗余序列进行手工检查并去除。利用ExPASy在线测试工具(http://expasy.org/tools/).用WoLF PSORT软件预测亚细胞位置(http://wolfpsort.org/).假定的跨膜螺旋也预测使用TMHMM Server V.2.0 (http://www.cbs.dtu.dk/services/TMHMM/).
系统发育分析
利用ClustalX2软件对4个棉花品种的HMAD结构域基因序列进行多序列比对[146使用默认参数。在MEGA X软件中使用邻居连接树(NJ)构建无根系统发育树[147) (https://www.megasoftware.net/)与1000次迭代的引导分析和ggtree (v2.2.4)包[148R (v4.0.3)软件。
染色体作图和基因复制
的物理位置数据HMAD从四个棉花品种的基因组序列数据中检索基因,随后使用Mapchart-2.23对这些基因进行绘制[149].演化的同义和非同义速率采用Ka/Ks计算器2.0的最大似然方法计算[150].
基因结构与结构域分析
的外显子和内含子组织HMAD基因结构显示服务器(http://gsds.cbi.pku.edu.cn/)通过比较基因组序列和CDS序列。保守的图案HMAD基因以MEME (http://meme-suite.org/tools/meme)及TBtools-0.6673 [151].
全基因组同步性分析HMAD基因
采用BLASTP方法比较两个同种异体四倍体棉花品种(g .分子而且g .取得)和两种二倍体棉花(g . raimondii就而且g . arboreum).根据BLASTP输出,采用circos-0.69-3软件包(http://circos.ca/software/),使用默认参数。
启动子中顺式元素的分析
启动子元件序列提取自基因上游2000 bp,顺式元件通过Plant CARE数据库(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/).
RNA-seq与Na处理之间的差异2所以4
中9835是一份保存自育系g .分子被我们实验室用于这项研究。种子播种在沙土盆里。将砂子冲洗干净,在121℃下消毒8 h。在光照强度为150 μmol·m-2·s-1、相对湿度为75%的条件下,每盆4株幼苗在28°C/16 h光照和25°C/8 h暗循环条件下培养约30 d。然后是300mm Na2所以4选择12 h后为适用应力集中和时间。将幼苗移植到正常水中作为对照。暴露12 h后,采集叶、茎和全根样品。每个样品测试三次。样品在液氮中冷冻,并保存在−80°C。
RNA提取和qRT-PCR分析
在300 mM Na处理和对照之间,从根、茎和叶中分离总RNA2所以4通过EASY spin Plant RNA Kit (TIANGEN)检测Zhong 9835基因。然后按照厂家说明书使用Prime Script TM II 1st strand cDNA Synthesis Kit (TaKaRa)合成第一链cDNA。qRT-PCR在20 μL体积中进行,含1.4 μL cDNA, 0.8 μL 10 μM正向和反向引物,10 μL SYBR Premix Ex Taq II (2×), 7.8 μL ddH2在95℃变性30 s下进行O. PCR扩增;在95°C下持续5秒,60°C下持续30秒,循环40次;随后Bio-Rad CFX96 Real-Time PCR系统在95℃孵育15 s, 60℃孵育1 min。采用基因特异性引物进行qRT-PCR,以hisstone3 (AF024716) (F: TCAAGACTGATTTGCGTTTCCA, R: GCGCAAAGGTTGGTGTCTTC)为内对照。最后,用2- - - - - -△△Ct方法。
数据和材料的可用性
所有支持我们研究发现的数据和材料都包含在手稿的方法部分。详细信息在附加文件中提供。在当前研究中生成和/或分析的数据集可在NCBI存储库[PRJNA248163和PRJNA703009]中获得。
缩写
- HMAD:
-
Heavy-metal-associated域
- 协会:
-
重金属atp酶
- 分区:
-
花后天数
- MAPK:
-
丝裂原活化蛋白激酶
- 电脑:
-
转移
- MTs:
-
金属硫蛋白
- 美国广播公司(ABC):
-
磷酸腺苷磁带
- NRAMP:
-
天然抗性和巨噬细胞蛋白
- 提供:
-
阳离子扩散促进器
- 伊夫圣罗兰:
-
Yellow-stripe-like
- HMA4:
-
重金属atp酶4
- IRT2:
-
铁调节蛋白2
- wgd:
-
全基因组复制
参考文献
- 1.
盐生植物——植物修复的新趋势。植物学报。2011;13(10):959-69。https://doi.org/10.1080/15226514.2010.532241.
- 2.
阿里夫N,亚达夫V,辛格S,辛格S,艾哈迈德P,米什拉RK,等。高、低水平植物有益重金属离子对植物生长发育的影响环境科学前沿,2016;4:69-80。
- 3.
陆敏,焦松,高娥,宋旭,李忠,郝旭,等。墨氏中华根瘤菌CCNWSX0020转录组对重金属的响应揭示了新的金属抗性决定因素,也促进了紫花苜蓿在金属污染土壤中的生物修复。应用环境科学学报,2017;29(3):344 - 344。
- 4.
段强,李晨,吴华。FERONIA受体样激酶对根毛发育RHO GTPase信号通路的调控。自然科学进展,2010;26(4):344 - 344。https://doi.org/10.1073/pnas.1005366107.
- 5.
Salam LB, Obayori OS, Ilori MO, Amund OO。镉摄动对热带农业土壤微生物群落结构和重金属抗性的影响生物资源生物过程,2020;7:1-19。
- 6.
Farcasanu IC, Popa CV, Ruta LL。钙和细胞对重金属的反应:酵母能提供答案吗?钙信号传输,2018;23:e78941。
- 7.
Jalmi SK, Bhagat PK, Verma D, Noryang S, Tayyeba S, Singh K,等。穿越重金属胁迫和植物信号之间的联系。植物科学,2018;9:12。https://doi.org/10.3389/fpls.2018.00012.
- 8.
Emamverdian A, Ding Y, Mokhberdoran F, Xie Y.重金属胁迫与植物防御反应的一些机制。科学通报,2015;
- 9.
乔dhary K, Agarwal S, Khan S.植物螯合素(PCs)、金属硫蛋白(MTs)和重金属atp酶(HMA)基因在重金属耐受中的作用。In:真菌修复与环境可持续性:施普林格;2018.39-60页。http://dx.doi.org/10.1007/978-3-319-77386-5_2.
- 10.
于瑞,李东,杜霞,夏松,刘超,石刚。两种小白菜根系镉转运相关关键基因的比较转录组分析(芸苔属植物拉伯l . ssp。对品种。BMC基因组学杂志,2017;18(1):1 - 14。
- 11.
夏霞,李娟,周志,王东,黄娟,王刚。多重重金属耐药菌高质量基因组序列草案Pseudaminobacter manganicus植物学报,2018;13(1):1 - 8。
- 12.
于伟,陈霞,盛勇,洪强美国maltophilia.bioRxiv。2018:404954。https://doi.org/10.1101/404954.
- 13.
Ghori N, Ghori T, Hayat MQ, Imadi SR, Gul A,阿勒泰V,等。重金属胁迫及其在植物中的响应。环境科学学报,2019;16(3):1807-28。https://doi.org/10.1007/s13762-019-02215-8.
- 14.
Belykh ES, Maystrenko TA, Velegzhaninov IO。通过转基因和转录程序增强栽培植物对重金属胁迫抗性的最新趋势。中国生物医学工程学报,2019;26(10):725-41。https://doi.org/10.1007/s12033-019-00202-5.
- 15.
李文杰,李志刚,李志刚。液泡区化在植物重金属排毒中的作用。植物细胞环境学报。2016;39(5):1112-26。https://doi.org/10.1111/pce.12706.
- 16.
刘志强,李志强,李志强,李志强,等。植物对重金属的吸收、动员和吸附特性研究。植物生态学报。2017;367-94。https://doi.org/10.1007/978-981-10-6593-4_15.
- 17.
Shahid M, Khalid S, Abbas G, Niazi NK, Murtaza B, Rashid MI,等。重金属胁迫下的氧化还原机制与植物耐受性:基因与调控网络。In:植物金属组学和功能组学:施普林格;2019.p . 71 - 105。https://doi.org/10.1007/978-3-030-19103-0_5.
- 18.
Axelsen KB, Palmgren MG。p型atp酶超家族底物特异性的进化。中华药理学杂志,1998;46(1):84-101。https://doi.org/10.1007/PL00006286.
- 19.
Zinati Z, Alemzadeh A, KayvanJoo AH。p型atp酶底物特异性的分类和预测的计算方法拟南芥.物理与分子生物学杂志,2016;22(1):163-74。https://doi.org/10.1007/s12298-016-0351-5.
- 20.
米德JC。利什曼原虫和锥虫中的p型转运atp酶。寄生虫。2019;26:69。https://doi.org/10.1051/parasite/2019069.
- 21.
Solioz M, Vulpe C. cpx型atp酶:一类泵浦重金属的p型atp酶。生物化学,1996;21(7):237-41。https://doi.org/10.1016/s0968 - 0004 (96) 20016 - 7.
- 22.
科贝特CS,侯赛因D,海顿MJ。1B型转运重金属p型atp酶的结构和功能关系拟南芥.植物科学进展。2003;26(2):329 - 329。https://doi.org/10.1046/j.1469-8137.2003.00785.x.
- 23.
Argüello JM, Eren E, González-Guerrero M.重金属转运p1b - atpases的结构和功能。Biometals。2007;20(3 - 4):233 - 48。https://doi.org/10.1007/s10534-006-9055-6.
- 24.
rønberg C, Sitsel O, Lindahl E, Gourdon P, Andersson M. P型atp酶铜转运的膜锚定和离子进入动力学。中国生物医学工程学报,2016;29(11):344 - 344。https://doi.org/10.1016/j.bpj.2016.10.020.
- 25.
龙欣E, Grønberg C,胡Q, Duelli AS, Andersen KR, Laursen NS,等。锌转运p型atp酶纳米体的分离与表征。抗体。2018;7(4):39。https://doi.org/10.3390/antib7040039.
- 26.
Smith AT, Ross MO, Hoffman BM, Rosenzweig AC. cd-, co-和zn转运p1b型atp酶的金属选择性。Biochemistry-US。2017; 56(1): 85 - 95。https://doi.org/10.1021/acs.biochem.6b01022.
- 27.
张志刚,张志刚,张志刚,张志刚,等。底物亲和力的微调导致结核分枝杆菌Fe的不同作用2 +atp酶。中国生物医学工程学报,2016;https://doi.org/10.1074/jbc.M116.718239.
- 28.
普罗希特R,罗斯MO,巴特鲁S, Kusowski A, Stemmler TL, Hoffman BM,等。铜+-特异性CopB转运体:修正p1b型atp酶分类。中国生物医学工程学报,2018;29(3):344 - 344。https://doi.org/10.1073/pnas.1721783115.
- 29.
王霞,龚霞,曹峰,王勇,张刚,吴峰。大麦耐镉积累与耐镉新基因p型atp酶HvPAA1编码(大麦芽l .)。国际分子生物学杂志,2019;20(7):1732。
- 30.
Keeran NS, Ganesan G, Parida AK。一种新的重金属atp酶肽Prosopis juliflora参与酵母和烟草中的金属吸收。转基因res 2017;26(2): 247-61。https://doi.org/10.1007/s11248-016-0002-1.
- 31.
王勇,王娥,孙晓明,杨杰,等。p型atp酶重金属转运蛋白在必需锌稳态中的作用拟南芥.植物学报。2004;16(5):1327-39。https://doi.org/10.1105/tpc.020487.
- 32.
黄霞,邓峰,山次,平森,藤卡野,丹库J,等。一种重金属p型atp酶OsHMA4可以阻止铜在大米中的积累。Nat community . 2016;7(1):1 - 13。
- 33.
Grispen VM, Hakvoort HW, Bliek T, Verkleij JA, Schat H.拟南芥金属硫蛋白MT2b与重金属转运atp酶HMA4的联合表达增强了烟草的镉耐受性和镉、锌的根茎转运。环境科学学报。2011;32(1):71-6。https://doi.org/10.1016/j.envexpbot.2010.01.005.
- 34.
丛伟,苗勇,徐林,张勇,袁超,王杰,等。重金属胁迫诱导水稻基因表达变化的跨代记忆(栽培稻l .)。BMC植物学报,2019;19(1):1 - 14。
- 35.
张勇,陈凯,赵峰,孙超,金超,石勇,等。OsATX1与重金属p1b型atp酶相互作用,影响铜的运输和分布。中国生物医学工程学报,2018;29(1):329 - 344。https://doi.org/10.1104/pp.18.00425.
- 36.
王晓明,王晓明,王晓明,王晓明,等。盐胁迫和镉胁迫下植物重金属转运基因的表达。植物。2020;9(4):475。https://doi.org/10.3390/plants9040475.
- 37.
Shrivastava M, Khandelwal A, Srivastava S.重金属超富集植物:了解植物对重金属极端适应的资源。In:植物-金属相互作用:施普林格;2019.p . 79 - 97。https://doi.org/10.1007/978-3-030-20732-8_5.
- 38.
戴伟,王敏,龚霞,刘建华。WRKY的转录因子fc为40Fortunella植通过直接调节SOS2和P5CS1同源物调节离子稳态和脯氨酸生物合成,在耐盐性中起积极作用。中国生物医学工程学报,2018;29(3):344 - 344。https://doi.org/10.1111/nph.15240.
- 39.
哈提瓦达B,哈桑MT,孙A, Kamath KS, Mirzaei M,孙娜A,等。探讨植物叶绿体在重金属耐受和积累中的作用眼虫属股薄肌.微生物。2020;8(1):115。https://doi.org/10.3390/microorganisms8010115.
- 40.
谢建平,Pilátová J,马丽娟,李志强,等。铜和铁代谢在Ostreococcus金牛座的-植物转铁蛋白、质体青苷和叶绿体铜转运atp酶的作用。Metallomics。2019;11(10):1657 - 66。https://doi.org/10.1039/C9MT00078J.
- 41.
Sikder RK,王旭,张华,桂华,董强,金东,等。氮通过调节植物抗氧化防御系统和渗透调节物质含量来增强植物的耐盐性陆地棉.植物。2020;9(4):450。https://doi.org/10.3390/plants9040450.
- 42.
Jahan B, AlAjmi MF, Rehman MT, Khan NA。氮硫配施氮氧化物对盐胁迫下芥菜光合性能和气孔行为有调节作用。中国生物医学工程学报。2020;32(2):489 - 491。
- 43.
MacFarlane GR, Burchett MD.灰色红树光合色素和过氧化物酶活性作为重金属胁迫的指标,矮小(Forsk)。Vierh。污染通报。2001;42(3):233-40。https://doi.org/10.1016/s0025 - 326 x (00) 00147 - 8.
- 44.
重金属胁迫下脯氨酸积累。中国植物科学,2001;29(5):344 - 344。
- 45.
杨晓明,王晓明,王晓明,等。盐胁迫下花椰菜幼苗脯氨酸积累的研究。应用科学与环境管理,2011;15(2):251-5。
- 46.
王晓明,王晓明,王晓明,等。重金属离子过量对向日葵叶片氧化应激的影响。植物科学学报,1996;26(2):344 - 344。https://doi.org/10.1016/s0168 - 9452 (96) 04528 - 1.
- 47.
刘志刚,李志刚,李志刚。植物抗氧化防御系统对盐胁迫的适应性反应向日葵l细胞。植物生长学报。2003;40(1):81-8。https://doi.org/10.1023/A:1023060211546.
- 48.
张峰,王勇,楼志,董娟。重金属胁迫对两种红树幼苗叶片和根系抗氧化酶和脂质过氧化的影响(Kandelia candel而且工业gymnorrhiza).臭氧层。2007;67(1):44-50。https://doi.org/10.1016/j.chemosphere.2006.10.007.
- 49.
杨晓明,王晓明,杨晓明,Férard .重金属胁迫对小鼠氧化应激的影响Fontinalis antipyreticaHedw。臭氧层。2009;75(3):297 - 302。https://doi.org/10.1016/j.chemosphere.2008.12.045.
- 50.
西迪基z。双重胁迫对植物抗氧化酶活性的影响豇豆属辐射动物(l)Wilczek。机器人学报。2013;72(1):145-56。https://doi.org/10.2478/v10184-012-0011-y.
- 51.
苏世杰,李文伟,李宗杰,黄世德,李延民,朴鸿辉,等。环境压力源(盐度、重金属和H2O2)调节谷胱甘肽还原酶(GR)基因的表达tigriopus对虾.水毒物。2006;80:281-9。
- 52.
李志强,李志强,李志强,等。芥菜对重金属的耐受性及其积累特性(芸苔属植物junceal)表达细菌γ-谷氨酰半胱氨酸合成酶或谷胱甘肽合成酶。植物学报。2008;10(5):440-54。https://doi.org/10.1080/15226510802100630.
- 53.
库玛,Asif MH, Chakrabarty D, Tripathi RD, Dubey RS, Trivedi PK.水稻lambda类谷胱甘肽S转移酶OsGSTL2的表达拟南芥提供对重金属和其他非生物应力的耐受性。J危险材料,2013;248:228-37。
- 54.
周勇,文忠,张娟,陈鑫,崔娟,徐伟,等。外源性谷胱甘肽通过调节谷胱甘肽代谢、氧化还原状态和抗氧化系统来缓解盐诱导的番茄幼苗氧化应激。Sci Hortic-Amsterdam。2017; 220:90 - 101。https://doi.org/10.1016/j.scienta.2017.02.021.
- 55.
Barroso C, Romero LC, Cejudo FJ, Vega JM, Gotor C.盐对细胞质的特异性调控o -乙酰丝氨酸(硫醇)裂解酶拟南芥基因依赖脱落酸。植物分子生物学,1999;40(4):729-36。https://doi.org/10.1023/A:1006285016296.
- 56.
Nocito FF, Lancilli C, Crema B, Fourcroy P, david dian J, Sacchi GA。玉米根系重金属胁迫与硫酸盐吸收。植物科学进展。2006;29(3):344 - 344。https://doi.org/10.1104/pp.105.076240.
- 57.
李玲,王勇,沈伟。硫化氢和一氧化氮在缓解镉诱导的苜蓿幼苗根系氧化损伤中的作用。Biometals。2012;25(3):617 - 31所示。https://doi.org/10.1007/s10534-012-9551-9.
- 58.
莫斯托法MG,佐古沙D,藤田M, Tran LP。硫化氢通过维持钠来调节水稻的耐盐性+/ K+过量盐胁迫下的平衡、矿物稳态与氧化代谢。前沿植物科学,2015;6:1055。
- 59.
杨晓明,张晓明,张晓明,等。植物生长素共轭吲哚-3-乙酰-天冬氨酸对镉和盐胁迫的响应Pisum一中国植物科学,2016;19(1):1 - 7。https://doi.org/10.1016/j.jplph.2015.11.012.
- 60.
Fässler杨晓明,杨晓明,杨晓明,杨晓明,等。乙烯二胺二琥珀酸(EDDS)与吲哚乙酸(IAA)配施对向日葵生长及重金属吸收的影响。臭氧层。2010;80(8):901 - 7。https://doi.org/10.1016/j.chemosphere.2010.04.077.
- 61.
张志强,李志强,李志强,等。油菜素内酯对萝卜生长的影响(萝卜l)镉胁迫下生长的幼苗。植物土壤环境。2007;53(11):465。
- 62.
杨晓明,李志强,李志强,等。植物激素表油菜素内酯对植物重金属胁迫耐受性的调节作用栽培稻通过调节抗氧化防御的表达。环境实验机器人。2016;122:1-9。https://doi.org/10.1016/j.envexpbot.2015.08.005.
- 63.
柯强,叶娟,王波,任军,尹林,邓霞,等。褪黑素通过调节多胺代谢来缓解小麦幼苗的盐胁迫。中国植物科学,2018;9:914。https://doi.org/10.3389/fpls.2018.00914.
- 64.
王晓燕,王晓燕,王晓燕,王晓燕,等。一氧化氮和硫化氢在辣椒褪黑素诱导耐受性中的综合作用(甜椒L.)植物对缺铁和盐胁迫单独或联合处理。中国植物科学。2020;68(2):256-77。
- 65.
马思迪基,Glick BR, PS Chauhan, Jong Yim W, Sa T.提高红辣椒幼苗生长和耐盐性(甜椒L.)通过含有1-氨基环丙烷-1-羧酸脱氨酶活性的耐盐细菌调节应激乙烯合成。植物生理学报,2011;49(4):427-34。https://doi.org/10.1016/j.plaphy.2011.01.015.
- 66.
韩艳,王荣,杨忠,詹艳,马艳,平松,等。stutzeri假单胞菌A1501中1-氨基环丙烷-1-羧酸脱氨酶对盐或重金属胁迫下水稻生长的促进作用。中国生物医学工程学报,2015;25(7):1119-28。https://doi.org/10.4014/jmb.1412.12053.
- 67.
宋文文,杨兴华,邵海波,郑亚智,Brestic M.水杨酸对麦芽过氧化氢酶和超氧化物歧化酶活性的抑制作用(大麦uhulgarel)幼苗叶片受重金属胁迫。土壤,空气,水。2014;42(1):88-97。https://doi.org/10.1002/clen.201200310.
- 68.
杨晓明,李志刚,李志刚,等。水杨酸缓解水稻盐胁迫的生理机制研究。中国水稻科学,2017;24(2):97-108。https://doi.org/10.1016/j.rsci.2016.07.007.
- 69.
王志强,王志强,王志强,等。水杨酸对小麦耐盐性的影响。中国生物医学工程学报(英文版);
- 70.
Saxena I, Shekhawat GS。一氧化氮(NO)在减轻重金属诱导植物毒性中的作用及其在蛋白质硝化中的作用。一氧化氮。2013;32:13-20。https://doi.org/10.1016/j.niox.2013.03.004.
- 71.
何俊,任勇,陈霞,陈宏。一氧化氮对水稻种子萌发和幼苗生长的保护作用(栽培稻l)在镉胁迫下。环境安全。2014;108:114-9。https://doi.org/10.1016/j.ecoenv.2014.05.021.
- 72.
伊姆兰QM, Falak N, Hussain A, Mun B, Sharma A, Lee S,等。一氧化氮反应性重金属相关基因AtHMAD1有助于发育和抗病拟南芥.前沿植物学报2016;7:1712。
- 73.
金Y, Khan AL, Kim D, Lee S, Kim K, Waqas M,等。硅通过调节p型重金属atp酶来缓解重金属胁迫,栽培稻低硅基因和内源性植物激素。中国生物医学工程学报。2014;14(1):1 - 13。
- 74.
朱忠,魏刚,李娟,钱强,余娟。硅对盐胁迫黄瓜叶片抗氧化酶活性的影响(Cucumis巨大成功l .)。中国植物科学(英文版);2004;37(3):344 - 344。https://doi.org/10.1016/j.plantsci.2004.04.020.
- 75.
盐胁迫下生物炭对豆苗抗氧化酶和渗透调节的影响。环境安全。2017;137:64-70。https://doi.org/10.1016/j.ecoenv.2016.11.029.
- 76.
Abd El- mageed TA, Rady MM, Taha RS, Abd El Azeam S, Simpson CR, Semida WM。盐胁迫下残硫增强生物炭与有效微生物配施对辣椒土壤性状、植株生长及短期生产力的影响Sci Hortic-Amsterdam。2020; 261:108930。https://doi.org/10.1016/j.scienta.2019.108930.
- 77.
王超,陈强,项宁,刘勇,孔霞,杨勇,等。SIP1是一种新型的SOS2相互作用蛋白,参与植物耐盐胁迫拟南芥.植物物理学报,2018;124:167-74。https://doi.org/10.1016/j.plaphy.2018.01.018.
- 78.
孔杰,金杰,董强,邱杰,李勇,杨勇,等。玉米因子ZmUBP15、ZmUBP16和ZmUBP19在植株耐受镉胁迫和盐胁迫中发挥重要作用。植物科学通报2019;https://doi.org/10.1016/j.plantsci.2018.11.014.
- 79.
舒凯,齐勇,陈峰,孟Y,罗霞,帅海,等。盐胁迫通过负向调节GA生物合成、正向调节ABA生物合成抑制大豆种子萌发。中国植物科学,2017;8:1372。https://doi.org/10.3389/fpls.2017.01372.
- 80.
邓波,杨凯,张勇,李哲。重金属污染能保护种子萌发免受热胁迫吗?重金属(Cu2 +、Cd2 +和汞2 +)对高温下玉米种子萌发的影响。环境污染,2016;216:46-52。https://doi.org/10.1016/j.envpol.2016.05.050.
- 81.
Shekhawat UKS, Srinivas L, Ganapathi TR. MusaDHN-1是一种新的多重胁迫诱导的sk3型脱氢蛋白基因,在香蕉耐干旱和耐盐胁迫中发挥了积极作用。足底。2011;234(5):915 - 32。https://doi.org/10.1007/s00425-011-1455-3.
- 82.
胡涛,朱松,谭亮,齐伟,何松,王刚,过表达OsLEA4转基因水稻抗旱、高盐和重金属胁迫能力增强(栽培稻l .)。环境实验机器人,2016;123:68-77。https://doi.org/10.1016/j.envexpbot.2015.10.002.
- 83.
张勇,王志,柴涛,文忠,张慧。印度芥菜水通道蛋白对烟草抗旱性和重金属抗性的改善。生物工程学报。2008;40(3):280-92。https://doi.org/10.1007/s12033-008-9084-1.
- 84.
胡伟,袁强,王勇,蔡锐,邓霞,王杰,等。小麦水通道蛋白基因TaAQP8的过表达增强了转基因烟草的盐胁迫耐受性。中国生物医学工程学报。2012;29(12):344 - 344。https://doi.org/10.1093/pcp/pcs154.
- 85.
贾尼卡- russak M, kabaaya K, burzyzynski M, kolobus G.质膜反应H+- atp酶对重金属胁迫的影响Cucumis sativu年代的根源。中国机械工程学报,2008;29(3):379 - 379。https://doi.org/10.1093/jxb/ern219.
- 86.
姚洁,沈震,张勇,吴旭,王杰,萨刚,等。胡杨WRKY1结合H的启动子+- atp酶基因增强基因表达和耐盐性。中国科学(d辑:自然科学),2015;https://doi.org/10.1093/jxb/erz493.
- 87.
倪伟民,李志伟,李志伟,Günther D, Tschiersch K, Nover L.热休克蛋白诱导植物对重金属的耐受性。足底。1994;194(3):360 - 7。
- 88.
Montero-Barrientos M, Hermosa R, Cardoza RE, Gutierrez S, Nicolas C, Monte e哈兹木霉HSP70基因会增加拟南芥耐热性和其他非生物应力。植物营养学报,2010;29(4):529 - 529。https://doi.org/10.1016/j.jplph.2009.11.012.
- 89.
黄超,周杰,杰勇,邢华,钟勇,余伟,等。苎麻bZIP转录因子BnbZIP2参与干旱、盐和重金属胁迫响应。DNA细胞生物学,2016;35(12):776-86。https://doi.org/10.1089/dna.2016.3251.
- 90.
金勇,姜华,安山。植物螯合酶AtPCS2的过表达增强了植物的耐盐性拟南芥.中国植物学报。2019;240:153011。https://doi.org/10.1016/j.jplph.2019.153011.
- 91.
梅凯维,孙夏,李志刚,李志刚,等。3型金属硫蛋白样基因(OsMT-3a),揭示了它具有耐盐和重金属胁迫的能力。环境实验机器人,2018;147:157-66。https://doi.org/10.1016/j.envexpbot.2017.12.002.
- 92.
王静,姚林,李波,孟Y,马晓霞,赖勇,等。盐生植物悬浮细胞培养的蛋白质组学比较分析Halogeton glomeratusiTRAQ的研究为盐胁迫的响应机制提供了见解。前沿植物科学,2016;7:110。
- 93.
孙文华,金玉杰,金恩恩,金德德,黄博凯,伊斯兰瑞,等。辣椒基本致病相关蛋白1基因在烟草植株中过表达增强了对重金属和病原胁迫的抗性。植物细胞学报2005;24(4):216-24。https://doi.org/10.1007/s00299-005-0928-x.
- 94.
Jain S, Kumar D, Jain M, Chaudhary P, Deswal R, Sarin NB。花生盐胁迫相关10类蛋白(PR10)基因异位过表达(落花生hypogaeaL.)转基因烟草具有广泛的非生物胁迫耐受性。植物细胞,组织和器官培养(PCTOC)胜38负2012;109(1):。
- 95.
moon a . Ospdr9编码pdr型ABC转运蛋白,在水稻根系中受到重金属、低氧胁迫和氧化还原扰动的诱导。中国农业科学,2003;29(3):344 - 344。https://doi.org/10.1016/s0014 - 5793 (03) 01060 - 3.
- 96.
Kim DY, Bovet L, Maeshima M, Martinoia E, Lee Y. ABC输送机AtPDR8是一种镉挤压泵,具有抗重金属性能。植物学报,2007;26(2):344 - 344。https://doi.org/10.1111/j.1365-313X.2007.03044.x.
- 97.
金迪,金建勇,李勇AtABCG36提高植物的抗旱性和耐盐性拟南芥.中国生物医学工程学报。2010;39(2):344 - 344。https://doi.org/10.1111/j.1399-3054.2010.01353.x.
- 98.
Singh AK, Kumar R, Pareek A, Sopory SK, Singla-Pareek SL.水稻CBS结构域含蛋白的过表达提高了转基因烟草对盐度、氧化和重金属的耐受性。生物工程学报。2012;52(3):205-16。https://doi.org/10.1007/s12033-011-9487-2.
- 99.
Kaur V, Yadav SK, Wankhede DP, Pulivendula P, Kumar A, Chinnusamy V.水稻MIZ1基因的克隆和鉴定及其在盐和干旱胁迫中的作用。原生质。2020;257(2):475 - 87。https://doi.org/10.1007/s00709-019-01452-5.
- One hundred.
郑松,刘松,冯杰,王伟,王勇,于强,等。应激反应膜蛋白基因的过表达OsSMP1提高水稻对盐、冷、重金属胁迫的耐受性。Environ Exp Bot. 2021;182:104327。https://doi.org/10.1016/j.envexpbot.2020.104327.
- 101.
刘志强,李志强,李志强,等。盐胁迫对小麦幼苗性状的影响。生物临床科学杂志J. 2020;2020:e5。
- 102.
张志刚,张志刚,张志刚,等。工业固体废弃物对黄瓜生长和重金属吸收的影响(Cucumis巨大成功l)在盐度胁迫下。Ecotox环境安全。2019;182:109347。https://doi.org/10.1016/j.ecoenv.2019.06.030.
- 103.
Bharti N, Singh RP。氯化钠在土壤生物量积累和硝酸盐同化方面对不同重金属毒性的拮抗作用胡麻属indicum幼苗。植物化学,1994,35(5):1157 - 61。https://doi.org/10.1016/s0031 - 9422 (00) 94813 - 1.
- 104.
李志刚,李志刚,李志刚。盐度对水仙生长及重金属积累能力的影响Spirodela polyrrhiza(浮萍科)。中华医学杂志,2011;35(2):215-20。
- 105.
艾因Q,阿赫塔尔J,阿姆贾德M,马哈克,萨奇布扎。盐胁迫下镍含量增加对小麦生长和生理的影响土壤科学通报。2016;47(22):2538-46。https://doi.org/10.1080/00103624.2016.1254796.
- 106.
王伟,柯成林,郝继伟,管霞,田霞。松柳初切对cd和cu的植物提取。植物学报,2019;21(2):84-91。https://doi.org/10.1080/15226514.2016.1183574.
- 107.
侯伟,陈旭,宋刚,王强,常成昌。铜和镉对浮萍修复重金属污染水体的影响(浮萍属小).植物生理学报,2007;45(1):62-9。https://doi.org/10.1016/j.plaphy.2006.12.005.
- 108.
张志刚,张志刚。接种抗逆境丛枝菌根真菌的研究进展血管球酶类关于成长茄属植物melogenal .,高粱苏丹葡萄球菌。盐胁迫和重金属胁迫下的幼苗。土壤科学进展,2013;29(2):344 - 344。https://doi.org/10.1080/03650340.2011.610029.
- 109.
Nawaz I、Iqbal M、Bliek M、Schat H. 4种生境偏好不同的嗜极生物蜗虫耐盐和重金属能力及候选耐盐基因表达水平环境科学学报,2017;
- 110.
印度孙德尔本植物Avicennia marina的Halomonas rhizobacteria通过产生胞外多糖促进水稻在盐和重金属胁迫下的生长。前沿微生物。2019;10:1207。https://doi.org/10.3389/fmicb.2019.01207.
- 111.
王敏,赵松,王林,陈松,李松,雷霞,等。盐胁迫引起的微生物群落结构和代谢过程的变化导致土壤镉有效性增加。科学总环境。2021;782:147125。https://doi.org/10.1016/j.scitotenv.2021.147125.
- 112.
韦兹niewska A, koukmizynska A, Hanus-Fajerska E, Dziurka M, Dziurka K.盐生植物多重胁迫耐受机制的研究Aster tripolium经受盐度和重金属胁迫。Ecotox环境安全。2019;180:12-22。https://doi.org/10.1016/j.ecoenv.2019.04.059.
- 113.
Topal MN, kiran S, ate什Ç, Ekİcİ M, Ellİaltıoğlu TR, Furtana GB,等。耐旱耐盐茄子选育系对重金属(Pb)的耐受性与商品砧木的比较研究。Derim。2017;34(1):1 - 10。
- 114.
冯松,任林,孙浩,乔凯,刘松,周安。不同生境两种柳树对盐胁迫的形态和生理响应。Sci Rep-Uk。2020; 10(1): 1 - 11。
- 115.
马力克,王旭,王旭,舒宁,崔荣,陈旭,等。全基因组表达分析表明,谷氨酰胺还蛋白基因对棉花不同胁迫有响应。中国生物医学杂志,2020;https://doi.org/10.1016/j.ijbiomac.2020.03.021.
- 116.
李敏,张旭,杨辉,李霞,崔哲。土壤可持续利用技术:黄酮醇在重金属抗性过程中的作用机理。环境科学学报,2018;25(26):26669-81。https://doi.org/10.1007/s11356-018-2485-1.
- 117.
张涛,胡勇,姜伟,方林,关霞,陈杰,等。同种异体四倍体棉花的测序(陆地棉lacc.TM-1)为光纤改进提供了资源。中国生物工程学报。2015;33(5):531-7。https://doi.org/10.1038/nbt.3207.
- 118.
杨晓明,王晓明,王晓明,等。一种基于微晶硅的重金属相关蛋白结构和功能分析方法芸苔属植物oleracea.自然科学进展,2016,26(2):344 - 344。
- 119.
李超,孙勇,刘辉,曾强,王勇,马俊,等。水稻重金属atp酶样基因的遗传变异分析。西南农业科学,2016;29(9):2009-15。
- 120.
吴勇,李霞,陈东,韩霞,李波,杨勇,等。重金属atp酶亚家族基因在耐cd和耐cd萝卜地方品种中的比较表达分析。植物多样性,2019;41(4):275-83。https://doi.org/10.1016/j.pld.2019.02.001.
- 121.
杨震,龚强,秦伟,杨震,程勇,卢林,等。全基因组分析WOX陆地棉基因及其在不同胁迫下的表达模式中国生物医学工程学报,2017;17(1):1 - 17。
- 122.
布尔PC,考克斯DW。威尔逊病和门克斯病:重金属运输的新认识。植物学报,1994;10(7):246-52。https://doi.org/10.1016/0168 - 9525 (94) 90172 - 4.
- 123.
Gitschier J, Moffat B, Reilly D, Wood WI, Fairbrother WJ。Menkes铜转运atp酶第四个金属结合域的解结构。中国生物工程学报。1998;5(1):47-54。https://doi.org/10.1038/nsb0198-47.
- 124.
王子VE,皮克特FB。分裂对:重复基因的不同命运。植物学报。2002;3(11):827-37。https://doi.org/10.1038/nrg928.
- 125.
Vandepoele K, Simillion C, Vande Peer Y.水稻和其他谷物是古代非整倍体的证据。植物学报。2003;15(9):2192-202。https://doi.org/10.1105/tpc.014019.
- 126.
杨晓明,杨晓明,杨晓明,杨晓明,等。非生物胁迫对植物花青素定位的影响拟南芥.植物信号行为研究。2015;10(7):e1027850。https://doi.org/10.1080/15592324.2015.1027850.
- 127.
张志刚,张志刚。花青素在强光胁迫响应中的作用。世界科学,2017;81(2):150-68。
- 128.
高杰,陈斌,林华,刘勇,魏勇,陈峰,等。萝卜中谷胱甘肽s -转移酶(GST)家族的鉴定和特征揭示了其在花青素生物合成和重金属胁迫耐受中的可能作用。基因。2020;743:144484。https://doi.org/10.1016/j.gene.2020.144484.
- 129.
王强,陆霞,陈霞,马立克,王东,赵玲,等。转录组分析揭示了陆地棉清除活性氧(ROS)的新途径2所以4宽容。Sci Rep-Uk。2021; 11(1): 8670。https://doi.org/10.1038/s41598-021-87999-x.
- 130.
薛涛,王东,张松,Ehlting J,倪峰,Jakab S,等。水稻和水稻蛋白质磷酸酶2C的全基因组及表达分析拟南芥.BMC基因组学杂志,2008;9(1):1 - 21。
- 131.
王旭,陆旭,马立克,陈旭,王杰,王东,等。差异表达bZIP转录因子赋予多重耐受性陆地棉中国生物医学工程学报,2015;26(2):366 - 366。https://doi.org/10.1016/j.ijbiomac.2020.01.013.
- 132.
万生,王伟,周涛,张勇,陈杰,肖波,等。转录组分析揭示了病毒的分子机制茶树对盐胁迫的反应。植物生长学报,2018;84(3):481-92。https://doi.org/10.1007/s10725-017-0354-4.
- 133.
许伟,黄伟。植物激素信号通路中的钙依赖蛋白激酶。国际分子化学杂志,2017;18(11):2436。https://doi.org/10.3390/ijms18112436.
- 134.
杨毅,郭毅。植物盐胁迫信号的解析。中国生物医学工程学报,2018;29(6):796-804。https://doi.org/10.1111/jipb.12689.
- 135.
利用程序性细胞死亡途径增强作物耐盐性。在:植物对盐度的响应和耐受性,vol. 2:施普林格;2018.p . 93 - 118。https://doi.org/10.1007/978-3-319-90318-7_5.
- 136.
韩敏,陆旭,余娟,陈旭,王旭,马立克,等。转录组分析显示棉花(陆地棉)基因在镉胁迫耐受性方面的差异表达。国际分子生物学杂志,2019;20(6):1479。https://doi.org/10.3390/ijms20061479.
- 137.
魏勇,徐勇,陆鹏,王旭,李忠,蔡旭,等。野生棉花品种对盐胁迫的反应(Gossypium klotzschianum)基于转录组分析。PLoS One. 2017;12(5):e178313。
- 138.
张伟,王鹏,包忠,马强,段丽,包阿,等。SOS1 HKT1;5, NHX1协同调节盐生草中Na+的稳态Puccinellia tenuiflora.中国植物科学,2017;8:576。
- 139.
前岛M.液泡H .+焦磷酸酶。生物化学与生物物理学报(BBA)-生物膜。2000; 1465(1 - 2): 37-51。
- 140.
金海涛,林斌,李艳,等。重金属对水稻Na转录和酶活性的影响+/ K+-单齿轮虫中的atp酶,Brachionus koreanus.毒性环境与治疗科学,2016;8(2):128-34。https://doi.org/10.1007/s13530-016-0270-4.
- 141.
陈丽娟,陈丽娟,陈丽娟,陈丽娟,陈丽娟,陈丽娟烟草与在耐金属植物中观察到的相似。足底。2017;246(3):433 - 51。https://doi.org/10.1007/s00425-017-2700-1.
- 142.
杨晓明,杨晓明,杨晓明,等鹅膏strobiliformis在cu/ag输运中具有独特的性质。前沿微生物,2018;9:747。https://doi.org/10.3389/fmicb.2018.00747.
- 143.
León-Torres A, Arango E, Castillo E, Soto CY. CtpB是一种输送结核分枝杆菌p型atp酶的质膜铜(I)。生物学报2020;53(1):1 - 13。
- 144.
López M, Quitian L, Calderón M, Soto C. p型atp酶CtpG优先转运Cd2 +在整个结核分枝杆菌等离子体膜。中国微生物学杂志,2018;200(3):483-92。https://doi.org/10.1007/s00203-017-1465-z.
- 145.
Finn RD, Clements J, Eddy SR. HMMER web服务器:交互式序列相似性搜索。Nucleic Acids res 2011;39(suppl_2): W29-37。
- 146.
拉金MA, Blackshields G, Brown NP, Chenna R, McGettigan PA, McWilliam H,等。Clustal W和Clustal X 2.0版本。生物信息学。2007;23(21):2947 - 8。https://doi.org/10.1093/bioinformatics/btm404.
- 147.
库马尔S, Stecher G,李M, Knyaz C, Tamura K. MEGA X:基于计算平台的分子进化遗传学分析。中国生物医学杂志,2018;35(6):1547-9。https://doi.org/10.1093/molbev/msy096.
- 148.
Yu G.使用ggtree在树状结构上可视化数据。生物信息学学报。2020;69(1):e96。https://doi.org/10.1002/cpbi.96.
- 149.
MapChart:用于链接映射和qtl的图形化表示的软件。中国科学(d辑)。2002;29(1):1 - 8。https://doi.org/10.1093/jhered/93.1.77.
- 150.
王东,张勇,张震,朱军,于军。KaKs_Calculator 2.0:一个包含gamma系列方法和滑动窗口策略的工具箱。生物信息学。2010;8(1):77-80。https://doi.org/10.1016/s1672 - 0229 (10) 60008 - 3.
- 151.
陈超,陈宏,何勇,夏荣。TBtools是一种集成了各种生物数据处理工具的生物学家工具包,具有友好的用户界面。BioRxiv。2018年,289660年。https://doi.org/10.1101/289660.
确认
我们非常感谢张冰冰提供的技术援助。
资金
国家重点研发计划(2016ZX08005004-005)资助。资助机构没有参与这项研究的设计;数据的收集、分析或解释;或者是手稿写作。
作者信息
从属关系
贡献
WY和QW构想了本研究;XL和XC准备植物材料;LZ和MH进行实验和数据分析;SW, YZ和YF进行了生物信息学分析。QW撰写稿件;WY修改了手稿。所有作者均已阅读并批准稿件。
相应的作者
道德声明
伦理批准并同意参与
不适用。
发表同意书
不适用。
相互竞争的利益
作者宣称他们没有竞争利益。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
附加文件1
:图S1。qRT-PCR表达谱HMAD300 mM Na处理与对照之间的基因差异2所以4在根、茎和叶之间。31的表达模式HMAD中9835基因在对照组和处理组之间的差异。采用qRT-PCR方法分析31个基因的相对表达量HMAD根、茎、叶中的基因。R代表根,S代表茎,L代表叶。CK_R表示根与控制,SS_R表示根与处理。CK_S表示带对照的茎干,SS_S表示带治疗的茎干。CK_L表示有对照的叶子,SS_L表示有处理的叶子。
附加文件2
:图S2。的共线性分析HMAD基因之间的G.barbadense而且G.hirsutum.A01-A13代表At亚基因组染色体,D01-D13代表Dt亚基因组染色体。阿拉伯数字(1-3)在G.hirsutum在bars中分别表示scaffold4952, scaffold11408, scaffold13298。
附加文件3
:图S3。表达水平HMAD不同组织中的基因和不同的压力。热图是根据来自网站(http://structuralbiology.cau.edu.cn/gossypium/).颜色条表示表达式值。颜色刻度显示在图的右边。红色表示表达水平较高,绿色表示表达水平较低。
附加文件4
:表S1。HMAD蛋白的信息分为四种Gossypiumspp。
附加文件5
:表S2。顺式元件高表达基因分析。
附加文件6
:表S3。P1B-ATPases蛋白之间的信息Gossypium_hirsutum而且答:芥.
附加文件7
:表S4。本研究使用的qRT-PCR引物。
附加文件8
:表S5。转录组数据的信息HMAD300 mM Na处理与对照之间的基因差异2所以4.
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
王,Q.,陆,X.,陈,X.。et al。的全基因组鉴定和功能分析HMAD棉花基因家族(Gossypium仕达屋优先计划.).BMC植物生物学21日,386(2021)。https://doi.org/10.1186/s12870-021-03170-8
收到了:
接受:
发表:
关键字
- HMAD(heavy-metal-associated域)
- 逆境条件
- 棉(g .分子)
- 转录因子