摘要
背景
植物线粒体转录终止因子(mTERF)家族成员通过调控细胞器基因的表达,在植物发育和逆境耐受中发挥重要作用。然而,它们的分子功能尚未被明确定义。
结果
这是一个mTERF基因第十四节是通过使用条件白化突变体的精细定位确定的吗第十四节结果显示,白化病只发生在前两片真叶上,这一点通过转基因互补试验得到了证实。亚细胞定位和实时PCR分析表明第十四节编码一种在叶片中普遍表达的叶绿体蛋白,同时在第二真叶中穗化。植物白叶叶绿体基因表达谱分析第十四节通过实时PCR和Northern blotting分析发现,未处理的转录本异常积累rpoB-rpoC1和/或rpoC1-rpoC2反电子束间的区域伴随着成熟的丰度减少rpoC1和rpoC2这些转录本编码了质体编码的质体RNA聚合酶(PEP)的两个核心亚基。随后的免疫印迹分析证实RpoC1和RpoC2的积累减少。光诱导光合基因psbDmRNA和蛋白水平均下调。有趣的是,这种特定阶段的异常转录后调控和psbD高温(30 ~ 35℃)可逆转表达第十四节表达缺乏热敏性。与此同时,三个第十四节同源基因被发现具有相似的热诱导时间表达模式,暗示它们可能的功能冗余第十四节.
结论
这些数据揭示了V14在叶绿体发育中的关键作用,它以一种阶段特异性和热敏的方式影响着叶绿体对水分的适当处理rpoB-rpoC1-rpoC2某些光合作用蛋白的前体和表达。因此,我们的发现扩大了对水稻mterf分子功能的认识,并提出了植物mterf对光合作用建立和温度驯化的贡献。
背景
线粒体转录终止因子(mTERF)家族由一组核酸结合蛋白组成,所谓的mTERF重复序列约为31个氨基酸,形成三个螺旋[1,2].相似性搜索和系统发育分析表明,mTERF家族只存在于真核生物中,真菌除外[3.].所有这些蛋白质都被预测定位于线粒体和/或叶绿体。哺乳动物基因组只编码4个mterf (MTERF1-4) [4],而高等植物则有大约30个成员[5].哺乳动物mterf调节线粒体基因表达。人类MTERF1是第一个被发现的mTERF,其功能是在16S rRNA/leucyl-tRNA边界终止l-链转录[6],转录激活[7,8]和DNA复制[9],随后发现MTERF2在抑制复制叉进展中的作用[10], MTERF3在转录抑制、复制中的作用[11]和核糖体生物发生[12], MTERF4参与转录激活[13]和核糖体生物发生[14].相比之下,植物的mterf在调节细胞器基因表达方面的作用几乎不为人所知。在拟南芥的35个mterf中,11个是叶绿体定位的[15].SOLDAT10是高等植物中第一个表征的mTERF,参与胁迫驯化反应,影响16S、23S rRNA和ClpP蛋白酶mRNA的丰度[j]。16在叶绿体中。BSM (RUG2)以线粒体和叶绿体为目标,是维持转录本在这两个细胞器中不断积累所必需的[15,17],其中包括剪接clpPIIA族内含子[15].对另外两种叶绿体mterf mTERF5 (MDA1)和mTERF9 (TWIRT1)的对比分析表明,它们之间存在功能关系,它们在基因表达调控中具有一些共同的靶点,都对盐和渗透胁迫作出反应,并且都在功能上与质体编码的质体RNA聚合酶(PEP)相关[qh]18].此外,TWIRT1可能是质体核糖体稳定性和/或组装所必需的[19], MDA1正调控psbEFLJ作为转录暂停因子的转录[20.),刺激psbE和ndhA转录,并促进加工的5 '端稳定psbE和ndhA信使rna (21].最近的一份报告进一步发现psbJ在psbEFLJ多反流还涉及另一种与pep相关的mTERF,mTERF8 / pTAC15的3′末端区域特异性结合psbJ[22].除了对叶绿体mterf的研究外,还有两种线粒体mterf拟南芥mTERF18 (SHOT1)和mTERF15干扰耐热性逆行信号[23的拼接nad2intron-3 [24),分别。同时,一些研究也为植物mterf的作用方式提供了一些线索。Zm-mTERF4是玉米中的BSM同源物,直接结合某些叶绿体转录本中的II组内含子,并与一些已知的叶绿体剪接因子相互作用,从而促进这些转录本的剪接,包括trnI-高斯,trnA-用户原创内容,rpl2[25].后来,两次研究拟南芥mTERF6在体内展示了其dna结合活性,这是在特定位点终止转录所必需的trnI-高斯在3 '端rpoA叶绿体中的多顺子[26,27].最近,线粒体ZmSmk3被发现参与了剪接nad4内含子1和nad1玉米内含子4 [28],拟南芥mTERF9通过与16S和23S rnas相互作用,促进叶绿体核糖体组装和翻译[29].尽管取得了这些进展,但植物mTERFs调控细胞器基因表达的分子机制仍远未完全了解,也不清楚mTERFs是否参与细胞器多顺反子转录物的加工。此外,到目前为止,关于mterf对水稻叶绿体和线粒体发育的影响的信息还很少(o .漂白亚麻纤维卷L.),一种模式作物。
从蓝藻的祖先,叶绿体拥有许多基因组织在基因簇。叶绿体mRNA成熟包括前体转录、5′和3′端加工、顺反子间裂解、5′和3′端成熟和编辑、内含子去除等多个步骤[qh]30.].至少有两种不同的RNA聚合酶,PEP和核编码RNA聚合酶(NEP),在叶绿体发育的所有阶段和非绿色质体类型中负责质体基因转录[31].该基因编码PEP的α亚基,rpoA该基因与多个核糖体蛋白编码基因聚集在一起rpoA而编码PEP的β、β′和β″亚基的基因,rpoB,rpoC1,rpoC2,分别形成一个单独的操纵子。两者都是rpoA和rpoB操纵子由NEP [31,32,33另一方面,光合作用基因,如psbA,psbD,psaB都是依赖于pep的。PEP与大多数这些基因的启动子区域之间的关联在光照下显著增加[34].例如,光响应启动子在psbI和psbD在psbK-psbI-psbD-psbC操纵子,它负责双音的转录psbD-psbC.的上游还有两个标准PEP启动子psbK和光反应启动子分别产生五种不同的重叠转录本,包括psbK-psbI-psbD-psbC,psbK-psbI,psbD-psbC[35].的光致psbD-psbC在黑暗中是无法察觉的,在绿色的水稻幼苗中大量积累[35].
在这里,我们描述了水稻mTERF, V14,对适当的顺反子间切割的影响rpoB-rpoC1-rpoC2叶绿体的前体和某些光系统蛋白质的积累,如PsbD,在幼苗叶片发育的早期阶段。有趣的是,这种调节模式是生长阶段特异性和温度敏感的。因此,我们认为V14在叶绿体发育和温度适应中起着重要作用。
结果
V14是一种对叶片早期发育至关重要的叶绿体蛋白
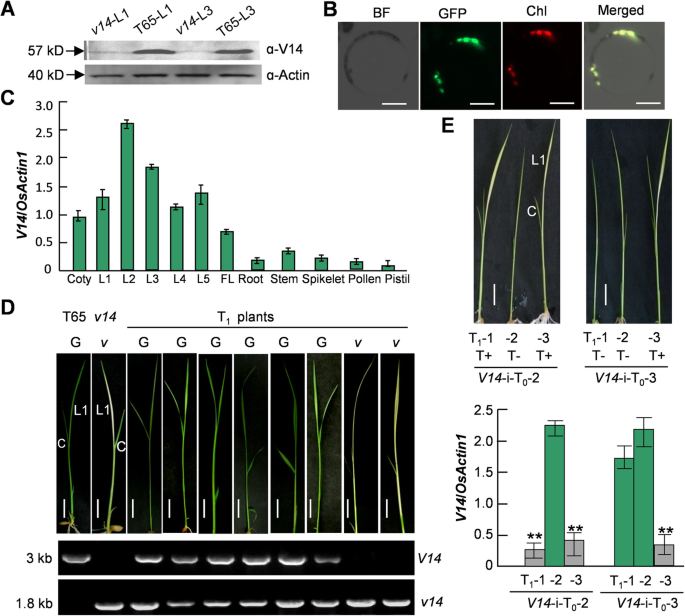
的第十四节先前使用分期条件法将位点定位为7号染色体上一个162kb的区域淡绿色的-14(第十四节台中65突变体(T65), a粳稻品种(36].该突变体在25°C时在头两片真叶中发生白化,此后返回绿色[30.].随后的精细映射缩小了范围第十四节位点到一个包含两个蛋白质编码基因的30kb区域(附加文件)1)。其中之一,Os07g0583200,突变体的启动子和5 '非翻译/编码区(−1245 ~ + 38)缺失1283 bp [36].的确,缺乏Os07g0583200信使rna (36]及其蛋白产物(图2)1A)被观察到第十四节.该基因编码一种假定的叶绿体蛋白(Refseq,https://www.ncbi.nlm.nih.gov),在水稻叶片原生质体中证实了其叶绿体定位Os07g0583200融合eGFP构造(图。1B,这些数据表明Os07g0583200是一个强有力的候选人吗第十四节轨迹。该基因的转录本在叶片的所有分析阶段都被观察到(图2)。1C),它们的产物在C端有7个连续的mTERF重复[36], Refseq将其注释为rice MTERF9。我们进一步进行了转基因互补和RNA干扰(RNAi)验证Os07g0583200代表了第十四节轨迹。白化基因在转基因基因中获得了成功的互补第十四节- t1携带细菌的植物Os07g0583200含-的片段及其原生启动子(图2)1D)第十四节在RNAi表达下调的植株中再现了类似表型Os07g0583200表达式(无花果。1E)第十四节到这个基因。
V14对幼苗早期叶片发育至关重要。一个维生素V14缺乏第十四节通过免疫印迹分析证实了突变体的存在第十四节.BV14融合EGFP在叶绿体中表达的绿色荧光表明V14的叶绿体定位。BF,亮场;Chl,叶绿素自身荧光(红色);Bar = 10 μM。C的表达第十四节在不同的器官和不同的发育阶段。科蒂,子叶;l1 ~ l5,第1 ~第5片真叶;FL,旗叶。D的补充第十四节表型分析证实突变体第十四节-和第十四节-特异性PCR1植物。G,绿色;v,淡绿色。未裁剪的凝胶图像在附加文件中提供1B.棒材= 0.5 cm (E)复制第十四节T细胞的类似表型1二代独立第十四节表型分析和基因表达分析证实了这一点第十四节中存在。Bar = 0.5 cm。通过学生实验分析了T+(含转基因)植株与T-(不含转基因)植株的显著性差异t测试(n= 3)。*,P< 0.05;**P< 0.01。(一个)及(B),这里的数据是三个独立实验的代表性图像。(C)及(E),这里显示的相对表达水平是三个独立实验的平均值
V14通过转录后前体分裂维持叶绿体的功能
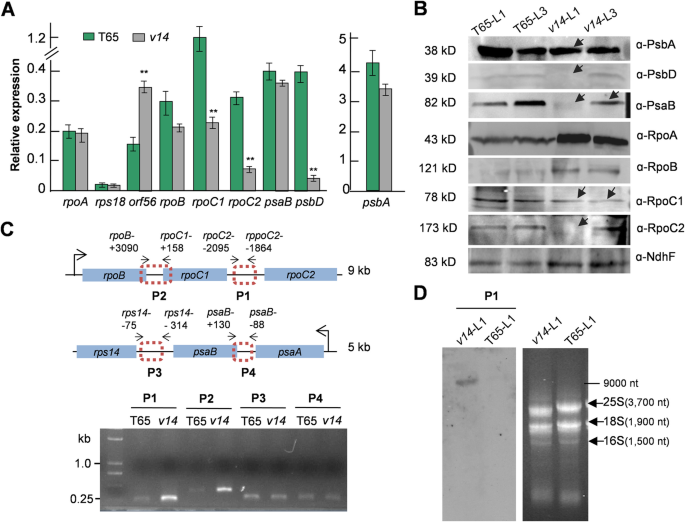
我们的先验知识第十四节表明在前两个真叶中叶绿体发育停止,从成熟的类囊体和淀粉粒的缺失可以明显看出[36].因此,我们假设转录缺陷存在于褪绿叶片的叶绿体中。为了确定受影响的叶绿体基因,我们首先使用qRT-PCR来评估第十四节第一片真叶中所有62个叶绿体基因的转录丰度均为T65。结果显示基因表达显著变化(最小2倍)第十四节与野生型T65相比,前者涉及编码PEP的β ' -和β " -亚基的两个基因,rpoC1和rpoC2光合作用基因psbD以及水稻独有的基因orf56[37,38编码截断的NdhH [39(图。2A)成绩单rpoC1,rpoC2,psbD在第十四节,同时orf56表达上调(图2)。2A).进一步对编码序列重叠区域进行半定量RT-PCR分析psbD和psbC揭示了它的缺席第十四节(附加文件2A,确认…的显著减少psbD信使rna。考虑到核编码的sigma因子在PEP激活中的重要作用,我们还利用qRT-PCR分析了所有5个sigma因子的表达。结果表明,它们都没有受到V14缺乏的影响2B).随后的免疫印迹分析证实了RpoC1、RpoC2和PsbD蛋白缺乏第十四节(无花果。2B、附加文件2C)。此外,用市售抗体评估了其他一些光合蛋白的蛋白质水平。我们发现另外两种光系统蛋白PsbA和PsaB也减少了第十四节(无花果。2B、附加文件2C),尽管它们的转录本丰度没有变化(图2)。2相比之下,RpoA和RpoB在第十四节比T65(图1)。2B、附加文件2C).这可能归因于在细菌中观察到的翻译的反馈抑制[40].
V14影响晶体的顺电子间裂解rpoB-rpoC1-rpoC2前体,psbD转录本丰度,以及幼苗发育早期PsbA和PsaB的积累。一个25°C培养的幼苗(L1)中叶绿体基因的qRT-PCR表达分析稳定表达的叶绿体基因psbE用于归一化。只有基因在第十四节这里显示了一些“未改变”的基因。与T65比较,差异有统计学意义t测试(n =3)。*,P< 0.05;**P< 0.01。B用市售抗体对L1和L3的叶绿体蛋白进行免疫印迹分析。箭头表示蛋白质减少或没有积累。以稳定表达的质体蛋白NdhF作为内参。C前体细胞转录本的异常积累覆盖了两个顺子间区(P1和P2)rpoB-rpoC1-rpoC2在L1(25°C生长)中第十四节半定量RT-PCR(31个循环)显示。结果表明:P3和P4为顺子间区psaA-psaB-rps14作为对照。引物的位置是相对于下游orf的起始密码子或它们所在的位置来指定的。D未加工前体的积累明显增加rpoB-rpoC1-rpoC2在L1中第十四节与T65相比,北方杂交显示。L1和L3,分别是第一个和第三个真叶。(B), (C),及(D),这里展示的图像是三个生物重复序列的代表
接下来,我们分析了V14如何影响叶绿体中的mRNA水平。我们注意到V14靶基因与其他非靶基因组织在共转录基因簇中。鉴于玉米Zm-mTERF4在内含子剪接中的作用[25],我们假设V14可能干预前体切割或RNA稳定。为了探索V14的行为,从多反电子的两个反电子间区(P1和P2)的丰度rpoB-rpoC1-rpoC2前体(无花果。2C)用半定量RT-PCR方法分析了苜蓿的前两片真叶第十四节和T65,利用来自多顺反子的两个顺反子间区(P3和P4)psaA-psaB-rps14前体(无花果。2C)作为控制。我们发现,褪绿的叶子拥有更多的未加工转录本,包括rpoB-rpoC1和/或rpoC1-rpoC2与野生型相比(图2)。2C、附加文件2P3和P4区未见明显变化第十四节(无花果。2C、附加文件2D).使用P1作为Northern杂交的探针,我们还检测到一个约9-kb的前体转录物含有rpoB,rpoC1,rpoC2只有在第十四节(无花果。2D)。
综上所述,这些数据反映了V14对多反顺子的适当反顺子间裂解的影响rpoB-rpoC1-rpoC2和psbDmRNA, PsbA和PsaB的积累。考虑到光在光合作用建立的第一阶段调控PEP组分的表达psbDmRNA、PsbA和PsaB丰度[41,42,43,44], V14可能通过叶绿体发育在光信号传导中发挥关键作用。
的白化表型第十四节依赖于温度
类似于之前报道的三种温度条件水稻嫩芽[45],第十四节在30°C和35°C的允许温度下,叶片发育为绿色。3.A).为了确定在高温下的完全恢复,我们首先评估了rpoC1,rpoC2,psbD在第一片真正的叶子里第十四节生长在25°C和35°C的植物。RT-PCR分析显示,这些转录本在35°C时的丰度可以达到与T65中对应转录本相当的水平(图5)。3.B).事实上,两个顺子间区域的适当切割rpoB-rpoC1-rpoC2是绿色回收的吗第十四节植物(附加文件)3.)。我们进一步评估了叶绿体的功能第十四节通过测量第一、第二和第三真叶的Fv/Fm比率(最大光合量子产量)(代表光系统II效率的测量),在35°C下生长的植物。与…的恢复一致rpoC1,rpoC2,psbD, 35℃生长时记录的Fv/Fm值第十四节在25°C或35°C条件下生长的植株与t65的植株没有显著差异(图2)。3.C)。相比之下,25°C的生长第十四节植物仍然不能完全恢复第三片叶子的光合作用,即使它们返回绿色。3.C)。有趣的是,第十四节mRNA在T65中的表达既不具有热敏性,也不具有分期特异性,尽管在第二个真叶中相对较高(图2)。1C,3.D)。
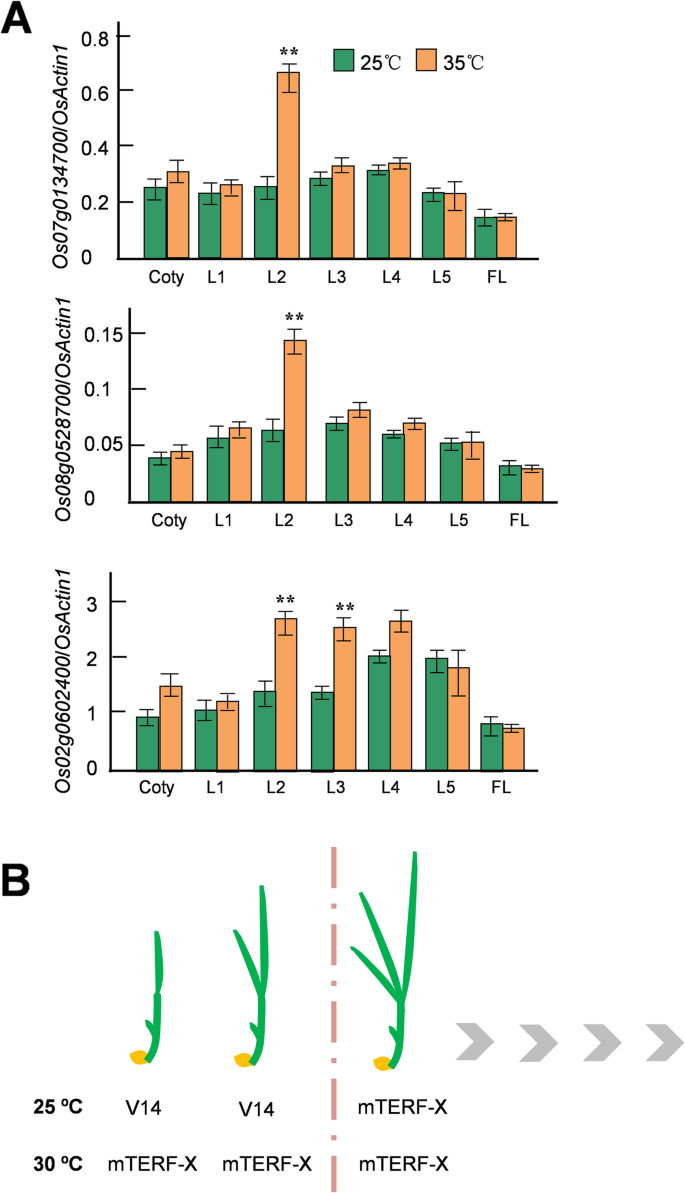
因此,我们假设可能有未知的V14平行因子在高温下作用,而V14是不活跃的。我们在NCBI上进行相似度搜索,在水稻中发现了另外30个v14同源物(附加文件)4)。对这些基因在25°C和35°C培养的t65中的表达分析表明,Os07g0134700,Os08g0528700,Os02g0602400,在第2真叶中,在35°C时显著上调第十四节表达达到峰值(图2)。4A、附加文件5,6和7)。Os07g0134700和Os02g0602400预测编码叶绿体mterf(分别被Refseq标注为水稻MTERF2和MTERF5同源物),而Os08g0528700编码一种无注释的mterf样蛋白。
讨论
mTERF家族得名于其创始成员人类MTERF1 [6],作为一组转录终止因子,但更多的分子功能已与它联系起来,如转录起始、DNA复制和内含子剪接。我们在这里提出的数据扩展了对mterf的分子功能的理解,它可能调节多顺反子前体的顺反子间裂解。我们证明了V14是适当的顺电子间裂解所必需的rpoB-rpoC1-rpoC2前体,从而调节成熟的丰度rpoC1和rpoC2编码PEP两个核心亚基的mrna。的表达式rpoB然而,它不是V14的目标。自rpoB是和rpoC1和rpoC2NEP [31,32,33],这一结果表明,V14特异性调节前体加工,而不是前体转录rpoB-rpoC1-rpoC2操纵子。尽管成熟的表达减少了rpoC1和rpoC2mrna在第十四节, pep依赖基因的表达不受影响,除了psbD这表明前质体中低水平的PEP可以维持大多数这些基因的表达。这一观察结果与小麦幼苗中PEP转录的发育和基因特异性调控一致[43].在发育的叶绿体中,不依赖光的PEP在黑暗和光照下都起作用,包括PEP依赖基因psbA,psbC,psbE,rrn16,除了…psbD,而依赖光的PEP则选择性地进行转录psbA和psbD在成熟叶绿体中[43].产生前体的光响应启动子,包括psbD和psbC也已确定在psbK-psbI-psbD-psbC基因簇[46].考虑psbC无表情变化第十四节当与共同转录时psbD,我们推测V14可能是至关重要的psbDmRNA的光依赖性稳定性。我们还注意到,其他两种光系统蛋白PsbA和PsaB也因为V14缺乏而减少,即使它们的转录物丰度没有改变,这可以解释为由V14编码的蛋白的翻译和稳定性受到影响psbA和psaB在叶绿体发育过程中是依赖光的[41].此外,在拟南芥中建立的光响应模型表明,光信号先于质体信号,其中光合作用建立的第一阶段依赖于光并触发启动叶绿体发育的变化,更重要的是启动PEP组分的表达[47].该模型支持的受损处理rpoB-rpoC1-rpoC2的前体和减少的积累psbD, PsbA和PsaB在第十四节表明V14对叶绿体发育过程中的光信号传导至关重要。V14可能不会直接作用于它的分子靶标,比如rpoB-rpoC1-rpoC2前体,但在叶绿体发育过程中引入这些变化的关键步骤中受到干扰,需要进一步研究。
我们证明了第十四节被更高的温度拯救了,并且有缺陷的反电子间裂解rpoB-rpoC1-rpoC2前驱体是温度相关的(图2)。3.B、附加文件3.)。然而,的表达第十四节野生型本身对温度不敏感(图2)。3.D).考虑到V14可能通过植物激素介导的热感通路起作用[48,49,我们研究了的反应第十四节幼苗对各种植物激素处理(附加文件8)。然而,这些处理都不能恢复在25°C下观察到的白化,这表明第十四节对植物激素无反应。我们进一步鉴定了三个mTERF基因,显示出类似的时间表达模式第十四节在第二叶的高温下显著上调(图2)。4A),这表明这些基因可能是未知的V14平行体的潜在候选者,其功能弥补了高温下V14的缺乏。这些数据支持这样一种观点,即植物进化出了功能冗余的基因家族成员,其中某些成员可以以有条件的方式被其他成员取代。
结论
V14是叶绿体中支持前两片真叶叶绿体生物发生的重要转录和翻译调节因子。而第十四节表达既不具有阶段特异性,也不具有热敏性,v14介导的调控受到发育阶段和温度的严格调节(图2)。4B). V14在叶绿体发育中的作用刚刚开始显现。需要进一步研究V14在顺胞间裂解、mRNA稳定性和翻译/翻译后调控中的分子功能,并确定这些调控如何响应温度,从而有助于了解细胞器基因表达对光合作用建立和温度驯化的贡献。
方法
植物材料及处理
T65的种子来自华南农业大学庄楚雄博士的实验室。幼苗在生长室中生长,在25°C下光照16 h /黑暗8 h。的位置映射的详细信息第十四节基因座已在先前的研究中提供[36].对于温度处理,幼苗在25°C、30°C和35°C的光照/黑暗周期下生长16 h /8 h。
eGFP融合的细胞内定位
对于eGFP可视化,cDNA片段第十四节使用引物V14-xho5和V14-spe3从T65中获得(附加文件9),并与的编码序列融合eGFP在基于puc18的向量中创建该构造p35区域::第十四节-eGFP.然后按照先前描述的程序将该结构体瞬间转化为水稻叶片原生质体[50].使用激光共聚焦扫描显微镜,在500 ~ 550 nm (eGFP荧光)和670 ~ 750 nm(叶绿素自身荧光)范围内采集图像,显微镜装有40 ×水浸物镜(7 DUO;蔡司)。
遗传转化
的互补试验第十四节使用引物V14P5和V14P3从T65基因组DNA中扩增出包含启动子、基因体和914bp 3 ' UTR区域的基因组片段(附加文件)9使用Gibson Assembly®Master Mix (New England Biolabs)将其克隆到植物表达载体pCAMBIA 1380中。通过表型分析和PCR分析,证实了互补的成功第十四节-先前研究中描述的特异性引物[36].对于一代第十四节利用两对引物从T65中获得cDNA片段(附加文件9), V14i-5-1和V14i-3-1, V14i-5-2和V14i-3-2,并克隆到植物表达载体pCAMBIA 1301与Gibson Assembly®Master Mix。引入了互补结构第十四节通过农杆菌介导的转化将RNAi转入T65。
叶绿体隔离
叶绿体按先前发表的方法制备[51].简而言之,将10克新鲜的幼苗叶片冷冻在液氮中,轻轻磨成细粉。然后将粉末悬浮在100 ml Medium A (50 mM HEPES-KOH pH 8.0, 330 mM山梨醇,2 mM EDTA-Na)中2(5 mM抗坏血酸,5 mM半胱氨酸,0.05% BSA),通过两层纱布和两层Miracloth(默克)过滤悬浮液。将滤液离心(1300×g, 4℃,5 min)收集叶绿体微球,然后将微球悬浮在200 μl Medium B (50 mM HEPES-KOH pH 8.0, 330 mM山梨醇,2 mM EDTA-Na)中,进行蔗糖密度梯度离心(30、40、55%蔗糖密度梯度,30000×g, 4℃,1 h)2)。收集30%和40%蔗糖界面处的绿色条带,用75 mL Medium B离心(2000×g, 4°C, 15 min)冲洗两次。最后,用50 μl TRIzol™Reagent (ThermoFisher Scientific)重悬微球,提取RNA。
核酸提取、qRT-PCR、northern blot、免疫印迹
用DNeasy Plant Mini Kit (Qiagen)从叶片中分离基因组DNA。按照TRIzol®试剂的说明从叶片或叶绿体中提取总RNA。在逆转录之前应用DNase I (Invitrogen)酶切。为了评估核转录本的丰度,Oligo (dT)20.从叶片中提取总RNA,用50 μM (μM)合成第一链cDNA。为了评估所有叶绿体转录本的数量,用随机六聚体(50 ng/μL)从叶绿体中提取的总RNA合成第一链cDNA。核酸编码因子的引物见附加文件9.所有用于检测叶绿体转录本的引物序列列在附加文件中10,除放大顺子间区(P1-P4)外,其余重叠区psbD和psbC的下游地区psbC(附加文件2A),在附加文件中给出9.Northern blot分析使用之前发表的总RNA [52].探针P1用0.01 μM digoxigenin (DIG)-脱氧尿苷三磷酸进行PCR标记。为了提取蛋白质,幼苗叶片在2 × SDS样品缓冲液(62.5 mm Tris-HCl, pH 6.8, 20% [v/v]甘油,4% [w/v] SDS, 100 mm二硫苏糖醇,0.05% [w/v]溴酚蓝)中均质,95℃孵育5分钟,最高转速离心20分钟。样品被定量并进行SDS-PAGE(12%),然后湿转移到PVDF膜(Millipore)上。然后将膜与抗V14、RpoA、RpoB、RpoC1、RpoC2、PsbA、PsbD、PsaB或NdhF的抗体孵育。除V14抗体由Abmart公司以合成肽EGRQPKTRDRCD为免疫原制备外,其余抗体均来自华大基因。所有蛋白水平通过ImageJ归一化为NdhF,结果见附加文件2C。
叶绿素荧光分析
实验是按照先前公布的方案进行的[53做了一些小的修改。在用PAM荧光计(Walz)测量之前,每组6株植物适应黑暗20分钟。所有的测量都在白天的同一时间进行。饱和脉冲辐射(2700 μmol m)−2年代−1)记录最大荧光产率(Fm),弱调制辐射(0.5 μmol m)−2年代−1)测定最小荧光产率(F0)。最大光合量子产率计算为Fv(可变荧光产率)/Fm = (Fm- f)0) / Fm。
数据和材料的可用性
的序列第十四节突变体第十四节已分别在提交号MZ299153和MZ299154下存入NCBI。
缩写
- mTERF:
-
线粒体转录终止因子
- 动员:
-
质体编码的质体RNA聚合酶
- 棉结:
-
核编码RNA聚合酶
- 阵线:
-
可变荧光产率
- Fm:
-
最大荧光量
- F0:
-
最小荧光产率
- NCBI:
-
国家生物技术信息中心
参考文献
- 1.
张建军,张建军,张建军,等。人类线粒体mTERF通过左旋超螺旋串联重复序列包裹DNA。中华生物医学工程学报,2010;17(7):893 - 93。
- 2.
Yakubovskaya E, Mejia E, Byrnes J, Hambardjieva E, Garcia-Diaz M.螺旋解绕和碱基翻转使人类MTERF1终止线粒体转录。细胞。2010;141(6):982 - 93。
- 3.
Linder T, Park CB, Asin-Cayuela J, Pellegrini M, Larsson NG, Falkenberg M,等。在后生动物和植物中共有的一组转录终止因子。现代医学,2005;48(4):265-9。
- 4.
robert M, Polosa PL, Bruni F, Manzari C, Deceglie S, Gadaleta MN,等。MTERF家族蛋白:线粒体转录调节因子及其他。生物化学学报,2009;17(5):303-11。
- 5.
拟南芥mTERF蛋白的进化与功能分类。植物科学,2012;3:233。
- 6.
李建军,张建军,张建军,等。线粒体转录终止机制的研究进展。细胞。58 1989;(2):391 - 7。
- 7.
李建军,李建军,李建军,等。人线粒体转录终止因子(mTERF)的单-三聚体转化与体外活性丧失相关。生物化学学报,2004;29(5):1567 - 1567。
- 8.
马建军,赵杰,李建军,等。线粒体rRNA合成中终止因子介导的DNA环。细胞。2005;123(7):1227 - 40。
- 9.
Hyvarinen AK, Pohjoismaki JL, Reyes A, Wanrooij S, yasawa T, Karhunen PJ,等。线粒体转录终止因子mTERF调节人类线粒体DNA的复制暂停。核酸学报,2007;35(19):6458-74。
- 10.
李建平,李建平。植物和哺乳动物基质蛋白的研究进展。生物化学学报,2015;1847(9):786-97。
- 11.
Park CB, Asin-Cayuela J, Camara Y, Shi Y, Pellegrini M, Gaspari M,等。MTERF3是哺乳动物mtDNA转录的负调控因子。细胞。2007;130(2):273 - 85。
- 12.
Wredenberg A, Lagouge M, Bratic A, Metodiev MD, Spahr H, Mourier A,等。MTERF3调节无脊椎动物和哺乳动物线粒体核糖体的生物发生。生物医学工程学报,2013;9(1):e1003178。
- 13.
Camara Y, Asin-Cayuela J, Park CB, Metodiev MD, Shi Y, Ruzzenente B,等。MTERF4通过靶向甲基转移酶NSUN4到哺乳动物线粒体核糖体来调节翻译。中华医学杂志,2011;13(5):527-39。
- 14.
Spahr H, Habermann B, Gustafsson CM, Larsson NG, Hallberg BM。调节线粒体核糖体生物发生的人MTERF4-NSUN4蛋白复合物的结构。中国科学:自然科学版,2012;39(5):563 - 563。
- 15.
Babiychuk E, Vandepoele K, Wissing J, Garcia-Diaz M, De Rycke R, Akbari H,等。质体基因的表达和植物的发育需要线粒体转录终止因子家族的质体蛋白。中国科学:自然科学版,2011;38(6):673 - 679。
- 16.
李建军,刘建军,李建军,等。拟南芥mterf相关质体蛋白SOLDAT10的突变激活逆行信号传导并抑制(1)O(2)诱导的细胞死亡。植物学报,2009;36(3):391 - 391。
- 17.
Quesada V, sammiento - manus R, Gonzalez-Bayon R, Hricova A, Perez-Marcos R, Gracia-Martinez E,等。拟南芥RUGOSA2编码线粒体、叶绿体和叶片发育所需的mTERF家族成员。植物学报,2011;38(4):738 - 738。
- 18.
王晓明,王晓明,王晓明,等。植物保守基因MTERF9突变对拟南芥叶绿体基因表达、发育及对非生物胁迫的耐受性的影响。植物物理学报,2015;39(2):357 - 357。
- 19.
刘建军,张建军,张建军,等。拟南芥mTERF5和mTERF9基因在耐盐性、质体基因表达和逆行信号传导中的功能分析。植物生物学(Stuttg)2020; 22(3): 459 - 71。
- 20.
丁松,张燕,胡忠,黄霞,张斌,陆青,等。mTERF5作为转录暂停因子正向调控叶绿体psbEFLJ的转录。植物学报,2019;12(9):1259-77。
- 21.
m - meerhoff K,齐默曼A, Chicher J, Baumberger N,等。拟南芥mTERF-repeat MDA1蛋白在转录和稳定特定叶绿体转录物中具有双重功能psbE和ndhH操纵子。中国生物医学工程学报,2014;22(5):1376 - 1391。
- 22.
熊宏斌,王军,黄超,Rochaix JD,林凤峰,张建新,等。线粒体转录终止因子家族成员mTERF8参与叶绿体基因的转录终止psbJ.植物生理学报,2014;32(1):448 - 456。
- 23.
金美,李宇,李晓明,等。拟南芥线粒体转录终止因子相关蛋白基因的克隆与表达。植物学报。2012;24(2):349 - 356。
- 24.
徐艳伟,王海军,谢明辉,谢海龙,焦光远。拟南芥mTERF15是线粒体nad2内含子3剪接和功能性复合体I活性所必需的。科学通报,2014;9(11):e112360。
- 25.
张建军,张建军。玉米叶绿体II族内含子剪接中mTERF结构域蛋白的功能。核酸学报,2014,42(8):5033-42。
- 26.
罗文辉,马纳夫斯基,莫洛塞蒂,李建平,等。拟南芥线粒体转录终止因子家族的一个成员是叶绿体转移RNAIle (GAU)成熟所必需的。植物生理学报,2015;32(1):444 - 444。
- 27.
张勇,崔玉玲,张晓玲,于启波,王旭,袁晓波,等。核编码蛋白mTERF6介导rpoA多顺子的转录终止,用于质体编码RNA聚合酶依赖的叶绿体基因表达和叶绿体发育。科学通报,2018;8(1):1 - 9。
- 28.
潘志,任鑫,赵慧,刘玲,谭忠,邱峰。玉米nad1内含子4和nad4内含子1剪接与籽粒发育所需的线粒体转录终止因子ZmSmk3。G3(贝塞斯达)。2019; 9(8): 2677 - 86。
- 29.
刘建军,刘建军,刘建军,等。拟南芥mTERF9蛋白通过建立核糖-核蛋白相互作用促进叶绿体核糖体组装和翻译在活的有机体内.中国生物医学工程学报,2011;49(2):1114-32。
- 30.
Stern DB, Goldschmidt-Clermont M, Hanson MR.叶绿体RNA代谢。植物学报,2010;31(1):444 - 444。
- 31.
Börner T, Aleynikova AY, Zubo YO, Kusnetsov。叶绿体RNA聚合酶:在叶绿体生物发生中的作用。生物化学学报,2015;1847(9):761-9。
- 32.
王晓明,王晓明,王晓明,等。小麦叶绿体转录组的研究进展。小麦叶绿体转录组的研究进展。植物学报,2012;24(1):123-36。
- 33.
张建军,张建军,张建军,等。RNA聚合酶复合物在基因表达中的作用。植物生理学报,2014,32(1):379 - 379。
- 34.
李建军,李建军,李建军,等。叶绿体DNA与RNA聚合酶的关系。植物学报,2013;36(5):849 - 856。
- 35.
陈绍光,卢建辉,程曼敏,陈丽丽,罗鹏鹏。水稻质体的4个启动子psbK-psbI-psbD-psbC操纵子。植物科学,1994;99(2):171-82。
- 36.
张强,薛东,李霞,龙勇,曾霞,刘勇。水稻一个新的翠绿突变体的鉴定和分子定位。基因工程学报,2014;41(6):353 - 356。
- 37.
Hiratsuka J, Shimada H, Whittier R, Ishibashi T, Sakamoto M, Mori M,等。米饭的完整序列(选用satira)叶绿体基因组:不同tRNA基因之间的分子间重组是谷物进化过程中质体DNA反转的主要原因。中华生物医学工程学报,2009;22(2):393 - 394。
- 38.
Shimada H, Sugiura M.叶绿体基因组的精细结构特征:序列叶绿体基因组的比较。核酸学报,1991;19(5):983-95。
- 39.
Kanno A, Hirai A.水稻叶绿体基因组的转录图谱。现代医学,1993;23(2):166-74。
- 40.
鲻鱼我。叶绿体转录的动态调控。植物生理学报,1993;43(2):394 - 394。
- 41.
甘布尔PE,穆雷特JE。质体编码蛋白的翻译和稳定性psbA和psbB大麦光诱导叶绿体发育过程中,基因受一个核基因调控。生物化学学报,1989;26(3):756 - 756。
- 42.
陈国光,程明,钟坤,于宁,陈明。水稻叶绿体的表达psaA -psaB -石头剪刀L4基因簇。植物科学,1992;81(1):93-102。
- 43.
李建军,李建军,李建军,李建军。小麦发育阶段特异性多亚单位质体RNA聚合酶的研究进展。植物学报,1999;18(4):407 - 915。
- 44.
Hernández-Verdeja T, Strand Å。逆行信号引导叶绿体发育的路径。植物生理学报,2018;36(2):967-76。
- 45.
Iba K, Takamiya KI, Toh Y, saoh H, Nishimura M.水稻绿色突变体叶片发育有限阶段功能活性叶绿体的形成。生物医学进展。1991;12:342-8。
- 46.
许鲁巴,王国华,魏思福。高粱绿苗质体基因表达的转录调控。足底。1991;183(1):101 - 11所示。
- 47.
Dubreuil C, Jin X, Barajas-Lopez JD, Hewitt TC, Tanz SK, Dobrenel T,等。通过叶绿体发育建立光合作用受两个不同的调控阶段控制。植物生理学报,2018;36(2):1199 - 1214。
- 48.
李宁,尤令东,查建勇,林志,陆明志,黄立军,等。植物激素对全球气候变化的耐热性调控。植物科学,2021;11:627969。
- 49.
8 .高油菜素内酯对盐和温度诱导的氧化应激的调控作用芸苔属植物juncea.科学通报,2018;8(1):835。
- 50.
张勇,苏军,段生,敖勇,戴军,刘军,等。水稻绿色组织原生质体的瞬时基因表达及光/叶绿体相关过程研究植物学报,2011;7(1):30。
- 51.
van Wijk KJ, Peltier JB, Giacomelli L.拟南芥叶绿体蛋白的分离及其蛋白质组学分析。方法:中华生物医学杂志。2007;35(3):43 - 8。
- 52.
Kazama T, Nakamura T, Watanabe M, Sugita M, Toriyama K. Rf1蛋白抑制bt型雄性不育水稻线粒体ORF79积累的机制。植物科学进展,2009;35(4):559 - 561。
- 53.
蔡玉春,陈克春,程天成,李超,林世生,董超。不同水稻品种的叶绿素荧光分析表明,幼苗耐盐性与光合效率呈正相关。植物学报,2019;19(1):403。
致谢
不适用。
资金
本研究得到农业部转基因研究国家重点项目(2016ZX08009002-003)、广东省自然科学基金(2015A030313414)和广州市科技计划(201607010196)的资助。
作者信息
从属关系
贡献
孟文、方志、洪伟、德旭:进行实验和数据分析;Q. Z.和Y. L.:构思项目和撰写手稿。所有作者都审阅了手稿。作者阅读并批准了最后的手稿。
相应的作者
道德声明
伦理批准并同意参与
不适用。
发表同意书
不适用。
相互竞争的利益
不适用。
额外的信息
出版商的注意
施普林格·自然对已出版的地图和机构关系中的管辖权要求保持中立。
补充信息
附加文件1。
(A)精细映射第十四节7号染色体上的位点。虚线表示启动子和5 '非翻译区和编码区(−1245 ~ + 38)的基因组缺失第十四节突变体。箭头表示检测内源和转基因片段的引物第十四节和第十四节如图所示。1D. (B)补充第十四节由第十四节-和第十四节-特异性PCR1植物。
附加文件2。
分析psbD-含转录本的半定量RT-PCR(31个循环)(A),水稻sigma因子的qRT-PCR表达分析(B),免疫印迹定量分析如图所示。2B通过ImageJ (C),并分析了两个顺电子间区(P1和P2)rpoB-rpoC1-rpoC2在第二个真叶(生长在25°C)第十四节通过半定量RT-PCR(31个循环)(D)、(A),引物的位置是相对于它们所在orf的起始密码子指定的。(B),与T65相比,通过t测试(n= 3)。(C),所有蛋白水平归一化为NdhF。(D),的两个顺子间区(P3和P4)psaA-psaB-rps14作为对照。(A)和(D),这里展示的图像是三个生物重复的代表。
附加文件3。
高温(35℃)恢复了两个顺电子间区(P1和P2)的解理rpoB-rpoC1-rpoC2的L1前体第十四节.半定量RT-PCR进行31个循环。L1,第一片叶子。P3和P4是两个间隔区域psaA-psaB-rps14操纵子如图所示。2C.这里呈现的图像是三个生物重复序列的代表。
附加文件4。
水稻V14基因的系统发育分析。利用philip软件(3.66版)在蛋白质序列上构建邻居连接树,并使用TreeView和MEGA5软件进行可视化。箭头表示在第二叶中温度敏感表达的三个基因(图2)。4)。
附加文件5。
其他27人的基因表达谱第十四节-同源基因在25°C和35°C下叶片发育的不同阶段。这里显示的相对表达水平是三个独立实验的平均值。
附加文件6。
其他27人的基因表达谱第十四节-同源基因在25°C和35°C下叶片发育的不同阶段。这里显示的相对表达水平是三个独立实验的平均值。
附加文件7。
其他27人的基因表达谱第十四节-同源基因在25°C和35°C下叶片发育的不同阶段。这里显示的相对表达水平是三个独立实验的平均值。
附加文件8
第十四节不同植物激素处理的幼苗在25°C下生长。棒材= 0.5 cm;L1,第一片真叶;L2,第二个真叶结点。
附加文件9。
引物序列的互补,RNAi,和加工中间体的评估。
附加文件10。
叶绿体基因转录物mRNA表达谱的引物序列。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域免责声明(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文中提供的数据,除非在数据的信用额度中另有说明。
关于本文
引用本文
王,M.,周,F.,王,H.M.et al。水稻mTERF蛋白V14在幼苗早期叶片中维持光合作用的建立和温度驯化。BMC Plant Biol21日,406(2021)。https://doi.org/10.1186/s12870-021-03192-2
收到了:
接受:
发表:
关键字
- mTERFs
- rpoB-rpoC1-rpoC2操纵子
- 叶绿体发育
- 温度响应
- 大米