抽象的
背景
链生绿藻在细胞生长和细胞壁形成方面与它们的亲缘植物胚胎植物有一些共同的特点。多裂体的多裂细胞壁Micrasterias denticulata细胞分裂后对称重建并由果胶和纤维素组成,使得这种单细胞链光藻属藻类是一种有趣的模型系统,用于研究绿色植物中细胞形状和细胞壁形成的分子对照。
结果
同步生长细胞的基因组转录物表达分析鉴定了107个基因,其中表达与生长阶段相关。四个转录物与之前未在绿藻中检查的扩展素相似。系统发育分析表明,这些基因与植物扩展素密切相关,虽然他们的域组织非常不同。一种GFP标记的扩展素类似蛋白质MDEPP2,其定位于细胞壁和GOLGI衍生的囊泡。过度表达表型从叶伸长率延伸到生长极性和平面性的损失。这些结果表明MDEPP2可以改变细胞壁结构,因此,在细胞形态发生期间可能具有与土地植物扩展蛋白相关的函数。
结论
我们的研究证明了m . denticulata作为一个单细胞模型系统,其中发现细胞生长机制与土地植物中的那些相似。另外,提供证据,即胚胎中许多细胞壁组分的进化起源和胚胎中的调节基因在陆地上殖民化之前。
背景
虽然植物细胞的形式和功能强烈相关,但是确定细胞形状的过程仍然很大程度上是未知的。植物细胞形态发生在周围组织中以非细胞自主方式调节[1],在个体发生过程中的激素干扰,有时是由核内再复制的结果产生的多倍性[2,3.].相反,在陆地植物的单细胞亲属中,可以在不受相互作用细胞干扰的情况下研究细胞形态发生的内源性控制,并更好地了解这些机制在绿色谱系中的进化过程。
desmid.Micrasterias denticulata是接合绿藻(接合藻科)的一种,由陆生植物最接近的现存单细胞亲属组成[4- - - - - -8].m . denticulata细胞由两个双侧对称的平面半结晶组成,深入地缠绕在其周边中成一个极性叶和四个主要的侧瓣。在细胞分裂之后,每个半区通过隔膜凸出和对称局部生长停止的过程建立一个新的一个,以形成连续的叶片(图1).在初生细胞壁完成后(在双峰期),一个坚硬的纤维质次级细胞壁被小孔穿透,随后脱落。这种特殊的生长机制使Micrasterias研究细胞壁生物发生时空模式的理想模型[9].
形态发生的Micrasterias denticulata形态发生阶段在同步样品系列中的分布.(a)形态发生m . denticulata.(1)营养细胞。(2)有丝分裂时,起源于细胞壁带的隔向内生长,生长时间为15-20分钟。鼻中隔均匀膨大。(4)第一对压痕(箭头)显影,间隔完成后约75分钟。(5)分裂的阶段。(6)第二对压痕(箭头)的发展。(7) Five-lobed阶段。(8)侧叶重叠(箭头)。(9)进一步形成压痕和裂片尖端,接着是双棱阶段。 N, Nucleus. Note the migration of the nucleus during cell growth. Scale bar = 100 μm. (B) Scheme of the synchronization protocol. After 3-4 weeks, a stationary culture is obtained and the growth medium is refreshed, concomitantly with the reduction in cell density, shortly before the beginning of the light period of that day. The majority of the cells divide in the second dark period afterward. This dark period is replaced by a light period and sampled. Black, dark period; white, light period. (C), Distribution of morphogenetic stages in the RNA samples for cDNA-AFLP, replication 1. (D) Table representing the characteristics of the samples used for cDNA-AFLP (replications 1 and 2) and real-time qPCR.
最终,植物细胞的形态是由细胞壁的组成和结构决定的,细胞壁的组成和结构决定了细胞膨胀的方向和速率。和陆生植物一样,植物的初生细胞壁m . denticulata游客。主要由果胶组成[10,11,纤维素微纤维[12),半纤维素(13]和阿拉伯半乳聚糖蛋白[10,13].二次电池壁归因于源自由作为六边形阵列组织的玫瑰花丝的纤维素微纤维造成的纤维素[14,15],而混合连接的葡聚糖是主要的半纤维素[13].
在陆地植物中,扩展素是Turgor驱动的细胞壁膨胀的重要调节因素。这些细胞壁蛋白质包含大量的多烯烃,其由四个家族(expa,Expb,exla和exlb)组成,其中进化关系很好地表现出来[16,17].它们的独特之处在于能够通过破坏连接纤维素和半纤维素壁成分的氢键,以非酶的方式松开细胞壁[18- - - - - -21].土地植物扩展蛋白由两个域和分泌信号组成。N-末端扩展蛋白结构域1和C-末端扩展蛋白结构域2与糖苷水解酶家庭45(GH45)蛋白的催化结构域同源,以及在草花粉过敏原家庭中存在的域,被鉴定为推定的纤维素结合位点[22),分别。扩展局在组织开发中发挥作用[23,24]并且在悬浮培养细胞的生长中[25,26].尽管编码扩张蛋白样蛋白的基因最近已在绿藻转录组中被确认[27],其生理功能及与陆生植物扩展素的系统发育关系尚不清楚。
在这里,我们探索细胞形态发生和细胞壁形成同步的分子基础m . denticulata以cdna扩增片段长度多态性(cDNA-AFLP)为基础的定量转录组分析[28].鉴定了几种细胞壁相关基因,其中包括膨胀蛋白。膨胀蛋白的检查提供了该基因家族内的绿藻同源物的第一种结构,系统发育和功能数据。
结果
cDNA-AFLP表达分析
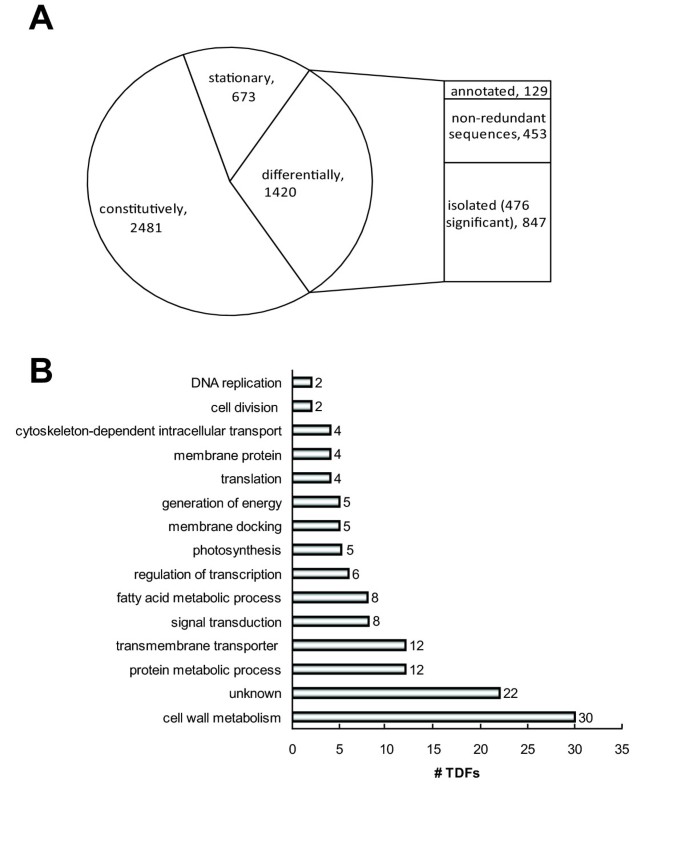
首先,我们开发了一种同步监控细胞形态发生相关基因表达的方案m . denticulata.该方案基于观察结果:在第二黑暗时期的14-H光/ 10-H暗时生长的大多数细胞在第二个黑暗时期除以固定培养的生长培养基(3-4周后获得)在光周期开始时,细胞密度被刷新并伴随着细胞密度。通过光周期替换暗时期,增强了同步分割细胞的量(图1 b).细胞密度对同步性有显著影响(GLM;F以及;P< 0.001),最佳细胞密度在80细胞mL以下-1.同步化后,高达85%的细胞群在8- 9小时内分裂,呈s形过程(图)1C,D;额外的文件1).通过在连续五个时间点进行对该时期进行抽样,我们在主要形态发生阶段的不同比例的细胞中获得样品(图1 a、C、D).这些样品的cDNA-AFLP表达分析允许将差异表达基因分配给细胞分裂的发作(图1 a2;数字2(C1A和C1B)),凸起(图1 a3;数字2(C2)),叶(图。1A4-A9;数字2(C3)),或二重体阶段,在此期间次级细胞壁形成(图2(C4和C5))。共监测了4574个转录衍生片段(TDFs)在细胞生长过程中的相对丰度m . denticulata(图3.额外的文件2),其中的表达模式在1420年随着时间的推移明显改变,且显著(P< 0.009;问<0.05)在476个TDF中。根据其他研究[29,30.,我们估计三分之二的mRNA群体被取样,这意味着在细胞生长过程中差异表达的基因的真实数量m . denticulata可以~ 2100。高度相似(e值< 1。有107个TDFs和22个TDFs与指定身份和未知或假设基因的数据库条目的相似性(E-01和相似性>50%),主要与胚胎植物有关,与绿藻无关。然而,大多数TDFs(324或71.5%)与任何数据库条目没有序列相似性(图3.;额外的文件3.).可粘合的解释可能是太短的,揭示了任何重要的身份,表示非保守部分的基因部分的短序列,源自基因的3'-未翻译区域的TDF,或表示特异性基因的TDFSm . denticulata或streptophytic藻类。
在129个注释的基因中,118个聚类为6个组(指定为C1a、C1b、C2、C3、C4和C5)(图1)2)根据他们最高表达的时间(图1C,D).除了一个由6个基因组成的簇(簇C1b;数字2),表达型材在两个独立的采样系列中可再现。不包括在所述簇之一中的少数基因通常显示出窄的时间表达模式。
基于它们的注释,TDFs被分为14个功能类别,按照基因本体术语(http://www.geneontology.org.)(图3.;额外的文件3.).功能分类与TDF聚类之间的相关性无统计学意义(χ2测试;p= 0.070)。受到重大打击的主要群体涉及细胞壁代谢。第二大类别对应于与未知或假想蛋白质具有显著相似性的序列。
在18个与涉及细胞壁生物发生或细胞模式形成的基因相似的TDFs中,第二个cDNA-AFLP复制序列的RNA样本和一个独立取样序列的RNA样本(附加文件)1通过实时定量逆转录(QRT)-PCR分析)分析。通常,通过cDNA-AFLP和QRT-PCR获得的表达谱(附加文件4)对应良好(附加文件5),确认获得的表达结果。
与细胞模式形成相关的基因
可以确定7个TDFs可能与细胞模式形成有关m . denticulata,其中Rab GTPase循环的2名成员和SNARE循环的2名成员进行膜融合反应。Rab8,类似于医学博士1852,已知参与后Golgi转运到质膜,诱导新表面延伸的形成,并据信由鸟嘌呤核苷酸解离抑制剂调节[31可能对应于医学博士0818.这两个医学博士1852年医学博士0818属于聚类C1a,因此在有丝分裂开始前mRNA水平升高。这一观察结果可能与确定a的基本对称性有关m . denticulata有丝分裂前的细胞,由除去细胞核后形成的三叶半细胞显示[32].相比之下,SNARE周期成员在C3簇中高表达,表明在叶期进一步分化中起作用医学博士1404(类似于植物棘突32)和医学博士1560(类似于调制性3a型atp酶)。
确定了两个TDFs编码假定的糖磷脂酰肌醇(GPI)锚:医学博士4071和医学博士4341,分别属于C1a和C4集群。在其他特性中,GPI锚定的功能可能是其针对特定膜域的主要靶向性[33,可能为形态发生建立膜模板。医学博士4341是一个含有179个氨基酸的蛋白,包含一个信号肽和一个束状蛋白结构域(假定的细胞粘附结构域)(e值为2.9E-07),与来自美国的一个束状蛋白样蛋白和一个agp样蛋白相似Brachypodium sylvaticum(CAJ26371.1)和拟南芥蒂利亚纳[AAM62616.1]分别(附加文件6).
医学博士3533 (C3簇)与一种非常长链的脂肪酸浓缩酶类似,根据其在植物形态发生过程中细胞膨胀的重要作用,可能参与了形态发生拟南芥[34].
参与细胞壁代谢的基因
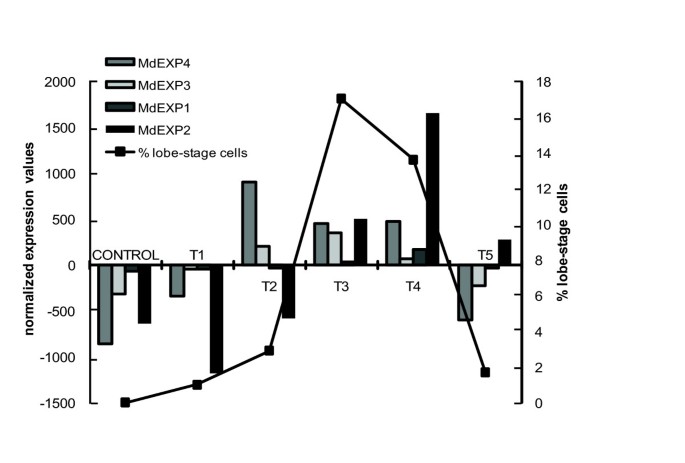
共鉴定出30个细胞壁相关基因。在单糖代谢过程中,分布在C1和C3上的6个TDFs可被鉴定为udp -焦磷酸化酶(医学博士1739年,医学博士2333年,医学博士2565),一种磷酸葡萄糖转化酶(医学博士2842),鼠李糖合酶(医学博士1089),以及gdp -甘露糖3,5-邻位酶(医学博士3053)。9种多糖合成酶几乎都聚集在C3中,其中2种纤维素合成酶,医学博士0757(另见[35])和医学博士3668和一种纤维素合酶样(CSL)基因CSLC的家庭,医学博士2838.外基质蛋白家族糖基转移酶医学博士0450,医学博士1114年,医学博士2144和糖基转移酶医学博士0257可能合成细胞壁的半纤维素或果胶部分,以及具有果胶性质的黏液[11]在细胞生长期间与细胞壁材料同时分泌[36].医学博士3598为半纤维素生物合成途径中典型的α-1,6-木糖基转移酶医学博士0888为木葡聚糖内转糖基酶/水解酶(XET/XTH),是木葡聚糖修饰酶。的开放阅读框(ORF)医学博士0888编码一个具有信号肽和GH16-XET结构域(e值6.10E-37)的276氨基酸蛋白,因此命名为MdXTH1。催化位点DEIDFEFLG,在GH16家族成员中保守[37最多的种子植物xth [38]在MDXTH1中作为Xexdxefxg存在,然后立即接下来是潜在的N-糖基化位点NXT / S [39](附加文件7).另外15种TDFs参与了壁组装、重组和选择性降解。其中4个给出了有意义的扩展:MdEXP1(C4),MdEXP2(C4),MdEXP3(C3),MdEXP4(C3)。然而MdEXP4和MdEXP3在早期的形态发生阶段(C3)表达,MdEXP1和MdEXP2在以后的阶段(C4)在上调(图4).细胞扩张所需的细胞壁内部结构的改变可能是通过iii类过氧化物酶介导的羟基自由基的释放来实现的医学博士0434和医学博士0493.过氧化物酶生成的羟基自由基可以通过各种多糖的裂解导致非酶壁松动[40].orf的医学博士0434包含分泌信号肽和Pfam过氧化物酶结构域(e值2.50E-97)(附加文件8).H.2O2过氧化物酶活性的底物可能是乙二醛氧化酶产生的医学博士0606,医学博士1709年,医学博士3495.水解酶包括果胶酯酶医学博士4415,endo-β-1,6-半乳蛋白酶医学博士1480和C5簇的两个成员:聚半乳糖醛酸酶医学博士3500和β-葡糖苷酶医学博士0559,可能参与初级细胞壁和次级细胞壁之间连接区的降解,从而使初级细胞壁脱落[41].
的系统发育关系m . denticulata扩展素类似蛋白质
由于尚未检查扩展蛋白在绿藻细胞生长中的累积,我们专注于这类蛋白质的实验。全长特征m . denticulataexpansin-resembling蛋白(医学博士EXPS)在附加文件中给出9.MdEXP1和MdEXP4显示出最高的序列相似性(74%的一致性,84%的相似性)(图5).
氨基酸序列的对准Micrasterias denticulata扩展素类似蛋白质氨基酸序列的对准m . denticulata扩展素类似蛋白质mdexp2,mdexp1,mdexp4和mdexp3拟南芥蒂利亚纳EXPA1 [NP_001117573]和EXPB1 [NP_179668]。省略了MdEXP2的c端扩展名(请参阅附加文件)11).深色白色字符表示N终端排序信号。对齐下方的深灰色和白色框分别表示扩展域1和2。保守的Cys(C)和TRP(W)残留物在对准方面表示。在expa和ExpB扩展素家族的结构结构域内保守的GH45催化位点的关键残留物以粗体显示。保守的扩展素残留物和图案很轻微阴影。星号标记相同的残留物;冒号和时期分别表明了强大的群体的全部保护。
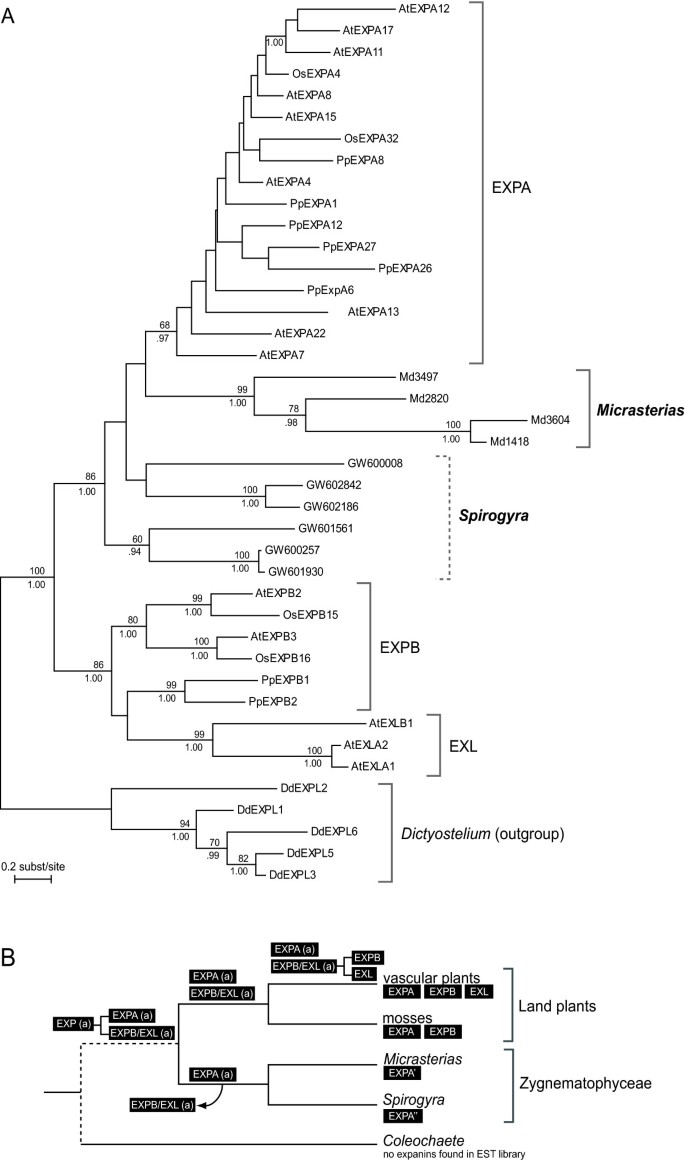
第一个数据集的系统发育分析表明医学博士EXPs恢复为高支持的单系组(BV = 99, PP = 1.00)(图6).的Micrasterias和水绵序列属于植物膨化蛋白,与EXPA家族关系最密切,与EXPA家族形成了一个支撑良好的分支(BV = 86, PP = 1.00)。的医学博士EXPA是EXPA分支的姐妹水绵序列形成了一种超速组合,但序列之间的关系Micrasterias和水绵扩展局和expa Clade支持不佳。内部和中间的高序列分歧Micrasterias和水绵是由相对较长的分支比EXPA分支显示的。在第二个数据集中,假定的绿藻扩张蛋白序列形成了一个高度分化的分支,通过一个非常长的分支与植物扩张蛋白分离(附加文件)10).虽然绿藻分支之间的关系dictyostelium.支系与植物扩展素科的分离较差,系统发育位置较差Micrasterias与EXPA家族关系密切的分支得到了很好的支持。
植物扩展蛋白基因家族的最大似然系统发育(a)植物扩展素基因家族的最大似然(ml)系统发育,显示出系统发育位置Micrasterias和水绵基因。节点上的数字表示ML bootstrap值(上)和贝叶斯后验概率(下);分别低于50和0.9的值没有显示出来。弟弟,盘基网柄菌discoideum(外);页,Physcomitrella金属盘;操作系统,栽培稻;在,拟南芥蒂利亚纳.(b)可能事件假设解释土壤植物和Zygnematophyceae中扩展蛋白基因家族的分布。有机体树是基于多聚烯系统发育分析[5,6]只有包括发现扩展的分类群,以及Coleochaete显然缺乏基于转录组分析的扩展蛋白[27].树中的虚线表示系统发育不确定性。“(a)”标志着祖先基因家庭,expa'和expa'代表发现的exca相关基因Micrasterias和水绵分别。
域组织的m . denticulata扩展素类似蛋白质
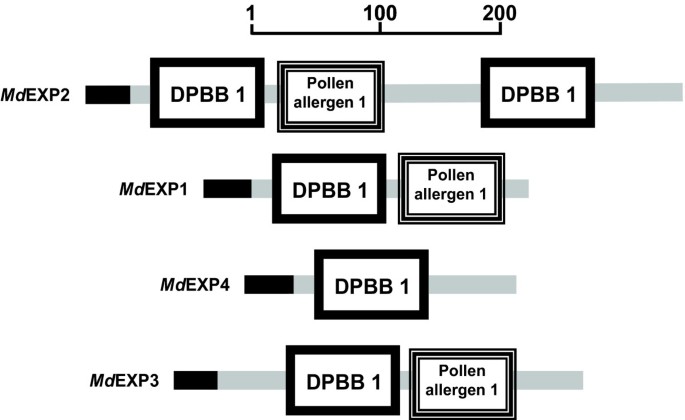
结构域组织的不同医学博士将EXPs与植物膨化素的典型结构特征进行了比较(表)1,图5,图7).在它们中都有一个分泌信号肽(图)5,图7, 桌子1).除MdEXP4外,所有蛋白均存在花粉过敏原-1结构域,而GH45结构域仅存在于MdEXP2和MdEXP3,但e值不显著。然而,在所有序列中都存在DPBB-1结构域,这是一种罕见的脂蛋白a- like double-psi beta-barrel结构域,GH45属于该结构域,甚至有两个结构域MdEXP2(附加文件11).在真菌GH45酶中形成二硫桥的八个胱烯基残基并保持其折叠结构[16]在一些植物膨化蛋白组的膨化蛋白域1中是保守的[22也在医学博士exp(图5).在m . denticulata,GGACGY基序作为GGSCGY / F存在,而同一扩展结构域1中的GXXCGXCF / Y基序完全保守。这个域的第三个主题特征,Y / FRRVPC主题,在医学博士Exps(表1).GH45催化位点的关键残基在EXPA和EXPB蛋白中保守(见图)5,用黑体字标出)。在陆地植物膨化蛋白中,花粉过敏原结构域包含四个保守的色氨酸残基,构成该结构域疏水核心的一部分[42)(图5).在医学博士当考虑到结构相关的苯基丙氨酸和酪氨酸时,最多两个这样的残基发生了EXPs,并且完全保守(图)5, 桌子1).虽然N-末端附近的高度保守的Hatfyg主题是Expa蛋白的特征[22],这个主题无法找到医学博士Exps。通过在GH45活性位点(α-和β-插入)中,通过在HFDL基序的任一侧的保守位置处存在或不存在短延伸的氨基酸的氨基酸的存在或不存在expa和ExpB蛋白。16,43].根据系统发育学,医学博士EXPAs含有EXPAs的α插入特征,但它们缺乏其他EXPAs中发现的四个高度保守的n端残基'GWCN' [16].在HFDL motif中,只有亮氨酸残基被保留(图)5).然而,长c端延伸MdEXP2是典型的EXLA蛋白[22].虽然医学博士EXPs具有异质性和差异性,它们明显具有EXPA蛋白结构域的几个特征,支持我们的系统发育结果。
扩展素类似的亚细胞定位MdEXP2和表型变化,因为它的过度表达
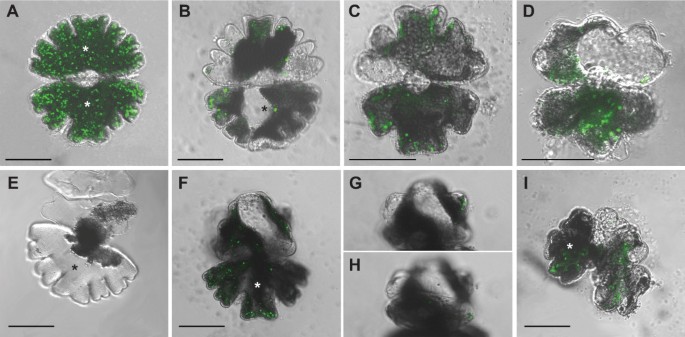
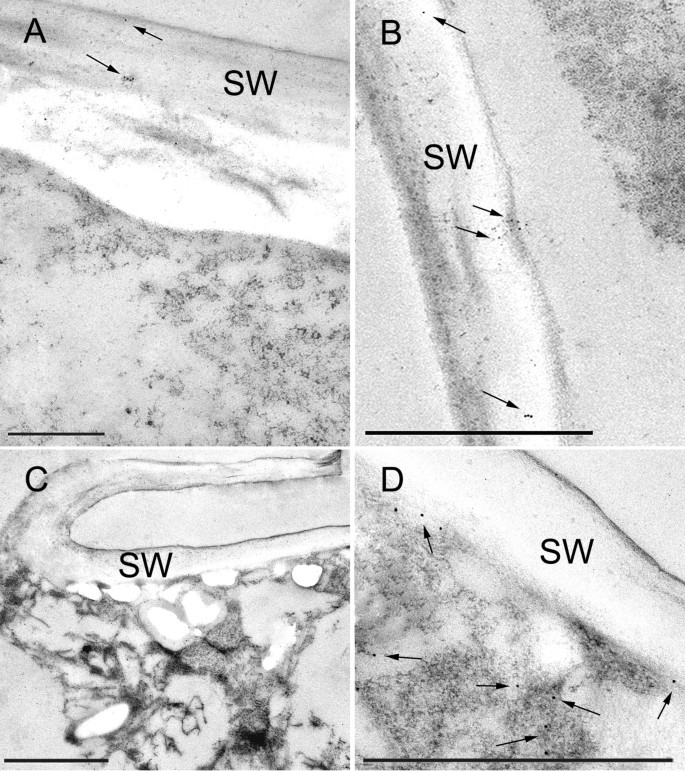
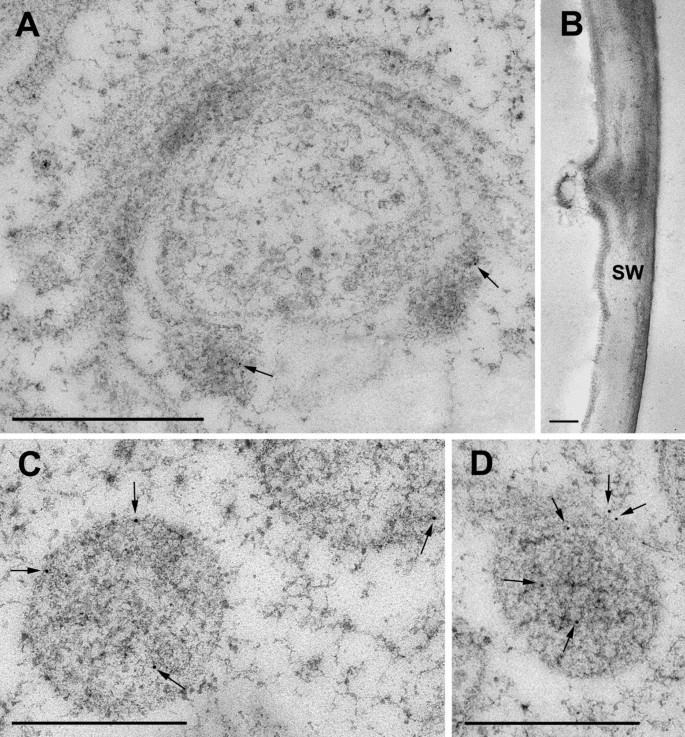
的ORFm . denticulata具有在细胞生长期间具有最高mRNA水平的扩展蛋白,即MDEXP2,克隆到过表达载体中以允许C末端融合到绿色荧光蛋白(GFP)[35].瞬态共聚焦激光扫描显微镜观察MdEXP2-GFP -过表达间期细胞,MdEXP2-GFP荧光以运动胞浆点的形式出现(图)8;额外的文件12),但在次级细胞壁本身无法观察到,可能是由于质外体pH值低而猝灭[44].因此,MdEXP2-GFP-过表达间期细胞进行透射电镜(TEM)处理,并用GFP抗体和蛋白a金染色,研究MdEXP2-GFP蛋白是否定位于次级细胞壁。确实,在次级细胞壁中观察到一个阳性信号,尽管不是大量的(图)9a,b),可能是由于在这个酸腔内的GFP蛋白质不稳定[44].此外,黏液囊泡仍附着在远端高尔基池(图10),还有一些从体中释放出来(图10 c, D)被染色了。这种免疫形式标记表明GFP荧光的点状模式(图8)与高尔基衍生的粘液囊泡相对应,融合蛋白通过内质网-高尔基分泌途径定向到细胞壁。特异性对照实验中,仅用蛋白a金处理的切片未见染色(图)10 b).在产生游离GFP的转基因细胞的控制部分中,在细胞质中发生标记,并从细胞壁和细胞细胞器中不存在(图9 c, D).
表型的Micrasterias denticulata细胞是暂时性overexpressingMdEXP2-GFP共聚焦荧光显微镜观察.合并透射光和GFP荧光单光学切片(B-I)或投影(A)MdEXP2-GFP由星号标记的过度表达。(a)未分开MdEXP2-GFP过度抑制细胞。(b-i)表型m . denticulata细胞是暂时性overexpressingMdEXP2-GFP根据表型严重程度排列。(b)细胞系11.在第一细胞分裂后形成的上半圆囊,表现出刺激的凸形伸长率。裂片伸展并圆形而不是在他们的尖端上扁平。(C-E)伸长率降低,侧瓣融合。(c)细胞系6.在第三细胞分裂后第二次上半圆形后形成的下半圆形。(d)细胞系7.在第二细胞分裂后第一,上半圆形之后形成的下半圆形。(e)细胞系18.由第一细胞分裂导致的上半块,之后细胞死亡。(F-I)细胞系13.细胞分裂的生长极性和平面性丧失。(g,h)(f)的其他焦点部分,表明存在三个生长平面而不是一个增长率。(i)融合在第二细胞分裂上的半圆形。 Scale bar = 50 μm.
接下来,分离和进一步分析26种独立的瞬时转基因细胞(附加文件13).一组细胞在几天内失去gfp荧光而分裂,导致正常子细胞,而大部分细胞死亡,可能是由于强MdEXP2通过它们明亮的GFP荧光表明过表达。然而,在8个独立的细胞系中,一系列表型与MdEXP2在细胞分裂和生长过程中可观察到过表达。第一次细胞分裂后,第11行细胞显示出强烈的叶伸长,且生长极性不变(图)8 b).脑叶被拉长和变圆,而不是顶端变平。在第11细胞系和其他细胞系(6、7、8、12、13、18、19)第二次细胞分裂后,生长极性发生改变。第13系在细胞分裂时失去平面性,因此具有最严重的表型。新的半细胞三维生长,没有典型的裂片形态,但几乎没有凹痕。当一个子细胞分裂时,观察到相同的表型,而新形成的半细胞也彼此融合(图)8外:我).在线6,7,8,11(从第二电池分割),12,18和19轴向但不是径向伸长率损害,导致具有发育不良的极性叶片和熔合的侧瓣的半圆形(图8汉英).有时,第二次分裂产生类似的形态(图8D.),但在大多数情况下,表型在后续几代内丢失了一次(图8C).所有的表型仍然有GFP信号,它们都不是由只表达GFP的转基因细胞的对照实验产生的GFP.[35]表明它们与转基因的表达有关。
讨论
基因组宽的表达分析显示RAB和肿瘤循环在膜融合中的作用和细胞模式建立中的AGP样蛋白。最近发现陆地植物的组成不同的AGPS存在于生长的主要细胞壁中存在Micrasterias[13].我们的分析进一步表明,iii类过氧化物酶、XTH和扩张蛋白参与了细胞壁的生长。iii类过氧化物酶曾被认为在绿藻中不存在[45,尽管有(部分)mRNA出现在结膜中梭形藻属[46].在这里,一个完整的海藻iii类过氧化物酶与细胞生长有关。此外,尽管它们被认为缺乏木葡聚糖[47,在链霉菌中发现XET活性夏洛和绿色植物乌尔瓦[48].近年来,(1→3,1→4)-β-葡聚糖(mixed - linked glucan, MLG)已被确定为细胞次生细胞壁的主要成分Micrasterias[13在这项研究中,首次发现了藻类XTH。
绿色的藻类Valonia(绿藻门),Nitella(Streptophyta)表现出酸诱导的壁延伸,但这种反应似乎不是由蛋白质介导的[49,50].与土地植物特定机制的假设相反[20., 4个与膨化蛋白有显著相似性的基因在细胞生长过程中上调Micrasterias,与假定的古代进化起源一致[16].基于BLAST与expansin域的显著相似性[22,全球两两比对和系统发育,和结构特征,如分泌信号,MdEXP2, MdEXP1和MdEXP3的存在被认为是扩展蛋白,但从结构域分析和系统发育来看,与胚胎发育的扩展蛋白在基因结构上存在相当大的分歧。这些结果进一步证明,膨胀蛋白并不是在进化过程中被强烈保存下来的[17].GH45结构域催化位点的关键残基和HFDL基基,主要存在于陆生植物和植物中水绵,不发生在Micrasterias.HFDL基序在大多数植物扩展蛋白中存在,但在少数植物expa和Expb蛋白中不存在[16].蛋白质折叠所需的八个n端半胱氨酸[16]和四个c端色氨酸或与纤维素结合有关的残基[42是保守的Micrasterias,绵和陆生植物,可以认为是植物膨化素的关键特征。GH45结构域的GGxCGY/F和GxxCGxCF/Y基序也被保留。唯一不变的区别是在保守氨基酸残基中Micrasterias与陆地植物相比,在GH45结构域的GGACGY基序中出现了丝氨酸残基而不是丙氨酸残基。由于膨胀蛋白破坏了纤维素微纤维和粘附在微纤维上的基质葡聚糖之间的非共价键[18],我们假设这一特征医学博士EXPs可能与继代细胞壁的显性MLG有关Micrasterias[13]取代双子叶植物中存在的(1→4)-β-葡聚糖主干。地衣中MLG的发生[51)、真菌(52]、绿藻(Micrasterias)[13],楔叶类[53]和Poales [54]已经建议由收敛演变引起[55],而distinct的出现医学博士EXPs可能与两种不同的细胞壁类型(初级和次级)相连接,这是由它们不同的时间表达模式所暗示的。
基于本发明的扩展蛋白,与当前假设相结合,对土厂最接近亲属的演变[6,56,膨化蛋白完全可以假定在陆生植物出现之前就已经进化了。然而,胚胎植物与链生植物谱系的关系尚不明确:接合子藻科、油藻藻科和轮藻藻科[57阻碍了对扩展蛋白基因历史的可靠重建。假设接合子藻科与陆生植物有最近的亲缘关系[8,一种可能的情况是expansins在胚胎植物和接合植物的共同祖先中进化成两个谱系(EXPA和EXPB + EXL)(图6 b).中明显缺乏EXPB和EXLMicrasterias和水绵可能是由于基因丢失,在接合子藻科进化的早期。然而,应该强调的是,扩大的家族之间的古老关系很难解决。因此,在解释绿藻扩张蛋白相似基因的系统发育位置时应该谨慎,这暗示了植物扩张蛋白家族在胚胎谱系中的完全分化。
在基因结构上有明显的差异Micrasterias和胚胎扩张素都提出了问题的问题吗?无论是生物化学功能医学博士EXPs和胚胎生长膨胀素相似。为此,我们从功能上进行了研究MdEXP2,MdEXP在生长过程中,通过定位和过表达达到最高表达水平。使用GFP抗体检测MdEXP2-GFP融合蛋白,因为现有的植物扩展蛋白抗体的序列保守性太低。不幸的是,目前,因为只有短暂的遗传转化Micrasterias可能[35],免疫电镜检测生长细胞壁是不可行的。然而,异位产生的蛋白是针对完全生长的次级细胞壁。此外,从其过表达获得的表型结果表明,MdEXP2可以改变细胞壁形状,但这种对生长的影响不能排除其他必需蛋白的膜运输饱和或堵塞。表型是显著可变的,因此表型严重程度似乎与膨胀蛋白丰度没有直接关联(从MdEXP2-GFP荧光强度推断),如前所述[58- - - - - -62].虽然可以观察到与预期的由于膨胀蛋白水平增加而增强的壁延展性相对应的表型[19[大多数情况下,伸长率生长损害,但不是横向膨胀,导致侧瓣的融合。许多因素可能解释番茄的增长率降低(Solanum lycopersicum)过表达扩展蛋白[59].总之,生长阶段特异性的表达,细胞壁的积累,以及它的过表达表型,让我们可以假设MdEXP2可能与土地植物扩展有关的生化功能。
结论
方法
文化条件,同步和采样
一个克隆Micrasterias denticulata在两倍稀释的Desmidiaceae培养基中培养[69在23°C和120-140 μmol photon.m-2.s-1在14小时光/ 10-H黑暗制度下。
通过替换固定培养物的生长介质、稀释密度、和扩展光周期24 h。细胞采样同步文化的RNA提取连续5次点在增长(T1 T5)被选择为每个时间点包括不同比例的细胞不同形态形成阶段(隆起,叶和紧身上衣阶段)(图1C,D).两个独立的静止培养物用作对照样品。通过在4℃和4000rpm下离心1分钟,用磷酸盐缓冲盐水(PBS)用细胞浓缩1分钟。将细胞粒料在液氮中搅拌冷冻并储存在-70℃。
RNA提取及cDNA-AFLP分析
如所述,在每个时间点从大约80000个冷冻细胞中分离出总RNA [70略作修改。以抗rna酶剂二硫苏糖醇2 M原液代替β-巯基乙醇加入提取缓冲液,最终浓度为50 mM [71].细胞在珠磨(Retsch)中被破坏并均匀化(5分钟,频率30秒)-1)与碳化硅尖锐颗粒(Biospec产品)后,细胞颗粒解冻和悬浮在提取缓冲液。在第一次氯乙烷:异戊醇萃取过程中加入植物纯树脂(GE-Healthcare),以消除RNA的黏液污染[72].RNA样本使用Bioanalyzer 2100(安捷伦技术)的RNA 6000 Nano试剂盒进行定性控制,并使用ND-1000 UV-Vis分光光度计(Nanodrop)进行定量。
从2μg的总RNA,cDNA合成和cDNA-AFLP分析开始Bstyi和MSE作为限制酶根据所描述的方法进行[28].对于选择性扩增,Bstyi + c / t + 1 /MSE利用I + 2对引物,得到128个引物组合。利用放射自显影平台(磷酸化imager 445 SI;分子动力学)。
用AFLP-QuantarPro图像分析软件(Keygene N.V)定量分析扫描的凝胶图像。通过减去复制平均值(附加文件,每种基因的表达值被标准化以进行复制效果2).与TMEV V4软件的平均链接分层群集(http://www.tm4.org)和基于质量的自适应聚类(聚类中最少两个标签,显著性水平为0.95)[73]进行归一化表达式数据。
为了评估不同细胞分裂阶段(T1-T5)对同步生长中基因表达的影响,建立了线性回归模型y=μ.+代表+时间+ε.与数据吻合,在哪里y表示原始表达式值,代表和时间固定的复制和时间效果,分别为ε随机误差。对于所有TDFS,AF统计计算,P-值被赋给主要术语时间然后转化为错误发现率,然后问值(74](附加文件2).除了具有重要TDF的TDF(问<0.05) 5个时间点的差异表达,在固定培养中明显缺失但在同步生长中存在的TDFs,从干燥凝胶中切除,不管它们在5个阶段的差异表达的重要性,然后进行扩增和随后的测序[28].
TDFS指定为医学博士(为了m . denticulata),后跟一个与AFLP片段相对应的数字。序列相互比对后,除了TDFs表现出不同的表达谱外,只保留了一组相同序列中最长的一条。每个序列都通过使用Blast2GO v1.7.2程序(http://www.Blast2GO.de)[75].除了显示E值<1.E-03的命中之外,保留了1.E + 00和1.E-03之间的e-value和相似性> 50%的击中以进行进一步分析。
实时QRT-PCR测定
引物(附加文件14)设计与信标设计人员7.0(Premier Biosoft International)和Oligo PerfectTm Designer(Invitrogen)设计。用DNASEI(GE-Healthcare)对分离的RNA进行处理。将来自每个样品的1μg总RNA的等分试样用于cDNA合成。根据制造商的说明,用寡聚-DT引物和SuperscriptTM II逆转录酶(Invitrogen)进行逆转录。
根据形态发生过程中内参基因的组成表达模式,选择内参基因作为qRT - pcr定量分析的标准化因子。他们的表达稳定性(米用GenormTM计划分析)[76].在10个组成型表达的TDF中,医学博士类似于网状的拟南芥蒂利亚纳) 和医学博士1473(类似挪威鼠的过氧化物酶6 [rattus norvegicus.])(米值分别为0.421和0.489)是两个表达最稳定的基因,其次是医学博士0386(类似于未知基因答:芥AT5G13390 T22N19_40)。为了确定可靠数据归一化所需的内部控制基因的数量,两个顺序归一化因子V之间的成对变化值V2/3用geNormTM计算得到,在我们的实验条件下为0.151,略高于截断值0.15。包含第四个内控基因导致了成对变异的增加,产生了V3/4值为0.129。因此,使用两个或三个表达最稳定的基因被认为足以实现可靠的数据规范化[76].PCR片段在LightCyclertm 480(Roche Application Science)平台上以三种方式扩增了Sybrtm Green QPCR主混合物(Stratagene),根据制造商的指示,循环条件为10分钟的预孵育在95°C和95°C的45次循环中15秒,58℃,72℃,15秒。通过从65℃至95℃加热来记录扩增子解离曲线。qbasetm [77]用于相对定量。
RACE pcr、蛋白结构域鉴定、序列比对和系统发育分析
通过使用来自生长同步的cDNA文库的CDNA文库的质粒DNA快速扩增CDNA的末端通过CDNA末端(RACE)PCR获得m . denticulata(从Invitrogen公司购买)作为模板。为mdexp1,mdexp3., 和医学博士0434只做了5’RACE PCR,因为TDF中含有终止密码子和部分3’非翻译区。为医学博士4341,MdXTH1, MdEXP2, 和MdEXP45' RACE和3' RACE都是必要的。利用引物3程序设计基因特异性引物[78],并与载体特异性(pDONR222.1)引物结合使用(附加文件15)预孵育1 min, 95℃30 s、54℃30 s、72℃2 min 30 s共30个循环,72℃5 min共1个循环。
使用智能工具识别ORF序列中的蛋白质结构域(http://smart.embl-heidelberg.de/)[79,80].信号序列由SignalP 3.0服务器(http://www.cbs.dtu.dk/services/SignalP)[81,82]和iPSORT预测(http://ipsort.hgc.jp/)[83].
从Genbank检索相似的序列(http://www.ncbi.nlm.nih.gov.)使用蛋白质BLAST和tblastx [84](附加文件16).使用肌肉对齐序列[85].为了去除信号肽和c端延伸,序列从n端附近的保守色氨酸修剪到c端附近的保守苯丙氨酸[17].
考虑了两组对准的系统发育分析。第一个数据集由四组成m . denticulataexpansin-resembling蛋白(医学博士EXPS),26种土地植物扩展素,代表四个土地植物扩展素家族内的17个原始植物[22]和六个EST序列的链孔绿藻Spirogyra pratensis这表明与土地植物扩展素有显着相似[27].社会性变形虫的五个类扩张蛋白序列,盘基网柄菌discoideum,根据它们与陆生植物扩展素的推断关系被选为外群[16,86].这种对齐是227个氨基酸长(附加文件17).第二个数据集包括了第一次比对的所有序列,以及在绿藻门(链藻类的姐妹分支)的4个物种中发现的9个推测的扩展蛋白基因(322个氨基酸长;额外的文件18)并且用于评估其他推定的绿藻序列的系统发育位置。
采用ProtTest 1.4选择蛋白质进化模型[87].在氨基酸取代的WAG模型中分析最大可能性(m1)和贝叶癌系统发育推理(BI),其具有PHYML v2.4.4的所有数据集的现场率异质性(具有八个类别的γ分布)[88]和非参数引导(1000次重复),以评估内部分支机构的统计支持,使用MrBayes 3.1.2 [89),分别。两次并行运行,每一次包含四个递增加热链运行2 × 106每1000代抽样一次。Tracer v1.4评估了对数似然的收敛性[90.].在构建多数原则共识树之前,500棵树的老化样本(远远超过了参数估计收敛的点)被删除了。
过度的MdEXP2和显微镜
orf的MdEXP2被克隆到SPE.我限制网站(ACTAGT)在叶绿素的控制下的载体psa405aa / b- 粘合蛋白编码DESMID的基因梭形藻属c端融合到绿色荧光蛋白基因(GFP.)[35].引物为:正向引物5'-ATGACTAGTATGAAAATCGGCATAATCCA-3'和反向引物5'-GGAACTAGTtaggcacccattaacggc-3'。PCR在94℃下为2分钟的预孵育,在94℃下为5℃,45℃,45℃,68℃,3分钟,然后在94℃下进行30次,45°S,55°C对于45s,68℃,2分钟,并在72℃下循环5分钟。将重组的质粒引入m . denticulata通过微粒轰击[35].
共聚焦显微镜使用100M显微镜(蔡司),配备LSM510 3.2版软件。样本用20倍(数值孔径为0.5)和63倍水校正物镜(数值孔径为1.2)扫描。采用488 nm氩气激光照射和500 ~ 530 nm波段发射滤光片观察GFP荧光。
对于透射电子显微镜(TEM),遵循GFP抗体(RB,(AB6556)ABCAM)相容方案,以制备样品。MdEXP2-GFP-overexpressingm . denticulata细胞包埋在膜载体(徕卡)的酵母膏中,并立即在高压冰箱中冷冻(EM PACT;徕卡微系统)。在徕卡电子显微镜AFS中进行了冷冻替代。样品在4°C逐步渗入LR-White,硬级(伦敦树脂公司),并嵌入胶囊。用EM UC6超微切片机(徕卡)切割超薄金干涉色切片,收集在模板涂层铜网格上。网格在阻断液上漂浮,然后在1:25和1:10稀释(1%牛血清白蛋白在PBS中)的一抗(GFP抗体,(Rb, (ab6556) Abcam)中孵育60分钟。网格用蛋白a - 10nm金(PAG10nm)标记(乌得勒支大学细胞生物学系)。对照实验包括单独用PAG10nm处理切片。切片在自动对比仪(EM AC20;Leica Microsystems GmbH)在20°C的醋酸铀酰中保存30分钟,在20°C的铅染色中保存7分钟。用80千伏的1010透射电子显微镜(JEOL)观察网格。
新获得的序列数据保存在GenBank中;其中,HE578289到HE578716的转录本衍生片段,HE580226到HE580228的内参基因,以及HE578717到HE578726的开放阅读框。
参考文献
- 1.
李志强,李志强,李志强:植物细胞分裂和扩张的协调机制。美国国家科学院学报。2010年,107:2711 - 2716。10.1073 / pnas.0906322107。
- 2.
杨志,傅莹:ROP/RAC GTPase信号转导。植物营养与肥料学报。2007,10:490-494。10.1016 / j.pbi.2007.07.005。
- 3.
Kryvych, Nikiforova V, Herzog M, Perezza D, Fisahn J:不同阶段的基因表达谱拟南芥蒂利亚纳单细胞水平的毛状体开发。植物理性生物化学。2008,46:160-173。10.1016 / J.Plaphy.2007.11.001。
- 4.
Karol KG, McCourt RM, Cimino MT, Delwiche CF:陆地植物的现存近亲。自然科学学报,2003,23(4):451 - 453。10.1126 / science.1065156。
- 5.
Turmel M, Pombert JF, Charlebois P, Otis C, Lemieux C:由叶绿体基因组揭示的陆生植物的绿藻祖先。植物生态学报,2017,36(6):759 - 762。10.1086/513470。
- 6.
Rodríguez-ezpeleta n,philippe h,Brinkmann H,Becker B,Melkonian M:核,线粒体和塑性多岛数据集的系统发育分析支持MesostigmaStreptophyta。中国生物科学(英文版),2007,27(6):723-731。
- 7.
Finet C, Timme RE, Delwiche CF, Marlétaz F:绿色谱系的多基因系统发育揭示了陆生植物的起源和多样性。生物谷学报。2010,20:2217-2222。10.1016 / j.cub.2010.11.035。
- 8.
王志强,王志强,王志强,等:陆生植物的起源:绿藻结合是关键吗?中国生物医学工程学报。2011,11:104-10.1186/1471-2148-11-104。
- 9。
Meindl U:Micrasterias细胞作为形态发生研究的模型系统。微生物学修订版,57:415-433。
- 10.
Lütz-Meindl U, Brosch-Salomon S:绿藻细胞壁分泌Micrasterias.微生态学报,2000,20(3):427 - 434。10.1046 / j.1365-2818.2000.00699.x。
- 11.
Eder M, Lütz-Meindl U:绿藻中的果胶样碳水化合物Micrasterias经细胞化学分析和能量过滤TEM表征。北京科技大学学报,2008,31(4):457 - 461。10.1111 / j.1365-2818.2008.02036.x。
- 12.
在质膜中粒子复合物的可视化Micrasterias denticulata与初级和次级细胞壁中纤维素原纤维的形成有关。中国生物医学工程杂志。10.1083 / jcb.84.2.327。
- 13.
e M, d R, e U:阿拉伯半乳糖样蛋白和半纤维素的发生和特性Micrasterias(Streptophyta)。J phycol。2008,44:1221-1234。10.1111 / J.1529-8817.2008.00576.x。
- 14.
王志强,王志强,王志强:纤维素系统在细胞壁中的作用Micrasterias.中国生物医学工程学报。1996,19(4):489 - 494。10.1006 / jsbi.1996.0083。
- 15.
Nakashima J,Heathman A,棕色RM:抗A抗体陆地棉重组纤维素合酶(Ces A)特异性标记纤维素合酶Micrasterias denticulata.纤维素。2006,13:181-190。10.1007 / s10570-006-9059-y。
- 16.
Li Y, Darley CP, Ongaro V, Fleming A, Schipper O, Baldauf SL, mcquinn - mason SJ:植物扩张蛋白是一个复杂的多基因家族,具有古老的进化起源。植物营养与肥料学报。2002,28(4):591 - 598。10.1104 / pp.010658。
- 17.
凯瑞·雷,科斯格罗夫DJ:《超级家庭》中不断扩大的家庭Physcomitrella金属盘:与被子植物膨化素比较。王志强。2007,99:1131-1141。10.1093 / aob / mcm044。
- 18.
McQueen-Mason S,Durachko DM,Cosgrove DJ:两个内源性蛋白质,诱导植物中的细胞壁延伸。植物细胞。1992年,4:1425-1433。
- 19.
Expansin对细胞壁的作用模式:细胞壁水解、应力松弛和结合的分析。植物营养与肥料学报,1995,21(4):457 - 461。
- 20.
科斯格罗夫DJ:植物细胞壁扩张生长。植物生态学报。2000,38:109-124。10.1016 / s0981 - 9428(00) 00164 - 9。
- 21.
科斯格罗夫DJ:扩张素使植物细胞壁松动。自然科学。2000,407:321-326。10.1038 / 35030000。
- 22.
Sampedro J,Cosgrove DJ:Expansin Superfamily。基因组Biol。2005,6:242-10.1186 / GB-2005-6-12-242。
- 23.
Pien S,Wyrzykowska J,McQueen-Mason S,Smart C,Fleming A:膨胀蛋白的局部表达诱导整个叶片发育过程和改变叶形。美国国家科学院学报。2001,98:11812-11817。10.1073 / pnas.191380498。
- 24.
CHO HT,Cosgrove DJ:拟南芥中根发发起和扩展素基因表达的调节。植物细胞。2002,14:3237-3253。10.1105 / TPC.006437。
- 25.
明黄2烟草悬浮培养的酸生长反应和α-扩张素。植物生理学。1998,18:907-916。10.1104 / pp.118.3.907。
- 26.
Wang CX, Wang L, Wang L ., McQueen-Mason SJ, Pritchard J, Thomas CR: pH和expansin对番茄单个悬浮培养的影响Lycopersicon esculentum)细胞。植物保护学报,2008,33(4):527-534。10.1007 / s10265 - 008 - 0176 - 6。
- 27.
揭示植物分子过程的进化起源:比较Coleochaete(鞘翅目)和水绵(Zygnematales)转录om。BMC植物BIOL。2010,10:96-10.1186 / 1471-2229-10-96。
- 28。
Vuylsteke M, Peleman JD, van Eijk MJT:基于aflp的转录组分析(cDNA-AFLP)用于全基因组表达分析。Nat协议。2007,2:1399-1413。10.1038 / nprot.2007.174。
- 29。
Milioni D, Sado PE, Stacey NJ, Roberts K, McCann MC:通过cdna扩增片段长度多态性分析,揭示了与植物管状元件的作用和分化相关的早期基因表达。acta botanica sinica(云南植物学报),2002,14(4):513 - 524。10.1105 / tpc.005231。
- 30。
Breyne P, Dreesen R, Cannoot B, Rombaut D, Vandepoele K, Rombauts S, Vanderhaeghen R, Inzé D, Zabeau M:全基因组表达研究的定量cDNA-AFLP分析。中国生物医学工程学报。2003,29(4):489 - 494。
- 31。
Schwartz SL,Cao C,Pylypenko O,Rak A,Wandinger-Ness A:Rab GTP酶一目了然。J Cell SCI。2007,100:3905-3910。10.1242 / JCS.015909。[呃。J Cell Sci.121,246 2008)]。
- 32。
Kallio P, Heikkilä H:关于消除核控制的影响Micrasterias.植物细胞。编辑:Bonotto S,Goutier R,Kirchmann K,Maisin JR。1972年,纽约,学术出版社,167-192。
- 33.
Takos AM, Dry IB, Soole KL:检测表面的糖基磷脂酰肌醇固定蛋白烟草原生质体。费用。1997年,405:1-4。10.1016 / S0014-5793(97)00064-1。
- 34.
郑H,罗兰O,昆斯特L:拟南芥eNoyl-CoA还原酶基因的破坏揭示了在植物形态发生过程中为细胞扩张中的非常长链脂肪酸合成的重要作用。植物细胞。2005,17:1467-1481。10.1105 / TPC.104.030155。
- 35.
关键词:纤维素合成酶,胞内定位,胞内定位Micrasterias denticulata(半叶目,绿藻门)通过短暂的遗传转化。中国科学(d辑:地球科学),2010,32(6):739 - 745。10.1111 / j.1529-8817.2010.00867.x。
- 36.
Oertel A, Aichinger N, Hochreiter R, Thalhamer J, Lütz-Meindl U:小鼠粘液分泌和排泄的分析Micrasterias通过免疫电子显微镜和数字延时视频显微镜。中国科学:地球科学。2004,40:711-720。10.1111 / j.1529-8817.2004.03222.x。
- 37.
Henrissat B,Coutinho PM,Davies GJ:基因组中的碳水化合物活性酶的人口普查拟南芥蒂利亚纳.植物mol biol。2001,47:55-72。10.1023 /答:1010667012056。
- 38.
Nishitani K:Endoxyloglucan转移酶在植物细胞壁组织中的作用。INT转速cytol。1997,173:157-206。
- 39.
Shakin-eShleman Sh,Spitalnik SL,Kasturi L:氨基酸XAsn-的位置X-ser semon是一个重要的决定因素N有关core-glycosylation效率。中国生物医学工程学报。1996,31(6):643 - 646。10.1074 / jbc.271.11.6363。
- 40.
水稻III类过氧化物酶多基因家族及其在陆生植物中的进化。植物化学学报。2004,32(4):457 - 461。10.1016 / j.phytochem.2004.06.023。
- 41.
Brook AJ:《德斯米德的生物学》。牛津布莱克韦尔科学;1981,《植物学专论》第16卷。
- 42.
蛋白质-碳水化合物复合物的结构和能量学。《科学与技术》,1994,4:719-728。10.1016 / s0959 - 440 x(94) 90170 - 8。
- 43.
吴勇:玉米α-扩展蛋白和β-扩展蛋白基因家族的分析和表达。植物生理学报。2001,22(4):423 - 427。10.1104 / pp.126.1.222。
- 44.
WW:绿色荧光蛋白的生化和物理性质。在绿色荧光蛋白:性质,应用和协议。编辑:Chalfie M, Kain SR. New York, Wiley;2005:39-66,生化分析方法,第47卷。
- 45.
帕萨迪F, Penel C, Dunand C:表现悖论:植物过氧化物酶如何修饰细胞壁。植物科学进展,2004,9:534-540。10.1016 / j.tplants.2004.09.002。
- 46.
Sekimoto H, Tanabe Y, Takizawa M, Ito N, Fukumoto Rh, Ito M:表达的序列标签腹膜术术术术术 - 峡谷复合体,一种单细胞藻,处于有性繁殖过程中。DNA Res. 2003, 10: 147-153。10.1093 / dnares / 10.4.147。
- 47.
popper za,fry sc:苔藓植物和龟骨菌的主要细胞壁组成。Ann Bot。2003,91:1-12。10.1093 / AOB / MCG013。
- 48.
Van Sandt Vst,Stieperaere H,Guisez Y,Verbelen JP,Vissenberg K:XET活动在苔藓植物和一些绿藻中的生长和细胞伸长率附近找到:新见解进入原发性细胞壁伸长的进化。Ann Bot。2007,99:39-51。10.1093 / AOB / MCL232。
- 49.
植物细胞扩张对细胞壁力学性能的调节。植物生理学报,1998,35(5):585-657。10.1146 / annurev.pp.35.060184.003101。
- 50.
TEPFER M,CLEAND RE:酸诱导的细胞壁松动的比较Valonia紫在燕麦芦荟中。植物理性。1979,63:898-902。10.1104 / pp.63.5.898。
- 51.
地衣多糖的结构和生物活性研究。植物学报,2001,67:199-208。10.1055 / s - 2001 - 12012。
- 52.
Pettolino F, Sasaki I, Turbic A, Wilson SM, Bacic A, Hrmova M, Fincher GB:植物病原菌丝细胞壁Rhynchosporium secalis含有(1,3 / 1,6)-β-D-葡聚糖,半乳糖-和鼠李诺曼聚糖,(1,3;1,4)-β-D葡聚糖和壳质。中国科学(d辑:地球科学),2009,33(2):337 - 341。10.1111 / j.1742-4658.2009.07086.x。
- 53.
Fry SC, Nesselrode BHWA, Miller JG, Mewburn BR: mixed linkage(1→3,1→4)-β-D葡聚糖是一种主要的半纤维素木贼属(马尾)细胞壁。新植物学报,2008,33(4):513 - 514。10.1111 / j.1469-8137.2008.02435.x。
- 54。
(1→4)-β-D-葡聚糖在Poales细胞壁:使用单克隆抗体的免疫金标记研究。中国科学(d辑:地球科学)。10.3732 / ajb.92.10.1660。
- 55。
超越绿色:理解植物和藻类细胞壁的进化之谜。植物营养与肥料学报,2010,29(4):531 - 534。10.1104 / pp.110.158055。
- 56。
Lemieux C,Otis C,Turmel M:一名植物的绿色藻类Mesostigma viride和Chlorokybus atmophyticus代表了在叶绿体基因组系统发育研究中链藻门的最深分支。BMC Biol. 2007, 5: 2-10.1186/1741-7007-5-2。
- 57.
Leliaert F, Verbruggen H, Zechman FW:深入深海:绿色植物系统发育基础的新发现。BioEssays。2011年,33:683 - 692。10.1002 / bies.201100035。
- 58.
研究表明,扩展蛋白基因表达与延伸率的相关性有限。植物营养与肥料学报。2000,22(1):1 - 7。10.1104 / pp.123.4.1399。
- 59.
过度表达膨化蛋白亚型的转基因植物的生长受损。植物生态学报。2001,46(6):581-589。10.1023 /: 1010650217100。
- 60.
β-expansins的表达与深水水稻节间伸长相关。植物生理学报。2001,27(6):645-654。10.1104 / pp.010345。
- 61.
张志强,李志强,张志强,等:基因表达调控对转基因水稻生长发育的影响。acta botanica sinica(云南植物学报),2003,30(5):593 - 598。10.1105 / tpc.011965。
- 62.
膨化蛋白碳水化合物结合模块的表达影响木质部和韧皮部的形成。生物技术学报,2007,6:1608-1616。
- 63.
陆生植物的起源和早期进化。自然科学进展。1997,39(4):457 - 461。10.1038/37918。
- 64.
格雷厄姆乐,厨师,巴士JS:植物的起源:身体计划改变有助于一个主要的进化辐射。美国国家科学院学报。2000,97:4535-4540。10.1073 / pnas.97.9.4535。
- 65.
Popper ZA, Tuohy MG:超越绿色:理解植物和藻类细胞壁的进化之谜。植物营养与肥料学报,2010,30(4):531 - 534。
- 66.
Sørenseni,Domozych D,Willats WGT:植物细胞墙如何进化?植物理性。2010,153:366-372。10.1104 / pp.110.154427。
- 67.
Popper ZA, Michel G, Hervé C, Domozych DS, Willats WGT, Tuohy MG, Kloareg B, Stengel DB:植物细胞壁的进化和多样性:从藻类到开花植物。植物营养与肥料学报,2011,32(6):567-590。10.1146 / annurev - arplant - 042110 - 103809。
- 68.
Sørensen I, Pettolino FA, Bacic A, Ralph J, Lu F, O'Neill MA, Fei Z, Rose JKC, Domozych DS, Willats WGT: charophyan绿藻为植物细胞壁的早期起源提供了见解。植物学报。2011
- 69.
Schlösserug:Sammlung von algenkulturen。Ber DTSCH BOT GES。1982,95:181-276。
- 70。
一种简单高效的从松树中分离RNA的方法。植物学报1993,11:113-116。10.1007 / BF02670468。
- 71。
Pearson G,Lago-aleston A,Valente M,Serrãoe:从棕海藻和海草的冻干组织中简单快速的RNA提取。欧语J Phycol。2006,41:97-104。10.1080 / 09670260500505011
- 72.
Kiefer E,Heller W,Ernst D:一种简单而有效的协议,用于将功能性RNA分离富含次级代谢物的植物组织。植物MOL BIOL REP。2000,18:33-39。10.1007 / bf02825291。
- 73.
De Smet F, Mathys J, Marchal K, Thijs G, De Moor B, Moreau Y:基因表达谱的自适应质量聚类。生物信息学。2002,18:735-746。10.1093 /生物信息学/ 18.5.735。
- 74.
Storey JD, Tibshirani R:全基因组研究的统计意义。美国国家科学院学报。2003年,100:9440 - 9445。10.1073 / pnas.1530509100。
- 75.
Conesa A, Götz S, García-Gómez JM, Terol J, Talón M, Robles M: Blast2GO:功能基因组学研究中用于注释、可视化和分析的通用工具。生物信息学。2005,21:3674-3676。10.1093 /生物信息学/ bti610。
- 76.
Vandesompele J, De Preter K, Pattyn F, Poppe B, Van Roy N, De Paepe A, Speleman F:通过多个内控基因的几何平均实现实时定量RT-PCR数据的精确归一化。中国生物医学工程学报。2002,3:研究
- 77.
Hellemans J,Mortier G,De Paepe A,Speleman F,Vandesompele J:QBase相对量化框架和软件,用于管理和自动分析实时定量PCR数据。基因组Biol。2007,8:R19.1-R19.14。
- 78。
EMBOSS:欧洲分子生物学开放软件套件。《趋势通讯》,2000,16:276-277。10.1016 / s0168 - 9525(00) 02024 - 2。
- 79。
Schultz J, Milpetz F, Bork P, Ponting CP: SMART,一个简单的模块化架构研究工具:识别信号域。美国国家科学院学报。1998年,95:5857 - 5864。10.1073 / pnas.95.11.5857。
- 80.
SMART 6:最近的更新和新发展。核酸学报2009,37(4):423 - 427。10.1093 / nar / gkn808。
- 81.
王志强,王志强,王志强:原核和真核信号肽的鉴定及其裂解位点的预测。蛋白质工程1997,10:1-6。10.1093 /蛋白质/大家。
- 82.
信号肽的预测:SignalP 3.0。中国生物医学工程学报,2004,30(4):593 - 598。10.1016 / j.jmb.2004.05.028。
- 83.
Bannai H,Tamada Y,Maruyama O,Nakai K,Miyano S:N末端蛋白质分选信号的广泛特征检测。生物信息学。2002,18:298-305。10.1093 / Bioinformatics / 18.2.298。
- 84.
Altschul SF, Madden TL, Schäffer AA, Zhang J, Zhang Z, Miller W, Lipman DJ: gap BLAST和psp -BLAST:新一代蛋白质数据库搜索程序。核酸学报1997,25:3389-3402。10.1093 / nar / 25.17.3389。
- 85.
Edgar RC:肌肉:具有高精度和高吞吐量的多个序列对齐。核酸RES。2004,32:1792-1797。10.1093 / nar / gkh340。
- 86.
ogasawara s,shimada n,kawata t:含有扩展素的分子的作用dictyostelium.信号换能器和转录蛋白DD-STATA的激活剂的形态发生和调节其基因表达。开发增长不同。2009,51:109-122。10.1111 / J.1440-169X.2009.01086.x。
- 87.
D:蛋白质进化的最佳拟合模型的选择。生物信息学。2005,21:2104-2105。10.1093 /生物信息学/ bti263。
- 88.
一种简单、快速、准确的算法,通过最大似然估计较大的系统发育。中国科学:地球科学。10.1080 / 10635150390235520。
- 89.
Ronquist F, Huelsenbeck JP: MrBayes 3:混合模型下的贝叶斯系统发育推断。生物信息学。2003,19:1572-1574。10.1093 /生物信息学/ btg180。
- 90.
Rambaut A, Drummond AJ: Tracer v1.4。2007年,(http://beast.bio.ed.ac.uk/]
确认
作者感谢Debbie Rombaut和sophie D'hondt对cDNA-AFLP分析的帮助,感谢Andy vierstrate和Wilson Ardilez-Diaz的测序,感谢Filip Waumans为本研究中确定的序列构建数据库,感谢Klaas Vandepoele的生物信息学帮助,感谢Mansour Karimi的克隆建议,Ellen Cocquyt获得系统发育学建议,Daniel Cosgrove获得命名法建议,Martine De Cock帮助准备手稿。这项工作得到了比利时国家、科学政策办公室、弗兰德斯研究基金会(向F.L.和L.D.V.提供博士后奖学金)发起的大学间吸引极点项目(UIAP VI/33)的支持。以及弗兰德斯科学技术创新机构(“战略Basisonderzoek”项目SBO040093和向k.v.、m.j.j.h.和J.G.提供博士预科奖学金)。
作者信息
从属关系
通讯作者
额外的信息
作者的贡献
KV进行了分子遗传学研究并起草了稿件。MJJH参与了实时QRT-PCR测定和遗传转化。RDR进行免疫电解显微镜。MV设计CDNA AFLP研究并进行了统计分析。流动进行了系统发育分析。JP和AG参加了比赛PCRS。UL-M参与了同步和RNA提取以及数据的解释。JG和LDV参与了实验的设计。DI和WV构思和监督该研究。WV,FL,LDV和MH有助于起草稿件。 All authors read and approved the final manuscript.
电子补充材料
12870 _2011_915_moesm1_esm.pdf
附加文件1:用于cDNA-AFLP、复制2和实时qRT-PCR的RNA样本中形态发生阶段的分布。(PDF 82 KB)
12870 _2011_915_moesm5_esm.pdf
附加文件5:复制2样本经cDNA-AFLP和qRT-PCR获得的选定TDFs表达谱比较。(PDF 42 KB)
12870_2011_915_moesm7_esm.pdf.
附加文件7:全长推导的MDXTH1氨基酸序列(医学博士0888)与其相关的爆炸点击对齐。(PDF 150 KB)
12870 _2011_915_moesm10_esm.pdf
附加文件10:植物扩展蛋白基因家族的推定叶绿素扩展素序列(Tblastx搜索中的植物扩展蛋白具有显着相似性的关系的最大似然性phylogy。(PDF 98 KB)
12870 _2011_915_moesm11_esm.pdf
附加文件11:MdEXP2的BLAST蛋白比对,显示了类似于expansin的c端延伸。(PDF 23 KB)
12870_2011_915_moesm12_esm.pdf.
附加文件12:共聚焦GFP荧光延时图像(间隔30秒)显示MdEXP2-GFP包含细胞内室的运动性。(PDF 51 KB)
12870_2011_915_moesm16_esm.pdf.
附加文件16:用于构建系统发育树的序列的登录号和附加Physcomitrella金属盘序列。(PDF 14 KB)
12870 _2011_915_moesm17_esm。NEX
附加文件17:Nexus文件具有本研究中使用的肌肉对齐的膨胀蛋白的系统发育分析。(NEX 10 KB)
12870 _2011_915_moesm18_esm。NEX
附加文件18:本研究中用于扩展蛋白(包括绿藻类序列)系统发育分析的MUSCLE alignment的Nexus文件。(NEX 17 KB)
作者为图像提交的原始文件
下面是作者提交的原始图片文件的链接。
权利和权限
开放获取本文由BioMed Central Ltd授权发表。这是一篇开放获取的文章,是根据知识共享署名许可协议(https://creativecommons.org/licenses/by/2.0.),允许在任何媒介上无限制地使用、分发和复制,但必须正确引用原作。
关于这篇文章
引用这篇文章
Vannerum,K.,Huysman,M.J.,De Rycke,R.et al。单细胞绿藻细胞生长和形态发生的转录分析Micrasterias(链霉素属),重点介绍了膨胀素的作用。BMC植物杂志11,128(2011)。https://doi.org/10.1186/1471-2229-11-128
已收到:
接受:
发表:
关键字
- 绿色荧光蛋白
- 土地植物
- 次生细胞壁
- 棒曲霉素
- 绿色荧光蛋白荧光