摘要
背景
尽管在一些作物品种中观察到基因组技术的巨大进步,但分子工具如微卫星标记的可用性在甜瓜(Cucumis梅洛L.)和葫芦物种。微卫星标志物的发展将对瓜膜遗传分析和繁殖的重大影响,特别是关于标记饱和遗传图的产生和标记辅助育种计划的实施。基因组微卫星富集的文库可以是在这些物种中的标记发育的有效替代方案。
结果
七百克隆含有a的微卫星序列茶匙鉴定了-AG/TC微卫星富集文库,设计合成了144对引物。利用67个微卫星标记对甜瓜和其他瓜类种质进行了DNA多态性检测,其中65个微卫星标记揭示了甜瓜种质间的DNA多态性。一些瓜类植物,如Cucumis巨大成功在美国,多达50%的甜瓜微卫星标记可方便地用于DNA多态性评估,显著降低了标记开发成本。从新微卫星标记集中随机抽取25个微卫星标记,对40份甜瓜种质进行了特征分析,建立了甜瓜等位基因频率数据库。平均期望杂合度为0.52,介于0.45 ~ 0.70之间,表明少量的筛选标记足以解决基因型鉴定和品种保护问题。基于微卫星多态性的遗传距离与RAPD标记分析结果一致。利用55个新开发的标记进行了定位分析,多数引物表现出孟德尔期望的分离。连锁分析发现56%的标记之间存在连锁,分布在9个连锁组中。
结论
基因组文库微卫星富集是甜瓜标记开发的有效方法。144个新标记被开发茶匙-AG / TC基因组图书馆。这是第一个报告的成功使用富集的图书馆在物种中使用富集的图书馆。经过测试的微卫星标记的样品证明了瓜遗传分析的有效,包括遗传距离估计和身份测试。联动分析表明,发育的标记分散在整个基因组中,并且对甜瓜的遗传分析非常有用。
背景
葫芦科包括几种具有重要经济价值的栽培植物,如西瓜(Citrullus lanatusl .)、南瓜(Cucurbita最大值l .)、甜瓜(Cucumis梅洛黄瓜(Cucumis巨大成功l .)。甜瓜和其他瓜类种质资源的形态变异很大。栽培基因之间的基因流动是由物种的异种共生习惯促进的[1].植物种内分类的难点c·梅洛,主要是在过去的40年中得到了解的(已经解决了)[2- - - - - -4].栽培甜瓜的形态通常分为三大类:reticulatus,cantaloupensis和Inodorus.[3.,4].最近,reticulatus该组织已被建议成为cantaloupensis集团(1].野生型甜瓜属于瓜类Flexuosus.,momordica,conomon,dudaim和跟组(4].
属于的甜瓜品种cantaloupensis或reticulatus团体是美国最种植的,通常称为“麝香蛋白”或“哈密瓜”,用荨麻或罗纹涂层和甜橙肉体生产芳香水果。然而,“瓦伦西亚诺”类型的黄瓜在巴西最重要的是[5]和其他市场。在欧洲国家,这是第二届最多商业化的甜瓜[6].瓦伦西亚诺甜瓜被分类在Inodorus.一组,无气味的水果,表皮光滑或起皱,果肉白色或绿色甜。鲜甜瓜的生产对巴西国内市场的消费很重要,但很大一部分产品出口到其他国家[7- - - - - -9].甜瓜实际上是巴西东北部最重要的农产品之一,那里的土壤和气候条件适合商业生产。水果品质,尤其是风味,是最受重视的商业品质之一,需要进一步改进[8].利用基因组技术,可以加速具有改善的果实质量的瓦伦西亚诺甜瓜品种。这将包括,例如,与果实质量控制相关的基因组区域的分子映射,最终,标记辅助选择。
分子标记已广泛应用于植物物种的遗传分析和育种,具有多种应用[10].在现有的各种类型的分子标记中,微卫星标记最近受到了越来越多的关注,特别是在育种方面。微卫星标记,也称为简单序列重复或SSRs [11,12,是一组短的(通常是2到6个)串联重复的核苷酸碱基,分布在整个基因组中。微卫星标记是共显性、多等位、高度多态性的遗传标记,需要少量的DNA进行直接的PCR和凝胶电泳分析。它的主要缺点是市场开发所需的初始投资成本高[13].微卫星标记的开发可以基于数据库中储存的DNA序列信息,也可以基于筛选专门构建的基因组DNA库,以发现基因组中的重复序列。利用微卫星序列丰富的基因组文库是一种策略,旨在降低标记开发的成本,同时增加标记发现的机会[14].
微卫星标记在甜瓜遗传分析中的实际应用非常有限。到目前为止,文献中只描述了大约70个微卫星标记[15.,16.只有少数用于连锁分析。这些标记被整合到利用形态学、isoenzimatic和其他分子标记如RFLP(限制性片段长度多态性)、AFLP(扩增片段长度多态性)和RAPD(随机扩增多态性DNA [16.- - - - - -28.].因此,需要发现和开发更多的微卫星标记用于甜瓜遗传连锁分析。
本工作的主要目的是基于微卫星序列基因组文库开发新的甜瓜微卫星标记,并检验其在遗传连锁分析中的应用价值:(a)在遗传连锁分析中的应用价值;(b)确定巴伦西亚诺瓜品种之间的遗传距离和(c)作为其他瓜类品种的分子标记。
结果与讨论
微卫星序列基因组文库丰富
一个茶匙-AG/TC基因组文库构建,1600个克隆与(AG/TC)杂交,共鉴定出700个阳性菌落。13探针,其中大多数含有微卫星重复序列。锚定-PCR反应确认了700个克隆450中的微卫星存在,并允许鉴定这些克隆中微卫星序列的尺寸,取向和位置。此信息对于选择要进行测序的克隆非常重要,降低成本和时间。侧翼微卫星区域的DNA序列的知识允许底漆设计和合成。最初基于由锚定PCR方法产生的信息开发一组237个引物对,并且合成一百四十四个引物对(额外的文件1).其中59个标记具有完全的AG或TC重复(41%),68个标记具有复杂重复(47%),17个标记具有复合重复(12%)(额外的文件1).与已经发表的40个甜瓜微卫星标记(34%的完美重复,24%的复合重复和42%的复杂重复)相比,在这个样本中检测到更多的完美重复[16.].在新的微卫星标记中观察到的重复单位数量从3个到40个不等(额外的文件1),而在已经公布的标记中,观察范围是7-15(二核苷酸)和5-10(三核苷酸)[15.,16.].
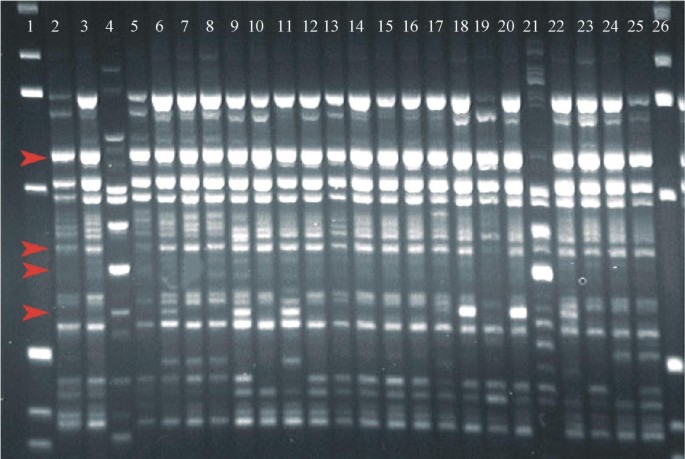
144对引物中有67对因PCR条件不需要进一步调整而立即进行基因检测。在11种六种葫芦属的面板上测试了六十七个标记物(c·梅洛,Citrullus lanatus,Cucurbita最大值,c . moschata,c .浆果和Cucumis巨大成功).65个标记检测到5份甜瓜种质之间的DNA多态性(图)1).
标记可转移到其他瓜类植物
在瓜类面板上检测的67个新瓜类微卫星标记中,有33个与黄瓜(Cucumis巨大成功),16种西瓜DNA(Citrullus lanatus),11Cucurbita moschataDNA和少量(8对引物)c .最大值和Cucurbita浆果DNA。此前的微卫星标记从甜瓜到黄瓜的可转移性估计与这些结果相似[16.].因此,微卫星标记在该属的可转移性水平Cucumis类似于在其他基因内比较中观察到的,例如甘氨酸在美国,高达65%的微卫星标记用于G. Max.可以转移到其他人甘氨酸物种(29.].当然,这导致了标记使用的快速传播,并促进了对定位和比较遗传学的研究。同样,利用瓜类微卫星标记进行瓜类物种的DNA多态性分析,可以显著降低标记开发成本,为瓜类物种的深入遗传分析提供了一条捷径。
6个标记(CMBR18、CMBR22、CMBR23、CMBR48、CMBR56、CMBR82)对7个物种的样本DNA进行了PCR扩增。这些序列与保存在Genbank的DNA序列进行了比较[30.]和标记物CMBR48与叶绿体16S核糖体RNA基因序列同源性极显著。这可以解释该标记具有较高的可转移性,并且如预期的那样,该标记位点在甜瓜和其他瓜类植物上未检测到DNA多态性。另一方面,在6种瓜类植物中检测到的3个微卫星标记(CMBR18、CMBR56和CMBR23)之间存在多态性Cucumis梅洛登记入册。这些标记位点的性质目前还不清楚。然而,微卫星多态性分析和标记可转移性需要考虑到每个瓜类物种的更大和更多样化的样本。
微卫星标记的遗传多样性分析
一组25个微卫星标记2)随机选择,进行40种甜瓜的多样性研究。无例外,新标记的PCR产物在从加入AF 686上测试DNA时具有预期的片段大小。每个基因座的等位基因数由两种(CMBR107,CMBR44,CMBR5,CMBR71)变为六(CMBR20和CMBR39)。预期的杂合子从0.45(CMBR100)变化至0.70(CMBR25)(表2).这些微卫星标记的平均期望杂合度为0.52。用六个微卫星标记进行观察[15.,每个位点的等位基因数为3 ~ 5个,杂合度为0.49 ~ 0.75,平均0.61。另一项研究利用38个微卫星标记检测到每个位点2-6个等位基因,观察到杂合度为0.26-0.79 [16.].这里估计的等位基因和观察到的杂合子的数量小于预期的甜瓜,如甜瓜。这显然是与研究选择的甜瓜样品的遗传关系有关。而不是为分析选择一个非常多样化的种质,这是一个大多数在巴西收集的瓦伦西亚诺加入的样品,代表该国种植的商业品种,占据了研究。因此,该样品代表了甜瓜遗传池的小亚组,其肯定可以解释相对低于预期的杂合子估计。还应该注意的是,内切染抑郁在葫芦科家庭中并不重要[1,31.- - - - - -33.].瓜类的居群通常是从小居群的一个或几个果实中获得的种子,不仅在农场,而且在野外,有利于内配子[34.].
对于25个标记估计多态性信息内容(PIC)(表2),值范围为0.28(CMBR100)至0.65(CMBR43)。对于DNA指纹识别目的,肯定可以选择一组这些标记,包括诸如身份试验,种子污染的申请,种子生产和品种保护。基于PIC和HE(预期杂合子)的估计,在40个甜瓜附加(标记CMBR7,CMBR2,20,CMBR2,CMBR39,CMBR43,CMBR73,CMBR39)上选择并研究了十种这些标记物,并研究了十种这些标记物。相同基因型的可能性估计为2.0×10-7,根据构建的等位基因频率数据库(表2).这表明,基于微卫星标记的DNA图谱可以有效地区分甜瓜个体和种质。
甜瓜种质间的遗传距离估计
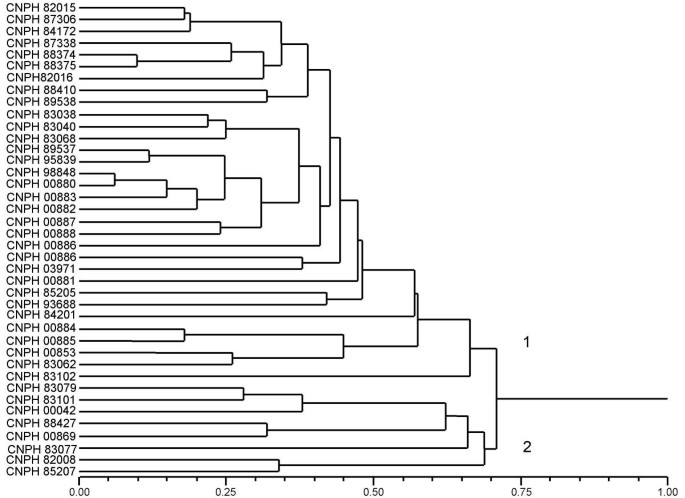
通过25个微卫星标记检测到的DNA多态性,可以估计遗传距离并将其聚类为两个主要类群(图)2).第一组(第一组)主要包括Inodorus.和cantaloupensis / reticulatus栽培的材料,其中聚集与瓜的材料,似乎是从这两种类型之间的杂交。这些种质具有两种类型所特有的形态特征,因此被归类为“中间型”。当没有形态学信息时,归入“未知”类型。第二组(第二组)包括aconomon加入,cantaloupensis入世(W6)和“中间”类型入世(图2).分离栽培甜瓜类型,如Inodorus.和cantaloupensis / reticulatus,来自非栽培类型,例如conomon,在其他基于DNA多态性的甜瓜研究中也观察到[20.,16.].在以栽培类型为主的类群中(类群1)cantaloupensis / reticulatusCNPH 85205、CNPH 84201、CNPH 00884、CNPH 00885、CNPH 00853、CNPH 83062、CNPH 83102)均可轻松分离Inodorus.登记入册(图2).将一些栽培的栽培分化为cantaloupensis和reticulatus群体并不总是通过DNA多态性分析来检测[20.,16.].另一方面,跃变性遗传的分离(cantaloupensis和reticulatus)由非更年期(Inodorus.)通常在基于不同类型的分子标记的研究中一致[35.].综上所述,这些数据似乎只支持栽培瓜的两种分类,Inodorus.和cantaloupensis,如已建议的[1].基于DNA多态性的形态学分类和聚类之间的差异可能反映了最近的遗传育种,可能是不同来源的种质组合[20.,16.].一个非常明显的例子是加利亚品种的分类(cantaloupensis),在不同的子组中聚类。Galia品种的大多数百分点报告父母分类为不同甜瓜类型,无论是在公共和私营部门的繁殖计划中。
本研究中包含的大多数甜瓜附加物先前被归类为Inodorus.(表1).CNPH 00884、CNPH 00885、CNPH 83102及CNPH 84201 (cantaloupensis)、来自2种或2种以上甜瓜品种组合的7份材料和3份没有形态学资料的材料(CNPH 88498、CNPH 89538和CNPH 93688)。虽然CNPH 89538和CNPH 93688的植物类型信息尚不清楚,但从微卫星标记分析可以很清楚地将其分类为CNPH 89538和CNPH 93688inodorus。
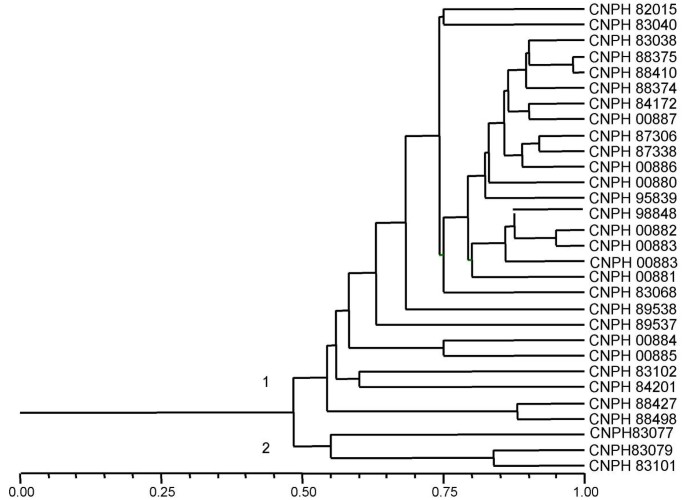
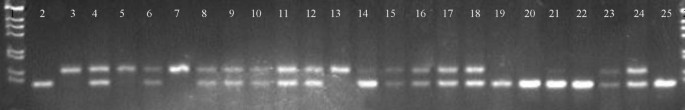
用SSR标记分析的40份甜瓜材料中,有30份也用RAPD标记进行了评价(图)3.).MicroTaTellite生成的矩阵之间估计了-0.70相关系数(图4)和RAPD(图5)标记,采用Mantel检验(t = - 5.0, P = 0.01)。RAPD生成的基质与大豆等其他物种微卫星标记之间的相关性大小麦和这里得到的值非常相似[36.- - - - - -38.].RAPD分析还将甜瓜种质分为两大类,一类为Inodorus.和cantaloupensis / reticulatus西瓜和其他由登记入册CNPH 83077年CNPH 83079和CNPH 83101,集群conomonSSR分析结果(CNPH 00042)。未获得任何形态学信息的CNPH 89538和CNPH 93688也被归为一类Inodorus.基于RAPD标记分析。
RAPD扩增产物琼脂糖凝胶电泳,溴化乙啶紫外染色显示。从左到右:道1和26:梯1 Kb;第2道到第27道:甜瓜的附属物按表上出现的顺序排列1.箭头表示用于分析的多晶型标记。
微卫星标记位点连锁分析
衍生自CNPH 82015和CNPH 84201之间的横桥的93个体的F2后代用于55微卫星标记的连杆分析。大多数底漆根据孟德尔期望显示隔离(图6).只有5%的引物(CMBR53、CMBR70和CMBR147)出现分离畸变(p < 0.001)。在发育过程中,由男性和/或女性配子流产、特定配子基因型的选择性受精或受精卵和胚胎流产引起的畸变[39.].在出现畸变的3个位点中,F2基因型均未按Hardy-Weinberg平衡比例分布,说明畸变的性质为合子。然而,这三个位点并没有相互联系,这表明如果观察到的扭曲有遗传基础,它不是由基因组中的一个有害位点引起的。应该指出,在种内交叉中通常预期会有一定程度的失真[40.],特别是在三角形的十字架中[39.].合子畸变的可能原因包括在标记位点所在的基因组区域绘制的生殖相关基因的有害影响。由于在这三个位点中,过量的基因型都是杂合子,杂交活力可能解释观察到的合子畸变,例如在紫花苜蓿中观察到的[41.]和马铃薯[42.].
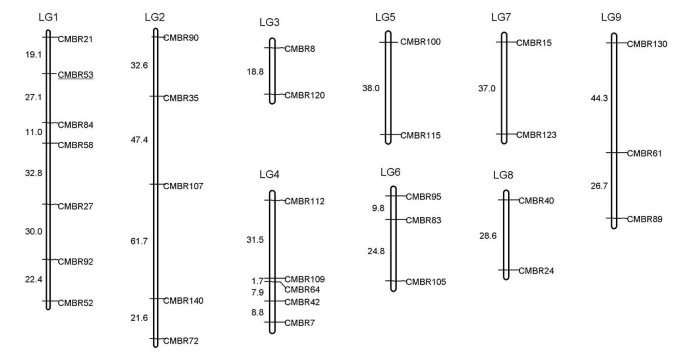
微卫星标记位点连锁分析c·梅洛检测到的链接关联(图7).将31个微卫星标记(583.6 cM)组装成9个连锁群。虽然是初步的,但基因组覆盖率约为甜瓜预期基因组大小(cM)的50% [23.].24个微卫星标记与任一标记均未表现出显著连锁不平衡。数据表明,所分析的微卫星标记分布在整个基因组中c·梅洛.来自的新标记茶匙-AG / TC基因组库目前在旨在基于微卫星标记的饱和遗传图建造饱和遗传图谱的分离群体中进行测试。
结论
基因组文库微卫星富集是甜瓜标记开发的有效方法。从中开发了一百四十四个新标记茶匙-AG / TC基因组图书馆。这是第一个报告在物种中使用丰富的图书馆成功尝试。用于瓜瓜遗传分析的微卫星标志物的样品证明了敏感性分析,包括遗传距离估计和潜在的身份试验。连杆分析表明,显影的标记分散在整个瓜基因组中,并且适合用于绘制目的。到目前为止观察到在标志物基因座和基因组覆盖范围内观察到的多态性水平表明,在甜瓜的遗传分析中产生的微卫星标记应该非常有用。
方法
高变序列丰富基因组文库的开发
利用CTAB法从甜瓜商业杂种af686(巴西坂田种子公司)幼苗新鲜叶片中提取基因组DNA [43.]作了一些修改[10].用Tsp 509 I、Sau III和Mse I酶切DNA,在300 ~ 800 bp范围内选择产生最多片段的酶。选择Tsp 509 I和Mse I片段谱,在3.5%琼脂糖凝胶中分离消化产物[44.,45.].在deae -纤维素NA-45膜中回收了300 - 800 bp的碎片[13].这些选定的片段在盐水中沉淀,并连接到含有互补序列的酶限制位点的适配器。微卫星序列文库的富集是通过将片段与生物素化的寡核苷酸连接来实现的。然后将生物磺化的片段与(AG)杂交13利用探针(AG)筛选Tsp 509 I衍生片段构建基因组文库13.用磁珠回收可能含有微卫星序列的碎片[13].利用与限制性内切酶靶位点互补的引物进行PCR富集对照。Southern Blot证实含有微卫星区域的片段优先恢复。将含有微卫星序列的片段克隆到pGEMT™质粒上,用于转化XL1Blue大肠杆菌细胞(Promega, Madison, WI)通过热休克[45.],得到甜瓜基因组文库Tsp-AG/TC。
阳性克隆的筛选与鉴定
Southern杂交鉴定了含有微卫星插入的基因组文库的克隆[46.].采用锚定pcr方法,通过质粒插入内的定位、大小和位置选择阳性克隆[13].提取选定克隆的质粒DNA,准备测序。
DNA测序和引物设计
使用应用的生物系统377 DNA测序仪,用“染料 - 终止剂”和“大染料”试剂盒(染料 - 终止剂,福斯特城,CA)进行测序反应。使用软件底漆V.3.0设计,设计与微卫星侧翼区域的特定引物对,独特和互补的侧面设计[46.].底漆设计考虑了底漆自动退火的限制参数,G + C含量为55-60℃范围内PCR反应的50%和退火温度。
新开发的微卫星标记的特性和可转移性
在三个甜瓜附口(CNPH 82015,CNPH 84201和CNPH 83102)上合成并测试底漆对并测试。在3.5%琼脂糖凝胶上观察到由扩增产生的片段的预期尺寸,并且在必要时,进行对退火温度的调整。144对引物中有67对因PCR条件不需要进一步调整而立即进行基因检测。在11种六种葫芦属的面板上测试了六十七个标记物(c·梅洛,Citrullus lanatus,Cucurbita最大值,c . moschata,c .浆果和Cucumis巨大成功),包括5种甜瓜品种。65个标记检测到5份甜瓜种质之间的DNA多态性(图)1).聚丙烯酰胺凝胶电泳(PAGE)重复实验,硝酸银染色证实琼脂糖的结果。PCR和电泳条件如下图所示。
微卫星标记数据分析
四十瓜附加(表1从新的微卫星标记集中随机抽取25个微卫星标记进行遗传分析(见表)2).分析中使用了每个加入的一个人。所使用的甜瓜种植主要是在巴西不同地区种植的商业瓦伦西亚诺品种。该样品包括该国种植的大部分商业品种。对于标记基因分型,40个甜瓜附加物的幼叶用于DNA提取[10].采用13 μl PCR方法对微卫星位点进行基因分型,检测条件为:DMSO 5%, dNTP 0.25 mM,引物对0.3 μM, Tris HCl 10 mM (pH 9.0), MgCl21.5 mM, taq -聚合酶1u + 7.5 ng DNA模板。热变化循环为94°C 4 min, 30个循环,94°C 1 min, 50-58°C(取决于引物)1 min, 72°C 1 min,最后一步72°C 7 min。在MJ Research的热循环器PTC 100上进行PCR。扩增产物在GIBCO/BRL S42模型电泳仪(Promega, Madison, WI)上提交到含有4%聚丙烯酰胺和7 M尿素的TBE 1X聚丙烯酰胺凝胶中。凝胶尺寸为20 cm × 34 cm × 0.4 mm。45瓦恒功率电泳,硝酸银染色可见条带[48.].在碱基对中检测到标记位点的等位基因。所有分析的微卫星位点均含有双核重复序列。除了使用已知片段大小的阶梯来判断等位基因的大小,还以一个位点上最常见的等位基因作为参考来调整同一位点上其他等位基因的片段大小。
利用gda -遗传数据分析软件估算了不同位点的等位基因频率[49.].然后构建了40个甜瓜的25微卫星基因座的等位基因频率数据库。观察到(HO)和预期的(HE)杂合性以及诸如每个微卫星基因座的尺寸范围和每个基因座的等位基因数量的遗传参数(额外的文件1)使用GDA软件[49.].观察到的杂合度百分比计算为每个位点杂合子个体基因型与分析基因型总数的比值。预期杂合度的估计是基于从给定样本中随机抽取的两个个体在一个位点上具有不同等位基因的概率[50].多个位点的期望杂合度的算术平均数定义为Hav = Hn / n,其中n为位点总数。多态性信息含量(PIC)也被估计为一个个体在其遗传等位基因分离方面具有信息的概率[51].
选择了一组10个新型微卫星基因座(CMBR7,CMBR22,CMBR24,CMBR25,CMBR27,CMBR3,CMBR39,CMBR43,CMBR73,CMBR89),以估算这些标志物的潜力在甜瓜中的线路识别和品种保护。相同基因型的概率[52,定义为PI =∑PI4+σ(2pipj)2分别对选定的位点进行估计,然后对所有10个位点进行整体估计。
微卫星标记的遗传距离分析
利用微卫星和RAPD标记对40份甜瓜种质进行遗传距离估计。基因分型实验中每个突变体使用一个个体。微卫星基因分型遵循上述步骤。RAPD基因分型是基于80条寡核苷酸引物(Operon Technologies, USA)在3份甜瓜材料(CNPH 82015, CNPH 83038, CNPH 83040)上的初步筛选数据。筛选出35条寡核苷酸引物。引物序列可根据要求提供。以纯化的BSA 1.04 μg/μl、dNTP 0.20 mM、引物0.5 μM、Tris HCl (pH 9,0) 10 mM、MgCl 1.5 mM为反应体积,PCR扩增DNA2, 50 mM KCl, 1 U taq -聚合酶和7.5 ng提取的甜瓜DNA [10].扩增条件为94°C 1 min, 35°C 1 min, 35°C 1 min, 72°C 2 min, 72°C延伸最后一步72°C 5 min, 40个循环。扩增产物在1.5%水平琼脂糖凝胶上用溴化乙啶染色分离。4-5小时在100伏恒定功率下进行电泳[10].
利用共享等位基因距离进行两两比较,估计微卫星标记多态性甜瓜种质间的遗传距离。这些估计是基于两个瓜的共有等位基因所占的比例之和除以两倍的被检测的基因座[53,54].通过使用遗传距离计算器的参数[-Ln(ps)]获得遗传距离[55].然后利用邻域连接法将对角线矩阵提交聚类分析,利用NTSYS 2.02 g软件构建遗传距离树状图[56].利用RAPD标记多态性,利用DICE遗传相似系数计算甜瓜种质间的两两距离[57].采用UPGMA方法(NTSYS软件)进行聚类分析[56,58].利用NTSYS软件MXCOMP程序估计的相关系数评价基于微卫星和RAPD标记的距离和相似性矩阵的对应关系[56].该程序绘图一个矩阵对另一个,元素一个元素,忽略对角值和估计乘积矩相关(r)之间的两个矩阵。通过t检验,将观察到的Z值与其排列分布进行比较,来声明统计显著性[56,59].
联系映射分析
F.2利用CNPH 82015和CNPH 84201杂交获得的93个个体的后代,对本文报道的55个微卫星标记进行连锁分析(额外的文件1).基于Chi-Square Consiventy表计算了预期孟德尔分离比的偏差。最终显示偏析偏差的标记基因座,进一步分析了扭曲的性质,如果是游戏或Zygotic,基于两个额外的Chi-Square条件[39.:(a)通过公式卡方(GL = 1) = [(2np - n)检验假设p=q2+(2nq - n)2/n[其中p (A) = (AA + AB/2)/n和q (B) = (BB + AB/2)/n和n =总个体数]和(B)如果基因型按哈迪-温伯格均衡的预期频率分布,则进行第二次检验:卡方= + [(AB - 2npq)]2n .[物][物]2)2] / nq2.这两种测试的关系允许将畸变分为配子畸变或合子畸变[39.].利用Mapmaker v 2.0程序进行连锁分析[60].仅考虑有81个或更多次较分的F2个体的标记进行分析。最小LOD评分为4.0和0.35的最大重组频率,用于将微卫星标记物分组到潜在的连接基团中。进行三点和多点分析,以在最终的联动组中找到最可能的基因座顺序。每次去除一个基因座并检查不一致的轨迹测试每个连锁组的最终轨迹顺序。检查双交叉事件,并在分配最终连锁组订单之前重新检查的原始分数。基于由MapMaker执行的卤化烷的地图距离功能来校正重组频率。
参考文献
- 1.
Robinson RW, Decker-Walters DS: Cucurbits New York: CABInternational;1997.
- 2。
惠特克TW,戴维斯GN:瓜类:植物学,栽培和利用纽约:跨科学出版物;1962.
- 3.
Munger HM,Robinson RW:命名法Cucumis梅洛胡晓燕。瓜类遗传合作报告。1991,14:43-44。
- 4。
Pitrat M,Hanelt K,Hammer K:一些关于甜瓜品种内含性分类的评论。Acta Horticulturae。2000,510:29-36。
- 5.
Pedrosa JF:Fitotecnia da Cultura DoMelãoPetrolina-Pe:Braba-Semiárido,巴西;1999.
- 6.
Araújo JLP: Mercado de melão na Europa。[http://www.cpatsa.embrapa.br/artigos/melaonaeuropa.html.].
- 7.
prorutas: Ações Básicas para o Desenvolvimento da agrtura iradano里约热内卢Grande do north Mossoró-RN,巴西;1996.
- 8.
Dias R, de CS: Cadeia productiva do Melão na Região Nordeste Petrolina-PE: Embrapa Semi-Árido,巴西;1997.
- 9.
戈梅斯:意想不到的增长和意外的溢出:巴西东北部Mossoró-Assú甜瓜产业的制造1999.
- 10.
Ferreira ME, Grattapaglia D: Introdução ao uso de marcadores molecularesem análise genética Brasília-DF: Embrapa Recursos Genéticos eBiotecnologia,巴西;1998.[http://jjap.ipap.jp/link?jjap/42/7625/].
- 11.
Litt M, Luty JA:一颗高变微卫星体外心肌肌动蛋白基因中二核苷酸重复序列的扩增。《中国科学院院刊》,1989,44:397-401。
- 12.
利用聚合酶链反应可分型的丰富的人类DNA多态性。中国科学(d辑):地球科学(英文版)。
- 13。
作者:张志强,张志强,张志强,张志强:植物DNA标记的产生与应用。非哺乳动物基因组分析:实用指南第1版。编辑:纽约:学术出版社赖恩;1996:73 - 134。
- 14。
Kandpal RP, Kandpal G, Weissman SM:序列重复和跳跃克隆富集文库的构建和区域特异性标记的杂交选择。美国国家科学院学报。1994年,91:88 - 92。
- 15.
Katzir N,Danin-Poleg Y,Tzuri G,Karchi Z,Lavi U,Cregan PB:几种葫芦科物种中微卫星的长度多态性和同源物。Al Appl Genet。1996,93:1282-1290。10.1007 / S001220050367。
- 16.
陈志强,陈志强,陈志强:微卫星标记的研究进展Cucumis.应用科学学报2001,102:61-72。10.1007 / s001220051618。
- 17.
Neuhausen SL:限制性片段长度多态性的评估Cucumis梅洛.Al Appl Genet。1992,83:379-384。10.1007 / BF00224286。
- 18.
Garcia E, Jamilena M, Alvarez JI。,一个rnedo T, Oliver JL, Lozano R: Genetic relationships among melon breeding lines revealed by DNA markers and agronomic traits. Theor Appl Genet. 1998, 96: 878-885. 10.1007/s001220050815.
- 19.
Staub JE, Danin-Poleg Y, Fazio G, Horejsi T, Reis N, Katzir N:栽培甜瓜类群的比较分析(Cucumis梅洛L.)使用随机扩增的多晶型DNA和简单的序列重复标记。Euphytica。2000,115:225-241。10.1023 /答:1004054014174。
- 20.
Staub Je,Meglic v,Mccreight JD:瓜的继承与联系关系(Cucumis梅洛L.)同工酶。J AM SoC Hortic SCI。1998,123:264-272。
- 21.
瓜的遗传图谱(Cucumis梅洛L.)与RFLP,RAPD,同工酶,抗病性和形态标志物。Al Appl Genet。1996,93:57-64。10.1007 / S001220050247。
- 22.
王毅,托马斯·雷,迪恩·雷:甜瓜的遗传地图(Cucumis梅洛L)基于扩增片段长度多态性(AFLP)标记。中国科学(d辑):地球科学(英文版)。10.1007 / s001220050627。
- 23.
Oliver M, Garcia-Mas J, Cardús M, Pueyo N, López-Sesé AI, Arroyo M, Gómez-Paniagua H, Arús P, de Vicente MC:构建甜瓜参考连锁图谱。基因组学杂志。2001,44:836-845。10.1139 / gen - 44 - 5 - 836。
- 24。
Périn C, Hagen LS, Giovinazzo N, beombess D, Dogimont C, Pitrat M:甜瓜开花前果实形状的遗传控制(Cucumis梅洛l)。分子遗传学和基因组学。2002,266:933-941。10.1007 / s00438-001-0612-y。
- 25。
Danin-Poleg Y, Reis N, Baudracco-Arnas S, Pitrat M, Staub JE, Oliver M, Arus P, deVicente CM, Katzir N:简单序列重复Cucumis映射和地图合并。基因组。2000,43:963-974。10.1139 / Gen-43-6-963。
- 26。
Danin-Poleg Y,Tadmor Y,Tzuri G,Reis N,Hirschberg J,Katzir N:与分子标记和园艺性状的甜瓜的遗传图建造,以及与ZymV抗性相关的基因的定位。Euphytica。2002,125:373-384。10.1023 /答:1016021926815。
- 27.
Périn C, Hagen LS, De Conto V, Katzir N, Danin-Poleg Y, Portnoy V, Baudracco-Arnas S, Chadoeuf J, Dogimont C, Pitrat M:参考地图Cucumis梅洛基于两个重组自交系群体。应用电子学报。2002,104:1017-1034。10.1007 / s00122 - 002 - 0864 - x。
- 28.
Silberstein L,Kovalski I,Brotman Y,Perin C,Dogimont C,Pitrat M,Klingler J,Thompson G,Portnoy V,Katzir N,Perl-Treves R:Cucumis Melo的联动地图,包括表型性状和序列表征基因。基因组。2003,46:761-73。10.1139 / g03-060。
- 29.
Peakall R,Gilmore S,Keys W,Morgante M,Rafalski A:大豆的交叉物种扩增(大豆)属内和其他豆科属内的简单序列重复(SSRs):对SSRs可转移性的影响。acta botanica sinica(云南植物学报),1998,15(4):457 - 461。
- 30.
国家生物技术信息中心。[http://www.ncbi.nlm.nih.gov.].
- 31。
Tatlioglu TP:黄瓜。《蔬菜作物遗传改良》第1版。编辑:Kaloo G, Bergh BO。纽约:佩加蒙出版社;1992:197 - 234。
- 32.
McCreight JD,Nerson H,Grumet R:甜瓜。蔬菜作物遗传改善第一版。编辑:Kaloo G, Bergh BO。纽约:Pergamon Press;1992年:267-294。
- 33.
Fehet T:西瓜。蔬菜作物的遗传改良。编辑:Kaloo G, Bergh BO。纽约:佩加蒙出版社;1992:295-314。
- 34.
Allard RW: Princípios do melhoramento genético de plantas。里约热内卢de Janeiro-RJ:美国国际开发署。1971
- 35.
郑晓燕,Wolff DW:甜瓜乙烯产量、保质期及乙烯相关基因RFLP多态性的证据Cucumis梅洛l .)。应用电子学报。2000,101:613-624。10.1007 / s001220051523。
- 36。
Powell W,Morgante M,Andréc,Hanafey M,Vogel J,Tingey S,Rafalski A:种质分析的RFLP,RAPD,AFLP和SSR(微卫星)标志物的比较。分子育种。1996年,2:225-228。10.1007 / BF00564200。
- 37。
孙志强,王志强,王志强:四倍体的分析大利用小麦微卫星标记和RAPD标记对小麦进行了鉴定。基因组学。1997,40:806-841。
- 38。
小麦、黑麦和野生近缘种的特异遗传标记:同工酶、rapd和小麦微卫星的比较。基因组学杂志。2001,44:610-621。10.1139 / gen - 44 - 4 - 610。
- 39.
Lorieux M,Perrier X,Goffinet B,Lanaud C,GonzálezdeLeónd:用于映射遗传标记的最大似然模型,显示隔离失真。2. F2人口。Al Appl Genet。1995,90:81-89。
- 40。
杨志强,李志强,李志强,李志强:关于不同年生物种之间的两个intraspecífic杂交的分离扭曲Medicago.(豆科)。中国科学(d辑):地球科学(英文版)。10.1007 / s001220050466。
- 41。
黄志强,王志强,王志强,等:二倍体和四倍体苜蓿SSR标记的定位。应用电子学报。2000,101:165-172。10.1007 / s001220051465。
- 42。
Bonierbale MW, Plaisted RL, Tanksley SD:基于普通无性系的RFLP图谱揭示了马铃薯和番茄染色体进化模式。遗传学报。1998,20(4):591 - 598。
- 43。
高分子量植物DNA的快速分离。核酸研究。1988,8:4321-4325。
- 44.
Ritschel PS, Buso GSC, Buso JA, Ferreira ME:甜瓜基因组高变分子标记的开发[摘要]。国民大会Genética。2001年,47岁。
- 45.
Ritschel PS, Buso GSC, Buso JA, Ferreira ME:基于微卫星标记的甜瓜遗传图谱研究进展(Cucumis梅洛)[摘要]。动物和微生物基因组现状国际会议。2002年,10:129。
- 46.
分子克隆:实验室手册。纽约:冷泉港。1989
- 47.
底漆v.3.0。[http:// http \\ www.genome.wi.mit.edu].
- 48。
Bassam BJ, Caetano-Anollés G, Gressholf PM:聚丙烯酰胺凝胶中快速灵敏的银染色。分析生物化学。1991年,196:80 - 83。
- 49。
Lewis Po,Zaykin D:遗传数据分析:用于分析等位基因数据的计算机程序。版本1.0(D16C)。[http://lewis.eeb.uconn.edu/lewishome/software.htm].
- 50。
分子进化遗传学。纽约:哥伦比亚大学出版社,1987
- 51。
利用限制性片段多态性构建人类遗传连锁图谱。中国人民大学学报(自然科学版),1998,32:314-331。
- 52。
王志强,王志强,王志强,等:微卫星序列的识别葡萄属锐利对不同基因型的适用性葡萄属物种。基因组。1999年,42:367-373。10.1139 / Gen-42-3-367。
- 53。
基于多态微卫星的高分辨率人类进化树。自然。1994,368:455-457。10.1038 / 368455 a0。
- 54。
Goldstein DB, Ruiz Linares A, Cavalli-Sforza LL, Feldman MW:基于微卫星和现代人类起源的基因绝对年代测定。美国国家科学院学报。1995年,92:6723 - 6727。
- 55。
遗传距离计算器。[http://www2.biology.ualberta.ca/jbrzusto/sharedst.php].
- 56.
RoHLF FJ:NTSYS-PC:数值分类和多变量分析系统 - 版本1.7。纽约:埃克塞特软件。1992年
- 57.
骰子LR:物种间生态联系量的量度。生态学。1945,26:297-302。
- 58.
Sneath PHA, Sokal RP:数值分类学。旧金山:WH Freeman公司,1973年
- 59.
Manly FJ:多变量统计方法。伦敦:查普曼霍尔。1994年
- 60.
MAPMAKER:一种交互式计算机程序包,用于构建实验群体和自然群体的初级遗传连锁图。基因组学。1987,1:174-181。
确认
该研究是Patricia Silva Ritritchel博士论文的一部分,部分由AvançaBrasil和Prodetab(030-02 / 01号)项目部分支持。
作者信息
从属关系
相应的作者
附加信息
作者的贡献
PSR开发了微卫星标记,分离群体,进行了微卫星分析并起草了手稿。TCLL和RLT进行RAPD研究,GSCB参与RAPD数据分析和微卫星标记的开发。JAB有助于RAPD和SSR多样性分析数据的解释。MEF构思了这项研究,参与了研究的设计和协调,检查了数据并审阅了手稿。所有作者阅读并批准了最终的手稿。
电子辅料
12870 _2004_33_moesm1_esm.xls
附加文件1:重复编号和类型,引物序列,退火温度和预期片段大小为144新的甜瓜微卫星标记。该表描述了从A开发的144个新的微卫星标记的重复数和类型,引物序列,退火温度和预期片段大小茶匙AG/TC富集基因组文库。(XLS 112 KB)
作者为图像提交的原始文件
权利和权限
关于这篇文章
引用这篇文章
Ritschel, p.s., Lins, t.c.d.l., Tristan, R.L.et al。从富集的基因组文库中培养微卫星标志物中瓜遗传分析(Cucumis梅洛l .)。BMC植物杂志4,9(2004)。https://doi.org/10.1186/1471-2229-4-9
收到:
接受:
发表:
关键字
- 微卫星标记
- 瓜
- 基因组文库
- 多态信息含量
- RAPD标记